4. Materialien und Methoden
|
|
|
- Elsa Amsel
- vor 7 Jahren
- Abrufe
Transkript
1 73 Materialien und Methoden 4. Materialien und Methoden 4.1. Materialien Bakterienstämme DH10B F`, mcra -(mrr hsdrms-mcrbc), ϕ80dlacz M15, lacx74, deor, reca1, arad139, (ara, leu)7697, galk, λ -, rpsl, enda1, nupg (Invitrogen) SCS-pSE111 Rec A1, enda1, gyra96, thi-1, hsdr17 (r K m K + ), supe44, rela1 (Stratagene) enthält Plasmid pse111 mit laci q Repressorgen und argu Gen für die seltene Arginin-tRNA (Buessow et al., 1998) Zelllinien COS-1 Fibroblasten-ähnliche Zellen, die in adhärenten Monolayern wachsen; Nierenzellen des afrikanischen grünen Affen, transformiert mit einer Replikationsursprungs-defekten Mutante von SV-40, Wirtszelle für die Vermehrung von rekombinanten SV-Viren (DSMZ, Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH) Plasmidvektoren pbluescript Klonierungsvektor der Firma Stratagene mit ColE1 Replikationsursprung zur Replikation in E. coli; β-lactamasegen, T7- und T3-Promotoren sowie lacz-gen zum Durchmustern von Transformanten nach Blau/Weiß-Kriterium; auch als Träger-DNA bei der Transfektion von Säugetierzellen verwendet
2 74 Materialien und Methoden ptl-ha (1, 2, 3) pqe 30, 31, 32 pgex-6p-1, 2, 3 pegfp-c1, pyegfp-c1 Derivat des Vektors psg5 mit einem frühen SV 40 Promotor für die Proteinexpression in vivo und einem T7 Promotor für die in vitro Expression (Stratagene). Veränderung durch Einführung einer größeren multiplen Klonierungstelle mit Erkennungsstellen für EcoR1, BamHI, HindIII, XhoI, NotI, SmaI, PstI, SacI, KpnI und BglII. Aufwärts von der Klonierungstelle (MCS) wurde die Kodierungssequenz für das HA-Epitop eingefügt. Dies erlaubt die Detektion von exprimierten HA-Fusionsproteinen in drei verschiedenen Leserahmen HA 1, 2, 3 mit dem monoklonalen HA- Antikörper. Auf pbr322 basierende Expressionsvektoren mit starken Phagen T5 Promotor und zwei lac-operatorsequenzen für IPTG-induzierbare Expression rekombinanter Proteine mit N-terminalen His6-Epitop (Qiagen) in allen drei Leserahmen. Glutathion S-Transferase (GST) Fusionsvektoren mit synthetischem tac-promotor für die IPTG-induzierbare Expression von GST- Fusionsproteinen; enthalten ist ein internes laci q Repressorgen für die Repression der Expression in jedem E. coli Stamm. Fusionsproteine enthalten nach der GST-Proteinsequenz eine Erkennungsstelle für die PreSission Protease, die die Abspaltung des GST-Epitops ermöglicht (Amersham Pharmacia Biotech-Europe GmbH). Green Fluorescence Protein (GFP) Fusionsvektor für Expression und Lokalisation von Proteinen in Säugetierzellen. Die zu exprimierende Sequenz wird in die multiple Klonierungsstelle dieser Vektoren stromaufwärts der GFP-Sequenz inseriert und als C-terminales GFP Fusionsprotein exprimiert. Der Promotor ist CMV IE, mit puc ori als Replikationsursprung zur Replikation in E. coli und SV40 ori Replikationsursprung zur Replikation in Säugetierzellen. Die Selektion in Prokaryonten ist mit Kanamycin, die in Eukaryonten mit Neomycin (G418) möglich. (Clontech)
3 75 Materialien und Methoden puc 19 Klonierungsvektor mit Ampicillin-Resistenz, lac Z, und Polylinker, High copy origin Medien und Puffer Mikrobiologische Medien und Standardpuffer 0,5x TBE 0,001 M EDTA, 0,045 M Tris-Borat ph x DNA-Probenpuffer 0,42% Bromphenolblau, 0,42% Xylencyanol, 25% Ficoll Typ 400, in aqua bidest, lagern bei 4 C 80 g NaCl, 2 g KCl, 14,4 g Na 2 HPO 4, 2,4 g KH 2 PO 4 ad 1 l aqua bidest 2 M KCl, 10% TWEEN 20, 1 M MgCl2, 0,1 M Cresolrot, 1 M Tris-base ph 10,4, 1 M Tris-HCl ph 4.8 0,5 M Tris-HCl ph 7,0, 1.5 M NaCl, 10 mm EDTA, autoklaviert 2% Paraformaldehyd 2% Paraformaldehyd in PBS bei 60 C lösen, steril filtrieren und begrenzt bei 20 C lagern 25x Proteaseinhibitoren C@mplete mini EDTA-free, 1 Tablette in 2 ml aqua bidest 2M CaCl 2 für die Transfektion 2x HBS für die Transfektion Steril filtriert 280 mm NaCl, 50 mm HEPES, 1,5 mm Na 2 HPO 4 ph 7,1, steril filtriert 10x PBS 10x PCR-Puffer 10x PreSission TM Protease- Puffer Coomassie-Blau- Färbelösung Entfärbelösung für Coomassie-Blau-gefärbte SDS-Gele Fixierer für SDS-Gele 50% Methanol, 9,2% Essigsäure, 0,179% Coomassie Brilliant Blau G250, 2h gerührt und durch einen Faltenfilter filtriert, bei Raumtemperatur zu lagern, wieder verwertbar 7% Essigsäure, 20% Methanol 10% Essigsäure und 45% Methanol
4 76 Materialien und Methoden GST-P1-Puffer LB-Medium Lysispuffer für Säugetierzellen Montagemedium SOB -Medium 50 mm NaH 2 PO 4, 5 mm Tris-HCl ph 8,0, 150 mm NaCl, 1 mm EDTA 10 g Trypton, 5 g Hefe Extrakt, 10 g NaCl, ad 1 l aqua bidest, für Agarplatten 2% Agar zusetzen 50 mm Tris-HCl ph 8,8, 100 mm NaCl, 5 mm MgCl 2, 0,5% NP-40, 1 mm EDTA 5% Propyllgallat, 25% Glycerin (für Mikroskope), in PBS 20 g Trypton, 5 g Hefe Extrakt, 0,584 g NaCl, 0,186 g KCl, ad 1 l aqua bidest T-PBS PBS mit 0,05% Triton X-100 TBS TBS-T TE TE für die Transfektion TY-Medium 20 mm Tris-HCl, ph 7,4, 150 mm NaCl 20 mm Tris-HCl, ph 7,4, 150 mm NaCl, 0,01% Triton 10 mm Tris-HCl, ph 7,4, 1 mm EDTA 1 mm Tris-HCl ph 7,4, 50 mm EDTA, steril filtriert 10 g Trypton, 5 g Hefe Extrakt, 5 g NaCl, ad 1 l aqua bidest Westernblot-Puffer 25 mm Tris-HCl ph 8,0, 192 mm Glycin, 20% Methanol Medien und Medienzusätze für die Zellkultur Dulbecco s Modified Eagle Medium (DMEM), mit Natriumpyruvat und Pyridoxin (Life Technologies); Fötales Kälberserum aus Südamerika (Life Technologies); PBS (Life Technologies); Einheiten/ml Penicillin G und µg/ml Streptomycinsulfat in 0,85% Saline (Life Technologies); 0,25% (w/v) Trypsin/ 1 mm EDTA in Dulbecco s Modified Eagle Medium (Life Technologies).
5 77 Materialien und Methoden Oligonukleotide Name: 5 -Sequenz-3 : Funktion: PGEX5- forward TATAGCATGGCCTTTGCAGG Sequenzierprimer für alle pgex-vektoren, forward PGEX5- reverse TGTCAGAGGTTTTCACCGTC Sequenzierprimer für alle pgex-vektoren, reverse PSG5- forward 90 TCTGCTAACCATGTTCATGCC Sequenzierprimer für ptl- Vektoren, forward, 90 Basen vor der MCS PSG5- reverse 90 GGACAAACCACAACTAGAATG Sequenzierprimer für ptl- Vektoren, reverse, 90 Basen nach der MCS N-OCT 3- KpnI CCGCATGGGGTCACTGGACGG GCGTCTGCA 3 Primer zur Aufamplifizierung von N- OCT3 mit KpnI- Restriktionsschnittstelle SalI-N-OCT3 GGACGCGTCGACCATGGCGAC CG 5 Primer zur Aufamplifizierung von N- OCT3 mit SalI- Restriktionsschnittstelle SalI-PQBP 1 GGACGCGTCGACCATGCCGCT GC 5 Primer zur Aufamplifizierung von PQBP- 1 mit SalI- Restriktionsschnittstelle PQBP 1-NotI ATAGTTAGCGGCCGCTCAATC CTGCTGCTTGGT 3 Primer zur Aufamplifizierung von PQBP- 1 mit NotI- Restriktionsschnittstelle PEGFP-C1 Sequenzierprimer CATGGTCCTGCTGGAGTTCGGT G Sequenzierprimer für pegfp- C1-Vektoren, forward
6 78 Materialien und Methoden FLAG-Sense GATCACATATGGACTACAAGG ACGACGATGACAAGTCGGGAT Adapter zur Einführung FLAG-Epitops in pgex-6p-1 CCGG FLAG- Antisense AATTCCGGATCCCGACTTGTCA TCGTCGTCCTTGTAGTCCATAT Adapter zur Einführung FLAG-Epitops in pgex-6p-1 GT T7 TAATACGACTCACTATAGGG Sequenzierprimer für T7 Promotor T3 ATTAACCCTCACTAAAGGGA Sequenzierprimer für T3 Promotor Die aufgelisteten Oligodesoxyribonukleotide wurden von der MPI Servicegruppe synthetisiert Antikörper Primäre Antikörper: Spezies: Herkunft: Anti-RGS-His Maus Qiagen Anti-Huntingtin (CAG53b), Anti-CAG- Antikörper, (gegen GST-Hdex1 53CAG), Kaninchen Eigene Herstellung, E. Scherzinger polyklonaler Antikörper Anti-Huntingtin (AGG), Anti-AGG- Antikörper, (gegen GST-Hdex1 53CAG Kaninchen Eigene Herstellung, E. Scherzinger Aggregate), polyklonaler Antikörper Anti-Huntingtin (HD1), Anti-HD1- Antikörper, (gegen His-Hdex1 53CAG), Kaninchen Eigene Herstellung, Dr. Scherzinger polyklonaler Antikörper Anti-FLAG, monoklonaler Antikörper Maus Anti-FLAG, polyklonaler Antikörper Kaninchen Anti-myc, monoklonaler Antikörper Maus Roche Anti-myc, monoklonaler Antikörper Maus Babco Anti-myc, polyklonaler Antikörper Kaninchen Clontech Anti-Brn-2, polyklonaler Antikörper Ziege Santa Cruz
7 79 Materialien und Methoden Anti-PQBP 1, polyklonaler Antikörper Kaninchen Geschenk von S. Okazawa Anti-HA, Monoclonal HA 11 MMS-101R Maus Babco (benutzt bei der Immunofloureszenz und im Westernblot), monoklonaler Antikörper Anti-HA, Monoclonal HA 12CA5 (benutzt beim Filtertest und im Westernblot), Maus Roche Diagnostics GmbH monoklonaler Antikörper Anti-GFP, polyklonaler Antikörper Kaninchen Clontech Sekundäre Antikörper Konjugat Spezies Herkunft Anti-Kaninchen IgG Cy3 oder FITC Esel Jackson ImmunoResearch Anti-Kaninchen IgG Peroxidase Fab 2 Fragmente Roche Diagnostics GmbH Anti-Kaninchen IgG Kolloidales Gold, 5 Ziege British BioCell oder 10 nm Anti-Maus IgG Cy3 oder FITC Esel Jackson ImmunoResearch Anti-Maus IgG Peroxidase Fab 2 Fragmente Roche Diagnostics GmbH Anti-Maus IgG Kolloidales Gold, 5 Ziege British BioCell oder 10 nm Monoklonaler Anti- Ziege/Schaf IgG Klon GT-34 Peroxidase Maus
8 80 Materialien und Methoden Enzyme, Proteine, und DNA 1kb DNA Marker Albumin aus Rinderserum, Fraktion V, BSA AmpliTaq DNA-Polymerase FS zur Sequenzierung Benzonase Broad Molekular Weight Marker Calpain Inhibitor I (N-Acetyl-Leu-Leu-norleucinal), ALLN Invitrogen Perkin Elmer Merck Eurolab GmbH Roche Diagnostics GmbH Roche Diagnostics GmbH CIP (calf instestine phosphatase) Expand TM Long Template PCR System, Mischung aus thermostabilen Taq und Pwo DNA-Polymerasen für die Amplifizierung von DNA-Sequenzen mit hohem GC-Anteil Heringssperm-DNA Lysozym pbluescript pgex pqe Alle Restriktionsenzyme, bis auf XhoI T4-DNA-Ligase Trypsin XhoI NEB Roche Diagnostics GmbH Clontech Stratagene Amersham Pharmacia Biotech Qiagen New England Biolab New England Biolab Invitrogen Roche Diagnostics GmbH Chemikalien und Säulenmaterialien 2-(N-Morpholino)ethansulfonsäure (MES) 2-Propanol 3-(N-Morpholino)-2-hydroxypropansulfonsäure (MOPS) Merck Eurolab GmbH 30% Acrylamid, 0,8%Bisacrylamid Rotiphorese Gel 30 Carl Roth Agarose Invitrogen
9 81 Materialien und Methoden Ammoniumpersulfat Ampicillin-Trihydrat Bis-Benzimid (DAPI) Bromphenolblau Calciumchlorid Dihydrat Chloroform Cresolrot (m-cresolsulfonphthalein) Cyan Blau Dimethylsulfoxid (DMSO) Dithiothreitol (DTT) Essigsäure Ethanol, absolut Ethidiumbromidlösung 10 mg/ml Ethylendiamintetraessigsäure (EDTA) Glutathion-Agarose Glutathion, reduziert Glycerin, wasserfrei Imidazol Isoamylalkohol Isopropyl-β-D-thiogalactosid (IPTG) Kanamycin A Monosulfat N-2-Hydroxyethylpiperazin-N-2-ethansulfonsäure (HEPES) Natriumazid Natriumfluorid Ni-NTA-Agarose p-t-octylphenyl-polyoxyethylen (Triton X-100) Paraformaldehyd Phenylmethylsufonylfluorid (PMSF) Polyoxyethylensorbitan-Monolaureat (TWEEN 20) Ponceau S Lösung BioRad Merck Eurolab GmbH Merck Eurolab GmbH Merck Eurolab GmbH Sigma Serva Merck Eurolab GmbH Merck Eurolab GmbH Merck Eurolab GmbH Merck Eurolab GmbH Merck Eurolab GmbH Merck Eurolab GmbH Merck Eurolab GmbH Qiagen Merck Eurolab GmbH
10 82 Materialien und Methoden Propylgallat Serva Blau G TEMED Thiamin, Vitamin B1 Tris (hydroxymethyl) aminomethan (Tris) TWEEN 20 (Polyethylene-Sorbitan Monolaureat Xylencyanol FF Serva Life Technologies Serva Alle anorganischen Salze, Säuren, Basen, Lösungsmittel und Alkohole waren pro analysis Qualität von Merck Eurolab GmbH Kits ABI PRISM TM reaction Kit Bradford Proteinassay Kit Dye Terminator, Cycle Sequencing Ready Perkin Elmer BioRad Expand TM Long Template PCR System Roche Diagnostics GmbH Lipofectin Reagenz Gibco BRL, Life Technologies QIAEX II Gel Extraction Kit QIAfilter Plasmid Maxi Kit QIAprep Spin Miniprep Kit QIAquick PCR Purification Kit Qiagen Qiagen Qiagen Qiagen Western Blot Chemiluminescence Reagenz Plus NEN TM Life Science Products Laborausstattung, Geräte und Zubehör Agarosegelkammer (Flachbett) Airfuge Amersham Pharmacia Biotech-Europe GmbH und Eigenbau der MPI Werkstätten Beckmann
11 83 Materialien und Methoden Analysenwaage AT 250 Ausstattung für SDS-Gelelektrophorese und Blotten von Gelen Autoklav GE 666 AC-1 Beckmann J6-HC (Rotor: JS-4.2) Biacore 2000 Brutschränke CD Spektren Celluloseacetatmembran (0,2 µm) Dialysefilter (0,025 mm) Dialyseschläuche, Molekulargewichtsausschlussgröße 3500 DA Durchlichtscanner, Epson GT-700 Photo Einmal-Impfösen Einweg-Säulen, 1,6 cm im Durchmesser Einweg-Skalpell Elektroporationskuvetten Entwicklermaschine Curix 60 Flourenzmikroskop Axioplan 2 Glasplatten Heizblock Inkubationsschüttler Kanülen, 20G Kryo Einfrierkontainer Kunststoffküvetten Laborhandschuhe Mettler Analytik Protean II System von BioRad Getinge Beckmann Biacore AB Heraeus Jasco J715 Spectropolarimeter, water jacketed Schleicher und Schüll Millipore Spectra/Por Seiko Epson Corporation Nunc Qiagen Braun BioRad Agfa Zeiss Eigenbau der MPI Werkstätten Eppendorf New Brunswick Scientific Becton-Dickinson Nalgene Sarstedt Latech
12 84 Materialien und Methoden Magnetrührer Mikrotiterplatten Mikrowelle Nitrocellulose Membran (0,2 µm) Objekträger, Deckgläschen Pasteurpipetten PCR-Maschine PTC-200 Petrischalen ( 60, 100, 145 mm) für Mikrobiologie Petrischalen ( 60, 100, 145 mm) für Zellkultur PH-Meter Pipetboy Pipetten, einstellbar Pipettenspitzen Plastikplättchen ( 13 mm) Power Supply Präzisionswaage PM 3000 Quarzglasküvetten Reaktionsgefäße Röntgenfilme X-OMAT AR Saran Verpackungsfolie Schüttler (Rocky) Sorvall Super T21 Sorvall Superspeed RC2-b (Rotoren: GSA, SS34) SpeedVac SC110 Spektral Photometer Ultraspec 3000 Spritzen 1, 5, 50 ml IKA-Combimag-REO Genetix AEG Schleicher und Schüll Brand Brand MJ Research Nerbe plus GmbH Greiner bio-one Radiometer Kopenhagen Hirschmann Gilson Gilson Thermanox Pharmacia Biotech und Werkstätten des MPI Mettler Hellmer Eppendorf Kodak The Dow Chemical CTF Labortechnik Scientific Sorvall Sorvall Savant Amersham Pharmacia Biotech-Europe GmbH Once
13 85 Materialien und Methoden Sterile Pipetten Thermocycler für Sequenzierung Tiefkühler, -20 C Tiefkühler, -80 C Tischzentrifuge 5415C Tischzentrifuge Z361 Ultrastab Homogenisierer W250 UV-Tisch (365 nm) UV-Transilluminator mit Videokamera Vortex Wasserbad Wasserbadschüttler Whatman Papier, 3 MM Chr Zellelektroporator Gene Pulser II Zellenkratzer Zellkulturflaschen 75 mm 2 Beckton-Dickmann ABI Bosch ReCon Eppendorf Hermle Branson Vilbert Lourmant Herolab Scientific Industries Haake S New Brunswick Whatman BioRad Costar Biochrom Computerprogramme AIDA 1.0, (AIDA, Deutschland) Corel Draw (PC, Corel Cooperation, USA) Endnote 4.0 (ISI ResearchSoft) Microsoft Office (PC, Microsoft Deutschland) Photoshop 7.0 (Windows, Adobe Systems, USA)
14 86 Materialien und Methoden Benutzte Internetadressen Primerdesign: ip/index.html /cat_primer.html ast.html Berechnung der Proteinparameter: Translation von DNA-Sequenz in die Proteinsequenz: Allgemeine Adresse für Molekularbiologische Seiten: Vergleich von DNA-bzw. Proteinsequenzen: Proteinstrukturanalyse: ml Literaturmeldeservice Allgemein Proteindatenbank: Literatursuche: Analyse von Restriktionserkennungsstellen:
15 87 Materialien und Methoden 4.2. Methoden Sofern nicht explizit erwähnt, wurden alle experimentellen Techniken gemäß den Ausführungen von Sambrook et al. (1998) durchgeführt Molekularbiologische Methoden DNA-Plasmidproduktion und -präparation Die Plasmidpräparation erfolgte mit dem QIAprep Spin Miniprep Kit bzw. dem QIAfilter Plasmid Maxi Kit entsprechend der Vorschrift des Herstellers. Die Zellen wurden durch alkalische Lyse aufgeschlossen und die DNA über Absorptionschromatographie an einer Silicamembran (QIAprep Spin Miniprep Kit) bzw. Anionenaustauscherchromatographie (QIAfilter Plasmid Maxi Kit) gereinigt. Für die Plasmidproduktion wurden die entsprechenden Kolonien auf 5 ml bzw. 250 ml LB-Medium überimpft und über Nacht bei 37 C bei 100 rpm inkubiert. Die Bakterien wurden durch Zentrifugation bei 14000g für 1 min bzw. 4000g für 15 min geerntet und die Plasmid-DNA entsprechend der Vorschrift des Herstellers gereinigt. Mit dem QIAprep Spin Miniprep Kit wurden Plasmid-Präparationen mit einer Konzentration von 0,2 mg/ml DNA gereinigt. Maxi Plasmid-Präparationen wurden auf eine DNA-Konzentration von 1 mg/ml eingestellt Konzentrationsbestimmung der DNA Die Konzentration wäßriger DNA-Lösungen wurde photometrisch durch die Messung der Absorption bei einer Wellenlänge von 260 nm ermittelt. Die Basen der Nukleinsäuren haben bei dieser Wellenlänge ein Absorptionsmaximum. Eine Absorption (A 260 ) von 1,0 entsprach einer Nukleinsäurekonzentration von 50 µg/ml für doppelsträngige DNA. Ist der Quotient A 260 /A 280 = 2 gilt die DNA-Lösung als rein Restriktionsverdau von DNA Die Restriktionsenzyme wurden in den Reaktionspuffern und in der Konzentration nach Angaben des Herstellers eingesetzt. Die Reaktionsansätze wurden 1-2h inkubiert. Die Reaktion wurde gegebenenfalls durch Zugabe von 10x DNA-Probenpuffer gestoppt und anschließend elektrophoretisch aufgetrennt.
16 88 Materialien und Methoden Dephosphorylierung von 5 -Phosphatgruppen Um die Religation eines Vektors zu verhindern, wurden die DNA 5 -Phosphatester hydrolisiert. Der Reaktionsansatz (50 µl) enthielt 10 µl 10x CIP-Puffer, 1U Phosphatase aus Kälberdarm (CIP) und 5-10 µg DNA. Nach 30 min Inkubation bei 37 C wurde der Ansatz durch Erhitzen auf C für min inaktiviert oder sofort mit dem QIAquick PCR Purification Kit gereinigt Aufreinigung von DNA-Fragmenten Beim QIAquick PCR Purification Kit kann Einzel- und Doppelstrang-DNA von 100 bp- 10 kb von Nukleotiden, Enzymen und Salzen getrennt werden. Der Reaktionsansatz wurde nach Anweisung des Herstellers gereinigt und mit 50 µl 10 mm Tris ph 8.0 eluiert DNA-Agarose-Gelelektrophorese In einem horizontalen Agarosegel konnten DNA-Fragmente unterschiedlicher Größe elektrophoretisch aufgetrennt werden. Die Agarose-Konzentration variierte nach Größe der aufzutrennenden Fragmente zwischen 0,8-1,5% (w/v). Die Gele enthielten 0,5 g/ml Ethidiumbromid zur Anfärbung der DNA. Als Laufpuffer wurde 0,5x TBE verwendet Ligation von DNA-Fragmenten Um ein DNA-Fragment in einen Vektor mit identischen kohäsiven Enden zu ligieren, wurden Fragment und Vektor in einem molaren Verhältnis von ungefähr 3:1 gemischt. Ein typischer Reaktionsansatz enthielt 400U T4-Ligase, einmal Ligasepuffer und insgesamt 1 µg DNA. Zur Kontrolle wurde der Vektor ohne Insert ligiert. Die Inkubation erfolgte über Nacht bei 16 C, oder bei Raumtemperatur für 45 min. Die Ligationsansätze wurden min auf Dialysefilter (0,025 µm Porengröße), gegen bidestilliertes Wasser dialysiert. Von beiden Ansätzen wurden je 0,3 µg DNA elektrisch in E. coli Zellen transformiert Polymerase-Kettenreaktion (PCR) Bei der Polymerase-Kettenreaktion (polymerase chain reaction = PCR) wurde die DNA, die als Vorlage dient, das sogenannte template, bei hoher Temperatur 0,5-5 min denaturiert, so dass die DNA einzelsträngig vorliegt. Synthetische Oligonukleotide, deren Sequenzen komplementär zur Vorlage waren konnten dann an das template binden und
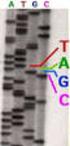
17 89 Materialien und Methoden so einen Startpunkt für eine temperaturstabile DNA-Polymerase bilden, die einen komplementären DNA-Strang synthetisiert. Dabei wurden die Oligonukleotide so entworfen, dass sie durch ein 25 bis 40 maliges Wiederholen dieses Vorganges den gewünschten DNA-Abschnitt exponentiell amplifizierten. Bei den in dieser Arbeit durchgeführten PCR-Reaktionen wurde amplitaq-polymerase FS (Perkin Elmer) oder das Expand TM Long Template PCR System nach Anweisungen des Herstellers benutzt. Eine typische PCR enthielt 0,25 µm von jedem Primer, 65 µm dntp, einmal PCR Puffer, ng template DNA, 0,02 U/µl Taq DNA-Polymerase. Ein typisches PCR- Programm war z.b. 2 min bei 94 C, gefolgt von 30 Zyklen 10 sec bei 94 C, 10 sec bei 65 C, 2 min bei 72 C und abgeschlossen durch 5 min bei 72 C. Für die Amplifizierung von DNA-Fragmenten zur Klonierung wurde folgendes Programm benutzt: 5 min bei 96 C, gefolgt von 5 Zyklen 20 sec bei 96 C, 30 sec bei 56 C, 2 min bei 72 C, gefolgt von 20 Zyklen 45 sec bei 96 C, 2 min bei 72 C und abgeschlossen durch 5 min bei 72 C Berechnung der Schmelztemperaturen von Primern Für Standard-PCRs wurde die Schmelztemperatur der Primer mit Tm [ C] = 2x(A + T) + 4x(G + T) berechnet. Zur Sequenzierung wurde die Schmelztemperatur der Primer mit Tm [ C] = 69,3 C + 0,41x (G% + C%) 650/N berechnet DNA-Sequenzierung Die Sequenzierung erfolgte nach der Kettenabbruchmethode von Sanger mit dem ABI PRISM TM Dye Terminator Cycle Sequencing Ready Reaction Kit. Die Didesoxy- Analoga der 4 verschiedenen Desoxyribonukleotide (dntp) waren jeweils mit einem anderen Fluoreszenz-Farbstoff kovalent verbunden. Die Strangverlängerung konnte somit in einem einzigen Reaktionsgefäß mit allen vier ddntps durchgeführt werden und in einer einzigen Laufspur auf einem Sequenziergel, oder in einer einzigen Kapillare elektrophoretisch aufgetrennt werden. Die dadurch entstehenden aufeinanderfolgenden Fluoreszenzspektren entsprachen der Basenfolge der zu sequenzierenden DNA DNA-Fällung Zur Aufkonzentrierung wurden die DNA-Lösungen mit Natriumacetat und Ethanol gefällt. Dazu wurden die Proben mit 1/10 des Probenvolumens 3 M Natriumacetat ph 5,6 und dem 2,5 fachen Probenvolumen an eiskaltem Ethanol gemischt und 20 min bei
18 90 Materialien und Methoden 80 C inkubiert. Anschließend wurde die gefällte DNA für 20 min bei 20000g pelletiert. Das Pellet wurde mit eiskaltem 70% Ethanol überschichtet und die DNA für 20 min bei 20000g pelletiert. Der Überstand wurde verworfen und das Pellet getrocknet und in H 2 O oder einmal TE aufgenommen Plasmidkonstruktionen pgex-flag Das Plasmid pgex-6p-1 wurde mit den Restriktionsenzymen BamHI und EcoRI geöffnet. Die Oligonukleotide FLAG forward und FLAG reverse wurden in TE gelöst und zu je 100 ng in einem Reaktionsgefäß gemischt. Dieses wurde in 500 ml Wasser auf 98 C erhitzt und langsam auf Raumtemperatur abgekühlt. So entstand ein doppelsträngiger Adapter der in das Plasmid eingeführt werden konnte. Der Adapter zerstört die ursprüngliche BamHI Restriktionserkennungsstelle, führt eine neue NdeI Restriktionserkennungsstelle ein, gefolgt von der DNA-Sequenz, die für das FLAG- Epitop kodiert und einer neuen BamHI Restriktionserkennungsstelle im Leserahmen wie pgex-6p-1. Der Adapter wurde mit den Restriktionsenzymen BamHI und EcoRI verdaut mit QIAquick PCR Purification Kit nach Anweisung des Herstellers gereinigt. Adapter und Plasmid wurden ligiert und transformiert pgex-flag-hd-exon 1(Q)n HD Exon 1 Fragmente mit 20, 32, 37, 39, 40, 45, 51 und 55 CAG Wiederholungen wurden aus den Plasmiden wie sie bei Sittler et al. (1999) beschrieben mit den Restriktionsenzymen EcoRI und NotI ausgeschnitten und gereinigt. Der Vektor pgex- FLAG wurde mit den Restriktionsenzymen EcoRI und NotI geöffnet, gereinigt und mit den gereinigten Fragmenten ligiert pegfp-hd 72Q und pyegfp-hd 17Q pegfp-hd 72Q und pyegfp-hd 17Q wurden vorher als pegfp-cag 72, pyegfp CAG 17 bezeichnet. Sie wurden wie von Sittler et al., 2001 beschrieben kloniert ptl-ha-n-oct3, ptl-ha-tbp, ptl-ha-pqbp1 Für ptl-ha-n-oct3 wurde aus dem Plasmid pgex-flag-n-oct3 mit BamHI und XhoI geschnitten. Ein 1,26 kb großes Fragment wurde aufgereinigt. ptl-ha2 wurde mit
19 91 Materialien und Methoden BamHI und XhoI geöffnet und gereinigt. Fragment und Vektor wurden ligiert und transformiert. ptl-ha-pqbp1 wurde aus dem Plasmid pgex-flag-pqbp1 mit EcoRI und NotI geschnitten und ein 0,8 kb großes Fragment wurde aufgereinigt. ptl-ha2 wurde mit EcoRI und NotI geöffnet und gereinigt. Fragment und Vektor wurden ligiert und transformiert. ptl-ha-tbp wurde von A. Sittler aus pbs2-ksp-tbp kloniert. pbs2-ksp-tbp ist ein pbluescript Vektor. Die TBP cdna wurde in Leserahmen zwischen BamHI- und EcoRI- Schnittstellen einkloniert (von Leslie Thompson, Irvine, USA) pgex-flag-n-oct3, pgex-flag-tbp, pgex-flag-pqbp1 Für pgex-flag-tbp wurde ein 1 kb großes Fragment aus ptl-ha-tbp (A. Sittler) mit EcoRI ausgeschnitten und gereinigt. Der Vektor pgex-flag wurde mit EcoRI geöffnet, mit CIP dephosphoryliert, gereinigt und mit dem TBP cdna Fragment ligiert. Für pgex-flag-n-oct3 wurde N-OCT3 mit den Primern SalI-N-OCT3 und N-OCT3- KpnI aus dem Vektor pbs + SK-N-OCT (A. Fonatana) durch PCR amplifiziert. Das erhaltene 1,25 kb große Fragment wurde mit den Enzymen SalI und KpnI geschnitten und gereinigt. Der Vektor pgex-flag wurde mit den Restriktionsenzymen SalI und KpnI geöffnet, gereinigt und mit der N-OCT3 cdna ligiert. Für pgex-flag-pqbp1 wurde PQBP1 mit den Primern SalI-PQBP1 und PQBP1-NotI aus dem Vektor pbs + SK-PQBP1 (H. Okazawa) mit PCR amplifiziert. Das erhaltene 0,8 kb große Fragment wurde mit den Enzymen SalI und NotI geschnitten und gereinigt. Der Vektor pgex-flag wurde mit den Restriktionsenzymen SalI und NotI geöffnet, gereinigt und mit der PQBP1 cdna ligiert Mikrobiologische Methoden Herstellung elektrisch kompetenter E. coli Zellen Die Präparation elektrisch kompetenter E. coli Zellen erfolgte durch das Waschen von Zellen in der exponentiellen Wachstumsphase in eiskalten 10%igen Glycerin. Dabei wurden die bei der Elektroporation störenden Elektrolyte aus dem Medium entfernt. Mit 1 ml einer Übernachtkultur E. coli Zellen in SOB - -Medium wurde 1l SOB - -Medium angeimpft. Bei 37 C und 100 rpm wurde die Kultur bis zu einer optischen Dichte bei
20 92 Materialien und Methoden 600 nm von 0,6-0,8 inkubiert. Die Zellen wurden bei 4000g und 4 C für 20 min abzentrifugiert, im gleichen Volumen eiskalten 10%igen Glycerin gewaschen und erneut bei 4000g und 4 C für 20 min abzentrifugiert. Dieser Waschvorgang wurde noch dreimal wiederholt, wobei die Pellets zu je 500 ml, 100 ml, und 10 ml resuspendiert und abzentrifugiert wurden. Nach erneuter Zentrifugation wurde das letzte Pellet in 1-2 ml eiskalten 10%igem Glycerin resuspendiert. Die kompetenten Zellen wurden dann zu je 100 µl aliquotiert, in flüssigem Stickstoff eingefroren und bei 80 C gelagert. Elektrisch kompetente Zellen wurden, wie bei Sambrook beschrieben, vor der Benutzung immer durch Transformation mit puc (NEB) und Wasser auf Kompetenz und Kontaminationen untersucht (Sambrook et al., 1989) Transformation in elektrisch kompetente E. coli Zellen Die Transformation von DNA in elektrisch kompetente E. coli Zellen erfolgte durch einen kurzen Impuls von hoher Feldstärke, wodurch die Bakterienzellwand durchlässig für die hochmolekularen DNA Moleküle wurde. Der Genepulser von BioRad wurde auf 200 Ω, 25 mf und 1,68 kv eingestellt. In einer Genpulserküvette mit 0,5 mm Durchmesser wurde 30 µl elektrisch kompetenter Zellsuspension mit 3 µl Ligationsansatz vermischt und elektroporiert. Die Zellen wurden schnell in eiskalten SOB -Medium oder LB-Medium resuspendiert und bei 37 C und 1h im Heizblock inkubiert. Je 100 µl und 900 µl Zellsuspensionen wurden auf LB- Agarplatten mit entsprechendem Antibiotikum bzw. Antibiotika (Konzentrationen wie bei Sambrook et al. (1989) ausgestrichen und über Nacht bei 37 C inkubiert Herstellung chemisch kompetenter E. coli Zellen Die Präparation chemisch kompetenter E. coli Zellen erfolgte durch das Waschen von Zellen in der exponentiellen Wachstumsphase in eiskaltem 0,1 M CaCl 2. Durch kurzes Erhitzen auf 42 C, dem sogenannten Hitzeschock, scheinen die Zellen den Zustand zu erreichen, bei dem sie DNA aufnehmen können. 100 ml LB-Medium wurden mit einer frischen Kolonie E. coli Zellen überimpft. Bei 37 C und 100 rpm wurde die Kultur bis zu einer optischen Dichte bei 600 nm von 0,3-0,6 inkubiert. Die Zellen wurden 20 min auf Eis inkubiert und anschließend bei 4000g und 4 C für 20 min abzentrifugiert. Die Pellets wurden mit 50 ml (entsprechend dem halben
21 93 Materialien und Methoden Volumen der Ausgangskultur) eiskaltem sterilen 0,1 M CaCl 2 gewaschen und erneut bei 4000 g und 4 C für 20 min abzentrifugiert. Die Pellets wurden anschließend nochmals in 5 ml 0,1 M CaCl 2 gewaschen und bei 4000g und 4 C für 20 min abzentrifugiert. Die Pellets wurden dann in 1-2 ml eiskaltem sterilen 0,1 M CaCl 2 mit 10% Glycerin aufgenommen und die resuspendierten Zellen zu je 100 µl aliquotiert, in flüssigem Stickstoff eingefroren und bei -80 C gelagert. Chemisch kompetente Zellen wurden vor der Benutzung immer durch Transformation mit puc Plasmid (NEB) und Wasser auf Kompetenz und Kontaminationen untersucht Transformation von chemisch kompetenten E. coli Zellen Transformation von chemisch kompetenten E. coli Zellen erfolgte durch kurzes Erhitzen auf 42 C, wodurch die Bakterienzellwand durchlässig für hochmolekulare DNA- Moleküle wird. 100 µl chemisch kompetente Zellen wurden mit 3 µl Ligationsansatz vermischt und für 30 min auf Eis inkubiert. Die Zellen wurden für 45 sec auf 42 C erhitzt und anschließend sofort für 5 min auf Eis inkubiert. Danach wurde der Transformationsansatz mit 1 ml eiskaltem SOB -Medium oder LB-Medium versetzt und für 1h bei 37 C und 800 rpm im Heizblock inkubiert. Je 100 µl und 900 µl wurden auf LB-Agarplatten mit entsprechenden Antibiotika (Konzentrationen wie bei Sambrook et al., 1989) ausgestrichen und über Nacht bei 37 C inkubiert Proteinbiochemische Methoden Expression von rekombinanten GST-Fusionsproteinen in E. coli Das Glutathion S-Transferase (GST) Genfusionssystem diente zur Expression und Reinigung von Fusionsproteinen in E. coli. Die pgex-6p Plasmide sind für die induzierbare, intrazelluläre Expression von Genen und Genfragmenten als Fusion mit dem GST-Gen aus Schistosoma japonicum entwickelt worden. Die Expression wird durch einen mit IPTG induzierbaren tac-promotor kontrolliert, der im nicht induzierten Zustand durch das Genprodukt vom internen lac I q Gen repremiert wird. Die Fusionsproteine konnten aus bakteriellen Lysaten durch Affinitätschromatographie mit Glutathion- Agarose gereinigt werden und in Western Blots mit Anti-GST-Antikörpern nachgewiesen werden. Zwischen der MCS und der stromabwärts gelegenen cdna kodierend für GST
22 94 Materialien und Methoden befand sich eine Sequenz, die für eine spezifische Proteaseschnittstelle, für die PreSission Protease, kodiert. Dies erlaubte die Abspaltung des N-terminalen GST- Anteils von dem Fusionsprotein. Für die Expression von GST-Fusionsproteinen wurden 200 ml LB (mit 20 mm MOPS/KOH ph 7.9, 0.2% Glucose, 20 µg/ml Thiamin, 100 µg/ml Ampicillin) mit einer Einzelkolonie, die das gewünschte Expressionsplasmid enthielt, inokuliert und bei 37 C über Nacht geschüttelt. Bei Benutzung des Bakterienstammes SCS1 wurde dem Medium 25 µg/ml Kanamycin für die Selektion auf das zusätzliche Plasmid pse111 zugesetzt. Das Plasmid pse111 enthält das laci q Repressorgen und das argu Gen für die seltene Arginin-tRNA. LacI q verbessert die Repression des tac-promotors und optimiert die Expression eukaryontischer Proteine (Buessow et al., 1998). Mit einer Übernachtkultur wurden 1,5 l LB (mit 20 mm MOPS/KOH ph 7.9, 0,2% Glucose, 20 µg/ml Thiamin, 100 µg/ml Ampicillin) mit einer optischen Dichte bei 600 nm von 0,15 angeimpft und bis zu einer optischen Dichte von 0,6 weiter kultiviert. Die Proteinexpression wurde dann mit 1 mm IPTG für 3,5h bei 37 C induziert. Die Zellen wurden bei 4000g für 20 min abzentrifugiert, das Pellet in Waschpuffer (50 mm Natriumphosphat ph 8, 150 mm NaCl, 1 mm EDTA) resuspendiert und erneut zentrifugiert. Das Zellpellet wurde in flüssigem Stickstoff eingefroren und konnte bei 80 C gelagert werden Reinigung von GST-Fusionsproteinen GST-Fusionsproteine können an immobilisierten Glutathion affinitätsgereinigt werden. Das gebundene Protein wird anschließend mit löslichem Glutathion eluiert, das die Bindung kompetitiert. Die Affinitätschromatographie mit Glutathion-Sepharose zeigte dabei nicht so gute Resultate wie die Affinitätschromatographie mit Glutathion-Agarose. Für die Reinigung von GST-Fusionsproteinen aus 1,5 l Bakterienkultur wurde 200 mg Glutathion-Agarose eingewogen und in 30 ml 1 M NaCl über Nacht bei 4 C gequollen. Die Glutathion- Agarose wurde bei 2000g für 10 min abzentrifugiert und mit 30 ml GST-P1-Puffer gewaschen. Das Waschen wurde zweimal wiederholt. Die Bakterienzellen wurden in 25 ml GST-P1-Puffer mit Protease-Inhibitoren und 0,5 mg/ml Lysozym resuspendiert und min auf Eis lysiert. Das Lysat wurde zweimal 45 sec auf Eis bei Stufe 3 sonifiziert. Dem Lysat wurde Triton X-100 in einer
23 95 Materialien und Methoden Endkonzentation von 0,1% (v/v) zugesetzt und für mindestens 2 min inkubiert. Das Lysat wurde durch Zentrifugation bei 30000g bei 4 C für 30 min geklärt. Der Überstand wurde mit je 200 mg gequollener und gewaschener Glutathion-Agarose versetzt und für 1h bei 4 C auf einem Rad rotiert. Diese Mischung wurde in eine 5 ml Säule gegossen und mit zweimal 30 ml GST-P1-Puffer mit 0,1% Triton X-100 und einmal mit GST-P1-Puffer gewaschen. Das Protein wurde mit GST-P1-Puffer mit 720 ng/ml Glutathion (reduziert) eluiert. Dazu wurde die fast ganz trockene Glutathion-Agarose mit gebundenen Protein mit 1 ml dieses Puffers für 5 min inkubiert und dann erst eluiert. Die Proteinkonzentration wurde photometrisch bei 280 nm bestimmt. Dieses schrittweise Verfahren von Inkubation und Elution wurde fortgesetzt bis die Konzentration geringer als 0,2 mg/ml war. Je 1.5 µg Gesamtprotein der verschiedenen eluierten Fraktionen wurden mittels SDS-Gel analysiert. Anschließend wurden die saubersten Fraktionen vereinigt und über Nacht gegen den Dialysepuffer (20 mm Tris-HCl ph 8, 150 mm NaCl, 0,1 mm EDTA, 8,7% Glycerin) dialysiert. Die Proteine wurden dann aliquotiert, in flüssigem Stickstoff eingefroren und bei 80 C gelagert Konzentrationsbestimmung von Proteinlösungen Konzentrationsbestimmung nach Bradford Bei der Bradford-Methode von verändert sich das Absorptionsmaximum des Farbstoffs Coomassie brilliant blue G250 durch Bindung an Proteine von 465 nm (ohne Protein) zu 595 nm (Bradford Proteinassay Kit, BioRad). Die Zunahme der Absorption bei 595 nm ist ein Maß für die Proteinkonzentration in der Lösung. Dabei verhalten sich alpha- und beta-sekundärstrukturen unterschiedlich. Als Standardreihe wurden BSA-Verdünnungen benutzt Photometrische Konzentrationsbestimmung von Proteinlösungen Zur schnellen Konzentrationsbestimmung von Proteinlösungen wurde die Absorption bei 280 nm gemessen. Dabei entspricht eine OD 280 von 1 einer Proteinkonzentration von 1 mg/ml. Für eine genauere Konzentrationsbestimmung wurde der theoretische Extinktionskoeffizient ε bei ph 6.5 in 6,0 M Guanidiumhydrochlorid und 0,02 M Phosphatpuffer ( berechnet und so die
24 96 Materialien und Methoden Proteinkonzentration über die Absorption bei 280 nm bestimmt. OD 280 von 1 entspricht dann 1 mg/ml = ε /Molekulargewicht (Gill et al., 1989) SDS-Polyacrylamidelektrophorese (SDS-PAGE) Die Auftrennung von Proteinen entsprechend ihrer Molekularmasse erfolgte nach der Methode von Laemmli (Laemmli, 1970). Benutzt wurde dabei ein starkes Detergenz, SDS, das die Dissoziation der Proteine in die einzelnen Polypeptid-Untereinheiten und erlaubt. SDS lagerte sich dabei gleichmäßig an die Proteine. Proteine unterschiedlicher Masse werden unterschiedlich stark negativ geladen. Demzufolge werden die Proteine im elektrischen Feld nach ihrer Größe aufgetrennt. Die SDS-Polyacrylamidelektrophorese wurde gemäß den Ausführungen von Sambrook wurde durchgeführt. Sofern nicht explizit erwähnt, wurde ein 12% Trenngel benutzt (Sambrook et al., 1998) Coomassie-Färbung von SDS-Gelen Die elektrophoretisch aufgetrennten Proteine wurden mit dem Farbstoff Coomassie brilliant blau G250 angefärbt. Die Proteine wurden mit 10% Essigsäure und 45% Methanol für 5 min im Gel fixiert und dem Gel dadurch Wasser entzogen. Das Gel wurde dann für 20 bis 60 min in der Färbelösung mit 50% Methanol, 9,2% Essigsäure und 0,179% Coomassie Brilliant Blau G250 geschüttelt und anschließend durch mehrmaliges Wechseln der Entfärberlösung aus 7% Essigsäure und 20% Methanol entfärbt Western Blotting Nach der Auftrennung der Proteinen im SDS-Gel wurden sie durch Elektroblotting auf eine Nitrocelluslosemembran transferiert. Anschließend konnten die immobilisierten Proteine immunologisch nachgewiesen werden. Das SDS-Gel wurde nach der Elektrophorese blasenfrei auf eine, in Westernblot-Puffer befeuchtete Nitrocellulosemembran gelegt. Auf jeder Seite wurden je zwei mit Puffer befeuchtete Whatman 3 MM Filterpapiere und je ein Schwamm gelegt. Dieses Blotsandwich wurde fest in die Transferapparatur der Firma BioRad eingespannt. Nach Auffüllen des Blot-Tanks mit Puffer erfolgte der Transfer der Proteine auf die Nitrocellulosemembran (1h bei 50 V). Anschließend wurde die Membran mit Ponceau S gefärbt, das die Proteine zusätzlich durch die darin enthaltene Trichloressigsäure fixiert. Die Banden des Proteinstandards wurden auf der Membran markiert.
25 97 Materialien und Methoden Für die Immunodetektion wurde die Membran nach 30 min in 3% Magermilchpulver in PBS für 1h oder über Nacht mit dem spezifischen, primären Antikörper in 3% Magermilchpulver in PBS inkubiert. Anschließend wurde die Membran zweimal mit T- PBS und einmal mit PBS für je 5 min gewaschen und dann mit dem sekundären, Peroxidase-konjugierten Antikörper (in einer Verdünnung 1: 2000) in 3% Magermilchpulver in PBS für 45 bis 60 min inkubiert und wie vorher gewaschen. Die Detektion der immunmarkierten Proteinbanden erfolgte mittels Chemoluminiszenz (ECL Kit, NEN). Die Peroxidase, die am sekundären Antikörper konjugiert ist, katalysiert in Anwesenheit von H 2 O 2 die Oxidation des Substrates Luminol. Dieses emittiert Licht mit einer Wellenlänge von 428 nm. Dieses emitierte Licht kann mit lichtempfindlichen Filmen detektiert werden. Die Lösungen wurden nach Angaben des Herstellers gemischt und mit der Membran inkubiert. Die Filme wurden in der Dunkelkammer auf die Membran aufgelegt und entwickelt. Die entstanden Färbungen wurden mit dem Durchlichtscanner Epson GT-700 Photo digitalisiert und mit dem Programm AIDA 1.0 quantifiziert Filtertest Zur Detektion von SDS-unlöslichen Aggregaten wurde der Filtertest eingesetzt (Scherzinger et al., 1997, Wanker et al., 1999). Auf einer Celluloseacetatmembran (0,2% Porengröße) werden SDS-unlösliche Aggregate aus polymeren Huntingtin zurückgehalten, SDS-lösliche Huntingtin-Monomere dagegen werden durch die Membran gefiltert. Proteinextrakte wurden mit 2% SDS und 50 mm DTT für 5 min auf 95 C erhitzt. Eine BRL Dot-Blot Filtrationseinheit wurde mit zwei mit SDS angefeuchteten Whatman 3 MM Filterpapieren und einer angefeuchteten Celluloseacetatmembran luftblasenfrei belegt und dicht verschlossen. Je 200 µl 0,2% SDS wurden pro Loch vorgelegt und die abgekochten Proteinlösungen hinzu pipettiert. Die Proben wurden durch den Filter gesaugt und zweimal mit 200 µl 0,2% SDS gewaschen. Der Filter wurde anschließend aus der BRL Dot-Blot Filtrationseinheit entfernt und dreimal 5 min mit PBS gewaschen. Dann wurde die Membran wie bei der Immundetektion eines Western Blots prozessiert.
26 98 Materialien und Methoden Proteinfällung mit Trichloressigsäure Proteine können durch eine Präzipitation mit Trichloressigsäure (TCA) angereichert werden. Dazu wurden bis zu 100 µg Protein auf 1 ml mit aqua bidest verdünnt und 5 µl Natriumoxycholat (20 ng/µl) als Detergenz zugegeben. Die Proben wurden auf Eis für 30 min inkubiert und dann mit frisch zubereiteter 20% TCA (w/v) für 1h auf Eis gefällt. Die Proben wurden mit 20000g bei 4 C für 15 min zentrifugiert und das Pellet zweimal mit eiskaltem Azeton gewaschen. Danach wurde wieder mit 20000g bei 4 C für 15 min zentrifugiert. Das Pellet wurde in der Vakuumzentrifuge für 30 min getrocknet und in 50% SDS-Ladepuffer und 50% 1 M Tris-HCl ph 8 gelöst. Anschließend wurden die Proben für das SDS-Gel eingesetzt PreSission Protease Verdau Die PreSission Protease ist ein Fusionsprotein aus GST und der humanen Rhinovirus (HRV) Typ 14 3C Protease (Walker et al., 1994). Die Protease spaltet spezifisch die Sequenz Leu-Phe-Gln/ Gly-Pro. Für einen PreSission Protease Verdau wurde der PreSission Protease-Puffer mit 1 mm frischem DTT, GST-Fusionsprotein in einer (Konz. 0,025-1 mg/ml) mit PreSission Protease gemischt. Für eine quantitative Spaltung wurden die Proteine für 2h bei 8 C mit 0,1U PreSission Protease inkubiert Gewinnung von Aggregationskeimen Aggregationskeime wurden durch Fragmentierung von Huntingtin Exon 1-Aggregaten durch Ultraschall gewonnen. Dafür wurde, sofern nicht anders erwähnt, 0,4 mg/ml GST-M-HD-Q52 wie oben beschrieben mit 0,1 U der PreSission Protease verdaut. Nach zwanzig Stunden Inkubation bei 37 C wurde die Probe mit 40 Pulsen pro Minute für zweimal eine Minute sonifiziert. Die Aggregationskeime wurden bei 20 C gelagert.
27 99 Materialien und Methoden Zellbiologische Methoden Auftauen von kryokonservierten Säugetierzellen Die bei 80 C gelagerten Zellen wurden im Wasserbad bei 37 C schnell aufgetaut und mit entsprechend angewärmtem Kulturmedium in Kulturflaschen ausgesät. Die Zellen wurden über Nacht bei 37 C und 5% CO 2 kultiviert. Am nächsten Morgen wurde das Kulturmedium gewechselt, um das DMSO zu entfernen und die Zellen wurden, wie unter beschrieben kultiviert Kultivierung von Säugetierzellen COS-1 Zellen wurden mit 5% FCS, 100 ie/ml Penicillin und 100 µg/ml Streptomycin bei 37 C und 5% CO 2 kultiviert. Die Zellen wurden bei einer Konfluenz von 80% geteilt und bis zu einer Konfluenz von 5% verdünnt. Dafür wurden die Zellen mit sterilem PBS gewaschen und mit 0,25% (w/v) Trypsin/ 1 mm EDTA bei 37 C für 5 min vom Flaschenboden abgelöst. Die Zellen wurden dann in 10 ml Kulturmedium zu einer homogenen Lösung resuspendiert und entsprechend verdünnt in neue Kulturflaschen ausgesät Lagerung von Säugetierzellen Für die langfristige Lagerung der Säugetierzellen wurden die Zellen in einer Kulturflasche mit 75 cm 2 Grundfläche bis zu einer 80%igen Konfluenz kultiviert. Die Zellen wurden wie oben beschrieben mit Trypsin abgelöst und bei 1000g für 10 min bei Raumtemperatur pelletiert. Die Zellen wurden dann in 1 ml Kulturmedium mit 20% FCS resuspendiert. Dann wurde bis zu 10% DMSO zugegeben. Die Zellen wurden in Kryoröhrchen langsam in einem Styroporbehälter auf 80 C gekühlt und anschließend in flüssigem Stickstoff gelagert Calciumphosphat-Transfektion von Säugetierzellen Die Calciumphosphat-Transfektion (Graham und van der Elb, 1973) beruht auf der Reaktion von Calciumchlorid mit Natriumphosphat, bei der ein wasserunlösliches Calciumphosphat-Präzipitat gebildet wird, das an DNA bindet. Dieses Präzipitat wird von den Zellen aufgenommen und die darin enthaltene DNA transkribiert. Zellen wurden in 9,5 cm 2 Gefäß zu ca. 30% konfluent ausgesät und für 3-5h bei 37 C und 5% CO 2 inkubiert. Für eine Flasche mit 3,5 cm 2 Oberfläche wurden mit 2 µg DNA
28 100 Materialien und Methoden und 4 µg Transport-DNA (pbluescript oder Heringsperma DNA) zu einem Endvolumen von 80 µl mit TE (Säugetierzellen) aufgefüllt. Dazu wurde 20 µl 2M CaCl 2 gegeben. Anschließend wurden 80 µl zweimal HBS unterschichtet und durch Pipettieren mit Luftblasen gemischt. Die Präziptitatbildung erfolgte durch Inkubation für 30 min bei Raumtemperatur. Das Präzipitat wurde vorsichtig auf die Zellen getropft und mit dem Medium vermischt. Nach 12-16h wurden die Zellen für 5 min mit sterilem PBS gewaschen und mit frischem Medium versetzt. Nach Stunden wurden die Zellen geerntet oder für die Immunofloureszenzmikroskopie vorbereitet Lipofectin -Transfektion von Säugetierzellen Lipofectin Reagenz ist eine 1:1 (w/w) Liposomenlösung des Lipids N-[1-(2,3- Dioleyloxypropyl]-n,n,n,-Trimethylammonuimchlorid (DOTMA) und Diolylphosphotidylethanolamin (DOPE) in Wasser. Es formt spontan einen Lipid-DNA Komplex. Die Fusion des Lipid-DNA-Komplexes mit Zellmembranen resultiert in einem effizienten Aufnahme von DNA. Die Zellen wurden entsprechend der Vorschrift des Herstellers mit je 1-2 µg DNA pro 3,5 cm 2 Gefäßoberfläche transfektiert Herstellung von Zelllysaten Die transfektierten Zellen wurden in eiskaltem PBS gewaschen und mit Lysispuffer für Säugetierzellen mit Proteaseinhibitoren und 25 U/ml Benzonase überschichtet. Die Zellen wurden für 30 min auf Eis zur vollständigen Lyse und zum DNA-Verdau inkubiert, dabei wurden die Zellen und Zellfragmente durch vorsichtiges Resuspendieren vom Gefäßboden gelöst und in ein Eppendorfreaktionsgefäß transferiert. Die Proteinkonzentration des Lysats wurde mit dem Bradford Proteinassay bestimmt Vorbereitung von Zellpräparaten für die Immunofloureszenz Bei der Immunofloureszenz werden Zellproteine mit spezifischen Antikörper und fluoreszierenden Farbstoffen markiert. Anschließend wurden sie im Floureszenz- Mikroskop sichtbar gemacht. Zellen wurden in 3,5 cm 2 Gefäßen (6-well) auf deren Boden ein steriles Glasplättchen gelegt worden ist mit einer Konfluenz von 30-50% ausgesät und wie oben beschrieben transfektiert. Nach h wurden die Zellen mit sterilen PBS gewaschen und mit 2%igen Paraformaldehyd für 15 min fixiert. Die Zellen wurden für zweimal 5 min mit T-
29 101 Materialien und Methoden PBS und einmal mit PBS gewaschen und mit 3% BSA/PBS für 30 min blockiert. Die primären Antikörper wurden in 3% BSA/PBS verdünnt und die Glasplättchen damit überschichtet. Um ein Austrocknen der Proben zu verhindern wurde ein gleich großes Stück Parafilm auf die Lösung gelegt und die Schale in einer feuchten Kammer für eine Stunde bei Raumtemperatur inkubiert. Die Zellen wurden für zweimal 5 min mit T-PBS und einmal mit PBS gewaschen. Anschließend wurden die Zellen in 3% BSA/PBS mit einer Verdünnung eines spezifischen sekundären Antikörpers, der mit Cy3 bzw. FITC konjugiert war, inkubiert. Die Zellen wurden für zweimal 5 min mit T-PBS und einmal mit PBS gewaschen. Die Kerne der Zellen wurden mit 3 µg/ml DAPI für 15 sec gefärbt und die Zellen für zweimal 5 min mit T-PBS und einmal mit PBS gewaschen. Die Glasplättchen wurden aus den Kulturgefäßen genommen und mit der Zellseite nach unten mit einem kleinen Tropfen Montagemedium luftblasenfrei auf einen Objekträger montiert Proteasom-Inhibition mit ALLN Für den Nachweis der Proteine HA-HD-Q 20, 32 und 37 mit Westernblots wurde zu den transfektierten Zellen der Proteasom-Inhibitor ALLN (N-Acetyl-Leu-Leu-Norleucinal) zugegeben. ALLN ist ein Calpain I Inhibitor, der auch das Proteasom hemmt. Nach Anweisung des Herstellers 100 mg/ml ALLN frisch in DMSO gelöst und den Zellen 8h vor Ernte der transfektierten Zellen dem Medium zugesetzt (Endkonzentration 17 µg/ml).
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS
 Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Molekulare Klonierung Praktikum
 Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
2. Ergebnisse. 15 Ergebnisse Analyse der Aggregation Huntingtin Exon 1 in vitro Herstellung des Vektors pgex-6p-flag
 15 Ergebnisse 2. Ergebnisse 2.1. Analyse der Aggregation Huntingtin Exon 1 in vitro 2.1.1. Herstellung des Vektors pgex-6p-flag Ziel dieser Arbeit ist es zu untersuchen, wie N-terminale Fragmente von Huntingtin
15 Ergebnisse 2. Ergebnisse 2.1. Analyse der Aggregation Huntingtin Exon 1 in vitro 2.1.1. Herstellung des Vektors pgex-6p-flag Ziel dieser Arbeit ist es zu untersuchen, wie N-terminale Fragmente von Huntingtin
SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen
 GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
2.5 Expression von Domänen des rgne-proteins in E.coli
 2.5 Expression von Domänen des rgne-proteins in E.coli Da die Kristallisation des rgne-gesamtproteins erfolglos verlief (2.4.5), wurde alternativ die Expression, Reinigung und Kristallisation der einzelnen
2.5 Expression von Domänen des rgne-proteins in E.coli Da die Kristallisation des rgne-gesamtproteins erfolglos verlief (2.4.5), wurde alternativ die Expression, Reinigung und Kristallisation der einzelnen
Materialien und Methoden...16
 Inhaltsverzeichnis I. Einleitung...1 1. Mitochondrien - Energielieferanten der eukaryontischen Zelle... 1 2. Die mitochondriale DNA-Replikation... 5 2.1. Transkriptionsabhängige mtdna-replikation... 5
Inhaltsverzeichnis I. Einleitung...1 1. Mitochondrien - Energielieferanten der eukaryontischen Zelle... 1 2. Die mitochondriale DNA-Replikation... 5 2.1. Transkriptionsabhängige mtdna-replikation... 5
Zellbiologie und Physiologie Labormethoden der Biologie
 Zellbiologie und Physiologie Labormethoden der Biologie Molekularbiologie I Dr. Stefan Weinl > Molekularbiologie I Plasmidpräparation Transformation Restriktionsverdau Gel-Elektrophorese 1 > Experimenteller
Zellbiologie und Physiologie Labormethoden der Biologie Molekularbiologie I Dr. Stefan Weinl > Molekularbiologie I Plasmidpräparation Transformation Restriktionsverdau Gel-Elektrophorese 1 > Experimenteller
GEBRAUCHSANLEITUNG. Glutatione Agarose Resin
 GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
3,58 g 0,136 g. ad 100 ml
 9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Transformation des Expressionsstammes
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Transformation des Expressionsstammes
Zellbiologie und Physiologie Labormethoden der Biologie
 Zellbiologie und Physiologie Labormethoden der Biologie > Molekularbiologie I Plasmidpräparation Molekularbiologie I Transformation Gel-Elektrophorese Dr. Stefan Weinl > Plasmid-Isolierung aus E. coli
Zellbiologie und Physiologie Labormethoden der Biologie > Molekularbiologie I Plasmidpräparation Molekularbiologie I Transformation Gel-Elektrophorese Dr. Stefan Weinl > Plasmid-Isolierung aus E. coli
Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten
 Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten erstellt vom Unterausschuß Methodenentwicklung des LAG 1. Zweck und Anwendungsbereich
Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten erstellt vom Unterausschuß Methodenentwicklung des LAG 1. Zweck und Anwendungsbereich
aktualisiert, 10.03.2011, Wera Roth, DE1 WESTERN BLOT
 1 aktualisiert, 10.03.2011, Wera Roth, DE1 WESTERN BLOT 1. Hinweise zu Membranen a. Nitrocellulose b. PVDF (alternativ) 2. Aufbau des Transfers a. Naßblot b. Semi-dry (alternativ) 3. Färben und Dokumentation
1 aktualisiert, 10.03.2011, Wera Roth, DE1 WESTERN BLOT 1. Hinweise zu Membranen a. Nitrocellulose b. PVDF (alternativ) 2. Aufbau des Transfers a. Naßblot b. Semi-dry (alternativ) 3. Färben und Dokumentation
2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
 Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
4. Materialien und Methoden
 4. Materialien und Methoden 4.1 Materialien 4.1.1 Bakterienstämme DH10B SCS1-pSE111 F`, mcra?-(mrr hsdrms-mcrbc), f80dlacz?m15,?lacx74, deor, reca1, arad139,?(ara, leu)7697, galu, galk,? -, rpsl, enda1,
4. Materialien und Methoden 4.1 Materialien 4.1.1 Bakterienstämme DH10B SCS1-pSE111 F`, mcra?-(mrr hsdrms-mcrbc), f80dlacz?m15,?lacx74, deor, reca1, arad139,?(ara, leu)7697, galu, galk,? -, rpsl, enda1,
Western Blot. Zuerst wird ein Proteingemisch mit Hilfe einer Gel-Elektrophorese aufgetrennt.
 Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Protokoll Praktikum für Humanbiologie Studenten
 Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Identifizierung eines Protein-Interaktionsnetzwerks für Huntingtin und polyglutaminabhängige Induktion von Hefeprionen
 Identifizierung eines Protein-Interaktionsnetzwerks für Huntingtin und polyglutaminabhängige Induktion von Hefeprionen Dissertation zur Erlangung des akademischen Grades des Doktors der Naturwissenschaften
Identifizierung eines Protein-Interaktionsnetzwerks für Huntingtin und polyglutaminabhängige Induktion von Hefeprionen Dissertation zur Erlangung des akademischen Grades des Doktors der Naturwissenschaften
Bioinformatik I: Grundlagen der Gentechnik
 Bioinformatik I: Grundlagen der Gentechnik Dr. Maik Böhmer Institut für Biologie und Biotechnologie der Pflanzen Schlossplatz 7 Schwerpunkte: Vorlesung 1: Einführung & Enzyme der Gentechnik Vorlesung 2:
Bioinformatik I: Grundlagen der Gentechnik Dr. Maik Böhmer Institut für Biologie und Biotechnologie der Pflanzen Schlossplatz 7 Schwerpunkte: Vorlesung 1: Einführung & Enzyme der Gentechnik Vorlesung 2:
Rekombinante Antikorper. fur,,lab-on-chip"
 Rekombinante Antikorper fur,,lab-on-chip" Von der Fakultat fur Lebenswissenschaften der Technischen Universitat Carolo-Wilhelmina zu Braunschweig zur Erlangung des Grades einer Doktorin der Naturwissenschaften
Rekombinante Antikorper fur,,lab-on-chip" Von der Fakultat fur Lebenswissenschaften der Technischen Universitat Carolo-Wilhelmina zu Braunschweig zur Erlangung des Grades einer Doktorin der Naturwissenschaften
8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung
 8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
3 ERGEBNISSE 3.1 PLASMIDKONSTRUKTIONEN UND -PRÄPARATIONEN
 ERGEBNISSE Die Zielsetzung dieser Arbeit ist es, ein in-vitro-modell zur Bestimmung der Zyto- und Genotoxizität zu konstruieren. Zur Entwicklung des Genotoxizitätsmodells wurde der Vektor pnf-κb/neo unter
ERGEBNISSE Die Zielsetzung dieser Arbeit ist es, ein in-vitro-modell zur Bestimmung der Zyto- und Genotoxizität zu konstruieren. Zur Entwicklung des Genotoxizitätsmodells wurde der Vektor pnf-κb/neo unter
6.3 Arbeiten mit Proteinen
 6 Methoden 47 6.3 Arbeiten mit Proteinen 6.3.1 Außenmembranproteinpräparation Um die Lokalisierung der Autotransporterproteine zu überprüfen, müssen die einzelnen Kompartimente der Bakterienzelle voneinander
6 Methoden 47 6.3 Arbeiten mit Proteinen 6.3.1 Außenmembranproteinpräparation Um die Lokalisierung der Autotransporterproteine zu überprüfen, müssen die einzelnen Kompartimente der Bakterienzelle voneinander
Modifizierte Gene Editor Mutagenese
 Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
3 GFP green fluorescent protein
 SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Gentechnologie: Isolierung und Charakterisierung von DNA
 Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Tab. 2-1: TKZT-Zelllinien, Herkunft, histologische Eigenschaften und Referenzen
 Material 28 2 MATERIAL 2.1 Zelllinien In der vorliegenden Studie wurden etablierte Zelllinien von nichtseminomatösen TKZT untersucht. Die Untersuchungen wurden zunächst an den drei Zelllinien H12.1, 2102EP
Material 28 2 MATERIAL 2.1 Zelllinien In der vorliegenden Studie wurden etablierte Zelllinien von nichtseminomatösen TKZT untersucht. Die Untersuchungen wurden zunächst an den drei Zelllinien H12.1, 2102EP
Phalloidin-Färbung an kultivierten adhärenten Säugerzellen. Formaldehyd-Fixierung
 Phalloidin-Färbung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen. Hier
Phalloidin-Färbung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen. Hier
7 Anhang. Tabelle I: Zusammensetzung der Restriktionsansätze.
 7 Anhang Tabelle I: Zusammensetzung der Restriktionsansätze. Reagenz Konzentration Volumen je Endkonzentration der Stammlösung Reaktionansatz Reaktionspuffer 10x NEB-Puffer 2 1.50 µl 1x MseI 4 U/µl 0.30
7 Anhang Tabelle I: Zusammensetzung der Restriktionsansätze. Reagenz Konzentration Volumen je Endkonzentration der Stammlösung Reaktionansatz Reaktionspuffer 10x NEB-Puffer 2 1.50 µl 1x MseI 4 U/µl 0.30
Bioanalytik-Vorlesung Western-Blot. Vorlesung Bioanalytik/ Westfälische Hochschule WS 1015/16
 Bioanalytik-Vorlesung Western-Blot Vorlesung Bioanalytik/ Westfälische Hochschule WS 1015/16 Western-Blot Western-Blot: Übertragung von elektrophoretisch aufgetrennten Proteinen auf eine Membran und Nachweis
Bioanalytik-Vorlesung Western-Blot Vorlesung Bioanalytik/ Westfälische Hochschule WS 1015/16 Western-Blot Western-Blot: Übertragung von elektrophoretisch aufgetrennten Proteinen auf eine Membran und Nachweis
Gentechnologie: Klonierung und Transformation von DNA
 Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
RESOLUTION OENO 24/2004 NACHWEIS VON EIWEISSSTOFFEN PFLANZLICHER HERKUNFT IN WEIN UND MOST
 NACHWEIS VON EIWEISSSTOFFEN PFLANZLICHER HERKUNFT IN WEIN UND MOST DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf 2 IV des Gründungsübereinkommens vom 3. April 2001 der Internationalen
NACHWEIS VON EIWEISSSTOFFEN PFLANZLICHER HERKUNFT IN WEIN UND MOST DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf 2 IV des Gründungsübereinkommens vom 3. April 2001 der Internationalen
5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp)
 8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
SCRIPTUM HIGH PRECISE
 Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
Pflanze direkt 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
GEIM- TECHIMOLOGISCHE ARBEITSMETHODEN
 GEIM- TECHIMOLOGISCHE ARBEITSMETHODEN Ein Handbuch experimenteller Techniken und Verfahren Herausgegeben von Rudolf Hagemann Bearbeitet von Frank Baldauf, Jörn Belter, Sabine Brantl, Baimund Eck, Karsten
GEIM- TECHIMOLOGISCHE ARBEITSMETHODEN Ein Handbuch experimenteller Techniken und Verfahren Herausgegeben von Rudolf Hagemann Bearbeitet von Frank Baldauf, Jörn Belter, Sabine Brantl, Baimund Eck, Karsten
1. Proteinnachweis mit Bradford-Farbreagenz
 1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen
 F2-Praktikum Genetik Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen Gruppe 4 (Susanne Duncker, Kristin Hofmann) Einleitung Wir untersuchten in diesem Versuch die Effizienz der VDJ-Rekombination
F2-Praktikum Genetik Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen Gruppe 4 (Susanne Duncker, Kristin Hofmann) Einleitung Wir untersuchten in diesem Versuch die Effizienz der VDJ-Rekombination
SERVA Ni-NTA Magnetic Beads
 GEBRAUCHSANLEITUNG SERVA Ni-NTA Magnetic Beads Magnetbeads zur Affinitätsreinigung von His-Tag-Fusionsproteinen (Kat.-Nr. 42179) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg Phone +49-6221-138400,
GEBRAUCHSANLEITUNG SERVA Ni-NTA Magnetic Beads Magnetbeads zur Affinitätsreinigung von His-Tag-Fusionsproteinen (Kat.-Nr. 42179) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg Phone +49-6221-138400,
Modul 5 Praktikum Western Blotting, Krauß / Lamparter, für Biologie 4. Semester Sommersemester 2017
 Modul 5 Praktikum Western Blotting, Krauß / Lamparter, für Biologie 4. Semester Sommersemester 2017 Einteilung in 2 Untergruppen, beide arbeiten parallel. 1. Tag: Gele gießen (1 h), Vorbesprechung (1 h),
Modul 5 Praktikum Western Blotting, Krauß / Lamparter, für Biologie 4. Semester Sommersemester 2017 Einteilung in 2 Untergruppen, beide arbeiten parallel. 1. Tag: Gele gießen (1 h), Vorbesprechung (1 h),
(Nur für die Forschung) Bei Kontakt mit Augen oder Haut sofort mit viel Wasser abspülen!
 Datenblatt Artikel-Nr. 56.200.0010 10 Aufreinigungen 56.200.0050 50 Aufreinigungen 56.200.0250 250 Aufreinigungen (Nur für die Forschung) Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und
Datenblatt Artikel-Nr. 56.200.0010 10 Aufreinigungen 56.200.0050 50 Aufreinigungen 56.200.0250 250 Aufreinigungen (Nur für die Forschung) Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und
Biochemie und. chemischer Mechanismus
 Dissertation zur Erlangung des Doktorgrades der Fakultät für Chemie und Pharmazie der Ludwig-Maximilians-Universität München Biochemie und chemischer Mechanismus der Thiomethylierung von RNA Dorothea Maria
Dissertation zur Erlangung des Doktorgrades der Fakultät für Chemie und Pharmazie der Ludwig-Maximilians-Universität München Biochemie und chemischer Mechanismus der Thiomethylierung von RNA Dorothea Maria
Antibiotika sind oft Inhibitoren der Genexpression
 Antibiotika sind oft Inhibitoren der Genexpression Inhibitoren der Transkription: Rifampicin, Actinomycin α-amanitin Inhibitoren der Translation: Puromycin, Streptomycin, Tetracycline, Chloramphenicol
Antibiotika sind oft Inhibitoren der Genexpression Inhibitoren der Transkription: Rifampicin, Actinomycin α-amanitin Inhibitoren der Translation: Puromycin, Streptomycin, Tetracycline, Chloramphenicol
DNA Isolierung. Praktikum Dr. László Kredics
 Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
Kerstin Brachhold (Autor) Das Basalapparat-Subproteom von Chlamydomonas reinhardtii
 Kerstin Brachhold (Autor) Das Basalapparat-Subproteom von Chlamydomonas reinhardtii https://cuvillier.de/de/shop/publications/1867 Copyright: Cuvillier Verlag, Inhaberin Annette Jentzsch-Cuvillier, Nonnenstieg
Kerstin Brachhold (Autor) Das Basalapparat-Subproteom von Chlamydomonas reinhardtii https://cuvillier.de/de/shop/publications/1867 Copyright: Cuvillier Verlag, Inhaberin Annette Jentzsch-Cuvillier, Nonnenstieg
Hochdurchsatz Generierung und Analyse von Arabidopsis thaliana-proteinen
 MAX-PLANCK-INSTITUT FÜR MOLEKULARE GENETIK Hochdurchsatz Generierung und Analyse von Arabidopsis thaliana-proteinen Dissertation zur Erlangung der Doktorwürde des Fachbereichs Biologie, Chemie, Pharmazie
MAX-PLANCK-INSTITUT FÜR MOLEKULARE GENETIK Hochdurchsatz Generierung und Analyse von Arabidopsis thaliana-proteinen Dissertation zur Erlangung der Doktorwürde des Fachbereichs Biologie, Chemie, Pharmazie
Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA
 Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
Vorlesung LV-Nr Molekularbiologie für Agrarwissenschaften. J. Glößl, SS 2007
 Vorlesung LV-Nr. 954.104 Molekularbiologie für Agrarwissenschaften J. Glößl, SS 2007 Thematik: Molekularbiologische Methoden Teil 2 Die ppt Folien wurden freundlicherweise von Prof. Florian Rüker aus der
Vorlesung LV-Nr. 954.104 Molekularbiologie für Agrarwissenschaften J. Glößl, SS 2007 Thematik: Molekularbiologische Methoden Teil 2 Die ppt Folien wurden freundlicherweise von Prof. Florian Rüker aus der
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila
 Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
SERVA IMAC Zn- and Cu-IDA Test Kit Agarosematrix zur Affinitätsreinigung von His-Tag-Fusionsporteinen
 GEBRAUCHSANLEITUNG SERVA IMAC Zn- and Cu-IDA Test Kit Agarosematrix zur Affinitätsreinigung von His-Tag-Fusionsporteinen (Kat.-Nr. 42170, 42171) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA IMAC Zn- and Cu-IDA Test Kit Agarosematrix zur Affinitätsreinigung von His-Tag-Fusionsporteinen (Kat.-Nr. 42170, 42171) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
Abbildung 1: Schematische Darstellung der Domänenorganisation von Survivin
 Abbildung 1: Schematische Darstellung der Domänenorganisation von Survivin Survivin weist eine N-terminale BIR-Domäne (grün) und eine C-terminale α-helix (blau) auf. Das intrinsische nuclear export signal
Abbildung 1: Schematische Darstellung der Domänenorganisation von Survivin Survivin weist eine N-terminale BIR-Domäne (grün) und eine C-terminale α-helix (blau) auf. Das intrinsische nuclear export signal
Biochemisches Praktikum SS07, Versuch II: Reinigung eines rekombinanten Proteins
 VERSUCH II: REINIGUNG EINES REKOMBINANTEN PROTEINS AUS ESCHERICHIA COLI Literatur: Einschlägige Biochemie und Genetik Lehrbücher. Sambrook and Russel: Molecular Cloning, 3rd Edition (2001) Prinzip: In
VERSUCH II: REINIGUNG EINES REKOMBINANTEN PROTEINS AUS ESCHERICHIA COLI Literatur: Einschlägige Biochemie und Genetik Lehrbücher. Sambrook and Russel: Molecular Cloning, 3rd Edition (2001) Prinzip: In
Untersuchungen zur Wirkung von Pasteurella multocida Toxin
 Institut fiir Experimentelle und Klinische Pharmakologie und Toxikologie der Albert-Ludwigs-Universitat Freiburg Untersuchungen zur Wirkung von Pasteurella multocida Toxin Dissertation zur Erlangung des
Institut fiir Experimentelle und Klinische Pharmakologie und Toxikologie der Albert-Ludwigs-Universitat Freiburg Untersuchungen zur Wirkung von Pasteurella multocida Toxin Dissertation zur Erlangung des
Modul 4 SS 2015. Western Blot. Tag 1: Proteinbestimmung, SDS-PAGE-Gel-Herstellung S. 3. Tag 2: Gelelektrophorese, Western Blot, Blockierung S.
 Modul 4 SS 2015 Western Blot Tag 1: Proteinbestimmung, SDS-PAGE-Gel-Herstellung S. 3 Tag 2: Gelelektrophorese, Western Blot, Blockierung S. 6 Tag 3: Detektion der Proteine auf der Membran S. 10 1 Über
Modul 4 SS 2015 Western Blot Tag 1: Proteinbestimmung, SDS-PAGE-Gel-Herstellung S. 3 Tag 2: Gelelektrophorese, Western Blot, Blockierung S. 6 Tag 3: Detektion der Proteine auf der Membran S. 10 1 Über
S-Dis Hotstart Polymerase
 Datenblatt Artikel-Nr. BS91.219.0200 Artikel-Nr. BS91.219.1000 200 Units 1000 Units (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen: Farbe: 1 Beschreibung Die
Datenblatt Artikel-Nr. BS91.219.0200 Artikel-Nr. BS91.219.1000 200 Units 1000 Units (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen: Farbe: 1 Beschreibung Die
3 Methoden. 3.1 Zellkultivierung
 Kap. 3 Methoden 15 3 Methoden 3.1 Zellkultivierung Zur Anzucht von Zellkulturen wurden sterile Zellkulturflaschen (25 ml oder 250 ml) verwendet. Die Kultivierung erfolgte mit RPMI-1640 Medium bei 37 C,
Kap. 3 Methoden 15 3 Methoden 3.1 Zellkultivierung Zur Anzucht von Zellkulturen wurden sterile Zellkulturflaschen (25 ml oder 250 ml) verwendet. Die Kultivierung erfolgte mit RPMI-1640 Medium bei 37 C,
Plasmidpräparation aus Bakterien Inhalt
 Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
F-I Molekulare Zoologie: Teil I: Expressionsanalysen. Expressionsanalyse mittels RT-PCR
 F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014
 Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014 Tag 1 PCR Die Polymerase-Kettenreaktion (engl. polymerase chain reaction) ermöglicht die selektive
Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014 Tag 1 PCR Die Polymerase-Kettenreaktion (engl. polymerase chain reaction) ermöglicht die selektive
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen. Formaldehyd-Fixierung
 Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu
Reagenzien Isolierung von Nukleinsäuren
 Aufbewahrung bei Raumtemperatur Anwendung Isolierung ultrareiner Plasmid-DNA aus Bakterienkulturen von 1 ml bis 800 ml. Die Plasmid-DNA eignet sich für Manuelle und automatisierte Sequenzierung mit Fluoreszenzfarbstoffen
Aufbewahrung bei Raumtemperatur Anwendung Isolierung ultrareiner Plasmid-DNA aus Bakterienkulturen von 1 ml bis 800 ml. Die Plasmid-DNA eignet sich für Manuelle und automatisierte Sequenzierung mit Fluoreszenzfarbstoffen
https://cuvillier.de/de/shop/publications/2978
 Andreas Christmann (Autor) Zur bakteriellen Oberflächenpräsentation kombinatorischer Peptidbibliotheken und deren Anwendung auf Fragestellungen der Immunologie, Molekularbiologie und der Molekualren Medizin
Andreas Christmann (Autor) Zur bakteriellen Oberflächenpräsentation kombinatorischer Peptidbibliotheken und deren Anwendung auf Fragestellungen der Immunologie, Molekularbiologie und der Molekualren Medizin
2 Material. 2.1 Stammlösungen und Puffer. 2 Material. 10x Dephosphorylierungspuffer 0,5 M Tris-Cl ph 8,5; 50 mm MgCl 2
 2 Material 2.1 Stammlösungen und Puffer 10x Dephosphorylierungspuffer 0,5 M Tris-Cl ph 8,5; 50 mm MgCl 2 0,5 M IPTG (Isopropyl-β-D-Thiogalactopyranosid) 5.96 g IPTG in 50 ml ddh 2 O; steril filtriert Lysispuffer
2 Material 2.1 Stammlösungen und Puffer 10x Dephosphorylierungspuffer 0,5 M Tris-Cl ph 8,5; 50 mm MgCl 2 0,5 M IPTG (Isopropyl-β-D-Thiogalactopyranosid) 5.96 g IPTG in 50 ml ddh 2 O; steril filtriert Lysispuffer
MPP Multiplex 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Ein interessanter und arbeitsreicher Tag im livfe Biolab in Darmstadt
 Ein interessanter und arbeitsreicher Tag im livfe Biolab in Darmstadt Als einer der ersten Kurse überhaupt durfte der Biologieleistungskurs der Alfred-Delp-Schule unter Kursleitung von Sven Remdisch das
Ein interessanter und arbeitsreicher Tag im livfe Biolab in Darmstadt Als einer der ersten Kurse überhaupt durfte der Biologieleistungskurs der Alfred-Delp-Schule unter Kursleitung von Sven Remdisch das
Versuchsprotokoll Klonierung eines amplifizierten PCR-Fragments. 0 Inhaltsverzeichnis
 0 Inhaltsverzeichnis 0 Inhaltsverzeichnis...- 1-1 Einleitung...- 2-2 Versuch...- 2-2.1 Versuchsteil 4.2.3.-4.2.4. (PCR und Gel der cdna)...- 2-2.1.1 Einleitung...- 2-2.1.2 Durchführung...- 2-2.1.3 Auswertung...-
0 Inhaltsverzeichnis 0 Inhaltsverzeichnis...- 1-1 Einleitung...- 2-2 Versuch...- 2-2.1 Versuchsteil 4.2.3.-4.2.4. (PCR und Gel der cdna)...- 2-2.1.1 Einleitung...- 2-2.1.2 Durchführung...- 2-2.1.3 Auswertung...-
Inhaltsverzeichnis. Polymerase Chain Reaction Theoretischer Hintergrund - 2 -
 Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Grundlagen der Klonierung. Analytische Methoden der Biologie SS09 7 Klonierung und Gentechnik. Modul
 Restriktion und Ligation: Restriktion und Ligation: Grundlagen der Klonierung Modul 2303-021 1 Restriktion und Ligation Verknüpfung von Fragmenten unterschiedlicher DNA Herkunft Restriktion und Ligation
Restriktion und Ligation: Restriktion und Ligation: Grundlagen der Klonierung Modul 2303-021 1 Restriktion und Ligation Verknüpfung von Fragmenten unterschiedlicher DNA Herkunft Restriktion und Ligation
PROTEINBESTIMMUNG. Vergleich Bradford und BCA
 PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
SERVALight EosUltra Western Blot Chemilumineszenz HRP Substrat Kit
 GEBRAUCHSANLEITUNG SERVALight EosUltra Western Blot Chemilumineszenz HRP Substrat Kit (Kat.-Nr. 42586) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG SERVALight EosUltra Western Blot Chemilumineszenz HRP Substrat Kit (Kat.-Nr. 42586) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
2 Materialien. Materialien 15. 2.1 Histondeacetylaseinhibitoren (HDIs) Sigma-Aldrich, Deutschland. 2.2 Zelllinien und Zellkultur.
 Materialien 15 2 Materialien 2.1 Histondeacetylaseinhibitoren (HDIs) Substanz Butyrat Trichostatin A (TSA) Valproat Hersteller Sigma-Aldrich, Sigma-Aldrich, Sigma-Aldrich, 2.2 Zelllinien und Zellkultur
Materialien 15 2 Materialien 2.1 Histondeacetylaseinhibitoren (HDIs) Substanz Butyrat Trichostatin A (TSA) Valproat Hersteller Sigma-Aldrich, Sigma-Aldrich, Sigma-Aldrich, 2.2 Zelllinien und Zellkultur
1. EINLEITUNG Der eukaryontische Translationsinitiationsfaktor 5A (eif5a) Der Polyaminbiosyntheseinhibitor Agmatin...
 1. EINLEITUNG... 14 1.1 Lebenszyklus der Malaria Erreger Plasmodium falciparum und Plasmodium vivax... 16 1.2 Molekulares Targeting... 18 1.2.1 Die alternative Fettesäurebiosynthese II in Plasmodium falciparum...
1. EINLEITUNG... 14 1.1 Lebenszyklus der Malaria Erreger Plasmodium falciparum und Plasmodium vivax... 16 1.2 Molekulares Targeting... 18 1.2.1 Die alternative Fettesäurebiosynthese II in Plasmodium falciparum...
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers (4) Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Proteinreinigung Techniken & Methoden der Proteinreinigung
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers (4) Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Proteinreinigung Techniken & Methoden der Proteinreinigung
AUFGABENSAMMLUNG. Restriktionsenzyme. Füllen Sie den Lückentext aus. Gentechnik Schroedel, Braunschweig
 Restriktionsenzyme Füllen Sie den Lückentext aus. PCR 1a Mit dem folgenden Quiz können Sie Ihr Wissen zum Thema PCR überprüfen. Klicken Sie jeweils die richtige Antwort an. PCR 1b Mit dem folgenden Quiz
Restriktionsenzyme Füllen Sie den Lückentext aus. PCR 1a Mit dem folgenden Quiz können Sie Ihr Wissen zum Thema PCR überprüfen. Klicken Sie jeweils die richtige Antwort an. PCR 1b Mit dem folgenden Quiz
SERVA IDA LD Agarose
 GEBRAUCHSANLEITUNG SERVA IDA LD Agarose Agarose zur Affinitätsreinigung von His-Tag-Fusionsproteinen (Kat.-Nr. 42144, 42145, 42146, 42147) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA IDA LD Agarose Agarose zur Affinitätsreinigung von His-Tag-Fusionsproteinen (Kat.-Nr. 42144, 42145, 42146, 42147) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
2. Material und Lösungen 2.1. Material
 Material und Lösungen 19 2. Material und Lösungen 2.1. Material 2.1.1. Gebrauchswaren Filmmaterial...Polaroid Glaspipetten...Hirschmann Laborgeräte Reaktionsgefäße, Plastikwaren...Greiner Labortechnik
Material und Lösungen 19 2. Material und Lösungen 2.1. Material 2.1.1. Gebrauchswaren Filmmaterial...Polaroid Glaspipetten...Hirschmann Laborgeräte Reaktionsgefäße, Plastikwaren...Greiner Labortechnik
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen. Methanol-Fixierung
 Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Methanol-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen.
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Methanol-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen.
Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres (Marmota monax)
 Aus der Abteilung Innere Medizin II der Medizinischen Universitätsklinik der Albert-Ludwigs-Universität Freiburg im Breisgau Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres
Aus der Abteilung Innere Medizin II der Medizinischen Universitätsklinik der Albert-Ludwigs-Universität Freiburg im Breisgau Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres
4 Methoden METHODEN Zellkultur Zellkulturmedien
 METHODEN 25 4 Methoden 4.1 Zellkultur 4.1.1 Zellkulturmedien Die Zellen wurden in folgenden Medien kultiviert: 5583-S, DLD1, SW480, LS174T und HCT116 in DMEM + 10% FCS. HT 29, CSC-1, NCM460 in RPMI + 10%
METHODEN 25 4 Methoden 4.1 Zellkultur 4.1.1 Zellkulturmedien Die Zellen wurden in folgenden Medien kultiviert: 5583-S, DLD1, SW480, LS174T und HCT116 in DMEM + 10% FCS. HT 29, CSC-1, NCM460 in RPMI + 10%
6 Anhang Verzeichnis häufig gebrauchter Lösungen und Puffer
 6 Anhang 85 6 Anhang 6.1 Verzeichnis häufig gebrauchter Lösungen und Puffer Alkoholreihe (30%, 70%, 90%, 100% Ethanol) Zur Vereinfachung wurde das käufliche 98,8%- Ethanol als 100%-ig gesetzt. Die entsprechenden
6 Anhang 85 6 Anhang 6.1 Verzeichnis häufig gebrauchter Lösungen und Puffer Alkoholreihe (30%, 70%, 90%, 100% Ethanol) Zur Vereinfachung wurde das käufliche 98,8%- Ethanol als 100%-ig gesetzt. Die entsprechenden
Protokoll Versuch A1 Klonierung des Tyro3-D1D2-Fragments mittels PCR
 Protokoll Versuch A1 Klonierung des Tyro3-D1D2-Fragments mittels PCR Gruppe 8 Susanne Duncker und Friedrich Hahn Einleitung und Aufgabenstellung Ziel dieses Versuchs ist es, das Gen für ein bestimmtes
Protokoll Versuch A1 Klonierung des Tyro3-D1D2-Fragments mittels PCR Gruppe 8 Susanne Duncker und Friedrich Hahn Einleitung und Aufgabenstellung Ziel dieses Versuchs ist es, das Gen für ein bestimmtes
PAGE POLYACRYLAMIDGELELEKTROPHORESE
 PAGE POLYACRYLAMIDGELELEKTROPHORESE In der modernen Bioanalytik stellt die Gelelektrophorese immer noch eine Technik dar, die durch keine andere ersetzt werden kann. Vertikale Gele werden dabei i.d.r.
PAGE POLYACRYLAMIDGELELEKTROPHORESE In der modernen Bioanalytik stellt die Gelelektrophorese immer noch eine Technik dar, die durch keine andere ersetzt werden kann. Vertikale Gele werden dabei i.d.r.
3.2. Untersuchungen zu Protein-Protein-Interaktionen der GNE
 3.2. Untersuchungen zu Protein-Protein-Interaktionen der GNE 3.2.1. Valosin-Containing-Protein (VCP, p97) Das bei der erblichen Einschlußkörperchenmyositis (h-ibm) krankheitsverursachende Gen ist das der
3.2. Untersuchungen zu Protein-Protein-Interaktionen der GNE 3.2.1. Valosin-Containing-Protein (VCP, p97) Das bei der erblichen Einschlußkörperchenmyositis (h-ibm) krankheitsverursachende Gen ist das der
1 µl BamHI H 2 O 21 µl H 2 O 30 µl Volumen 18 µl H 2 O 30 µl Inkubation 2h @ 37 C 2h @ 37 C
 F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
1 Einleitung... 13. 1.1 Staphylokokken... 13. 1.2 Koagulase-negative Staphylokokken... 13. 1.4 MSCRAMM-Proteine... 16. 1.5 LPXTG-Motive...
 Inhaltsverzeichnis 1 Einleitung... 13 1.1 Staphylokokken... 13 1.2 Koagulase-negative Staphylokokken... 13 1.3 Staphylococcus saprophyticus... 14 1.4 MSCRAMM-Proteine... 16 1.5 LPXTG-Motive... 16 1.6 Oberflächenassoziierte
Inhaltsverzeichnis 1 Einleitung... 13 1.1 Staphylokokken... 13 1.2 Koagulase-negative Staphylokokken... 13 1.3 Staphylococcus saprophyticus... 14 1.4 MSCRAMM-Proteine... 16 1.5 LPXTG-Motive... 16 1.6 Oberflächenassoziierte
4. Methoden. 4.1 Molekularbiologische Methoden
 4. Methoden 4.1 Molekularbiologische Methoden Extraktion und Ethanolfällung von DNA oder RNA Die zu extrahierende DNA oder RNA wurde mit einem Volumen Phenol/Chloroform/Isoamylalkohol versetzt, stark gevortext
4. Methoden 4.1 Molekularbiologische Methoden Extraktion und Ethanolfällung von DNA oder RNA Die zu extrahierende DNA oder RNA wurde mit einem Volumen Phenol/Chloroform/Isoamylalkohol versetzt, stark gevortext
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016
 Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 7 (11.07-15.07.) Methoden und Techniken II 1. Sie bekommen
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 7 (11.07-15.07.) Methoden und Techniken II 1. Sie bekommen
Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013
 Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013 Projekt: Zellbiologie: Expression und Reinigung der onkogenen Kinase Abl an der Ecole Polytechnique Fédérale de Lausanne, EPFL
Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013 Projekt: Zellbiologie: Expression und Reinigung der onkogenen Kinase Abl an der Ecole Polytechnique Fédérale de Lausanne, EPFL
Jens Tilsner (Autor) Aminosäuretransport in Raps unter besonderer Berücksichtigung des Entwicklungsstadiums der Pflanze und der Stickstoffdüngung
 Jens Tilsner (Autor) Aminosäuretransport in Raps unter besonderer Berücksichtigung des Entwicklungsstadiums der Pflanze und der Stickstoffdüngung https://cuvillier.de/de/shop/publications/3133 Copyright:
Jens Tilsner (Autor) Aminosäuretransport in Raps unter besonderer Berücksichtigung des Entwicklungsstadiums der Pflanze und der Stickstoffdüngung https://cuvillier.de/de/shop/publications/3133 Copyright:
2 Material und Methoden
 Material und Methoden 24 2 Material und Methoden 2.1 Material 2.1.1 Laborgeräte Kühl- und Tiefkühlschrank (-20 C) Zentrifugen: Tischzentrifuge 5415C Avanti J20 Avanti J25 Sigma 4K15C Elektroporator (Gene
Material und Methoden 24 2 Material und Methoden 2.1 Material 2.1.1 Laborgeräte Kühl- und Tiefkühlschrank (-20 C) Zentrifugen: Tischzentrifuge 5415C Avanti J20 Avanti J25 Sigma 4K15C Elektroporator (Gene
SERVA Lightning Sci2. SERVA Lightning Sci3. SERVA Lightning Sci5. SERVA Lightning SciDye Set
 GEBRAUCHSANLEITUNG SERVA Lightning Sci2 (Kat.-Nr. 43404) SERVA Lightning Sci3 (Kat.-Nr. 43405) SERVA Lightning Sci5 (Kat.-Nr. 43406) SERVA Lightning SciDye Set (Kat.-Nr. 43407) Fluoreszenzfarbstoffe für
GEBRAUCHSANLEITUNG SERVA Lightning Sci2 (Kat.-Nr. 43404) SERVA Lightning Sci3 (Kat.-Nr. 43405) SERVA Lightning Sci5 (Kat.-Nr. 43406) SERVA Lightning SciDye Set (Kat.-Nr. 43407) Fluoreszenzfarbstoffe für
Plasmid DNA purification
 Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
F-I Molekulare Zoologie: Teil II: Expressionsanalysen. Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse
 F-I Molekulare Zoologie: Teil II: Expressionsanalysen Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse Inhalt: Seite I. Allgemeines 1 II. Durchführung der Elektrophorese
F-I Molekulare Zoologie: Teil II: Expressionsanalysen Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse Inhalt: Seite I. Allgemeines 1 II. Durchführung der Elektrophorese
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen Vorbereitung auf diesen Praktikumsteil: Organisation 2. Praktikumstag: - Für den Bioinformatik-Teil benötigen Sie am 2. Tag dieses
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen Vorbereitung auf diesen Praktikumsteil: Organisation 2. Praktikumstag: - Für den Bioinformatik-Teil benötigen Sie am 2. Tag dieses
MODULE für den SCHULKOFFER GENTECHNIK
 MODULE für den SCHULKOFFER GENTECHNIK Modul 1 - DNA-Bastel-Set Zusammenbau eines Papiermodells in Form einer Doppelhelix sehr einfach, Unterstufe, ohne Koffer möglich Modul 2 - DNA-Isolierung aus Gemüse
MODULE für den SCHULKOFFER GENTECHNIK Modul 1 - DNA-Bastel-Set Zusammenbau eines Papiermodells in Form einer Doppelhelix sehr einfach, Unterstufe, ohne Koffer möglich Modul 2 - DNA-Isolierung aus Gemüse
Kapillarelektrophorese DNA-Sequenzierung
 Kapillarelektrophorese DNA-Sequenzierung DNA Kettenanalyse oder DNA-Sequenzierung wird bei der Anordnung der Primärstruktur und Bestimmung der Nukleotid-Basensequenz verwendet. Die Analyse basiert auf
Kapillarelektrophorese DNA-Sequenzierung DNA Kettenanalyse oder DNA-Sequenzierung wird bei der Anordnung der Primärstruktur und Bestimmung der Nukleotid-Basensequenz verwendet. Die Analyse basiert auf
1 EINLEITUNG Epilepsie Fokale Epilepsie und Temporallappen-Epilepsie... 2
 Inhaltsverzeichnis 1 EINLEITUNG... 1 1.1 Epilepsie... 1 1.2 Fokale Epilepsie und Temporallappen-Epilepsie... 2 1.3 Neuropathologie der Fokalen Epilepsie... 3 1.3.1 Ammonshornsklerose...4 1.3.2 Glioneuronale
Inhaltsverzeichnis 1 EINLEITUNG... 1 1.1 Epilepsie... 1 1.2 Fokale Epilepsie und Temporallappen-Epilepsie... 2 1.3 Neuropathologie der Fokalen Epilepsie... 3 1.3.1 Ammonshornsklerose...4 1.3.2 Glioneuronale
4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd30-igg1-tnf- Fusionsproteins
 ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
