1. Nomenklatur (Fettgedruckt...IUPAC Namen) 1.1. Alkane
|
|
|
- Gotthilf Bergmann
- vor 7 Jahren
- Abrufe
Transkript
1 rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG. omenklatur (Fettgedruckt...IUPA amen).. Alkane Die längste Kohlenstoffkette wird bestimmt und daraus ergibt sich der ame Alkan: Methan, Ethan, Propan, Butan, Pentan, exan, eptan, ctan, onan, Decan, Undecan,... Diese längste Kette wird durchnummeriert, sodass die erste Verzweigung die niedrigste Ziffer bekommt. Die kürzeren Kohlenwasserstoffseitenketten werden als Alkyl- bezeichnet. (Sind auch die Seitenketten verzweigt, werden sie in Klammer gesetzt und die ummerierung beginnt am -Atom neben der auptkette) In Klammer gesetzte Regeln und Beispiele sind nicht Stoff der Prüfung. Beispiele: 6 5,6-Dimethyl--ethyloctan -Methylhexan 5-(,-Dimethylpropyl)decan.. yclische Alkane yclopropan (-Ring), yclobutan, yclopentan, yclohexan,.. Bei disubstituierten ycloalkanen tritt die cis-trans Stereoisomerie auf. trans-,-dimethylcyclopentan cis-yclohexan-,-diol cis-,-dihydroxycyclohexan.. Alkene, Alkine Alkene werden wie Alkane benannt und die Doppelbindungen werden mit en (-dien, -trien, -tetraen) bezeichnet, wobei die Ziffer sich auf das. Atom der Doppelbindung bezieht. Stereoisomerien an den Doppelbindungen werden jeweils mit Z o. E gekennzeichnet, wobei an jedem Ende die Substituenten nach der Priorität gereiht werden sind die beiden größeren Substituenten auf derselben Seite (zusammen) ist die Stereoisomerie Z (sonst E). Bei symmetrischen Alkenen, kann man auch noch cis, trans als Unterscheidung der Stereoisomeren verwenden. Alkine werden mit in bezeichnet a b b a Ethylen Ethen,-Dimethyl--buten,-Butadien Buta-,-dien (E)--Methyl--hexen Acetylen Ethin -Methyl--butin (Z)--Penten--in trans -Buten (E)--Buten Ass.Prof. Dr. Daniel Krois
2 rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG.. Alkylhalogenide u.a. Derivate Diese Verbindungen werden als Derivate der Kohlenwasserstoffe benannt. Die Reihung ist alphabetisch. ier nur einige Beispiele: l l l l Tetrachlorkohlenstoff Tetrachlormethan hloroform Trichlormethan Methylenchlorid Dichlormethan -om--chlor--methylpentan.5. Alkohole Alkohole werden entweder als Kohlenwasserstoffe mit der Endsilbe (Suffix) ol bezeichnet, können bei komplexeren Strukturen aber auch mit dem Gruppennamen (Präfix) als hydroxy- Derivate benannt werden. Methylalkohol Methanol Isopropylalkohol -Propanol oder Propan--ol tert-butylalkohol tert-butanol -Methyl--propanol,-Butandiol! Diastereomere : RS-omenklatur But--en--ol ol>en in ummerierung.6. Ether ach der älteren omenklatur benennt man die beiden Alkylgruppen und hängt den Ausdruck ether an. ach IUPA werden die Ether als Alkoxyalkane benannt: Diethylether Ethoxyethan tert-butylmethylether -Methoxy--methylpropan Ethylenglycoldimethylether,-Dimethoxyethan Anisol Phenylmethylether Methoxybenzol.. Aldehyde, Ketone Aldehyde werden als Alkan mit der Endung al benannt (stets Position ), Ketone mit der Endung on. (Ist das für die amensgebung zu kompliziert kann die Aldehydgruppe mit -carbaldehyd bezeichnet werden, die = Gruppe kann als oxo- benannt werden).(in einer veralteten omenklatur werden Ketone als Alkylalkylketone benannt. Aceton wäre demnach Dimethylketon) Formaldehyd Methanal Aceton -Propanon Acetaldehyd Ethanal Pentan-,-dion -Methylpent--enal (Propiophenon) -Phenylpropan--on (E)--ydroxy--methyl--octen--on Benzaldehyd Phenylmethanal Benzolcarbaldehyd Universität Wien, Fakultät f. hemie, Ass.Prof. Dr. Daniel Krois
3 .8. arbonsäuren rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG arbonsäuren werden als Alkansäuren bezechnet. Als Substituent an z.b. ycloalkanen wird die Gruppe als carbonsäure benannt. Ameisensäure formic acid Methansäure Essigsäure acetic acid Ethansäure -Methylpentansäure Bernsteinsäure succinic acid Butandisäure Acrylsäure Propensäure yclohexancarbonsäure Benzoesäure Benzolcarbonsäure.9. arbonsäurederivate (arbonsäurehalogenide werden als Alkanoylhalogenide bezeichnet, die Gruppe (=)-X wird als arbonylhalogenid bezeichnet). arbonsäureanhydride heißen Alkansäureanhydride. l Propionsäurebromid Benzoylchlorid Essigsäureanhydrid -Methylpropansäureanhydrid Propanoylbromid Benzolcarbonylchlorid Acetanhydrid arbonsäureester: werden als Alkancarbonsäurealkylester oder Alkylalkanoate bezeichnet: Essigsäureethylester Ethylacetat Isobuttersäuremethylester Methyl--methylpropanoat Ethylacetoacetat Butan--onsäureethylester Ethyl--oxobutanoat itrile R : Alkannitrile, die Gruppe wird auch cyano genannt Acetonitril Ethannitril yanocylohexan yclohexancarbonitril Universität Wien, Fakultät f. hemie, Ass.Prof. Dr. Daniel Krois
4 .0. Amine rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG Amine werden als Alkanamine oder Aminoalkane bezeichnet. Methylamin Aminomethan Methanamin Diethylamin -Ethylethanamin,-Dimethyl--propanamin,-Dimethylaminopropan Anilin Aminobenzol Benzolamin.. Benzolderivate Benzolderivate werden als substituiertes Benzol (engl: benzene) bezeichnet. (ach einer älteren omenklatur werden disubstitierte Benzole als ortho, meta und para substituierte Benzolderivate bezeichnet.) Einige Beispiele: l l Toluol Methylbenzol o-xylol,-dimethylbenzol m-dichlorbenzol,-dichlorbenzol p-omnitrobenzol -om--nitrobenzol S p-toluolsulfonsäure -Methylbenzolsulfonsäure Phenol ydroxybenzol Styrol Phenylethen Ethenylbenzol Biphenyl.. Polycyclische Verbindungen (nicht Stoff der Prüfung) ier bestimmt man zunächst die Zahl der vorhandenen Ringe (daran ekennbar, wie oft man mindestens die Kette durchschneiden muss bis eine offenkettige Verbindung erhalten wird) Vorsilbe: bicyclo, tricyclo-, tetracyclo-... Dann bestimmt man ückenkopfatome, die über ücken miteinander verbunden sind, sodass die längsmöglichen ücken erhalten werden. Dann beginnt man die ummerierung vom. ückenkopfatom über die längste ücke zum. ückenkopfatom und zurück über die zweitlängste ücke, dann die ummerierung der verbleibenden Atome der. ücke. Die Lage weiterer ücken wird dann über die entsprechenden (schon nummerierten) ückenkopfatome festgelegt ochzahlen. Die Zahl der einzelnen ückenglieder wird in eckige Klammern getrennt durch Punkte geschrieben, dann folgt der Alkanname (aller Gerüstatome). ier Beispiele: 6 5 Bicyclo[..]heptan 6 5 Bicyclo[..0]heptan Adamantan Tricyclo[..., ]decan Universität Wien, Fakultät f. hemie, Ass.Prof. Dr. Daniel Krois
5 rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG.. Bezeichnung chiraler Verbindungen nach der R,S-omenklatur Verbindungen sind chiral, wenn Bild und Spiegelbild nicht miteinander zur Deckung gebracht werden können. Dies ist dann der Fall wenn eine -dimensionale Struktur keine Spiegelebene und kein Inversionszentrum aufweist. Meist liegt der Grund für hiralität bei organischen Verbindungen an der Anwesenheit von asymmetrischen -Atomen (Zentrochiralität) (Es gibt aber auch Axialchiralität und Planarchiralität... hier nicht behandelt) Die Konfiguration asymmetrischer -Atome ( verschiedene Reste) erfolgt nach der sog. R,S- omenklatur. Dazu werden die Reste nach einer Prioritätsregel der Größe nach bezeichnet: a,b,c,d. Blickt man dann so auf das -Atom, dass der kleinste Rest (d) vom Betrachter wegweist (hinter der Papierebene liegt) so ist die Konfiguration R wenn die Reste a,b,c im Uhrzeigersinn angeordnet sind und S, wenn sie gegen den Uhrzeigersinn angeordnet sind. Für die Prioritätsreihung wird das ahn-ingold-prelog System verwendet: Die Atome werden nach der rdnungszahl (bei Isotopen nach der Massenzahl) gereiht. Bei jeder der Substituenten entfernt man sich immer weiter vom Zentrum bis man zu einem Unterschied in der Priorität kommt. Dabei wird eine Doppelbindung wie Einfachbindungen zu den entsprechenden Atomen aufgefasst. ier einige Beispiele: 5 R (R) 5-ydroxy--methyl--pentanon a b c d.ebene.ebene R S (S,R)--Methylcyclo--hexen--ol a b c d a b c d.ebene.ebene,,, S l R (S,R) -hlor-,-dimethyl--phenylpentanal a b c d a b c d.ebene l.ebene,, l,,,,, Bei der Verbindung links tritt bei ein Problm auf, dem man öfter begegnet. Schaut der kleinste Rest in einer Darstellung zum Betrachter (ist vor der Papierebene), kann man entweder (i) versuchen alles umzuzeichnen, DER (ii) man stellt sich vor man ist hinter der Papierebene, DER (iii) man schaut das entsprechende asymmetrische -Atom eben bewusst von der falschen Seite an und tauscht das scheinbar erhaltene Zeichen am Schluss einfach um. Z.B. bei in dieser Ansicht sind die Reste a (-l-), b (Phenyl) und c (Isopropyl) gegen den Uhrzeigersinn angeordnet,aber da Rest d zum Betrachter weist muss man S R. Universität Wien, Fakultät f. hemie, Ass.Prof. Dr. Daniel Krois
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Alkane und Cycloalkane
 Systematik und Nomenklatur Alkane und ycloalkane einfachstes Alkan: Methan 4 Summenformel Strukturformel schrittweise Verlängerung um eine - 2 - Einheit homologe Reihe rganische hemie I 1 Alkane Gesättigte
Systematik und Nomenklatur Alkane und ycloalkane einfachstes Alkan: Methan 4 Summenformel Strukturformel schrittweise Verlängerung um eine - 2 - Einheit homologe Reihe rganische hemie I 1 Alkane Gesättigte
Zur Benennung organischer Moleküle
 Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Seminar Organische Chemie für Biochemiker BBCM 1.7
 Juni 2017 Organische Chemie SS 2017 Trivialnamen Seite 1 Organische Chemie für Biochemiker BBCM 1.7 Trivialnamen Dr. Jürgen Vitz Institut für Organische Chemie und Makromolekulare Chemie (IOMC) Philosophenweg
Juni 2017 Organische Chemie SS 2017 Trivialnamen Seite 1 Organische Chemie für Biochemiker BBCM 1.7 Trivialnamen Dr. Jürgen Vitz Institut für Organische Chemie und Makromolekulare Chemie (IOMC) Philosophenweg
Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln.
 Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln. Einfache Formeln, Verzweigungen, längste Kette, Nummerierung Nr Formel Name A1 Propan 3 2
Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln. Einfache Formeln, Verzweigungen, längste Kette, Nummerierung Nr Formel Name A1 Propan 3 2
Organische Chemie. 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8. Lehrstuhl für Organische Chemie
 Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Einführung in die Nomenklatur der organischen Chemie. Einteilung der Kohlenwasserstoffe
 organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
Nomenklatur. 2. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen. 3,3,4,4-Tetramethylheptan
 Nomenklatur Alkane. Ermittle die längte Kohlenstoffkette Stammname 8 8 8 -Methyloctan -Ethyloctan -Propyloctan. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen
Nomenklatur Alkane. Ermittle die längte Kohlenstoffkette Stammname 8 8 8 -Methyloctan -Ethyloctan -Propyloctan. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel!
 Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel! Prof. Dr. Ivo C. Ivanov Einführung (interaktive Vorlesung) Die genaue Benennung organischer Verbindungen nach
Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel! Prof. Dr. Ivo C. Ivanov Einführung (interaktive Vorlesung) Die genaue Benennung organischer Verbindungen nach
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Prof. Dr. Urs Séquin: Organische Chemie für Studierende der Medizin 1
 rof. Dr. Urs équin: rganische hemie für tudierende der Medizin 1 Übersicht über die wichtigsten Verbindungsklassen und ihre funktionellen Gruppen Verbindungsklasse allgemeine Form; Beispiel ame ( = Kohlenstoffrest,
rof. Dr. Urs équin: rganische hemie für tudierende der Medizin 1 Übersicht über die wichtigsten Verbindungsklassen und ihre funktionellen Gruppen Verbindungsklasse allgemeine Form; Beispiel ame ( = Kohlenstoffrest,
Kohlenwasserstoffe. sp 3 -Orbitale. Alkane. Alkene. sp 2 - Orbitale p z - Orbital. sp -Orbitale p y, p z - Orbitale. Alkine
 Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Systematische Nomenklatur
 Systematische Nomenklatur Je größer eine chemische Verbindung wird, desto komplizierter wird in der Regel deren Struktur, und desto schwieriger wird es, diese Verbindung eindeutig zu benennen. Dieses Problem
Systematische Nomenklatur Je größer eine chemische Verbindung wird, desto komplizierter wird in der Regel deren Struktur, und desto schwieriger wird es, diese Verbindung eindeutig zu benennen. Dieses Problem
Ein Alkan, dem ein H-Atom fehlt, wird Alkyl-Rest genannt. Der Name ergibt sich aus dem Alkan, jedoch mit der Endung yl:
 Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Chemie für Biologen WS 2005/6. Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen WS 2005/6 Arne Lützen Institut für Organische hemie der Universität Duisburg-Essen (Teil 10: Organische hemie gesättigte Kohlenwasserstoffe) Sonderstellung des Elements Elektronegativität
hemie für Biologen WS 2005/6 Arne Lützen Institut für Organische hemie der Universität Duisburg-Essen (Teil 10: Organische hemie gesättigte Kohlenwasserstoffe) Sonderstellung des Elements Elektronegativität
2. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
 2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen
 2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 11 2.1 Funktionellen Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer Substanzen.
2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 11 2.1 Funktionellen Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer Substanzen.
Kohlenwasserstoffe. Benzol Naphthalin usw. Alkane Alkene Alkine Cycloaliphaten. Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w.
 OI_folie47 Kohlenwasserstoffe Aliphaten Aromaten Benzol Naphthalin usw. Alkane Alkene Alkine ycloaliphaten Methan Ethan u.s.w Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w. ycloalkane ycloalkene
OI_folie47 Kohlenwasserstoffe Aliphaten Aromaten Benzol Naphthalin usw. Alkane Alkene Alkine ycloaliphaten Methan Ethan u.s.w Ethen (Ethylen) Propen u.s.w. Ethin (Acetylen) Propin u.s.w. ycloalkane ycloalkene
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
CH CH 2 H 2 C H 2 C CH 2 CH CH CH 2 CH 2 C H H 2 C CH 2 C 2 CH 2 H CH 2 CH 2
 Eine spezielle Form von Kohlenwasserstoffen, die ebenfalls nur Einfachbindungen besitzt, genügt nicht der allgemeinen Summenformel n n+ sondern besitzt die allgemeine Summenformel n n. Diese Alkane sind
Eine spezielle Form von Kohlenwasserstoffen, die ebenfalls nur Einfachbindungen besitzt, genügt nicht der allgemeinen Summenformel n n+ sondern besitzt die allgemeine Summenformel n n. Diese Alkane sind
Kohlenstoffverbindungen
 Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane: Moleküle ohne funktionelle Gruppen
E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane: Moleküle ohne funktionelle Gruppen
Chemie. für die Berufsmaturität. Günter Baars. Chemie. Baars. Unter Mitarbeit von Franz Heini, Markus Isenschmid und Doris Kohler
 www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
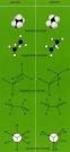 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Benennung (Nomenklatur) von Alkanen. zusammengestellt von W. Habelitz-Tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S.
 Benennung (Nomenklatur) von Alkanen zusammengestellt von W. abelitz-tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S. 34 + 35 istorische Entwicklung ursprünglich: Trivialnamen für viele Stoffe, z.
Benennung (Nomenklatur) von Alkanen zusammengestellt von W. abelitz-tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S. 34 + 35 istorische Entwicklung ursprünglich: Trivialnamen für viele Stoffe, z.
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Grundwissen 10. Klasse NTG 1
 Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Organische Chemie. Maximilian Ernestus
 rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
I. Alkane Homologe Reihe, Nomenklatur
 Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
Homologe Reihe der Alkane. Benennung der Alkane. Konstitutionsisomerie. Isomerie. Was versteht man unter der Homologen Reihe der Alkane?
 Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Aldehyde und Ketone. Aldehyde C 2 H 5 H 3 C. H Propanal Propionaldehyd. H Ethanal Acetaldehyd. H Methanal Formaldehyd. Benzaldehyd.
 Aldehyde und Ketone Aldehyde Methanal Formaldehyd 3 Ethanal Acetaldehyd 2 5 Propanal Propionaldehyd Benzaldehyd Ketone 3 3 2 5 Propanon Aceton 3 2 5 2-Butanon 2 5 3-Pentanon Acetophenon 3 Natürliche Aldehyde
Aldehyde und Ketone Aldehyde Methanal Formaldehyd 3 Ethanal Acetaldehyd 2 5 Propanal Propionaldehyd Benzaldehyd Ketone 3 3 2 5 Propanon Aceton 3 2 5 2-Butanon 2 5 3-Pentanon Acetophenon 3 Natürliche Aldehyde
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Systematische Nomenklatur
 Systematische Nomenklatur IUPAC-Nomenklatur Alle Verbindungen sind Derivate der längsten im Molekül vorkommenden Kohlenstoff-Kette. Von der Kette abzweigende Gruppen werden als Vorsilben angefügt. Die
Systematische Nomenklatur IUPAC-Nomenklatur Alle Verbindungen sind Derivate der längsten im Molekül vorkommenden Kohlenstoff-Kette. Von der Kette abzweigende Gruppen werden als Vorsilben angefügt. Die
1. Aspekte der Energie- und Rohstoffversorgung Gegenwärtiger und absehbarer Energiebedarf 2
 Inhalt 1. Aspekte der Energie- und Rohstoffversorgung 1 1.1. Gegenwärtiger und absehbarer Energiebedarf 2 1.2. Verfügbarkeit einzelner Energieträger 3 1.2.1. Erdöl 3 1.2.2. Erdgas 4 1.2.3. Kohle 4 1.2.4.
Inhalt 1. Aspekte der Energie- und Rohstoffversorgung 1 1.1. Gegenwärtiger und absehbarer Energiebedarf 2 1.2. Verfügbarkeit einzelner Energieträger 3 1.2.1. Erdöl 3 1.2.2. Erdgas 4 1.2.3. Kohle 4 1.2.4.
Vorlesung Chemie für Mediziner: Formeln OC
 Vorlesung hemie für Mediziner: Formeln In diesem Dokument sind die wichtigsten Formeln der Vorlesung zusammengestellt, die man für die Klausur kennen sollte. Die Zusammenstellung erhebt keinen Anspruch
Vorlesung hemie für Mediziner: Formeln In diesem Dokument sind die wichtigsten Formeln der Vorlesung zusammengestellt, die man für die Klausur kennen sollte. Die Zusammenstellung erhebt keinen Anspruch
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
Clara Schumann -Gymnasium Grundlagen der organischen Chemie
 1 lara Schumann -Gymnasium Grundlagen der organischen hemie Ein Leitprogramm für den Grundlagen-hemieunterricht der Sekundarstufe II Dr. Daniel Bürgisser Neue Kantonsschule Aarau Revision 2003 Modifiziert:
1 lara Schumann -Gymnasium Grundlagen der organischen hemie Ein Leitprogramm für den Grundlagen-hemieunterricht der Sekundarstufe II Dr. Daniel Bürgisser Neue Kantonsschule Aarau Revision 2003 Modifiziert:
Prüfungsvorbereitung organische Chemie
 Prüfungsvorbereitung organische hemie 2L Alle diese Aufgaben lehnen sich an Aufgaben zur gestreckten Abschlussprüfung für hemielaboranten Teil 1 an. Sie sind jedoch umformuliert und von den Stoffsystemen/Zahlenwerten
Prüfungsvorbereitung organische hemie 2L Alle diese Aufgaben lehnen sich an Aufgaben zur gestreckten Abschlussprüfung für hemielaboranten Teil 1 an. Sie sind jedoch umformuliert und von den Stoffsystemen/Zahlenwerten
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Grundwissen Chemie Mittelstufe (10 MNG)
 Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
IUPAC Nomenklatur. Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten. Feld 2: Stammname der Verbindung
 Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten Feld 2: Stammname der Verbindung Feld 3: Grad der Ungesättigtheit Feld 4: funktionelle Gruppe mit höchster
Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten Feld 2: Stammname der Verbindung Feld 3: Grad der Ungesättigtheit Feld 4: funktionelle Gruppe mit höchster
Grundwissen Chemie Jahrgangsstufe 10 (NTG)
 Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Grundwissen der 10.Klasse NTG
 Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Die Welt der Gifte. Bearbeitet von Karsten Strey
 Die Welt der Gifte Bearbeitet von Karsten Strey 2., erweiterte und überarbeitete Auflage 2015. Buch. 512 S. Softcover ISBN 978 3 86541 728 2 Format (B x L): 14,9 x 21,1 cm Gewicht: 954 g Weitere Fachgebiete
Die Welt der Gifte Bearbeitet von Karsten Strey 2., erweiterte und überarbeitete Auflage 2015. Buch. 512 S. Softcover ISBN 978 3 86541 728 2 Format (B x L): 14,9 x 21,1 cm Gewicht: 954 g Weitere Fachgebiete
Übungsbeispiele Kapitel Organische Verbindungen
 Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
Kennsilbe. -an. -en -in. -yl. -ol. -al (VI) -on. (VII) -säure (VIII)
 Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Kapitel 9: Kohlenwasserstoffe
 Ursprünglich bezeichnete man die Stoffe, die in Lebewesen (Organismen) gebildet werden, als organische Verbindungen. Organische Stoffe sind z.b. in olz enthalten, im leisch, in lebenden Pflanzen und Bakterien,
Ursprünglich bezeichnete man die Stoffe, die in Lebewesen (Organismen) gebildet werden, als organische Verbindungen. Organische Stoffe sind z.b. in olz enthalten, im leisch, in lebenden Pflanzen und Bakterien,
Alkane. Name: Summenformel: vereinfachte Formel: Zustand: Methan CH 4 CH 4 g (gaseous) Ethan C 2 H 6 CH 3 CH 3 g. Propan C 3 H 8 CH 3 CH 2 CH 3 g
 Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Prüfungsfragen aus dem Bereich organische Chemie für Biologielaboranten
 Prüfungsfragen aus dem Bereich organische hemie für Biologielaboranten Vorbemerkung: Die folgenden Fragen sind von PAL-Prüfungsfragen aus dem Bereich der organischen hemie aus den Abschlussprüfungen (Teil
Prüfungsfragen aus dem Bereich organische hemie für Biologielaboranten Vorbemerkung: Die folgenden Fragen sind von PAL-Prüfungsfragen aus dem Bereich der organischen hemie aus den Abschlussprüfungen (Teil
Zum Schutz vor mechanischen Risiken verwendet SuperDrecksKëscht folgende Schutzhandschuhe:
 Schutzhandschuhe Beim Umgang mit Gefahrstoffen sollen Schutzhandschuhe die Hände vor mechanischen Risiken und vor Chemikalien schützen. Sie müssen den Anforderungen der europäischen Richtlinie 89/686/EWG
Schutzhandschuhe Beim Umgang mit Gefahrstoffen sollen Schutzhandschuhe die Hände vor mechanischen Risiken und vor Chemikalien schützen. Sie müssen den Anforderungen der europäischen Richtlinie 89/686/EWG
Stoffklasse Alkane Alkene/Alkine Aromaten
 Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Stoffklassen und Stammsysteme organischer Verbindungen
 rganische und Bioorganische hemie A-8010 Graz, einrichstr. 28 eminar zu den Laborübungen aus rganischer hemie (Bakk.) Institut für hemie, toffklassen und tammsysteme organischer Verbindungen 20.11.2012
rganische und Bioorganische hemie A-8010 Graz, einrichstr. 28 eminar zu den Laborübungen aus rganischer hemie (Bakk.) Institut für hemie, toffklassen und tammsysteme organischer Verbindungen 20.11.2012
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Konfigurationsisomerie
 Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Organische Experimentalchemie für Mediziner, Zahnmediziner und Naturwissenschaftler
 rganische Experimentalchemie für Mediziner, Zahnmediziner und Naturwissenschaftler Vorlesung: Mo-Fr. 8:00-8:45 Uhr Klausur: Abschlussklausur I Fr. 15.01.2016 18:15 19:45 Abschlussklausur II Fr. 05.02.2016
rganische Experimentalchemie für Mediziner, Zahnmediziner und Naturwissenschaftler Vorlesung: Mo-Fr. 8:00-8:45 Uhr Klausur: Abschlussklausur I Fr. 15.01.2016 18:15 19:45 Abschlussklausur II Fr. 05.02.2016
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Organische Stofflehre
 Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231
 Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
Vom Alkohol zum Oxidationsprodukte der Alkohole
 Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Chemie 2. Klausur. Nachname: Vorname: Matrikelnummer: SoSem 2008 ( ) Bei den Multiple-Choice Fragen ist immer nur eine mögliche Antwort
 Chemie 2 Klausur A SoSem 2008 (16.07.2008) Nachname: Vorname: Matrikelnummer: Welche Jahreszulassung? Erreichte Klausur-Punktzahl: Bei den Multiple-Choice Fragen ist immer nur eine mögliche Antwort - und
Chemie 2 Klausur A SoSem 2008 (16.07.2008) Nachname: Vorname: Matrikelnummer: Welche Jahreszulassung? Erreichte Klausur-Punktzahl: Bei den Multiple-Choice Fragen ist immer nur eine mögliche Antwort - und
s- und p-orbitale MO-Schema des Wasserstoffmoleküls H 2 y z z x p x p y p z antibindendes MO bindendes MO
 s- und p-rbitale y y z z x x s p x p y p z M-Schema des Wasserstoffmoleküls 2 antibindendes M 1s 1s bindendes M Merkmale wichtiger ybridorbitale sp 3 -ybridisierung: Tetraedrische Ausrichtung der ybridorbitale,
s- und p-rbitale y y z z x x s p x p y p z M-Schema des Wasserstoffmoleküls 2 antibindendes M 1s 1s bindendes M Merkmale wichtiger ybridorbitale sp 3 -ybridisierung: Tetraedrische Ausrichtung der ybridorbitale,
O Br. o-xylol Wie könnte man folgende Verbindungen aus mono-substituierten Benzolen herstellen? Br
 Grundlagen der rganischen Chemie, SS 2002, Kroutil Übungszettel 10 10.1. Benennen sie nomenklaturgerecht N 10.2. Zeichnen sie die Struktur von 2-Chlor-6-methyl naphthalin N 2 10.3. Was entsteht bei folgender
Grundlagen der rganischen Chemie, SS 2002, Kroutil Übungszettel 10 10.1. Benennen sie nomenklaturgerecht N 10.2. Zeichnen sie die Struktur von 2-Chlor-6-methyl naphthalin N 2 10.3. Was entsteht bei folgender
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Kapitel 6: Organische Verbindungen mit funktionellen Gruppen
 Kapitel 6: rganische Verbindungen mit funktionellen Gruppen 2 nhalt Kapitel 6: rganische Verbindungen mit funktionellen Gruppen... 1 nhalt... 2 Übersicht über wichtige Stoffklassen der organischen Chemie...
Kapitel 6: rganische Verbindungen mit funktionellen Gruppen 2 nhalt Kapitel 6: rganische Verbindungen mit funktionellen Gruppen... 1 nhalt... 2 Übersicht über wichtige Stoffklassen der organischen Chemie...
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Lösungen zu Übung 22
 rganische hemie I Lösungen zu Übung 22 1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan
rganische hemie I Lösungen zu Übung 22 1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan
Grundwissen Chemie 10. Klasse SG
 Grundwissen hemie 10. Klasse SG Molekülstruktur und Stoffeigenschaften Elektronegativität - Abkürzung: EN - relatives Maß für die Fähigkeit eines Atoms, in einer chemischen Bindung das Bindungselektronenpaar
Grundwissen hemie 10. Klasse SG Molekülstruktur und Stoffeigenschaften Elektronegativität - Abkürzung: EN - relatives Maß für die Fähigkeit eines Atoms, in einer chemischen Bindung das Bindungselektronenpaar
Charakterisierung Anthropogener Emissionen durch Immissions- und Emissionsuntersuchungen
 Charakterisierung Anthropogener Emissionen durch Immissions- und Emissionsuntersuchungen 29.5.22 Bedeutung von Emissions- und Immissionsmessungen Emissionsdaten stellen Hauptunsicherheit in luftchemischen
Charakterisierung Anthropogener Emissionen durch Immissions- und Emissionsuntersuchungen 29.5.22 Bedeutung von Emissions- und Immissionsmessungen Emissionsdaten stellen Hauptunsicherheit in luftchemischen
Aufgabe S. 2/a (2 Punkte) Wodurch können Sie Cyclohexan von Cyclohexen unterscheiden?
 16-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
16-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
Carbonylgruppe Aldehyd Keton. Nomenklatur (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart S ; Buddrus, S.
 Vorlesung 35 Aldehyde und Ketone Beiden Substanzklassen gemeinsam ist die arbonylgruppe.. arbonylgruppe Aldehyd Keton Nomenklatur (Vollhardt, 3. Aufl., S. 782783, 4. Aufl., S. 857859; art S. 304305; Buddrus,
Vorlesung 35 Aldehyde und Ketone Beiden Substanzklassen gemeinsam ist die arbonylgruppe.. arbonylgruppe Aldehyd Keton Nomenklatur (Vollhardt, 3. Aufl., S. 782783, 4. Aufl., S. 857859; art S. 304305; Buddrus,
Beuth Hochschule für Technik Berlin, Studiengang Pharma- und Chemietechnik Tutorium Organische Chemie 1 (SS 2011), Tutor: Sascha Behne
 IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
Das Elektronenpaar- Abstoßungs-Modell (EPA) unpolare / polare Atombindung. Dipol-Molekül. Beispiele für. zwischenmolekulare Wechselwirkungen
 Das Elektronenpaar- Abstoßungs-Modell (EPA) SG 10.1 Elektronenpaare stoßen einander ab, und nehmen daher möglichst großen Abstand zueinander ein. Orbitale nicht bindender Elektronenpaare (EP) nehmen mehr
Das Elektronenpaar- Abstoßungs-Modell (EPA) SG 10.1 Elektronenpaare stoßen einander ab, und nehmen daher möglichst großen Abstand zueinander ein. Orbitale nicht bindender Elektronenpaare (EP) nehmen mehr
Inhaltsverzeichnis VII. Vorwort... V
 VII Vorwort... V 1 Einleitung... 1 1.1 Der Begriff der Organischen Chemie... 1 1.2 Vielfalt organischer Verbindungen... 1 1.3 Ordnung in der Vielfalt... 2 2 Grundlegendes... 3 2.1 Kohlenstoff hat vier
VII Vorwort... V 1 Einleitung... 1 1.1 Der Begriff der Organischen Chemie... 1 1.2 Vielfalt organischer Verbindungen... 1 1.3 Ordnung in der Vielfalt... 2 2 Grundlegendes... 3 2.1 Kohlenstoff hat vier
Übungsaufgaben: Alkohole und Aldehyde/Ketone
 Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
4. Stereochemie. Das wichtigste Kriterium für Chiralität ist, dass sich Objekt und Spiegelbild nicht zur Deckung bringen lassen.
 4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
Die Herstellung von Alkenen aus Chloralkanen bzw. aus anderen Estern oder Alkoholen durch E2- oder E1-Eliminierungen wurde bereits besprochen.
 Vorlesung 18. Alkene ie erstellung von Alkenen aus hloralkanen bzw. aus anderen Estern oder Alkoholen durch E2- oder E1-Eliminierungen wurde bereits besprochen. Technische erstellung von Ethylen (= Ethen)
Vorlesung 18. Alkene ie erstellung von Alkenen aus hloralkanen bzw. aus anderen Estern oder Alkoholen durch E2- oder E1-Eliminierungen wurde bereits besprochen. Technische erstellung von Ethylen (= Ethen)
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
NMR Spektroskopie. Aufgaben
 hemische Verschiebung 1. Zeichnen Sie zu den nachfolgend aufgeführten Stoffen die Strukturformeln! Unterscheiden Sie dann zwischen chemisch äquvalenten und nichtäquivalenten Kernen. Bezeichnen Sie die
hemische Verschiebung 1. Zeichnen Sie zu den nachfolgend aufgeführten Stoffen die Strukturformeln! Unterscheiden Sie dann zwischen chemisch äquvalenten und nichtäquivalenten Kernen. Bezeichnen Sie die
Übungen Kapitel 1 Alkane- Radikalische Substitution
 Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
Die Verwendung von Rot- und Bleistift sowie Tipp-Ex ist untersagt!!!
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Hydroxylderivate. Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit. Bruch der C-H- und der C-OBindungen. Prof. Dr. Ivo C.
 Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
Organische Chemie. David Vajda
 rganische hemie David Vajda 27. August 2016 2 Kapitel 1 Teil 1, rganische hemie 1.1 Allgemeines 1.1.1 Das Schalenmodell Schale. maximal 8 verschiedene Schalen. Valenzelektronen, Aussenelektronen, auptgruppe
rganische hemie David Vajda 27. August 2016 2 Kapitel 1 Teil 1, rganische hemie 1.1 Allgemeines 1.1.1 Das Schalenmodell Schale. maximal 8 verschiedene Schalen. Valenzelektronen, Aussenelektronen, auptgruppe
Selbsteinschätzungstest zum Vorkurs Organische Chemie
 WS 15/16 1/16 Selbsteinschätzungstest zum Vorkurs rganische hemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NIT die späteren Studieninhalte. Die Inhalte des Vorkurses
WS 15/16 1/16 Selbsteinschätzungstest zum Vorkurs rganische hemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NIT die späteren Studieninhalte. Die Inhalte des Vorkurses
13.1. Struktur der Carbonyl-Gruppe, Prinzipielle Reaktivität
 13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
Claisen-Kondensation (Nucleophile Substitution am Acyl-C-Atom) Mechanismus der Claisen-Kondensation
 2 I_folie321 laisen-kondensation (ucleophile Substitution am Acyl--Atom) 3 2 5 1) a 2 3 2) 2 / γ β α 3 2 2 5 "Acetessigsäureethylester" ein β-ketoester 2 2 3 3 1) a 3 2) 2 / 5 4 3 2 1 3 2 3 3 2-Methyl-3-oxopentansäuremethylester
2 I_folie321 laisen-kondensation (ucleophile Substitution am Acyl--Atom) 3 2 5 1) a 2 3 2) 2 / γ β α 3 2 2 5 "Acetessigsäureethylester" ein β-ketoester 2 2 3 3 1) a 3 2) 2 / 5 4 3 2 1 3 2 3 3 2-Methyl-3-oxopentansäuremethylester
Übungsaufgaben zu Carbonylen, Carbonsäuren und deren Derivate sowie zu Fetten
 Übungsaufgaben zu arbonylen, arbonsäuren und deren Derivate sowie zu Fetten Lernen, ohne zu denken, ist eitel, denken, ohne zu lernen, ist gefährlich. Konfuzius, chin. Philosoph, (551 v. hr. 479 v. hr.)
Übungsaufgaben zu arbonylen, arbonsäuren und deren Derivate sowie zu Fetten Lernen, ohne zu denken, ist eitel, denken, ohne zu lernen, ist gefährlich. Konfuzius, chin. Philosoph, (551 v. hr. 479 v. hr.)
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
