Verfahrenstechnisches Praktikum WS 2016/2017. Versuch D3: Energiebilanz einer Verbrennung
|
|
|
- Heini Baum
- vor 6 Jahren
- Abrufe
Transkript
1 Fakultät für Chemieingenieurwesen und Verfahrenstechnik Verfahrenstechnisches Praktikum WS 201/2017 Versuch D3: Energiebilanz einer Verbrennung Betreuer: Matthias Sentko Geb.: Engler-Bunte-Institut Bereich Verbrennungstechnik
2 1. Einführung und Grundlagen 1.1 Energiebilanz einer Verbrennung Die Energiebilanz einer Verbrennung wird am Beispiel einer kleinen Brennkammer untersucht, in welcher die bei der Verbrennung von Erdgas freiwerdende Energie zur Erwärmung des Wassers benutzt wird. Der Apparat führt also den gleichen Prozess durch, wie er in einem Heizungskessel abläuft. Aus versuchstechnischen Gründen wurde eine andere geometrische Anordnung gewählt als bei Heizkesseln üblich. Der Grad der Energieausnutzung in feuerungstechnischen Anlagen lässt sich durch eine Bilanz aller die Grenzen des Apparates überschreitenden Wärmeströme bestimmen. Folgende Ströme überschreiten die Kontrollraumgrenze, die mit der äußeren Wand der Versuchsanlage zusammenfällt. Bild 1: Zur Herleitung der Energiebilanz In das System hinein gehen die folgenden Massenströme: 1. M B = Massenstrom des Brennstoffes in kg s 2. M L = Massenstrom der Verbrennungsluft in kg s 3. M w,i = Gesamtmassenstrom des Kühlwassers in kg s 2
3 Diese Massenströme transportieren die folgenden Energieströme in das System hinein (h i ist die spezifische Enthalpie): 1. B = M B h B = Energiestrom des Brennstoffes in kj/h 2. L = M L h L = Energiestrom der Luft in kj h (fühlbare Wärme der Verbrennungsluft) 3. w,i,ein = M w,i h w,i,ein = Energiestrom von Wasser in kj 4. R = Δ R h M B = Die bei der Verbrennung freigesetzte Wärmeleistung (λ 1) Δ R h bezeichnet dabei die pro kg Brennstoff freigesetzte Reaktionsenergie. Aus dem System heraus gehen die Massenströme: h 1. M A = Massenstrom des Abgases in kg/s 2. M w,i = Gesamtmassenstrom des Kühlwassers in kg/s Die Massenströme transportieren die folgenden Energieströme aus dem System heraus: 1. A = M A h A = Energiestrom des Abgases in J/s (fühlbare Wärme des Abgases) 2. w,i,aus = M w,i h w,i,aus = Energiestrom des Kühlwassers in J/s am Austritt Zudem gibt die Brennkammer über ihre warmen Wände Energie in Form eines Verlustwärmestroms ab: V = Verlustwärmestrom Der Satz von der Energieerhaltung sagt aus, dass die zugeführten und die abgeführten Energieströme gleich sind: E zu = E ab L + w,i,ein + R = A + w,i,aus+ V Die Energieströme ergeben sich aus den Massenströmen und den Stoffeigenschaften (spezifische Wärmekapazitäten c p sowie den Temperaturen (in K)) zu: B = M B h B = M B c pb Δθ B = M B c pb (ϑ B ϑ 0 ) 3
4 L = M L h L = M L c pl Δϑ L = M L c pl (ϑ L ϑ 0 ) w,ein = M w h w,ein = M w,i c pw Δϑ w,ein = c pw Δϑ w,ein M w,i = c pw (ϑ w,ein ϑ 0 ) M w,i w,aus = M w h w,aus = M w,i c pw Δϑ w,i,aus = M w,i c pw (ϑ w,i,aus ϑ 0 ) mit der Bezugstemperatur ϑ 0 = 273,15 K. Da der Brennstoff- und Luftstrom in Volumenströmen gemessen werden und die spezifischen Wärmen in kj m3 gegeben sind, ist es zweckmäßig, die Massenströme für Brennstoff, Luft und n Abgas in Volumenströme bzw. in Normvolumenströme umzurechnen. L = V L ρ L h L = V L c pl ϑ L = V n,l c pn L Δϑ L = V n,l c pn L (ϑ L ϑ 0 ) B = V B ρ B h B = V L c pb ϑ B = V n,b c pn B Δϑ B = V n,b c pn B (ϑ B ϑ 0 ) A = V A ρ A h A = V A c pa ϑ A = V n,a c pn A Δϑ A = V n,a c pn A (ϑ A ϑ 0 ) Wobei c p = c p ρ bzw. c pn = c p ρ n die volumenspezifische Wärmekapazität ist und die Einheit J m 3 bzw. J K m 3 n K besitzt. Die freigesetzte Reaktionswärme Δ R H wird in der Feuerungstechnik auch als unterer Heizwert Hu bezeichnet. Er ist im Allgemeinen auf den Normvolumenstrom des Brennstoffs bezogen und kj besitzt die Einheit 3. Für die freigesetzte Reaktionswärme gilt damit: m n, Brenngas R = V n,b H u Aus den bekannten bzw. messbaren Größen: V B V L V A H u m3 h m3 h m3 h kj m n 3 Brennstoffvolumenstrom Verbrennungsluftstrom Abgasvolumenstrom Heizwert des Brennstoffs M w,i kg Kühlwasserströme (1-) h c pn kj m n 3 K mittlere (volumenbezogene) spezifische Wärmekapazität (Gase) 4
5 c pw kj kg K mittlere spezifische Wärmekapazität (Wasser) ϑ [K] Temperaturen lässt sich nun aus der Wärmebilanz der schwer messbare Wärmeverlust V berechnen. V = L + R + w,i,ein w,i,aus A Die Energieausnutzung einer feuerungstechnischen Anlage wird durch den Wirkungsgrad ausgedrückt. Dafür gibt es zwei Definitionen: 1. Der feuerungstechnische Wirkungsgrad η f ist Maß für die Qualität des Wärmeaustausches innerhalb der Feuerungsanlage. Dabei werden alle von den Flammengasen abgegebenen Wärmeströme ( nutz und V) gleichartig behandelt, da ein Wärmeaustausch nötig ist, um diese Ströme zum Fließen zu bringen. Die Abgasenergie wird hingegen davon unterschieden, da sie ohne Wärmeaustausch zustande kommt. η f = nutz + V zu bzw. η f = nutz + V R + L A = 1 R + L Der dem Prozess entzogene Nutzwärmestrom Q Nutz ist dabei die an das Kühlwasser abgegebene Leistung: nutz = w,aus w,ein = M w,i c pw c (ϑ w,i,aus ϑ w,ein ) 2. Der Gesamtwirkungsgrad gibt den Anteil der für den jeweiligen Prozess genutzten Wärme an. Als Verluste werden hierbei außer der Abgasenergie auch die Wandverluste angesehen: nutz η ges = R + L = 1 A + V R + L 5
6 1.2 Rauchgaszusammensetzung Für die Auslegung von technischen Verbrennungseinrichtungen spielt der spezifische Luftbedarf eine wichtige Rolle (Dimensionierung der Leitungen, Pumpen, Verdichter etc.). Ebenso sind die Volumenströme der Verbrennungsgase (Rauchgase) zur Auslegung von Verbrennungseinrichtungen wichtige Größen. Die spezifische Mindestrauchgasmenge ist die Menge der Verbrennungsprodukte (Stoffmenge der Rauchgase), die bei stöchiometrischer Verbrennung eines Mols des Brennstoffes für eine vorgegebene Reaktionsgleichung entstehen. Für die Verbrennung von Methan ergibt sich: oder CH 4 + 2O 2 CO H 2 O CH 4 + 2O ,79 0,21 N 2 CO H 2 O + 2 0,79 0,21 N 2 Der Sauerstoffbedarf der Reaktion mit reinem Sauerstoff ist wie folgt definiert: O 2min = 2 mmm O 2 mmm CH 4 Für die Rauchgasmenge, die bei stöchiometrischer Verbrennung von Methan mit Luft entsteht, gilt: R min Luft = n CO2 + n H 2 O + n N 2 = 10,524 mol Rauchgas n CH mol 4 min Brenngas Für andere Brennstoffe oder Gemische aus Brennstoffen sind die entsprechenden Beziehungen leicht aus den entsprechenden Umsatzgleichungen abzuleiten. Für die Auslegung von technischen Verbrennungseinrichtungen ist schließlich noch die Zusammensetzung der Rauchgase eine wichtige Information. Die Zusammensetzung der Rauchgase in Volumenanteilen oder Molanteilen kann leicht mit Hilfe der Reaktionsgleichungen für die betrachteten Verbrennungsreaktionen, die als Volumengleichungen zu lesen sind, angegeben werden. Wird der Volumenanteil bzw. Molanteil des Verbrennungsprodukts j im Rauchgas mit X j bezeichnet, ist X j = Für die Verbrennung von Methan mit Luft bei einer Luftzahl von λ 1 ergibt sich damit n j j n j = n j R CH 4 + 2λO ,79 0,21 λn 2 CO H 2 O + 2(λ 1)O ,79 0,21 λn 2 n j = R = 1 + 9,524 λ j Damit berechnen sich die Anteile der einzelnen Rauchgaskomponenten gemäß X CO 2 = n CO2 = n CO2 j n j R = 1 R = ,524 λ mmm CO2 mmm RRRRhggg
7 X H2 O = n H2O j n j = n H2O R = 2 R = 2 mmm H 2O 1+9,524 λ mmm RRRRhggg X O 2 = n O2 = n O2 2( λ 1) = = j n j R R 2(λ 1) 1 + 9,524 λ mmm O2 mmm RRRRhggg X N 2 = n N2 = n N2 j n j R = 7,524 λ = 7,524 λ R 1 + 9,524 λ mmm N2 mmm RRRchggg Die Zusammensetzung des Rauchgases bei der Verbrennung von Methan mit Luft ist in der nebenstehenden Abbildung in Abhängigkeit der Luftzahl angegeben. Methan ist der wasserstoffreichste Kohlenwasserstoff. Das Rauchgas bei der Verbrennung von Methan (oder Erdgas) enthält daher den niedrigsten Anteil an Kohlendioxid. Bei anderen Brennstoffen ergeben sich andere Verhältnisse. Beispiel: Verbrennung von Kohlenwasserstoffen (Heizöl) mit Luft: Dann ist C m H n + m + n 4 λo 2 + m + n 0,79 4 0,21 λn 2 m CO 2 + n 2 H 2O + m + n 4 (λ 1)O 2 + m + n 0,79 4 0,21 λn 2 n j = R = n 4 j + 4,72 λ(m + n 4 ) Damit wird der Anteil von Kohlendioxid im Rauchgas mit nachfolgender Gleichung ermittelt: X CO2 = n CO 2 = n CO2 j n j R = m R = 4m n + 4,72λ(4m + n) Die Volumenanteile der anderen Rauchgaskomponenten ergeben sich entsprechend. Die untere Abbildung gibt einen Vergleich des Kohlendioxidanteils im Rauchgas bei der Verbrennung von Methan bzw. Heizöl mit Luft in Abhängigkeit der Luftzahl wieder. Die Zusammensetzung von Heizöl ist dabei mit m = 12 angenommen. Für andere Brennstoffe ergeben sich durch die entsprechenden Definitionen der Reaktionsgleichungen für die Verbrennung analoge Beziehungen für Luftbedarf, Rauchgasmenge, Rauchgaszusammensetzung. Diese Größen beziehen sich jeweils auf eine vorgegebene Reaktionsgleichung, für die vollständiger Umsatz vorausgesetzt wird. Tatsächlich liegt aber für jede chemische Reaktion ein Gleichgewicht vor. Für Verbrennungsreaktionen liegen die Gleichgewichte weit auf der Seite der Produkte, so dass die bisherige Schreibweise eine gute Annäherung an den tatsächlichen Zustand ist. Zu beachten ist jedoch, dass in den Verbrennungsreaktionen auch Komponenten auftreten, die bisher noch vernachlässigt wurden. 7
8 2. Aufgabenstellung An einer wassergekühlten Brennstrecke sind für drei verschiedene Einstellungen die Wärmebilanzen aufzustellen und die Wärmeverluste zu bestimmen. Es werden drei verschiedene Luftzahlen (Verhältnis von tatsächlichem zu stöchiometrischem Luftstrom, vgl. Grundlagen) eingestellt (λ = 1; λ = 1,1; λ = 1,2), der Brennstoffdurchsatz beträgt dabei 4 m 3 n /h. Die Kühlwasser-volumenströme sind für jede Luftzahlvariation so einzustellen, dass die Kühlwassertemperatur in jeder der fünf Segmente der Brennkammer (s. Bild 2) 70 C beträgt. Zusätzlich muss für jede Luftzahlvariation die CO 2 Konzentration mittels eines Messgeräts, wie es auch Schornsteinfeger benutzen, gemessen werden. 3. Versuchsaufbau und Durchführung Die Brennstrecke besteht aus einem zylindrischen, in fünf Abschnitte gegliederten Brennraum, dessen Wände durch Wasser gekühlt werden (Bild 2). Zusätzlich ist am Ende der Brennkammer eine spiralförmige Kühlschlange eingebaut. Als Brennstoff wird Erdgas verwendet. Die Ströme von Erdgas und Verbrennungsluft werden mit Rotametern (od. Schwebekörperdurchflußmessgeräten) bestimmt und dann dem Brenner zugeführt. Als Temperatur der beiden Ströme kann Raumtemperatur (20 C) angenommen werden. Die bei den einzelnen Einstellungen entstehenden Abgasmengen werden angegeben, die Art der Bestimmung zeigt das Kapitel "Grundlagen". Die Abgastemperatur wird mit Hilfe eines Platin-Rhodium/Platin-Thermoelements gemessen. Die Kühlwasserdurchsätze durch die fünf Abschnitte und die Spirale werden mit Rotametern gemessen. Die Kühlwassereintrittstemperaturen sind gleich und werden von einem gemeinsamen Thermometer angezeigt. 8
9 Bild 2: Versuchsaufbau 4. Auswertung und Darstellung der Ergebnisse Die Energiebilanzen sind in übersichtlicher Form darzustellen. Der feuerungstechnische Wirkungsgrad und der Gesamtwirkungsgrad sind als Funktion der Luftzahl in jeweils einem Diagramm darzustellen. Dabei muss c pn, Abgas mit den Werten aus der untenstehenden Tabelle linear extrapoliert werden. Die Molenbrüche von CO 2, H 2 O, O 2, N 2 im Abgas sind zu berechnen und in Abhängigkeit von der Luftzahl in einem Diagramm darzustellen. Für diese Berechnung soll vereinfacht angenommen werden, dass das Erdgas zu 100% aus Methan besteht. Zusätzlich sind die gemessene und die berechnete CO 2 Konzentration für alle drei Luftzahlen zu vergleichen. Außerdem sollen die an der Anlage und mit dem Messgerät gemessene Abgastemperatur bei allen drei Luftzahlen verglichen werden. 9
10 5. Anhang Stoffeigenschaften Erdgaszusammensetzung: CH 4 95%; C 2 H 2,5%; N 2 2%; CO 2 0,5% Unterer Heizwert: H u = kj m 3 Spezifische Wärmen: Wasser c pn W = 4,18 kj kg K Luft c pn L = 1,007 kj m 3 n K Erdgas c pn B = 2,210 kj m 3 n K Abgas c pn A in kj m 3 (siehe Tabelle) n K ϑ \ λ 1,00 1,05 1,10 1,15 1,20 1,25 1,30 1,40 1, K 1,381 1,377 1,373 1,373 1,39 1,35 1,35 1,33 1, K 1,398 1,394 1,390 1,38 1,38 1,381 1,381 1,377 1, K 1,411 1,40 1,402 1,402 1,398 1,394 1,390 1,390 1,38 Temperatur Brennstoff und Luft bei Zufuhr: 20 C Abgasmenge: -spezifische (für Methan): R = 1 + 9,524 λ m n,abgas -gesamte: V n,a = R V n,b [m n 3 /h] 3 m3 n,brenngas Hinweise zur Auswertung: Die Umrechnung von Normvolumenströmen V n in Volumenströme V bzw. umgekehrt erfolgt unter der Annahme idealen Gasverhaltens mit Hilfe der folgenden Gleichung: V = V n p n p T = V n ρ n T n ρ mit p n = 1,013 bar T n = 273,15 K p = Druck des Gases in bar T = Temperatur des Gases in K ρ = Dichte des Gases beim Druck p und der Temperatur T ρ n = Dichte des Gases beim Druck p n und der Temperatur T n 10
Versuch D3: Energiebilanz einer Verbrennung
 Versuch D: Eergiebilaz eier Verbreug 1. Eiführug ud Grudlage 1.1 Eergiebilaz eier Verbreug Die Eergiebilaz eier Verbreug wird am eispiel eier kleie rekammer utersucht, i welcher die bei der Verbreug vo
Versuch D: Eergiebilaz eier Verbreug 1. Eiführug ud Grudlage 1.1 Eergiebilaz eier Verbreug Die Eergiebilaz eier Verbreug wird am eispiel eier kleie rekammer utersucht, i welcher die bei der Verbreug vo
Betriebsfeld und Energiebilanz eines Ottomotors
 Fachbereich Maschinenbau Fachgebiet Kraft- u. Arbeitsmaschinen Fachgebietsleiter Prof. Dr.-Ing. B. Spessert März 2013 Praktikum Kraft- und Arbeitsmaschinen Versuch 1 Betriebsfeld und Energiebilanz eines
Fachbereich Maschinenbau Fachgebiet Kraft- u. Arbeitsmaschinen Fachgebietsleiter Prof. Dr.-Ing. B. Spessert März 2013 Praktikum Kraft- und Arbeitsmaschinen Versuch 1 Betriebsfeld und Energiebilanz eines
Bruttoreaktionen sagen nichts darüber aus, wie der Umsatz tatsächlich abläuft.
 7. Chemische Stoffumwandlungen 7.1 Massenbilanz bei chemischen Stoffumwandlungen Bruttoreaktionen, z. B. die Knallgasreaktion H 2 + ½ O 2 = H 2 O, beschreiben die Mengenverhätnisse beim Umsatz H 2 zu O
7. Chemische Stoffumwandlungen 7.1 Massenbilanz bei chemischen Stoffumwandlungen Bruttoreaktionen, z. B. die Knallgasreaktion H 2 + ½ O 2 = H 2 O, beschreiben die Mengenverhätnisse beim Umsatz H 2 zu O
Übungssunterlagen. Energiesysteme I. Prof. Dr.-Ing. Bernd Epple
 Übungssunterlagen Energiesysteme I Prof. Dr.-Ing. Bernd Epple 1 1. Allgemeine Informationen Zum Bearbeiten der Übungen können die Formelsammlungen aus den Fächern Technische Thermodynamik 1, Technische
Übungssunterlagen Energiesysteme I Prof. Dr.-Ing. Bernd Epple 1 1. Allgemeine Informationen Zum Bearbeiten der Übungen können die Formelsammlungen aus den Fächern Technische Thermodynamik 1, Technische
Übungen zur Vorlesung. Energiesysteme
 Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
Brennstoffverbrennung
 Brennstoffverbrennung Typologisierung der Verbrennungen Verbrennungsreaktionen Globalreaktionen Elementarschritte Reaktion und Dissoziation, Reaktionsrichtung Einführung in die Brennerkonstruktion Flammentemperatur,
Brennstoffverbrennung Typologisierung der Verbrennungen Verbrennungsreaktionen Globalreaktionen Elementarschritte Reaktion und Dissoziation, Reaktionsrichtung Einführung in die Brennerkonstruktion Flammentemperatur,
Thermodynamik 2 Klausur 17. Februar 2015
 Thermodynamik 2 Klausur 17. Februar 2015 Bearbeitungszeit: Umfang der Aufgabenstellung: 120 Minuten 5 nummerierte Seiten 2 Diagramme Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner
Thermodynamik 2 Klausur 17. Februar 2015 Bearbeitungszeit: Umfang der Aufgabenstellung: 120 Minuten 5 nummerierte Seiten 2 Diagramme Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner
Gasbeschaffenheit. Siegfried Bajohr. Engler-Bunte-Institut Bereich Gas, Erdöl, Kohle
 Gasbeschaffenheit Siegfried Bajohr 1 Inhalt Brenntechnische Kenndaten Brennwert H S und Heizwert H i Wobbe-Index W Anwendungsdaten Abgasvolumen Sicherheitskennwerte Zündgrenze Z 2 Brenntechnische Kenndaten
Gasbeschaffenheit Siegfried Bajohr 1 Inhalt Brenntechnische Kenndaten Brennwert H S und Heizwert H i Wobbe-Index W Anwendungsdaten Abgasvolumen Sicherheitskennwerte Zündgrenze Z 2 Brenntechnische Kenndaten
Übungen zur Thermodynamik (PBT) WS 2004/05
 1. Übungsblatt 1. Berechnen Sie ausgehend von der allgemeinen Gasgleichung pv = nrt das totale Differential dv. Welche Änderung ergibt sich hieraus in erster Näherung für das Volumen von einem Mol eines
1. Übungsblatt 1. Berechnen Sie ausgehend von der allgemeinen Gasgleichung pv = nrt das totale Differential dv. Welche Änderung ergibt sich hieraus in erster Näherung für das Volumen von einem Mol eines
kg K dp p = R LuftT 1 ln p 2a =T 2a Q 12a = ṁq 12a = 45, 68 kw = 288, 15 K 12 0,4 Q 12b =0. Technische Arbeit nach dem Ersten Hauptsatz:
 Übung 9 Aufgabe 5.12: Kompression von Luft Durch einen Kolbenkompressor sollen ṁ = 800 kg Druckluft von p h 2 =12bar zur Verfügung gestellt werden. Der Zustand der angesaugten Außenluft beträgt p 1 =1,
Übung 9 Aufgabe 5.12: Kompression von Luft Durch einen Kolbenkompressor sollen ṁ = 800 kg Druckluft von p h 2 =12bar zur Verfügung gestellt werden. Der Zustand der angesaugten Außenluft beträgt p 1 =1,
Klausur Thermische Kraftwerke (Energieanlagentechnik I)
 Klausur Thermische Kraftwerke (Energieanlagentechnik I) Datum: 09.03.2009 Dauer: 1,5 Std. Der Gebrauch von nicht-programmierbaren Taschenrechnern und schriftlichen Unterlagen ist erlaubt. Aufgabe 1 2 3
Klausur Thermische Kraftwerke (Energieanlagentechnik I) Datum: 09.03.2009 Dauer: 1,5 Std. Der Gebrauch von nicht-programmierbaren Taschenrechnern und schriftlichen Unterlagen ist erlaubt. Aufgabe 1 2 3
5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme
 5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme Für isotherme reversible Prozesse gilt und daher Dies
5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme Für isotherme reversible Prozesse gilt und daher Dies
2.11 Innere Energie und Enthalpie für Gasgemische
 2.11 Innere Energie und Enthalpie für Gasgemische Komponenten: Partielle spezifische und partielle molare innere Energie der Komponente: u i, u i,m Partielle spezifische und partielle molare innere Enthalpie
2.11 Innere Energie und Enthalpie für Gasgemische Komponenten: Partielle spezifische und partielle molare innere Energie der Komponente: u i, u i,m Partielle spezifische und partielle molare innere Enthalpie
Thermodynamik des Kraftfahrzeugs
 Cornel Stan Thermodynamik des Kraftfahrzeugs Mit 199 Abbildungen Inhaltsverzeichnis Liste der Formelzeichen... XV 1 Grundlagen der Technischen Thermodynamik...1 1.1 Gegenstand und Untersuchungsmethodik...1
Cornel Stan Thermodynamik des Kraftfahrzeugs Mit 199 Abbildungen Inhaltsverzeichnis Liste der Formelzeichen... XV 1 Grundlagen der Technischen Thermodynamik...1 1.1 Gegenstand und Untersuchungsmethodik...1
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer. Brennstoffe. Wir Unterscheiden grundsätzlich Brennstoffe in:
 Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Institut für Energiesysteme und Energietechnik. Vorlesungsübung 1. Musterlösung
 Institut für Energiesysteme und Energietechnik Vorlesungsübung 1 Musterlösung 3.1 Kohlekraftwerk Aufgabe 1 Gesucht: Aufgrund der Vernachlässigung des Temperaturunterschiedes des Luft-, Rauchgas- und Brennstoffstromes
Institut für Energiesysteme und Energietechnik Vorlesungsübung 1 Musterlösung 3.1 Kohlekraftwerk Aufgabe 1 Gesucht: Aufgrund der Vernachlässigung des Temperaturunterschiedes des Luft-, Rauchgas- und Brennstoffstromes
Zur exergetischen Systematik von Brennstoffen
 Dieser Aufsatz ist Basis für den Vortrag Zur exergetischen Systematik von Brennstoffen am 8. 1. 3 in Lahnstein (VDI-Thermodynamikkolloquium Zur exergetischen Systematik von Brennstoffen Prof. Dr.-Ing.
Dieser Aufsatz ist Basis für den Vortrag Zur exergetischen Systematik von Brennstoffen am 8. 1. 3 in Lahnstein (VDI-Thermodynamikkolloquium Zur exergetischen Systematik von Brennstoffen Prof. Dr.-Ing.
Thermodynamik Formelsammlung
 RH-öln Thermoynamik ormelsammlung 2006 Thermoynamik ormelsammlung - I 1 Grunlagen Boltzmannkonstante: 1.3 Größen un Einheitensysteme Umrechnung ahrenheit nach Celsius: Umrechnung Celsius nach elvin: abgeschlossenes
RH-öln Thermoynamik ormelsammlung 2006 Thermoynamik ormelsammlung - I 1 Grunlagen Boltzmannkonstante: 1.3 Größen un Einheitensysteme Umrechnung ahrenheit nach Celsius: Umrechnung Celsius nach elvin: abgeschlossenes
Stand: September 2015. ERDGAS.praxis. Gasbeschaffenheit und Thermoprozessanlagen
 Stand: September 2015 ERDGAS.praxis Gasbeschaffenheit und Thermoprozessanlagen Einführung Bei industriellen und gewerblichen Thermoprozessen weist Erdgas einen hohen Marktanteil in Industrie und Gewerbe
Stand: September 2015 ERDGAS.praxis Gasbeschaffenheit und Thermoprozessanlagen Einführung Bei industriellen und gewerblichen Thermoprozessen weist Erdgas einen hohen Marktanteil in Industrie und Gewerbe
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Abb. 1: Exotherme und endotherme Reaktionen Quelle: http://www.seilnacht.com/lexikon/aktivi.htm#diagramm
 Energie bei chemischen Reaktionen Chemische Reaktionen sind Stoffumwandlungen bei denen Teilchen umgeordnet und chemische Bindungen gespalten und neu geknüpft werden, wodurch neue Stoffe mit neuen Eigenschaften
Energie bei chemischen Reaktionen Chemische Reaktionen sind Stoffumwandlungen bei denen Teilchen umgeordnet und chemische Bindungen gespalten und neu geknüpft werden, wodurch neue Stoffe mit neuen Eigenschaften
Bilanzgleichung der i-ten Komponente eines Systems mit r Reaktionen
 3.5 Die chemische Produktionsdichte Bilanzgleichung der i-ten Komponente eines Systems mit r Reaktionen und mit folgt Die rechte Seite der Gleichung wird als chemische Produktionsdichte bezeichnet: Sie
3.5 Die chemische Produktionsdichte Bilanzgleichung der i-ten Komponente eines Systems mit r Reaktionen und mit folgt Die rechte Seite der Gleichung wird als chemische Produktionsdichte bezeichnet: Sie
Erdgasmotor E 0834 E 312 Technische Daten
 Seite 1 Bauart: Viertakt-Otto-Gasmotor Zylinder: 4 in Reihe Motorkühlung: Ohne Motorwasserpumpe, der Kühlwasserumlauf ist durch externe Wasserpumpe mit Temperaturregelung auszuführen. Schmierung: Druckumlaufschmierung
Seite 1 Bauart: Viertakt-Otto-Gasmotor Zylinder: 4 in Reihe Motorkühlung: Ohne Motorwasserpumpe, der Kühlwasserumlauf ist durch externe Wasserpumpe mit Temperaturregelung auszuführen. Schmierung: Druckumlaufschmierung
13.1 NORMEN, RICHTLINIEN UND MASSEINHEITEN
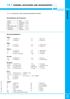 .6 EINHEITEN UND UMRECHNUNGSFAKTOREN Grundeinheiten des SI-Systems Länge Meter m Masse Kilogramm kg Zeit Sekunde s Elektrischer Strom Ampere A Temperatur Kelvin K Lichtstärke Candela cd Umrechnungsfaktoren
.6 EINHEITEN UND UMRECHNUNGSFAKTOREN Grundeinheiten des SI-Systems Länge Meter m Masse Kilogramm kg Zeit Sekunde s Elektrischer Strom Ampere A Temperatur Kelvin K Lichtstärke Candela cd Umrechnungsfaktoren
R. Rauch, H. Hofbauer Technische Universität Wien
 Dezentrale Strom- und Wärmeerzeugung auf Basis Biomasse-Vergasung R. Rauch, H. Hofbauer Technische Universität Wien Gaserzeugung aus Biomasse autotherm allotherm Luft O 2,H 2 O H 2 O CO 2 gering mittel
Dezentrale Strom- und Wärmeerzeugung auf Basis Biomasse-Vergasung R. Rauch, H. Hofbauer Technische Universität Wien Gaserzeugung aus Biomasse autotherm allotherm Luft O 2,H 2 O H 2 O CO 2 gering mittel
Verflüssigung von Gasen / Joule-Thomson-Effekt
 Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Chemische Verbrennung
 Christopher Rank Sommerakademie Salem 2008 Gliederung Die chemische Definition Voraussetzungen sgeschwindigkeit Exotherme Reaktion Reaktionsenthalpie Heizwert Redoxreaktionen Bohrsches Atommodell s Elektrochemie:
Christopher Rank Sommerakademie Salem 2008 Gliederung Die chemische Definition Voraussetzungen sgeschwindigkeit Exotherme Reaktion Reaktionsenthalpie Heizwert Redoxreaktionen Bohrsches Atommodell s Elektrochemie:
Thermodynamik I. Sommersemester 2012 Kapitel 4, Teil 2. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 4, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 4, Teil 2: Übersicht 4 Zweiter Hauptsatz der Thermodynamik 4.5 Entropiebilanz 4.5.1 Allgemeine Entropiebilanz 4.5.2
Thermodynamik I Sommersemester 2012 Kapitel 4, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 4, Teil 2: Übersicht 4 Zweiter Hauptsatz der Thermodynamik 4.5 Entropiebilanz 4.5.1 Allgemeine Entropiebilanz 4.5.2
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Professor Dr. Dr.-Ing. habil. H. Müller-Steinhagen. Praktikum
 UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Professor Dr. Dr.-Ing. habil. H. Müller-Steinhagen Praktikum Gesamtbilanzierung und Wirkungsgradbestimmung eines erdgasbetriebenen Mini-Blockheizkraftwerks
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Professor Dr. Dr.-Ing. habil. H. Müller-Steinhagen Praktikum Gesamtbilanzierung und Wirkungsgradbestimmung eines erdgasbetriebenen Mini-Blockheizkraftwerks
Bild 1: Siedeverhalten im beheizten Rohr (Nach VDI- Wärmeatlas, hier liegend gezeichnet)
 erdampfung Labor für Thermische erfahrenstechnik bearbeitet von Prof. r.-ing. habil. R. Geike. Grundlagen der erdampfung In der chemischen, pharmazeutischen und Lebensmittelindustrie sowie in weiteren
erdampfung Labor für Thermische erfahrenstechnik bearbeitet von Prof. r.-ing. habil. R. Geike. Grundlagen der erdampfung In der chemischen, pharmazeutischen und Lebensmittelindustrie sowie in weiteren
Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K
![Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K](/thumbs/26/9282771.jpg) Fundamentalgleichung für die Entropie Entropie S [S] = J/K spezifische Entropie: s = S/m molare Entropie: s m = S/n Mit dem 1. Hauptsatz für einen reversiblen Prozess und der Definition für die Entropie
Fundamentalgleichung für die Entropie Entropie S [S] = J/K spezifische Entropie: s = S/m molare Entropie: s m = S/n Mit dem 1. Hauptsatz für einen reversiblen Prozess und der Definition für die Entropie
Oxyfuel-Verbrennung Bilanzierung und Schadstoffbildung
 Oxyfuel-Verbrennung Bilanzierung und Schadstoffbildung Dipl.-Ing. R. Wilhelm, TU Dresden, Dresden; Dipl.-Ing. S. Weigl, TU Dresden, Dresden; Prof. Dr.-Ing. M. Beckmann, TU Dresden, Dresden; Kurzfassung
Oxyfuel-Verbrennung Bilanzierung und Schadstoffbildung Dipl.-Ing. R. Wilhelm, TU Dresden, Dresden; Dipl.-Ing. S. Weigl, TU Dresden, Dresden; Prof. Dr.-Ing. M. Beckmann, TU Dresden, Dresden; Kurzfassung
Elektrische Energie, Arbeit und Leistung
 Elektrische Energie, Arbeit und Leistung Wenn in einem Draht ein elektrischer Strom fließt, so erwärmt er sich. Diese Wärme kann so groß sein, dass der Draht sogar schmilzt. Aus der Thermodynamik wissen
Elektrische Energie, Arbeit und Leistung Wenn in einem Draht ein elektrischer Strom fließt, so erwärmt er sich. Diese Wärme kann so groß sein, dass der Draht sogar schmilzt. Aus der Thermodynamik wissen
wegen Massenerhaltung
 3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
Praktikum Kleinventilator
 Gesamtdruckerhöhung in HTW Dresden V-SM 3 Praktikum Kleinventilator Lehrgebiet Strömungsmaschinen 1. Kennlinien von Ventilatoren Ventilatoren haben unabhängig von ihrer Bauart einen bestimmten Volumenstrom
Gesamtdruckerhöhung in HTW Dresden V-SM 3 Praktikum Kleinventilator Lehrgebiet Strömungsmaschinen 1. Kennlinien von Ventilatoren Ventilatoren haben unabhängig von ihrer Bauart einen bestimmten Volumenstrom
Mensch und Technik. Berechnungen und Beispiele
 1 Berechnungen und Beispiele Wärmekapazität Wird einem Stoff durch Erwärmen Energie zugeführt, so steigt deren Temperatur, dies ist stoffabhängig und der Temperaturanstieg ist proportional zur Wärmemenge:
1 Berechnungen und Beispiele Wärmekapazität Wird einem Stoff durch Erwärmen Energie zugeführt, so steigt deren Temperatur, dies ist stoffabhängig und der Temperaturanstieg ist proportional zur Wärmemenge:
Klausur zur Vorlesung. Thermodynamik
 Institut für Thermodynamik 25. August 2010 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Institut für Thermodynamik 25. August 2010 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Inhaltsverzeichnis XVII. Häufig verwendete Formelzeichen. 1 Allgemeine Grundlagen l
 Inhaltsverzeichnis Häufig verwendete Formelzeichen XVII 1 Allgemeine Grundlagen l 1.1 Thermodynamik 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 Was ist Thermodynamik? 9 1.2 System
Inhaltsverzeichnis Häufig verwendete Formelzeichen XVII 1 Allgemeine Grundlagen l 1.1 Thermodynamik 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 Was ist Thermodynamik? 9 1.2 System
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 1. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 1 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 1: Übersicht 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie 3.1.2 Innere Energie U 3.1.3 Energietransfer
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 1 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 1: Übersicht 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie 3.1.2 Innere Energie U 3.1.3 Energietransfer
Allgemeine Information zur Vergasung von Biomasse
 Allgemeine Information zur Vergasung von Biomasse Grundlagen des Vergasungsprozesses Die Vergasung von Biomasse ist ein komplexer Prozess. Feste Brennstoffe werden durch einen thermochemischen Prozess
Allgemeine Information zur Vergasung von Biomasse Grundlagen des Vergasungsprozesses Die Vergasung von Biomasse ist ein komplexer Prozess. Feste Brennstoffe werden durch einen thermochemischen Prozess
Fachbereich Ingenieurwissenschaften und Mathematik. Praktikum Dezentrale Energiesysteme. DEZ 1 Brennstoffzellen
 Fachbereich Ingenieurwissenschaften und Mathematik Praktikum Dezentrale Energiesysteme DEZ 1 Brennstoffzellen Lehrgebiet Regenerative Energiesysteme und Elektrotechnik Prof.-Dr.-Ing. Jens Haubrock Inhalt
Fachbereich Ingenieurwissenschaften und Mathematik Praktikum Dezentrale Energiesysteme DEZ 1 Brennstoffzellen Lehrgebiet Regenerative Energiesysteme und Elektrotechnik Prof.-Dr.-Ing. Jens Haubrock Inhalt
Aufgabe 1 : (10 + 6 + 4 = 20 Punkte)
 Aufgabe 1 : (10 + 6 + 4 = 20 Punkte) Wirtschaftlichkeitsbetrachtung Als Jungingenieur arbeiten Sie in einer mittleren Firma an der Auslegung eines neuen Produktionsprozesses. Bei der Planung haben Sie
Aufgabe 1 : (10 + 6 + 4 = 20 Punkte) Wirtschaftlichkeitsbetrachtung Als Jungingenieur arbeiten Sie in einer mittleren Firma an der Auslegung eines neuen Produktionsprozesses. Bei der Planung haben Sie
Stöchiometrie. (Chemisches Rechnen)
 Ausgabe 2007-10 Stöchiometrie (Chemisches Rechnen) ist die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen sowie der Mengenverhältnisse der beteiligten Stoffe bei chemischen Reaktionen
Ausgabe 2007-10 Stöchiometrie (Chemisches Rechnen) ist die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen sowie der Mengenverhältnisse der beteiligten Stoffe bei chemischen Reaktionen
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6
 Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
VERSUCH 16 CHEMISCHES GLEICHGEWICHT IN DER GASPHASE
 GRUNDPRAKTIKUM PHYSIKALISCHE CHEMIE VERSUCH 16 CHEMISCHES GLEICHGEWICHT IN DER GASPHASE Kurzbeschreibung: Die Temperaturabhängigkeit des chemischen Gasphasen-Gleichgewichts wird unter isobaren Bedingungen
GRUNDPRAKTIKUM PHYSIKALISCHE CHEMIE VERSUCH 16 CHEMISCHES GLEICHGEWICHT IN DER GASPHASE Kurzbeschreibung: Die Temperaturabhängigkeit des chemischen Gasphasen-Gleichgewichts wird unter isobaren Bedingungen
Kleine Formelsammlung Technische Thermodynamik
 Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
Lösungen (ohne Aufgabenstellungen)
 Kapitel 1 Das chemische Gleichgewicht Lösungen (ohne Aufgabenstellungen) Aufgaben A 1 Die Hin- und die Rückreaktion läuft nach der Einstellung des Gleichgewichts mit derselben Geschwindigkeit ab, d. h.
Kapitel 1 Das chemische Gleichgewicht Lösungen (ohne Aufgabenstellungen) Aufgaben A 1 Die Hin- und die Rückreaktion läuft nach der Einstellung des Gleichgewichts mit derselben Geschwindigkeit ab, d. h.
6.4.2 VerdampfenundEindampfen... 427 6.4.3 Destillieren und Rektifizieren... 430 6.4.4 Absorbieren... 436
 Inhaltsverzeichnis 1 Allgemeine Grundlagen... 1 1.1 Thermodynamik... 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 WasistThermodynamik?... 9 1.2 SystemundZustand... 11 1.2.1 SystemundSystemgrenzen...
Inhaltsverzeichnis 1 Allgemeine Grundlagen... 1 1.1 Thermodynamik... 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 WasistThermodynamik?... 9 1.2 SystemundZustand... 11 1.2.1 SystemundSystemgrenzen...
Formel X Leistungskurs Physik 2005/2006
 System: Wir betrachten ein Fluid (Bild, Gas oder Flüssigkeit), das sich in einem Zylinder befindet, der durch einen Kolben verschlossen ist. In der Thermodynamik bezeichnet man den Gegenstand der Betrachtung
System: Wir betrachten ein Fluid (Bild, Gas oder Flüssigkeit), das sich in einem Zylinder befindet, der durch einen Kolben verschlossen ist. In der Thermodynamik bezeichnet man den Gegenstand der Betrachtung
Spezifische Wärmekapazität
 Versuch: KA Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: L. Jahn B. Wehner J. Pöthig J. Stelzer am 01. 06. 1997 Bearbeitet: M. Kreller J. Kelling F. Lemke S. Majewsky i. A. Dr. Escher am
Versuch: KA Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: L. Jahn B. Wehner J. Pöthig J. Stelzer am 01. 06. 1997 Bearbeitet: M. Kreller J. Kelling F. Lemke S. Majewsky i. A. Dr. Escher am
Thermodynamik. Eine Einführung in die Grundlagen. Von. Dr.-Ing. Hans Dieter Baehr. o. Professor an der Technischen Hochschule Braunschweig
 Thermodynamik Eine Einführung in die Grundlagen und ihre technischen Anwendungen Von Dr.-Ing. Hans Dieter Baehr o. Professor an der Technischen Hochschule Braunschweig Mit 325 Abbildungen und zahlreichen
Thermodynamik Eine Einführung in die Grundlagen und ihre technischen Anwendungen Von Dr.-Ing. Hans Dieter Baehr o. Professor an der Technischen Hochschule Braunschweig Mit 325 Abbildungen und zahlreichen
Praktikum Physik. Protokoll zum Versuch 1: Viskosität. Durchgeführt am 26.01.2012. Gruppe X
 Praktikum Physik Protokoll zum Versuch 1: Viskosität Durchgeführt am 26.01.2012 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuerin: Wir bestätigen hiermit, dass wir das Protokoll
Praktikum Physik Protokoll zum Versuch 1: Viskosität Durchgeführt am 26.01.2012 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuerin: Wir bestätigen hiermit, dass wir das Protokoll
Mischungslücke in der flüssigen Phase
 Übungen in physikalischer Chemie für B. Sc.-Studierende Versuch Nr.: S05 Version 2015 Kurzbezeichnung: Mischungslücke Mischungslücke in der flüssigen Phase Aufgabenstellung Die Entmischungskurven von Phenol/Wasser
Übungen in physikalischer Chemie für B. Sc.-Studierende Versuch Nr.: S05 Version 2015 Kurzbezeichnung: Mischungslücke Mischungslücke in der flüssigen Phase Aufgabenstellung Die Entmischungskurven von Phenol/Wasser
6 Energiebilanz am 4-Takt-Dieselmotor
 33 6 Energiebilanz am 4-Takt-Dieselmotor Einem Motor wird Energie in Form von Brennstoff zugeführt. Indem man die Brennstoffmenge misst und den Energiegehalt des Brennstoffs (Heizwert) bestimmt, kann man
33 6 Energiebilanz am 4-Takt-Dieselmotor Einem Motor wird Energie in Form von Brennstoff zugeführt. Indem man die Brennstoffmenge misst und den Energiegehalt des Brennstoffs (Heizwert) bestimmt, kann man
Praktikum Physikalische Chemie I (C-2) Versuch Nr. 1. Bestimmung der Verbrennungsenthalpie
 Praktikum Physikalische Chemie I (C-2) Versuch Nr. 1 Bestimmung der Verbrennungsenthalpie Praktikumsaufgaben 1. Ermittlung der Kalorimeterkonstante durch Verbrennung von Benzoesäure. 2. Bestimmung der
Praktikum Physikalische Chemie I (C-2) Versuch Nr. 1 Bestimmung der Verbrennungsenthalpie Praktikumsaufgaben 1. Ermittlung der Kalorimeterkonstante durch Verbrennung von Benzoesäure. 2. Bestimmung der
Der Normkubikmeter. oder: Warum ist Vakuum so teuer wie Druckluft? Zum besseren Verständnis im Umgang mit den Gasen
 Im alltäglichen Umgang wird die Mengenbestimmung der Gase oftmals kritiklos mit deren Volumen in Verbindung gebracht. Zum Beispiel messen wir den häuslichen Gasverbrauch gemeinhin in m³ ab. Gas besteht
Im alltäglichen Umgang wird die Mengenbestimmung der Gase oftmals kritiklos mit deren Volumen in Verbindung gebracht. Zum Beispiel messen wir den häuslichen Gasverbrauch gemeinhin in m³ ab. Gas besteht
D = 10 mm δ = 5 mm a = 0, 1 m L = 1, 5 m λ i = 0, 4 W/mK ϑ 0 = 130 C ϑ L = 30 C α W = 20 W/m 2 K ɛ 0 = 0, 8 ɛ W = 0, 2
 Seminargruppe WuSt Aufgabe.: Kabelkanal (ehemalige Vordiplom-Aufgabe) In einem horizontalen hohlen Kabelkanal der Länge L mit einem quadratischen Querschnitt der Seitenlänge a verläuft in Längsrichtung
Seminargruppe WuSt Aufgabe.: Kabelkanal (ehemalige Vordiplom-Aufgabe) In einem horizontalen hohlen Kabelkanal der Länge L mit einem quadratischen Querschnitt der Seitenlänge a verläuft in Längsrichtung
Inhaltsverzeichnis. Hans-Joachim Kretzschmar, Ingo Kraft. Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6
 Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
Peltier-Element kurz erklärt
 Peltier-Element kurz erklärt Inhaltsverzeichnis 1 Peltier-Kühltechnk...3 2 Anwendungen...3 3 Was ist ein Peltier-Element...3 4 Peltier-Effekt...3 5 Prinzipieller Aufbau...4 6 Wärmeflüsse...4 6.1 Wärmebilanz...4
Peltier-Element kurz erklärt Inhaltsverzeichnis 1 Peltier-Kühltechnk...3 2 Anwendungen...3 3 Was ist ein Peltier-Element...3 4 Peltier-Effekt...3 5 Prinzipieller Aufbau...4 6 Wärmeflüsse...4 6.1 Wärmebilanz...4
Arbeitsblatt zur Ventilberechnung Berechnungsbeispiele
 Arbeitsblatt zur Ventilberechnung Berechnungsbeisiele Inhalt Seite Ventilberechnung bei Flüssigkeiten Ventilberechnung bei Wasserdamf 5 Ventilberechnung bei Gas und Damf 7 Ventilberechnung bei Luft 9 Durchfluss
Arbeitsblatt zur Ventilberechnung Berechnungsbeisiele Inhalt Seite Ventilberechnung bei Flüssigkeiten Ventilberechnung bei Wasserdamf 5 Ventilberechnung bei Gas und Damf 7 Ventilberechnung bei Luft 9 Durchfluss
Moorburg und Fernwärme Klimaschutz mit Kohle?
 HINTERGRUNDPAPIER Landesverband Hamburg Landesarbeitsgemeinschaft Energie Jörg Behrschmidt (Sprecher) joerg.behrschmidt@hamburg.gruene.de Christoph Schreiber (Sprecher) christoph.schreiber@hamburg.gruene.de
HINTERGRUNDPAPIER Landesverband Hamburg Landesarbeitsgemeinschaft Energie Jörg Behrschmidt (Sprecher) joerg.behrschmidt@hamburg.gruene.de Christoph Schreiber (Sprecher) christoph.schreiber@hamburg.gruene.de
Übung Nummer 1.0. Schätzen Sie den ca. Strom- und Gasverbrauch eines Ein- Zwei-, Dreiund Vierpersonenhaushaltes ab.
 Übung Nummer 1.0 Schätzen Sie den ca. Strom- und Gasverbrauch eines Ein- Zwei-, Dreiund Vierpersonenhaushaltes ab. Übung Nummer 1.0 Haushalt Jahresstrombedarf Jahresgasbedarf Personen kwh/a kwh/a 1 1.500
Übung Nummer 1.0 Schätzen Sie den ca. Strom- und Gasverbrauch eines Ein- Zwei-, Dreiund Vierpersonenhaushaltes ab. Übung Nummer 1.0 Haushalt Jahresstrombedarf Jahresgasbedarf Personen kwh/a kwh/a 1 1.500
2.6 Zweiter Hauptsatz der Thermodynamik
 2.6 Zweiter Hauptsatz der Thermodynamik Der zweite Hauptsatz der Thermodynamik ist ein Satz über die Eigenschaften von Maschinen die Wärmeenergie Q in mechanische Energie E verwandeln. Diese Maschinen
2.6 Zweiter Hauptsatz der Thermodynamik Der zweite Hauptsatz der Thermodynamik ist ein Satz über die Eigenschaften von Maschinen die Wärmeenergie Q in mechanische Energie E verwandeln. Diese Maschinen
Praktische Einführung in die Chemie Integriertes Praktikum:
 Praktische Einführung in die Chemie Integriertes Praktikum: Versuch 1-2 (MWG) Massenwirkungsgesetz Versuchs-Datum: 20. Juni 2012 Gruppenummer: 8 Gruppenmitglieder: Domenico Paone Patrick Küssner Michael
Praktische Einführung in die Chemie Integriertes Praktikum: Versuch 1-2 (MWG) Massenwirkungsgesetz Versuchs-Datum: 20. Juni 2012 Gruppenummer: 8 Gruppenmitglieder: Domenico Paone Patrick Küssner Michael
c C 2 K = c A 2 c B 2mol /l 2 0,5mol /l 2 4 mol /l K =4l /mol
 Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 010 10. 14. Mai 010 Physik für Bauingenieure Übungsblatt 4 1. Wie viele Luftmoleküle befinden sich im Hörsaal Gruppenübungen
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 010 10. 14. Mai 010 Physik für Bauingenieure Übungsblatt 4 1. Wie viele Luftmoleküle befinden sich im Hörsaal Gruppenübungen
Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der Pkw- Klimatisierung
 Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der Pkw- Klimatisierung Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der
Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der Pkw- Klimatisierung Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der
Allgemeine Chemie. SS 2014 Thomas Loerting. Thomas Loerting Allgemeine Chemie
 Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Gaswärme-Institut e.v. Essen
 Experimentelle Untersuchung der Integration von Sensoren in die Steuerung industrieller Feuerungsprozesse zum Zweck der Erkennung wechselnder Erdgasbeschaffenheiten Christian Storm Kurzfassung des Abschlussberichts
Experimentelle Untersuchung der Integration von Sensoren in die Steuerung industrieller Feuerungsprozesse zum Zweck der Erkennung wechselnder Erdgasbeschaffenheiten Christian Storm Kurzfassung des Abschlussberichts
Druckgleichung nach Daniel Bernoulli (Bernoulligleichung)
 HTW Dresden V-SL1 Lehrgebiet Strömungslehre 1. Vorbetrachtung Druckgleichung nach Daniel Bernoulli (Bernoulligleichung) In ruhenden und bewegten Flüssigkeiten gilt, wie in der Physik allgemein, das Gesetz
HTW Dresden V-SL1 Lehrgebiet Strömungslehre 1. Vorbetrachtung Druckgleichung nach Daniel Bernoulli (Bernoulligleichung) In ruhenden und bewegten Flüssigkeiten gilt, wie in der Physik allgemein, das Gesetz
Chemische Reaktionen - physikalisch beschrieben
 Chemische Reaktionen - physikalisch beschrieben M. Seitz, M. Steinbrenner und P. Zachmann Chemische Reaktionen physikalisch beschrieben 1. Einleitung 2. Der Antrieb chemischer Reaktionen 3. Umsatz und
Chemische Reaktionen - physikalisch beschrieben M. Seitz, M. Steinbrenner und P. Zachmann Chemische Reaktionen physikalisch beschrieben 1. Einleitung 2. Der Antrieb chemischer Reaktionen 3. Umsatz und
Grundlagen der Chemie Elektrolyt- und Nichtelektrolytlösungen
 Elektrolyt- und Nichtelektrolytlösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektrolyt- und Nichtelektrolytlösungen
Elektrolyt- und Nichtelektrolytlösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektrolyt- und Nichtelektrolytlösungen
Der Dampfdruck von Wasser
 Physikalisches Grundpraktikum Versuch 8 Der Dampfdruck von Wasser Praktikant: Tobias Wegener Alexander Osterkorn E-Mail: tobias.wegener@stud.uni-goettingen.de a.osterkorn@stud.uni-goettingen.de Tutor:
Physikalisches Grundpraktikum Versuch 8 Der Dampfdruck von Wasser Praktikant: Tobias Wegener Alexander Osterkorn E-Mail: tobias.wegener@stud.uni-goettingen.de a.osterkorn@stud.uni-goettingen.de Tutor:
2. Zusammensetzung des Verbrennungsgases
 . Zusammensetzung des Verbrennungsgases Die Verbrennung ist die xidation des rennstoffs. Der benötigte Sauerstoff, die Zusammensetzung des Verbrennungsgases und die freiwerdende Wärme hängen von der Zusammensetzung
. Zusammensetzung des Verbrennungsgases Die Verbrennung ist die xidation des rennstoffs. Der benötigte Sauerstoff, die Zusammensetzung des Verbrennungsgases und die freiwerdende Wärme hängen von der Zusammensetzung
Laborbericht Temperaturmessung
 Laborbericht Temperaturmessung Gruppe IV SS 2001 Labortermin: 14.05.01 Versuchsleiter: Herr Tetau Betreuender Professor: Prof. Dr. H. Krisch Versuchsteilnehmer: Matthias Heiser Matr. Nr.: 1530330 Marco
Laborbericht Temperaturmessung Gruppe IV SS 2001 Labortermin: 14.05.01 Versuchsleiter: Herr Tetau Betreuender Professor: Prof. Dr. H. Krisch Versuchsteilnehmer: Matthias Heiser Matr. Nr.: 1530330 Marco
Grundlagen der Elektro-Proportionaltechnik
 Grundlagen der Elektro-Proportionaltechnik Totband Ventilverstärkung Hysterese Linearität Wiederholbarkeit Auflösung Sprungantwort Frequenzantwort - Bode Analyse Der Arbeitsbereich, in dem innerhalb von
Grundlagen der Elektro-Proportionaltechnik Totband Ventilverstärkung Hysterese Linearität Wiederholbarkeit Auflösung Sprungantwort Frequenzantwort - Bode Analyse Der Arbeitsbereich, in dem innerhalb von
Befreiung von der Strom- und Mineralölsteuer
 BHKW spart Ökosteuer Strom und Wärme Befreiung von der Strom- und Mineralölsteuer Bei einer Leistung kleiner als 2000 kw und einem Jahresnutzungsgrad von mehr als 70% sind BHKW von der Mineralöl- und der
BHKW spart Ökosteuer Strom und Wärme Befreiung von der Strom- und Mineralölsteuer Bei einer Leistung kleiner als 2000 kw und einem Jahresnutzungsgrad von mehr als 70% sind BHKW von der Mineralöl- und der
Thürnlhofstraße 5/8/809; 1110 Wien T: +43 660 405 67 92 E: bernhard.streibl@drs3.at
 Technischer Bericht Projekt: TOW / Fa. Wienerberger Datum: 0.05.013 Zusammenfassung: Erstellt durch: Durchführung von CFD-Berechnungen an einer mit Rauchgas durchströmten Ziegel/Kassetten-Einheit mit dem
Technischer Bericht Projekt: TOW / Fa. Wienerberger Datum: 0.05.013 Zusammenfassung: Erstellt durch: Durchführung von CFD-Berechnungen an einer mit Rauchgas durchströmten Ziegel/Kassetten-Einheit mit dem
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Physikalisches Anfängerpraktikum, Fakultät für Physik und Geowissenschaften, Universität Leipzig
 Physikalisches Anfängerpraktikum, Fakultät für Physik und Geowissenschaften, Universität Leipzig W 10 Wärmepumpe Aufgaben 1 Nehmen Sie die Temperatur- und Druckverläufe einer Wasser-Wasser-Wärmepumpe auf!
Physikalisches Anfängerpraktikum, Fakultät für Physik und Geowissenschaften, Universität Leipzig W 10 Wärmepumpe Aufgaben 1 Nehmen Sie die Temperatur- und Druckverläufe einer Wasser-Wasser-Wärmepumpe auf!
1. Aufgabe (18,5 Punkte)
 TECHNISCHE UNIVERSITÄT MÜNCHEN LEHRSTUHL FÜR THERMODYNAMIK Prof. Dr.-Ing. T. Sattelmayer Prof. W. Polifke, Ph.D. Diplomvorprüfung Thermodynamik I Wintersemester 2008/2009 5. März 2009 Teil II: Wärmetransportphänomene
TECHNISCHE UNIVERSITÄT MÜNCHEN LEHRSTUHL FÜR THERMODYNAMIK Prof. Dr.-Ing. T. Sattelmayer Prof. W. Polifke, Ph.D. Diplomvorprüfung Thermodynamik I Wintersemester 2008/2009 5. März 2009 Teil II: Wärmetransportphänomene
Berechnung von ORC-Prozessen mit Kältemitteln
 Hochschule für Angewandte Wissenschaften Hamburg Hamburg University of Applied Sciences Berechnung von ORC-Prozessen mit Kältemitteln Diplomarbeit Christoph Wiesner Matr.-Nr.: 1858108 1. Betreuer: Prof.
Hochschule für Angewandte Wissenschaften Hamburg Hamburg University of Applied Sciences Berechnung von ORC-Prozessen mit Kältemitteln Diplomarbeit Christoph Wiesner Matr.-Nr.: 1858108 1. Betreuer: Prof.
Motorkennlinie messen
 Aktoren kennlinie messen von Roland Steffen 3387259 2004 Aktoren, kennlinie messen Roland Steffen Seite 1/5 Aufgabenstellung: Von einer Elektromotor-Getriebe-Einheit ist eine vollständige kennlinienschar
Aktoren kennlinie messen von Roland Steffen 3387259 2004 Aktoren, kennlinie messen Roland Steffen Seite 1/5 Aufgabenstellung: Von einer Elektromotor-Getriebe-Einheit ist eine vollständige kennlinienschar
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht
 8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
Die moderne Ölheizung
 Fachtagung altbau plus, 03. September 2010 Die moderne Ölheizung aktuelle Forschungsprojekte am OWI: Untersuchungen zum Stand der Technik und aktuelle Entwicklungsarbeiten Dr.-Ing. Ralph Edenhofer, Gruppenleiter
Fachtagung altbau plus, 03. September 2010 Die moderne Ölheizung aktuelle Forschungsprojekte am OWI: Untersuchungen zum Stand der Technik und aktuelle Entwicklungsarbeiten Dr.-Ing. Ralph Edenhofer, Gruppenleiter
4 Die chemische Reaktion
 4 Die chemische Reaktion Chemische Reaktionen sind Stoffumwandlungsprozesse. In einer submikroskopischen Betrachtungsweise ist eine chemische Reaktion stets mit einer Änderung der relativen Lage der Atomkerne
4 Die chemische Reaktion Chemische Reaktionen sind Stoffumwandlungsprozesse. In einer submikroskopischen Betrachtungsweise ist eine chemische Reaktion stets mit einer Änderung der relativen Lage der Atomkerne
Ersatz von Erdgas durch gasförmige Energieträger aus der thermischen Biomassevergasung
 Ersatz von Erdgas durch gasförmige Energieträger aus der thermischen Biomassevergasung Fachworkshop Erneuerbare Energieträger in der Baustoff- und Dämmstoffproduktion Univ. Prof. Dr. Hermann Hofbauer Institute
Ersatz von Erdgas durch gasförmige Energieträger aus der thermischen Biomassevergasung Fachworkshop Erneuerbare Energieträger in der Baustoff- und Dämmstoffproduktion Univ. Prof. Dr. Hermann Hofbauer Institute
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Willkommen. welcome. bienvenu. Raumlufttechnik hx-diagramm Energierückgewinnung und Energieeffizienztechnologien
 Willkommen bienvenu welcome Raumlufttechnik hx-diagramm Energierückgewinnung und Energieeffizienztechnologien in der Lüftungstechnik Dipl.-Ing. Christian Backes backes@howatherm.de Dr.-Ing. Christoph Kaup
Willkommen bienvenu welcome Raumlufttechnik hx-diagramm Energierückgewinnung und Energieeffizienztechnologien in der Lüftungstechnik Dipl.-Ing. Christian Backes backes@howatherm.de Dr.-Ing. Christoph Kaup
Hocheffiziente KWK-Technik für Wärmeerzeuger in mittelständischen Unternehmen
 Hocheffiziente KWK-Technik für Wärmeerzeuger in mittelständischen Unternehmen Referent: Dipl.-Ing. (FH) Ralph von der Hagen Leiter der Niederlassung West der SAACKE Service GmbH in Erkrath 1 Felderfahrungen
Hocheffiziente KWK-Technik für Wärmeerzeuger in mittelständischen Unternehmen Referent: Dipl.-Ing. (FH) Ralph von der Hagen Leiter der Niederlassung West der SAACKE Service GmbH in Erkrath 1 Felderfahrungen
KÜHLKÖRPER RISIKEN UND NEBENWIRKUNGEN EINE ART BEIPACKZETTEL ALEXANDER C. FRANK, DIPL. ING. ETH ZÜRICH, V1.0 MÄRZ 2008 WWW.CHANGPUAK.
 KÜHLKÖRPER RISIKEN UND NEBENWIRKUNGEN EINE ART BEIPACKZETTEL ALEXANDER C. FRANK, DIPL. ING. ETH ZÜRICH, V1.0 MÄRZ 2008 WWW.CHANGPUAK.CH EINLEITUNG In Halbleitern entstehen Verluste, die in Form von Wärme
KÜHLKÖRPER RISIKEN UND NEBENWIRKUNGEN EINE ART BEIPACKZETTEL ALEXANDER C. FRANK, DIPL. ING. ETH ZÜRICH, V1.0 MÄRZ 2008 WWW.CHANGPUAK.CH EINLEITUNG In Halbleitern entstehen Verluste, die in Form von Wärme
- Chemie und Energie -
 Name: Datum: - Chemie und Energie - Eine Einführung zum 1. Hauptsatz der Thermodynamik 1: Heißer Kaffee aber wie?! Versuch 1: Kaffeetasse to go Becher Isolierbecher Sie haben heute Morgen verschlafen,
Name: Datum: - Chemie und Energie - Eine Einführung zum 1. Hauptsatz der Thermodynamik 1: Heißer Kaffee aber wie?! Versuch 1: Kaffeetasse to go Becher Isolierbecher Sie haben heute Morgen verschlafen,
Temperatur Wärme Thermodynamik
 Temperatur Wärme Thermodynamik Stoffwiederholung und Übungsaufgaben... 2 Lösungen... 33 Thermodynamik / 1 Einführung: Temperatur und Wärme Alle Körper haben eine innere Energie, denn sie sind aus komplizierten
Temperatur Wärme Thermodynamik Stoffwiederholung und Übungsaufgaben... 2 Lösungen... 33 Thermodynamik / 1 Einführung: Temperatur und Wärme Alle Körper haben eine innere Energie, denn sie sind aus komplizierten
Energieeffiziente Abluftreinigung
 Energieeffiziente Abluftreinigung Wärmerückgewinnungssysteme in Kombination mit thermischen Abluftreinigungsanlagen Dipl.-Ing. Ernst Luthardt YIT Abluftreinigung YIT 1 Internal Angenehme Wohn- und Arbeitsverhältnisse
Energieeffiziente Abluftreinigung Wärmerückgewinnungssysteme in Kombination mit thermischen Abluftreinigungsanlagen Dipl.-Ing. Ernst Luthardt YIT Abluftreinigung YIT 1 Internal Angenehme Wohn- und Arbeitsverhältnisse
Da eine Elektrolyse unter Anlegen einer äußeren Spannung erzwungen, d.h. mit G > 0, abläuft, ist der Zusammenhang zwischen G und U 0 nach
 Versuch PCA E 2 Polarisation und Zersetzungsspannung Aufgabenstellung Es sind die Temperaturabhängigkeit der Zersetzungsspannung einer 1,2 M HCl-Lösung sowie die Konzentrationsabhängigkeit der Zersetzungsspannung
Versuch PCA E 2 Polarisation und Zersetzungsspannung Aufgabenstellung Es sind die Temperaturabhängigkeit der Zersetzungsspannung einer 1,2 M HCl-Lösung sowie die Konzentrationsabhängigkeit der Zersetzungsspannung
wobei L die Länge der Wärmeübertragung und U der Umfang des Rohres oder Kanals Temperaturverläufe bei einem elektrisch beheizten Rohr
 5 5 Wärmeübertrager Wärmeübertrager sind Apparate, in denen ein Fluid erwärmt oder abgekühlt wird Das Heiz- oder Kühlmedium ist in der Regel ein anderes Fluid Verdampft oder kondensiert ein Fluid dabei,
5 5 Wärmeübertrager Wärmeübertrager sind Apparate, in denen ein Fluid erwärmt oder abgekühlt wird Das Heiz- oder Kühlmedium ist in der Regel ein anderes Fluid Verdampft oder kondensiert ein Fluid dabei,
Numerische Auslegung und CFD-Simulation einer Anlage zur Nutzung biogener Energieträger in Brennstoffzellen
 Numerische Auslegung und CFD-Simulation einer Anlage zur Nutzung biogener Energieträger in Brennstoffzellen Dr. Wolfram Heineken, Dipl.-Ing. T. Birth Fraunhofer-Institut für Fabrikbetrieb und -automatisierung
Numerische Auslegung und CFD-Simulation einer Anlage zur Nutzung biogener Energieträger in Brennstoffzellen Dr. Wolfram Heineken, Dipl.-Ing. T. Birth Fraunhofer-Institut für Fabrikbetrieb und -automatisierung
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008
 Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
Thermische Isolierung mit Hilfe von Vakuum. 9.1.2013 Thermische Isolierung 1
 Thermische Isolierung mit Hilfe von Vakuum 9.1.2013 Thermische Isolierung 1 Einleitung Wieso nutzt man Isolierkannen / Dewargefäße, wenn man ein Getränk über eine möglichst lange Zeit heiß (oder auch kalt)
Thermische Isolierung mit Hilfe von Vakuum 9.1.2013 Thermische Isolierung 1 Einleitung Wieso nutzt man Isolierkannen / Dewargefäße, wenn man ein Getränk über eine möglichst lange Zeit heiß (oder auch kalt)
