Herstellung kompetenter Zellen und Überprüfung des Kompetenzerhaltes
|
|
|
- Sven Brauer
- vor 6 Jahren
- Abrufe
Transkript
1 Bernhard-Strigel-Gymnasium Memmingen 1 Kollegstufe Jahrgang: 2006/2008 Leistungskurs: Biologie Kollegiat: Jana Krieger FACHARBEIT Herstellung kompetenter Zellen und Überprüfung des Kompetenzerhaltes Abgegeben am: Bewertung: Facharbeit: Mündliche Prüfung: Gesamtergebnis: Punkte Punkte Punkte Datum und Unterschrift des Kursleiters:
2 2 Inhaltsverzeichnis 1. Einleitung.2 2. Plasmidisolation Die Isolation von Plasmiden mit Hilfe eines Kits Der Nachweis der Isolation der Plasmide mit einer Agarose- Gelelektrophorese Durchführung der Gelelektrophorese Vorbereitung für die Herstellung kompetenter Zellen Vorbereitungen Bau einer geeigneten Vorbereitung der Chemikalien Messen der Optischen Dichte Herstellung chemisch kompetenter Zellen (CaCl 2 -Methothode) Transformation chemisch kompetenter Zellen Auswertung Langzeitstudie Ergebnis Fehleranalyse Literaturverzeichnis Anhang...15
3 3 1. Einleitung Das Thema der Facharbeit entstand während eines Praktikums im Biotechnologie Labor des Bernhard - Strigel Gymnasiums in Memmingen. Während dieses Praktikums wurden verschiedene Methoden und Arbeitsvorgänge die man mit Zellen (in unserem Fall mit E.coli) durchführen kann erläutert, unter anderem auch die Transformation. Da zu diesem Zeitpunkt noch keine chemisch kompetenten Zellen vorrätig waren, hat der Vorgang des Transformierens viel Zeit in Anspruch genommen, daraus entstand die Idee solche Zellen mit der Calciumchlorid - Methode zu erzeugen und auf Vorrat ein zu frieren, was die Arbeit anderer im Labor erleichtern würde. In einem zweiten Teil meiner Facharbeit soll mit Hilfe einer Langzeitstudie untersucht werden, wie lange man mit den Zellen arbeiten kann. Normalerweise werden die Zellen bei -80 C eingefroren und sind dadurch sehr lang haltbar. Da die Zellen im Labor lediglich bei -18 C eingefroren werden können, stellt sich die Frage ob die Zellen nach einem gewissen Zeitraum immer noch kompetent sind und wenn ja, wie lange genau sich die Kompetenz erhält. 2. Plasmidisolation 2.1 Die Isolation von Plasmiden mit Hilfe eines Kits Um das Plasmid puc18 zu isolieren wurde ein Kit der Firma Qiagen (QIAprep Miniprep aus dem Jahr 2003 Cat. No ) verwendet. Zur Durchführung der Isolation von Plasmiden hab ich das Original-Protokoll des Quiaprep- Kits übersetzt und unserer Durchführung angepasst. Die original Anleitung findet sich in dem beigefügten Handbuch des Kits (QIAGEN; 2003) auf der Seite Alle Schritte müssen bei Raumtemperatur durchgeführt werden 1. Ein Eppi mit Bakterienlösung muss zentrifugiert werden und der Überstand wird verworfen. 2. Das Pellet wird nun mit 250 µl Puffer P1 resuspendiert. Es ist wichtig sicherzustellen das RNase A zu dem Puffer P1 hinzugefügt wurde. Nach dem Resuspendieren sollten keine Zellklumpen mehr zu sehen sein. 3. Jetzt müssen 250 µl des Buffers P2 hinzugefügt werden und das Eppi muss zum Mischen 4 6 mal vorsichtig gedreht werden. Das Eppi muss zum Mischen vorsichtig gedreht und nicht geschüttelt werden, da sonst die chromosomale DNA zerrissen wird und diese dann bei der Gelelektrophorese zu Schwierigkeiten bei der Identifizierung der Plasmide bereitet. Wenn es notwendig ist, dann muss das Eppi solange gedreht werden bis die Lösung dickflüssig und leicht durchsichtig wird, aber die Lyse darf nicht mehr als 5 min dauern. 4. Nun müssen 350 µl des Puffers N3 hinzu gegeben werden und das Eppi muss vorsichtig gemischt werden, indem man es erneut 4 6 mal dreht. Damit es nicht zum nur teilweisen Ausfall kommt, muss die Lösung vorsichtig aber gründlich gemischt werden nachdem der Puffer N3 hinzugefügt wurde. Die Lösung sollte jetzt trüb werden.
4 4 5. Anschließend muss die Lösung 10 min bei rpm zentrifugiert werden. Eis bildet sich nun ein festes weißes Pellet. 6. Der Überstand wird in die Reinigungssäule des QIAprep Kits gefüllt oder pipettiert. (Die Reinigungssäule muss in ein Eppi gesteckt werden.) 7. Nun muss erneut für s zentrifugiert werden. Der Rückstand der sich im Eppi befindet wird verworfen. 8. Die Reinigungssäule muss jetzt gereinigt werden, indem man 0,75 ml des Puffers PE dazugibt und wieder für s zentrifugiert. (Wahlweise): muss die Reinigungssäule nochmals 0,5 ml des Puffers PB dazugegeben werden und erneut für s zentrifugiert werden. Dies ist in unserem Gebrauch nicht nötig da wir mit normalen Plasmiden arbeiten. 9. Der Rest, der sich nun in dem Eppi befindet, muss verworfen werden und die Reinigungssäule muss erneut für 1 min zentrifugiert werden, um den Rest des Reinigungspuffers zu entfernen. Wichtig: der Reinigungspuffer wird nicht vollständig entfernt, wenn vor dem zweiten Mal des Zentrifugierens der Rest der sich in dem Eppi befindet nicht entfernt wird. Reste von Ethanol die sich in dem Puffer PE befinden können die nachfolgende enzymatische Reaktion hemmen. 10. Die Reinigungssäule muss nun in ein neues steriles 1,5 ml Eppi gesteckt werden und um die DNA aus der Säule zu lösen müssen 50 µl des Puffers EB oder Wasser dazugegeben werden nachdem es eine Minute stehen gelassen wird muss es eine Minute zentrifugiert werden. Der jetzt entstehende Rest der sich in dem Eppi befindet ist die Plasmid - Lösung. Zusammenfassung 1. Eppi mit Bakterienlösung zentrifugieren und Überstand verwerfen; 2. Pellet mit 250 µl Puffer P1 resuspendieren µl Puffer P2 hinzu geben und 4 6 mal drehen µl Puffer N3 hinzugeben und erneut 4 6 mal drehen 5. Lösung 10 min zentrifugieren 6. Überstand in Reinigungssäule pipettieren s zentrifugieren Rückstand verwerfen 8. 0,75 ml Puffer PE dazugeben und erneut s zentrifugieren 9. Rückstand verwerfen und noch mal 1 min zentrifugieren 10. Reinigungssäule in steriles Eppi und 50 µl Puffer EB hinzu pipettieren; 1 min stehen lassen und 1 min zentrifugieren 11. Entstandener Rest ist die Plasmidlösung
5 5 2.2 Der Nachweis der Isolation der Plasmide mit Hilfe einer Agarose- Gelelektrophorese "Die Agarose - Gelelektrophorese ist die einfachste und effektivste Methode, mit der DNA-Fragmente zwischen 0,5 und 25 kb (= kilo - Basen) Länge voneinander getrennt und identifiziert werden können. Das Prinzip der Elektrophorese beruht darauf, dass geladene Moleküle, wie z.b. DNA im elektrischen Feld wandern. Die Auftrennung erfolgt in einem elektrischen Gleichstromfeld unter konstantem ph-wert (= Elektrophoresepuffer), wobei die Fragmente ja nach Ladung, Masse und Gestallt unterschiedlich schnell durch das Agarosegel wandern. (SCHMITT; 2006 Seite 19) Durchführung der Gelelektrophorese Die Durchführung der Gelelektrophorese wird nach dem Protokoll vom Biotechnologie Labor durchgeführt (SCHMITT; 2006 Seiten19-22) durchgeführt. Giesen des Gels Material: Agarose TAE-Puffer Rührfisch und Glasflasche Gelkammer mit Kamm Lederhandschuhe Durchführung: Um ein 1% -iges Agarosegel herzustellen werden 0,6 g Agarose abgewogen und mit 60 ml TAE-Puffer aufgegossen. Der Rührfisch wird gleich dazu gegeben, um den Siedeverzug zu vermeiden. Nun muss die Flasche unter Beobachtung in der Mikrowelle aufkochen. Anschließend wird die Flasche mit den Handschuhen entnommen und vorsichtig in die Gelkammer gegossen. Nach dem Gießen wird nur noch der Kamm eingesetzt und gewartet bis das Gel abkühlt und trüb wird. Zusammenfassung: 1. 0,6 g Agarose mit 60 ml TAE Puffer in einer Flasche aufgießen 2. in der Mikrowelle aufkochen 3. vorsichtig in die Gelkammer gießen 4. Gelkamm einsetzen und warten bis das Gel kühl wird
6 6 Beladen und Lauf des Gels Material: Plasmidlösung Gelladungspuffer DNA - Größenstandart TAE Puffer ( liegt in der richtigen Konzentration im Labor vor) Sterile Eppis Gelkammer und Spannungsquelle Labormixer Durchführung: Zuerst muss die Plasmid - Lösung in ein steriles Eppi mit 2µl Gelladungspuffer vermischt werden. Anschießend muss der TAE-Puffer in die Gelkammer gegossen werden, bis das Gel leicht bedeckt ist. Danach muss der Gelkamm entfernt werden. In die beiden äußeren Taschen müssen je 5 µl des Größenmarkers pipettiert werden. Die Größenmarker dienen dazu die Plasmide nach der Färbung zu identifizieren. Jetzt können die Proben vorsichtig in die Geltaschen zwischen den Markern pipettiert werden. Dabei ist es wichtig darauf zu achten, dass schriftlich festgehalten wird, welche Probe in welche Tasche gefüllt wird. Nach dem Pipettieren wird die Spannung angeschlossen, dabei muss die Polung beachtet werden. (DNA ist negativ geladen und wandert daher zum positiven Pol) Beim einschalten der Spannungsquelle ist es wichtig darauf zu achten dass maximal 7 V Spannung je cm Elektrodenabstand einzuhalten sind. In diesem Versuch entspricht es 98 V bei einem Elektrodenabstand von 14 cm. Das Gel muss nun so lange laufen bis die blaue Bande fast am Ende des Gels angelangt ist. Färbung und Auswertung des Gels: Material: Ethidiumbromidlösung UV Leuchttisch Aufgrund des vermuteten krebserregenden Potentials von Ethidiumbromid werden [diese Arbeitsschritte] durch die Lehrkraft Durchgeführt (SCHMITT; 2006 Seite 19) Erst nach der Färbung mit Ethidiumbromid werden die DNA Banden unter dem UV Licht sichtbar und man kann sie durch den Abgleich mit dem DNA - Größenstandart identifizieren.
7 7 Abbildung 1: Foto der Färbung des Elektrophoresegels im Biotechnologie Labor des Bernhard-Strigel-Gymnasiums in Memmingen 3. Vorbereitung für die Herstellung chemisch kompetenter Zellen 3.1 Vorbereitungen: Bau einer geeigneten Kühlbox Abbildung 2: Foto der Kühlbox
8 8 Materialien: 2 Styroporboxen Styroporkleber Spanngurte Styroporschneidedraht Teppichmesser Bauanleitung : Die Kühlbox wird verwendet und darin die Zentrifuge auf Eis stellen zu können, da es wichtig ist bei der CaCl 2 -Methothode die 4 C einzuhalten. Da im Labor keine geeignete Styroporbox in die eine Zentrifuge hinein passt vorhanden war, musste eine gebaut werden. Dazu wurden zwei kleine Boxen je an einer Seite aufgeschnitten, dabei ist es wichtig den Deckel auf der Box zulassen, da es sonst dazu kommen kann dass der Deckel anschließend nicht mehr passt. Danach müssen die beiden Hälften der großen Box zusammengeklebt werden, dazu muss unbedingt ein geeigneter Styroporkleber (Patex) benutzt werden. Nach dem Auftragen des Klebers müssen die beiden Teile fest auf einender gedrückt werden und der überstehende Kleber mit einer Spachtel abgekratzt werden (Innen und Außen). Zum Fixieren der Box, die nun über Nacht trocknen muss, benutzt man am besten Spanngurte. Um besser arbeiten zu können, muss man den Deckel zweigeteilt lassen, so kann man später zum Beispiel die Temperatur im Inneren besser kontrollieren. Am nächsten Tag, wenn die Box ausgetrocknet ist, wird ein Podest für die Zentrifuge gebaut, da das Eis welches später hineingefüllt wird schmilzt und es zu einem Kurzschluss in der Zentrifuge führen kann. Dazu wird das restliche Styropor das übrig geblieben ist verwendet. Es reicht aus wenn das Podest ca. 4 cm hoch ist. Des weiteren muss die Styroporbox aufgrund der Breite der Zentrifuge an den Seiten (Innen) mit dem Teppichmesser ausgeschnitten werden. Nachdem die Box zusammengebaut ist, ist es wichtig diese auch darauf zu testen ob sie dicht ist, dazu füllt man diese mit Wasser und schaut dann, ob etwas ausläuft, wenn dass der Fall ist dann sollte man auf diese Stelle noch mal Styroporkleber auftragen, noch mal trocknen lassen und dann einen erneuten Test durchzuführen. Außer auf die Dichte muss die Kühlbox auch noch darauf getestet werden, ob sie die 4 C auch über längere Zeit hält. Dazu gibt man Eis und ein Thermometer in die Box und schaut ob die gewünschte Gradzahl erreicht wird und über die gewünschte Zeitspannen gehalten wird. Um die 4 C während des ganzen Arbeitsvorganges zu halten, ist es am besten wenn man für den Mixer auch eine entsprechende Kühlbox baut, diese kann jedoch auch ohne Deckel sein. Wichtig: Damit es mit dem Eis und den Geräten keine Zwischenfälle gibt benutzt man am besten Eisbeutel statt der normalen Eiswürfelformen, da das Eis in den Beuteln gelassen werden kann, weil diese (selbst wenn das Eis schmilzt) auslaufsicher sind und das Eis mehrfach verwendet werden kann.
9 Vorbereitungen der Chemikalien Material: (ALBERT; 2007 a) 100 ml Mol. Calciumchlorid (autoklaviert) 100 ml Mol. Calciumchlorid in 90 % Glycerin Lösung (autoklaviert) LB Medium (autoklaviert) in zwei Behältern Genügend Eis Hinweis: Bevor man mit der Herstellung chemisch kompetenter Zellen beginnen kann, ist es wichtig zu kontrollieren ob alle Chemikalien vorhanden sind (am besten ein bis zwei Tage vorher, so hat man die Möglichkeit die fehlenden Komponenten zu besorgen) Messen der optischen Dichte Material: E.coli Bakterien LB Medium Spektralphotometer Pipetten und Spitzen Küvetten Am (einen Tag vor dem Beginn der Arbeit mit den E.coli Bakterien) wurde eine Übernachtkultur E.coli Bakterien angelegt. Dazu wurde LB - Medium angeimpft und bei 37 C über Nacht in den Inkubator gestellt. Am konnte mit der Herstellung chemisch kompetenter Zellen begonnen werden. Hierzu wird 1 ml der Übernachtkultur in den zweiten Behälter mit dem LB - Medium pipettiert und wiederum bei 37 C in den Inkubator gegeben. Da bei der Herstellung chemisch kompetenter Zellen nach der CaCl 2 Methode ein Wert der optischen Dichte von 0,4-0,6 bei 600 nm verlangt wird, musst dieser nun mit der Hilfe eines Spektralphotometers gemessen werden. Damit bei der Messung die richtigen Werte resultieren, muss das LB Medium als Nullwert festgelegt werden. Zum Bestimmen der OD wird nun in immer kürzer werdenden Zeitabständen gemessen, indem immer wieder etwas aus der neu angelegten Kultur entnommen und in die Küvette gegeben und gemessen wird, bis nach 2,5 h der gewünschte Wert von 0,452 erreicht wurde.
10 10 Zeit OD Zeit OD 11: :15 0,148 13:44 0,276 14:05 0,382 14:16 0,452 13: :10 0,101 13:40 0,120 14:30 0,288 14:50 0,430 Tabelle1: Messung vom Tabelle 2: Messung vom Herstellung chemisch kompetenter Zellen (CaCl 2 -Methothode) Anschließend wird die Herstellung chemisch kompetenter Zellen laut dem Protokoll (ALBERT; 2007 a) durchgeführt: Hinweis: Dazu muss zuerst die Bakterienlösung in sterile Eppis umgefüllt werden. Materialien: Kühlbox Eppis (steril) Pipetten und Spitzen Zentrifuge und Mixer Inkubator Plasmid - Lösung E.coli Bakterien Calciumchlorid und CaCl 2 in 90% Glycerin Durchführung: Die Zellen werden 5 min bei rpm und bei 4 C zentrifugiert. Anschließend wird der Überstand verworfen und die Zellen in dem vorgekühlten Calciumchlorid resuspendiert. Danach erneut 5 min bei rpm zentrifugiert und der Überstand verworfen. Jetzt muss in jedes Eppi noch ca. 1 ml CaCl 2 in 90% Glycerinlösung pipettiert werden. Danach kommen alle Eppis in den Gefrierschrank.
11 11 Um nachzuweisen, dass die E.coli Bakterien nun chemisch kompetent sind, wird jetzt eine Transformation durchgeführt. Dabei werden die Plasmide puc18 die wir bei der Isolation erhalten haben und die eine Ampicilin - Resistenz enthalten in die E.coli Bakterien transformiert. 4. Transformation chemisch kompetenter Zellen Material: Hitzeblock Plasmid - Lösung Eis LB - Medium Schüttler Klebeband Ampicillin- Agarplatten Um die Transformation der Zellen durchführen zu können muss ein Hitzeblock oder ein Wasserbad vorbereitet und die Menge der Plasmide berechnet werden, dies ist mit Hilfe der QIAprep Miniprep Handbook (QIAGEN; 2003) möglich diese Anleitung findet sich auf der Seite 13 unter dem Punkt DNA Yield (bei mir waren es 5 µl). Durchführung: Die Herstellung kompetenter Zellen wird nach Protokoll durchgeführt (ALBERT; 2007 a): Wichtig: Alle Arbeitsschritte müssen bei 4 C stattfinden! Bevor mit der Transformation begann werden kann, müssen die Zellen auf Eis aufgetaut werden, dies dauerte ca. 20 Minuten beim ersten Mal werden gleich die neuen noch nicht eingefrorenen Bakterien verwendet. Nach dem auftauen der Zellen, wird die berechnete Menge an Plasmid - Lösung dazugegeben, darauf folgt ein Hitzeschock von s bei 42 C im Wasserbad oder Hitzeblock. Danach werden die Bakterien für 2 Minuten auf Eis gestellt und 400 µl LB -Medium dazu pipettiert. Anschließend kamen die Zellen für eine Stunde bei 37 C auf den Schüttler (das Eppi muss mit einem Streifen Klebeband auf dem Schüttler fixiert werden). Nach einer Stunde werden die Zellen auf Ampicillin- Agarplatten ausplattiert um zu kontrollieren ob die Bakterien das Plasmid aufgenommen haben. 5. Auswertung : Um zu beweisen, dass die Bakterien die vorher kein Plasmid hatten, nun eins aufgenommen haben werden diese zu 50 µl auf Ampicillin -Agarplatten ausplattiert und über Nacht in den Inkubator gegeben. Wenn die Bakterien das Plasmid aufgenommen haben, so müssen sie auf
12 12 den Ampicillin - Agarplatten wachsen, wenn sie es nicht tun, dann ist die Herstellung der kompetenten Zellen fehlgeschlagen. Am nächsten Tag müssen die auf denn Platten wachsenden Bakterienkolonien ausgezählt und notiert. Hinweis: Beim Auszählen sollten die Kolonien mit einem dünnen Edding markiert werden damit keine doppelt gezählt werden, nebenbei sollte eine Strichliste geführt werden auf der für je 10 Kolonien einen Strich gemacht wird, so ist es am Ende einfacher alles zusammen zu zählen. Abbildung 3: Ampicillin Agarplatte Abbildung 4: Ampicillin Agarplatten der Transformation vom der Transformation vom Langzeitstudie Die Langzeitstudie ist der zweite Teil der Facharbeit, sie soll zeigen wie lange Zellen kompetent sind. Dazu wurde in regelmäßigen Zeitabständen eine Transformation durchgeführt und die Bakterienkolonien auf den Ampicillin - Agarplatten ausgezählt. Da aufgrund der Sommerferien, 6 Wochen lang nicht die Möglichkeit bestand Transformationen durchzuführen, wurden neue chemisch kompetente Zellen Hergestellt, um die fehlende Zeit nachvollziehen zu können. Dies war jedoch nicht aussagekräftig, da bei der zweiten Durchführung Fehler unterlaufen sind (siehe 5.3 Fehleranalyse). Um die neuen Zellen leichter von den alten unterscheiden zu können, wurden beim zweiten mal andere Eppis genommen. Des weiteren musste nun bei der Transformation darauf geachtet werden, dass die Ampicillin Agarplatten immer richtig beschriftet waren (in diesem Fall wurden die Platten mit ALT und mit NEU gekennzeichnet. Das nachfolgende Diagramm zeigt die Anzahl der Kolonien und die Wochenabstände in denen eine Transformation durchgeführt wurde.
13 Ergebnis: Diagramm 1: Ergebnis der Langzeitstudie Der schraffierte Balken zeigt einen konstruierten Wert, da es ein Bakterienrasen war und es aufgrund des Verlaufes der Kurve anzunehmen ist, dass das die ungefähre Anzahl der Kolonien ist, die sich auf der Platte befanden. Wie man ich dem Diagramm erkennen kann ist bereits der erste Balken der Kompetenz vom weitaus niedriger als der vom , des weiteren erreichen die Balken der zweiten Herstellung schon nach 9 Wochen den Nullwert. Das liegt daran dass mir bei der zweiten Herstellung der chemisch kompetenten Zellen einige Fehler unterlaufen sind (siehe Fehleranalyse) des weiteren sind die Bakterien der ersten Herstellung viel länger haltbar, so sind die Zellen vom nach 20 Wochen immer noch kompetent die vom jedoch sind bereits nach der 9 Woche schon nicht mehr zum weiterarbeiten zu gebrauchen. Es kann davon ausgegangen werden, dass die ausgangs Menge der Zellen entscheidend dafür ist, wie lange die Zellen kompetent bleiben (weitere Ausführungen dazu in der Fehleranalyse).
14 Fehleranalyse Da aufgrund der Ferien die Transformationen für die Langzeitstudie nicht konstant durchgeführt werden konnte, ist eine Lücke von ca. 6 Wochen entstanden. Um diese fehlende Zeit nachvollziehen zu können, wurden am neue kompetente Zellen erzeugt. Dabei sind aber einige Fehler unterlaufen. Da aufgrund dessen, dass bei der zweiten Herstellung andere Eppis benutzt wurden, die nicht komplett in den Hitzeblock gepasst haben, wurde ein Wasserbad vorbereitet, um dies als Fehlerquelle ausschließen zu können. Jedoch hatte der Wechsel vom Hitzeblock zum Wasserbad keine Auswirkungen auf die Ergebnisse der Transformation. Eine anderer Fehler war der, dass bei der ersten Herstellung der chemisch kompetenten Zellen die Menge der Bakterienlösung die in die Eppis gefüllt wurde nicht genau bestimmt war, sondern lediglich 1 ml der Bakterienlösung abgefüllt und dann zentrifugiert, den Überstand verworfen und erneut 1ml abgefüllt wurde. Dadurch kam es dazu, dass ich bei der zweiten Herstellung nicht die gleiche Menge an Bakterien in den Eppis hatte wie beim ersten Mal. Dies könnte ein Grund dafür sein, dass die Bakterien der zweiten Herstellung nicht so lange kompetent waren wie die der ersten. Ein weiterer Grund für die kürzere Haltbarkeit der chemisch kompetenten Bakterien der zweiten Durchführung des Versuches, könnte ein Fehler sein der durch Nachlässigkeit entstanden ist. Da bei den Vorbereitungen der zweiten Herstellung der Zellen das LB- Medium in das 1 ml der Bakterienlösung der Übernachtkultur gehört hätte, lediglich angeimpft wurde, wurden nach einer Absprache mit Herrn Schmitt (Betreuende Lehrkraft) weitere 3 ml mehr von der Bakterienlösung in das LB-Medium hinzu geben.. Dadurch waren jetzt aber mehr Stoffwechselprodukte der Bakterien in dem Behälter, was dazu führt dass das Ergebnis der Messung der Optischen Dichte verfälscht wurde, da die Lösung jetzt durch die Stoffwechselprodukte trüber war als die der ersten Herstellung. Hinzu kommt noch, dass der OD der ersten Durchführung höher war als der der zweiten (vergleiche Tabellen 3.1.3). 6. Literaturangaben: (1) a ALBERT; Markus; Dr. (2007): Persönliche Mitteilung : Durchführungsprotokoll Transformation chemisch kompetenter Zellen Uni Darmstadt (2) b ALBERT; Markus; Dr. (2007): Persönliche Mitteilung: Herstellung chemisch kompetenter Zellen (CaCl 2 -Methode) Uni Darmstadt (3) MÜHLHARDT; Cornel. (2003): Der Experimentator: Molekurbiologie/ Genomics. 4.Auflage. München: Spektrum Akademischer Verlag, ISBN: (4) SCHMITT; Patrick, (2006): Einführung in die Grundarbeitstechniken der Molekularbiologie, Memmingen (5) Q IAGEN (2003); QIAprep Miniprep Handbook Cat. No Bilder: Abbildung1: Quelle: SCHMITT; Patrick, (2006): Persönliche Mitteilung
15 15 7. Anhang: Schülererklärung: Ich erkläre, dass ich die Facharbeit ohne fremde Hilfe angefertigt und nur die im Literaturverzeichnis angeführten Quellen und Hilfsmittel benützt habe. Memmingen, den Jana Krieger
2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
 Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
Facharbeit. Restriktionsverdau am Plasmid puc 18 mit verschiedenen Enzymen
 Bernhard Strigel Gymnasium Kollegstufe/ Jahrgang: 2007/ 2009 Memmingen Leistungskurs: Biologie Kollegiat: Stefanie Funk Facharbeit Restriktionsverdau am Plasmid puc 18 mit verschiedenen Enzymen Abgegeben
Bernhard Strigel Gymnasium Kollegstufe/ Jahrgang: 2007/ 2009 Memmingen Leistungskurs: Biologie Kollegiat: Stefanie Funk Facharbeit Restriktionsverdau am Plasmid puc 18 mit verschiedenen Enzymen Abgegeben
Versuchsanleitung: RFLP als Modell für einen DNA-Fingerprint
 RFLP als Modell für einen DNA-Fingerprint Teil 1: Restriktionsverdau 1.1: Thermoblock / Wasserbad auf 37 C vorheizen 1.2: Puffer Y+/Tango auftauen und auf Eis stellen 1.3: 4 Proben, RSA I und H 2 O demin.
RFLP als Modell für einen DNA-Fingerprint Teil 1: Restriktionsverdau 1.1: Thermoblock / Wasserbad auf 37 C vorheizen 1.2: Puffer Y+/Tango auftauen und auf Eis stellen 1.3: 4 Proben, RSA I und H 2 O demin.
Zellbiologie und Physiologie Labormethoden der Biologie
 Zellbiologie und Physiologie Labormethoden der Biologie > Molekularbiologie I Plasmidpräparation Molekularbiologie I Transformation Gel-Elektrophorese Dr. Stefan Weinl > Plasmid-Isolierung aus E. coli
Zellbiologie und Physiologie Labormethoden der Biologie > Molekularbiologie I Plasmidpräparation Molekularbiologie I Transformation Gel-Elektrophorese Dr. Stefan Weinl > Plasmid-Isolierung aus E. coli
Klonierung von GFP in E.coli
 Bernhard-Strigel-Gymnasium Memmingen Kollegstufe Jahrgang:...2007/2009 Leistungskurs:...Biologie Kollegiatin:...Nicole Makowski Facharbeit Klonierung von GFP in E.coli Abgegeben am: 30.01.2009 Bewertung:
Bernhard-Strigel-Gymnasium Memmingen Kollegstufe Jahrgang:...2007/2009 Leistungskurs:...Biologie Kollegiatin:...Nicole Makowski Facharbeit Klonierung von GFP in E.coli Abgegeben am: 30.01.2009 Bewertung:
Probe und Probenmenge Wassermenge Auftragspuffermenge 5 µl Kaninchenmuskelextrakt 50 µl 100 µl
 Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
Plasmidisolierung. Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern.
 Plasmidisolierung Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern. Was können Sie lernen? Sie lernen eine ringförmige DNA, ein Plasmid, zu isolieren. Mit diesem
Plasmidisolierung Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern. Was können Sie lernen? Sie lernen eine ringförmige DNA, ein Plasmid, zu isolieren. Mit diesem
Facharbeit. Sphagnumklassifikation durch Sequenzanalyse
 Bernhard-Strigel-Gymnasium Kollegstufe Jahrgang:... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiatin:... Marina Schweizer Facharbeit Sphagnumklassifikation durch Sequenzanalyse Abgegeben am:
Bernhard-Strigel-Gymnasium Kollegstufe Jahrgang:... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiatin:... Marina Schweizer Facharbeit Sphagnumklassifikation durch Sequenzanalyse Abgegeben am:
Bernhard-Strigel-Gymnasium Kollegstufe /2011 Leistungskurs:... Biologie Kollegiat:... Tamara Bruno. Facharbeit
 - 1 - Bernhard-Strigel-Gymnasium Kollegstufe... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiat:... Tamara Bruno Facharbeit Versuch einer Sphagnum-Klassifikation durch Restriktionsverdau Abgegeben
- 1 - Bernhard-Strigel-Gymnasium Kollegstufe... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiat:... Tamara Bruno Facharbeit Versuch einer Sphagnum-Klassifikation durch Restriktionsverdau Abgegeben
1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II
 Arbeitsblatt 1 Analyse von DNA 1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II Bevor Sie anfangen: Alle Reagenzien müssen vor Gebrauch vollständig aufgetaut sein und durchmischt
Arbeitsblatt 1 Analyse von DNA 1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II Bevor Sie anfangen: Alle Reagenzien müssen vor Gebrauch vollständig aufgetaut sein und durchmischt
Plasmidpräparation aus Bakterien Inhalt
 Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele
 Versuch 1: Restriktionsenzyme als molekulare Werkzeuge Versuchsinhalt Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele Zwei
Versuch 1: Restriktionsenzyme als molekulare Werkzeuge Versuchsinhalt Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele Zwei
Molekulare Klonierung Praktikum
 Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
3 GFP green fluorescent protein
 SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen
 F2-Praktikum Genetik Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen Gruppe 4 (Susanne Duncker, Kristin Hofmann) Einleitung Wir untersuchten in diesem Versuch die Effizienz der VDJ-Rekombination
F2-Praktikum Genetik Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen Gruppe 4 (Susanne Duncker, Kristin Hofmann) Einleitung Wir untersuchten in diesem Versuch die Effizienz der VDJ-Rekombination
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS
 Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Herstellung kompetenter Zellen und Nachweis durch Blau-Weiß-Selektion
 Bernhard-Strigel-Gymnasium Memmingen Kollegstufe Jahrgang: 2006/2008 Leistungskurs: Biologie Kollegiat: Martha Dziuk FACHARBEIT Herstellung kompetenter Zellen und Nachweis durch Blau-Weiß-Selektion Abgegeben
Bernhard-Strigel-Gymnasium Memmingen Kollegstufe Jahrgang: 2006/2008 Leistungskurs: Biologie Kollegiat: Martha Dziuk FACHARBEIT Herstellung kompetenter Zellen und Nachweis durch Blau-Weiß-Selektion Abgegeben
Modifizierte Gene Editor Mutagenese
 Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
1. Proteinnachweis mit Bradford-Farbreagenz
 1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
Auf der Suche nach der Wundermedizin
 Auf der Suche nach der Wundermedizin Experimente im Schullabor 1 Herausgeber Novartis Pharma AG, CH-4002 Basel Autoren: Dr. Gesche Standke und Dr. Christiane Röckl Michel Zeichnungen: Fonds der Chemischen
Auf der Suche nach der Wundermedizin Experimente im Schullabor 1 Herausgeber Novartis Pharma AG, CH-4002 Basel Autoren: Dr. Gesche Standke und Dr. Christiane Röckl Michel Zeichnungen: Fonds der Chemischen
Auf der Suche nach der Wundermedizin
 Auf der Suche nach der Wundermedizin Experimente im Schullabor 1 Herausgeber Novartis Pharma AG, CH-4002 Basel Autoren: Dr. Gesche Standke und Dr. Christiane Röckl Michel Zeichnungen: Fonds der Chemischen
Auf der Suche nach der Wundermedizin Experimente im Schullabor 1 Herausgeber Novartis Pharma AG, CH-4002 Basel Autoren: Dr. Gesche Standke und Dr. Christiane Röckl Michel Zeichnungen: Fonds der Chemischen
GFP - Klonierung in E.coli
 Bernhard-Strigel-Gymnasium Kollegstufe Jahrgang:...2008/2010 Memmingen Leistungskurs:...Biologie Kollegiatin:...Anja Rießenberger Facharbeit GFP - Klonierung in E.coli Abgegeben am Bewertung: Facharbeit:
Bernhard-Strigel-Gymnasium Kollegstufe Jahrgang:...2008/2010 Memmingen Leistungskurs:...Biologie Kollegiatin:...Anja Rießenberger Facharbeit GFP - Klonierung in E.coli Abgegeben am Bewertung: Facharbeit:
Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten
 Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten erstellt vom Unterausschuß Methodenentwicklung des LAG 1. Zweck und Anwendungsbereich
Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten erstellt vom Unterausschuß Methodenentwicklung des LAG 1. Zweck und Anwendungsbereich
Western Blot. Zuerst wird ein Proteingemisch mit Hilfe einer Gel-Elektrophorese aufgetrennt.
 Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Gentechnologie: Isolierung und Charakterisierung von DNA
 Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
MODULE für den SCHULKOFFER GENTECHNIK
 MODULE für den SCHULKOFFER GENTECHNIK Modul 1 - DNA-Bastel-Set Zusammenbau eines Papiermodells in Form einer Doppelhelix sehr einfach, Unterstufe, ohne Koffer möglich Modul 2 - DNA-Isolierung aus Gemüse
MODULE für den SCHULKOFFER GENTECHNIK Modul 1 - DNA-Bastel-Set Zusammenbau eines Papiermodells in Form einer Doppelhelix sehr einfach, Unterstufe, ohne Koffer möglich Modul 2 - DNA-Isolierung aus Gemüse
Durchführung einer Gel-Elektrophorese mit einem DNA-Gemisch
 Durchführung einer Gel-Elektrophorese mit einem DNA-Gemisch (Fotos vom 6. März 2013 Molekularbiologisches Praktikum 12 G-Kurs Biologie Herr Korne - am KOMM Homburg/Saar unter Anleitung von Frau Dr. Amoroso)
Durchführung einer Gel-Elektrophorese mit einem DNA-Gemisch (Fotos vom 6. März 2013 Molekularbiologisches Praktikum 12 G-Kurs Biologie Herr Korne - am KOMM Homburg/Saar unter Anleitung von Frau Dr. Amoroso)
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Plasmid DNA purification
 Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
(Nur für die Forschung) Bei Kontakt mit Augen oder Haut sofort mit viel Wasser abspülen!
 Datenblatt Artikel-Nr. 56.200.0010 10 Aufreinigungen 56.200.0050 50 Aufreinigungen 56.200.0250 250 Aufreinigungen (Nur für die Forschung) Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und
Datenblatt Artikel-Nr. 56.200.0010 10 Aufreinigungen 56.200.0050 50 Aufreinigungen 56.200.0250 250 Aufreinigungen (Nur für die Forschung) Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und
Biotechnologie Forscher TM. Genes in a Bottle Kit DNA Necklace Module
 Biotechnologie Forscher TM Genes in a Bottle Kit DNA Necklace Module Bestellnummer 166 2200 EDU für 18 Schüler Bestellen Sie 2 Module für 36 Schüler Nur für den Schulgebrauch. 1 Gene in der Flasche Isolieren
Biotechnologie Forscher TM Genes in a Bottle Kit DNA Necklace Module Bestellnummer 166 2200 EDU für 18 Schüler Bestellen Sie 2 Module für 36 Schüler Nur für den Schulgebrauch. 1 Gene in der Flasche Isolieren
F-I Molekulare Zoologie: Teil I: Expressionsanalysen. Expressionsanalyse mittels RT-PCR
 F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
1 µl BamHI H 2 O 21 µl H 2 O 30 µl Volumen 18 µl H 2 O 30 µl Inkubation 2h @ 37 C 2h @ 37 C
 F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
3,58 g 0,136 g. ad 100 ml
 9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
Blut DNA Midi Kit. Datenblatt. (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen: Farbe: Bio&SELL
 Datenblatt Artikel-Nr. BS44.721.0010 Artikel-Nr. BS44.721.0050 Artikel-Nr. BS44.721.0250 10 Präparationen 50 Präparationen 250 Präparationen (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens
Datenblatt Artikel-Nr. BS44.721.0010 Artikel-Nr. BS44.721.0050 Artikel-Nr. BS44.721.0250 10 Präparationen 50 Präparationen 250 Präparationen (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens
Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie
 Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
ORIGINS-Project Laboratory Manuals. free educational use as long as unmodified. version_de. (c) the ORIGINS team
 ORIGINS-Project Laboratory Manuals free educational use as long as unmodified version_de (c) the ORIGINS team Restriktion von DNA Pipette (gelb, 20:200), Pipettenspitzen Eppendorfgefäße Gestell Eisbox
ORIGINS-Project Laboratory Manuals free educational use as long as unmodified version_de (c) the ORIGINS team Restriktion von DNA Pipette (gelb, 20:200), Pipettenspitzen Eppendorfgefäße Gestell Eisbox
Versuchsprotokoll Klonierung eines amplifizierten PCR-Fragments. 0 Inhaltsverzeichnis
 0 Inhaltsverzeichnis 0 Inhaltsverzeichnis...- 1-1 Einleitung...- 2-2 Versuch...- 2-2.1 Versuchsteil 4.2.3.-4.2.4. (PCR und Gel der cdna)...- 2-2.1.1 Einleitung...- 2-2.1.2 Durchführung...- 2-2.1.3 Auswertung...-
0 Inhaltsverzeichnis 0 Inhaltsverzeichnis...- 1-1 Einleitung...- 2-2 Versuch...- 2-2.1 Versuchsteil 4.2.3.-4.2.4. (PCR und Gel der cdna)...- 2-2.1.1 Einleitung...- 2-2.1.2 Durchführung...- 2-2.1.3 Auswertung...-
Johannes Gutenberg-Universität Mainz Fachbereich Biologie, Institut für Zoologie Leitung: Prof. Dr. Wolfrum Datum: 15. April 2005
 Johannes Gutenberg-Universität Mainz Fachbereich Biologie, Institut für Zoologie Leitung: Prof. Dr. Wolfrum Datum: 15. April 2005 F1 Molekulare Zoologie Teil II: Expressionsanalyse Proteinexpressionsanalyse
Johannes Gutenberg-Universität Mainz Fachbereich Biologie, Institut für Zoologie Leitung: Prof. Dr. Wolfrum Datum: 15. April 2005 F1 Molekulare Zoologie Teil II: Expressionsanalyse Proteinexpressionsanalyse
Pflanze direkt 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Transformation des Expressionsstammes
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Transformation des Expressionsstammes
SOP_018_Glucosebestimmung
 SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
Kurstage 7 und 8: Klassische Experimente der Gentechnologie
 Kurstage 7 und 8: Klassische Experimente der Gentechnologie Liga;on von DNA (Tag 7) Transforma;on von Bakterien (Tag 7) Auswertung der Transforma;on (Tag 8) Isolierung und Analyse von rekombinanter Plasmid
Kurstage 7 und 8: Klassische Experimente der Gentechnologie Liga;on von DNA (Tag 7) Transforma;on von Bakterien (Tag 7) Auswertung der Transforma;on (Tag 8) Isolierung und Analyse von rekombinanter Plasmid
Praktikum: Einleitung zu den technischen Geräten. Die automatische Pipette
 Die automatische Pipette Die Pipette ist wohl das wichtigste Werkzeug bei der Laborarbeit. Ständig müssen kleine bzw. kleinste Flüssigkeitsvolumina im ml- bzw. μl-bereich dosiert werden. Dabei sind die
Die automatische Pipette Die Pipette ist wohl das wichtigste Werkzeug bei der Laborarbeit. Ständig müssen kleine bzw. kleinste Flüssigkeitsvolumina im ml- bzw. μl-bereich dosiert werden. Dabei sind die
1 Aus dem Englischen übersetzt: Saps Photosynthese Kit
 Untersuchung der Photosynthese mit Algenbällen 1 Herstellung der Algenbälle: (Passend zur schriftlichen Beschreibung finden Sie die Arbeitsschritte auch in Bildern in der Datei (Herstellung von Algenbällen/Bilder)
Untersuchung der Photosynthese mit Algenbällen 1 Herstellung der Algenbälle: (Passend zur schriftlichen Beschreibung finden Sie die Arbeitsschritte auch in Bildern in der Datei (Herstellung von Algenbällen/Bilder)
UE Biochemie II: Flow Cytometry
 UE Biochemie II: Flow Cytometry Lerninhalt: Grundlagen der Durchflußzytometrie: Forward Scatter, Side Scatter, Fluoreszenzintensität; FACS; Lymphozytenpräparation über Ficoll; Hintergrund: Siehe Vorlesung
UE Biochemie II: Flow Cytometry Lerninhalt: Grundlagen der Durchflußzytometrie: Forward Scatter, Side Scatter, Fluoreszenzintensität; FACS; Lymphozytenpräparation über Ficoll; Hintergrund: Siehe Vorlesung
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung
 V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
DNA Isolierung. Praktikum Dr. László Kredics
 Isolierung Praktikum Dr. László Kredics Aufgabe: Isolierung von Plasmid aus Bakterienzellen Plasmid : pbluescript Vektor, Gröβe: 2960 Bps 1. 1,5 ml Bakterienkultur in Eppendorf-Röhrchen pipettieren, 2
Isolierung Praktikum Dr. László Kredics Aufgabe: Isolierung von Plasmid aus Bakterienzellen Plasmid : pbluescript Vektor, Gröβe: 2960 Bps 1. 1,5 ml Bakterienkultur in Eppendorf-Röhrchen pipettieren, 2
SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen
 GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
Inhaltsverzeichnis. Polymerase Chain Reaction Theoretischer Hintergrund - 2 -
 Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Plasmid-Restriktionsverdau
 Schülerdossier Plasmid-Restriktionsverdau der selbst gezüchteten Bakterien 1 Zur Maturaarbeit 2006, Kantonsschule Trogen Autoren: Joel Bänziger und Susanne Widmer Zucht der Bakterien 1 Zucht der Bakterien
Schülerdossier Plasmid-Restriktionsverdau der selbst gezüchteten Bakterien 1 Zur Maturaarbeit 2006, Kantonsschule Trogen Autoren: Joel Bänziger und Susanne Widmer Zucht der Bakterien 1 Zucht der Bakterien
MPP Multiplex 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
SDS Polyacrylamidgelelektrophorese (SDS-PAGE) Mini-Gelträger nach Anleitung zusammenbauen. Saubere Handschuhe tragen!!!
 aktualisiert, 08.03.2011, Wera Roth1 SDS Polyacrylamidgelelektrophorese (SDS-PAGE) Anleitung für Minigele Mini-Gelträger nach Anleitung zusammenbauen. Saubere Handschuhe tragen!!! Glasscheiben ordentlich
aktualisiert, 08.03.2011, Wera Roth1 SDS Polyacrylamidgelelektrophorese (SDS-PAGE) Anleitung für Minigele Mini-Gelträger nach Anleitung zusammenbauen. Saubere Handschuhe tragen!!! Glasscheiben ordentlich
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
Biochemisches Praktikum 1 DNA-Analytik Praktischer Teil
 Biochemisches Praktikum 1 DNA-Analytik Praktischer Teil 2 Inhaltsverzeichnis Sicherheitshinweise DNA-Analytik 1 Arbeitshinweise DNA-Analytik 2 Gießen von Agarosegelen 3 Isolierung genomischer DNA 4 Isolierung
Biochemisches Praktikum 1 DNA-Analytik Praktischer Teil 2 Inhaltsverzeichnis Sicherheitshinweise DNA-Analytik 1 Arbeitshinweise DNA-Analytik 2 Gießen von Agarosegelen 3 Isolierung genomischer DNA 4 Isolierung
Facharbeit. Versuch einer Sphagnum-Klassifikation durch PCR
 Bernhard-Strigel-Gymnasium Kollegstufe Jahrgang:... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiatin:... Mohammed Graibei Facharbeit Versuch einer Sphagnum-Klassifikation durch PCR Abgegeben
Bernhard-Strigel-Gymnasium Kollegstufe Jahrgang:... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiatin:... Mohammed Graibei Facharbeit Versuch einer Sphagnum-Klassifikation durch PCR Abgegeben
Molekulargenetische Experimente IV: Plasmidpräparation
 Molekulargenetische Experimente IV: Plasmidpräparation Plasmide sind kleine, ringförmige DNA-Moleküle in Bakterien, die in der Lage sind, sich selbst mit Hilfe von Enzymen zu replizieren. Gene, die auf
Molekulargenetische Experimente IV: Plasmidpräparation Plasmide sind kleine, ringförmige DNA-Moleküle in Bakterien, die in der Lage sind, sich selbst mit Hilfe von Enzymen zu replizieren. Gene, die auf
Versuch einer Sphagnum-Klassifikation durch Sequenzierung
 Bernhard-Strigel-Gymnasium Kollegstufe /Jahrgang... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiatin:... Vlora Murseli Facharbeit Versuch einer Sphagnum-Klassifikation durch Sequenzierung Bewertung:
Bernhard-Strigel-Gymnasium Kollegstufe /Jahrgang... 2009/2011 Memmingen Leistungskurs:... Biologie Kollegiatin:... Vlora Murseli Facharbeit Versuch einer Sphagnum-Klassifikation durch Sequenzierung Bewertung:
Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA
 Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
Versuch 3. Elektrophorese
 Versuch 3 Elektrophorese Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Prof. Dr. Schäfer Wird benotet?: 1. Einleitung Ziel des ersten Versuches
Versuch 3 Elektrophorese Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Prof. Dr. Schäfer Wird benotet?: 1. Einleitung Ziel des ersten Versuches
Insectomed SF express: Hinweise zur z. len. Information der Biochrom AG vom 05. Mai 2010
 Insectomed SF express: Hinweise zur z Adaption der Insektenzellen len Information der Biochrom AG vom 05. Mai 2010 Das neue serumfreie Insektenzellmedium Insectomed SF express der Biochrom AG eignet sich
Insectomed SF express: Hinweise zur z Adaption der Insektenzellen len Information der Biochrom AG vom 05. Mai 2010 Das neue serumfreie Insektenzellmedium Insectomed SF express der Biochrom AG eignet sich
Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013
 Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013 Projekt: Zellbiologie: Expression und Reinigung der onkogenen Kinase Abl an der Ecole Polytechnique Fédérale de Lausanne, EPFL
Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013 Projekt: Zellbiologie: Expression und Reinigung der onkogenen Kinase Abl an der Ecole Polytechnique Fédérale de Lausanne, EPFL
Mycoplasma gallisepticum
 BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR
 Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR Vorbereitung Lehrer Für jede Arbeitsgruppe werden 550 µl InstaGene-Matrix aliquotiert! Das Tube wird mit IG beschriftet!
Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR Vorbereitung Lehrer Für jede Arbeitsgruppe werden 550 µl InstaGene-Matrix aliquotiert! Das Tube wird mit IG beschriftet!
Gentechnologie: Klonierung und Transformation von DNA
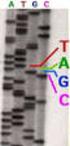 Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
Standardabweichung und Variationskoeffizient. Themen. Prinzip. Material TEAS Qualitätskontrolle, Standardabweichung, Variationskoeffizient.
 Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Inorganic Environmental Geochemistry (Anorganische Umweltgeochemie)
 Geographie Amalia Aventurin Inorganic Environmental Geochemistry (Anorganische Umweltgeochemie) Praktikumsbericht / -arbeit Praktikum Inorganic Environmental Geochemistry (Anorganische Umweltgeochemie)
Geographie Amalia Aventurin Inorganic Environmental Geochemistry (Anorganische Umweltgeochemie) Praktikumsbericht / -arbeit Praktikum Inorganic Environmental Geochemistry (Anorganische Umweltgeochemie)
CHEMIE-EXPERTEN IM EINSATZ
 CHEMIE-EXPERTEN IM EINSATZ Materialliste: Das Wirken des KLEBSTOFFS - Gummibärchen - Speisestärke - Topf - Wasser - Locher - Waage - Wäscheklammern - Verschiedene Gewichte - 28 Holzspatel - Tasse Versuch
CHEMIE-EXPERTEN IM EINSATZ Materialliste: Das Wirken des KLEBSTOFFS - Gummibärchen - Speisestärke - Topf - Wasser - Locher - Waage - Wäscheklammern - Verschiedene Gewichte - 28 Holzspatel - Tasse Versuch
Wettbewerbsbeitrag von Alexander Schmitt, 5a
 Wettbewerbsbeitrag von Alexander Schmitt, 5a Aufgabe 1 2008/09 Baue ein Raketenboot, das mit einer Brausetablette betankt wird. Versuche, möglichst einfachste Materialien zu verwenden, z.b. eine Filmdose.
Wettbewerbsbeitrag von Alexander Schmitt, 5a Aufgabe 1 2008/09 Baue ein Raketenboot, das mit einer Brausetablette betankt wird. Versuche, möglichst einfachste Materialien zu verwenden, z.b. eine Filmdose.
Borrelia burgdorferi s.l.
 BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Harnstoffspaltung durch Urease
 Martin Raiber Chemie Protokoll Nr.5 Harnstoffspaltung durch Urease Versuch 1: Materialien: Reagenzglasgestell, Reagenzgläser, Saugpipetten, 100 ml-becherglas mit Eiswasser, 100 ml-becherglas mit Wasser
Martin Raiber Chemie Protokoll Nr.5 Harnstoffspaltung durch Urease Versuch 1: Materialien: Reagenzglasgestell, Reagenzgläser, Saugpipetten, 100 ml-becherglas mit Eiswasser, 100 ml-becherglas mit Wasser
Seminarbericht Jugendakademie Mannheim
 Seminarbericht Jugendakademie Mannheim Stiftung Begabtenförderung der Stadt Mannheim Oberstufe 2014/2015 Seminarthema: Biotechnologisches Praktikum Ort: BASF Agrarzentrum Limburgerhof BASF Ludwigshafen
Seminarbericht Jugendakademie Mannheim Stiftung Begabtenförderung der Stadt Mannheim Oberstufe 2014/2015 Seminarthema: Biotechnologisches Praktikum Ort: BASF Agrarzentrum Limburgerhof BASF Ludwigshafen
GENSPIRALE- PRAKTIKUM 1
 GENSPIRALE- PRAKTIKUM 1 FRAGE- UND PROBLEMSTELLUNG In diesem Praktikum, das am Anfang von dreien Genspirale-Praktika steht, soll zuerst das gentechnische und sterile Arbeiten gelernt werden. Anschliessend
GENSPIRALE- PRAKTIKUM 1 FRAGE- UND PROBLEMSTELLUNG In diesem Praktikum, das am Anfang von dreien Genspirale-Praktika steht, soll zuerst das gentechnische und sterile Arbeiten gelernt werden. Anschliessend
Dünnschichtchromatografie (DC1) von Eiweißen (Aminosäure) Best.- Nr
 Dünnschichtchromatografie (DC1) von Eiweißen (Aminosäure) Best.- Nr. 201.3275 I P R O D U K T U M F A N G 1. Produktbeschreibung a) Dieser Versuch vertieft verschiedene bedeutsame Grundkenntnisse: - Das
Dünnschichtchromatografie (DC1) von Eiweißen (Aminosäure) Best.- Nr. 201.3275 I P R O D U K T U M F A N G 1. Produktbeschreibung a) Dieser Versuch vertieft verschiedene bedeutsame Grundkenntnisse: - Das
Fortbildung für Biologen an der Oranienschule
 Fortbildung für Biologen an der Oranienschule Am 28.01.08 fand die erste ganztägige schulinterne Lehrerfortbildung für Biologen an der Oranienschule unter der Leitung von Frau Dr. Wismar und Herrn Bender
Fortbildung für Biologen an der Oranienschule Am 28.01.08 fand die erste ganztägige schulinterne Lehrerfortbildung für Biologen an der Oranienschule unter der Leitung von Frau Dr. Wismar und Herrn Bender
GVO-Screening Kit. Nachweis von gentechnischen Veränderungen mittels Polymerasekettenreaktion (PCR)
 GVO-Screening Kit Nachweis von gentechnischen Veränderungen mittels Polymerasekettenreaktion (PCR) I. Einführung Die Gentechnik stellt die Landwirtschaft vor neue Herausforderungen. Einerseits eröffnet
GVO-Screening Kit Nachweis von gentechnischen Veränderungen mittels Polymerasekettenreaktion (PCR) I. Einführung Die Gentechnik stellt die Landwirtschaft vor neue Herausforderungen. Einerseits eröffnet
Robin Martin. Elektrophorese. von Nucleinsäuren
 Robin Martin Elektrophorese von Nucleinsäuren Abkürzungen 11 Vorwort 13 Danksagung 15 I. Grundprinzipien und Methoden 1. Einleitung: Verschiedene Arten und Formen von Nucleinsäure 19 1.1 Überblick 19
Robin Martin Elektrophorese von Nucleinsäuren Abkürzungen 11 Vorwort 13 Danksagung 15 I. Grundprinzipien und Methoden 1. Einleitung: Verschiedene Arten und Formen von Nucleinsäure 19 1.1 Überblick 19
Biochemie und. chemischer Mechanismus
 Dissertation zur Erlangung des Doktorgrades der Fakultät für Chemie und Pharmazie der Ludwig-Maximilians-Universität München Biochemie und chemischer Mechanismus der Thiomethylierung von RNA Dorothea Maria
Dissertation zur Erlangung des Doktorgrades der Fakultät für Chemie und Pharmazie der Ludwig-Maximilians-Universität München Biochemie und chemischer Mechanismus der Thiomethylierung von RNA Dorothea Maria
SingleQuant Assay Kit
 GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
en zum sicheren Einfrieren und Auftauen von Zellkulturen in TPP-Kryoröhrchen
 Empfehlung mpfehlungen en zum sicheren Einfrieren und Auftauen von Zellkulturen in TPP-Kryoröhrchen Information der Biochrom AG vom 23. Mai 2011 Zellkulturen können durch Kryokonservierung nahezu unbegrenzt
Empfehlung mpfehlungen en zum sicheren Einfrieren und Auftauen von Zellkulturen in TPP-Kryoröhrchen Information der Biochrom AG vom 23. Mai 2011 Zellkulturen können durch Kryokonservierung nahezu unbegrenzt
Nachweis von DNA im Wein
 Abschlussbericht über den Forschungsauftrag Nachweis von DNA im Wein Projektlaufzeit: 01.01.2001 bis 31.03.2003 Prof. Dr. Ralf Kaldenhoff Universität Würzburg Julius-von-Sachs-Institut für Biowissenschaften
Abschlussbericht über den Forschungsauftrag Nachweis von DNA im Wein Projektlaufzeit: 01.01.2001 bis 31.03.2003 Prof. Dr. Ralf Kaldenhoff Universität Würzburg Julius-von-Sachs-Institut für Biowissenschaften
DNA Isolierung. Praktikum Dr. László Kredics
 Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
1 Einleitung... 13. 1.1 Staphylokokken... 13. 1.2 Koagulase-negative Staphylokokken... 13. 1.4 MSCRAMM-Proteine... 16. 1.5 LPXTG-Motive...
 Inhaltsverzeichnis 1 Einleitung... 13 1.1 Staphylokokken... 13 1.2 Koagulase-negative Staphylokokken... 13 1.3 Staphylococcus saprophyticus... 14 1.4 MSCRAMM-Proteine... 16 1.5 LPXTG-Motive... 16 1.6 Oberflächenassoziierte
Inhaltsverzeichnis 1 Einleitung... 13 1.1 Staphylokokken... 13 1.2 Koagulase-negative Staphylokokken... 13 1.3 Staphylococcus saprophyticus... 14 1.4 MSCRAMM-Proteine... 16 1.5 LPXTG-Motive... 16 1.6 Oberflächenassoziierte
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Spezifische Drehung von gelöstem Rohrzucker - Rohrzuckerinversion
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 33 Spezifische Drehung von gelöstem Rohrzucker - Rohrzuckerinversion Aufgabe: 1. Bestimmen Sie den Drehwinkel für Rohrzucker für
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 33 Spezifische Drehung von gelöstem Rohrzucker - Rohrzuckerinversion Aufgabe: 1. Bestimmen Sie den Drehwinkel für Rohrzucker für
Experiment Isolierung, Aktivität und Hemmung der Carboanhydrase
 Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Vorbereitung: Materialien: 1 Kartoffel 1 Apfelausstecher 1 Messer 1 Lineal 3 Bechergläser 1 Spatel 1 Glasstab
 Salzwasser Vorbereitung: Materialien: 1 Kartoffel 1 Apfelausstecher 1 Messer 1 Lineal 3 Bechergläser 1 Spatel 1 Glasstab Chemikalien: Destilliertes Wasser Natriumchlorid Durchführung: Schritt 1: Es werden
Salzwasser Vorbereitung: Materialien: 1 Kartoffel 1 Apfelausstecher 1 Messer 1 Lineal 3 Bechergläser 1 Spatel 1 Glasstab Chemikalien: Destilliertes Wasser Natriumchlorid Durchführung: Schritt 1: Es werden
Drosophila melanogaster
 Modul biol113 Zellbiologie Drosophila melanogaster Komponenten der angeborenen Immunabwehr Experimente 1) RT (Reverse Transkriptase)-PCR zum Nachweis einer AMP- Expression nach Infektion 1.1 PCR-Reaktion
Modul biol113 Zellbiologie Drosophila melanogaster Komponenten der angeborenen Immunabwehr Experimente 1) RT (Reverse Transkriptase)-PCR zum Nachweis einer AMP- Expression nach Infektion 1.1 PCR-Reaktion
Arbeitsblatt 1 Teil 1
 Arbeitsblatt 1 Teil 1 Klonierung Schneiden und Religieren der DNA Bevor Sie anfangen, prüfen Sie ob alle Materialen vorhanden, bzw. eingeschaltet oder beschriftet sind: - Isolierende Styroporkiste mit
Arbeitsblatt 1 Teil 1 Klonierung Schneiden und Religieren der DNA Bevor Sie anfangen, prüfen Sie ob alle Materialen vorhanden, bzw. eingeschaltet oder beschriftet sind: - Isolierende Styroporkiste mit
GEBRAUCHSANLEITUNG. Glutatione Agarose Resin
 GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
AdnaTest ER/PR-Detect
 PCR-Expressionsanalyse der Östrogen- und Progesteron- Hormonrezeptoren in angereicherten Tumorzellen Zur In-vitro-Diagnostik Gebrauchsanweisung T-1-532 Inhaltsverzeichnis Bestellinformation... 3 Anwendungszweck...
PCR-Expressionsanalyse der Östrogen- und Progesteron- Hormonrezeptoren in angereicherten Tumorzellen Zur In-vitro-Diagnostik Gebrauchsanweisung T-1-532 Inhaltsverzeichnis Bestellinformation... 3 Anwendungszweck...
Photochemische Reaktion
 TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
8. Simultane UV/VIS-Zweikomponentenanalyse
 Simultane UV/VIS-Zweikomponentenanalyse 89 8. Simultane UV/VIS-Zweikomponentenanalyse Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb
Simultane UV/VIS-Zweikomponentenanalyse 89 8. Simultane UV/VIS-Zweikomponentenanalyse Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb
Protokoll Praktikum für Humanbiologie Studenten
 Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Martin Raiber Chemie Protokoll Nr Gruppe 2 (Schrankseite) Untersuchung von Glycin
 Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila
 Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein (1) Kolonie-PCR Polymerase
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein (1) Kolonie-PCR Polymerase
Chlamydia sp. BACTOTYPE PCR Amplification Kit. Gebrauchsanweisung. Labor Diagnostik Leipzig
 BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
HybriScan D Abwasser Gesamtkeimzahlbestimmung
 HybriScan D Abwasser Gesamtkeimzahlbestimmung Modul I Molekularbiologisches Schnelltestsystem zum Nachweis von Bakterien im Abwasser Produkt-Nr.: 78436 Kontaktinformationen: HybriScan - Schnelltestsystem
HybriScan D Abwasser Gesamtkeimzahlbestimmung Modul I Molekularbiologisches Schnelltestsystem zum Nachweis von Bakterien im Abwasser Produkt-Nr.: 78436 Kontaktinformationen: HybriScan - Schnelltestsystem
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
