Pflanzenphysiologie Praktikum Sommersemester 2017
|
|
|
- Edith Kalb
- vor 6 Jahren
- Abrufe
Transkript
1 Pflanzenphysiologie Praktikum Sommersemester 2017
2 Leitung: Dr. Jeannette Pfalz 1
3 Praktikum Pflanzenphysiologie Sommersemester 2017 Zum Pflanzenphysiologischen Praktikum im Sommersemester 2017 werden Ihnen 7 Praktikumskomplexe in vier Praktikumstagen vorgelegt. Anhand der verschiedenen Komplexe soll Ihnen eine Wiederholung des in der Vorlesung gebotenen Stoffes ermöglicht werden. Die Literaturangaben sollen Ihnen eine Vorbereitung auf die durchzuführenden Versuche ermöglichen. Eine Praktikumsanleitung, wie die Ihnen vorliegende, kann nicht die erforderlichen theoretischen Grundlagen liefern. Das Anliegen und die Versuchsdurchführung müssen Ihnen vor Beginn des Praktikums bekannt sein, da wir sonst Ihre Teilnahme nicht akzeptieren können. Einige Komplexe werden durch ein Gespräch mit einem zuständigen Tutor abgeschlossen. Während des Praktikums stehen Ihnen Betreuer zur Verfügung, deren Aufgabe auch darin besteht, Ihre Vorbereitung zu kontrollieren. Wir laden Sie ausdrücklich zu einem schöpferischen Umgang mit dem Praktikum ein: wenn Sie bestimmte Versuche im Rahmen der vorhandenen Möglichkeiten variieren wollen, so freuen wir uns darüber. Sprechen Sie das aber bitte mit uns ab. Das erste Praktikum beinhaltet die Komplexe 1 (Ernährung), 2 (Wachstum und Differenzierung) und 3 (Auxinwirkungen), das zweite Praktikum die Komplexe 4 (Phytohormone) und 5 (Pflanzeninhaltsstoffe), das dritte Praktikum den Komplex 6 (Enzyme) und das vierte Praktikum den Komplex 7 (Photosynthese und Respiration. Die Langzeitversuche werten Sie bitte in eigener Regie im Verlauf des Praktikums aus. Die Tutorien beziehen sich auf folgende Themen: Ernährung, Wachstum, Differenzierung (1. Praktikumstag), Phytohormone (2. Praktikumstag), Pflanzliche Enzyme und Enzymologie (3. Praktikumstag) und Photosynthese (4. Praktikumstag). Zu Beginn des Praktikums bitten wir einige Studenten, das Prinzip einiger Versuche zu erklären. Dies dient der Kontrolle der individuellen Vorbereitung. Jeder der drei Praktikumsdurchläufe umfasst 45 Unterrichtsstunden. In jeder zweiten Woche findet jeweils 18 Uhr s. t. ein Institutscolloquium statt. Dort werden Probleme der Forschung dargestellt, die sich auf die Arbeiten unseres Institutes beziehen. Wir laden Sie zur Teilnahme herzlich ein. Die Arbeit im Praktikum wird in Arbeitsgruppen aus jeweils 3 Studenten durchgeführt. Jede Gruppe erstellt ein Praktikumsprotokoll. Die Praktikumsprotokolle sind die Grundlage für die Bestätigung der erfolgreichen Teilnahme am Praktikum. Teile des Praktikums werden betreut von Dr. Jeannette Pfalz (Pflanzenphysiologie Jena). Viel Erfolg und Spaß Dr. Jeannette Pfalz; jeannette.pfalz@uni-jena.de 2
4 INHALTSVERZEICHNIS Seite Allgemeine Literatur:....4 Komplex 1: Ernährung von Pflanzen Biomonitoring Ernährung heterotropher Pflanzenorgane: Kultur isolierter Wurzeln in künstlicher Nährlösung. 8 Komplex 2: Wachstum und Differenzierung Verteilungsfunktion einer Population von Keimlingen Die Wirkung eines Herbizids - SAN 9789 (Norflurazon)...12 Komplex 3: Multiple Auxinwirkungen Untersuchungen an Coleussprossen Induktion des Streckungswachstums von Maiskoleoptilsegmenten durch Auxin Selektive Herbizidwirkung..16 Komplex 4: Wirkungen weiterer Phytohormone und das Phytochromsystem Zwergmutanten der Erbse und ihre Normalisierung durch Gibberellinsäure Einfluss von Abscisinsäure auf die Samenkeimung Ein klassisches Experiment zur Phytochromwirkung Komplex 5: Pflanzliche Inhaltsstoffe Quantitative Bestimmung von Gesamtproteinen Ein Vorversuch zur pflanzlichen Molekularbiologie: Isolierung von DNA Fett-Kohlenhydratumwandlung bei der Keimung fetthaltiger Samen Isolierung und Nachweis der Alkaloide des Schöllkrauts..28 Komplex 6: Pflanzliche Enzyme Operationale Kriterien der Enzymaktivitätsbestimmung - Fallstudie Fumarathydratase Die kinetische Charakterisierung eines Enzyms - Fallstudie Peroxidase Konkurrenz um Phosphat - die Wirkung von Phosphatasen Dissimilation von Speicherstärke durch Amylasen.35 Komplex 7: Photosynthese und Respiration Vergleich der Pigmente aus Chloroplasten und Chromoplasten Fluoreszenz von Chlorophyll in vitro und in vivo CO 2-Aufnahme bei C3- und C4-Pflanzen Demonstration & Messung des photosynthetischen Elektronentransports an isolierten Chloroplasten 41 Methodenanhang..39 Hydrokulturen von Pflanzen.. 42 Quantitative Bestimmung der Plastidenpigmente..43 Proteinbestimmung.44 Bestimmung von Kohlenhydraten 45 Anthocyane..46 Probit- und t-tabellen..44 Liste der im Pflanzenphysiologischen Praktikum verwendeten Pflanzen 45 3
5 Allgemeine Literatur: BUCHANAN/ GRUISSEM/ JONES. Biochemistry and Molecular Biology of Plants. Rockville, Maryland, USA KUTSCHERA, U.: Prinzipien der Pflanzenphysiologie. Spektrum Akademischer Verlag KUTSCHERA, U.: Grundpraktikum zur Pflanzenphysiologie. Quelle & Meyer, Wiesbaden METZNER, H.: Pflanzenphysiologische Experimente. Fischer, Jena WEILER, E, NOVER, L., NULTSCH, W: Allgemeine und molekulare Botanik. Thieme, Stuttgart SCHOPFER, P.: Experimentelle Pflanzenphysiologie. Einführung in die Methoden. Band I. Springer- Verlag, Berlin SCHOPFER, P.: Experimentelle Pflanzenphysiologie. Einführung in die Anwendung. Band II. Springer-Verlag, Berlin SCHOPFER, P und BRENNICKE, A: Pflanzenphysiologie. 7. Auflage, Spektrum, STRASBURGER. Lehrbuch der Botanik. A. Bresinsky, C. Körner, J.W. Kadereit, G. Neuhaus, U. Sonnewald. Spektrum Akademischer Verlag, TAIZ, L. und E. ZEIGER: Plant Physiology. Palgrave Macmillian, USA. 5th edition (Besonders empfohlen für das Gesamtgebiet: 1-3 ) 4
6 Komplex 1 Ernährung von Pflanzen 1.1 Biomonitoring Literatur: Schopfer/ Brennicke; Kutschera 1. Kurstag Dieser Versuch hat über die mineralische Ernährung hinausgehende Bedeutung. Die Versuchspflanzen (Wasserlinsengewächse = Lemnaceae, besonders Lemna minor) werden als Biotestsysteme zur Routineüberprüfung von Wasserqualität eingesetzt. und (23/03/2011) Materialien & Geräte: - Beschriftete Pipetten - Beschriftete Standzylinder 500 ml, 100 ml - Erlenmeyerkolben (100 ml) - Beschriftungsband - Wattestopfen - Glasstäbe, Impfösen, Wägeschälchen - Sterile Vorkultur von Wasserlinsen, z.b. Spirodela polyrhiza - ph-messgerät - Bunsenbrenner, Streichhölzer Chemikalien & Lösungen: - Glucose - Stammlösungen und Ersatzlösungen (vgl. Tabelle Pipettierschema im Text) Durchführung Es hat sich als günstig erwiesen, wenn Sie als Gruppen kooperieren, indem Sie gleich die doppelte Menge an Vollmedien herstellen. Bitte legen Sie ca. 450 ml Reinstwasser in einen Plastikzylinder vor und pipettieren Sie in der angegebenen Reihenfolge. Die Konzentration an Glucose soll 50 mm betragen (Festsubstanz einwiegen). Nach Zugabe der Komponenten zur Nährlösung (siehe Tabelle) mit einem Glasstab umrühren, am Schluss auf 500 ml auffüllen. Überführen Sie von jedem Ansatz 4 x 75 ml in 100 ml Erlenmeyerkolben. Der ph-wert muss vor dem Autoklavieren gemessen werden. Wegen der zugesetzten Glucose müssen die Erlenmeyerkolben autoklaviert werden. Diese Arbeit muss zu Praktikumsbeginn ausgeführt werden, damit unter Sterilbedingungen am gleichen Tag noch jeweils ein Triplett von Spirodela polyrhiza eingeimpft werden kann. Die Pflanzen werden bis zum letzten Praktikumstag kultiviert. Dazu wird das Fensterbrett im Praktikumsraum genutzt. Zum Ansetzen des Versuches: Überimpfen Sie 3 5 Sprosse in einen Kolben. Die Anzahl der Sprosse muss nach dem Überimpfen genau bestimmt werden, da es meist nur schwer möglich ist, genau eine Kolonie aus einem Triplett einzuimpfen (Was ist ein Lemnaceen-Spross?). 5
7 Stammlösungen 1. Kurstag Tabelle: Pipettierschema für die Medienvarianten (Angaben ml/ 500 ml): Voll-medium Mangelvarianten -N -P -S -K -Mg -Fe -Ca KH2PO4 (100 mm) 2,5 2,5-2,5-2,5 2,5 2,5 Ca(NO3)2 (0,2 M) 2,5-2,5 2,5 2,5 2,5 2,5 - KNO3 (1,6 M) 2,5-2,5 2,5-2,5 2,5 2,5 MgSO4 (0,2 M) 2,5 2,5 2,5-2,5-2,5 2,5 H3BO3 (1 mm); 2,5 2,5 2,5 2,5 2,5 2,5 2,5 2,5 MnCl2 (2,6 mm); Na2MoO4 (80 μm) Fe (III) EDTA (5 mm) 2,5 2,5 2,5 2,5 2,5 2,5-2,5 Ersatzlösungen KCl (1,6 M) - x x CaCl2 (0,2 M) - x MgCl2 (1 M) - x NaH2PO4 (0,15 M) - x NaNO3 (1 M) - x x Na2SO4 (0,2 M) - x Na2EDTA (5 mm) - x Die in den Mangelvarianten fehlenden Gegenionen müssen durch die Ersatzlösungen in Form von Cl - oder Na + äquimolar ersetzt werden. Bitte machen Sie sich zur Berechnung kundig und berechnen Sie die mit Fragezeichen markierten Stellen für Ihre Ansätze v o r Beginn des Praktikums. Tabelle: Eine Vorgabe zur Aufteilung auf die Gruppen: Gruppe Vollmedium -N -P -S -K -Mg -Fe -Ca 1 x x 3 x x 5 x x 7 x x 9 x x 11 x x 13 x x Zur Auswertung im Verlaufe des Praktikums: Bitte beobachten Sie die Entwicklung Ihrer Pflanzen. In jeder Praktikumswoche müssen die Sprosszahlen bestimmt werden (solange die Zahl nicht so hoch wird, dass eine Zählung im geschlossenen Kolben nicht mehr möglich ist) und das Erscheinungsbild der Pflanzen beurteilt werden. Ähnlich umfassende Begutachtungen finden in der Pflanzenzüchtung statt und werden gewöhnlich als Bonitierung (lat. bonitas = gute Beschaffenheit, Güte), damit meint man eine visuelle Begutachtung, bezeichnet. Zur Auswertung am letzten Praktikumstag: Es sind erneut der ph-wert, letztmalig die Sprosszahl pro Kolben (zum Auszählen können große 6
8 1. Kurstag Petrischalen verwendet werden) sowie zum Abschluss das Frischgewicht zu messen. Sollten sich Turionen gebildet haben, so ist deren Zahl zu bestimmen. Ebenfalls soll eine Bonitierung stattfinden, wobei besonders der Chlorophyllgehalt (wie grün sind die Pflanzen?) und der Anthocyangehalt (wie rot sind die Pflanzen?) zu berücksichtigen sind. Biochemische Verfahren wie Protein-, Enzym- oder Pigmentbestimmung (Chlorophyll- und Anthocyangehalt; siehe Methodenanhang) könnten beim Biomonitoring folgen, sprengen aber den Rahmen eines Grundpraktikums. Zur schriftlichen Auswertung: Alle numerischen Daten (Sprosszahlen, Frischgewichte) sowie die Bonitierungsergebnisse sind anzugeben (Originaldaten). Zur Berechnung der Wachstumsraten werden die Ausgangszahlen und die Zahlen nach 3 Wochen Kultivierung verwendet. Mittelwerte und Standardabweichungen sind zu berechnen. Aus den Sprosszahlen (Z1, Z2) über die Zeit (t1, t2) werden die Wachstumsraten (WR) und die Verdoppelungszeit (Td) nach folgenden Formeln berechnet: WR= (lnz2 lnz1)/(t2 - t1). Td = ln2/ WR (Dimension beträgt Tage, falls t1 und t2 in Tagen verwendet wurden). Mittels t-test ist zu entscheiden, ob die Mangelvarianten signifikant von den Kontrollen verschieden sind. Verwenden Sie dazu die Wachstumsraten und nicht die Sprosszahlen. Warum ist diese Entscheidung wichtig? 7
9 1. Kurstag 1.2 Ernährung heterotropher Pflanzenorgane: Kultur isolierter Wurzeln in künstlicher Nährlösung Literatur: Schopfer/ Brennicke;.Schopfer I; Schopfer II. Materialien & Geräte: - Beschriftete Standzylinder - Erlenmeyerkolben (100 ml-weithals) - Große Petrischalen werden zusammen mit der Nährlösung im Praktikum autoklaviert - Wattestopfen - Glasstab, Impföse, Skalpell, Millimeterpapier in Plastikfolie - Axenisch vorkultivierte Wurzeln von Tomate - Klebeband und Marker ( Edding ) - Laminarbox - Autoklav (mit Prof. M. Mittag absprechen) - Trichter für Standzylinder Chemikalien & Lösungen: - Bäckerhefe oder Hefeextrakt - Die Hefesuspension wird im Praktikum filtriert und anschließend mit Wasser aufgefüllt - Stammlösungen (s. u.) - Von den Lösungen I - IX werden jeweils 500 ml hergestellt - Für alle Arbeiten wird de-mineralisiertes Wasser verwendet. Stammlösungen für die verschiedenen Nährlösungen nach White: Lösung I: MgSO4 (30 mm) Lösung II: Ca(NO3) 2 (12 mm) Na2SO4 (14 mm) KNO3 (8 mm) KCl (9 mm) NaH2PO4 (1,2 mm) Lösung III: Fe2(SO4)3 (60 μm) Lösung IV: MnSO4 (0,3 mm) ZnSO4 (94 μm) H3BO4 (0,24 mm) KI (45 μm) Lösung V: Saccharose (0,6 M) Lösung VI: Nicotinsäure (40 μm) Lösung VII: Pyridoxin (4,9 μm) Lösung VIII: Thiamin (3 μm) Lösung IX: Hefeextrakt (100 mg 100 ml -1 ). Wird im Praktikum hergestellt Durchführung 1. Ansetzen der Nährlösungen Ansatz 1 Ansatz 8: Jeweils 25 ml der Stammlösungen werden nach folgendem Plan vereinigt und auf 250 ml aufgefüllt (um Ausfällungen zu vermeiden, etwas Wasser vorlegen und Lösung I und II als letztes zugeben). Gut mischen! 8
10 1. Kurstag Ansatz 1 (nur anorganische Komponenten): Ansatz 2 (mit Saccharose, ohne Vitamine): Ansatz 3 (ohne Thiamin): Ansatz 4 (ohne Pyridoxin): Ansatz 5 (ohne Nicotinsäure): Ansatz 6 (Hefe statt Vitaminzusatz): Ansatz 7 (Vollmedium): Ansatz 8 (ohne anorganische Komponenten): Lösung I - IV Lösung I - V Lösung I VII Lösung I VI, VIII Lösung I - V, VII - VIII Lösung I - V, IX Lösung I IX Lösung V - IX Tabelle: Eine Vorgabe zur Aufteilung auf die Gruppen: Gruppe A 1 A 2 A 3 A 4 A 5 A 6 A 7 A 8 2 x x 4 x x 6 x x 8 x x 10 x x 12 x x 2. Herstellen der Kulturansätze: Pro Ansatz werden 3 Erlenmeyerkolben (100 ml) mit ca. 50 ml Medium gefüllt, mit einem Zellstoffstopfen verschlossen und autoklaviert. Unter sterilen Bedingungen werden 2 genau 1 cm lange Wurzeln pro Kolben übertragen. Unter die große Petrischale wird Millimeterpapier gelegt, um 1 cm-segmente mit dem Skalpell abschneiden zu können. Die Wurzelspitzen sind entweder vorher zu entfernen oder (bei ausreichendem Material) ausschließlich zu verwenden. Die Kultivierung über 3 Wochen erfolgt bei Raumtemperatur, die Lichtbedingungen sind unerheblich. Von 5 Wurzelsegmenten ist am Tag des Versuchsstartes das Frischgewicht zu bestimmen. Danach sind diese Wurzelsegmente insteril und können nicht mehr weiterverwendet werden. Auswertung Die Entwicklung der Wurzeln in den einzelnen Ansätzen wird wöchentlich registriert. Unsterile Kulturen werden aussortiert. Die Wurzelentwicklung wird wie folgt im Bezug zum Inoculum (vgl. dazu Ansatz 1) registriert: (A) nicht gewachsen (B) leicht gewachsen (C) stark gewachsen (D) stark gewachsen, Seitenwurzeln ausgeprägt. Nach drei Wochen Entwicklungszeit, d.h. am Ende des Praktikums, erfolgt eine 1. genaue Längenbestimmung aller Wurzeln in den 3 Proben und 2. Frischgewichtsbestimmung der Wurzeln (die 3 Proben einer Variante werden zuvor vereint) zur Quantifizierung der Biomassezunahme. Eine Bestimmung der Trockenmasse wäre eigentlich sinnvoll, lässt sich aber aus Zeitgründen im Praktikum nicht ausführen. Die Wurzellängen werden zu Mittelwerten und Standardabweichung verrechnet und der (einseitige, ungepaarte) t-test ist zum Vergleich der Variante mit den Kontrollen 1 (nur anorganische 9
11 1. Kurstag Komponenten) und den Kontrollen 2 (Vollmedium) einzusetzen. Vergleichen Sie Ihre Ergebnisse auch dann mit den Ansätzen 1 und 7, wenn Sie diese Ansätze nicht selbst untersucht haben. Treten Sie in kollegialen Kontakt mit einer geeigneten Gruppe, zitieren Sie aber die Herkunft der Daten im Protokoll. Arbeitszeit: 1. Teil: 40 Minuten; 2. Teil: Minuten 10
12 1. Kurstag Komplex 2: Wachstum und Differenzierung 2.1 Verteilungsfunktion einer Population von Keimlingen Literatur: Schopfer I, Schopfer II, Kutschera Der Versuch hat das Anliegen, Ihnen einen praktischen Zugang zum Kapitel Biostatistik zu ermöglichen. Bei der Protokollführung sollen Sie diese Methoden anwenden. Materialien & Geräte: - Maßstab (15 x 15 cm großes Millimeterpapier, mit Plastikfolie geschützt) - Pinzetten, - Probit-Tabelle (Anhang) - etiolierte und grüne Keimpflanzen von Raps oder Senf (je 140 Stück auf Filterpapier und Reinstwasser in großen Petrischalen im Dunkeln bzw. in Dauerweißlicht für ca. 5 d bei 25 C vorkultiviert) Chemikalien & Lösungen: keine Durchführung Die Keimlinge werden vorsichtig vom Keimpapier abgenommen und die Länge des Hypokotyls (Wurzelansatz bis Gabelung der Kotyledonen-Petioli) auf 0,5 mm genau (!) von 140 zufällig ausgewählten Keimlingen gemessen. Man hält dazu den Keimling mit einer Hand an der Wurzel auf der Messplatte fest, greift die Kotyledonen mit einer Pinzette und zieht den Hypokotylhaken gerade (ohne ihn abzubrechen). Die Messwerte x werden in eine Tabelle eingetragen. Jede Gruppe sollte entweder etiolierte oder grüne Keimlinge ausmessen. Zwei Gruppen sollen dann die Daten austauschen, damit ein Vergleich möglich ist. Die Partnergruppe ist im Protokoll anzugeben. Auswertung (siehe Schopfer I, Schopfer II) 1. Prüfen Sie zunächst mittels Probit-Transformation die Normalverteilung. Dazu müssen die Hypokotyllängen in Klassen eingeteilt werden. Mehr als 10 Klassen haben sich als nicht sinnvoll erwiesen. Beide Stichproben sollten in die gleiche Zahl von Klassen eingeteilt werden. Stellen Sie die Verteilung und die Summenverteilung (absolut und relativ) graphisch dar. Die Summenverteilung wird dann mittels einer Tabelle in einen Probitmaßstab umgerechnet und ebenfalls graphisch dargestellt. Daraus lässt sich auf die Normalverteilung schließen. 2. Berechnen Sie die Mittelwerte und die Standardabweichung und vergleichen Sie von zwei verschiedenen Kulturen die Mittelwerte der Hypokotyllängen durch den t-test. Arbeitszeit: 1 Stunde 11
13 1. Kurstag 2.2 Die Wirkung eines Herbizids - SAN 9789 (Norflurazon) Literatur: Schopfer II; Kutschera; Schopfer/Brennicke (dort weitere Hinweise) Materialien & Geräte: - Erlenmeyerkolben (100 ml), 2 Stück pro Gruppe - Wattestopfen - Impföse, Messzylinder für 50 ml - Etwa 14 d alte autotroph vorkultivierte Sprosse von z. B. Lemna minor oder eine andere Spezies. Chemikalien & Lösungen: - Autotrophe Nährlösung (siehe Methodenanhang) mit und ohne Norflurazon (10 µm; Molekulargewicht 269,1 g mol -1 ) Durchführung Zehn Sprosse werden mit einer Impföse unter insterilen Bedingungen (d. h. direkt am Arbeitstisch) in die Nährlösungen mit und ohne Norflurazon überführt (25 ml in 100 ml-kolben). Die Kultur wird im Tageslicht weiterkultiviert. Der Versuch ist nach einer Woche abzubrechen und auszuwerten. Eine Erweiterung des Versuches mit verringerter Hemmstoffkonzentration oder veränderter Lichtintensität (z.b. Abdunkeln mit Alu-Folie) ist leicht möglich und wird deshalb empfohlen. Die Norflurazonabfälle werden gesondert gesammelt und entsorgt. Auswertung Die Beschaffenheit der Sprosse (grün bzw. ausgebleicht) und ihre genaue Zahl ist nach einer Woche zu bestimmen und auf die Ausgangszahlen zu beziehen. Interpretation der beobachteten Ergebnisse mit Literaturhilfe (vgl. Schopfer/Brennicke). Arbeitszeit: 20 Minuten plus Auszählen nach einer Woche 12
14 1. Kurstag Komplex 3: Multiple Auxinwirkungen 3.1 Untersuchungen an Coleussprossen - Krümmung der Sprossachse, Verhinderung des Blattabfalls und Bildung von Adventivwurzeln Literatur: Schopfer II; Schopfer/ Brennicke. Für das Thema Phytohormone ist zurzeit das entsprechende Kapitel in Taiz/Zeiger (5. Auflage 2010) unübertroffen. Materialien & Geräte: - 3 Coleus-Pflanzen pro Gruppe - Schere - Spatel oder Streichhölzer - Beschriftungsband Chemikalien & Lösungen: Auxin- und Wasserpaste: Die Pasten werden im Mörser durch inniges Vermischen gleicher Teile von (wasserfreiem) Wollfett und Wasser bzw. wässriger Auxinlösung hergestellt. Lösungen bzw. Suspensionen 0,5 % IAA werden unter Vermittlung von wenigen Tropfen Ethanol bereitet. Durchführung Teil 1: Induktion von Adventivwurzeln Um junge und ältere Internodien einer Pflanze von Coleus wird Auxinpaste gestrichen, als Kontrolle dient Wasserpaste. Nach 3 Wochen wird der Versuch ausgewertet. Wenn Interesse besteht, so kann auch eine mikroskopische Analyse der Adventivwurzelbildung (Sprossquerschnitt) erfolgen. Teil 2: Auxin-induzierte Streckungsbewegung der Sprossachse An jüngeren Sprossachsenabschnitten gut gegossener Coleus-Pflanzen wird Auxinpaste einseitig aufgetragen. Kontrolle der sehr feucht, hell und warm zu haltenden Pflanzen (Kulturenraum) möglichst nach zwei Tagen (in Absprache mit dem Versuchsbetreuer) und nach einer Woche. Teil 3: Verhinderung der Abszission von Blättern durch Auxin An einer Coleus-Pflanze werden die Blätter wie folgt behandelt: a) Abtrennen der Blattspreite (Positivkontrolle) b) Abschneiden von 4/5 der Blattspreite (Negativkontrolle) c) Abschneiden der Blattspreite, Auftragen von Auxinpaste auf die Schnittfläche des Blattstieles (experimentelle Probe). Kontrolle erfolgt nach einer Woche. Auswertung (Bitte aber nicht ins Protokoll) 1. Welche Beziehung könnte zwischen Auxinwirkung und Phototropismus bestehen? 2. Diskutieren Sie die Wechselwirkung von Auxin und Ethylen beim Blattabfall! 13
15 1. Kurstag 3.2 Induktion des Streckungswachstums von Maiskoleoptilsegmenten durch Auxin Literatur: Kutschera Materialien & Geräte: - 8 Schalen etiolierte Maiskeimlinge 5 d bei 28 C auf feuchtem Filterpapier im Dunkeln angezogen (Die Keimlinge sollten zusätzlich 12 h vor Verwendung für 10 min mit Weißlicht bestrahlt werden, da dann die Koleoptile besser ausgebildet werden) - etwa 1 mm stumpfer Metallstift zur Entfernung des Primärblattes aus den Segmenten - Koleoptil-Schneidegerät (2 parallel im Abstand von 10 mm befestigte Rasierklingen) - Inkubationsapparatur mit elektrischer Pumpe. - Becherglas mit Wasser, Messpapier Chemikalien & Lösungen: - IAA-Stammlösung (1 mm) ist schon fertig. (Herstellung: 0,1 M Indolylessigsäure in 0,5 ml Ethanol vorlösen und auf 100 ml mit Aqua demin. auffüllen (kühl und dunkel etwa 1 Woche haltbar).) - Daraus Verdünnungen (= IAA-Testlösungen) 0,1 mm, 0,01 mm und 0,001 mm IAA herstellen. - Phosphatpuffer (5 mm) mit ph 3,0, 5,0 und 7,0; je 250 ml. Durchführung Aus geraden, etwa 25 mm langen Koleoptilen werden 30 Segmente von 10 mm Länge etwa 3 mm unter der Spitze herausgeschnitten und das darin befindliche Primärblatt vorsichtig herausgestoßen. Segmente in einem Becherglas mit Wasser sammeln. Je 10 Segmente fugenfrei auf die Nadel einer Messapparatur aufreihen und in demin. Wasser bei Raumtemperatur und kräftiger Belüftung aufbewahren. Nach 30 min (gerechnet ab Schneiden der Segmente) werden die Ansätze in 2 vorbereitete Reagenzröhrchen mit den IAA-Testlösungen umgesetzt. Die Längenmessung erfolgt zum Zeitpunkt t = 0 und dann über 3 h in 30 min-abständen. Die Nadel mit den Segmenten muss kurz herausgenommen und an ein Lineal angelegt werden (es ist darauf zu achten, dass zwischen den Segmenten während der Messung keine Fugen auftreten und die Segmente nicht überlappen). Jede Gruppe sollte 3 Varianten untersuchen: 1. Wasserkontrolle (Leitungswasser) 2. verdünntes Auxin 0,1 mm oder 0,01 mm 3. Eine in Absprache mit dem Versuchsbetreuer zu variierende Probe (siehe Varianten) Varianten: 1. Vergleich zweier IAA-Konzentrationen, also zusätzlich 0,001 mm 2. IAA-Konzentration (0,01 mm), jedoch nach einer Stunde Messung die IAA-Lösung durch Leitungswasser ersetzen und das Wachstum weiter verfolgen 3. Keine Auxinlösung verwenden, sondern Puffer mit den ph-werten 3,0, 5,0 oder 7,0. Bei Wunsch können auch nur diese Pufferlösungen miteinander verglichen werden. Auswertung Es ist der Wachstumsanstieg in Abhängigkeit von der IAA-Konzentration zu ermitteln (grafische Darstellung). Dazu muss darauf geachtet werden, dass die Messpunkte einen linearen Anstieg über 14
16 1. Kurstag die Zeit nehmen. Fragen zu Ihrer Vorbereitung (nicht für das Protokoll): 1. Was versteht man unter der Säure-Wachstumshypothese? 2. Warum dürfen die Koleoptile nicht zu alt sein? Arbeitszeit: 50 Minuten plus Messung aller 30 Minuten über 3 Stunden 15
17 1. Kurstag 3.3 Selektive Herbizidwirkung Literatur: Kutschera; R. Wejnar et al. (1994) Der Einfluss des selektiven Herbizids 2,4-Dichlorphenoxyessigsäure auf Wachstum und Pigmentbildung bei mixo-, auto- und heterotroph kultivierten Lemna gibba-pflanzen. Angew. Bot. 68, Materialien & Geräte: 1. Je Gruppe 4-5 mit Komposterde gefüllte Blumentöpfe; Karyopsen von Getreide (Avena, Triticum) und Samen von Sinapis oder Kresse gemischt gesät (nicht zu dicht) und etwa 14 Tage im Gewächshaus vorkultiviert 2. Erlenmeyerkolben (100 ml), Impföse, Messzylinder (für 50 ml) 3. Sprühflaschen 4. große Plastikschale für jede Variante Chemikalien & Lösungen: 1. 0,05 %ige 2,4-Dichlorphenoxyessigsäure-Lösung (wässrig) und 0,05 %ige IAA-Lösung zum Besprühen Wichtiger Hinweis: Die verwendeten Getreidearten und Lemnaceen gehören zu den Liliopsida, Senf und Kresse zu den Rosopsida. Durchführung Besprühen je eines Blumentopfes mit (i) dem Herbizid 2,4-D bzw. (ii) dem natürlichen Auxin IAA. (iii) Kontrolle: Besprühen mit Wasser. Vorsicht beim Besprühen mit Herbizidlösung, damit andere Pflanzen (und Menschen) nicht kontaminiert werden. Das Herbizid wird im Abzug versprüht. Variationsmöglichkeit: 0,005 % oder 0,0005 % IAA. Zusatzversuch: Mit 10 ml 0,05 % 2,4-D-Lösung gießen. Wie verhält es sich hierbei mit der Selektivität des Herbizides? Arbeitszeit: 30 Minuten plus Auswertung nach einer Woche 16
18 2. Kurstag Komplex 4: Wirkungen weiterer Phytohormone und das Phytochromsystem Noch einmal: Für das Thema Phytohormone ist zurzeit das entsprechende Kapitel in Taiz/ Zeiger (5. Auflage) unübertroffen. 4.1 Zwergmutanten der Erbse und ihre Normalisierung durch Gibberellinsäure Literatur: Kutschera Materialien & Geräte: Keimlinge von Pisum sativum Zwerg-Markerbsen z.b. Sorte Bördi, 2 Wochen im Gewächshaus vorkultiviert; Pro Gruppe 4 Töpfe mit jeweils mindestens 10 Pflanzen Plastikpipetten, Sprühflaschen Chemikalien & Lösungen: - Gibberellinsäure-Lösung (2 mm). - Für Teil 1: Vor Gebrauch die Stammlösung auf 0,2 mm verdünnen, - Für Teil 2: 1 mm, 0,1 mm, 0,01 mm, mit einer 0,1%igen Tween 20-Lösung vor Gebrauch aus der Stammlösung verdünnen Die Lösungen sind im Kühlschrank aufzubewahren. Durchführung Teil 1: Die vorkultivierten Kulturen werden (i) mit ca. 10 ml Lösung besprüht, (ii) mit ca. 10 ml GA3 gegossen bzw. (iii) nicht behandelt. Alle Töpfe sind hinreichend zu wässern. Die Auswertung erfolgt am folgenden Praktikumstag (Länge der Sprosse bis zur Knospe, Anzahl der Internodien). Bitte Mittelwerte und Standardabweichung angeben. Teil 2: Ein Tropfen der GA3-Verdünnungen (1 mm, 0,1 mm, 0,01 mm, 0 mm mit Tween = Kontrolle) wird auf die Apikalknospe von jeweils zwei oder drei Sprossen gegeben. Die Auswertung (siehe Teil 1) erfolgt nach einer und nach zwei Wochen. Hinweis: Tween ist ein nichtionisches Detergenz, das die Oberflächenspannung von wässrigen Lösungen herabsetzt. Auswertung nach einer und zwei Wochen: Von möglichst 10 Pflanzen werden die Mittelwerte und die Standardabweichung berechnet. Welche statistischen Tests können Sie ausführen? Hinweis: Vermiculit (Erklärung z.b. bei Wikipedia) ist ein hocherhitzter Dämmstoff aus der Bauindustrie. Als Ersatz für Boden sichert er eine ausgezeichnete Durchlüftung des Wurzelraumes. Er gibt von sich aus fast keine Nährstoffe ab, hat aber eine hohe Wasserspeicherkapazität. Arbeitszeit: 30 Minuten plus Auswertung nach ein und zwei Wochen. 17
19 2. Kurstag 4.2 Einfluss von Abscisinsäure auf die Samenkeimung Materialien & Geräte: - Samen von Sinapis alba (Senf) - Petrischalen - Filterpapier (autoclaviert) ml-bechergläser - Parafilm zum verschließen - 4 x 10 ml Standzylinder oder grad. Gläser Chemikalien & Lösungen: - Stammlösung 10-4 M ABA. - Lösungen von ABA: 10-4 M, 10-5 M, 10-6 M, 10-7 M, jeweils 100 ml, plus Kontrolle (ohne ABA). Die Verdünnungen werden im Praktikum mit Leitungswasser hergestellt. Durchführung Die Petrischalen werden mit 3 Lagen Filterpapier belegt und jeweils 5 ml ABA-Lösung bzw. Wasser (Kontrolle) werden eingefüllt. Danach werden 30 Samen ausgelegt. Die Petrischalen werden mit Parafilm verschlossen und im Praktikumsraum oder im Gewächshaus aufgestellt. Auswertung 1. Die Keimprozente sind nach 7 Tagen zu bestimmen und gegen die Konzentration von ABA graphisch aufzutragen. 2. Die Keimfähigkeit der nicht gekeimten Samen ist zu überprüfen. Wie kann man das erreichen? Arbeitszeit: 15 Minuten plus Auswertung nach einer Woche. 18
20 2. Kurstag 4.3 Ein klassisches Experiment zur Phytochromwirkung Literatur: Kutschera; Schopfer/Brennicke Theorieteil: Skotomorphogenese und De-Etiolierung Vergleich verschiedener Entwicklungsstrategien Der eher theoretische erste Teil hat das Anliegen, die Eigenschaften etiolierter und grüner Pflanzen miteinander zu vergleichen. Da es sehr viele Unterschiede gibt (bitte frischen Sie Ihre Kenntnisse bei dieser Gelegenheit auf, so über unterschiedliche Phytochrome), könnten entsprechende Experimente fast beliebig erweitert werden. Der De-Etiolierungsprozess läuft bekanntlich auf allen Ebenen der Pflanze ab. Um Ihnen einen Überblick zu geben, sollen Sie in Ihrer Gruppe das Erscheinungsbild etiolierter und grüner Pflanzen gemeinsam mit einem Betreuer diskutieren. Materialien & Geräte: Pflanzenmaterial: Im Dunkeln und im Licht gewachsene Arabidopsis thaliana (auf Filterpapier) oder Tomate (auf Agar mit Nährmedium), 8 Tage alt, Ansatz in zwei Petrischalen aussäen. Falls sie verfügbar gemacht werden können, sollten photomorphogenetische Mutanten einbezogen werden, z.b. die aurea-mutante von Tomate. Diese Pflanzen werden für Sie vorkultiviert. Chemikalien & Lösungen: keine Praxisteil Experiment: Materialien & Geräte: - Lactuca-Achänen, Sorte Grand Rapid - Rundfilter, Messgläser - Petrischalen - Alu-Folie zum Verdunkeln - Dia-Projektoren mit Filtern für Rotlicht (R) und dunkelrotes Licht (FR), schwaches Grünlicht - Kisten zum Abdunkeln, Klebeband zum Beschriften Chemikalien & Lösungen: keine Durchführung In 6 Petrischalen mit 3 Lagen autoklaviertem Filterpapier wird so viel Leitungswasser gegeben, dass darauf ausgelegte Achänen gerade noch nicht wegschwimmen (etwa 5 ml). In jede Schale werden 30 Achänen gleichmäßig verteilt ausgelegt. Die Achänen werden nach der Quellung sehr rasch lichtempfindlich. Schalen nun sofort nach der Aussaat in Alufaolie einpacken und für 1h - 2 h ins Dunkle stellen (Holzkiste verwenden)! Die Schalen werden danach mit folgenden 6 Programmen bestrahlt: 19
21 2. Kurstag Ansatz 1: Ansatz 2: Ansatz 3: Ansatz 4: Ansatz 5: Ansatz 6: 2 min R + Dunkel 10 min FR + Dunkel 2 min R + 10 min FR + Dunkel 10 min FR + 2 min R + Dunkel Weißlicht (Tageslicht) Dunkel Bitte kombinieren Sie bei der Bestrahlung alle Varianten einer Bestrahlungsart so, dass insgesamt möglichst wenig Bestrahlungszeit benötigt wird. Die Auszählung erfolgt nach einer Woche. Als gekeimt gilt eine Achäne, wenn die Radicula die Achänenwand durchbrochen hat. Auswertung Die Keimprozente jeder Variante sind zu bestimmen und die Ergebnisse in Beziehung zum Phytochromsystem zu bringen. 20
22 2. Kurstag Komplex 5: Pflanzliche Inhaltsstoffe 5.1 Quantitative Bestimmung von Gesamtproteinen Müssen bei der Isolierung Detergentien eingesetzt werden, so versagt die übliche Bradford-Methode. Dies gilt z.b. für die Isolierung von Membranproteinen und damit auch, wenn eine Gesamtproteinbestimmung erforderlich ist. Materialien & Geräte: - Verschiedenes Saatgut, gemahlen - Vorrichtungen zum Homogenisieren - Eisbad - Tisch-Zentrifuge - Spektrophotometer - Koch-Wasserbad - Eppendorfpipetten mit Spitzen - Zentrifugenröhrchen - Vortexer - Kolbenpipetten (= automatische Pipetten) - Reagenzgläser, Pipetten Chemikalien & Lösungen: - Aceton - TRIS 50 mm, 20 g l -1 Na-Dodecylsulfat (SDS) - mit HCl auf ph = 8,3 einstellen; direkt vor der Verwendung im Praktikum (nicht vorher, auch wegen der Messelektrode) 10 ml l -1 Mercaptoethanol zugeben - TCA-Lösung (250 g l -1 Triochloressigsäure; Vorsicht, starke Säure! Hautkontakt vermeiden!) - Biuret-Reagenz - NaOH-Lösung (100 ml) - BSA-Stammlösung: 10 mg ml -1 Durchführung Jeweils eine Gruppe kann sich (muss aber nicht) auf eine Samen-(Karyopsen-)sorte beschränken. Von jeder Sorte sind 2 parallele Proben zu untersuchen. 1. Erstellen einer Eichkurve: Zunächst wird aus der Standardproteinlösung eine Verdünnungsreihe hergestellt um eine Eichkurve zu erhalten: 0,2/ 0,4/ 0,6/ 0,8 und 1 ml werden mit Wasser auf 1 ml aufgefüllt. Allen Ansätzen 4 ml Biuret-Reagenz zufügen, gut mischen und vor der Messung etwa 15 min warten. Die Referenzlösung enthält 1 ml Wasser + 4 ml Reagenz. Die klaren Lösungen werden gegen die Referenzlösungen photometrisch vermessen (1 cm Küvetten, 546 nm). 2. Homogenisation und Extraktion: Es werden 2 Proben zu genau 100 mg abgewogen. Mit 7 ml Extraktionspuffer versetzt, werden die Proben unter gelegentlichem Schütteln 10 min bei 100 o C in Zentrifugenröhrchen extrahiert. Nach dem Abkühlen erfolgt Zentrifugation (10 min bei 5000 rpm). 3. Fällung: Vom klaren Überstand werden jeweils 1 ml abgenommen und durch Zugabe von 1 ml TCA-Lösung im Eisbad gefällt. Nach 15 min den Niederschlag abzentrifugieren, mit 2 x 2 ml eiskaltem Aceton aufwirbeln und nochmals zentrifugieren. Aceton mit Kolbenpipette absaugen (Rest durch kurzes Erwärmen entfernen, es darf kein Lösungsmittel mehr vorhanden sein). Das Pellet wird in 1 ml 0,1 M NaOH gelöst und zur Proteinbestimmung wie bei der Erstellung der Eichkurve mit 4 ml Reagenz versetzt. 21
23 2. Kurstag 4. Colorimetrischer Test: Die Proben werden wie bei der Erstellung der Eichkurve bei 546 nm vermessen. Auswertung Ergebnisangabe: Proteingehalt pro Frischgewicht (achten Sie auf alle Verdünnungsschritte und auf die Angaben der Eichkurve!) Arbeitszeit: 90 Minuten plus 30 Minuten Eichkurve für die erste Gruppe 22
24 2. Kurstag 5.2 Ein Vorversuch zur pflanzlichen Molekularbiologie: Isolierung von DNA Materialien & Geräte: - Blattmaterial, z.b. Erbse - Reaktionsgefäße (2,0 ml, von Sarstedt) - Eppiständer - Pipetten - Eisbad - Schere - Tisch-Zentrifuge - UV-Spektrophotometer und UV-Küvetten (lila Markierung) - Nitrilhandschuhe (blau) - Vortex Chemikalien & Lösungen: - Lyse-Puffer - Chloroform:Isoamylalkohol (24:1) - 75% Ethanol - Isopropanol alle Phenol/Chloroform-haltigen Sachen kommen in ein separates Abfallgefäß Isolation von DNA aus Pflanzen: 1) ~ 0,3 g Blattmaterial abwiegen (Gewicht aber genau notieren) und im Mörser auf Eis lagern 2) Blattmaterial mechanisch im Mörser in 1 ml Lyse-Puffer zerkleinern, auf zwei 2,0-ml-Reaktionsgefäße (Sarstedt) verteilen und anschließend für 5 min bei RT inkubieren 3) 600 µl Phenol/Chloroform/Isoamylalkohol (steht im Kühlschrank) zugeben (im Abzug arbeiten!) 4) Proben kurz vortexen (jede Probe 5 sec ) 5) 5 min bei rpm bei RT zentrifugieren 6) Oberphase abnehmen, in neues 2 ml Eppi überführen (Abzug!) Hinweis: Die Interphase besteht aus Protein und darf nicht weiterverwendet werden. 7) 500 µl Chloroform/Iosamylalkohol zugeben (Abzug!) 8) Proben kurz vortexen (jede Probe 5 sec ) 9) 5 min bei rpm zentrifugieren 10) Oberphase abnehmen, in neues 2 ml Eppi überführen (Abzug!), 11) Chloroform/Isoamylalkohol-Extraktion noch 2x wiederholen 12) 1 Probenvolumen Isopropanol zugeben (vorgekühlt aus dem Kühlschrank) und gut mischen (Nicht vortexen!) 13) Proben 5 min auf Eis inkubieren, wenn möglich länger 14) 15 min bei rpm bei 4 C zentrifugieren 15) Flüssigkeit vorsichtig abnehmen bzw. abschütten 16) Pellet in 750 µl 75% EtOH (vorgekühlt aus dem Kühlschrank) waschen - Pellet muss schwimmen! 17) 5 min bei rpm bei 4 C zentrifugieren 23
25 2. Kurstag 18) Flüssigkeit vorsichtig abnehmen bzw. abschütten (nach einem kurzen Zentrifugationsschritt kann die restliche Flüssigkeit abpipettiert werden) [Vorsicht: Pellet nicht verlieren] 19) Pellet für min bei RT trocknen lassen 20) Pellet in 25 µl bis 50 µl dh 2O lösen (hängt von der Pelletgröße ab). 21) 25 μl dieser Lösung in eine Küvette mit 975 µl Wasser pipettieren, mischen und im Spektrophotometer messen Mit dem Programm DNA (Life sciences) wird die Konzentration und die Reinheit der DNA-Lösung gemessen. Es werden die Extinktionen bei 260 nm (Hauptextinktion von Nukleinsäuren), 280 nm (Hauptabsorption von Proteinen) und 230 nm (Gerbsäuren und Kohlenhydrate) gemessen. Zur Ermittlung der DNA-Reinheit werden die Quotienten E260/E280 und E260/E230 berechnet bzw. abgelesen (siehe dazu die oben genannten Hauptextinktionen). Wenn nur Absorptionswerte angezeigt werden: Extinktion 1 entspricht 50 µg dsdna ml -1. Fragen: 1. Welche DNA-Menge (total und pro Frischgewicht) haben Sie isoliert? 2. Was können Sie über die Reinheit Ihrer Präparation sagen? 3. Wie kann man RNA isolieren? (Die letzte Frage ist nur zu Ihrer Vorbereitung, nicht für das Protokoll). Arbeitszeit: 100 Minuten 24
26 2. Kurstag 5.3 Fett-Kohlenhydratumwandlung bei der Keimung fetthaltiger Samen Literatur: Schopfer II; Schopfer/Brennicke. Teil 1: Nachweis der Saccharosebildung: Materialien & Geräte: - 50 trockene Rapssamen sowie 50 Keimpflanzen (5-6 d nach Aussaat) - Präzisionswaage - Mörser - Quarzsand - Zentrifugenröhrchen (Hermle, verschließbar) - Zentrifuge mit swing-out-rotor - skalierte Glasröhrchen - Eppendorfgefäße (1,5 ml) - Pipetten + Spitzen - Wasserbad (100 C) - Spektrophotometer (578 nm) - Küvetten (1 cm) - Handschuhe Chemikalien & Lösungen: - Anthron-Reagenz (max. 2 Wochen alt; Vorsicht: konzentrierte Schwefelsäure!) - Saccharose-Stammlösung (50 mm) Durchführung: 1. Colorimetrischer Test: Zur Erstellung der Eichkurve wird die Saccharose-Stammlösung so verdünnt, dass folgende Mengen (Vorsicht: das sind keine Konzentrationsangaben!) in 200 µl Reinstwasser in Reaktionsgefäßen enthalten sind: 0, 2, 4, 6, 8, 10 µmol. Zu jedem Ansatz der Proben für die Eichkurve sowie zur Verdünnungsreihe der Messproben kommt 1 ml Anthron-Reagenz. Alle Proben werden dann 15 min im kochenden Wasserbad erhitzt und nach Abkühlung im Eisbad kräftig geschüttelt. Bei 578 nm wird gegen Luft (ohne Küvette im Vergleichsstrahlengang) vermessen. Die Nullprobe bedeutet Wasser plus Anthronreagenz, der sich dabei ergebende Wert muss subtrahiert werden. Bei Extinktionen über 0,9 muss entweder der Küvetteninhalt 1:10 verdünnt werden oder die Messungen mit der kleineren Konzentration erfüllen bereits das Kriterium. 2. Extraktion: Die ausgekeimten 50 Samen werden in Wurzeln, Sprosse und Kotyledonenpaare geteilt, auf Alu-Folie gewogen und anschließend in einem Mörser homogenisiert. Die 50 trockenen Samen werden ebenfalls gewogen und homogenisiert. Zur Homogenisation werden ca. 8 ml Reinstwasser und sehr wenig Sand mit den Proben in den Mörser gegeben. Das Homogenat wird in Zentrifugenröhrchen 5 min im kochenden Wasserbad erhitzt und anschließend 10 min bei 5000 rpm zentrifugiert. Der Überstand wird sofort nach der Zentrifugation in skalierte Glasröhrchen überführt und auf genau 10 ml aufgefüllt. Diese werde mit Parafilm verschlossen und vorsichtig geschüttelt. Daraus werden je zweimal 10, 50 und 100 µl für eine Verdünnungsreihe in Eppendorfgefäße pipettiert und mit Reinstwasser auf 200 µl ergänzt (Leerwert 200 µl Reinstwasser). Dazu werden 1 ml Anthronreagenz (siehe Colorimetrischer Test) pipettiert und die Lösung wird gut gemischt. Danach kommt das Gemisch 15 min ins kochende Wasserbad, wird danach im Eisbad abgekühlt und die Extinktion gemessen. Auswertung Anhand der erstellten Eichkurve (nur eine Gruppe) ist die Saccharose-Konzentration zu berechnen. Arbeitszeit: 3,5 Stunden 25
27 2. Kurstag Teil 2: Triacylglycerinbestimmung: Materialien & Geräte - 50 trockene Rapssamen sowie 50 Keimpflanzen (5-6 d nach Aussaat) - Glycerol-UV-Test-Kit [R-Biopharm Nr. E ], Informationsblatt des Herstellers (Kopie) - verschließbare Röhrchen (10 ml) - normale Röhrchen - skalierte Glasröhrchen - Eppendorf-Reaktionsgefäße - Pipetten + Spitzen - Eisbad - Spektrophotometer (340 nm) - 3 ml-küvetten (1 cm) Chemikalien & Lösungen - Extraktionsmedium: 80 ml Chloroform + 40 ml Methanol - ethanolische KOH-Lösung (0,5 M): 1,4 g KOH in reinem EtOH lösen, auf 50 ml mit EtOH auffüllen - MgSO 4-Lsg. (0,15 M) Durchführung 1. Extraktion: Die ausgekeimten 50 Samen werden in Wurzeln, Sprosse und Kotyledonenpaare geteilt, auf Alu-Folie gewogen und anschließend homogenisiert. Die 50 trockenen Samen werden ebenfalls gewogen und homogenisiert. Zur Homogenisation werden ca. 6 ml Extraktionsmedium und sehr wenig Sand mit den Proben in den Mörser gegeben. Die Homogenate werden in verschließbare Röhrchen gefüllt, 20 min in ein Eisbad gestellt und gelegentlich kräftig geschüttelt. Nach Absetzen des Rückstandes (eine eventuell vorhandene Interphase wird nicht mitverwendet) wird der Überstand in skalierte Glasröhrchen überführt. Daraus werden 50 µl- Proben entnommen und in Eppendorfgefäße pipettiert. Eine Kontrolle (Extraktionsmedium ohne Pflanzenmaterial) wird analog den 3 Proben behandelt. 200 µl KOH-Lösung zugegeben, mischen (Schüttler) und 10 min bei Raumtemperatur stehen lassen. 500 µl MgSO4-Lsg. zugeben und erneut mischen (Schüttler). Anschließend 5 min bei 5000 rpm zentrifugieren. 2. Enzymatischer Test: Kopie (Die Lösung 1 wird zwecks Materialersparnis nicht mit 11 ml demin. H2O aufgefüllt, sondern 1,0 g abgewogen und mit 5,5 ml gelöst. Die Lösung soll etwa 10 min bei Raumtemperatur stehen. Die Lösungen 2 und 3 sind gebrauchsfertig. (Die Enzyme enthaltenden Lösungen während der gesamten Dauer des Testes - auf Eis belassen!) In die normalen Röhrchen werden pipettiert: oder in 2 ml Eppis: 1. Lösung 1: 1,00 ml 500 µl 2. demin. H2O: 1,50 ml 750 µl (900µl) 3. Probelösung (bzw. Kontrolle): 0,5 ml 250 µl (50µl) 4. Lösung 2: 0,01 ml 50 µl (5µl) mischen und anschließend 10 min bei 37 C im Wasserbad im Reagenzglasständer inkubieren bzw. im Inkubator in die Küvetten füllen und bei 340 nm gegen Wasser vermessen. Nach der Messung werden 0,01 ml von Lösung 3 zugegeben und sorgfältig gemischt. Nach 15 min 26
28 2. Kurstag bei Raumtemperatur wird die Extinktion bei 340 nm erneut gemessen. Hinweis: Die Teilreaktionen und die Extinktionskoeffizienten sind in Schopfer II beschrieben! Auswertung: siehe Schopfer und die Anleitung des Herstellers des Testbestecks. Die molare Glycerin(=Triacylglycerol-)Konzentration läßt sich mit Hilfe des Extinktionskoeffizienten von NADH (ε366 = 3.5 x 10 3 l x mol -1 cm) und der Verdünnungsfaktoren berechnen (LAMBERT- BEERsches Gesetz). Arbeitszeit: 4 Stunden 27
29 2. Kurstag 5.4 Isolierung und Nachweis der Alkaloide des Schöllkrauts Literatur: Schopfer I und II; Schopfer/ Brennicke Materialien & Geräte: - Frischer Spross von Chelidonium majus - TLC-Fertigfolien aus Kieselgel (in vier Teile aufteilen) - TLC-Tank, Pipetten, Kapillarröhrchen zum Auftragen - UV-Lampe, Schutzbrillen Chemikalien & Lösungen: - Berberin (feste Vergleichssubstanz), stark verdünnt einsetzen - Extraktionsmedium: 14 ml Methanol + 1 ml Essigsäure (Eisessig) - Laufmittel: 85 ml Chloroform + 15 ml Methanol + 1 ml demin. Wasser + 2 ml Essigsäure (Eisessig) Durchführung Ein Tropfen des bei frischen Pflanzen an der Schnittfläche austretenden Milchsaftes wird mit 100 μl Extraktionsmedium in einem 2 ml Reaktionsgefäß (Eppi) suspendiert. Es hat sich für praktisch erwiesen, dazu der Stängel direkt in das Eppi einzutaucht. Auf der Kieselgelfolie wird etwa 2 cm vom unteren Rand entfernt eine Bleistiftlinie gezogen. Nebeneinander werden mit einer Glaskapillare drei Tropfen dieses Gemisches auf die Linie aufgetragen, so dass eine Bande entsteht ( ). Zwischendurch trocknen lassen, damit die Bande nicht auseinanderläuft. Eine weitere Bande wird mit der doppelten Menge erstellt (auf jeden Punkt ein zweites Mal tupfen). Nach dem Trocknen der Flecken wird die Platte in den mit dem Laufmittel gefüllten Tank (Füllhöhe höchstens 0,5 cm) gestellt (im Abzug!). Kurz bevor die Laufmittelfront den oberen Rand der Platte erreicht hat, wird der Lauf abgebrochen (Laufzeit ca. 30 min). Sofort Laufmittelfront mit einem Bleistift markieren und die Rf-Werte ermitteln. Die Banden werden mit Bleistift markiert und die Farbe daneben notiert. Unter einer UV-B-Lampe (Dunkelkammer) werden die fluoreszierenden Banden ebenfalls mit der Farbe beschriftet. Zum Vergleich kann man z.b. Hylomecon japonicum, wie Schöllkraut ein Mohngewächs, benutzen. Achtung: Bitte Schutzbrille & Handschuhe unter UV-Licht tragen! Vergleichswerte: (s. Schopfer II) Die angegebenen Rf-Werte können nur eine grobe Orientierung sein, die Reihenfolge jedoch bleibt erhalten. - Sanguinarin (Farbe rot-orange; Fluoreszenz orange) Rf = 0,9 - Chelerythrin (Farbe goldgelb-zitronengelb; Fluoreszenz goldgelb) Rf = 0,8 - Berberin (Farbe zitronengelb; Fluoreszenz grün) Rf = 0,3 - Coptisin (Farbe gelb-gelbbraun; Fluoreszenz zitronengelb) Rf = 0,2 Es müssen auch die Fluoreszenzfarben zur Charakterisierung herangezogen werden. Anmerkungen 1. Ein Vergleich mit Rf-Werten aus der Literatur ist erfahrungsgemäß nur bedingt möglich. Das stellt jedoch kein Problem dar, weil der Vergleich von Absorptions- und Fluoreszenzfarbe eine eindeutige Zuordnung ermöglicht. 2. Als Vergleichssubstanz ist Berberin vorhanden. Um sie als Hilfe bei der Zuordnung einsetzen zu können, werden steigende Volumina auf die TLC-Folie mit aufgetragen. 28
30 2. Kurstag 3. Bitte nicht mehr als 5 Platten in ein Gefäß stellen, weil sich die Gruppen sonst gegenseitig durch zu häufiges Öffnen behindern. Arbeitszeit: 15 Minuten plus Minuten Laufzeit der TLC 29
31 3. Kurstag Komplex 6: Pflanzliche Enzyme 6.1 Operationale Kriterien der Enzymaktivitätsbestimmung - Fallstudie Fumarathydratase Literatur: Schopfer II, Schopfer/Brennicke Materialien & Geräte: - Keimlinge von Sinapis alba, 3 oder 4 d bei 25 C auf feuchtem Filterpapier angezogen, je Gruppe 2 Petrischalen mit mindestens 25 Keimlingen - Eisbad - Mörser - Quarzsand - Eppendorf-Zentrifuge mit Festwinkelrotor für U min -1 - Reaktionsgefäße (1,5 ml) - Peleusball und Glaspipetten - Spektrophotometer (240 nm, Kinetik), - 3 Quarzküvetten (1 cm, 3 ml), Stoppuhr oder Handy Chemikalien & Lösungen: - K-Phosphat-Puffer 50 mm, ph= 7,4 - L-Malatlösung (Na-Salz der Apfelsäure, 1,5 M; nicht mit Maleat verwechseln!) - Triton X Polyclar AT (PVP) (das ist unlösliches Polyvinylpyrrolidon!) - Dithioerythrit (CLELANDs Reagenz) 1 mm Durchführung Achtung! Vor Versuchsbeginn bitte die weiterführenden Experimente zur Kenntnis nehmen und nach Wunsch und in Absprache mit dem Versuchsbetreuer die eine oder andere Variante zusammen mit der Kontrolle einplanen. Alle Lösungen während der Präparation kalt halten (Eisbad). 1. Kotyledonen von 20 Keimlingen ernten und Frischgewicht bestimmen 2. Homogenisieren im Mörser mit wenig Quarzsand und 1 ml Puffer (ebenfalls eiskalt) im Eisbad. 3. Wenn keine Partikel mehr erkennbar sind, weitere 4,5 ml Puffer zugeben, gut durchmischen. Mit weiteren 4,5 ml nachspülen. Davon werden 2 ml in ein Reaktionsgefäß ( Eppi ) gegeben 4. Zentrifugation bei rpm für 10 min (gekühlte Tischzentrifuge) 5. Reaktionsgefäße vorsichtig aus dem Rotor nehmen und etwa 1 ml des klaren Überstandes unter der Fettschicht langsam absaugen (Pipette und Ball) 6. In eine Küvette (für kleinere Küvetten entsprechend herunterskalieren) wird pipettiert und auf Raumtemperatur temperiert: 2,8 ml Puffer 0,1 ml Malatlösung Jetzt wird der Leerwert gemessen. 7. plus 0,1 ml Enzymextrakt ( = Start der Reaktion) 30
32 3. Kurstag 8. Messung bei 240 nm gegen Puffer in Abständen von 1-3 min (je nach der Geschwindigkeit der Extinktionszunahme, d.h. der Enzymaktivität) über etwa 30 min. Weiterführende Experimente: 1. Ist das Enzym im Rohextrakt in der Kontrolle im Vergleich zum Ansatz maximal aktiv? (Welchen Effekt hat der Zusatz von Dithioerythrit (1 mm) auf die Enzymaktivität?) Zum Test dem Homogenisationspuffer Dithioerythrit zusetzen (1 ml Stammlösung herstellen auf Eis), ansonsten wie im Grundexperiment. 2. Gibt es Anhaltspunkte für Hemmstoffe im Extrakt? (Welchen Effekt hat eine Behandlung des Extraktes mit PVP?) PVP (10 mg) wird dem Puffer vor der Homogenisation zugesetzt. Achtung! PVP quillt im Puffer, dadurch nimmt das Extraktvolumen stark ab. Das Extraktvolumen muss bei der Berechnung der Enzymaktivität berücksichtigt werden. 3. Wird das Enzym durch die Extraktion optimal in Lösung gebracht? (Welchen Effekt hat der Zusatz von 0,5 ml Triton X-100 zu 100 ml Extraktionspuffer?) Auswertung Die Enzymaktivität von zwei unterschiedlich behandelten Proben (z.b. Kontrolle und Zusatz von Dithioerythrit) ist zu berechnen (siehe dazu Schopfer II) und zu vergleichen. Der Extinktionskoeffizient von Fumarat beträgt bei 240 nm 2, L mol -1 cm -1. Arbeitszeit: 2 Stunden 31
33 3. Kurstag 6.2 Die kinetische Charakterisierung eines Enzyms - Fallstudie Peroxidase Literatur: Schopfer II. Besonders bei diesem Versuch sollten Sie den entsprechenden Abschnitt vor Versuchbeginn gelesen haben. Materialien & Geräte - Meerrettichwurzel (im Kühlschrank aufbewahren für alle Kurse) - Messer, Mörser, Schneidbrettchen - Eisbad, Eppis 1,5 ml - Spektrophotometer (436 nm, 25 C) - Küvetten (1 cm) - Uhr - Glaspipetten, Peleusbälle - Tischzentrifuge - Schutzhandschuhe, Schutzbrille - Reagenzgläser (kurz) - Nitrilhandschuhe (blau) - Bechergläser 100 ml - Messzylinder 100 ml Chemikalien & Lösungen - Phosphatpuffer (50 mm, ph = 7,0) - Wasserstoffperoxid, 1 mm und 4 mm frisch verdünnen (die Perhydrol-Ausgangslösung enthält 30 Gew.-% = 9,8 M) - Guajakol (Lösung: 20 mm = 220 μl in 100 ml Reinstwasser, frisch ansetzen) Guajacol ist ein in Guajak-Bäumen vorkommender sekundärer Pflanzenstoff, der sich strukturell vom Anisol und vom Phenol ableitet. Guajacol ist einer der Aromastoffe von Whisky und Kaffee. Man macht auch Vanillin daraus. Sicherheitshinweis: Wasserstoffperoxid wirkt stark oxidierend, auch auf menschlicher Haut! Bitte Schutzhandschuhe und Schutzbrille beim Verdünnen tragen. Unverdünntes Guajacol sollte im Abzug gehandhabt werden. Es reizt Haut und Augen. Durchführung Herstellung des Enzymextraktes: 0,250 g fein zerschnittene Stückchen Meerrettich mit 1 ml Puffer und einer Prise Sand in einem Mörser auf Eis homogenisieren. Wenn keine Partikel mehr erkennbar sind, Suspension in Zentrifugenröhrchen (im Eisbad) gießen. Mörser mit 3 ml Puffer ausspülen, ebenfalls in das Röhrchen geben. 2 x 1,5 ml der Suspension in ein Reaktionsgefäß ( Eppi ) zum Zentrifugieren füllen. Danach Zentrifugation: Tischzentrifuge 10 min, rpm (= U min -1 ). Vom Überstand 1 ml abnehmen und mit 3 ml Puffer verdünnen (1+3-Verdünnung). Dies ist der Enzymextrakt. Hinweis: Die enzymatische Reaktion verläuft über verschiedene Teilreaktionen. Testansatz unter Verwendung von Teilreaktion 1: 32
34 3. Kurstag 0,4 ml Puffer + 1 ml Guajakol-Lösung + 0,05 ml Enzymextrakt in Küvette mischen (dann auf Raumtemperatur einstellen lassen). Leerwert messen. 0,05 ml H2O2-Lösung (1 mm) zugeben, mischen und Stoppuhr starten. Messung alle 10 s über 2 min. Testansatz unter Verwendung von Teilreaktion 2: Ebenfalls in eine Küvette pipettiert werden 1,4 ml Puffer, 0,025 ml Guajakol-Lösung, 0,05 ml Enzymextrakt. Die Reaktion wird mit 0,05 ml H2O2-Lösung (4 mm) gestartet und wie oben verfahren. Hinweis: Testansatz 1 sollte eine höhere Anfangsgeschwindigkeit haben als Testansatz 2. Warum ist das so? Die beiden vorverdünnten Wasserstoffperoxid-Lösungen (1 mm, 4 mm) sollten beim Einsatz nicht älter als 10 min sein. Wenn die Küvette durch Bildung eines Farbstoffes von innen beschlägt, dann bitte zwischen 2 Messreihen mit Aceton reinigen und mit Reinstwasser nachspülen. Auswertung Bestimmen Sie die Anfangsgeschwindigkeiten der beiden Enzymreaktionen und vergleichen Sie die Geschwindigkeiten miteinander (siehe Schopfer II). Arbeitszeit: ca. 30 min 33
Pflanzenphysiologie. Praktikum Sommersemester Leitung: Dr. Jeannette Pfalz
 Pflanzenphysiologie Praktikum Sommersemester 2017 Leitung: Dr. Jeannette Pfalz Praktikum Pflanzenphysiologie Sommersemester 2017 Zum Pflanzenphysiologischen Praktikum im Sommersemester 2017 werden Ihnen
Pflanzenphysiologie Praktikum Sommersemester 2017 Leitung: Dr. Jeannette Pfalz Praktikum Pflanzenphysiologie Sommersemester 2017 Zum Pflanzenphysiologischen Praktikum im Sommersemester 2017 werden Ihnen
Versuch 1: Extraktion von ß-Carotin aus Lebensmitteln
 Name Datum Versuch 1: Extraktion von aus Lebensmitteln Geräte: 4 Reagenzgläser, 4 Gummistopfen, Reagenzglasständer, 1 Erlenmeyerkolben mit Stopfen, Messer, Mörser, Spatel, Messpipette, 1 kleine Petrischale,
Name Datum Versuch 1: Extraktion von aus Lebensmitteln Geräte: 4 Reagenzgläser, 4 Gummistopfen, Reagenzglasständer, 1 Erlenmeyerkolben mit Stopfen, Messer, Mörser, Spatel, Messpipette, 1 kleine Petrischale,
2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
 Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie
 Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
PROTEINBESTIMMUNG. Vergleich Bradford und BCA
 PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
Plasmid Mini Kit. Artikel-Nr Präparationen Präparationen Präparationen
 1 Datenblatt Artikel-Nr. 55.4000.010 10 Präparationen 55.4000.050 50 Präparationen 55.4000.250 250 Präparationen Verbessertes Protokoll mit neuen Puffern! Sicherheitsanweisungen Bitte gehen Sie mit allen
1 Datenblatt Artikel-Nr. 55.4000.010 10 Präparationen 55.4000.050 50 Präparationen 55.4000.250 250 Präparationen Verbessertes Protokoll mit neuen Puffern! Sicherheitsanweisungen Bitte gehen Sie mit allen
GEBRAUCHSANLEITUNG. Lowry Assay Kit. Kit für die Proteinkonzentrationsbestimmung. (Kat.-Nr )
 GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
Plasmid Mini Kit PLUS
 Datenblatt Artikel-Nr.: 55.4500.010 10 Präparationen 55.4500.050 50 Präparationen 55.4500.250 250 Präparationen Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und Reagenzien, die im Kit enthalten
Datenblatt Artikel-Nr.: 55.4500.010 10 Präparationen 55.4500.050 50 Präparationen 55.4500.250 250 Präparationen Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und Reagenzien, die im Kit enthalten
Kohlenhydrate in Lebensmitteln Schokolade ist nicht gleich Schokolade!
 Kohlenhydrate in Lebensmitteln ist nicht gleich! Einführung Sicher hast du schon davon gehört, dass es verschiedene Zuckerarten gibt. So gibt es Traubenzucker (Glucose), Fruchtzucker (Fructose) und natürlich
Kohlenhydrate in Lebensmitteln ist nicht gleich! Einführung Sicher hast du schon davon gehört, dass es verschiedene Zuckerarten gibt. So gibt es Traubenzucker (Glucose), Fruchtzucker (Fructose) und natürlich
Versuch 03: Enzyme. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
 Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Protokoll Praktikum für Humanbiologie Studenten
 Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung)
 Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Novartis Pharma AG Schullabor. Wundermedizin. Experimente im Schullabor
 Novartis Pharma AG Schullabor Wundermedizin Experimente im Schullabor 2017 Experiment A 1. Markieren Sie die bunten Röhrchen auf dem Deckel mit Ihrem Gruppenzeichen (zum Beispiel *, X, oder etc.) 2. Die
Novartis Pharma AG Schullabor Wundermedizin Experimente im Schullabor 2017 Experiment A 1. Markieren Sie die bunten Röhrchen auf dem Deckel mit Ihrem Gruppenzeichen (zum Beispiel *, X, oder etc.) 2. Die
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
3 150 ml-bechergläser als Wasserbäder Thermometer 2 ml-plastikpipetten Parafilm
 Nachweis der Enzymaktivität und Enzymhemmung Chemikalien: Harnstofflösung (10% w/v) Phenolphtalein-Lösung Urease rohe Kartoffel Wasserstoffperoxid-Lösung (30 % w/v) Bäckerhefe verdünnte Lösung von Methylenblau
Nachweis der Enzymaktivität und Enzymhemmung Chemikalien: Harnstofflösung (10% w/v) Phenolphtalein-Lösung Urease rohe Kartoffel Wasserstoffperoxid-Lösung (30 % w/v) Bäckerhefe verdünnte Lösung von Methylenblau
Für enzymkinetische Untersuchungen legen Sie 0.2 ml einer 5 mm Substratlösung vor. Der fertige Inkubationsansatz hat ein Volumen von 2 ml.
 Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
Labormethoden. Versuch 1: Messgenauigkeit beim Pipettieren und Wiegen
 Labormethoden Einführung Mit den Versuchen an diesem ersten Praktikumstag sollen Sie wichtige Methoden wiederholen bzw. ergänzen, die Sie bereits im Chemischen Praktikum kennengelernt haben. Diese Fertigkeiten
Labormethoden Einführung Mit den Versuchen an diesem ersten Praktikumstag sollen Sie wichtige Methoden wiederholen bzw. ergänzen, die Sie bereits im Chemischen Praktikum kennengelernt haben. Diese Fertigkeiten
Pflanze direkt 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Biochemische Labormethoden
 Biochemische Labormethoden, Seite 1 Biochemische Labormethoden Einführung Mit den Versuchen an diesem ersten Praktikumstag sollen Sie wichtige Methoden wiederholen bzw. ergänzen, die Sie bereits im Chemischen
Biochemische Labormethoden, Seite 1 Biochemische Labormethoden Einführung Mit den Versuchen an diesem ersten Praktikumstag sollen Sie wichtige Methoden wiederholen bzw. ergänzen, die Sie bereits im Chemischen
Kohlenhydrat-Analytik
 Kohlenhydrat-Analytik Kohlenhydrate sind in ihrem strukturellen Aufbau sehr ähnlich. Eine spezifische Bestimmung wird dadurch erschwert. Ein gruppenweises Unterscheiden mit verschiedenen einfachen Nachweisreaktionen
Kohlenhydrat-Analytik Kohlenhydrate sind in ihrem strukturellen Aufbau sehr ähnlich. Eine spezifische Bestimmung wird dadurch erschwert. Ein gruppenweises Unterscheiden mit verschiedenen einfachen Nachweisreaktionen
SOP_018_Glucosebestimmung
 SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen
 GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Modifizierte Gene Editor Mutagenese
 Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
Kurzinformation: Je nach Qualität und Entwicklungsstufe können die verschiedenen Böden unterschiedlich große Mengen an Wasser speichern.
 Wasserspeicherung 30 Minuten V 14 Kurzinformation: Je nach Qualität und Entwicklungsstufe können die verschiedenen Böden unterschiedlich große Mengen an Wasser speichern. Material: 3 verschiedene Bodenproben
Wasserspeicherung 30 Minuten V 14 Kurzinformation: Je nach Qualität und Entwicklungsstufe können die verschiedenen Böden unterschiedlich große Mengen an Wasser speichern. Material: 3 verschiedene Bodenproben
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Zusatzveranstaltung 4: Es werde Licht!
 Zusatzveranstaltung 4: Es werde Licht! Station 1: Licht aus Öl E1 Dochte Helfer beim Leuchten E2 Welches Öl leuchtet am hellsten? E3 Dem Öl auf der Spur Station 2: Romantik im Kerzenschein E4 Teelichter
Zusatzveranstaltung 4: Es werde Licht! Station 1: Licht aus Öl E1 Dochte Helfer beim Leuchten E2 Welches Öl leuchtet am hellsten? E3 Dem Öl auf der Spur Station 2: Romantik im Kerzenschein E4 Teelichter
Pflanzenphysiologie. Versuch Stickstoffmetabolismus - Induktion der Nitratreduktase
 Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Pflanzenphysiologie Versuch Stickstoffmetabolismus - Induktion der Nitratreduktase Mitarbeiter: Brill, Martin Mai, Oliver Schoof,
Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Pflanzenphysiologie Versuch Stickstoffmetabolismus - Induktion der Nitratreduktase Mitarbeiter: Brill, Martin Mai, Oliver Schoof,
Photochemische Reaktion
 TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
Enzymologie 10. Kurs
 Arbeitsgruppe D Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs : Enzymologie Einleitung Enzyme ermöglichen durch ihre katalytische Wirkung viele Reaktionen im Stoffwechsel von Lebewesen.
Arbeitsgruppe D Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs : Enzymologie Einleitung Enzyme ermöglichen durch ihre katalytische Wirkung viele Reaktionen im Stoffwechsel von Lebewesen.
Halte das Papier sofort nach dem Auftupfen gegen das Licht. Föhne die Flecken trocken und halte das Filterpapier noch einmal gegen das Licht.
 Fettfleckprobe Pipetten, Filterpapier, Föhn Speiseöl, Wasser, verschiedene Milchsorten, Sahne Tropfe auf ein Filterpapier 1 Tropfen Wasser, 1 Tropfen Öl und jeweils einen Tropfen von jeder Milchsorte und
Fettfleckprobe Pipetten, Filterpapier, Föhn Speiseöl, Wasser, verschiedene Milchsorten, Sahne Tropfe auf ein Filterpapier 1 Tropfen Wasser, 1 Tropfen Öl und jeweils einen Tropfen von jeder Milchsorte und
Standardabweichung und Variationskoeffizient. Themen. Prinzip. Material TEAS Qualitätskontrolle, Standardabweichung, Variationskoeffizient.
 Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
QUALITATIVE UNTERSUCHUNGEN
 QUALITATIVE UNTERSUCHUNGEN Allgemeiner Alkaloid-Nachweis Cinchonae cortex 0.5 g gepulverte Droge werden mit 10 ml 0.2 M Schwefelsäure geschüttelt und abfiltriert. 2 ml aus den Extrakten werden in Reagenzgläser
QUALITATIVE UNTERSUCHUNGEN Allgemeiner Alkaloid-Nachweis Cinchonae cortex 0.5 g gepulverte Droge werden mit 10 ml 0.2 M Schwefelsäure geschüttelt und abfiltriert. 2 ml aus den Extrakten werden in Reagenzgläser
AnC I Protokoll: 6.1 Extraktionsphotometrische Bestimmung von Cobalt mit HDEHP! SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Biochemische UE Alkaline Phosphatase.
 Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Chemie-Labothek zur Photochemie
 Fluoreszenz und Phosphoreszenz, Echtfarbenemissionsspektren (EFES) V1: Fluoreszenz und Phosphoreszenz Arbeitsmaterialien: Waage Mörser mit Pistill Porzellanschale Bunsenbrenner UV-Handlampe 7 Reagenzgläser
Fluoreszenz und Phosphoreszenz, Echtfarbenemissionsspektren (EFES) V1: Fluoreszenz und Phosphoreszenz Arbeitsmaterialien: Waage Mörser mit Pistill Porzellanschale Bunsenbrenner UV-Handlampe 7 Reagenzgläser
SingleQuant Assay Kit
 GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
Untersuchungen zu Gärungsbedingungen (projektartiger Unterricht)
 Untersuchungen zu Gärungsbedingungen (projektartiger Unterricht) Biotechnische Verfahren werden seit frühgeschichtlicher Zeit angewendet. Aus der Beobachtung, dass süße Früchte und Fruchtsäfte bei der
Untersuchungen zu Gärungsbedingungen (projektartiger Unterricht) Biotechnische Verfahren werden seit frühgeschichtlicher Zeit angewendet. Aus der Beobachtung, dass süße Früchte und Fruchtsäfte bei der
Versuche zu Stärke. AGENS Arbeitsgemeinschaft NaturStoffe Leipzig
 Versuche zu Stärke Versuch 1 - Stärkegewinnung aus Kartoffeln Geräte: 2 Kunststoffschüssel groß 1 Kunststoffschüssel klein 1 Kartoffelreibe 1 Baumwoll- oder Leinentuch 2 Kartoffeln 1 Löffel 1 Trichter
Versuche zu Stärke Versuch 1 - Stärkegewinnung aus Kartoffeln Geräte: 2 Kunststoffschüssel groß 1 Kunststoffschüssel klein 1 Kartoffelreibe 1 Baumwoll- oder Leinentuch 2 Kartoffeln 1 Löffel 1 Trichter
Übungsaufgabe 1. Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz
 Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Auf der Suche nach der Wundermedizin
 Auf der Suche nach der Wundermedizin Experimente im Schullabor 1 Herausgeber Novartis Pharma AG, CH-4002 Basel Autoren: Dr. Gesche Standke und Dr. Christiane Röckl Michel Zeichnungen: Fonds der Chemischen
Auf der Suche nach der Wundermedizin Experimente im Schullabor 1 Herausgeber Novartis Pharma AG, CH-4002 Basel Autoren: Dr. Gesche Standke und Dr. Christiane Röckl Michel Zeichnungen: Fonds der Chemischen
Protokoll Tag 4, Teil 1
 Protokoll Tag 4, Teil 1 D. Titrationsverfahren D.1. Einführung in die quantitative Analyse; D.2. Acidimetrie (Bestimmung der Konzentration einer Säure) Am heutigen letzten Tag des Praktikums geht es um
Protokoll Tag 4, Teil 1 D. Titrationsverfahren D.1. Einführung in die quantitative Analyse; D.2. Acidimetrie (Bestimmung der Konzentration einer Säure) Am heutigen letzten Tag des Praktikums geht es um
DNA Isolierung. Praktikum Dr. László Kredics
 Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
Kolorimeter Best.- Nr. MD13230
 Kolorimeter Best.- Nr. MD13230 1. Allgemein: Das Kolorimeter ist mit zwei Küvetten ausgestattet, die sich gegenüberstehen, es wird mit zwei Abdeckungen geliefert, die es erlauben, das Gerät zu "nullen".
Kolorimeter Best.- Nr. MD13230 1. Allgemein: Das Kolorimeter ist mit zwei Küvetten ausgestattet, die sich gegenüberstehen, es wird mit zwei Abdeckungen geliefert, die es erlauben, das Gerät zu "nullen".
1. Proteinnachweis mit Bradford-Farbreagenz
 1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
Pflanzenphysiologie. Versuch Pflanzenhormone
 Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Pflanzenphysiologie Versuch Pflanzenhormone Mitarbeiter: Brill, Martin Mai, Oliver Schoof, Nils Betreuer: Hr. Hinz Versuchsdatum:
Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Pflanzenphysiologie Versuch Pflanzenhormone Mitarbeiter: Brill, Martin Mai, Oliver Schoof, Nils Betreuer: Hr. Hinz Versuchsdatum:
peqgold RNA Pure FL Methode zur Isolierung von RNA aus flüssigen Proben
 peqgold RNA Pure FL Methode zur Isolierung von RNA aus flüssigen Proben Lot-Nr. Best.-Nr. 30-1110 100 ml 30-1120 200 ml 30-1130 500 ml Lagerung: Lichtgeschützt bei 4 C für 12 Monate haltbar. Einleitung
peqgold RNA Pure FL Methode zur Isolierung von RNA aus flüssigen Proben Lot-Nr. Best.-Nr. 30-1110 100 ml 30-1120 200 ml 30-1130 500 ml Lagerung: Lichtgeschützt bei 4 C für 12 Monate haltbar. Einleitung
Wir untersuchen das Grün der Blätter
 Naturwissenschaften Kantonsschule Freudenberg Wir untersuchen das Grün der Blätter Messzylinder: Mörser: 1. Schritt: Farbe aus grünen Blättern extrahieren Jede Gruppe wählt im Park eine andere Pflanze
Naturwissenschaften Kantonsschule Freudenberg Wir untersuchen das Grün der Blätter Messzylinder: Mörser: 1. Schritt: Farbe aus grünen Blättern extrahieren Jede Gruppe wählt im Park eine andere Pflanze
Bradford Reagent, 5x
 GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
Gefahr für 100 Kressesamen
 Gefahr für 100 Kressesamen Stand: 9.06.018 Jahrgangsstufen 11/1 Fach/Fächer Biologie (Ausbildungsrichtung ABU) Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material 180 Minuten Kressesamen,
Gefahr für 100 Kressesamen Stand: 9.06.018 Jahrgangsstufen 11/1 Fach/Fächer Biologie (Ausbildungsrichtung ABU) Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material 180 Minuten Kressesamen,
Protokoll für den 6. Praktikumstag
 Protokoll für den 6. Praktikumstag http://www.biomedizinischechemie.de Autor: Werner Schwalbach Version 2.0 Quellen: Anorganisches Grundpraktikum kompakt von Gertrud Kiel Versuch 4.1 des Permanganations
Protokoll für den 6. Praktikumstag http://www.biomedizinischechemie.de Autor: Werner Schwalbach Version 2.0 Quellen: Anorganisches Grundpraktikum kompakt von Gertrud Kiel Versuch 4.1 des Permanganations
Zweistrahlphotometer, Mikropipetten (1 ml), Vortexer, Eppis mit Deckel (2 ml), Analysewaage, Glasküvetten mit Deckel,
 Illumina-Chemie.de - Artikel Analytik Dithizonmethode Im Folgenden wird die Dithizonmethode beschrieben. Die Dithizonmethode ist eine Methode zum quantitativen, photometrischen Nachweis von Schwermetallionen
Illumina-Chemie.de - Artikel Analytik Dithizonmethode Im Folgenden wird die Dithizonmethode beschrieben. Die Dithizonmethode ist eine Methode zum quantitativen, photometrischen Nachweis von Schwermetallionen
NAD+/NADH ADH CH 3 CH 2 OH + NAD + CH 3 CHO + NADH + H + Hier unterscheiden sich Ethanol und NAD + in der Tat funktionell nicht.
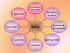 NAD+/NADH NAD + (Nicotinamid-adenin-dinukleotid) ist das häufigste "Coenzym" enzymatischer Redox-reaktionen. Von den Lehrbüchern wird es teils als Coenzym, teils als Cosubstrat eingeordnet. Das erstere
NAD+/NADH NAD + (Nicotinamid-adenin-dinukleotid) ist das häufigste "Coenzym" enzymatischer Redox-reaktionen. Von den Lehrbüchern wird es teils als Coenzym, teils als Cosubstrat eingeordnet. Das erstere
Extraktion. Aufgabe und Material. Lehrer-/Dozentenblatt. Lehrerinformationen. Lernziele. Hinweise zu Aufbau und Durchführung. H- und P-Sätze.
 Lehrer-/Dozentenblatt Extraktion Aufgabe und Material Lehrerinformationen Lernziele Farbstoffe lassen sich durch Extraktion aus den gefärbten Substanzen herauswaschen. Extraktion ist ein sowohl im Alltag
Lehrer-/Dozentenblatt Extraktion Aufgabe und Material Lehrerinformationen Lernziele Farbstoffe lassen sich durch Extraktion aus den gefärbten Substanzen herauswaschen. Extraktion ist ein sowohl im Alltag
Projekt- Nachweisreaktionen. Dieses Skript gehört: NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz
 Projekt- Nachweisreaktionen NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz Dieses Skript gehört: 1 Nachweise von Anionen 1. Nachweis von Sulfat 3 Reagenzgläser im Reagenzglasständer
Projekt- Nachweisreaktionen NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz Dieses Skript gehört: 1 Nachweise von Anionen 1. Nachweis von Sulfat 3 Reagenzgläser im Reagenzglasständer
Nukleinsäuren (Prof. Stradal)
 26.11. 30.11.2012 Nukleinsäuren (Prof. Stradal) 1 Laborbiologie: Biomoleküle Versuchswoche DNA Lernziele sind die Kenntnis: des molekularen Aufbaus und der wichtigsten Eigenschaften der Nukleinsäurebasen,
26.11. 30.11.2012 Nukleinsäuren (Prof. Stradal) 1 Laborbiologie: Biomoleküle Versuchswoche DNA Lernziele sind die Kenntnis: des molekularen Aufbaus und der wichtigsten Eigenschaften der Nukleinsäurebasen,
Nachweis kleiner Mengen Arsen neben Antimon mit der Bettendorff-Probe
 Illumina-Chemie.de - Artikel Analytik Nachweis kleiner Mengen Arsen neben Antimon mit der Bettendorff-Probe In Mineralien ist das Arsen oft ein natürlicher Begleiter des Antimons (und umgekehrt). Wenn
Illumina-Chemie.de - Artikel Analytik Nachweis kleiner Mengen Arsen neben Antimon mit der Bettendorff-Probe In Mineralien ist das Arsen oft ein natürlicher Begleiter des Antimons (und umgekehrt). Wenn
Versuch: Welche Farben sind im Blattgrün?
 Name: Datum: Versuch: Welche Farben sind im Blattgrün? Materialien: Mörser, Pistill, 100-mL-Becherglas, Schere, 10-mL-Pipette oder Tropfpipette, Trichter, Faltenfilter, Erlenmeyerkolben (50 oder 100 ml),
Name: Datum: Versuch: Welche Farben sind im Blattgrün? Materialien: Mörser, Pistill, 100-mL-Becherglas, Schere, 10-mL-Pipette oder Tropfpipette, Trichter, Faltenfilter, Erlenmeyerkolben (50 oder 100 ml),
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung
 V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
Dokumentation Projekt Chromatografie PLUS-Kurs SU 4+, GGS Vaalserquartier, Aachen
 Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 220 SchülerInnen
Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 220 SchülerInnen
Biologische Übungen III Donnerstag, Kurs 2- Ames Test. Arbeitsgruppe D6: Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann
 Biologische Übungen III Donnerstag, 14.11.2003 Kurs 2- Ames Test Arbeitsgruppe D6: Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Protokoll: Einleitung Im heutigen Kurs haben wir den Ames Test
Biologische Übungen III Donnerstag, 14.11.2003 Kurs 2- Ames Test Arbeitsgruppe D6: Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Protokoll: Einleitung Im heutigen Kurs haben wir den Ames Test
Fleckis Milchlabor Mein Forscherheft
 Fleckis Milchlabor Mein Forscherheft Name Experiment 1 Fülle ein echerglas ungefähr halbvoll mit Milch, ein zweites halbvoll mit Wasser. Decke beide echergläser jeweils mit einem Uhrglas ab und stelle
Fleckis Milchlabor Mein Forscherheft Name Experiment 1 Fülle ein echerglas ungefähr halbvoll mit Milch, ein zweites halbvoll mit Wasser. Decke beide echergläser jeweils mit einem Uhrglas ab und stelle
Säurekonstante des p-nitrophenols
 Säurekonstante des p-nitrophenols Grundlagen Sie bestimmen spektralphotometrisch die Säurekonstante einer schwachen Säure. Voraussetzung dafür ist, dass die undissoziierte Säure in einem anderen Spektralbereich
Säurekonstante des p-nitrophenols Grundlagen Sie bestimmen spektralphotometrisch die Säurekonstante einer schwachen Säure. Voraussetzung dafür ist, dass die undissoziierte Säure in einem anderen Spektralbereich
Biotechnologie Forscher TM. Genes in a Bottle Kit DNA Necklace Module
 Biotechnologie Forscher TM Genes in a Bottle Kit DNA Necklace Module Bestellnummer 166 2200 EDU für 18 Schüler Bestellen Sie 2 Module für 36 Schüler Nur für den Schulgebrauch. 1 Gene in der Flasche Isolieren
Biotechnologie Forscher TM Genes in a Bottle Kit DNA Necklace Module Bestellnummer 166 2200 EDU für 18 Schüler Bestellen Sie 2 Module für 36 Schüler Nur für den Schulgebrauch. 1 Gene in der Flasche Isolieren
Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin. Steffen Blaurock Thomas Zimmermann
 Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin Steffen Blaurock Thomas Zimmermann 1.1 Einleitung Titrationen werden in der chemischen Analytik durchgeführt, um die Stoffmenge
Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin Steffen Blaurock Thomas Zimmermann 1.1 Einleitung Titrationen werden in der chemischen Analytik durchgeführt, um die Stoffmenge
peqgold RNAPure Optimierte Guanidinisothiocyanat/Phenol-Methode für die Extraktion von RNA.
 peqgold RNAPure Optimierte Guanidinisothiocyanat/Phenol-Methode für die Extraktion von RNA. Lot-Nr. Best.-Nr. 30-1010 100 ml 30-1020 200 ml 30-1030 500 ml Lagerung: Lichtgeschützt bei 4 C für 12 Monate
peqgold RNAPure Optimierte Guanidinisothiocyanat/Phenol-Methode für die Extraktion von RNA. Lot-Nr. Best.-Nr. 30-1010 100 ml 30-1020 200 ml 30-1030 500 ml Lagerung: Lichtgeschützt bei 4 C für 12 Monate
Inhaltsverzeichnis. II Erläuterung. DNA-Extraktion aus Tomate
 DNA-Extraktion aus Tomate Inhaltsverzeichnis Erläuterung Seite 2 Materialien Seite 2 Zeitaufwand Seite 3 Praktikumsvorbereitung Seite 3 Laborverfahren Seite 4 II Erläuterung DNA (Desoxyribonukleinsäure)
DNA-Extraktion aus Tomate Inhaltsverzeichnis Erläuterung Seite 2 Materialien Seite 2 Zeitaufwand Seite 3 Praktikumsvorbereitung Seite 3 Laborverfahren Seite 4 II Erläuterung DNA (Desoxyribonukleinsäure)
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Inhalt SEMINAR 1: mit zu bringen ist: 1. DC von Aminosäuren. 2. Pipettierübung (Präzisionskontrolle) 3. Gelfiltration
 SEMINAR 1: mit zu bringen ist: Arbeitsmantel Skriptum Rechner, Bleistift, Lineal... Protokollheft Und darin eingeklebt das Anwesenheitsblatt 1 Inhalt 1. DC von Aminosäuren 2. Pipettierübung (Präzisionskontrolle)
SEMINAR 1: mit zu bringen ist: Arbeitsmantel Skriptum Rechner, Bleistift, Lineal... Protokollheft Und darin eingeklebt das Anwesenheitsblatt 1 Inhalt 1. DC von Aminosäuren 2. Pipettierübung (Präzisionskontrolle)
OLED Herstellung: Elektrolumineszenz mit PVK / TPD als Lochleiter
 FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. OLED Herstellung: Elektrolumineszenz mit PVK / TPD als Lochleiter Versuchsdurchführung: Es sollen mehrere unterschiedliche OLED`s hergestellt
FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. OLED Herstellung: Elektrolumineszenz mit PVK / TPD als Lochleiter Versuchsdurchführung: Es sollen mehrere unterschiedliche OLED`s hergestellt
Fette, Öle und Tenside
 Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Probe- und Vergleichslösungen: Trennschicht (stationäre Phase): Kieselgel. Fließmittel (mobile Phase):
 , der Allrounder aus dem Supermarkt Welche Zucker sind in enthalten? Nachweis mittels Dünnschichtchromatografie (DC) [6] 27.06.03 / 04.07.03 Jessica Bornemann Grundlagen: Für die DC verwendet man Kunststofffolien,
, der Allrounder aus dem Supermarkt Welche Zucker sind in enthalten? Nachweis mittels Dünnschichtchromatografie (DC) [6] 27.06.03 / 04.07.03 Jessica Bornemann Grundlagen: Für die DC verwendet man Kunststofffolien,
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
Arbeitsprotokoll. Proteinanalytik. Stand
 Arbeitsprotokoll Stand 16. 07. 2003 Dieses Protokoll basiert auf folgenden Publikationen: Mass spectrometric sequencing of proteins silver-stained polyacrylamide gels, Shevchenko A, Wilm M, Vorm O, Mann
Arbeitsprotokoll Stand 16. 07. 2003 Dieses Protokoll basiert auf folgenden Publikationen: Mass spectrometric sequencing of proteins silver-stained polyacrylamide gels, Shevchenko A, Wilm M, Vorm O, Mann
Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände
 Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände 5. Bestimmung von Einzelsubstanzen 5.25 Wasserstoffperoxid 1. Allgemeine Angaben H 2
Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände 5. Bestimmung von Einzelsubstanzen 5.25 Wasserstoffperoxid 1. Allgemeine Angaben H 2
Gruppe I : Darstellung und Nachweis von Säuren
 Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
RIDA TUBE Calprotectin
 RIDA TUBE Calprotectin Zubehör für RIDASCREEN Calprotectin Art. No. GZ3016 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 / Telefax: +49 (0) 61 51 81
RIDA TUBE Calprotectin Zubehör für RIDASCREEN Calprotectin Art. No. GZ3016 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 / Telefax: +49 (0) 61 51 81
Entwicklungsbiologie der Pflanzen biol 130
 Entwicklungsbiologie der Pflanzen biol 130 WS 2017/2018 Prof. Dr. Margret Sauter und Mitarbeiter Inhaltsverzeichnis Versuchsplan der einzelnen Kurstage 3 Seite Versuch 1 Auftrennung von Proteinen über
Entwicklungsbiologie der Pflanzen biol 130 WS 2017/2018 Prof. Dr. Margret Sauter und Mitarbeiter Inhaltsverzeichnis Versuchsplan der einzelnen Kurstage 3 Seite Versuch 1 Auftrennung von Proteinen über
Mustervorschrift Versuch
 Mustervorschrift Versuch 10.2.3 N-Acetylierung von D-/L- Methionin (1.Stufe) 5.20 g (34.86 mmol) D-/L- Methionin (racemisch) werden in 51.13 g (48.80 ml, 349 mmol) reiner Essigsäure (Eisessig) gelöst 1.
Mustervorschrift Versuch 10.2.3 N-Acetylierung von D-/L- Methionin (1.Stufe) 5.20 g (34.86 mmol) D-/L- Methionin (racemisch) werden in 51.13 g (48.80 ml, 349 mmol) reiner Essigsäure (Eisessig) gelöst 1.
Zuckernachweis mit Tollens-Reagenz
 Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Versuchsprotokoll Kapitel 6
 Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
DAC-Probe 10. Hochleistungsdünnschichtchromatographie (HPTLC) Einleitung. Allgemeine Angaben
 DAC-Probe 0 Probe_0 DAC-Probe 0 Hochleistungsdünnschichtchromatographie (HPTLC) Sofern in der Monographie nichts anderes angegeben ist, wird die Auftrennung mit den folgenden Angaben durchgeführt: es werden
DAC-Probe 0 Probe_0 DAC-Probe 0 Hochleistungsdünnschichtchromatographie (HPTLC) Sofern in der Monographie nichts anderes angegeben ist, wird die Auftrennung mit den folgenden Angaben durchgeführt: es werden
Pyrophores Eisen. Experimentieranleitung für Schüler/-innen. September Stephan Knébel, Marianne Dietiker, Christoph Meili.
 Bildungsplattform zur Mikro- und Nanotechnologie für Berufsfach- und Mittelschulen sowie Höhere Fachschulen Pyrophores Eisen Experimentieranleitung für Schüler/-innen September 2014 Stephan Knébel, Marianne
Bildungsplattform zur Mikro- und Nanotechnologie für Berufsfach- und Mittelschulen sowie Höhere Fachschulen Pyrophores Eisen Experimentieranleitung für Schüler/-innen September 2014 Stephan Knébel, Marianne
SERVA Lightning Sci2. SERVA Lightning Sci3. SERVA Lightning Sci5. SERVA Lightning SciDye Set
 GEBRAUCHSANLEITUNG SERVA Lightning Sci2 (Kat.-Nr. 43404) SERVA Lightning Sci3 (Kat.-Nr. 43405) SERVA Lightning Sci5 (Kat.-Nr. 43406) SERVA Lightning SciDye Set (Kat.-Nr. 43407) Fluoreszenzfarbstoffe für
GEBRAUCHSANLEITUNG SERVA Lightning Sci2 (Kat.-Nr. 43404) SERVA Lightning Sci3 (Kat.-Nr. 43405) SERVA Lightning Sci5 (Kat.-Nr. 43406) SERVA Lightning SciDye Set (Kat.-Nr. 43407) Fluoreszenzfarbstoffe für
Umschmelzen und Tiefziehen von Polystyrol
 Umschmelzen und Tiefziehen von Heißluftgebläse, Keramiknetz, Tiegelzange, Saugflasche mit Gummiring, Glasfritte, Wasserstrahlpumpe, Stativ mit Muffe und Klammer Joghurtbecher aus (PS) Schutzbrille! Das
Umschmelzen und Tiefziehen von Heißluftgebläse, Keramiknetz, Tiegelzange, Saugflasche mit Gummiring, Glasfritte, Wasserstrahlpumpe, Stativ mit Muffe und Klammer Joghurtbecher aus (PS) Schutzbrille! Das
Nanotechnologie. Schüler- unterlagen. (9-10 Jg.) Bildung für nachhaltige. Entwicklung
 Nanotechnologie Bildung für nachhaltige Entwicklung Schüler- unterlagen (9-10 Jg.) Versuch 1 Herstellung von Zinkoxid (ZnO)-Nanopartikel Materialien: 2 Bechergläser (50 ml, 100 ml), Heizrührer, Magnetrührstäbchen,
Nanotechnologie Bildung für nachhaltige Entwicklung Schüler- unterlagen (9-10 Jg.) Versuch 1 Herstellung von Zinkoxid (ZnO)-Nanopartikel Materialien: 2 Bechergläser (50 ml, 100 ml), Heizrührer, Magnetrührstäbchen,
5 NUKLEINSÄUREN. In diesem Versuch wird ein kommerzielles Plasmid (plitmus38, Firma: NEB, siehe Abbildung) eingesetzt.
 5 NUKLEINSÄUREN Nukleinsäuren sind Polynukleotide, wobei jedes Nukleotid sich aus einem Phosphat, einer Ribose (RNA) oder Desoxyribose (DNA) und einer Purin- oder Pyrimidin-Base zusammensetzt. Die einzelnen
5 NUKLEINSÄUREN Nukleinsäuren sind Polynukleotide, wobei jedes Nukleotid sich aus einem Phosphat, einer Ribose (RNA) oder Desoxyribose (DNA) und einer Purin- oder Pyrimidin-Base zusammensetzt. Die einzelnen
ANALYSE VON SERUMBESTANDTEILEN II
 130 PLATZ 5: ANALYE VON ERUMBETANDTEILEN II Mit der Dialyse wird ein einfaches Prinzip gezeigt, welches bei der Hämodialyse in der Medizin zur Anwendung gelangt. Im weiteren wird in diesem wie im vorangegangenen
130 PLATZ 5: ANALYE VON ERUMBETANDTEILEN II Mit der Dialyse wird ein einfaches Prinzip gezeigt, welches bei der Hämodialyse in der Medizin zur Anwendung gelangt. Im weiteren wird in diesem wie im vorangegangenen
(Nur für die Forschung) Bei Kontakt mit Augen oder Haut sofort mit viel Wasser abspülen!
 Datenblatt Artikel-Nr. 56.200.0010 10 Aufreinigungen 56.200.0050 50 Aufreinigungen 56.200.0250 250 Aufreinigungen (Nur für die Forschung) Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und
Datenblatt Artikel-Nr. 56.200.0010 10 Aufreinigungen 56.200.0050 50 Aufreinigungen 56.200.0250 250 Aufreinigungen (Nur für die Forschung) Sicherheitsanweisungen Bitte gehen Sie mit allen Materialien und
Stelle pflanzliche Farbstoffe her, die zur Säureidentifizierung dienen können.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757200).3 Pflanzliche Farbstoffe dienen als Indikatoren Experiment von: Phywe Gedruckt: 5.0.203 :9:42 intertess (Version 3.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757200).3 Pflanzliche Farbstoffe dienen als Indikatoren Experiment von: Phywe Gedruckt: 5.0.203 :9:42 intertess (Version 3.06 B200, Export
8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung
 8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
Schulversuchspraktikum. Isabel Großhennig. Sommersemester Klassenstufen 11 & 12. Farbstoffe. Kurzprotokoll
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P )
 Lehrer-/Dozentenblatt Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P757000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
Lehrer-/Dozentenblatt Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P757000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
Hämoglobinbestimmung
 Hämoglobinbestimmung TEAS Themen Erythrozyten, Photometrie, Hämoglobin, Cyanhämoglobin, Oxyhämoglobin, Carboxyhämoglobin, Methämoglobin, Anämie. Prinzip Eine quantitative Hämoglobinbestimmung ist unerlässlich,
Hämoglobinbestimmung TEAS Themen Erythrozyten, Photometrie, Hämoglobin, Cyanhämoglobin, Oxyhämoglobin, Carboxyhämoglobin, Methämoglobin, Anämie. Prinzip Eine quantitative Hämoglobinbestimmung ist unerlässlich,
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
