Einführung Risiko- minimierender Maßnahmen zur Prävention von West Nil Virus- Übertragung durch nicht pathogen-inaktivierte Blutkomponenten
|
|
|
- Astrid Kruse
- vor 5 Jahren
- Abrufe
Transkript
1 Paul-Ehrlich-Institut Postfach Langen PD Dr. med. Markus Funk Fachgebietsleiter Pharmakovigilanz II An alle Inhaber einer Zulassung von zellulären Blutzubereitungen und therapeutischem Frischplasma (gefrorenes Frischplasma GFP und lyophilisiertes Plasma aus Einzelspenden) Telefon / Phone 0+49 (0) Fax +49 (0) pharmakovigilanz2@pei.de 16. November 2011 Abwehr von Arzneimittelrisiken Stufenplan Stufe I: wissenschaftlicher Informationsaustausch Einführung Risiko- minimierender Maßnahmen zur Prävention von West Nil Virus- Übertragung durch nicht pathogen-inaktivierte Blutkomponenten Sehr geehrte Damen und Herren, in den vergangenen Jahren wurde eine zunehmende Anzahl von West Nil Virus (WNV)-Infektionen beim Menschen im Mittelmeerraum (Israel, Italien, Griechenland und Nordafrika) sowie in Rumänien, Ungarn, Russland und einigen Zentralasiatischen Staaten gemeldet. Die Infektionen werden sowohl von WNV der Linie 1 wie auch der Linie 2 hervorgerufen. Bei einem kleinen Teil der Infizierten kam es zu schwerwiegenden Verläufen. Das European Centre for Diesease Prevention and Control (ECDC) dokumentiert mittlerweile die Meldungen der europäischen Länder auf seiner Internetseite ( und benennt einzelne europäische Regionen, u. a. in Griechenland, Rumänien, Österreich und Italien, in denen es zu einer Häufung autochthoner WNV- Neuinfektionen gekommen ist. In den Gremien der Europäischen Kommission wird daher eine intensive Diskussion über das aktuelle Gefährdungspotential und die Einführung präventiver Maßnahmen zur Risikominimierung von West Nil Virus-Übertragungen durch Blutkomponenten geführt. Das Paul-Ehrlich-Institut möchte daher mit Ihnen in einen Informationsaustausch treten, um die Notwendigkeit und Durchführbarkeit Risiko-minimierender Maßnahmen besser einschätzen zu können. Aktueller Kenntnisstand Während eine WNV-Infektion nach der Entscheidung der Europäischen Kommission (2009/312/EC) eine meldepflichtige Erkrankung darstellt, besteht in Deutschland gemäß dem
2 Infektionsschutzgesetz keine Meldepflicht. Dem RKI liegen daher offiziell keine Daten zu WNV- Neuinfektionen vor. Bisher wurde jedoch in Deutschland kein Fall einer autochthonen WNV- Neuinfektion bekannt. Fälle von importierten WNV-Infektionen wurden 2003 (USA) und 2004 (USA, Irland) gemeldet. In den letzten Jahren ist aber kein weiterer Fall bekannt geworden. Eine Untersuchung des Paul-Ehrlich-Instituts aus den Jahren 2004 und 2005 von ca Blutspenden in Hessen und Österreich ergab eine niedrige Rate von serologisch positiven Spendern [Pfleiderer et al., 2006, 2008.]. Die Anzahl der bestätigten WNV positiven Ergebnisse entsprachen einer Rate von 0,03% aller untersuchten Spenden. Bei dem PCR-Screening von Spenden gelang in keinem Fall der Nachweis des WNV-Genoms [Pfleiderer et al., 2008], so dass keine akute WNV-Infektion bestätigt werden konnte. Aktuelle Daten zur WNV-Infektion bei Spendern in deutschen Blutspende-Einrichtungen liegen dem PEI nicht vor. Die Untersuchung von Immunglobulinpräparaten, die in den Jahren aus Plasmaspenden deutscher, österreichischer und tschechischer Spender hergestellt wurden, ergab hingegen einen Anstieg der WNV- Antikörper-Titer für den Zeitraum 2009 und 2010 [Rabel et al., 2011]. Diese Daten deuten auf eine Zunahme der Serokonversionen bei europäischen Spendern hin. Die meisten WNV-Infektionen (ca. 80%) verlaufen beim Menschen asymptomatisch. Bei etwa 20% der Infizierten kommt es nach einer Inkubationszeit von 2 14 Tagen zu einer selbst-limitierenden fieberhaften Erkrankung mit Symptomen eines grippalen Infekts (Unwohlsein, Kopf- und Muskelschmerzen, Übelkeit, Erbrechen, etc.). Bei weniger als einem Prozent der Infizierten kommt es zum Auftreten von neurologischen Symptomen (Meningitis, Enzephalitis, Paresen etc.) [DeBiasi, 2011]. Von schweren Verläufen mit neurologischer Symptomatik sind vor allem ältere Patienten (> 70 Jahre) und Patienten mit einer Immunschwäche betroffen. In dieser Gruppe kam es bei 4% bis 14% zu tödlichen Verläufen der Infektion [Lindsey et al., 2010]. Bedeutung für die Sicherheit von nicht inaktivierten Blutkomponenten Mit der Ausbreitung der WNV-Infektion in Nordamerika wurden von den Einrichtungen der American Blood Centers 23 transfusionsvermittelte WNV-Infektionen für das Jahr 2002 gemeldet. Die Blutkomponenten stammten von Spendern, die zum Zeitpunkt der Blutspende keine Krankheitssymptome aufwiesen [Tobler et al., 2005]. Aufgrund dieser WNV-Transmissionen wurde in den Vereinigten Staaten Ende Juni 2003 die Minipool-Testung auf WNV-Genom eingeführt [Stramer et al., 2005]. Trotz der Einführung der NAT-Testung kam es jedoch in einzelnen Fällen zu WNV-Transmissionen durch Spenden, die eine niedrige Viruskonzentration aufwiesen [Busch et al., 2005; CDC, 2007]. Bei den Untersuchungen der amerikanischen Blutspendeeinrichtungen fanden sich maximale Viruskonzentrationen von Genomäquivalenten/ml [Stramer et al., 2005; Zou et al., 2010]. Aufgrund der bisweilen vergleichsweise geringen Viruskonzentrationen frisch infizierter aber infektiöser Spender werden in amerikanischen und kanadischen Blutspendeeinrichtungen ausschließlich Minipools mit einer Größe von sechs bis maximal sechzehn Spender untersucht, Seite 2/5
3 abhängig vom verwendeten Testsystem. In Regionen mit einer erhöhten WNV-Inzidenz wird zudem die Einzelspendentestung empfohlen [Cameron et al., 2005; Vamvakas et al. 2006]. Um eine WNV-Transmission durch Blutkomponenten in Deutschland weitgehend auszuschließen, hat das PEI mit dem Bescheid vom 02. September 2003 eine zeitlich befristete Spenderrückstellung vorgeschrieben. Rückkehrende aus den USA, Kanada und Mittelamerika müssen in der Zeit zwischen 1. Mai und 31. Oktober jedes Jahres mindestens für 28 Tage von der Blutspende ausgeschlossen werden. Andere insbesondere europäische Länder waren bisher von dieser Maßnahme nicht betroffen. Präventive Maßnahmen Als Präventivmaßnahmen bieten sich grundsätzlich eine zeitlich befristete Spenderrückstellung oder die gezielte Spendertestung an. Die Anordnung einer Rückstellung von Spendern aus europäischen Gebieten mit einer Häufung von WNV-Neuinfektionen wäre eine kurzfristig zu realisierende Maßnahme. Die organisatorische Umsetzung sollte jedoch im Detail diskutiert werden. So müssen europäische Inzidenzgebiete definiert und fortlaufend dem aktuellen Erkenntnisstand angepasst werden. Auf der ECDC- Internetseite ( werden sowohl die Regionen mit einer erhöhten Anzahl von WNV-Infektionen in einem definiertem Zeitraum (z. B. Gebiete mit Fälle für die Monate Juli/September 2010) wie auch die aktualisierten Daten der Neuinfektionen in Europa (z. B ) dargestellt. Die Spenderrückstellung könnte somit auf die Regionen beschränkt werden, bei denen von der ECDC eine höhere Melderate gezeigt wurde. Bei dieser Regelung läge es in der Verantwortung des Inhabers der Zulassung bzw. Pharmazeutischen Unternehmers, die Kriterien zur Rückstellung eines Spenders der jeweiligen aktuellen Entwicklung anzupassen. Es ist zu erwarten, dass in den kommenden Jahren aufgrund weiterer epidemiologischer Untersuchungen die Anzahl der betroffenen Regionen zunehmen wird. Als zweite mögliche Maßnahme ist die Spendertestung zu diskutieren, wie sie in Nordamerika bereits umgesetzt wurde. Eine Einzel-Spendertestung mit einem Antikörpersuchtest stellt hierbei keine sinnvolle präventive Maßnahme dar, da positive Testergebnisse erst nach dem Abklingen der akuten WNV-Infektion (virämische Phase) zu erwarten sind. So ist bei der Mehrzahl der Patienten (90%) etwa acht Tage nach Symptombeginn das Auftreten von IgM-Antikörpern zu erwarten. Bei der Einführung einer NAT-Minipool-Testung müsste darauf geachtet werden, dass der verwendete NAT-Test die bekannten WNV-Sequenzen erfasst (WNV Linie 1 und Linie 2 sowie deren Subgruppen). Weiterhin sollten alle bekannten Varianten mit vergleichbarer Sensitivität und Spezifität detektiert werden. Entsprechend den Erfahrungen aus den USA und Kanada sollte die Größe der untersuchten Minipools von der Sensitivität des eingesetzten NAT-Tests abhängen und bis auf maximal Seite 3/5
4 sechzehn Spender beschränkt bleiben. Bei Rückkehrern aus Gebieten mit sehr hoher Inzidenz wäre eine Einzelspendertestung am effektivsten. Informationsaustausch Wie bereits dargestellt soll bei dem angestrebten Informationsaustausch sowohl die Notwendigkeit wie auch die Durchführbarkeit möglicher Maßnahmen diskutiert werden. Wir bitten Sie daher die folgenden Fragen zu beantworten. 1. Wäre es für Blutspendeeinrichtungen vertretbar, aktuelle Informationen über das Auftreten von WNV- Infektionen in Europa aus dem Internet zu beziehen (z. B. ECDC- Homepage)? 2. Wäre es sinnvoll, die Entscheidung zur Spenderrückstellung von einer Häufung der gemeldeten Erkrankungen in den betroffenen Regionen abhängig zu machen? 3. Können Sie abschätzen, wie viele Spender (in %) in den Monaten Mai bis Oktober von einer generellen Rückstellung aller Reiserückkehrer aus Südeuropa betroffen wären? 4. Ist die Blutversorgung im Falle einer zeitlich begrenzten Rückstellung von der Spende (28 Tage) nach Reisen in betroffene Gebiete in den Monaten Mai bis Oktober gewährleistet oder sind Engpässe z.b. für seltene Blutgruppen zu erwarten? 5. Halten Sie eine Testung von Reiserückkehrern auf WNV-RNA mittels NAT (Minipool- oder Einzelspender-Testung) in Ihrer Einrichtung für durchführbar bzw. praktikabel? 6. Haben Sie bereits Erfahrungen mit dieser Testung gemacht (Kosten, organisatorischer Aufwand)? 7. Halten Sie die Durchführung einer epidemiologischen Untersuchung (Surveillance) in definierten Blutspendeeinrichtungen für sinnvoll, um aktuelle Daten zu der Häufigkeit von WNV sero-positiven bzw. RNA-positiven Spendern zu erhalten? Werden solche Untersuchungen bei Ihnen im Rahmen von Forschungsprojekten gegebenenfalls bereits durchgeführt? Wir bitten Sie, die Fragen bis zum zu beantworten. Mit freundlichen Grüßen Im Auftrag Dr. med. M. Funk Fachgebietsleiter Pharmakovigilanz II, Paul-Ehrlich-Institut Seite 4/5
5 Literatur Busch MP, Caglioti S, Robertson EF et al. (2005) Screening the blood supply for West Nile virus RNA by nucleic acid amplification testing. N Engl J Med 353: Cameron C, Reeves J, Antonishyn N et al. (2005) West Nile virus in Canadian blood donors. Transfusion 45: CDC, Centers for Disease Control and Prevention (2007) West Nile virus transmission through blood transfusion--south Dakota, MMWR Morb Mortal Wkly Rep 56:76 79 DeBiasi RL (2011) West Nile virus neuroinvasive disease. Curr Infect Dis Rep 13: EMEA, European Agency for the Evaluation of Medicinal Products. CPMP position statement on west nile virus and plasma-derived medicinal products, EMEA/CPMP/BWP/3752/03, London, 25 July pdf es/west_niles_fever_risk_maps.aspx. Lindsey NP, Staples JE, Lehman JA, Fischer M (2010) Surveillance for human West Nile virus disease United States, MMWR Surveill Summ 59:1 17 MMWR 51(43); ). Public Health Dispatch: Investigations of West Nile Virus Infections in Recipients of Blood Transfusions November 1, 2002 Pfleiderer C, König C, Chudy M, Schmidt M, Roth WK, Nübling CM (2006) Molecular epidemiology of West Nile Virus in humans. Dev Biol (Basel) 126: ; discussion Pfleiderer C, Blümel J, Schmidt M et al. (2008) West Nile virus and blood product safety in Germany. J Med Virol 80: Rabel PO, Planitzer CB, Farcet MR et al. (2011) Increasing West Nile virus antibody titres in central European plasma donors from 2006 to Euro Surveill 16:pii=19812 Stramer SL, Fang CT, Foster GA, Wagner AG, Brodsky JP, Dodd RY (2005) West Nile virus among blood donors in the United States, 2003 and N Engl J Med 353: Tobler LH, Bianco C, Glynn SA et al.; NHLBI Retrovirus Epidemiology Study (REDS) (2005) Detection of West Nile virus RNA and antibody in frozen plasma components from a voluntary market withdrawal during the 2002 peak epidemic. Transfusion 45: Vamvakas EC, Kleinman S, Hume H, Sher GD (2006) The development of West Nile virus safety policies by Canadian blood services: guiding principles and a comparison between Canada and the United States. Transfus Med Rev 20: Zou S, Foster GA, Dodd RY, Petersen LR, Stramer SL (2010) West Nile fever characteristics among viremic persons identified through blood donor screening. J Infect Dis 202: Seite 5/5
Stufenplanverfahren (Bescheide) des Paul-Ehrlich-Instituts zu Zika-Virus, West-Nil-Virus, Chikungunya-Virus und Prionen; Plasmodien.
 Paul-Ehrlich-Institut Postfach 63207 Langen Der Präsident An alle pharmazeutischen Unternehmer von Blutkomponenten, Stammzellen und gefrorenem Frischplasma Ansprechpartner/in: Prof. Dr. M. Funk Telefon:
Paul-Ehrlich-Institut Postfach 63207 Langen Der Präsident An alle pharmazeutischen Unternehmer von Blutkomponenten, Stammzellen und gefrorenem Frischplasma Ansprechpartner/in: Prof. Dr. M. Funk Telefon:
Einführung Risiko- minimierender Maßnahmen zur Prävention einer Hepatitis E Virus- Übertragung durch nicht pathogen-inaktivierte Blutkomponenten
 Paul-Ehrlich-Institut Postfach 63207 Langen Prof. Dr. med. Markus Funk Fachgebietsleiter Pharmakovigilanz II An alle Inhaber einer Zulassung von zellulären Blutzubereitungen und therapeutischem Frischplasma
Paul-Ehrlich-Institut Postfach 63207 Langen Prof. Dr. med. Markus Funk Fachgebietsleiter Pharmakovigilanz II An alle Inhaber einer Zulassung von zellulären Blutzubereitungen und therapeutischem Frischplasma
hier: Abwehr von Arzneimittelrisiken Testung auf Antikörper gegen Hepatitis-B-Core-Antigen (anti-hbc) im Blutspendewesen
 Paul-Ehrlich-Institut Postfach 63207 Langen An die Inhaber der Zulassung von zellulären Blutkomponenten und gefrorenem Frischplasma sowie Inhaber von Genehmigungen von allogenen Stammzellzubereitungen
Paul-Ehrlich-Institut Postfach 63207 Langen An die Inhaber der Zulassung von zellulären Blutkomponenten und gefrorenem Frischplasma sowie Inhaber von Genehmigungen von allogenen Stammzellzubereitungen
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 14/18
 VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 4/8 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle, Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp, Prof. Dr. E. Puchhammer Redaktion:
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 4/8 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle, Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp, Prof. Dr. E. Puchhammer Redaktion:
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 21/18
 VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 2/8 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle, Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp, Prof. Dr. E. Puchhammer Redaktion:
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 2/8 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle, Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp, Prof. Dr. E. Puchhammer Redaktion:
West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren
 West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren 100 nm HEV, Abb.: Center of Disease Control and Prevention WNV, Abb.: Dr. H. Gelderblohm, RKI Institut für Transfusionsmedizin
West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren 100 nm HEV, Abb.: Center of Disease Control and Prevention WNV, Abb.: Dr. H. Gelderblohm, RKI Institut für Transfusionsmedizin
Abwehr von Arzneimittelrisiken Stufenplanverfahren Stufe 2 Testung auf Antikörper gegen Hepatitis B-Core-Antigen (anti-hbc) im Blutspendewesen
 An alle pharmazeutischen Einrichtungen, die Blut oder Blutkomponente gewinnen oder herstellen S1-23 600 06103 / 77-1023 06103 / 77-1263 30.03.2006 Abwehr von Arzneimittelrisiken Stufenplanverfahren Stufe
An alle pharmazeutischen Einrichtungen, die Blut oder Blutkomponente gewinnen oder herstellen S1-23 600 06103 / 77-1023 06103 / 77-1263 30.03.2006 Abwehr von Arzneimittelrisiken Stufenplanverfahren Stufe
15. FSME (Frühsommer-Meningo-Encephalitis) Tick-borne Encephalitis (TBE)
 1 15. FSME (Frühsommer-Meningo-Encephalitis) Tick-borne Encephalitis (TBE) Die FSME ist eine durch Viren hervorgerufene Erkrankung des zentralen Nervensystems. Entsprechend der Verbreitung werden drei
1 15. FSME (Frühsommer-Meningo-Encephalitis) Tick-borne Encephalitis (TBE) Die FSME ist eine durch Viren hervorgerufene Erkrankung des zentralen Nervensystems. Entsprechend der Verbreitung werden drei
Erfahrungen zu Rückverfolgungsverfahren bei Anti-HBc Serokonversion
 Erfahrungen zu Rückverfolgungsverfahren bei Anti-HBc Serokonversion KOLT 2011 Paul - Ehrlich - Institut W. Sireis, I. Helman, A. Vornwald, T. Dengler, U. Mayr - Wohlfart, M. Schmidt DRK Blutspendedienst
Erfahrungen zu Rückverfolgungsverfahren bei Anti-HBc Serokonversion KOLT 2011 Paul - Ehrlich - Institut W. Sireis, I. Helman, A. Vornwald, T. Dengler, U. Mayr - Wohlfart, M. Schmidt DRK Blutspendedienst
Votum 42 AK Blut und Überarbeitung Stufenplan zur Anti-HBc-Testung
 www.pei.de Votum 42 AK Blut und Überarbeitung Stufenplan zur Anti-HBc-Testung M. Heiden Abklärung eines initial reaktiven Anti-HBc bei negativem HBsAg Freigabe von Blutkomponenten möglich, sofern eindeutig
www.pei.de Votum 42 AK Blut und Überarbeitung Stufenplan zur Anti-HBc-Testung M. Heiden Abklärung eines initial reaktiven Anti-HBc bei negativem HBsAg Freigabe von Blutkomponenten möglich, sofern eindeutig
Department für Virologie
 ZikaVirus Stephan Aberle, Medizinsiche Universität Wien Nationale Referenzzentrale für Arboviren Zika Virus Flavivirus Nah verwandt mit Dengue, West Nil, Gelbfieber, FSME Virus Zwei Subtypen: afrikanisch
ZikaVirus Stephan Aberle, Medizinsiche Universität Wien Nationale Referenzzentrale für Arboviren Zika Virus Flavivirus Nah verwandt mit Dengue, West Nil, Gelbfieber, FSME Virus Zwei Subtypen: afrikanisch
West Nil Fieber beim Menschen in Österreich
 West Nil Fieber beim Menschen in Österreich Stephan Aberle Department für Virologie Nationale Referenzzentrale für Flaviviren Franz X. Heinz, Karin Stiasny Medizinische Universität Wien West Nil Virus
West Nil Fieber beim Menschen in Österreich Stephan Aberle Department für Virologie Nationale Referenzzentrale für Flaviviren Franz X. Heinz, Karin Stiasny Medizinische Universität Wien West Nil Virus
Evaluierung der derzeit angeordneten Spendertestungen auf virale Marker
 www.pei.de Evaluierung der derzeit angeordneten Spendertestungen auf virale Marker 4. Sitzung der DGTI Sektion Sicherheit von Blutprodukten 27.-28.03.2014 Lübeck - Travemünde Michael Chudy Molekulare Virologie
www.pei.de Evaluierung der derzeit angeordneten Spendertestungen auf virale Marker 4. Sitzung der DGTI Sektion Sicherheit von Blutprodukten 27.-28.03.2014 Lübeck - Travemünde Michael Chudy Molekulare Virologie
Ergebnisprotokoll des Expertengesprächs am im Paul-Ehrlich-Institut (PEI)
 Ergebnisprotokoll des Expertengesprächs am 08.06.2011 im Paul-Ehrlich-Institut (PEI) Sitzungsleitung: Prof. K. Cichutek Teilnehmer: Vertreter des Paul-Ehrlich-Institutes: Prof. K. Cichutek, Prof. R. Seitz,
Ergebnisprotokoll des Expertengesprächs am 08.06.2011 im Paul-Ehrlich-Institut (PEI) Sitzungsleitung: Prof. K. Cichutek Teilnehmer: Vertreter des Paul-Ehrlich-Institutes: Prof. K. Cichutek, Prof. R. Seitz,
Look back Kommunikation zwischen Anwender & Pharmazeutischem Hersteller
 Look back Kommunikation zwischen Anwender & Pharmazeutischem Hersteller Blutspendedienst des BRK Dr. Petra Michel Stufenplanbeauftragte Hannover, 27. September 2011 Rückverfolgung Regulatorische Vorgaben
Look back Kommunikation zwischen Anwender & Pharmazeutischem Hersteller Blutspendedienst des BRK Dr. Petra Michel Stufenplanbeauftragte Hannover, 27. September 2011 Rückverfolgung Regulatorische Vorgaben
Mitteilung des Arbeitskreises Blut des Bundesministeriums für Gesundheit und Soziale Sicherung
 Mitteilung des Arbeitskreises Blut des Bundesministeriums für Gesundheit und Soziale Sicherung Bei der 58. Sitzung des Arbeitskreises Blut am 17.03.2005 wurde folgendes Votum (V 31) verabschiedet: Erhöhung
Mitteilung des Arbeitskreises Blut des Bundesministeriums für Gesundheit und Soziale Sicherung Bei der 58. Sitzung des Arbeitskreises Blut am 17.03.2005 wurde folgendes Votum (V 31) verabschiedet: Erhöhung
Stufenplan zur Anti-HBc-Testung und Votum 42 AK Blut
 www.pei.de Stufenplan zur Anti-HBc-Testung und Votum 42 AK Blut M. Heiden DGTI Sektion Sicherheit von Blutprodukten Bad Oeynhausen, 21.03.2013 Antikörper gegen Hepatitis-B-Core-Antigen Epidemiologischer
www.pei.de Stufenplan zur Anti-HBc-Testung und Votum 42 AK Blut M. Heiden DGTI Sektion Sicherheit von Blutprodukten Bad Oeynhausen, 21.03.2013 Antikörper gegen Hepatitis-B-Core-Antigen Epidemiologischer
FSME (Frühsommermeningoenzephalitis) West-Nil-Virus (WNV) West-Nil-Virus Foto: CNN
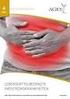 FSME (Frühsommermeningoenzephalitis) West-Nil-Virus (WNV) 95 West-Nil-Virus Foto: CNN West-Nil-Virus (WNV) DEFINITION Das West Nile Fieber ist eine wenig charakteristische grippeartige Infektion, die von
FSME (Frühsommermeningoenzephalitis) West-Nil-Virus (WNV) 95 West-Nil-Virus Foto: CNN West-Nil-Virus (WNV) DEFINITION Das West Nile Fieber ist eine wenig charakteristische grippeartige Infektion, die von
Neue Studie über unerwartete Auswirkung der Hepatitis-B-Impfung
 Impfstoff-Egoismus mit Folgen Neue Studie über unerwartete Auswirkung der Hepatitis-B-Impfung Gießen (20. Januar 2011) - Ein internationales Forscherteam, darunter die Virusforscher Ulrike Wend und Wolfram
Impfstoff-Egoismus mit Folgen Neue Studie über unerwartete Auswirkung der Hepatitis-B-Impfung Gießen (20. Januar 2011) - Ein internationales Forscherteam, darunter die Virusforscher Ulrike Wend und Wolfram
HIV-Postexpositionsprophylaxe beim Krankenhauspersonal
 HIV-Postexpositionsprophylaxe beim Krankenhauspersonal Stefanie Döbele 16. Symposium Infektionsmedizin in Tübingen 10. März 2018 Übertragungsmöglichkeiten im Gesundheitsbereich Relevant: Blut, blutige
HIV-Postexpositionsprophylaxe beim Krankenhauspersonal Stefanie Döbele 16. Symposium Infektionsmedizin in Tübingen 10. März 2018 Übertragungsmöglichkeiten im Gesundheitsbereich Relevant: Blut, blutige
Die CMV-Infektion bei Blutspendern und Patienten
 Die CMV-Infektion bei Blutspendern und Patienten Holger Hennig PEI - KOLT 11.05.2011 Das Humane Cytomegalovirus (HCMV) CMV CMV ist ein Herpesvirus DNA im Viruspartikel linear, in der Wirtszelle zirkulär,
Die CMV-Infektion bei Blutspendern und Patienten Holger Hennig PEI - KOLT 11.05.2011 Das Humane Cytomegalovirus (HCMV) CMV CMV ist ein Herpesvirus DNA im Viruspartikel linear, in der Wirtszelle zirkulär,
Die Epidemiologie von HIV in der
 Induction of HIV-1 broadly neutralizing antibodies: The role of host Schweiz and viral determinants Die Epidemiologie von HIV in der Roger D. Kouyos Klinik für Infektionskrankheiten und Spitalhygiene roger.kouyos@usz.ch
Induction of HIV-1 broadly neutralizing antibodies: The role of host Schweiz and viral determinants Die Epidemiologie von HIV in der Roger D. Kouyos Klinik für Infektionskrankheiten und Spitalhygiene roger.kouyos@usz.ch
USUTU-VIRUS. AGES - Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH
 USUTU-VIRUS AGES - Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH www.ages.at WAS IST DAS USUTU-VIRUS? Das Usutu-Virus ist ein Flavivirus und gehört zum Antigenkomplex des Japan-Enzephalitis
USUTU-VIRUS AGES - Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH www.ages.at WAS IST DAS USUTU-VIRUS? Das Usutu-Virus ist ein Flavivirus und gehört zum Antigenkomplex des Japan-Enzephalitis
Ergänzende Empfehlungen zur Testung von Blut- und Plasmaspenden und zum Rückverfolgungsverfahren
 Bundesgesundheitsbl - Gesundheitsforsch - Gesundheitsschutz 1999 42: 888 892 Springer-Verlag 1999 Bekanntmachung des Arbeitskreises Blut des Bundesministeriums für Gesundheit Bei der 34. Sitzung des Arbeitskreis
Bundesgesundheitsbl - Gesundheitsforsch - Gesundheitsschutz 1999 42: 888 892 Springer-Verlag 1999 Bekanntmachung des Arbeitskreises Blut des Bundesministeriums für Gesundheit Bei der 34. Sitzung des Arbeitskreis
Tropenmedizin und Reisemedizin
 Fortbildung 14.03.2019 Tropenmedizin und Reisemedizin KANTONALE AERZTEGESELLSCHAFT SCHAFFHAUSEN KANTONSSPITAL SCHAFFHAUSEN Fortbildungskommission 08.15 Begrüssung Dr. med. Alex Crivelli 08.20 08.50 Fall
Fortbildung 14.03.2019 Tropenmedizin und Reisemedizin KANTONALE AERZTEGESELLSCHAFT SCHAFFHAUSEN KANTONSSPITAL SCHAFFHAUSEN Fortbildungskommission 08.15 Begrüssung Dr. med. Alex Crivelli 08.20 08.50 Fall
CMV in Plasma. Dr. Marijke Weber-Schehl
 CMV in Plasma Dr. Marijke Weber-Schehl Inhalt Nachweis von HCMV in Plasma Ergebnisse Spenderscreening CMV und Plasmaprodukte Weber-Schehl 2 Weber-Schehl 3 Strategie Vermeidung von CMV-Infektionen durch
CMV in Plasma Dr. Marijke Weber-Schehl Inhalt Nachweis von HCMV in Plasma Ergebnisse Spenderscreening CMV und Plasmaprodukte Weber-Schehl 2 Weber-Schehl 3 Strategie Vermeidung von CMV-Infektionen durch
Erfahrungen mit dem Anti-HBc-Stufenplan 2006
 Erfahrungen mit dem Anti-HBc-Stufenplan 2006 Notwendigkeit der Anti-HBc-Testung lt. Votum 31 des AK Blut Anti-HBc auch vorhanden, wenn HBsAg-Bildung gering oder/und Escape-Mutanten vorliegen USA: 0,24
Erfahrungen mit dem Anti-HBc-Stufenplan 2006 Notwendigkeit der Anti-HBc-Testung lt. Votum 31 des AK Blut Anti-HBc auch vorhanden, wenn HBsAg-Bildung gering oder/und Escape-Mutanten vorliegen USA: 0,24
Neuigkeiten bei CMV / Herpes Panel, Enterovirus 68 Ausbruch in Nordamerika
 Neuigkeiten bei CMV / Herpes Panel, Influenza / respiratorische Viren, sowie Enterovirus 68 Ausbruch in Nordamerika Dr. Johannes Kehle Seminar Molekulare Diagnostik 2014 Hotel Fleming s Wien-Westbahnhof
Neuigkeiten bei CMV / Herpes Panel, Influenza / respiratorische Viren, sowie Enterovirus 68 Ausbruch in Nordamerika Dr. Johannes Kehle Seminar Molekulare Diagnostik 2014 Hotel Fleming s Wien-Westbahnhof
Update Virologie Was ist relevant für das Blutspendewesen? Virologie
 Update Virologie Was ist relevant für das Blutspendewesen? 1 Transfusionsmedizin 1981 HIV!! 1989 HCV! 1999 WNV Influenza- alle Jahre wieder Pandemie- Alarm HTLV regional begrenztes Problem ( cave Migration)
Update Virologie Was ist relevant für das Blutspendewesen? 1 Transfusionsmedizin 1981 HIV!! 1989 HCV! 1999 WNV Influenza- alle Jahre wieder Pandemie- Alarm HTLV regional begrenztes Problem ( cave Migration)
Abschlussbericht über die Erstellung eines Merkblatts HIV-Test in der Schwangerschaft
 Erstellung eines Merkblatts für die Schwangere zur Unterstützung des ärztlichen Aufklärungsgespräches über die HIV-Testung im Rahmen der Mutterschafs-Richtlinie des G-BA Abschlussbericht über die Erstellung
Erstellung eines Merkblatts für die Schwangere zur Unterstützung des ärztlichen Aufklärungsgespräches über die HIV-Testung im Rahmen der Mutterschafs-Richtlinie des G-BA Abschlussbericht über die Erstellung
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 02/18
 VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 02/18 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle, Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp, Prof. Dr. E. Puchhammer Redaktion:
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 02/18 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle, Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp, Prof. Dr. E. Puchhammer Redaktion:
Meldungen unerwünschter Wirkungen an das PEI
 Meldungen unerwünschter Wirkungen an das PEI Brigitte Keller-Stanislawski Markus Funk Annette Lohmann Paul-Ehrlich-Str. 5-59 635 Langen arzneimittelsicherheit@pei.de http://www.pei.de Hämovigilanz in Deutschland
Meldungen unerwünschter Wirkungen an das PEI Brigitte Keller-Stanislawski Markus Funk Annette Lohmann Paul-Ehrlich-Str. 5-59 635 Langen arzneimittelsicherheit@pei.de http://www.pei.de Hämovigilanz in Deutschland
Für Sie gelesen: Mitteilung* der European Centre for Disease Prevention and Control (ECDC) in Stockholm
 Seite 1 von 5 20.01.2015 1. Ausgabe 2015 Für Sie gelesen: Mitteilung* der European Centre for Disease Prevention and Control (ECDC) in Stockholm * http://www.ecdc.europa.eu/en/pages/home.aspx Mit der Überschrift
Seite 1 von 5 20.01.2015 1. Ausgabe 2015 Für Sie gelesen: Mitteilung* der European Centre for Disease Prevention and Control (ECDC) in Stockholm * http://www.ecdc.europa.eu/en/pages/home.aspx Mit der Überschrift
nachrichtlich: an alle Stufenplanbeteiligte. Anlagen
 Paul-Ehrlich-Institut Postfach 63207 Langen An alle Inhaber der Zulassung von zellulären Blutzubereitungen und therapeutischem Einzelplasma sowie Inhaber der Genehmigung von Stammzellen zur hämatopoietischen
Paul-Ehrlich-Institut Postfach 63207 Langen An alle Inhaber der Zulassung von zellulären Blutzubereitungen und therapeutischem Einzelplasma sowie Inhaber der Genehmigung von Stammzellen zur hämatopoietischen
Screening zur Prävention von transfusionsübertragenen viralen Infektionen
 Screening zur Prävention von transfusionsübertragenen viralen Infektionen Christoph Niederhauser CNI/2010 Hämovigilanztagung Bern 2010 1 Topics Sicherheit von Blutprodukten bezüglich Infektionserregern
Screening zur Prävention von transfusionsübertragenen viralen Infektionen Christoph Niederhauser CNI/2010 Hämovigilanztagung Bern 2010 1 Topics Sicherheit von Blutprodukten bezüglich Infektionserregern
ZIKA-Virusinfektion Version3 vom Vorgehen bei Verdacht auf ZIKA Virusinfektion
 Vorgehen bei Verdacht auf ZIKA Virusinfektion Verbreitung des ZIKA Virus Häufig gestellte Fragen 1. Was ist das Zikavirus? - Meist von Mücken (Aedes) übertragene Viruserkrankung - Bei Kindern im Mutterleib
Vorgehen bei Verdacht auf ZIKA Virusinfektion Verbreitung des ZIKA Virus Häufig gestellte Fragen 1. Was ist das Zikavirus? - Meist von Mücken (Aedes) übertragene Viruserkrankung - Bei Kindern im Mutterleib
Chlamydia MIF IgG. Leistungsmerkmale. Produktnummer: IF1250G Rev. J. Nicht für den Vertrieb in den USA
 Produktnummer: IF1250G Rev. J Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Produktnummer: IF1250G Rev. J Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Epidemiologie - Aktuelle Daten zu Infektionen bei Blut- und Plasmaspendern
 Epidemiologie - Aktuelle Daten zu Infektionen bei Blut- und Plasmaspendern XV. Fortbildungsveranstaltung der ARGE Plasmapherese e.v., 20.-21.11.2015, Berlin Dr. Ruth Offergeld, Robert Koch-Institut, Berlin
Epidemiologie - Aktuelle Daten zu Infektionen bei Blut- und Plasmaspendern XV. Fortbildungsveranstaltung der ARGE Plasmapherese e.v., 20.-21.11.2015, Berlin Dr. Ruth Offergeld, Robert Koch-Institut, Berlin
Prävalenz bei ambulanten Patienten mit ambulant erworbener Pneumonie nach Erreger
 Produktnummer: IF1250M Rev. I Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Produktnummer: IF1250M Rev. I Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Hepatitis E, NRW 2016
 Hepatitis E, NRW 2016 Das Hepatitis E-Virus (HEV) ist ein einzelsträngiges, nicht umhülltes RNA-Virus. Für den Menschen relevant sind die Orthohepeviren vom Typ A. Die Orthohepeviren beinhalten vier humanpathogene
Hepatitis E, NRW 2016 Das Hepatitis E-Virus (HEV) ist ein einzelsträngiges, nicht umhülltes RNA-Virus. Für den Menschen relevant sind die Orthohepeviren vom Typ A. Die Orthohepeviren beinhalten vier humanpathogene
Prevenar 13 für Erwachsene von 18 bis 49 Jahren
 Pneumokokken-Schutz jetzt für alle Altersgruppen Europäische Kommission erteilt Zulassung für Prevenar 13 für Erwachsene von 18 bis 49 Jahren Berlin (17. Juli 2013) - Pfizer hat für den 13-valenten Pneumokokken-Konjugatimpfstoff
Pneumokokken-Schutz jetzt für alle Altersgruppen Europäische Kommission erteilt Zulassung für Prevenar 13 für Erwachsene von 18 bis 49 Jahren Berlin (17. Juli 2013) - Pfizer hat für den 13-valenten Pneumokokken-Konjugatimpfstoff
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 19/15
 VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 19/15 Für den Inhalt verantwortlich: Prof. Dr. Franz X. Heinz Prof. Dr. J. Aberle, Prof. Dr. St. Aberle Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp Prof. Dr.
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 19/15 Für den Inhalt verantwortlich: Prof. Dr. Franz X. Heinz Prof. Dr. J. Aberle, Prof. Dr. St. Aberle Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp Prof. Dr.
Vorschläge zur Änderung der Anhänge B1 und B2 des AK Blut Votums zur Rückverfolgung
 www.pei.de Vorschläge zur Änderung der Anhänge B1 und B2 des AK Blut Votums zur Rückverfolgung V 35 Anhang B1 Hepatitis B Virus (HBV) Untersuchungs-Schema zum Rückverfolgungsverfahren HBsAg Anti-HBc 1
www.pei.de Vorschläge zur Änderung der Anhänge B1 und B2 des AK Blut Votums zur Rückverfolgung V 35 Anhang B1 Hepatitis B Virus (HBV) Untersuchungs-Schema zum Rückverfolgungsverfahren HBsAg Anti-HBc 1
HIV-1 NAT Blutspenderscreening Testversagen: Ursachen und mögliche Konsequenzen - Müssen zwei Zielregionen erkannt werden?
 www.pei.de HIV-1 NAT Blutspenderscreening Testversagen: Ursachen und mögliche Konsequenzen - Müssen zwei Zielregionen erkannt werden? NAT screening and blood safety Mandatory NAT testing HCV RNA: 5 000
www.pei.de HIV-1 NAT Blutspenderscreening Testversagen: Ursachen und mögliche Konsequenzen - Müssen zwei Zielregionen erkannt werden? NAT screening and blood safety Mandatory NAT testing HCV RNA: 5 000
Schutz der Patienten vor der schweren Viruserkrankung PML
 Natalizumab bei Multipler Sklerose Schutz der Patienten vor der schweren Viruserkrankung PML Berlin (29. Juni 2012) Das Medikament Natalizumab gilt seit seiner Einführung in Europa vor etwa sechs Jahren
Natalizumab bei Multipler Sklerose Schutz der Patienten vor der schweren Viruserkrankung PML Berlin (29. Juni 2012) Das Medikament Natalizumab gilt seit seiner Einführung in Europa vor etwa sechs Jahren
NAT & Sicherheit von Blutprodukten Ein Update Markus M. Müller und Michael Schmidt Institut für Transfusionsmedizin und Immunhämatologie
 DRK-Blutspendedienst Baden-Württemberg Hessen gemeinnützige GmbH NAT & Sicherheit von Blutprodukten Ein Update 2015 Markus M. Müller und Michael Schmidt Institut für Transfusionsmedizin und Immunhämatologie
DRK-Blutspendedienst Baden-Württemberg Hessen gemeinnützige GmbH NAT & Sicherheit von Blutprodukten Ein Update 2015 Markus M. Müller und Michael Schmidt Institut für Transfusionsmedizin und Immunhämatologie
Mit dem Meldebogen (1b) sollen solche Ereignisse erfasst werden, bei denen eines oder mehrere der folgenden Kriterien erfüllt sind:
 Meldeverpflichtungen von schwerwiegenden Zwischenfällen und schwerwiegenden unerwünschten Transfusionsreaktionen gem. 63i Absatz 1 7 Arzneimittelgesetz (AMG) vom 23. Juli 2009, geändert am 01.03.2013 Das
Meldeverpflichtungen von schwerwiegenden Zwischenfällen und schwerwiegenden unerwünschten Transfusionsreaktionen gem. 63i Absatz 1 7 Arzneimittelgesetz (AMG) vom 23. Juli 2009, geändert am 01.03.2013 Das
Hepatitis C Elimination. Benedikt Schäfer
 Hepatitis C Elimination Benedikt Schäfer Hepatitis hasbeenlargely ignored as a health and development priority until recently New Engl J Med1986 Milestones in clinical HCV research Manns MP, et al. Nat
Hepatitis C Elimination Benedikt Schäfer Hepatitis hasbeenlargely ignored as a health and development priority until recently New Engl J Med1986 Milestones in clinical HCV research Manns MP, et al. Nat
Middle East Respiratory Syndrome - MERS-Coronavirus
 Middle East Respiratory Syndrome - MERS-Coronavirus Stephan Aberle Department für Virologie, Medizinische Universität Wien Nationale Referenzzentrale für Influenza und respiratorische Virusinfektionen
Middle East Respiratory Syndrome - MERS-Coronavirus Stephan Aberle Department für Virologie, Medizinische Universität Wien Nationale Referenzzentrale für Influenza und respiratorische Virusinfektionen
Kurzbericht über die im Rahmen der Infektionskrankheiten-Surveillance nach IfSG in Hamburg registrierten Krankheiten
 Zentrum für Impfmedizin und Infektionsepidemiologie INFEKT - INFO Ausgabe 3 / 29, 9. Juni 29 Kurzbericht über die im Rahmen der Infektionskrankheiten-Surveillance nach IfSG in Hamburg registrierten Krankheiten
Zentrum für Impfmedizin und Infektionsepidemiologie INFEKT - INFO Ausgabe 3 / 29, 9. Juni 29 Kurzbericht über die im Rahmen der Infektionskrankheiten-Surveillance nach IfSG in Hamburg registrierten Krankheiten
Evolution mit Folgen. Klimawandel und Infektionen. 21. Infekttag Matthias v. Kietzell
 Evolution mit Folgen Klimawandel und Infektionen 21. Infekttag 3.3.2016 Matthias v. Kietzell Schon wieder Evolution! Wie (Tiger)-Mücken und (Zika-)Viren uns in Schwung halten 21.Infekttag 3.3.2016 Matthias
Evolution mit Folgen Klimawandel und Infektionen 21. Infekttag 3.3.2016 Matthias v. Kietzell Schon wieder Evolution! Wie (Tiger)-Mücken und (Zika-)Viren uns in Schwung halten 21.Infekttag 3.3.2016 Matthias
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 15/16
 VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 15/16 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp Prof. Dr. E. Puchhammer Redaktion:
VIRUSEPIDEMIOLOGISCHE INFORMATION NR. 15/16 Für den Inhalt verantwortlich: Prof. Dr. J. Aberle, Prof. Dr. St. Aberle Prof. Dr. H. Holzmann, Prof. Dr. Th. Popow-Kraupp Prof. Dr. E. Puchhammer Redaktion:
Entwicklung der HIV-Epidemie Trends und Risikogruppen. Dr. Viviane Bremer MPH Nürnberg,
 Entwicklung der HIV-Epidemie Trends und Risikogruppen Dr. Viviane Bremer MPH Nürnberg, UNAIDS-Ziel bis 2020: 90 90-90 90% der Menschen mit HIV kennen ihren Status 90% der mit HIV diagnostizierten Menschen
Entwicklung der HIV-Epidemie Trends und Risikogruppen Dr. Viviane Bremer MPH Nürnberg, UNAIDS-Ziel bis 2020: 90 90-90 90% der Menschen mit HIV kennen ihren Status 90% der mit HIV diagnostizierten Menschen
Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international
 Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Dr. med. Dirk Mentzer Referatsleiter Arzneimittelsicherheit Facharzt für Kinder- und Jugendmedizin Paul-Ehrlich-Institut Bundesinstitut
Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Dr. med. Dirk Mentzer Referatsleiter Arzneimittelsicherheit Facharzt für Kinder- und Jugendmedizin Paul-Ehrlich-Institut Bundesinstitut
Hepatitis-E-Virus: Anstehende Konsequenzen für die Transfusionsmedizin
 Prof. Dr. Jörg Hofmann, Dr. rer. nat. Michael Chudy Hepatitis-E-Virus: Anstehende Konsequenzen für die Transfusionsmedizin Zusammenfassung Das Hepatitis-E-Virus rückt wegen der aktuellen Diskussionen um
Prof. Dr. Jörg Hofmann, Dr. rer. nat. Michael Chudy Hepatitis-E-Virus: Anstehende Konsequenzen für die Transfusionsmedizin Zusammenfassung Das Hepatitis-E-Virus rückt wegen der aktuellen Diskussionen um
Quellensuche: Der Patient zwischen Bezirksverwaltungsbehörde und BehandlerIn
 Quellensuche: Der Patient zwischen Bezirksverwaltungsbehörde und BehandlerIn Robert Zangerle Abteilungsleiter HIV & STI Univ. Klinik für Dermatologie, Venerologie und Allergologie Medizinische Universität
Quellensuche: Der Patient zwischen Bezirksverwaltungsbehörde und BehandlerIn Robert Zangerle Abteilungsleiter HIV & STI Univ. Klinik für Dermatologie, Venerologie und Allergologie Medizinische Universität
HIV-1 NAT-Testversager durch Mutationen
 HIV-1 NAT-Testversager durch Mutationen Dr. B. Müller, NAT-Labor, Hagen Aktueller Fall in Österreich vom 28.02.2013 Diagnostische Fensterspende Folie 2 Überblick Prävalenz bei Neuspendern100.000 Untersuchungen:
HIV-1 NAT-Testversager durch Mutationen Dr. B. Müller, NAT-Labor, Hagen Aktueller Fall in Österreich vom 28.02.2013 Diagnostische Fensterspende Folie 2 Überblick Prävalenz bei Neuspendern100.000 Untersuchungen:
Aspirin auch bei Typ-2-Diabetikern nur gezielt zur Sekundärprävention einsetzen
 Neue Erkenntnisse zur Prävention von Gefäßerkrankungen: Aspirin auch bei Typ-2-Diabetikern nur gezielt zur Sekundärprävention einsetzen Bochum (3. August 2009) Herzinfarkt und Schlaganfall sind eine häufige
Neue Erkenntnisse zur Prävention von Gefäßerkrankungen: Aspirin auch bei Typ-2-Diabetikern nur gezielt zur Sekundärprävention einsetzen Bochum (3. August 2009) Herzinfarkt und Schlaganfall sind eine häufige
Infektmarker im schweizerischen Blutspendedienst Dr. phil. nat. Caroline Tinguely, Labor Infektmarker IRB SRK AG / nationales Referenzlabor B-CH SRK
 Infektmarker im schweizerischen Blutspendedienst Dr. phil. nat. Caroline Tinguely, Labor Infektmarker IRB SRK AG / nationales Referenzlabor B-CH SRK Seite 1 Übersicht Blutspendewesen und Rotes Kreuz Gesetz
Infektmarker im schweizerischen Blutspendedienst Dr. phil. nat. Caroline Tinguely, Labor Infektmarker IRB SRK AG / nationales Referenzlabor B-CH SRK Seite 1 Übersicht Blutspendewesen und Rotes Kreuz Gesetz
Risikobewertung von IDs in der Transfusionsmedizin
 Risikobewertung von IDs in der Transfusionsmedizin Christof Jungbauer Fortbildung für Blutdepotbeauftragte, Mai 2017 BLUTSPENDEDIENST Inhalt 1. Blutsicherheit ein sensibles Thema 2. Wie sicher sind Blutkomponenten
Risikobewertung von IDs in der Transfusionsmedizin Christof Jungbauer Fortbildung für Blutdepotbeauftragte, Mai 2017 BLUTSPENDEDIENST Inhalt 1. Blutsicherheit ein sensibles Thema 2. Wie sicher sind Blutkomponenten
Nationale Referenzzentrale für Polioviren
 Nationale Referenzzentrale für Polioviren Jahresbericht 2014 Österreichische Agentur für Gesundheit und Ernährungssicherheit (AGES) Institut für medizinische Mikrobiologie und Hygiene Wien Währinger Straße
Nationale Referenzzentrale für Polioviren Jahresbericht 2014 Österreichische Agentur für Gesundheit und Ernährungssicherheit (AGES) Institut für medizinische Mikrobiologie und Hygiene Wien Währinger Straße
West-Nil-Virus, Influenza A H7N9 und MERS-Coronavirus
 West-Nil-Virus, Influenza A H7N9 und MERS-Coronavirus Stephan Aberle Department für Virologie, Medizinische Universität Wien Nationale Referenzzentrale für Flaviviren Nationale Referenzzentrale für Influenza
West-Nil-Virus, Influenza A H7N9 und MERS-Coronavirus Stephan Aberle Department für Virologie, Medizinische Universität Wien Nationale Referenzzentrale für Flaviviren Nationale Referenzzentrale für Influenza
Sexuelle Übertragbarkeit von Borrelien- Erste Ergebnisse der Studie mit der Universität Jyväskylä, Finnland
 Sexuelle Übertragbarkeit von Borrelien- Erste Ergebnisse der Studie mit der Universität Jyväskylä, Finnland Ärztliche Fortbildung Augsburg, 27.2.2016 Dr. H.G.Maxeiner, BCA-lab, Augsburg, Germany Literatur
Sexuelle Übertragbarkeit von Borrelien- Erste Ergebnisse der Studie mit der Universität Jyväskylä, Finnland Ärztliche Fortbildung Augsburg, 27.2.2016 Dr. H.G.Maxeiner, BCA-lab, Augsburg, Germany Literatur
Agenda. 1. Aviäre Influenza A(H7N9) 2. Novel Coronavirus 3. Körperwäsche mit Chlorhexidin 4. Isolationsmassnahmen bei ESBL E.coli.
 Agenda 1. Aviäre Influenza A(H7N9) 2. Novel Coronavirus 3. Körperwäsche mit Chlorhexidin 4. Isolationsmassnahmen bei ESBL E.coli Seite 1 Aviäre Influenza A(H7N9) Seite 2 Influenza: Hämagglutinin und Neuraminidase
Agenda 1. Aviäre Influenza A(H7N9) 2. Novel Coronavirus 3. Körperwäsche mit Chlorhexidin 4. Isolationsmassnahmen bei ESBL E.coli Seite 1 Aviäre Influenza A(H7N9) Seite 2 Influenza: Hämagglutinin und Neuraminidase
Immunhämatologische Resultate in der Hausarztpraxis
 Immunhämatologische Resultate in der Hausarztpraxis Interpretation, Konsequenzen Dr. med. T. Braschler, OAmbF Hämatologie 08.03.2018 Inhalt Der Immunhämatologische Befund Type and Screen Untersuchung Bedeutung
Immunhämatologische Resultate in der Hausarztpraxis Interpretation, Konsequenzen Dr. med. T. Braschler, OAmbF Hämatologie 08.03.2018 Inhalt Der Immunhämatologische Befund Type and Screen Untersuchung Bedeutung
Akute hämolytische TR. Schmerzen in der Nierengegend Hypotonie Übelkeit, Erbrechen RR-Abfall Blutiger Urin (auch bei Schock) Nierenversagen Schock
 Patient 73 Jahre Hüftendoprothesen OP Postoperative Nachblutung, Notfall-OP Hämorrhagischer Schock, Notfalltransfusion Nach 3 EK, Blutdruckabfall, Temperaturanstieg um 2 C Blutiger Urin Akute hämolytische
Patient 73 Jahre Hüftendoprothesen OP Postoperative Nachblutung, Notfall-OP Hämorrhagischer Schock, Notfalltransfusion Nach 3 EK, Blutdruckabfall, Temperaturanstieg um 2 C Blutiger Urin Akute hämolytische
ENDGÜLTIGES GUTACHTEN DES AUSSCHUSSES FÜR ARZNEISPEZIALITÄTEN GEMÄSS ARTIKEL 12 DER RICHTLINIE 75/319/EWG DES RATES, EINSCHLIESSLICH ÄNDERUNGEN, FÜR
 The European Agency for the Evaluation of Medicinal Products Human Medicines Evaluation Unit CPMP/375/97-DE ENDGÜLTIGES GUTACHTEN DES AUSSCHUSSES FÜR ARZNEISPEZIALITÄTEN GEMÄSS ARTIKEL 12 DER RICHTLINIE
The European Agency for the Evaluation of Medicinal Products Human Medicines Evaluation Unit CPMP/375/97-DE ENDGÜLTIGES GUTACHTEN DES AUSSCHUSSES FÜR ARZNEISPEZIALITÄTEN GEMÄSS ARTIKEL 12 DER RICHTLINIE
Vogelgrippe und Influenza. Allgemeines
 Vogelgrippe und Influenza Allgemeines Wann sollte man an eine Influenza A/H5N1 Infektion denken Welche Maßnahmen sollten im Verdachtsfall ergriffen werden Erregernachweis - Labor Enders Allgemeines Die
Vogelgrippe und Influenza Allgemeines Wann sollte man an eine Influenza A/H5N1 Infektion denken Welche Maßnahmen sollten im Verdachtsfall ergriffen werden Erregernachweis - Labor Enders Allgemeines Die
WNV: Preparedness-Plan Schweiz
 WNV: Preparedness-Plan Schweiz Christoph Niederhauser Interregionale Blutspende SRK 5. Sitzung der DGTI Sektion Sicherheit von Blutprodukten 19. März 2015 in München page 1 Inhalt West Nile Virus Situation
WNV: Preparedness-Plan Schweiz Christoph Niederhauser Interregionale Blutspende SRK 5. Sitzung der DGTI Sektion Sicherheit von Blutprodukten 19. März 2015 in München page 1 Inhalt West Nile Virus Situation
Kurzbericht über die im Rahmen der Infektionskrankheiten-Surveillance nach IfSG in Hamburg registrierten Krankheiten
 Zentrum für Impfmedizin und Infektionsepidemiologie INFEKT - INFO Ausgabe / 00, 4. Juni 00 Kurzbericht über die im Rahmen der Infektionskrankheiten-Surveillance nach IfSG in Hamburg registrierten Krankheiten
Zentrum für Impfmedizin und Infektionsepidemiologie INFEKT - INFO Ausgabe / 00, 4. Juni 00 Kurzbericht über die im Rahmen der Infektionskrankheiten-Surveillance nach IfSG in Hamburg registrierten Krankheiten
MultiVir NAT - erster personalisierter Ringversuch zum Genomnachweis von 8 Viren (HAV, HBV, HCV, HIV-1, HIV-2, PB19, WNV, HCMV)
 MultiVir NAT - erster personalisierter Ringversuch zum Genomnachweis von 8 Viren (HAV, HBV, HCV, HIV-1, HIV-2, PB19, WNV, HCMV) INHALT Inhaltsverzeichnis 1 Editorial 3-4 2 Ringversuchsprinzip 5-6 3 Pilotstudie
MultiVir NAT - erster personalisierter Ringversuch zum Genomnachweis von 8 Viren (HAV, HBV, HCV, HIV-1, HIV-2, PB19, WNV, HCMV) INHALT Inhaltsverzeichnis 1 Editorial 3-4 2 Ringversuchsprinzip 5-6 3 Pilotstudie
Meldepflichtige Infektionskrankheiten bei Personen mit Migrationshintergrund
 Meldepflichtige Infektionskrankheiten bei Personen mit Migrationshintergrund Dr. D. Schmid, Mag. E. Kanitz Abt. Infektionsepidemiologie & Surveillance, Institut für medizinische Mikrobiologie und Hygiene
Meldepflichtige Infektionskrankheiten bei Personen mit Migrationshintergrund Dr. D. Schmid, Mag. E. Kanitz Abt. Infektionsepidemiologie & Surveillance, Institut für medizinische Mikrobiologie und Hygiene
Was ist eigentlich los mit den Meningokokken B?
 Was ist eigentlich los mit den Meningokokken B? meningitis_300 MenC_(c)GSK Jahreskongress Pädiatrie 2018 Dr. med. Markus Kirchner, MPH Senior Medical Advisor, Medizinischer Fachbereich Impfstoffe GlaxoSmithKline
Was ist eigentlich los mit den Meningokokken B? meningitis_300 MenC_(c)GSK Jahreskongress Pädiatrie 2018 Dr. med. Markus Kirchner, MPH Senior Medical Advisor, Medizinischer Fachbereich Impfstoffe GlaxoSmithKline
Bescheid: Der Präsident. An alle pharmazeutischen Unternehmer von nicht pathogen-inaktivierte Blutkomponenten und gefrorenem Frischplasma
 Paul-Ehrlich-Institut Postfach 63207 Langen Der Präsident An alle pharmazeutischen Unternehmer von nicht pathogen-inaktivierte Blutkomponenten und gefrorenem Frischplasma Ansprechpartner/in: Prof. Dr.
Paul-Ehrlich-Institut Postfach 63207 Langen Der Präsident An alle pharmazeutischen Unternehmer von nicht pathogen-inaktivierte Blutkomponenten und gefrorenem Frischplasma Ansprechpartner/in: Prof. Dr.
Viruswirksame Desinfektion aus Anwenderperspektive und was bedeutet. Maren Eggers. 14. Kongress für Krankenhaushygiene Berlin
 Viruswirksame Desinfektion aus Anwenderperspektive und was bedeutet begrenzt viruzid PLUS?! Maren Eggers 14. Kongress für Krankenhaushygiene Berlin Inhalt - Saisonalität von Viren: Auftreten von Noro/Adeno/Rota
Viruswirksame Desinfektion aus Anwenderperspektive und was bedeutet begrenzt viruzid PLUS?! Maren Eggers 14. Kongress für Krankenhaushygiene Berlin Inhalt - Saisonalität von Viren: Auftreten von Noro/Adeno/Rota
Chemoprävention der Tuberkulose
 Chemoprävention der Tuberkulose Dr. med. Hilte Geerdes-Fenge Universitätsklinikum Rostock, Abt. für Infektiologie und Tropenmedizin Tuberkulose bei Kindern 0-9 Jahre in D. insgesamt 0-9 Jahre 2008 4531
Chemoprävention der Tuberkulose Dr. med. Hilte Geerdes-Fenge Universitätsklinikum Rostock, Abt. für Infektiologie und Tropenmedizin Tuberkulose bei Kindern 0-9 Jahre in D. insgesamt 0-9 Jahre 2008 4531
Informationsbroschüre Risiko Hepatitis C
 Dres. med. Fenner & Kollegen Gemeinschaftspraxis für Labormedizin und Humangenetik Informationsbroschüre Risiko Hepatitis C Das Hepatitis-C-Virus ein Silent Killer Dr. med. Claus Fenner FA Laboratoriumsmedizin,
Dres. med. Fenner & Kollegen Gemeinschaftspraxis für Labormedizin und Humangenetik Informationsbroschüre Risiko Hepatitis C Das Hepatitis-C-Virus ein Silent Killer Dr. med. Claus Fenner FA Laboratoriumsmedizin,
Curriculum Entwicklungspsychopharmakologie: Arzneimittel in der Kinder- und Jugendpsychiatrie, Ulm 2017
 Curriculum Entwicklungspsychopharmakologie: Arzneimittel in der Kinder- und Jugendpsychiatrie, Ulm 2017 Welche Nebenwirkungen sollten gemeldet werden? Erläuterung und Diskussion anhand von Fallbeispielen
Curriculum Entwicklungspsychopharmakologie: Arzneimittel in der Kinder- und Jugendpsychiatrie, Ulm 2017 Welche Nebenwirkungen sollten gemeldet werden? Erläuterung und Diskussion anhand von Fallbeispielen
Aspekte einer modernen Norovirusdiagnostik
 Aspekte einer modernen Norovirusdiagnostik Roesebeckstr. 4-6 30449 Hannover Fon 0511/4505-0 Fax 0511/4505-140 Cornelia Henke-Gendo Abt.2: Krankenhaushygiene www.nlga.niedersachsen.de Die ideale Diagnostik
Aspekte einer modernen Norovirusdiagnostik Roesebeckstr. 4-6 30449 Hannover Fon 0511/4505-0 Fax 0511/4505-140 Cornelia Henke-Gendo Abt.2: Krankenhaushygiene www.nlga.niedersachsen.de Die ideale Diagnostik
Influenza 2009 in Europa
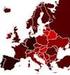 Influenza 2009 in Europa (Stand Freitag 11.09.2009; Erfassung bis 36. Kalenderwoche) In den Anfängen einer Influenza-Pandemie ist deren Ausbreitung über die zahlenmäßige Erfassung von Virusnachweisen in
Influenza 2009 in Europa (Stand Freitag 11.09.2009; Erfassung bis 36. Kalenderwoche) In den Anfängen einer Influenza-Pandemie ist deren Ausbreitung über die zahlenmäßige Erfassung von Virusnachweisen in
Übertragung von Mycobacterium tuberculosis: Was wissen wir aus der Surveillance und was würden wir gerne wissen?
 Übertragung von Mycobacterium tuberculosis: Was wissen wir aus der Surveillance und was würden wir gerne wissen? Dr. Lena Fiebig, RKI Berlin, 20. März 2017 Tuberkulose Trend: Ergebnis aller Szenarien und
Übertragung von Mycobacterium tuberculosis: Was wissen wir aus der Surveillance und was würden wir gerne wissen? Dr. Lena Fiebig, RKI Berlin, 20. März 2017 Tuberkulose Trend: Ergebnis aller Szenarien und
Infektionsrisiko Flüchtling? 24.August 2016 Ärztehaus Göttingen Simone Scheithauer
 Infektionsrisiko Flüchtling? 24.August 2016 Ärztehaus Göttingen Simone Scheithauer Bad news are good news Good news are good news?! Zwischen Panik und political correctness Ich wohne neben Flüchtlingswohnheim
Infektionsrisiko Flüchtling? 24.August 2016 Ärztehaus Göttingen Simone Scheithauer Bad news are good news Good news are good news?! Zwischen Panik und political correctness Ich wohne neben Flüchtlingswohnheim
Infektion mit dem Zytomegalievirus (CMV) in der Schwangerschaft. CMV-Serologie: IgM, IgG und Avidität? Christoph Koidl April 2013
 Infektion mit dem Zytomegalievirus (CMV) in der Schwangerschaft CMV-Serologie: IgM, IgG und Avidität? Christoph Koidl April 2013 Einleitung-Systematik - Familie: Herpesviridae - Subfamilie: Betaherpesvirinae
Infektion mit dem Zytomegalievirus (CMV) in der Schwangerschaft CMV-Serologie: IgM, IgG und Avidität? Christoph Koidl April 2013 Einleitung-Systematik - Familie: Herpesviridae - Subfamilie: Betaherpesvirinae
Asylsuchende und Gesundheit
 Asylsuchende und Gesundheit Dr. Andreas Gilsdorf Abteilung für Infektionsepidemiologie, RKI Fortbildung für den ÖGD, 06. April 2016 Aktuelle Situation der Asylsuchenden in Deutschland Registrierte Zugänge
Asylsuchende und Gesundheit Dr. Andreas Gilsdorf Abteilung für Infektionsepidemiologie, RKI Fortbildung für den ÖGD, 06. April 2016 Aktuelle Situation der Asylsuchenden in Deutschland Registrierte Zugänge
Impfen und Intensivstation. Dr. Anita Niederer-Loher Infektiologie und Spitalhygiene Ostschweizer Kinderspital und KSSG
 Impfen und Intensivstation Dr. Infektiologie und Spitalhygiene Ostschweizer Kinderspital und KSSG Impfen bei Risikopatienten: Factsheet Influenza Pneumokokken Meningokokken Varizellen Hepatitis A/B Influenza
Impfen und Intensivstation Dr. Infektiologie und Spitalhygiene Ostschweizer Kinderspital und KSSG Impfen bei Risikopatienten: Factsheet Influenza Pneumokokken Meningokokken Varizellen Hepatitis A/B Influenza
ANeoPedS (ANeoS/APedS) Infektiossurveillance in pädiatrischen & neonatologischen Intensivstationen
 ANeoPedS (ANeoS/APedS) Infektiossurveillance in pädiatrischen & neonatologischen Intensivstationen Nationales Referenzzentrum für Nosokomiale Infektionen des BMG Univ. Klinik für Krankenhaushygiene und
ANeoPedS (ANeoS/APedS) Infektiossurveillance in pädiatrischen & neonatologischen Intensivstationen Nationales Referenzzentrum für Nosokomiale Infektionen des BMG Univ. Klinik für Krankenhaushygiene und
17. St. Galler Infekttag. Hot topics. Das aktuelle heisse Eisen oder zur Rolle des Grundversorgers bei neuen Epidemien
 17. St. Galler Infekttag Hot topics Das aktuelle heisse Eisen oder zur Rolle des Grundversorgers bei neuen Epidemien 1. Ausbruchabklärung: Was ist zu tun? (Matthias Schlegel) 2. Wer macht was? Rolle des
17. St. Galler Infekttag Hot topics Das aktuelle heisse Eisen oder zur Rolle des Grundversorgers bei neuen Epidemien 1. Ausbruchabklärung: Was ist zu tun? (Matthias Schlegel) 2. Wer macht was? Rolle des
Kasuistiken aus der Rheumatologie
 Fortbildung der SLÄK zur Lyme-Borreliose Dresden, 20.02.2013 Kasuistiken aus der Rheumatologie Dr. Christoph Lübbert Fachbereich Infektions- und Tropenmedizin Prof. Dr. Christoph Baerwald Sektion Rheumatologie
Fortbildung der SLÄK zur Lyme-Borreliose Dresden, 20.02.2013 Kasuistiken aus der Rheumatologie Dr. Christoph Lübbert Fachbereich Infektions- und Tropenmedizin Prof. Dr. Christoph Baerwald Sektion Rheumatologie
Epidemiologie der Hepatitis A bei österreichischen und ausländischen Kindern in Wien ( )
 Mitt. Österr. Ges. Tropenmed. Parasitol. () - Abt. für Kinderinfektionskrankheiten und interne Kinderkrankheiten des Wilhelminenspitals der Stadt Wien () Institut für Immunologie der Universität Wien ()
Mitt. Österr. Ges. Tropenmed. Parasitol. () - Abt. für Kinderinfektionskrankheiten und interne Kinderkrankheiten des Wilhelminenspitals der Stadt Wien () Institut für Immunologie der Universität Wien ()
Inzidenz von HEV in Hessen Evaluationsstudie von 2012 bis 2014
 Inzidenz von HEV in Hessen Evaluationsstudie von 2012 bis 2014 Deutsches Rotes Kreuz Baden-Württemberg-Hessen Goethe Universität Frankfurt / Main Institut für Transfusionsmedicine und Immunhämatologie
Inzidenz von HEV in Hessen Evaluationsstudie von 2012 bis 2014 Deutsches Rotes Kreuz Baden-Württemberg-Hessen Goethe Universität Frankfurt / Main Institut für Transfusionsmedicine und Immunhämatologie
Paul-Ehrlich-Institut ordnet Hepatitis E Virus Testung von Blutspenden an
 Pressemitteilung Bad Oeynhausen, 15. Juni 2018 Bad Oeynhausener Institut ist der Zeit voraus: Paul-Ehrlich-Institut ordnet Hepatitis E Virus Testung von Blutspenden an Die Bundesoberbehörde ordnet den
Pressemitteilung Bad Oeynhausen, 15. Juni 2018 Bad Oeynhausener Institut ist der Zeit voraus: Paul-Ehrlich-Institut ordnet Hepatitis E Virus Testung von Blutspenden an Die Bundesoberbehörde ordnet den
Erregerresistenz und Antibiotikagebrauch: Huhn oder Ei?
 56. Hygienekreis Dienstag, 30. Oktober 2018 Erregerresistenz und Antibiotikagebrauch: Huhn oder Ei? Dr. med. Lionel Chok, Assistenzarzt PD Dr. med. Stefan P. Kuster, Leitender Arzt Klinik für Infektionskrankheiten
56. Hygienekreis Dienstag, 30. Oktober 2018 Erregerresistenz und Antibiotikagebrauch: Huhn oder Ei? Dr. med. Lionel Chok, Assistenzarzt PD Dr. med. Stefan P. Kuster, Leitender Arzt Klinik für Infektionskrankheiten
Weltgesundheitsorganisation
 Gremien Seite 2 ECAC Seite 3 Die Weltgesundheitsorganisation (engl. World Health Organization, WHO) ist eine Sonderorganisation der Vereinten Nationen mit Sitz in Genf (Schweiz). Sie wurde am 7. April
Gremien Seite 2 ECAC Seite 3 Die Weltgesundheitsorganisation (engl. World Health Organization, WHO) ist eine Sonderorganisation der Vereinten Nationen mit Sitz in Genf (Schweiz). Sie wurde am 7. April
Impfen für Säuglinge: Was ist neu und warum der Zeitpunkt eine Rolle spielt
 Impfen für Säuglinge: Was ist neu und warum der Zeitpunkt eine Rolle spielt Impfforum Zürich Prof. Dr. med. Christoph Berger Abteilung für Infektiologie und Spitalhygiene Universitäts-Kinderspital Zürich
Impfen für Säuglinge: Was ist neu und warum der Zeitpunkt eine Rolle spielt Impfforum Zürich Prof. Dr. med. Christoph Berger Abteilung für Infektiologie und Spitalhygiene Universitäts-Kinderspital Zürich
Kleine Stiche - große Wirkung: Zika-Virus-Infektionen in Mittel- und Südamerika breiten sich rasant aus.
 Seite 1 von 5 16.02.2016 2. Ausgabe 2016 Kleine Stiche - große Wirkung: Zika-Virus-Infektionen in Mittel- und Südamerika breiten sich rasant aus. Infektionen durch das Zika-Virus, vormals endemisch in
Seite 1 von 5 16.02.2016 2. Ausgabe 2016 Kleine Stiche - große Wirkung: Zika-Virus-Infektionen in Mittel- und Südamerika breiten sich rasant aus. Infektionen durch das Zika-Virus, vormals endemisch in
PRO. Infektionsdiagnostik in der Schwangerschaft: Reicht die gesetzliche Schwangerschaftsvorsorge? Monika Rehn
 Frauenklinik und Hebammenschule Direktor: Prof. Dr. med. Johannes Dietl Infektionsdiagnostik in der Schwangerschaft: Reicht die gesetzliche Schwangerschaftsvorsorge? PRO Monika Rehn Infektionsdiagnostik
Frauenklinik und Hebammenschule Direktor: Prof. Dr. med. Johannes Dietl Infektionsdiagnostik in der Schwangerschaft: Reicht die gesetzliche Schwangerschaftsvorsorge? PRO Monika Rehn Infektionsdiagnostik
HIV, Syphilis & Co. Fakten zur aktuellen Verbreitung
 HIV, Syphilis & Co. Fakten zur aktuellen Verbreitung Dr. med. Dominique Braun Oberarzt Klinik für Infektionskrankheiten&Spitalhygiene UniversitätsSpital Zürich dominique.braun@usz.ch Anstieg aller STI
HIV, Syphilis & Co. Fakten zur aktuellen Verbreitung Dr. med. Dominique Braun Oberarzt Klinik für Infektionskrankheiten&Spitalhygiene UniversitätsSpital Zürich dominique.braun@usz.ch Anstieg aller STI
Neuester Stand der Council of Europe - Guidelines
 Neuester Stand der Council of Europe - Guidelines Prim. Univ.-Doz. Dr. Harald Schennach Zentralinstitut für Bluttransfusion und Immunologische Abteilung, TILAK, Landeskrankenhaus - Univ.-Kliniken, Innsbruck
Neuester Stand der Council of Europe - Guidelines Prim. Univ.-Doz. Dr. Harald Schennach Zentralinstitut für Bluttransfusion und Immunologische Abteilung, TILAK, Landeskrankenhaus - Univ.-Kliniken, Innsbruck
PROCALCITONIN (PCT) ALS WICHTIGE KOMPONENTE KLINISCHER ENTSCHEIDUNGSALGORITHMEN ZUR STEUERUNG DER ANTIBIOTIKA-THERAPIE
 PROCALCITONIN (PCT) ALS WICHTIGE KOMPONENTE KLINISCHER ENTSCHEIDUNGSALGORITHMEN ZUR STEUERUNG DER ANTIBIOTIKA-THERAPIE Dr. Jutta Odarjuk, Global Marketing Thermo Scientific Biomarkers Workshop Infektionsdiagnostik
PROCALCITONIN (PCT) ALS WICHTIGE KOMPONENTE KLINISCHER ENTSCHEIDUNGSALGORITHMEN ZUR STEUERUNG DER ANTIBIOTIKA-THERAPIE Dr. Jutta Odarjuk, Global Marketing Thermo Scientific Biomarkers Workshop Infektionsdiagnostik
