(Thioacetoxy-S-methyl) diorganylsilane und (Mercaptomethyl) diorganylsilane: Synthese und Eigenschaften
|
|
|
- Daniela Winter
- vor 5 Jahren
- Abrufe
Transkript
1 57 Journal of Organometallic Chemistry, 388 (1990) Elsevier Sequoia S.A., Lausanne- Printed in The Netherlands JOM (Thioacetoxy-S-methyl) diorganylsilane und (Mercaptomethyl) diorganylsilane: Synthese und Eigenschaften einhold Tacke *, Beate Becker und Hartwig Lange nstitutfuranorganische Chemie, Universität Kar/sruhe, Engesserstraße, D-7500 Karlsruhe (B..D.) (Eingegangen den 8. Dezember 1989) Abstract The novel synthesis of the (thioacetoxy-s-methyl)diorganylsilanes (CH 3 ) 2 Si(H) CH2SC(O)CH3 (9) and (C 6 H 5 ) 2 Si(H)CH 2 SC(O)CH 3 (10) and the (mercaptomethyl)diorganylsilanes (CH 3 ) 2 Si(H)CH 2 SH (11) and (C 6 H 5 ) 2 Si(H)CH 2 SH (12) is described. The silanes 11 and 12 areeasy to handle, whereas the structurally analogous (hydroxymethyl)diorganylsilanes (CH 3 ) 2 Si(H)CH 2 0H (1) and (C 6 H 5 ) 2 Si(H)CH 2... OH (2) tend to undergo a base-catalyzed decomposition (formation of oligomeric (polymeric) alkoxysilanes and hydrogen). n cantrast to the thermally unstable (acetoxymethyl)diorganylsilanes (CH 3 ) 2 Si(H)CH 2 0C(O)CH 3 (3) and (C 6 H 5 ) 2 Si (H)CH20C(O)CH3 (4) (--+ rearrangement to the corresponding acetoxy(methyl)diorganylsilanes (CH 3 ) 3 SiOC(O)CH 3 (5) and CH 3 (C 6 H 5 ) 2 Si0C(O)CH 3 (6)), the thio-analogues 9 and 10 are thermally stable (1 molar solutions in C 6 D 6, 30 h at 180 C). Zusammenfassung Die erstmalige Synthese der (Thioacetoxy-S-methyl)diorganylsilane (CH 3 ) 2 Si (H)CH2SC(O)CH3 (9) und (c;h 5 ) 2 Si(H)CH 2 SC(O)CH 3 (10) und der (Mercaptomethyl)diorganylsilane (CH 3 ) 2 Si(H)CH 2 SH (11) und (C 6 H 5 ) 2 Si(H)CH 2 SH (12) wird beschrieben. Während sich die Silane 9 und 10 leicht handhaben lassen, neigen die strukturanalogen (Hydroxymethyl)diorganylsilane (CH 3 ) 2 Si(H)CH 2 0H (1) und (C 6 H 5 ) 2 Si(H)CH 2 0H (2) zu einer basenkatalysierten Zersetzung (Bildung oligomerer (polymerer) Alkoxysilane und Wasserstoff). m Gegensatz zu den thermisch labilen (Acetoxymethyl)diorganylsilanen (CH 3 ) 2 Si(H)CH 2 0C(O)CH 3 (3) und (C 6 H 5 )2,Si (H)CH 2 0C(O)CH 3 (4) (--+ Umlagerung zu den entsprechenden Acetoxy(methyl) diorganylsilanen (CH 3 ) 3 SiOC(O)CH 3 (5) und CH 3 (C 6 H 5 ) 2 SiOC(O)CH 3 {6)) sind die Thio-Analoga 9 und 10 thermisch stabil (-molare Lösungen in c;o 6, 30 h bei 180 o C) Xj90j$ Elsevier Sequoia S.A.
2 58 Einleitung n vorangegangenen Mitteilungen haben wir über die Synthese der (Hydroxymethyl)diorganylsilane 1 und 2 [1] und der davon abzuleitenden (Acetoxymethyl)diorganylsilane 3 und 4 [2] berichtet (Schema 1). Die Silane 3 und 4 unterliegen einer thermisch induzierten Umlagerung zu den entsprechenden Acetoxy(methyl)diorganylsilanen 5 und 6 (Schema 1) [2]. Wir berichten hier über die Darstellung der von l-4 abzuleitenden Thio-Analoga, den (Mercaptomethyl)diorganylsilanen 11 und 12 und den (Thioacetoxy-Smethyl)diorganylsilanen 9 und 10 (Schema 1). Ziel dieser synthetischen Arbeiten war ein Eigenschafts-Vergleich der 0/S-Analoga 1/11, 2/12, 3/9 und 4/10. m Zusammenhang mit unseren Untersuchungen zur thermischen Stabilität von Elementsauerstoffsäure-Estern von (Hydroxymethyl)diorganylsilanen (vgl. hierzu ef. 2-6) waren wir vor allem an der Fr~ge interessiert, ob die (Thioacetoxy-Smethyl)diorganylsilane 9 und 10 in Analogie zu den entsprechenden (Acetoxymethyl)diorganylsilanen 3 und 4 einer thermisch induzierten Umlagerung unterliegen. Ergebnisse und Diskussion Die Synthese der (Thioacetoxy-S-methyl)diorganylsilane 9 und 10 gelang auf einfache Weise gemäß Schema 2 durch Umsetzung der entsprechenden (Chlormethyl)diorganylsilane 7 und 8 mit Kaliumthioacetat in THF bei aumtemperatur (Ausbeute 63 bzw. 76%). Durch Umsetzung von 9 bzw. 10 mit Lithiumaluminiumhydrid in Diethylether - gefolgt von einer sauren wässerigen Aufarbeitung - konnten dann die entsprechenden (Mercaptomethyl)diorganylsilane 11 und 12 dargestellt werden (Schema 2). Unseres Wissens sind die Silane 9 und 10 die ersten Vertreter der Stoffklasse der (Thioacetoxy-S-methyl)diorganylsilane, die Silane 11 und 12 die ersten Vertreter der Stoffklasse der (Mercaptomethyl)diorganylsilane. Die Verbindungen 9, 11 und 12 sind farblose, im Vakuum unzersetzt destillierbare Flüssigkeiten, 10 liegt bei aumtemperatur als farbloser, kristalliner Feststoff vor. Während die (Hydroxymethyl)diorganylsilane l und 2 sehr leicht zu einer basenkatalysierten, unter Wasserstoff-Entwicklung ablaufenden Selbstzersetzung zu oligomeren (polymeren) Alkoxysilanen und Wasserstoff neigen [1], sind die entsprechenden Thio-Analoga 9 und 10 vergleichsweise stabil - ein Verhai ten, das sich zwanglos durch die unterschiedliche eaktivität strukturanaloger Alkohole OH 1~ 3, 5 CH3 21 4~ 6 C 6 H 5 0 A -Si-CH2-0-C-CH3- -Si-CH3 H 0 3,4 5,6 C=O CH3 -Si-CH 2 SH H 11,12 Schema 1 9, 11 CH 3 10, 12 «;Hs 0 -Si-CH2- S-C-CH 3 H 9,10
3 -~i-ch,cl l<lch)cosl.,. H7,B/ ~ 0 -Si-CH2- S-C-CH3 H , 11~ 13 CH3 -Si-CH3 0 13,14 c=s CH3 -Si-CH2SH H 11,12 B, 10, 12, 14 c6~ Schema 2 (bzw. Alkoxide O-) und Mercaptane SH (bzw. Mercaptide S-) gegenüber Hydridosilanen deuten läßt (vgl. hierzu z.b. ef. 7-9; zur Chemie von SiS-Verbindungen vgl. ef. 10). Auch die 0/S-Analoga 3/9 und 4/10 zeigen ein sehr unterschiedliches chemisches Verhalten. Während 3 und 4 einer thermisch induzierten Umlagerung zu den entsprechenden Silanen 5 und 6 unterliegen (Schema 1), sind die Thio-Analoga 9 und 10 thermisch stabil: Nach 30-stündigem Erhitzen 1-molarer Lösungen von 9 und 10 auf 180 C konnte keine Umlagerung zu den von 5 und 6 abzuleitenden Thio-Analoga 13 und 14 beobachtet werden CH-NM Analyse). Dieses Ergebnis soll an anderer Stelle im Zusammenhang mit der mechanistischen Deutung der thermisch induzierten Umlagerung von Elementsauerstoffsäure-Estern von (H ydroxymethyl)diorganylsilanen diskutiert werden. Experimentelles Alle eaktionen wurden unter einer Schutzgasatmosphäre von trockenem Stickstoff durchgeführt; die verwendeten Lösungsmittel waren wasserfrei. Der Siedebereich des verwendeten Petrolethers betrug C. Schmelzpunkte (unkorrigiert): Gerät 530 der Fa. Büchi (Ölbad). 1 H-NM-Spektren (Lösungsmittel CDC1 3 bzw. C 6 D 6 ; int. Standard TMS (ö 0.00)): WM-400-Gerät (400.1 MHz) der Fa. Broker. 13 C-NM-Spektren (Lösungsmittel und int. Standard CDC1 3 ( ) bzw. C 6 D 6 ( )): WM Gerät (100.6 MHz) der Fa. Bruker. Die Signalzuordnungen wurden durch DEPT-Experimente unterstützt; die Ergebnisse dieser Experimente sind in den Zuordnungen enthalten. 29 Si-Spektren (Lösungsmittel C 6 D 6, int. Standard TMS (ß 0.0, eferenzfrequenz von TMS in C 6 D MHz)): AM-200-Gerät (39.8 MHz) der Fa. Bruker. Massenspektren (70 ev; die angegebenen m/z-werte (ausgewählte Schlüsselfragmente, registriert ab m;z ~ 40) basieren auf den Massenzahlen der jeweiligen sotope mit der größten natürlichen relativen Häufigkeit): 8430-Gerät der Fa. Finnigan MAT. -Spektren: AccuLab- 9-Gerät der Fa. Deckman bzw Gerät der Fa. Perkin Elmer. Das verwendete Kaliumthioacetat (Fluka 60595) wurde vor Gebrauch unter N 2.. Atmosphäre zermörsert. Kieselgel (Kieselgel 60, Komgröße mm, mesh ASTM, Merck 7734) und Al (Al aktiv, neutral, Merck 1077) wurden von der Fa. Merck bezogen.
4 60 ( Chlormethyl)dimethylsi/an (7) 7 wurde in Anlehnung an Lit allerdings mit wässeriger Aufarbeitung - dargestellt: Zu einer Suspension von 10.6 g (0.28 mol) LiAH 4 in 100 ml Diethylether wurde unter ühren und Eiskühlung im Verlauf von 20 min eine Lösung von g (1 mol) Chlor(chlormethyl)dimethylsilan in 100 ml Diethylether getropft. Das eaktionsgemisch wurde 20 h bei aumtemperatur gerührt und anschließend vorsichtig bei 0 C zu 100 ml 12.5%iger Salzsäure gegeben. Man trennte die wässerige Phase ab, extrahierte diese zweimal mit je 30 ml Pentan, trocknete die vereinigten organischen Phasen über A , destillierte das Lösungsmittel bei Normaldruck ab und destillierte den ückstand fraktionierend über eine Vigreux Kolonne. Es wurden 58.0 g (53%) einer farblosen Flüssigkeit erhalten, Sdp C (Lit. 11: Cj740 Torr). 1 H-NM (C 6 D 6 ): (d, J 3.8 Hz, 6H; SiCH 3 ), 2.42 (d, J 2.6 Hz, 2H; SiCH 2 Cl), 4.01 (tsept, J 3.6 Hz, J 2.6 Hz, J(SiH) Hz, 1H; SiH). 13 C-NM (C 6 D 6 ): ~ -6.0 (SiCH 3 ), 28.7 (SiCH 2 C). 29 Si-NM (C 6 D 6 ): (CC1 4 ): 2140 cm -t (SiH). MS: mjz 108 ( < 2%, M+ ), 107 (3%, M+- H), 93 (25%, M+- CH 3 ), 59 (100%, M+- CH 2 Cl), 43 (17%, SiCHj). C 3 H 9 C1Si (108.6). (Chlormethyl)diphenylsilan (8) 8 wurde in Anlehnung an Lit. 12 mit 70%iger Ausbeute dargestellt, Sdp. 102 o C/0.01 Torr (Lit. 12: o C/17 mmhg). 1 H-NM (C 6 D 6 ): ( d, J 3.1 Hz, 2H; SiCH 2 Cl), 5.11 (t, J 3.0 Hz, J(SiH) Hz, 1H; SiH), und {m, loh; SiC 6 H 5 ). 13 C-NM (C 6 D 6 ): o 26.5 (SiCH 2 Cl), (m-c), (p-c), {i-c), (o-c). 29 Si.. NM (C 6 D 6 ): ö (Film): 2160 cm- 1 (SiH). MS: mjz = 232 (8%, M+), 183 (100%, M+- CH 2 Cl), 105 (10%, SiC 6 Ht). C 13 H 13 C1Si (232.8). Dimethyl( thioacetoxy-s -methy/)si/an (9) Ein Gemisch aus 8.0 g (73.6 mmol) 7 und 10.1 g (88.4 mrnol) Kaliumthioacetat in 90 ml THF wurde 24 h bei aumtemperatur gerührt. Man entfernte das Lösungsmittel im Vakuum, nahm den ückstand in 200 ml Petrolether auf, filtrierte über 50 g Kieselgel (aufgeschwemmt in Diethylether), befreite das Filtrat unter vermindertem Druck vom Lösungsmittel und destillierte den ückstand im Vakuum fraktionierend über eine Vigreux-Kolonne. Es wurden 6.9 g (63%) einer farblosen Flüssigkeit erhalten, Sdp. 82 o Cj68 Torr. 1 H-NM (CDC1 3 ): (d, J 3.6 Hz, 6H; SiCH 3 ), 2.12 (d, J 3.2 Hz, 2H; SiCH 2 S), 2.31 (s, 3H; C(O)CH 3 )~ 3.95 (tsept, J 3.6 Hz, J 3.2 Hz, J(SiH) Hz, H; SiH). 13 C-NM (CDC1 3 ): ß -4.6 (SiCH 3 ), 11.7 (SiCH 2 S), 30.1 (QO)CH 3 ), (C(O)CH 3 ). 29 Si-NM (C 6 D 6 ): Si-NM (CDC 3 ): ß (Film): 2125 (SiH), 1695 cm -l {C=O). MS: mjz 147 (31 %, M+- H), 133 (76%, M+- CH 3 ), 105 (42%, M+- CH 3 CO), 59 (67%, M+- CH 2 SqO)CH 3 ), 43 (100%, SiCHj undjoder CH 3 CO+). Gef.: C, 40.7; H, 8.2; Si, C 5 H 12 0SSi (148.3) ber.: C, 40.50; H, 8.16; Si, 18.94%. Diphenyl(thioacetoxy-S -methyl)silan ( 1 0) 10 wurde analog zu 9 aus 9.0 g (38.7 mmol) 8 und 5.3 g (46.4 mmol) Kaliumthioacetat in 45 ml THF hergestellt. Es wurden 8.0 g (76%) einer farblosen Flüssigkeit erhalten, die bei - 20 C kristallisierte und sich aus Ether 1 Petrolether (1/5 (v jv)) bei - 20 o C umkristallisieren ließ. Sdp. 131 C/0.001 Torr. Schmp.
5 41 C. 1 H-NM (CDC1 3 ): (s, 3H; C(O)CH 3 ), 2.65 (d, J 3.1 Hz, 2H; SiCH 2 S), 4.96 (t, J 3.6 Hz, J(SiH) Hz, lh; SiH), und (m, loh; SiC 6 H 5 ). 13 C-NM (CDC1 3 ): ~ 10.1 (SiCH 2 S), 30.0 (C(O)CH 3 ), (m-c), (p-c), (i-c), (o-c), (C(O)CH 3 ). 29 Si-NM (c;d 6 ): (Film): 2140 (SiH), 1700 cm- 1 (C=O). MS: mjz 271 (7%, M+- H), 257 (3%, M+- CH 3 ), 195 (100%, M+- C 6 H 5 ), 183 (78%, M+- CH 2 SC(O)CH 3 ), 105 (33%, SiC 6 H;). Gef.: C, 66.6; H, 6.0; Si, C 15 H 16 0SSi (272.4) ber.: C, 66.13; H, 5.92; Si, 10.31%. 61 ( Mercaptomethyl)dimethylsilan (11) Zu einer Suspension von 5.62 g (148 mmol) LiAlH 4 in 100 ml Diethylether wurde unter Eiskühlung und ühren innerhalb von 30 min eine Lösung von g (185 mmol) 9 in 100 ml DiethyletherjPentan (1/1 (vjv)) getropft. Nach beendeter Zugabe ließ man 3.5 h unter ückfluß rühren. Das erkaltete eaktionsgemisch wurde vorsichtig durch Zugabe zu 200 ml 12.5%iger, eisgekühlter Salzsäure hydrolysiert. Man trennte die wässerige Phase ab, extrahierte diese dreimal mit je 40 ml Pentan, trocknete die vereinigten organischen Phasen über Na 2 S0 4, destillierte das Lösungsmittel unter Normaldruck über eine Vigreux-Kolonne ab, destillierte den ückstand fraktionierend über eine Vigreux-Kolonne (die zur Destillation bestimm ten Glasgeräte wurden durch 12stündiges Einwirken von konz. Salzsäure und anschließendes Trocknen auf 150 C vorbehandelt) und destillierte erneut. Es wurden 8.45 g (43%) einer farblosen, übel riechenden Substanz erhalten, Sdp. 104 C. 1 H-NM (C 6 D 6 ): ß (d, J 3.1 Hz, 6H; SiCH 3 ), 0.95 (t, J 7.2 Hz, lh; SH), 1.36 (dd, J 1.1 Hz, J 2.9 Hz, 2H; SiCH 2 S), 3.99 (m, J(SiH) Hz, lh; SiH). 13 C-NM (c;,d 6 ): (SiCH 3 ), 5.6 (SiCH 2 S). 29 Si-NM (C 6 D 6 ): ß (Film): 2120 cm -t (SH). MS: m/ z 105 (100%, M+- H), 91 (21 %, M+- CH 3 ), 73 (43%, M+- SH), 59 (98%, M+- CH 2 SH). Gef.: C, 33.9; H, 9.1. C 3 H 10 SSi (106.3) ber.: C, 33.91; H, 9.49%. (Mercaptomethyl)diphenylsilan (12) Zu einer Suspension von 600 mg (15.8 mmol) LiAH 4 in 30 ml Diethylether wurde bei 0 C unter ühren innerhalb von 10 min eine Lösung von 5.37 g (19.7 mmol) 10 in 20 ml Diethylether getropft. Nach beendeter Zugabe ließ man 7 h unter ückfluss rühren. Das erkaltete eaktionsgemisch wurde unter starkem ühren unter Eiskühlung zu 20 ml 12.5 %iger Salzsäure gegeben, die wässerige Phase abgetrennt und diese dreimal mit je 20 ml Diethylether extrahiert. Man trocknete die vereinigten organischen Phasen über Na 2 S0 4, entfernte das Lösungsmittel unter vermindertem Druck und destillierte den ückstand im Kugelrohrverdampfer ( C/0.1 Torr; die zur Destillation bestimmten Glasgeräte wurden durch 12stündiges Einwirken von konz. Salzsäure und anschließendes Trocknen bei 150 o C vorbehandelt). Es wurden 3.06 g (67%) einer farblosen Flüssigkeit erhalten. 1 H-NM (CDC1 3 ): ß 1.24 {t, J 1.2 Hz, 1H; SH), 2.19 (dd, J 1.1 Hz, J 3.4 Hz, 2H; SiCH 2 S), 4.97 (t, J 3.5 Hz, J(SiH) Hz, lh; SiH), (m, loh; SiC 6 H 5 ). 13 C-NM (CDC1 3 ): (SiCH 2 S), (m-c), (p-c), (i-c), (o-c). 29 Si-NM (C 6 D 6 ): ß (Film): 2130 cm- 1 (SiH). MS: m/z 230 (25%, M+), 183 (100%, M+- CH 2 SH), 105 (9%, SiC 6 Ht). Gef.: C, 68.5; H, 6.4; Si, C 13 H 14 SSi (230.4) ber.: C, 67.77; H, 6.12; Si, 12.19%.
6 62 Untersuchungen zur thermischen Stabilität von 9 und 10 Eine ca. 1 M Lösung von 9 bzw. 10 in C 6 D 6 wurde im abgeschmolzenen NM-öhrchen 30 h auf 180 C erhitzt. 1 H-NM-spektroskopisch konnte keine Veränderung festgestellt werden. Danksagung Diese Arbeit wurde dankenswerterweise von der Deutschen Forschungsgemeinschaft und vom Fonds der Chemischen ndustrie unterstützt. Der Bayer AG danken wir für großzügige Chemikalienspenden. Literatur 1. Tacke, H. Lange und A. Bentlage, Chem. Ber., 115 (1982) Tacke und H. Lange, Chem. Ber., 116 (1983) Tacke, M. Link, A. Bentlage~Felten und H. Zilch, Z. Naturforsch. B, 40 (1985) Tacke, M. Link und H. Zilch, Chem. Ber., 118 (1985) S. Sarge, H.K. Cammenga, B. Becker,. ohr-aehle und. Tacke, J. Thermal Analysis, 33 (1988) Tacke und. ohr-aehle, J. Organomet. Chem. 354 (1988) Laplcin und A.S. Novichkova~ J. Gen. Chem. USS, 43 (1973) 775; Übersetzung aus: Zh. Obshch. Khim., 43 (1973) J.P. Corriu, F. Larcher und G. oyo, J. Organomet. Chem., 129 (1977) Tacke, H. Lange und M.T. Attar-Bashi, Liebigs Ann. Chem., (1982) D. Brandes, J. Organoxnet. Chem. Libr., 7 (1979) H. Schmidbaur und~aldmann, Chem. Ber., 97 (1964) Z.V. Belyakova und S.A. Golubtsov, J. Gen. Chem. USS, 31 (1961) 2966; Übersetzung aus: Zh. Obshch. Khim., 31 (1961) 3178.
Synthese und Eigenschaften von (Hydroxymethyl)diorganylsilanen
 R. Tacke, H. LangeundA. Bentlage 3673 Notizen Synthese und Eigenschaften von (Hydroxymethyl)diorganylsilanen Reinhold Tacke*, Hartwig Lange und Anke Bentlage nstitut für Anorganische Chemie der Technischen
R. Tacke, H. LangeundA. Bentlage 3673 Notizen Synthese und Eigenschaften von (Hydroxymethyl)diorganylsilanen Reinhold Tacke*, Hartwig Lange und Anke Bentlage nstitut für Anorganische Chemie der Technischen
2. Herstellung der α,β-ungesättigten Kupplungskomponenten C H 3 H 33. Br 22 25
 2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
( Acetoxymethyl)methylphenylgerman: Synthese, thermisches V erhalten und olfaktorische Eigenschaften
 !n.t t e ( Acetoxymethyl)methylphenylgerman: Synthese, thermisches V erhalten und olfaktorische Eigenschaften (Acetoxymethyl)methylphenylgermane: Synthesis, Thermal Behaviour and Olfactoric Properties
!n.t t e ( Acetoxymethyl)methylphenylgerman: Synthese, thermisches V erhalten und olfaktorische Eigenschaften (Acetoxymethyl)methylphenylgermane: Synthesis, Thermal Behaviour and Olfactoric Properties
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
1024 Eliminierung von Wasser aus 4-Hydroxy-4-methyl-2- pentanon
 0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Baseninduzierte 1,2-Hydridverschiebungen vom Silicium zum Kohlenstoff: "Anomale" Substitutionsreaktionen an (Halogenmethyl)diorganylsilanen
 1946 R. Tacke, H. Lange und M. T. Attar-Bashi, 1946-1951 Baseninduzierte 1,2-Hydridverschiebungen vom Silicium zum Kohlenstoff: "Anomale" Substitutionsreaktionen an (Halogenmethyl)diorganylsilanen Reinhold
1946 R. Tacke, H. Lange und M. T. Attar-Bashi, 1946-1951 Baseninduzierte 1,2-Hydridverschiebungen vom Silicium zum Kohlenstoff: "Anomale" Substitutionsreaktionen an (Halogenmethyl)diorganylsilanen Reinhold
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
Zum thermischen Verhalten einiger Kohlensäure [(methylphenylsilyl) methyl] ester-derivate
![Zum thermischen Verhalten einiger Kohlensäure [(methylphenylsilyl) methyl] ester-derivate Zum thermischen Verhalten einiger Kohlensäure [(methylphenylsilyl) methyl] ester-derivate](/thumbs/91/107687677.jpg) Zum thermischen Verhalten einiger Kohlensäure [(methylphenylsilyl) methyl] ester-derivate On the Thermal Behaviour of Some (Methylphenylsilyl)methyl Carbonate Derivatives Reinhold Tacke*, Matthias Link,
Zum thermischen Verhalten einiger Kohlensäure [(methylphenylsilyl) methyl] ester-derivate On the Thermal Behaviour of Some (Methylphenylsilyl)methyl Carbonate Derivatives Reinhold Tacke*, Matthias Link,
Mustervorschrift 2.3.1
 Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
3011 Synthese von erythro-9,10-dihydroxystearinsäure aus Ölsäure
 311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
2017 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid
 217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
5 Chemisch-experimenteller Teil
 5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
Experimenteller Teil
 II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol
 3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4002 Synthese von Benzil aus Benzoin
 4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
Darstellung von Chelidamsäure (gekürzte Version)
 CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse
 Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
4010 Synthese von p-methoxyacetophenon aus Anisol
 4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon)
 1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
Organisch-chemisches Praktikum Wintersemester 2005/06. 1-Phenyl-propan-1-ol. Stephan Steinmann
 Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Synthese von Acetessigsäureethylester
 Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
4 Experimenteller Teil
 4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid
 4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren Brombutanen
 1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
Titration von Metallorganylen und Darstellung der dazu benötigten
 Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
NO 2 Rühren mit Magnetrührer, Extrahieren, Ausschütteln, Abrotieren, Umkristallisieren, Abfiltrieren,
 1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von DOC (2,5-Dimethoxy-4-chloramphetamin)
 T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv)
 Cp2(H) Seite 1 Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv) [Cp 2 (H)] H (SCHWARTZ Reagens) Cp2(H) Seite 2 1. Synthese [1,2,3] 1.1 Methode Dicyclopentadien wird in einer Retro-DIELS-ALDER-Reaktion
Cp2(H) Seite 1 Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv) [Cp 2 (H)] H (SCHWARTZ Reagens) Cp2(H) Seite 2 1. Synthese [1,2,3] 1.1 Methode Dicyclopentadien wird in einer Retro-DIELS-ALDER-Reaktion
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid
 2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
Organisches Praktikum I - SS 2006 Assistentin: Gabi Marti. Synthese von. Isobutylacetat. Zürich, Balzers & Eschen, Mai 2005
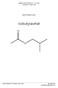 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
3021 Oxidation von Anthracen zu Anthrachinon
 xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
SKRIPT ZUM INTEGRIERTEN SYNTHESEPRAKTIKUM
 Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol
 Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b).
 2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
5009 Synthese von Kupferphthalocyanin
 P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
Synthese von tert-butylchlorid (2-Chloro-2-methylpropan)
 Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
3012 Synthese von Adamantylidenadamantan aus Adamantanon
 Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
6011 Hippursäure aus Glycin und Benzoylchlorid
 P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
2023 Reduktion von D-(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b).
 23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid
 NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
(±)-4-Methyl-3- heptanon
 Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Tris(acetylacetonato)cobalt(III)
 Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
Kaliumdioxalatocuprat(II)- dihydrat
 Kaliumdioxalatocuprat(II)- dihydrat K[Cu(C4)]H Zürich, 17. November 004 Raphael Aardoom, ACP 300 o C 00 50 150 50 ml 100 A N AUS AN AUS 1000 50 ml 0 U/min 1500 50 750 500 1 Synthese 1.1 Methode [1] Kupfer(II)sulfat-pentahydrat
Kaliumdioxalatocuprat(II)- dihydrat K[Cu(C4)]H Zürich, 17. November 004 Raphael Aardoom, ACP 300 o C 00 50 150 50 ml 100 A N AUS AN AUS 1000 50 ml 0 U/min 1500 50 750 500 1 Synthese 1.1 Methode [1] Kupfer(II)sulfat-pentahydrat
4009 Synthese von Adipinsäure aus Cyclohexen
 4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
Dibenzoylmethan
 9.1.2. Dibenzoylmethan Dibenzoylmethan ist eine Stufe eines Zweistufenprärates: Benzoylchlorid (8.1.11) Benzoesäureethylester (8.1.3) Dibenzoylmethan Reaktion: Ansatz: 1,75 g Natrium, 16,0 g Acetophenon,
9.1.2. Dibenzoylmethan Dibenzoylmethan ist eine Stufe eines Zweistufenprärates: Benzoylchlorid (8.1.11) Benzoesäureethylester (8.1.3) Dibenzoylmethan Reaktion: Ansatz: 1,75 g Natrium, 16,0 g Acetophenon,
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
2008 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester
 28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
3002 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure
 32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)-
 Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid
 1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
Chloro(triphenylphosphin)gold(I)
 raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
Berichte OCP1. Manuela Bieri 17. Januar 2007
 Berichte CP1 SYNTESE VN ISAMYLACETAT Manuela Bieri 17. Januar 2007 1 Berichte CP1 1. Methode Isoamylacetat wurde durch eine säurekatalysierte Veresterung von Isoamylalkohol (3-Methyl-1-butanol) mit Essigsäure
Berichte CP1 SYNTESE VN ISAMYLACETAT Manuela Bieri 17. Januar 2007 1 Berichte CP1 1. Methode Isoamylacetat wurde durch eine säurekatalysierte Veresterung von Isoamylalkohol (3-Methyl-1-butanol) mit Essigsäure
Synthese von 3-Menthen
 Synthese von 3-Menthen Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 22/29.11.25 Rémy Denzler, D-Biol 1 1. Methode (-)-Menthol wird in einer säurekatalysierten E1-Eliminierungsreaktion
Synthese von 3-Menthen Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 22/29.11.25 Rémy Denzler, D-Biol 1 1. Methode (-)-Menthol wird in einer säurekatalysierten E1-Eliminierungsreaktion
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Organisch-chemisches Grundpraktikum
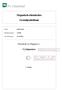 Name: Prakti Kant Matrikelnummer: 123456 Versuchsdatum: 21.10.2016 Protokoll zu Präparat 1: Cyclopenten IUPAC-Name oder Trivialname Diese Abbildung als ACS Document 1996, in 150 % Größe 1. Abgabe 2/5 1
Name: Prakti Kant Matrikelnummer: 123456 Versuchsdatum: 21.10.2016 Protokoll zu Präparat 1: Cyclopenten IUPAC-Name oder Trivialname Diese Abbildung als ACS Document 1996, in 150 % Größe 1. Abgabe 2/5 1
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b
 3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von 1-(p-Tolyl)butan-1,4-diol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid
 NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
Organisch Chemisches Praktikum II. Gruppenpräparat: Darstellung von Z Crotonsäure
 Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 303. Band, Heft 2, Seite 145 148 Verlag Chemie, GmbH, Weinheim / Bergstr. W. Wiegrebe und W. D. Sasse Synthese und Hofmann-Abbau des l-hydroxymethyl-2,2 dimethyl-l,2,3,4-tetrahydroisochinolinium-ions
Sonderdruck aus Archiv der Pharmazie 303. Band, Heft 2, Seite 145 148 Verlag Chemie, GmbH, Weinheim / Bergstr. W. Wiegrebe und W. D. Sasse Synthese und Hofmann-Abbau des l-hydroxymethyl-2,2 dimethyl-l,2,3,4-tetrahydroisochinolinium-ions
S YNTHESE 6: Bis(benzol)chrom(0) [Cr(η 6 -C 6 H 6 ) 2 ] Zürich, WS 04/05 OACP 2
![S YNTHESE 6: Bis(benzol)chrom(0) [Cr(η 6 -C 6 H 6 ) 2 ] Zürich, WS 04/05 OACP 2 S YNTHESE 6: Bis(benzol)chrom(0) [Cr(η 6 -C 6 H 6 ) 2 ] Zürich, WS 04/05 OACP 2](/thumbs/68/58445554.jpg) S YNTHESE 6: Bis(benzol)chrom(0) Cr [Cr(η 6 -C 6 H 6 ) 2 ] Zürich, 1.2.2005 WS 04/05 OACP 2 D-CHAB, ETHZ Raphael Sigrist 1. Synthese 1.1 Methode, Prinzip [1] In einem ersten Schritt wird mit der Fischer-Hafner-Methode,
S YNTHESE 6: Bis(benzol)chrom(0) Cr [Cr(η 6 -C 6 H 6 ) 2 ] Zürich, 1.2.2005 WS 04/05 OACP 2 D-CHAB, ETHZ Raphael Sigrist 1. Synthese 1.1 Methode, Prinzip [1] In einem ersten Schritt wird mit der Fischer-Hafner-Methode,
Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure
 Illumina-Chemie.de - Artikel Synthesen Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure Geräte: Erlenmeyerkolben, Becherglas, Scheidetrichter, Pipetten, Trichter und Faltenfilter Chemikalien: Kaliumhexacyanoferrat(III)
Illumina-Chemie.de - Artikel Synthesen Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure Geräte: Erlenmeyerkolben, Becherglas, Scheidetrichter, Pipetten, Trichter und Faltenfilter Chemikalien: Kaliumhexacyanoferrat(III)
Darstellung von Oxalylchlorid
 Illumina-Chemie.de - Artikel Synthesen Darstellung von Hier wird die Darstellung von aus Oxalsäure-Dihydrat und Phosphorpentachlorid beschrieben, wobei die für die Reaktion nötige wasserfreie Oxalsäure
Illumina-Chemie.de - Artikel Synthesen Darstellung von Hier wird die Darstellung von aus Oxalsäure-Dihydrat und Phosphorpentachlorid beschrieben, wobei die für die Reaktion nötige wasserfreie Oxalsäure
Nickelocen. Bis(cyclopentadienyl)-nickel
 Nickelocen Bis(cyclopentadienyl)-nickel Ni Zürich, 11.1.5 Anna Evans, 1 SYNTHESE 1.1 Methode [1], [] Die Synthese von Nickelocen verläuft über das Cracken von Dicyclopentadien und die Herstellung von Natriumcyclopentadien.
Nickelocen Bis(cyclopentadienyl)-nickel Ni Zürich, 11.1.5 Anna Evans, 1 SYNTHESE 1.1 Methode [1], [] Die Synthese von Nickelocen verläuft über das Cracken von Dicyclopentadien und die Herstellung von Natriumcyclopentadien.
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 03.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 1.1: Einführung in die Laboratoriumstechnik Einleitung Um die in diesem Praktikum verwendeten Glasgeräte
Endersch, Jonas 03.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 1.1: Einführung in die Laboratoriumstechnik Einleitung Um die in diesem Praktikum verwendeten Glasgeräte
Organisch-chemisches Praktikum Wintersemester 2005/06. o-chlortoluen. Stephan Steinmann
 rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
Indan-1,3-dion. Reaktionsgleichung. H- und P-Sätze. Für alle Reagenzien und Produkte. Ausformulierte H- und P-Sätze. Vor(Abschluss)protokoll
 Indan-1,3-dion Reaktionsgleichung H- und P-Sätze Substanz Gefahrensymbol Smp. ( C) Sdp. ( C) Phtalsäurediethylester Essigsäureethylester Flammpkt. ( C) H-Sätze P-Sätze - -40 302 150 - - Gefahr -83 77-4
Indan-1,3-dion Reaktionsgleichung H- und P-Sätze Substanz Gefahrensymbol Smp. ( C) Sdp. ( C) Phtalsäurediethylester Essigsäureethylester Flammpkt. ( C) H-Sätze P-Sätze - -40 302 150 - - Gefahr -83 77-4
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Si-e-SPALTUNG IN 2-THIENYLSILANEN DURCH SEKUNDÄRE AMINE*
 21 Journal o/ Organametallic Chemistry, 172 (1979) 21-29 Elsevier Sequoia S.A., Lausanne - Printed in The Netherlands Si-e-SPALTUNG IN 2-THIENYLSILANEN DURCH SEKUNDÄRE AMINE* REINHOLD TACKE *, EMESE ZIMONYI-HEGEDÜS
21 Journal o/ Organametallic Chemistry, 172 (1979) 21-29 Elsevier Sequoia S.A., Lausanne - Printed in The Netherlands Si-e-SPALTUNG IN 2-THIENYLSILANEN DURCH SEKUNDÄRE AMINE* REINHOLD TACKE *, EMESE ZIMONYI-HEGEDÜS
5. Beschreibung der Versuche
 5. Beschreibung der Versuche Die analytischen Daten wurden mit folgenden Geräten bestimmt: 1 H-NMR: Varian Gemini (300/75 Mhz) IR: Philips PU 9624 FTIR-Spektrometer Elementaranalyse: Leco CHNS-923 UV/VIS:
5. Beschreibung der Versuche Die analytischen Daten wurden mit folgenden Geräten bestimmt: 1 H-NMR: Varian Gemini (300/75 Mhz) IR: Philips PU 9624 FTIR-Spektrometer Elementaranalyse: Leco CHNS-923 UV/VIS:
Synthese: Triphenylcarbinol
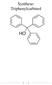 Synthese: Triphenylcarbinol 1 Inhaltsverzeichnis Synthese von Triphenylcarbinol 1.1 Allgemeine Angaben..... 3 1.2 Strukturformel...3 1.3 Reaktionsgleichung.......3 1.4 Ansatz........4 1.5 Ausbeuteberechnung.4
Synthese: Triphenylcarbinol 1 Inhaltsverzeichnis Synthese von Triphenylcarbinol 1.1 Allgemeine Angaben..... 3 1.2 Strukturformel...3 1.3 Reaktionsgleichung.......3 1.4 Ansatz........4 1.5 Ausbeuteberechnung.4
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol
 1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
Synthese von Glutarsäure (1,5-Pentandicarbonsäure)
 Praktikum rganische Chemie I Chemnitz, 07.01.2006 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Glutarsäure (1,5-Pentandicarbonsäure)
Praktikum rganische Chemie I Chemnitz, 07.01.2006 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Glutarsäure (1,5-Pentandicarbonsäure)
Synthese eines Fruchtesters
 Synthese eines Fruchtesters 1/5 Synthese eines Fruchtesters Theorie arbonsäuren können mit Alkoholen unter Abspaltung eines Wasser-Moleküls zu arbonsäure-estern reagieren: ' ' Die Einstellung der Gleichgewichts-Lage
Synthese eines Fruchtesters 1/5 Synthese eines Fruchtesters Theorie arbonsäuren können mit Alkoholen unter Abspaltung eines Wasser-Moleküls zu arbonsäure-estern reagieren: ' ' Die Einstellung der Gleichgewichts-Lage
