3 Moleküle. X = (R 1,R 2,...R M ) und x = (r 1,s 1,r 2,s 2,...r N,s N ).
|
|
|
- Klaus Sommer
- vor 7 Jahren
- Abrufe
Transkript
1 3 Moleküle Bei M gebundenen Atomen werden die gleichen Näherungen wie bei den Atomen zugrunde gelegt, wobei aber die Koordinaten R J der Atomkerne, ihre Massen M J und Ladungen Z J e 0 mit J = 1,2,...M zu berücksichtigen sind. In vielen Fällen genügt es die Atome in der Näherung der unveränderlichen Ionen zu berücksichtigen. Das Atom besteht danach aus einem Ion mit dem Atomkern und den inneren abgeschlossenen Elektronenschalen, die sich in unterschiedlicher chemischer Umgebung nicht verändern, und den Valenzelektronen, die die chemische Bindung verursachen. Die Ladung des Ions entspricht dabei der Anzahl der Valenzelektronen, die sich in einem kugelsymmetrischen effektiven ( atomaren Potenzial v J r RJ ) des Ions am Ort R J befinden. Ist dann N die Anzahl der Valenzelektronen aller Atome zusammen genommen, so verwenden wir für die Kernkoordinaten bzw. die Elektronenkoordinaten die Vektoren im Konfigurationsraum X = (R 1,R 2,...R M ) und x = (r 1,s 1,r 2,s 2,...r N,s N ). Mit den Operatoren der kinetischen Energie der Elektronen T El (x) bzw. der Ionen T Ion (X) T El (x) = N j=1 h2 2m e r 2 j und T Ion (X) = M J=1 h2 2M J schreiben wir den Energieoperator im Produkt-Hilbert-Raum H = H El H Ion in der Form H(x,X) = H El (x,x)+t Ion (X) mit H El (x,x) = T El (x)+v El-Ion (x,x)+v El-El (x)+v Ion-Ion (X)
2 N M mit den Potenzialoperatoren V El-Ion ( (x,x) = v J rj R J ), j=1 J=1 V El-El (x) = e2 0 8πε 0 1,...N i,j i j 1 r i r j und V Ion-Ion (X) = e2 0 8πε 0 1,...M I,J I J Z I Z J R I R J. Bei V El-Ion und V Ion-Ion wird im Falle der Näherung der unveränderlichen Ione davon ausgegangen, dass sich die Ionenladungen nicht mit denen den nächsten Nachbarn überlappen. Nur im Falle einer ( All-Elektronen-Rechnung hat das Ionenpotenzial die Form: v J r RJ ) = Z Je πε 0 r R J. 3.1 Born-Oppenheimer-Näherung Der Massenunterschied zwischen Elektronen und Atomkernen bzw. Ionen ist außer bei Wasserstoff und Helium m e < 10 4, und das ermöglicht näherungsweise eine getrennte Berechnung der Zustände der M J Elektronen und der der Ionen. Nach der klassischen Statistik freier Teilchen hat jeder Freiheitsgrad im Mittel die gleiche Energie: 1 2 m eve 2 = 1 2 M J v2 J, woraus v J me = < 10 2 folgt, sodass sich die Ionen v e M J mit v J viel langsamer bewegen als die Elektronen mit der Geschwindigkeit v e. Deshalb lösen wir in einer ersten Näherung die Schrödinger-Gleichung der Elektronenzustände bei ruhenden Ionen an den Orten X 0 und berücksichtigen anschließend die Ionenbewegung.
3 Mit den Kernkoordinaten X 0 als Parameter lautet dann die Elektronengleichungim Hilbert-Raum H El H El (x,x 0 )φ ν (x,x 0 ) = E El ν (X 0 )φ ν (x,x 0 ) mit φ ν(x,x 0 )φ µ (x,x 0 )dx = δ νµ. Die Eigenwerte E El ν und Eigenfunktionen φ ν hängen vom Parameter X 0 ab, und die allgemeine Eigenwertgleichung des Moleküls im Hilbert-Raum H = H El H Ion lautet H(x,X)Ψ(x,X) = [ ] H El (x,x)+t Ion (X) Ψ(x,X) = EΨ(x,X). Zur Lösung entwickeln wir die Molekülzustände Ψ(x,X) H = H El H Ion nach den Eigenzuständen φ ν (x,x) H El von H El bei festgehaltenem X, die φ µ (x,x) φν (x,x) El = δ µν erfüllen, Ψ(x,X) = µ φ µ (x,x)χ µ (X) mit χ µ (X) = φ µ (x,x) Ψ(x,X) El HIon, wobei El das innere Produkt im Hilbert-Raum H El bezeichnet. Einsetzen liefert HΨ = [ H El (x,x)+t Ion (X) ] Ψ(x,X) = µ H El (x,x)φ µ χ µ + µ T Ion (X)φ µ χ µ = E µ φ µ χ µ = µ E El µ (X)φ µ χ µ + µ M J=1 h2 2M J R 2 φ µ χ µ = E J µ φ µ χ µ.
4 In der Born-Oppenheimer-Näherung werden die beiden Terme der Elektron-Gitter-Wechselwirkung vernachlässigt φ µ χ µ = ( φµ χ ) µ χ µ +φ µ R J R J R J = φ µ χ µ +2 φ µ χ µ φ µ +χ µ R J R J R 2, J und man erhält mithilfe der Näherung µ T Ion φ µ χ µ µ φ µ T Ion χ µ, die Gleichung µ E El µ (X)φ µχ µ + µ φ µ T Ion χ µ = E µ φ µ χ µ, und nach Multiplikation mit φ ν und Integration über die Elektronenkoordinaten x mit der Orthonormalitätsrelation φ ν φ µ El = δ νµ eine Eigenwertgleichung für die Ionen im Hilbert-Raum H Ion [ T Ion (X)+E El ν (X)] χ ν = Eχ ν. Die elektronischen Eigenwerte E El ν (X) bilden also die potenzielle Energie der Ionen im elektronischen Zustand φ ν, und wenn alle Kräfte auf die Atome verschwinden, und das Molekül keine Translationen oder Rotationen ausführt, ergeben sich ihre Ruhelagen X 0 aus ( E El ν (X) ) = 0. X X=X 0
5 Zur praktischen Anwendung zerlegen wir den Energieoperator der Moleküle in drei Teile H = H E +H I +V EI = T El (x)+t Ion (X)+V El-Ion (x,x)+v El-El (x)+v Ion-Ion (X), wobei H E die elektronischen Zustände und H I die der Ionen bestimmt H E = T El (x)+ [ V El-Ion (x,x 0 )+V El-El (x)+v Ion-Ion (X 0 ) ] H I = T Ion (X)+ [ E El ν (X) E El ν (X 0 ) ] V EI = [ V El-Ion (x,x) V El-Ion (x,x 0 ) ] + [ V Ion-Ion (X) V Ion-Ion (X 0 ) ] [ E El ν (X) E El ν (X 0 ) ]. Beim Elektronensystem überwiegt das anziehende Elektron-Ion-Potenzial V El-Ion das Potenzial der elektrostatischenabstoßungderelektronenuntereinanderv El-El unddasderionenv Ion-Ion, sodassdie eckigeklammerbeih E insgesamteineanziehendewechselwirkungdarstellt,diediechemischebindung des Moleküls verursacht. Beim Ionensystem verschwindet das Potenzial, wenn sich alle Atome in ihren RuhelagenX 0 befinden. Der OperatorH I beschreibtsomitdiemolekülschwingungenim elektronischen Zustand φ ν. Der Elektron-Ion-WechselwirkungsoperatorV EI ist die Differenz zwischen H und H E +H I und verschwindet für X = X 0, sodass die Kopplung zwischen Elektronen und Molekülschwingungen für kleine Auslenkungen klein ist und mit steigender Temperatur zunimmt. Die Born-Oppenheimer-Näherung besteht also darin den Operator V EI zu vernachlässigen und die Energie durch den Operator H E +H I zu bestimmen, was eine getrennte Berechnung der elektronischen und der Schwingungseigenschaften ermöglicht.
Vorlesung 21. Identische Teilchen und das Pauli-Prinzip
 Vorlesung 1 Identische Teilchen und das Pauli-Prinzip Identische Teilchen: Jede Art von Teilchen in der Natur definieren wir durch ihre Eigenschaften, z.b. Massen, Spins, Ladungen usw. Das bedeutet, dass
Vorlesung 1 Identische Teilchen und das Pauli-Prinzip Identische Teilchen: Jede Art von Teilchen in der Natur definieren wir durch ihre Eigenschaften, z.b. Massen, Spins, Ladungen usw. Das bedeutet, dass
: Quantenmechanische Lösung H + 2. Molekülion und. Aufstellen der Schrödingergleichung für das H + 2
 H + 2 Die molekulare Bindung : Quantenmechanische Lösung Aufstellen der Schrödingergleichung für das H + 2 Molekülion und Lösung Wichtige Einschränkung: Die Kerne sind festgehalten H Ψ(r) = E Ψ(r) (11)
H + 2 Die molekulare Bindung : Quantenmechanische Lösung Aufstellen der Schrödingergleichung für das H + 2 Molekülion und Lösung Wichtige Einschränkung: Die Kerne sind festgehalten H Ψ(r) = E Ψ(r) (11)
Molekülphysik. April Grundzustand und angeregte Zustände eines Moleküls
 Molekülphysik April 2010 1 Grundzustand und angeregte Zustände eines Moleküls 1.1 Hamiltonoperator für das Gesamtproblem Die Quantenmechanik ist die fundamentale Theorie der Materie. Sowohl die Koordinaten
Molekülphysik April 2010 1 Grundzustand und angeregte Zustände eines Moleküls 1.1 Hamiltonoperator für das Gesamtproblem Die Quantenmechanik ist die fundamentale Theorie der Materie. Sowohl die Koordinaten
Bewegung im elektromagnetischen Feld
 Kapitel 6 Bewegung im elektromagnetischen Feld 6. Hamilton Operator und Schrödinger Gleichung Felder E und B. Aus der Elektrodynamik ist bekannt, dass in einem elektrischen Feld E(r) und einem Magnetfeld
Kapitel 6 Bewegung im elektromagnetischen Feld 6. Hamilton Operator und Schrödinger Gleichung Felder E und B. Aus der Elektrodynamik ist bekannt, dass in einem elektrischen Feld E(r) und einem Magnetfeld
Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt
 Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
5 Anwendung der Dichtefunktionaltheorie
 5 Anwendung der Dichtefunktionaltheorie Im Rahmen der Born-Oppenheimer-Näherung lässt sich der elektronische Grundzustand E g mithilfe der Dichtefunktionaltheorie berechnen, wobei das Einelektronenpotenzial
5 Anwendung der Dichtefunktionaltheorie Im Rahmen der Born-Oppenheimer-Näherung lässt sich der elektronische Grundzustand E g mithilfe der Dichtefunktionaltheorie berechnen, wobei das Einelektronenpotenzial
Quantenzahlen. A B z. Einführung in die Struktur der Materie 67
 Quantenzahlen Wir haben uns bis jetzt nur mit dem Grundzustand des H + 2 Moleküls beschäftigt Wie sieht es aus mit angeregten Zuständen wie z.b. 2p Zuständen im H Atom? Bezeichnung der Molekülorbitale
Quantenzahlen Wir haben uns bis jetzt nur mit dem Grundzustand des H + 2 Moleküls beschäftigt Wie sieht es aus mit angeregten Zuständen wie z.b. 2p Zuständen im H Atom? Bezeichnung der Molekülorbitale
z n z m e 2 WW-Kern-Kern H = H k + H e + H ek
 2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
Gliederung. Potentialenergieflächen für chemische Reaktionen. und konische Durchschneidungen. 1 Born-Oppenheimer-Näherung
 Gliederung Potentialenergieflächen für chemische Reaktionen 1 2 adiabatische und diabatische Potentialflächen 3 Kreuzungsverbot für Potentialflächen, nicht-adiabatische Übergänge und konische Durchschneidungen
Gliederung Potentialenergieflächen für chemische Reaktionen 1 2 adiabatische und diabatische Potentialflächen 3 Kreuzungsverbot für Potentialflächen, nicht-adiabatische Übergänge und konische Durchschneidungen
Da Atome viele ununterscheidbare Elektronen besitzen, sind ihre Zustände durch interelektronische Coulomb- und Austausch-Wechselwirkungen bestimmt.
 12 Moleküle Slide 267 Vorbemerkungen Da Atome viele ununterscheidbare Elektronen besitzen, sind ihre Zustände durch interelektronische Coulomb- und Austausch-Wechselwirkungen bestimmt. Je 2 Elektronen
12 Moleküle Slide 267 Vorbemerkungen Da Atome viele ununterscheidbare Elektronen besitzen, sind ihre Zustände durch interelektronische Coulomb- und Austausch-Wechselwirkungen bestimmt. Je 2 Elektronen
9. Moleküle. 9.1 Wasserstoff-Molekül Ion H Wasserstoff-Molekül H Schwerere Moleküle 9.4 Angeregte Moleküle. Physik IV SS
 9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
Experimentalphysik Modul PH-EP4 / PH-DP-EP4
 6 Moleküle Universität Leipzig, Fakultät für Physik und Geowissenschaften Experimentalphysik Modul PH-EP4 / PH-DP-EP4 Script für Vorlesung 08. Juni 009 Nach der Beschreibung Ein- und Mehrelektronen-Atomen
6 Moleküle Universität Leipzig, Fakultät für Physik und Geowissenschaften Experimentalphysik Modul PH-EP4 / PH-DP-EP4 Script für Vorlesung 08. Juni 009 Nach der Beschreibung Ein- und Mehrelektronen-Atomen
Theoretische Chemie / Computerchemie
 Theoretische Chemie / Computerchemie Bernd Hartke Theoretische Chemie Institut für Physikalische Chemie Christian-Albrechts-Universität Kiel Max-Eyth-Straße 2 Erdgeschoß, Raum 29 Tel.: 43/88-2753 hartke@pctc.uni-kiel.de
Theoretische Chemie / Computerchemie Bernd Hartke Theoretische Chemie Institut für Physikalische Chemie Christian-Albrechts-Universität Kiel Max-Eyth-Straße 2 Erdgeschoß, Raum 29 Tel.: 43/88-2753 hartke@pctc.uni-kiel.de
Die Hartree-Fock-Methode
 February 11, 2016 1 Herleitung der Hartree-Fock-Gleichung 2 Das Heliumatom Gauß sche s-basis Roothaan-Hall-Gleichung Moleküle Herleitung der Hartree-Fock-Gleichung Betrachten wir zunächst das H 2 -Molekül:
February 11, 2016 1 Herleitung der Hartree-Fock-Gleichung 2 Das Heliumatom Gauß sche s-basis Roothaan-Hall-Gleichung Moleküle Herleitung der Hartree-Fock-Gleichung Betrachten wir zunächst das H 2 -Molekül:
10. Das Wasserstoff-Atom Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Die Erwartungswerte von Operatoren sind gegeben durch. (x, t)a (x, t) =h A i
 Die Wahrscheinlichkeit, das System zu einem bestimmten Zeitpunkt in einem bestimmten Zustand anzutreffen, ist durch das Betragsquadrat der Wellenfunktion (x, t) 2 gegeben Die Erwartungswerte von Operatoren
Die Wahrscheinlichkeit, das System zu einem bestimmten Zeitpunkt in einem bestimmten Zustand anzutreffen, ist durch das Betragsquadrat der Wellenfunktion (x, t) 2 gegeben Die Erwartungswerte von Operatoren
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 5. Vorlesung, 25. 4. 2013 Born Oppenheimernäherung, Molekülrotation, Molekülschwingungen
Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 5. Vorlesung, 25. 4. 2013 Born Oppenheimernäherung, Molekülrotation, Molekülschwingungen
TP2: Elektrodynamik WS Arbeitsblatt 10 21/ Dipole und Multipole in stationären Feldern
 TP2: Elektrodynamik WS 2017-2018 Arbeitsblatt 10 21/22.12. 2017 Dipole und Multipole in stationären Feldern Die Multipolentwicklung ist eine hilfreiche Näherung zur Lösung der Poisson Gleichung, wenn eine
TP2: Elektrodynamik WS 2017-2018 Arbeitsblatt 10 21/22.12. 2017 Dipole und Multipole in stationären Feldern Die Multipolentwicklung ist eine hilfreiche Näherung zur Lösung der Poisson Gleichung, wenn eine
Hochschule Düsseldorf University of Applied Sciences. 22. Dezember 2016 HSD. Physik. Schwingungen
 Physik Schwingungen Zusammenfassung Mechanik Physik Mathe Einheiten Bewegung Bewegung 3d Newtons Gesetze Energie Gravitation Rotation Impuls Ableitung, Integration Vektoren Skalarprodukt Gradient Kreuzprodukt
Physik Schwingungen Zusammenfassung Mechanik Physik Mathe Einheiten Bewegung Bewegung 3d Newtons Gesetze Energie Gravitation Rotation Impuls Ableitung, Integration Vektoren Skalarprodukt Gradient Kreuzprodukt
Festkörperelektronik 3. Übung
 Festkörperelektronik 3. Übung Felix Glöckler 02. Juni 2006 1 Übersicht Themen heute: Motivation Ziele Rückblick Quantenmechanik Aufgabentypen/Lösungsmethoden in der QM Stückweise konstante Potentiale Tunneln
Festkörperelektronik 3. Übung Felix Glöckler 02. Juni 2006 1 Übersicht Themen heute: Motivation Ziele Rückblick Quantenmechanik Aufgabentypen/Lösungsmethoden in der QM Stückweise konstante Potentiale Tunneln
Theoretische Physik: Mechanik
 Ferienkurs Theoretische Physik: Mechanik Blatt 4 - Lösung Technische Universität München 1 Fakultät für Physik 1 Zwei Kugeln und der Satz von Steiner Nehmen Sie zwei Kugeln mit identischem Radius R und
Ferienkurs Theoretische Physik: Mechanik Blatt 4 - Lösung Technische Universität München 1 Fakultät für Physik 1 Zwei Kugeln und der Satz von Steiner Nehmen Sie zwei Kugeln mit identischem Radius R und
Das Bohrsche Atommodell
 Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
Ferienkurs Quantenmechanik - Probeklausur
 Seite Ferienkurs Quantenmechanik - Sommersemester 5 Fabian Jerzembeck und Sebastian Steinbeiÿer Fakultät für Physik Technische Universität München Aufgabe FRAGEN ( BE): a) Wie lautet die zeitabhängige
Seite Ferienkurs Quantenmechanik - Sommersemester 5 Fabian Jerzembeck und Sebastian Steinbeiÿer Fakultät für Physik Technische Universität München Aufgabe FRAGEN ( BE): a) Wie lautet die zeitabhängige
H LS = W ( r) L s, (2)
 Vorlesung 5 Feinstruktur der Atomspektren Wir betrachten ein Wasserstoffatom. Die Energieeigenwerte des diskreten Spektrums lauten E n = mα c n, (1 wobei α 1/137 die Feinstrukturkonstante, m die Elektronmasse
Vorlesung 5 Feinstruktur der Atomspektren Wir betrachten ein Wasserstoffatom. Die Energieeigenwerte des diskreten Spektrums lauten E n = mα c n, (1 wobei α 1/137 die Feinstrukturkonstante, m die Elektronmasse
Moleküle und Wärmestatistik
 Moleküle und Wärmestatistik Musterlösung.08.008 Molekülbindung Ein Molekül bestehe aus zwei Atomkernen A und B und zwei Elektronen. a) Wie lautet der Ansatz für die symmetrische Wellenfunktion in der Molekülorbitalnäherung?
Moleküle und Wärmestatistik Musterlösung.08.008 Molekülbindung Ein Molekül bestehe aus zwei Atomkernen A und B und zwei Elektronen. a) Wie lautet der Ansatz für die symmetrische Wellenfunktion in der Molekülorbitalnäherung?
Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten oder in Festkörpern vor.
 phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
Physikalische Ursachen der Molekülbindung
 Physikalische Ursachen der Molekülbindung Molekülbindungen können auf verschiedene Arten entstehen: gemeinsame Elektronen durch räumliche Umrodnung der W keitverteilung - - + + Verringerung der kinetischen
Physikalische Ursachen der Molekülbindung Molekülbindungen können auf verschiedene Arten entstehen: gemeinsame Elektronen durch räumliche Umrodnung der W keitverteilung - - + + Verringerung der kinetischen
TC1 Grundlagen der Theoretischen Chemie
 TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Sarah Römer (roemer@em.uni-frankfurt.de) Simona Scheit (simona.scheit@googlemail.com) Juanma
TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Sarah Römer (roemer@em.uni-frankfurt.de) Simona Scheit (simona.scheit@googlemail.com) Juanma
Störungstheorie. Kapitel Motivation. 8.2 Zeitunabhängige Störungstheorie (Rayleigh-Schrödinger) nicht-entartete Störungstheorie
 Kapitel 8 Störungstheorie 8.1 Motivation Die meisten quantenmechanischen Problemstellungen lassen sich (leider) nicht exakt lösen. So kommt zum Beispiel der harmonische Oszillator in der Natur in Reinform
Kapitel 8 Störungstheorie 8.1 Motivation Die meisten quantenmechanischen Problemstellungen lassen sich (leider) nicht exakt lösen. So kommt zum Beispiel der harmonische Oszillator in der Natur in Reinform
k m = 2 f (Frequenz) k = 2 m gilt näherungsweise für alle Schwingungen, falls die Auslenkungen klein genug sind (ähnliches Potential ähnliche Kraft)
 8. Der lineare harmonische Oszillator (1D) klass.: E = k m = f (Frequenz) x k = m U = k x = m x m größer -> ω kleiner (deuterierte Moleküle) gilt näherungsweise für alle Schwingungen, falls die Auslenkungen
8. Der lineare harmonische Oszillator (1D) klass.: E = k m = f (Frequenz) x k = m U = k x = m x m größer -> ω kleiner (deuterierte Moleküle) gilt näherungsweise für alle Schwingungen, falls die Auslenkungen
6.2 Kovalente Bindung + + r B. r AB. πε0. Ĥ Nicht separierbar. Einfachstes Molekül: Hamiltonoperator: Kinetische Energie. Potentielle Energie
 6. Kovalente indung Einfachstes Molekül: - r H + r + + r e Hamiltonoperator: Ĥ ħ ħ ħ = + m m Kern Kern e me Elektron Kinetische Energie + e 1 1 1 4 πε r r r Kern Kern e nziehung bstoßung Kern Kern e nziehung
6. Kovalente indung Einfachstes Molekül: - r H + r + + r e Hamiltonoperator: Ĥ ħ ħ ħ = + m m Kern Kern e me Elektron Kinetische Energie + e 1 1 1 4 πε r r r Kern Kern e nziehung bstoßung Kern Kern e nziehung
5. Atome mit 1 und 2 Leucht-Elektronen 5.1 Alkali-Atome 5.2 He-Atom
 5. Atome mit 1 und 2 Leucht- 5.1 Alkali-Atome 5.2 He-Atom 5.1 5.1 Alkali Atome ein "Leuchtelektron" Alkali Erdalkali 5.2 Tauchbahnen grosser Bahndrehimpuls l: geringes Eintauchen kleiner Bahndrehimpuls
5. Atome mit 1 und 2 Leucht- 5.1 Alkali-Atome 5.2 He-Atom 5.1 5.1 Alkali Atome ein "Leuchtelektron" Alkali Erdalkali 5.2 Tauchbahnen grosser Bahndrehimpuls l: geringes Eintauchen kleiner Bahndrehimpuls
Kapitel 2. Zeitunabhängige Störungstheorie. 2.1 Ohne Entartung der ungestörten Energie Niveaus
 Kapitel Zeitunabhängige Störungstheorie.1 Ohne Entartung der ungestörten Energie Niveaus Näherungs-Verfahren In den meisten Fällen läßt sich die Schrödinger Gleichung nicht streng lösen. Aus diesem Grund
Kapitel Zeitunabhängige Störungstheorie.1 Ohne Entartung der ungestörten Energie Niveaus Näherungs-Verfahren In den meisten Fällen läßt sich die Schrödinger Gleichung nicht streng lösen. Aus diesem Grund
Theoretische Physik I: Lösungen Blatt Michael Czopnik
 Theoretische Physik I: Lösungen Blatt 2 15.10.2012 Michael Czopnik Aufgabe 1: Scheinkräfte Nutze Zylinderkoordinaten: x = r cos ϕ y = r sin ϕ z = z Zweimaliges differenzieren ergibt: ẍ = r cos ϕ 2ṙ ϕ sin
Theoretische Physik I: Lösungen Blatt 2 15.10.2012 Michael Czopnik Aufgabe 1: Scheinkräfte Nutze Zylinderkoordinaten: x = r cos ϕ y = r sin ϕ z = z Zweimaliges differenzieren ergibt: ẍ = r cos ϕ 2ṙ ϕ sin
Vorlesung Statistische Mechanik: N-Teilchensystem
 Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
3.7 Das magnetische Feld in Materie
 15 KAPITEL 3. MAGNETOSTATIK 3.7 Das magnetische Feld in Materie Wie wir in den vorangegangenen Kapiteln bereits gesehen haben, wird die magnetische Induktionsdichte B durch ein Vektorpotenzial A charakterisiert,
15 KAPITEL 3. MAGNETOSTATIK 3.7 Das magnetische Feld in Materie Wie wir in den vorangegangenen Kapiteln bereits gesehen haben, wird die magnetische Induktionsdichte B durch ein Vektorpotenzial A charakterisiert,
Kapitel 6. Der Lagrange-Formalismus. 6.2 Lagrange-Funktion in der relativistischen Feldtheorie. 6.1 Euler-Lagrange-Gleichung
 92 Teilchenphysik, HS 2007-SS 2008, Prof. A. Rubbia (ETH Zurich) 6.2 Lagrange-Funktion in der relativistischen Felheorie Kapitel 6 Der Lagrange-Formalismus 6.1 Euler-Lagrange-Gleichung In der Quantenmechanik
92 Teilchenphysik, HS 2007-SS 2008, Prof. A. Rubbia (ETH Zurich) 6.2 Lagrange-Funktion in der relativistischen Felheorie Kapitel 6 Der Lagrange-Formalismus 6.1 Euler-Lagrange-Gleichung In der Quantenmechanik
Theoretische Chemie (TC II) Computational Chemistry
 Theoretische Chemie (TC II) Computational Chemistry Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Dr. Matthias Ruckenbauer (matruc@theochem.uni-frankfurt.de) Dr. Haleh Hashemi
Theoretische Chemie (TC II) Computational Chemistry Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Dr. Matthias Ruckenbauer (matruc@theochem.uni-frankfurt.de) Dr. Haleh Hashemi
6 Der Harmonische Oszillator
 6 Der Harmonische Oszillator Ein Teilchen der Masse m bewege sich auf der x-achse unter dem Einfluß der Rückstellkraft Fx = mω x. 186 Die Kreisfrequenz ω bzw. die Federkonstante k := mω ist neben der Masse
6 Der Harmonische Oszillator Ein Teilchen der Masse m bewege sich auf der x-achse unter dem Einfluß der Rückstellkraft Fx = mω x. 186 Die Kreisfrequenz ω bzw. die Federkonstante k := mω ist neben der Masse
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Quantenmechanik 2009
 Ferienkurs Quantenmechanik 2009 Grundlagen der Quantenmechanik Vorlesungsskript für den 3. August 2009 Christoph Schnarr Inhaltsverzeichnis 1 Axiome der Quantenmechanik 2 2 Mathematische Struktur 2 2.1
Ferienkurs Quantenmechanik 2009 Grundlagen der Quantenmechanik Vorlesungsskript für den 3. August 2009 Christoph Schnarr Inhaltsverzeichnis 1 Axiome der Quantenmechanik 2 2 Mathematische Struktur 2 2.1
Dr. Jan Friedrich Nr
 Übungen zu Experimentalphysik 4 - Lösungsvorschläge Prof. S. Paul Sommersemester 5 Dr. Jan Friedrich Nr. 4.7.5 Email Jan.Friedrich@ph.tum.de Telefon 89/89-586 Physik Department E8, Raum 564 http://www.e8.physik.tu-muenchen.de/teaching/phys4/
Übungen zu Experimentalphysik 4 - Lösungsvorschläge Prof. S. Paul Sommersemester 5 Dr. Jan Friedrich Nr. 4.7.5 Email Jan.Friedrich@ph.tum.de Telefon 89/89-586 Physik Department E8, Raum 564 http://www.e8.physik.tu-muenchen.de/teaching/phys4/
Vorlesung Physikalische Chemie IV Handout 1: Einführung in die elektronische Strukturtheorie
 Dr Martin O Steinhauser Universität Basel Physikalische Chemie IV (Teil 2) Herbstsemester 2014 Vorlesung Physikalische Chemie IV Handout 1: Einführung in die elektronische Strukturtheorie 1 Einleitung
Dr Martin O Steinhauser Universität Basel Physikalische Chemie IV (Teil 2) Herbstsemester 2014 Vorlesung Physikalische Chemie IV Handout 1: Einführung in die elektronische Strukturtheorie 1 Einleitung
Gesamtdrehimpuls Spin-Bahn-Kopplung
 Gesamtdrehimpuls Spin-Bahn-Kopplung > 0 Elektron besitzt Bahndrehimpuls L und S koppeln über die resultierenden Magnetfelder (Spin-Bahn-Kopplung) Vektoraddition zum Gesamtdrehimpuls J = L + S Für J gelten
Gesamtdrehimpuls Spin-Bahn-Kopplung > 0 Elektron besitzt Bahndrehimpuls L und S koppeln über die resultierenden Magnetfelder (Spin-Bahn-Kopplung) Vektoraddition zum Gesamtdrehimpuls J = L + S Für J gelten
Ferienkurs Quantenmechanik I WKB-Näherung und Störungstheorie
 Ferienkurs Quantenmechanik I WKB-Näherung und Störungstheorie Sebastian Wild Freitag, 6.. Inhaltsverzeichnis Die WKB-Näherung. Grundlegendes............................. Tunnelwahrscheinlichkeit.......................
Ferienkurs Quantenmechanik I WKB-Näherung und Störungstheorie Sebastian Wild Freitag, 6.. Inhaltsverzeichnis Die WKB-Näherung. Grundlegendes............................. Tunnelwahrscheinlichkeit.......................
Quantenchemie WS 2008/2009 Zusammenfassung 1. Teil
 Quantenchemie WS 2008/2009 Zusammenfassung 1. Teil 1. Grundlagen der Quantenmechanik (a) Wellenfunktion: Die Wellenfunktion Ψ(x, t) beschreibt den quantenmechanischen Zustand eines Teilchens am Ort x zur
Quantenchemie WS 2008/2009 Zusammenfassung 1. Teil 1. Grundlagen der Quantenmechanik (a) Wellenfunktion: Die Wellenfunktion Ψ(x, t) beschreibt den quantenmechanischen Zustand eines Teilchens am Ort x zur
Übungsblatt 06. PHYS4100 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, oder 3. 6.
 Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
1.4 Die Dirac-Gleichung
 .4 Die Dirac-Gleichung Suche Differentialgleichung. Ordnung in der Zeit, relativistische Kovarianz. Ordnung auch in Ortskoordinaten 2. Vorlesung, 9.4.2 H rel Ψ = i Ψ t (ħ = c = ) zu bestimmen Ansatz: H
.4 Die Dirac-Gleichung Suche Differentialgleichung. Ordnung in der Zeit, relativistische Kovarianz. Ordnung auch in Ortskoordinaten 2. Vorlesung, 9.4.2 H rel Ψ = i Ψ t (ħ = c = ) zu bestimmen Ansatz: H
PC III Aufbau der Materie
 PC III Aufbau der Materie Kapitel 3 Einfache Anwendungen Vorlesung: http://www.pci.tu-bs.de/aggericke/pc3 Übung: http://www.pci.tu-bs.de/aggericke/pc3/uebungen Die Schrödingergleichung zeitunabhängige
PC III Aufbau der Materie Kapitel 3 Einfache Anwendungen Vorlesung: http://www.pci.tu-bs.de/aggericke/pc3 Übung: http://www.pci.tu-bs.de/aggericke/pc3/uebungen Die Schrödingergleichung zeitunabhängige
in Molekülen: möglicherweise unterschiedliche Polarisierbarkeiten in verschiedenen Richtungen p = ᾱ E
 orlesung Dienstag. Maxwellgleichungen der Elektrostatik E = ρ ɛ 0 () B = 0 (2) E = 0 (3) B = µ 0 j (4).2 Polarisation Einteilung der Materie - Leiter (freie Ladungsträger) - Isolatoren (nur gebundene Ladungsträger)
orlesung Dienstag. Maxwellgleichungen der Elektrostatik E = ρ ɛ 0 () B = 0 (2) E = 0 (3) B = µ 0 j (4).2 Polarisation Einteilung der Materie - Leiter (freie Ladungsträger) - Isolatoren (nur gebundene Ladungsträger)
Das Noether-Theorem. Philipp Arras, Jakob Moritz. 18. Juli Quellen 6
 Das Noether-Theorem Philipp Arras, Jakob Moritz 18. Juli 013 Inhaltsverzeichnis 1 Herleitung des Noether-Theorems in der Feldtheorie 1 1.1 Voraussetzungen.......................................... 1 1.
Das Noether-Theorem Philipp Arras, Jakob Moritz 18. Juli 013 Inhaltsverzeichnis 1 Herleitung des Noether-Theorems in der Feldtheorie 1 1.1 Voraussetzungen.......................................... 1 1.
Im Folgenden finden Sie den Text der am geschriebenen Theorie D-Klausur, sowie Lösungen zu den einzelnen Aufgaben. Diese Lösungen sind
 Im Folgenden finden Sie den Text der am 28.7.2010 geschriebenen Theorie D-Klausur, sowie Lösungen zu den einzelnen Aufgaben. Diese Lösungen sind unter Umständen nicht vollständig oder perfekt, und sie
Im Folgenden finden Sie den Text der am 28.7.2010 geschriebenen Theorie D-Klausur, sowie Lösungen zu den einzelnen Aufgaben. Diese Lösungen sind unter Umständen nicht vollständig oder perfekt, und sie
Wir haben gesehen, dass wir den Wirkungsquerschnitt als eine Summe über Partialwellen. l=0
 Vorlesung 11 Streuung bei nieigen Energien Wir haben gesehen, dass wir den Wirkungsquerschnitt als eine Summe über Partialwellen darstellen können σ = 4π k l + 1 sin δ l. 1 l= Allerdings hat diese Reihe
Vorlesung 11 Streuung bei nieigen Energien Wir haben gesehen, dass wir den Wirkungsquerschnitt als eine Summe über Partialwellen darstellen können σ = 4π k l + 1 sin δ l. 1 l= Allerdings hat diese Reihe
Stark-Effekt für entartete Zustände
 Stark-Effekt für entartete Zustände Die Schrödingergleichung für das Elektron im Wasserstoff lautet H nlm = n nlm mit H = p2 e2 2 m e 4 r Die Eigenfunktion und Eigenwerte dieses ungestörten Systems sind
Stark-Effekt für entartete Zustände Die Schrödingergleichung für das Elektron im Wasserstoff lautet H nlm = n nlm mit H = p2 e2 2 m e 4 r Die Eigenfunktion und Eigenwerte dieses ungestörten Systems sind
Klein-Gordon-Gleichung
 Seminar zur Theorie der Atome, Kerne und kondensierten Matierie Klein-Gordon-Gleichung Judith Beier 17.12.2014 1 Inhaltsverzeichnis 1 Einblick in die Geschichte der relativistischen Quantenmechanik 3 2
Seminar zur Theorie der Atome, Kerne und kondensierten Matierie Klein-Gordon-Gleichung Judith Beier 17.12.2014 1 Inhaltsverzeichnis 1 Einblick in die Geschichte der relativistischen Quantenmechanik 3 2
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie. Messungen in der Quantenmechanik
 Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Das H + 2 -Molekülion
 Das Näherungen für das elektronische Problem und Kernbewegungen 7. Dezember 2011 Schrödinger-Gleichung des s Abbildung: Arthur Beiser; Atome, Moleküle, Festkörper; Vieweg, Braunschweig 1983 ( K/E 2 2 +
Das Näherungen für das elektronische Problem und Kernbewegungen 7. Dezember 2011 Schrödinger-Gleichung des s Abbildung: Arthur Beiser; Atome, Moleküle, Festkörper; Vieweg, Braunschweig 1983 ( K/E 2 2 +
Theoretische Chemie (TC II) Computational Chemistry
 Theoretische Chemie (TC II) Computational Chemistry Lecture 2 28/10/2011 Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Vorlesung: Mi 11h30-13h, Fr 8h-9h30 Praktikum (gemäß Ankündigung, statt Vorlesung):
Theoretische Chemie (TC II) Computational Chemistry Lecture 2 28/10/2011 Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Vorlesung: Mi 11h30-13h, Fr 8h-9h30 Praktikum (gemäß Ankündigung, statt Vorlesung):
Klausur zur Vorlesung Physikalische Chemie II: Aufbau der Materie / Kinetik
 Name:... Vorname:... Matrikelnummer:. geb. am:... in:... Klausur zur Vorlesung Physikalische Chemie II: Aufbau der Materie / Kinetik WS 2007/2008 am 5.02.2008 Zugelassene Hilfsmittel: Taschenrechner. Naturkonstanten
Name:... Vorname:... Matrikelnummer:. geb. am:... in:... Klausur zur Vorlesung Physikalische Chemie II: Aufbau der Materie / Kinetik WS 2007/2008 am 5.02.2008 Zugelassene Hilfsmittel: Taschenrechner. Naturkonstanten
11. Quantenchemische Methoden
 Computeranwendung in der Chemie Informatik für Chemiker(innen) 11. Quantenchemische Methoden Jens Döbler 2004 "Computer in der Chemie", WS 2003-04, Humboldt-Universität VL11 Folie 1 Grundlagen Moleküle
Computeranwendung in der Chemie Informatik für Chemiker(innen) 11. Quantenchemische Methoden Jens Döbler 2004 "Computer in der Chemie", WS 2003-04, Humboldt-Universität VL11 Folie 1 Grundlagen Moleküle
Einführung in die Boltzmann-Gleichung. Flavius Guiaş Universität Dortmund
 Einführung in die Boltzmann-Gleichung Flavius Guiaş Universität Dortmund Antrittsvorlesung, 19.04.2007 INHALT 1 Herleitung der Boltzmann-Gleichung 2 Boltzmann-Ungleichung und Maxwell-Verteilung 3 H-Theorem
Einführung in die Boltzmann-Gleichung Flavius Guiaş Universität Dortmund Antrittsvorlesung, 19.04.2007 INHALT 1 Herleitung der Boltzmann-Gleichung 2 Boltzmann-Ungleichung und Maxwell-Verteilung 3 H-Theorem
HÖHERE PHYSIK SKRIPTUM VORLESUNGBLATT XI
 Prof. Dr. F. Koch Dr. H. E. Porteanu fkoch@ph.tum.de porteanu@ph.tum.de WS 4-5 HÖHEE PHYSIK SKIPTUM VOLESUNGBLATT XI 4..5 Molekülphysik Atome binden zu Molekülen und Festkörpern durch interatomare Kräfte
Prof. Dr. F. Koch Dr. H. E. Porteanu fkoch@ph.tum.de porteanu@ph.tum.de WS 4-5 HÖHEE PHYSIK SKIPTUM VOLESUNGBLATT XI 4..5 Molekülphysik Atome binden zu Molekülen und Festkörpern durch interatomare Kräfte
Atome im elektrischen Feld
 Kapitel 3 Atome im elektrischen Feld 3.1 Beobachtung und experimenteller Befund Unter dem Einfluss elektrischer Felder kommt es zur Frequenzverschiebung und Aufspaltung in optischen Spektren. Dieser Effekt
Kapitel 3 Atome im elektrischen Feld 3.1 Beobachtung und experimenteller Befund Unter dem Einfluss elektrischer Felder kommt es zur Frequenzverschiebung und Aufspaltung in optischen Spektren. Dieser Effekt
Atomphysik Klasse 9. Aufgabe: Fülle die freien Felder aus!
 1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
(a) Λ ist eine Erhaltungsgröße. (b) Λ ist gleich der Exzentrizität ε der Bahnkurve.
 PD Dr. S. Mertens S. Falkner, S. Mingramm Theoretische Physik I Mechanik Blatt 7 WS 007/008 0.. 007. Lenz scher Vektor. Für die Bahn eines Teilchens der Masse m im Potential U(r) = α/r definieren wir mit
PD Dr. S. Mertens S. Falkner, S. Mingramm Theoretische Physik I Mechanik Blatt 7 WS 007/008 0.. 007. Lenz scher Vektor. Für die Bahn eines Teilchens der Masse m im Potential U(r) = α/r definieren wir mit
Relativistische Quantenmechanik und die Klein-Gordon Gleichung
 Relativistische Quantenmechanik und die Klein-Gordon Gleichung Oliver Smith o smit01 wwu.de) 17. Februar 2015 Wir wollen die Klein-Gordon Gleichung untersuchen und Formalismen einführen, um Parallelen
Relativistische Quantenmechanik und die Klein-Gordon Gleichung Oliver Smith o smit01 wwu.de) 17. Februar 2015 Wir wollen die Klein-Gordon Gleichung untersuchen und Formalismen einführen, um Parallelen
Der harmonische Oszillator anhand eines Potentials
 Quantenmechanikvorlesung, Prof. Lang, SS04 Der harmonische Oszillator anhand eines Potentials Christine Krasser - Tanja Sinkovic - Sibylle Gratt - Stefan Schausberger - Klaus Passler Einleitung In der
Quantenmechanikvorlesung, Prof. Lang, SS04 Der harmonische Oszillator anhand eines Potentials Christine Krasser - Tanja Sinkovic - Sibylle Gratt - Stefan Schausberger - Klaus Passler Einleitung In der
Theoretische Physik 4 - Blatt 1
 Theoretische Physik 4 - Blatt 1 Christopher Bronner, Frank Essenberger FU Berlin 21.Oktober.2006 Inhaltsverzeichnis 1 Compton-Effekt 1 2 Bohrsches Atommodell 2 2.1 Effektives Potential..........................
Theoretische Physik 4 - Blatt 1 Christopher Bronner, Frank Essenberger FU Berlin 21.Oktober.2006 Inhaltsverzeichnis 1 Compton-Effekt 1 2 Bohrsches Atommodell 2 2.1 Effektives Potential..........................
1 Kristallsymmetrie. 1.1 Punkttransformationen und Translationen
 Inhalt Einleitung...................................................................... 3 Kristallsymmetrie.............................................................. 4. Punkttransformationen und Translationen..................................
Inhalt Einleitung...................................................................... 3 Kristallsymmetrie.............................................................. 4. Punkttransformationen und Translationen..................................
Klassische Theoretische Physik II. V: Prof. Dr. M. Mühlleitner, Ü: Dr. M. Rauch. Klausur 1 Lösung. 27. Juli 2015, Uhr
 KIT SS 05 Klassische Theoretische Physik II V: Prof. Dr. M. Mühlleitner, Ü: Dr. M. Rauch Klausur Lösung 7. Juli 05, 6-8 Uhr Aufgabe : Kurzfragen (+4++3=0 Punkte) (a) Zwangsbedingungen beschreiben Einschränkungen
KIT SS 05 Klassische Theoretische Physik II V: Prof. Dr. M. Mühlleitner, Ü: Dr. M. Rauch Klausur Lösung 7. Juli 05, 6-8 Uhr Aufgabe : Kurzfragen (+4++3=0 Punkte) (a) Zwangsbedingungen beschreiben Einschränkungen
UNIVERSITÄT GREIFSWALD. Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE. Arbeitskreis Biophysikalische Chemie
 UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Biophysikalische Chemie Prof. Dr. Walter Langel Modelle für elektronische Zustände Einfachstes klassisches
UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Biophysikalische Chemie Prof. Dr. Walter Langel Modelle für elektronische Zustände Einfachstes klassisches
ν und λ ausgedrückt in Energie E und Impuls p
 phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
TC1 Grundlagen der Theoretischen Chemie
 TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Robert Binder (rbinder@theochem.uni-frankfurt.de) Madhava Niraghatam (niraghatam@chemie.uni-frankfurt.de)
TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Robert Binder (rbinder@theochem.uni-frankfurt.de) Madhava Niraghatam (niraghatam@chemie.uni-frankfurt.de)
n 2 2 n n 2 1 cos 2 {θ} = n 1 cos{θ} 1 r 1 + r
 Elektromagnetische Felder und Wellen: zur Klausur Frühjahr 22 Aufgabe 3 Punkte) Das elektrische Feld liegt parallel zur Grenzfläche, also ist die Welle TE- polarisiert Der Reflektionsfaktor ist laut Skript
Elektromagnetische Felder und Wellen: zur Klausur Frühjahr 22 Aufgabe 3 Punkte) Das elektrische Feld liegt parallel zur Grenzfläche, also ist die Welle TE- polarisiert Der Reflektionsfaktor ist laut Skript
Gruppentheorie ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD. Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE
 ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie. Messungen in der Quantenmechanik
 Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
10.6 Mehratomige ideale Gase
 10.6 Mehratomige ideale Gase Wir wenden uns jetzt dem Problem molekularer idealer Quantengase zu. 10.6.1 Quantenmechanik der starren Hantel Eine starre Hantel aus zwei Punktmassen m 1 und m 2, die durch
10.6 Mehratomige ideale Gase Wir wenden uns jetzt dem Problem molekularer idealer Quantengase zu. 10.6.1 Quantenmechanik der starren Hantel Eine starre Hantel aus zwei Punktmassen m 1 und m 2, die durch
Ferienkurs Theoretische Mechanik. Mechanik des starren Körpers
 Ferienkurs Theoretische Mechanik Mechanik des starren Körpers Sebastian Wild Freitag, 16.09.011 Inhaltsverzeichnis 1 Einführung und Definitionen Kinetische Energie und Trägheitstensor 4.1 Definition des
Ferienkurs Theoretische Mechanik Mechanik des starren Körpers Sebastian Wild Freitag, 16.09.011 Inhaltsverzeichnis 1 Einführung und Definitionen Kinetische Energie und Trägheitstensor 4.1 Definition des
10. Innere Koordinaten/Kraftfelder
 Computeranwendung in der Chemie Informatik für Chemiker(innen) 10. Innere Koordinaten/Kraftfelder Jens Döbler 2004 "Computer in der Chemie", WS 2003-04, Humboldt-Universität VL10 Folie 1 Dr. Jens Döbler
Computeranwendung in der Chemie Informatik für Chemiker(innen) 10. Innere Koordinaten/Kraftfelder Jens Döbler 2004 "Computer in der Chemie", WS 2003-04, Humboldt-Universität VL10 Folie 1 Dr. Jens Döbler
Physikalische Chemie I SS 2018
 Physikalische Chemie I SS 2018 Vorlesung für BA Chemie und BA Nanoscience Prof. Dr. K. Hauser Fachbereich Chemie Karin.Hauser@uni-konstanz.de Advance Organizer Polymerchemie Kolloidchemie Molekülanalytik
Physikalische Chemie I SS 2018 Vorlesung für BA Chemie und BA Nanoscience Prof. Dr. K. Hauser Fachbereich Chemie Karin.Hauser@uni-konstanz.de Advance Organizer Polymerchemie Kolloidchemie Molekülanalytik
7.3 Der quantenmechanische Formalismus
 Dieter Suter - 389 - Physik B3 7.3 Der quantenmechanische Formalismus 7.3.1 Historische Vorbemerkungen Die oben dargestellten experimentellen Hinweise wurden im Laufe der ersten Jahrzehnte des 20. Jahrhunderts
Dieter Suter - 389 - Physik B3 7.3 Der quantenmechanische Formalismus 7.3.1 Historische Vorbemerkungen Die oben dargestellten experimentellen Hinweise wurden im Laufe der ersten Jahrzehnte des 20. Jahrhunderts
Chern-Simons Theorie. Thomas Unden, Sabrina Kröner 01. Feb Theorie der kondensierten Materie. Fraktionaler Quanten-Hall-Effekt
 Chern-Simons Theorie Thomas Unden, Sabrina Kröner 01. Feb. 2012 Theorie der kondensierten Materie Fraktionaler Quanten-Hall-Effekt Seite 2 Chern-Simons Theorie Thomas Unden, Sabrina Kröner 01. Feb. 2012
Chern-Simons Theorie Thomas Unden, Sabrina Kröner 01. Feb. 2012 Theorie der kondensierten Materie Fraktionaler Quanten-Hall-Effekt Seite 2 Chern-Simons Theorie Thomas Unden, Sabrina Kröner 01. Feb. 2012
ORGANISCHE CHEMIE 1. Stoff der 15. Vorlesung: Atommodell, Bindungsmodell...
 Stoff der 15. Vorlesung: Atommodell, Bindungsmodell... ORGANISCHE CHEMIE 1 15. Vorlesung, Dienstag, 07. Juni 2013 - Einelektronensysteme: H-Atom s,p,d Orbital - Mehrelektronensysteme: He-Atom Pauli-Prinzip,
Stoff der 15. Vorlesung: Atommodell, Bindungsmodell... ORGANISCHE CHEMIE 1 15. Vorlesung, Dienstag, 07. Juni 2013 - Einelektronensysteme: H-Atom s,p,d Orbital - Mehrelektronensysteme: He-Atom Pauli-Prinzip,
Theoretische Physik: Mechanik
 Ferienkurs Theoretische Physik: Mechanik Sommer 2013 Probeklausur Technische Universität München 1 Fakultät für Physik 1 Kurze Fragen [20 Punkte] Beantworten Sie folgende Fragen. Für jede richtige Antwort
Ferienkurs Theoretische Physik: Mechanik Sommer 2013 Probeklausur Technische Universität München 1 Fakultät für Physik 1 Kurze Fragen [20 Punkte] Beantworten Sie folgende Fragen. Für jede richtige Antwort
Chemische Bindung zweiatomiger Moleküle
 Die Born Oppenheimer Näherung vernachlässigt Elektronenimpulse gegenüber Kernimpulsen und erlaubt die Gesamtwellenfunktion als ein Produkt aus einer Kernwellenfunktion F q ( R) und der einer Elektronenwellenfunktion
Die Born Oppenheimer Näherung vernachlässigt Elektronenimpulse gegenüber Kernimpulsen und erlaubt die Gesamtwellenfunktion als ein Produkt aus einer Kernwellenfunktion F q ( R) und der einer Elektronenwellenfunktion
Das H + 2 -Molekül. Das Wasserstoffmolekülion H + 2 ist das einfachste
 Moleküle Wir haben in den vergangenen Wochen gelernt, wie sich Atome, zusammengesetzt aus elektrisch geladenen Kernen und Elektronen, verhalten. Wie aber verbinden sich elektrisch neutrale Atome zu Molekülen
Moleküle Wir haben in den vergangenen Wochen gelernt, wie sich Atome, zusammengesetzt aus elektrisch geladenen Kernen und Elektronen, verhalten. Wie aber verbinden sich elektrisch neutrale Atome zu Molekülen
10 Quantenmechanik in 3 Dimensionen
 Skript zur 2. Vorlesung Quantenmechanik, Freitag den 27. Mai, 20. 0 Quantenmechanik in 3 Dimensionen 0. Freies Teilchen Die Operatoren H = ˆp 2 /2m, p x, p y, p z sind alle unter einander vertauschbar:
Skript zur 2. Vorlesung Quantenmechanik, Freitag den 27. Mai, 20. 0 Quantenmechanik in 3 Dimensionen 0. Freies Teilchen Die Operatoren H = ˆp 2 /2m, p x, p y, p z sind alle unter einander vertauschbar:
Physik IV - Schriftliche Sessionsprüfung Sommer 2009
 Physik IV - Schriftliche Sessionsprüfung Sommer 2009 9:00 11:00, Samstag, 8. August 2009, HG F1 & HG F3 Bitte zur Kenntnis nehmen: Es befinden sich insgesamt SECHS Aufgaben auf VIER SEITEN. Es können insgesamt
Physik IV - Schriftliche Sessionsprüfung Sommer 2009 9:00 11:00, Samstag, 8. August 2009, HG F1 & HG F3 Bitte zur Kenntnis nehmen: Es befinden sich insgesamt SECHS Aufgaben auf VIER SEITEN. Es können insgesamt
2.2 4-Stromdichte [Griffiths , Jackson 11.9]
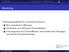
![2.2 4-Stromdichte [Griffiths , Jackson 11.9] 2.2 4-Stromdichte [Griffiths , Jackson 11.9]](/thumbs/52/29912127.jpg) Um zu verstehen, wie sich die elektromagnetischen Felder transformieren, gehen wir von den Maxwellgleichungen aus. Dazu brauchen wir zunächst die. 4-Stromdichte [Griffiths 1.3.4, Jackson 11.9] Die Ladungsdichte
Um zu verstehen, wie sich die elektromagnetischen Felder transformieren, gehen wir von den Maxwellgleichungen aus. Dazu brauchen wir zunächst die. 4-Stromdichte [Griffiths 1.3.4, Jackson 11.9] Die Ladungsdichte
Theoretische Biophysikalische Chemie
 Theoretische Biophysikalische Chemie Thermochemie (und Schwingungsspektroskopie) Christoph Jacob DFG-CENTRUM FÜR FUNKTIONELLE NANOSTRUKTUREN 0 KIT 17.12.2012 Universität deschristoph Landes Baden-Württemberg
Theoretische Biophysikalische Chemie Thermochemie (und Schwingungsspektroskopie) Christoph Jacob DFG-CENTRUM FÜR FUNKTIONELLE NANOSTRUKTUREN 0 KIT 17.12.2012 Universität deschristoph Landes Baden-Württemberg
Theorie der Kondensierten Materie I WS 2017/2018
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Theorie der Kondensierten Materie I WS 17/18 Prof. Dr. A. Mirlin, PD Dr. I. Gornyi Blatt 3 Dr. N. Kainaris, Dr. S. Rex,
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Theorie der Kondensierten Materie I WS 17/18 Prof. Dr. A. Mirlin, PD Dr. I. Gornyi Blatt 3 Dr. N. Kainaris, Dr. S. Rex,
Vorlesung "Molekülphysik/Festkörperphysik" Sommersemester 2014 Prof. Dr. F. Kremer
 Vorlesung "Molekülphysik/Festkörperphysik" Sommersemester 04 Prof. Dr. F. Kremer Übersicht der Vorlesung am.6.04 Wiederholung (Drude-Modell ( freies Elektronengas ), Plasmaschwingung, Grenzen des Drude-
Vorlesung "Molekülphysik/Festkörperphysik" Sommersemester 04 Prof. Dr. F. Kremer Übersicht der Vorlesung am.6.04 Wiederholung (Drude-Modell ( freies Elektronengas ), Plasmaschwingung, Grenzen des Drude-
TC1 Grundlagen der Theoretischen Chemie
 TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Robert Binder (rbinder@theochem.uni-frankfurt.de) Jan von Cosel (janvoncosel@gmx.de) Haleh
TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Robert Binder (rbinder@theochem.uni-frankfurt.de) Jan von Cosel (janvoncosel@gmx.de) Haleh
Ferienkurs Experimentalphysik IV
 Ferienkurs Experimentalphysik IV Michael Mittermair, Daniel Jost 04.09.14 Inhaltsverzeichnis 1 Moleküle 2 1.1 Das H + 2 Molekül-Ion....................... 2 1.2 Näherungen............................ 3
Ferienkurs Experimentalphysik IV Michael Mittermair, Daniel Jost 04.09.14 Inhaltsverzeichnis 1 Moleküle 2 1.1 Das H + 2 Molekül-Ion....................... 2 1.2 Näherungen............................ 3
7. Gekoppelte Harmonische Schwingungen
 7. Gekoppelte Harmonische Schwingungen Ausgehend von einer allgemeinen Lagrange-Funktion wollen wir in harmonischer Näherung die Eigenrequenzen und Eigenschwingungen eines Systems mit vielen Freiheitsgraden
7. Gekoppelte Harmonische Schwingungen Ausgehend von einer allgemeinen Lagrange-Funktion wollen wir in harmonischer Näherung die Eigenrequenzen und Eigenschwingungen eines Systems mit vielen Freiheitsgraden
4.3 Das Wasserstoffatom
 1.3 Das Wasserstoffatom Das Wasserstoffatom besteht aus einem Atomkern, der für den normalen Wasserstoff einfach durch ein Proton gegeben ist, mit der Masse m p, und einem Elektron mit der Masse m e. Vernachlässigen
1.3 Das Wasserstoffatom Das Wasserstoffatom besteht aus einem Atomkern, der für den normalen Wasserstoff einfach durch ein Proton gegeben ist, mit der Masse m p, und einem Elektron mit der Masse m e. Vernachlässigen
