Biomoleküle II Enzymkinetik, Hämoglobin, Signalkaskaden (MAPK & G-Protein)
|
|
|
- Clemens Meinhardt
- vor 7 Jahren
- Abrufe
Transkript
1 Biomoleküle II Enzymkinetik, Hämoglobin, Signalkaskaden (MAPK & G-Protein) 1. Was sind Enzyme? - Biokatalysatoren - Beschleunigen chem. Reaktionen in der Zelle - Spezifität/ Affinität zum Substrat - katalytische Aktivität regulierbar (feedback Hemmung) - E + S ES E + P Substrate werden bevorzugt gebildet, verschiedene Annahmen: - 1. Theorie: Schlüssel-Schloss-Prinzip -. Theorie: Induced Fit (Enzyme-Substrate-Complex) - erst wenn erste Wechselwirkungen durch räumliche nähe auftreten - Bindung wird in der katalytischen Spalte (active Site) gebunden (H- Brücken, Kovalenzbindungen durch komplementäre Strukturen) - Konformationsänderung des Enzym-Substrate- Komplex verstärkt Bindung Regulatorproteine: Calmodulinsensor Ca + bindet Veränderung der Enzymaktivität kovalente Modifikation: Phosphorylierung von z.b. Sr, Thr, Tyr protolyt. Aktivierung : Enzyme in inaktiver Vorstufe am physilog. geeigneten Ort + Zeitpkt. aktiviert (das Enzym passt sich dem Substrat an, das es ideal in die katalytische Spalte passt) kovalente Reaktionen sind länger anhaltend, dauern ca ms nichtkovalente Verbindungen/Mechanismen (auch Feedback-Mechanismen): (Diffusionskontrolliert, sehr schnelle Reaktionen) Schrittmacherenzyme: (sind die regulierten Enzyme) bestimmen die Reaktiongeschwindigkeit. Fließgleichgewicht: Theorie der Thermodynamik beschreibt die Gleichgewichtreaktion Feedback-Mechanismus: Mechanismus der am Ende der Enzymkettenreaktion die Enzyme am Anfang der Kette reguliert. Feedforward-Mechanismus: Mechanismus der am Anfang der Enzymkettenreaktion die Enzyme am Anfang der Kette reguliert. Allosterie: sind Wechselwirkungen an räumlich getrennten Regionen am Enzym. (siehe Oligomere) Bsp. für allosterische E. ACTASE; Ribonucliotid-Reduktase; Glykogen-Phosphorylase Interkonvertierung: enzymatisch katalysierte Aktivierung von Enzymen Beispiel ist die Phosphorregulierung von Aminosäuren durch Kinasen (Proteinkinasen). 1
2 . Bsp. Hämoglobin Hämoglobin (Blut) und Myoglobin (Muskel) Aufgabe: Transport von Sauerstoff aus der Lunge zu den Geweben und CO von den Geweben zurück zur Lunge. Das Hämoglobin (0 ml O pro l) ist notwendig, um die schlechte Wasserlöslichkeit von Sauerstoff im Blutplasma (3. ml O ) zu überwinden. Struktur: - Tetramer besteht aus (-alpha und -beta- Ketten mit Massen von jeweils 16kDa). 80% Prozent des Globins sind alpha Helices. - Jede Untereinheit () trägt eine Häm-Gruppe mit einem - wertigen Eisen-Ion - Die Tetramere zusammengehalten von nichtkovalenten Bindungen zusammengehalten. - Zustände: Oxygenierung, Desoxygenierung - Von den sechs Koordinationsstellen des Eisens sind vier mit dem Stickstoff der Pyrrolringe besetzt. Eine Bindungstelle mit dem proximalen Histidin. An der letzten Stelle koordiniert im Oxy-Hämoglobin der O. - HbF : Hämoglobin im Fötus (Zeta-Ketten werden zu den Alpha-Ketten, die Epsilon-Ketten zu den Beta-Ketten) Allosterische Effekte im Hämoglobin: T-Form (tense-form): starr, gepannt (über Salzbrücken stabilisiert): desoxygen besitzt eine viel geringere O-Affinität als die R-Form (relaxed-form). Bindet O aneine der Untereinheiten der T-Form, kommt es zu einer konformationsänderung, die den Zusammenhalt der Untereinheiten schwächt. Mit zunehmendem O Partialdruck gehen immer mehr Moleküle in die affinere R-Form über. Daher: mit zunehmender O (positiv homotroper Effektor) Konzentration steigt auch die Aufnahmefähigkeit des Sauerstoffs man spricht hier von kooperativen Wechselwirkungen. Die Sättigungskurve des Bindungsverhaltens ist sigmoidal allosterische Effektoren, die das O Bindungsverhalten ändern: die Anwesenheit von,3 Biphosphogycerat, CO und H + (homotrophe Effektoren; additive Wirkung) sinkt die O -Affinität des Hämoglobins. CO, H + lagern sich an anderen Stellen an. (nicht Häm-Gruppe). Wenn der ph-wert im Blut zunimmt, verschiebt sich die Sättigungskurve nach unten. O po pco, ph [ BGP] + + HbT BGP HbR ( O + H + BGP ) po pco, ph [ BGP] Myoglobin: Myoglobin ist ein Monomer, die Struktur ähnelt den Untereinheiten des Hämoglobins. Es zeigt kein allosterisches Verhalten.
3 3. Enzymkinetik: Michaelis-Menten-Modell: einfaches Modell zur Erklärung der charakteristischen Abhängikeit der Enzymaktivität von der Substratkonzentration. (Grafik in den Kopien) Annahmen: 1. Substrat A wird vom Enzym E gebunden, die Reaktion geht weitaus schneller zum Produkt P als in Abwesenheit von E. k cat (Wechselzahl) entspricht einem Enzym-Molekül pro Sekunde umgesetzten Zahl von Substrat-Molekülen. Dabei überwiegt der ES Anteil > E Anteil in Lsg. 3. Annahme das E, A und EA im chemischen Gleichgewicht Michaelis-Menten-Gleichung: k v = cat [ E] g [ S] + [ S] K m Kritik: 1. Es wird angenommen, dass die Umwandlung vom Enzym-Substrat-Komplex in das Enzym und das Produkt irreversibel ist.. Das ein Gleichgewicht zwischen dem Enzym, dem Substrat und auf der anderen Seite dem Enzym- Substrat-Komplex existiert. 3. Das nur das Enzym X und der Enzym-Substrat-Komplex an der Reaktion beteiligt sind. V max = die Maximalgeschwindigkeit der Reaktion V = k cat *[E] g, K M = gibt die Affinität des Substrats an. [E]*[A]/[EA]= K m Unter diesen Annahmen entspricht K M der Dissoziationskonstante des E-S-Komplexes, k cat der Geschwindigkeitskonstante der Reaktion des E-S-Komplexes E + Produkt. Eadie Hofstee 5 3 v ungehemmte Reaktion kompetitive Hemmung nicht kompetitive 1 [v]/[s] 0 0 0,5 1 1,5 Abb. Eadie Hofstee Lineweaver Burk ungehemmte Reaktion nicht kompetetive Hemmung kompetetive Hemmung Abb. Lineweaver Burk / [ S ] - -1,5-1 -0,5 0 0,5 1 1,5 1/ v V-S Diag.: V max ist Annäherung 0,09 mm/s und das Abtragen von V max / an der X-Achse ist K M -Wert Burk Dia.: V max ist der Schnittpunkt mit der Y-Achse, wobei V max = 1/v für 1/[S]= 0 ist. K M ist der Schnittpunkt mit der X-Achse, wobei K M = -1/s für 1/v= 0. Eadie Dia. : V max ist der Schnittpunkt mit der Y-Achse. K M ist der Betrag des neg. Anstiegs der Geraden. PH-Wert: Dissoziationsgleichung: HA H + + A + K = [H + ][A - ]/[HA] [HA]=[A] ph-wert: pi=ph=1/ (p K1 +p K ) der negative dekadische Logarithmus vom Wasserstoffionenkonzentration pk-wert: ist der neg. dekadische log. der Dissoziation von HA H + + A - 3
4 kompetetiver, nicht kompetetiv und allosterischer Inhibitor kompetetive Hemmung: Bei der kompetetiven Hemmung wird die Substratbindungstelle am Enzym besetzt. Die Affinität des Enzyms wird kleiner und der K M -Wert dadurch grösser. Wenn die Substratkonzentration erhöht wird, wird der Inhibitor aus der Bindungsstelle verdrängt, die Hemmung ist somit reversibel, durch eine hohe Konzentration von Substrat lässt sich das V max der ungehemmten Reaktion erreichen, V max bleibt daher unverändert. Bsp. Multienzymkomplex (Pyruvat-Dehydrogenase) nicht kompetetive Hemmung: Bei der nicht kompetetiven Hemmung verringert sich die Geschwindigkeit der Reaktion und somit auch V max. Der Inhibitor reagiert mit dem Enzym so, dass die Funktion des Enzyms gehemmt wird. Die Bindungsstelle für das Substrat bleibt dabei unbetroffen. Die Affinität des Enzyms zum Substrat bleibt dadurch erhalten, sowie der K M -Wert des Enzyms. allosterische Hemmung: Die allosterischen Inhibitoren binden an seperate Bindungsstellen außerhalb des aktiven Zentrums. Dadurch kommt es zu einer Konformationsänderung des Enzymproteins, die indirekt die Aktivität vermindert. Allosterische Effekte treten nur bei oligomeren Enzymen auf. (Bsp. Hämoglobin : ) Kopplung von Proteinmodifikation und Protein-Protein-WW: SH Domänen & P-Tyr Kopplung von Proteinmodifikation und zellulärer Lokalisation: STATs, MAPK
5 3. Signalkaskaden: Metabolischer Mechanismus: (Kontrolle der Zelle des ATP Haushalts) Hormoneller Mechanismus: (Adrenalin) steuert den metabolischen Mechanismus Kaskaden: Reversibilität (Phosphorylierung-Dephosphorylierung, GDP-GTP-GDP) Signalverstärkung (intrazelluläre "second messenger", Enzymkaskaden) MAP Kinase Kaskade: Katalytische Rezeptoren - Rezeptor-Tyrosin-Kinasen (MAPK-Weg, Jak- STAT-Weg) - Rezeptor-Serin/Threonin-Kinasen Durch Bindung der Liganden (Wachstumsfaktoren)dimerisieren die Rezeptor-Tyrosin-Kinasen bzw. ändern ihre intrazelluläre Konformation derartig, dass eine gegenseitige Phosphorylierung der intrazellulären Kinase-domänen (Autophosphorylierung) oder eine Phosphorylierung bestimmter Effektorproteine möglich wird Signaltransduktion bei G-Protein gekoppelte Rezeptoren Hier sollten wir uns zunächst folgende sekundäre Botenmoleküle (second messengers) ansehen: camp (cyclic AMP, 3'5'AMP): camp wird aus ATP durch das Enzym Adenylatzyklase gebildet und kann durch Phosphodiesterase zu AMP abgebaut werden Diacylglycerol (DAG) und Inositol-1,,5-trisphosphat (IP3) entstehen durch Spaltung des Zellmembranlipides Phosphatidylinositol-,5-bisphosphat (PIP) weitere Botenmoleküle sind Kalzium-Ionen (Ca+) und Stickoxid-Radikale (NO) 5
6 Adenylat-Zyklase-Kaskade Nach Ligandenbindung (z.b. Adrenalin) an den G- Protein-gekoppelten Rezeptor wird ein Gα-Protein freigesetzt und aktiviert die Adenylatzyklase, welche die Bildung von camp katalysiert. camp aktiviert die camp-abhängige Proteinkinase (PKA) PKA phosphoryliert den Transkriptionsfaktor CREB,CREB aktiviert Transkription CRE-kontrollierter Gene PKA phosphoryliert und aktiviert Phosphorylasekinase und phosphoryliert und deaktiviert Glykogensynthetase, damit Erhöhung der Glykogenolyse und Hemmung der Glykogensynthese in der Leber - Erhöhung der Glukosekonzentration im Blut Phosphoinositid-Kaskade - Nach Ligandenbindung (z.b. Azetylcholine) an den G-Protein-gekoppelten Rezeptor wird ein Gα- Protein freigesetzt und aktiviert die Phospholipase Cβ, welche PIP zu IP3 und DAG spaltet. - DAG stimulier die membranlokalisierte Proteinkinase C (PKC) - IP3 bindet an den IP3-Rezeptors des ER, Ca+ strömt in das Cytoplasma ein, bindet an das Protein Calmodulin (CaM) und aktiviert dann CaMabhängige Enzyme, z.b. Proteinkinasen oder Proteinphosphatasen Signaltransduktion bei Katalytischen Rezeptoren Der erste Schritt bei der weiteren Signalübertragung durch viele Wachstumsfaktorrezeptoren ist die spezifische Bindung von sogenannten Adaptorproteinen an die Phosphotyrosinreste der intrazellulären Domäne des Rezeptors bzw. an ein rezeptorassoziiertes Protein wie z.b. Insulin-Rezeptor-Substrat IRS-1. Die Bindung an Phosphotyrosin wird durch sogenannte Scr-Homologie (SH) -Domänen in den Adaptorproteinen realisiert. Über verschiedenen Phosphotyrosinreste und verschiedene Adaptorproteine können dann verschiedene Signalwege stimuliert werden: o Über das Wachstumsfaktorrezeptor-bindende Protein (GRB) wird die Mitogen-aktivierte Proteinkinase- Kaskade aktiviert o Über andere Effektorproteine kann z.b. die Phospholipase Cγ stimuliert werden, die dann ähnlich wie Phospholipase Cβ agiert. GRB-Bindung an den Rezeptor führt zur Aktivierung des kleinen monomeren GTP-bindenden Proteins Ras (Austausch GDP zu GTP), welches dann die erste Kinase der MAP-Kinase-Kaskade, Raf, aktivieren kann Raf phosphoryliert und aktiviert die Kinase MEK und MEK wiederum die MAP-Kinase ERK ERK transloziert dann in den Zellkern und phosphoryliert und aktiviert den Transkriptionsfaktor Elk, der die Transkription Mitogen-abhängiger Gene stimuliert 6
7 . Proteomics-Vorlesung Beispiel für eine Protein Analyse: Reaktion: Ziel: NAD+ + ATP NADP+ + ADP gesuchtes Protein ist für die obige Reaktion zuständig folgende Schritte zur Reinigung: 1. Zellaufschluss // Zerstörung der Zellmembran. Homogenisierung: // Zerkleinern a. langsame Zentrifugation zur Auftrennung der Zellorganellen und des plasmatischen Reticulums i. Kerne ii. Membranen iii. Cytosol b. alle Prozesse bei Celsius c. Ionenaustauscher 3. Chromatographie // Überprüfen aller Fraktionen auf Aktivität. Photometer: messen der Absorption der Produkte der Reaktion Zu überprüfen anhand der U/mg (Units: Anteil der Enzyme) 5. Elektrophorese // SDS Nachteil: nach Auftrennen gibt es keine Enzymaktivität mehr a. nach dem Auftrennen wird das gesuchte Enzym geblottet b. Edman-Sequenzierung: vom N-terminus des Proteins Aminosäuren abgespalten funktioniert nur mit NH Terminus (keine Modifikation) c. Proteasen, die gezielt schneiden (z.b. Trypsin; schneidet Arginin, Lysin) es entstehen Peptide + Massen mit Aminosäureketten 6. Massenspektroskopie (MALDI-TOF) 7
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail. Mag. Gerald Trutschl
 Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Allgemeine Pharmakologie
 Allgemeine Pharmakologie Pharmakologie Arzneistoff: Wirkstoff, der zur Vorbeugung, Linderung, Heilung oder Erkennung von Erkrankungen dient Pharmakon: biologisch Wirksame Substanz Lehre von den Wirkungen
Allgemeine Pharmakologie Pharmakologie Arzneistoff: Wirkstoff, der zur Vorbeugung, Linderung, Heilung oder Erkennung von Erkrankungen dient Pharmakon: biologisch Wirksame Substanz Lehre von den Wirkungen
Versuch 4. Enzymkinetik
 Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
G-Protein gekoppelte Rezeptoren. Prof. Dr. Albert Duschl
 G-Protein gekoppelte Rezeptoren Prof. Dr. Albert Duschl Rezeptoren Rezeptoren können intrazellulär vorliegen, wie die Steroidrezeptoren aber die meisten Rezeptoren sind Transmembranproteine der Plasmamembran
G-Protein gekoppelte Rezeptoren Prof. Dr. Albert Duschl Rezeptoren Rezeptoren können intrazellulär vorliegen, wie die Steroidrezeptoren aber die meisten Rezeptoren sind Transmembranproteine der Plasmamembran
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 4. Allosterische Regulation Organismen
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 4. Allosterische Regulation Organismen
Enzym-Regulation (Abb. 1) Heute werde ich mich mit dem Thema Enzym-Regulation auseinandersetzen. Im Stoffwechsel von lebenden Zellen arbeiten Gruppen
 1 Enzym-Regulation (Abb. 1) Heute werde ich mich mit dem Thema Enzym-Regulation auseinandersetzen. Im Stoffwechsel von lebenden Zellen arbeiten Gruppen von Enzymen nacheinander in dem Sinne, dass das Produkt
1 Enzym-Regulation (Abb. 1) Heute werde ich mich mit dem Thema Enzym-Regulation auseinandersetzen. Im Stoffwechsel von lebenden Zellen arbeiten Gruppen von Enzymen nacheinander in dem Sinne, dass das Produkt
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000
 Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasse
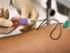 Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Glucose/Fettstoffwechsel
 Glucose/Fettstoffwechsel Glucose/Fettstoffwechsel Blutzuckerspiegel immer konstant 60 100 mg/100 ml oder 3,33 5,55 mmol/l. Synthese: Pankreas Hormon-Antagonisten Insulin Glucagon hemmt steigert Zucker-Neubildung
Glucose/Fettstoffwechsel Glucose/Fettstoffwechsel Blutzuckerspiegel immer konstant 60 100 mg/100 ml oder 3,33 5,55 mmol/l. Synthese: Pankreas Hormon-Antagonisten Insulin Glucagon hemmt steigert Zucker-Neubildung
7. Regulation der Genexpression
 7. Regulation der Genexpression 7.1 Regulation der Enzymaktivität Stoffwechselreaktionen können durch Kontrolle der Aktivität der Enzyme, die diese Reaktionen katalysieren, reguliert werden Feedback-Hemmung
7. Regulation der Genexpression 7.1 Regulation der Enzymaktivität Stoffwechselreaktionen können durch Kontrolle der Aktivität der Enzyme, die diese Reaktionen katalysieren, reguliert werden Feedback-Hemmung
Herz und Kreislauf Teil 3
 24. TOGGENBURGER ANÄSTHESIE REPETITORIUM Herz und Kreislauf Teil 3 Zellphysiologie Medikamente Salome Machaidze Miodrag Filipovic miodrag.filipovic@kssg.ch Anästhesiologie & Intensivmedizin Unter Verwendung
24. TOGGENBURGER ANÄSTHESIE REPETITORIUM Herz und Kreislauf Teil 3 Zellphysiologie Medikamente Salome Machaidze Miodrag Filipovic miodrag.filipovic@kssg.ch Anästhesiologie & Intensivmedizin Unter Verwendung
Membranen. U. Albrecht
 Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Asmaa Mebrad Caroline Mühlmann Gluconeogenese
 Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Enzyme als Biokatalysatoren
 1 Enzymwirkung Enzyme als Biokatalysatoren Versuch: Wasserstoffperoxid wird bei RT mit a) Mn(IV)-oxid und b) Katalase versetzt. Beobachtung: a) Gasentwicklung Glimmspanprobe positiv b) Gasentwicklung Glimmspanprobe
1 Enzymwirkung Enzyme als Biokatalysatoren Versuch: Wasserstoffperoxid wird bei RT mit a) Mn(IV)-oxid und b) Katalase versetzt. Beobachtung: a) Gasentwicklung Glimmspanprobe positiv b) Gasentwicklung Glimmspanprobe
GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN
 53 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu gehören
53 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu gehören
STICKSTOFFMONOXYD (NO) Intra- und interzellulärer Botenstoff. - Nicht nur im Gefäßsystem -
 STICKSTOFFMONOXYD (NO) Intra- und interzellulärer Botenstoff - Nicht nur im Gefäßsystem - 1962 Chemische und physikalische Eigenschaften von N=O. - Radikalisches Gas (ungepaartes Elektron) - - relativ
STICKSTOFFMONOXYD (NO) Intra- und interzellulärer Botenstoff - Nicht nur im Gefäßsystem - 1962 Chemische und physikalische Eigenschaften von N=O. - Radikalisches Gas (ungepaartes Elektron) - - relativ
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease
 K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
E Bio 2 KW Enzyme
 E Bio 2 KW 15-21 Enzyme Wdh. Enzyme Funktion und Bedeutung für den Stoffwechsel Aufbau und Strukturen Effektoren Versuch 1 (Enzyme und Temperatur) RGT-Regel Enzyme: RGT-Regel Die Reaktions-Geschwindigkeits-Temperatur-Regel
E Bio 2 KW 15-21 Enzyme Wdh. Enzyme Funktion und Bedeutung für den Stoffwechsel Aufbau und Strukturen Effektoren Versuch 1 (Enzyme und Temperatur) RGT-Regel Enzyme: RGT-Regel Die Reaktions-Geschwindigkeits-Temperatur-Regel
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Enzympraktikum Theorie Entstanden: Nutzung: Entdeckung: Taufe: Aktivierungsenergie Geschichte der Enzyme
 Enzympraktikum Theorie In diesem Praktikum werden Sie die Bekanntschaft mit einer der ungewöhnlichsten Stoffklasse der Natur machen. Ein kurzer Steckbrief dieser Stoffklasse lautet: Entstanden: vor ungefähr
Enzympraktikum Theorie In diesem Praktikum werden Sie die Bekanntschaft mit einer der ungewöhnlichsten Stoffklasse der Natur machen. Ein kurzer Steckbrief dieser Stoffklasse lautet: Entstanden: vor ungefähr
Bioorganische Chemie Enzymatische Katalyse 2011
 Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Endokrinologie und Stoffwechsel
 Block 10 Endokrinologie und Stoffwechsel Einführung A. Univ. Prof. Dr. W. Marktl www.meduniwien.ac.at/umweltphysiologie Lehrinhalte Definition Prinzipien des Informationsaustausches Einteilungsmöglichkeiten
Block 10 Endokrinologie und Stoffwechsel Einführung A. Univ. Prof. Dr. W. Marktl www.meduniwien.ac.at/umweltphysiologie Lehrinhalte Definition Prinzipien des Informationsaustausches Einteilungsmöglichkeiten
Versuch 6. Leitenzyme
 Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Übung 8. 1. Zellkommunikation. Vorlesung Bio-Engineering Sommersemester 2008. Kapitel 4. 4
 Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Translation. Auflesung- Proteinsynthese
 Translation Auflesung- Proteinsynthese Proteinsynthese DNA mrna Transkription elágazási hely Translation Polypeptid Vor dem Anfang Beladen der trnas spezifische Aminosäure + spezifische trna + ATP Aminoacyl-tRNA
Translation Auflesung- Proteinsynthese Proteinsynthese DNA mrna Transkription elágazási hely Translation Polypeptid Vor dem Anfang Beladen der trnas spezifische Aminosäure + spezifische trna + ATP Aminoacyl-tRNA
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Praktikum. Enzymkinetik am Beispiel der Protease Trypsin
 Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
Genregulation bei Eukaryoten II
 Genregulation bei Eukaryoten II Aktivierung und Repression der Transkription erfolgen durch Protein-Protein-Wechselwirkungen Protein-Protein-Wechselwirkungen spielen bei der Genregulation der Eukaryoten
Genregulation bei Eukaryoten II Aktivierung und Repression der Transkription erfolgen durch Protein-Protein-Wechselwirkungen Protein-Protein-Wechselwirkungen spielen bei der Genregulation der Eukaryoten
Unterrichtsvorhaben IV: Thema/Kontext: Enzyme im Alltag Welche Rolle spielen Enzyme in unserem Leben/beim Ablauf verschiedener Stoffwechselreaktionen?
 Unterrichtsvorhaben IV: Thema/Kontext: Enzyme im Alltag Welche Rolle spielen Enzyme in unserem Leben/beim Ablauf verschiedener Stoffwechselreaktionen? Inhaltsfelder: IF 1 (Biologie der Zelle), IF 2 (Energiestoffwechsel)
Unterrichtsvorhaben IV: Thema/Kontext: Enzyme im Alltag Welche Rolle spielen Enzyme in unserem Leben/beim Ablauf verschiedener Stoffwechselreaktionen? Inhaltsfelder: IF 1 (Biologie der Zelle), IF 2 (Energiestoffwechsel)
8. Translation. Konzepte: Translation benötigt trnas und Ribosomen. Genetischer Code. Initiation - Elongation - Termination
 8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation - Elongation - Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse human bacteria
8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation - Elongation - Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse human bacteria
Übung 11 Genregulation bei Prokaryoten
 Übung 11 Genregulation bei Prokaryoten Konzepte: Differentielle Genexpression Positive Genregulation Negative Genregulation cis-/trans-regulation 1. Auf welchen Ebenen kann Genregulation stattfinden? Definition
Übung 11 Genregulation bei Prokaryoten Konzepte: Differentielle Genexpression Positive Genregulation Negative Genregulation cis-/trans-regulation 1. Auf welchen Ebenen kann Genregulation stattfinden? Definition
Biophysikpraktikum. Kontrolle glykolytischer Oszillationen
 Biophysikpraktikum Versuch: Kontrolle glykolytischer Oszillationen I Ziel des Versuches: Es soll die nichtlineare Dynamik von komplexen Stoffwechselwegen anhand des glykolytischen Zuckerabbaus in einem
Biophysikpraktikum Versuch: Kontrolle glykolytischer Oszillationen I Ziel des Versuches: Es soll die nichtlineare Dynamik von komplexen Stoffwechselwegen anhand des glykolytischen Zuckerabbaus in einem
Versuch 5: Enzyme (Alkalische Phosphatase) (V )
 Versuch 5: Enzyme (Alkalische Phosphatase) (V10 6.03.2012) Lernziele: 1) Reaktionsgeschwindigkeit, Aktivierungsenergie, chemisches Gleichgewicht; 2) Was tun Katalysatoren und Enzyme, 3) Michaelis-Menten
Versuch 5: Enzyme (Alkalische Phosphatase) (V10 6.03.2012) Lernziele: 1) Reaktionsgeschwindigkeit, Aktivierungsenergie, chemisches Gleichgewicht; 2) Was tun Katalysatoren und Enzyme, 3) Michaelis-Menten
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
G-Protein gekoppelte Rezeptoren
 G-Protein gekoppelte Rezeptoren Bedeutung, Funktionen, Liganden Prinzipielle Funktionsmechanismen Klassifizierung und Eigenschaften von G-Proteinen Desensitivierung Beispiele G-Protein gekoppelte Rezeptoren
G-Protein gekoppelte Rezeptoren Bedeutung, Funktionen, Liganden Prinzipielle Funktionsmechanismen Klassifizierung und Eigenschaften von G-Proteinen Desensitivierung Beispiele G-Protein gekoppelte Rezeptoren
Enzymatische Reaktionen
 Enzymatische Reaktionen 1. Chemische Kinetik 2. Enzymatische Kinetik 3. Inhibition 4. ph Effekte Voet Biochemistry 3e 5. Bisubstrat Reaktionen 1. Chemische Kinetik Kinetik ist das Studium der Raten bei
Enzymatische Reaktionen 1. Chemische Kinetik 2. Enzymatische Kinetik 3. Inhibition 4. ph Effekte Voet Biochemistry 3e 5. Bisubstrat Reaktionen 1. Chemische Kinetik Kinetik ist das Studium der Raten bei
Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät
 Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät Grundlagen Lipid-Doppelschicht als Barriere für polare Moleküle! Abgrenzung für biochemische
Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät Grundlagen Lipid-Doppelschicht als Barriere für polare Moleküle! Abgrenzung für biochemische
Reaktionskinetik. Katalyse
 Reaktionskinetik Katalyse Katalysatoren beshleunigen hemishe Reaktionen, ohne das Gleihgewiht zu beeinflussen. Sie beeinflussen nur die Aktiierungsenergie Katalyse Katalysatoren beeinflussen den Reaktionsweg
Reaktionskinetik Katalyse Katalysatoren beshleunigen hemishe Reaktionen, ohne das Gleihgewiht zu beeinflussen. Sie beeinflussen nur die Aktiierungsenergie Katalyse Katalysatoren beeinflussen den Reaktionsweg
Erregungsübertragung an Synapsen. 1. Einleitung. 2. Schnelle synaptische Erregung. Biopsychologie WiSe Erregungsübertragung an Synapsen
 Erregungsübertragung an Synapsen 1. Einleitung 2. Schnelle synaptische Übertragung 3. Schnelle synaptische Hemmung chemische 4. Desaktivierung der synaptischen Übertragung Synapsen 5. Rezeptoren 6. Langsame
Erregungsübertragung an Synapsen 1. Einleitung 2. Schnelle synaptische Übertragung 3. Schnelle synaptische Hemmung chemische 4. Desaktivierung der synaptischen Übertragung Synapsen 5. Rezeptoren 6. Langsame
Enzyme. Prof. Dr. Albert Duschl
 Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Na + -Konzentrationen und Gleichgewichtspotenzial. K + -Konzentrationen und Gleichgewichtspotenzial. Ca 2+ -Konzentrationen. Cl - -Konzentrationen
 Na + -Konzentrationen und Gleichgewichtspotenzial K + -Konzentrationen und Gleichgewichtspotenzial Ca 2+ -Konzentrationen Cl - -Konzentrationen Ficksches Diffusionsgesetz Na + /K + -ATPase Na + /Ca 2+
Na + -Konzentrationen und Gleichgewichtspotenzial K + -Konzentrationen und Gleichgewichtspotenzial Ca 2+ -Konzentrationen Cl - -Konzentrationen Ficksches Diffusionsgesetz Na + /K + -ATPase Na + /Ca 2+
Vertiefendes Seminar zur Vorlesung Biochemie
 Vertiefendes Seminar zur Vorlesung Biochemie 31.10.2014 Proteine: Struktur Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Vertiefendes Seminar zur Vorlesung Biochemie 31.10.2014 Proteine: Struktur Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Stoffwechsel. Metabolismus (1)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (1) Zum Nachlesen Bücher Campbell: Kap. 6 59.95 Kap. 3 Kap. 13-14 29.95 www.icbm.de/pmbio - - - > Teaching diese Folien, VL Physiologie der
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (1) Zum Nachlesen Bücher Campbell: Kap. 6 59.95 Kap. 3 Kap. 13-14 29.95 www.icbm.de/pmbio - - - > Teaching diese Folien, VL Physiologie der
spaltet. Der Sauerstoff entflammt den Glimmspan. Bei der katalytischen Substanz handelt es sich um das Enzym Katalase.
 ENZYMATIK 1. Vorversuch Versuch Spaltung von Wasserstoffperoxid (H 2 O 2 ) Material: Bäckerhefe, Braunstein (MnO 2 ), Wasserstoffperoxid, Rundkolben, Stativ, Brenner, Glimmspan Durchführung 1: 5ml Wasserstoffperoxid
ENZYMATIK 1. Vorversuch Versuch Spaltung von Wasserstoffperoxid (H 2 O 2 ) Material: Bäckerhefe, Braunstein (MnO 2 ), Wasserstoffperoxid, Rundkolben, Stativ, Brenner, Glimmspan Durchführung 1: 5ml Wasserstoffperoxid
Zelluläre Reproduktion: Zellzyklus. Regulation des Zellzyklus - Proliferation
 Zelluläre Reproduktion: Zellzyklus Regulation des Zellzyklus - Proliferation Alle Zellen entstehen durch Zellteilung Der Zellzyklus kann in vier Haupt-Phasen eingeteilt werden Interphase Zellwachstum;
Zelluläre Reproduktion: Zellzyklus Regulation des Zellzyklus - Proliferation Alle Zellen entstehen durch Zellteilung Der Zellzyklus kann in vier Haupt-Phasen eingeteilt werden Interphase Zellwachstum;
Biochemische Übungen
 Dr. Arnulf Hartl Biochemische Übungen Proteine Tag 1: Tag 2: Tag 3: Konzentrieren Denaturierende und native Fällungen Protein Konzentrationsbestimmung Entsalzen Gelchromatographie Dialyse Elektrophorese
Dr. Arnulf Hartl Biochemische Übungen Proteine Tag 1: Tag 2: Tag 3: Konzentrieren Denaturierende und native Fällungen Protein Konzentrationsbestimmung Entsalzen Gelchromatographie Dialyse Elektrophorese
6. Induktion der Galactosidase von Escherichia coli
 Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 19.1.2005 6. Induktion der Galactosidase
Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 19.1.2005 6. Induktion der Galactosidase
Das Komplementsystem. Effektorwirkungen. Der humorale Effektorapparat des angeborenen Immunsystems
 Das Komplementsystem Der humorale Effektorapparat des angeborenen Immunsystems Hitzeempfindlicher Bestandteil des Plasmas Hitzebehandlung (56 ºC): Inaktivierung der bakteriziden Wirkung des Plasmas Ergänzt
Das Komplementsystem Der humorale Effektorapparat des angeborenen Immunsystems Hitzeempfindlicher Bestandteil des Plasmas Hitzebehandlung (56 ºC): Inaktivierung der bakteriziden Wirkung des Plasmas Ergänzt
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2
 Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
Sauerstofftransport im Blut. von Ralph Althoff Christoph Mittmann
 Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis o- Toluidin positiv, Glu-Oxidase-Peroxidase neg? Begründung!
 TEST1 Schreiben sie 2 saure Aminosäuren an! Was sind essentielle As geben sie 3 Beispiele an! Was versteht man unter Glykopyranose? Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis
TEST1 Schreiben sie 2 saure Aminosäuren an! Was sind essentielle As geben sie 3 Beispiele an! Was versteht man unter Glykopyranose? Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Musterlösung - Übung 5 Vorlesung Bio-Engineering Sommersemester 2008
 Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Übung 6 Vorlesung Bio-Engineering Sommersemester Nervenzellen: Kapitel 4. 1
 Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 21. 04. 08-16:30
Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 21. 04. 08-16:30
Entwicklungs /gewebespezifische Genexpression. Coexpression funktional überlappender Gene
 Übung 11 Genregulation bei Prokaryoten Konzepte: Entwicklungs /gewebespezifische Genexpression Coexpression funktional überlappender Gene Positive Genregulation Negative Genregulation cis /trans Regulation
Übung 11 Genregulation bei Prokaryoten Konzepte: Entwicklungs /gewebespezifische Genexpression Coexpression funktional überlappender Gene Positive Genregulation Negative Genregulation cis /trans Regulation
Das endokrine System GK I 11.1; 18.1±18.9
 Das endokrine System GK I 11.1; 18.1±18.9 17 " Die zellulären Funktionen höherer Organismen müssen genau reguliert werden. Eine entscheidende Rolle hierbei spielt das endokrine System. Es besteht aus endokrinen
Das endokrine System GK I 11.1; 18.1±18.9 17 " Die zellulären Funktionen höherer Organismen müssen genau reguliert werden. Eine entscheidende Rolle hierbei spielt das endokrine System. Es besteht aus endokrinen
Ungefähre Zusammensetzung des Blutes und des Blutplasmas. Die häufigsten Bestandteile des Blutplasmas (Mittelwerte)
 Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
21 Signaltransduktion
 540 Signaltransduktion Signaltransduktion Gerhard Püschel Damit spezialisierte Zellen in Geweben und Organen ihre Funktionen koordinieren können, müssen sie Informationen austauschen. Dies kann durch direkte
540 Signaltransduktion Signaltransduktion Gerhard Püschel Damit spezialisierte Zellen in Geweben und Organen ihre Funktionen koordinieren können, müssen sie Informationen austauschen. Dies kann durch direkte
Ei ne P ä r sentati ti on vo n T om D ro t s e, P t e er Haak k und Patrick Schürmann
 Ei P ä tti T D t P t H k d Eine Präsentation von Tom Droste, Peter Haak und Patrick Schürmann Inhaltsverzeichnis Allgemein: Was ist Stickstofffixierung? Welche Arten der Fixierung gibt es? Welchen Zweck
Ei P ä tti T D t P t H k d Eine Präsentation von Tom Droste, Peter Haak und Patrick Schürmann Inhaltsverzeichnis Allgemein: Was ist Stickstofffixierung? Welche Arten der Fixierung gibt es? Welchen Zweck
Der ras/raf Pathway. Prof. Dr. Albert Duschl
 Der ras/raf Pathway Prof. Dr. Albert Duschl Biologische Regelsysteme Behalten Sie bitte im Gedächtnis, daß biologische Systeme immer wieder vor vergleichbaren Aufgaben stehen, bei denen es darum geht,
Der ras/raf Pathway Prof. Dr. Albert Duschl Biologische Regelsysteme Behalten Sie bitte im Gedächtnis, daß biologische Systeme immer wieder vor vergleichbaren Aufgaben stehen, bei denen es darum geht,
DNA Replikation ist semikonservativ. Abb. aus Stryer (5th Ed.)
 DNA Replikation ist semikonservativ Entwindung der DNA-Doppelhelix durch eine Helikase Replikationsgabel Eltern-DNA Beide DNA-Stränge werden in 5 3 Richtung synthetisiert DNA-Polymerasen katalysieren die
DNA Replikation ist semikonservativ Entwindung der DNA-Doppelhelix durch eine Helikase Replikationsgabel Eltern-DNA Beide DNA-Stränge werden in 5 3 Richtung synthetisiert DNA-Polymerasen katalysieren die
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik
 Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Energie und Energiestoffwechsel von Zellen
 Energie und Energiestoffwechsel von Zellen Wiederholung: Signalübertragung in Zellen Die Übertragung von Signalen erfolgen in Zellen und zellulären Systemen in erster Linie über Botenstoffe ( Chemische
Energie und Energiestoffwechsel von Zellen Wiederholung: Signalübertragung in Zellen Die Übertragung von Signalen erfolgen in Zellen und zellulären Systemen in erster Linie über Botenstoffe ( Chemische
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Aufnahme- und Enzymkinetik
 Aufnahme- und Enzymkinetik Kinetik = Verlauf einer Reaktion unter verschiedenen Bedingungen Alle enzym-katalysierten Reaktionen unterliegen Geschwindigkeitsgesetzen Carrier = Enzyme Enzyme sind Biokatalysatoren
Aufnahme- und Enzymkinetik Kinetik = Verlauf einer Reaktion unter verschiedenen Bedingungen Alle enzym-katalysierten Reaktionen unterliegen Geschwindigkeitsgesetzen Carrier = Enzyme Enzyme sind Biokatalysatoren
ANALYTISCHE CHEMIE I Trennmethoden 3. Spezielle LC-Methoden WS 2007/2008
 ANALYTISCHE CHEMIE I Trennmethoden 3. Spezielle LC-Methoden WS 2007/2008 Spezielle LC Methoden Molekülausschlußchromatographie (Gelfiltrations- oder Gelpermeationschromatographie) Durch unterschiedliche
ANALYTISCHE CHEMIE I Trennmethoden 3. Spezielle LC-Methoden WS 2007/2008 Spezielle LC Methoden Molekülausschlußchromatographie (Gelfiltrations- oder Gelpermeationschromatographie) Durch unterschiedliche
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
7. Arachidonsäurestoffwechsel: Prostaglandine
 7. Arachidonsäurestoffwechsel: Prostaglandine Synthese von Prostaglandin (PG) Vorstufen Arachidonsäure wird durch Hydrolyse von Phospholipiden erzeugt Cyclischer und linearer Weg des Arachidonsäurestoffwechsels
7. Arachidonsäurestoffwechsel: Prostaglandine Synthese von Prostaglandin (PG) Vorstufen Arachidonsäure wird durch Hydrolyse von Phospholipiden erzeugt Cyclischer und linearer Weg des Arachidonsäurestoffwechsels
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
OSTEOPOROSE - häufigste alterungsbedingte Knochenerkrankung - F.Neuschäfer-Rube, 11-12-03
 OSTEOPOROSE - häufigste alterungsbedingte Knochenerkrankung - F.Neuschäfer-Rube, 11-12-03 OSTEOPOROSE - häufigste alterungsbedingte Knochenerkrankung -! Verringerung der Knochenmasse und der Knochenarchitektur
OSTEOPOROSE - häufigste alterungsbedingte Knochenerkrankung - F.Neuschäfer-Rube, 11-12-03 OSTEOPOROSE - häufigste alterungsbedingte Knochenerkrankung -! Verringerung der Knochenmasse und der Knochenarchitektur
vom Meldenden Personengruppe, die von der Angabe erfasst werden, eingeschränkt auf
 81 Calcium 82 Calcium 83 Calcium 84 Calcium 85 Calcium 86 Calcium 87 Calcium 88 Calcium 89 Calcium 90 Calcium 91 Calcium 92 Calcium Mineralisierung und Knochendichte/- Calcium ist notwendig für normale
81 Calcium 82 Calcium 83 Calcium 84 Calcium 85 Calcium 86 Calcium 87 Calcium 88 Calcium 89 Calcium 90 Calcium 91 Calcium 92 Calcium Mineralisierung und Knochendichte/- Calcium ist notwendig für normale
Der Sehprozess - Überblick
 Der Sehprozess - Überblick? optischer Reiz?? el. Signal (Nerven) Thema und Inhalt Biophysik des Sehens vom Reiz zum Signal Fragen: Wie funktioniert die Signalwandlung? Wie wird das Signal verstärkt (>
Der Sehprozess - Überblick? optischer Reiz?? el. Signal (Nerven) Thema und Inhalt Biophysik des Sehens vom Reiz zum Signal Fragen: Wie funktioniert die Signalwandlung? Wie wird das Signal verstärkt (>
BK07_Vorlesung Physiologie. 05. November 2012
 BK07_Vorlesung Physiologie 05. November 2012 Stichpunkte zur Vorlesung 1 Aktionspotenziale = Spikes Im erregbaren Gewebe werden Informationen in Form von Aktions-potenzialen (Spikes) übertragen Aktionspotenziale
BK07_Vorlesung Physiologie 05. November 2012 Stichpunkte zur Vorlesung 1 Aktionspotenziale = Spikes Im erregbaren Gewebe werden Informationen in Form von Aktions-potenzialen (Spikes) übertragen Aktionspotenziale
Signaltransduktion. T-Zell Rezeptor-Komplex: Signalauslösung und Regulation
 Signaltransduktion Möglichkeiten der interzellulären Kommunikation Signalweiterleitung in die Zelle ( Transduktion ) Rezeptoren als Signalumwandler T-Zell Rezeptor-Komplex: Signalauslösung und Regulation
Signaltransduktion Möglichkeiten der interzellulären Kommunikation Signalweiterleitung in die Zelle ( Transduktion ) Rezeptoren als Signalumwandler T-Zell Rezeptor-Komplex: Signalauslösung und Regulation
Enzymkinetik Seite 1. Enzyme. Einführung
 Enzymkinetik Seite 1 Enzyme Einführung In jeder Zelle laufen Hunderte chemischer Reaktionen ab, die (mit wenigen Ausnahmen) alle von hochwirksamen Biokatalysatoren (Enzymen ) beschleunigt und gesteuert
Enzymkinetik Seite 1 Enzyme Einführung In jeder Zelle laufen Hunderte chemischer Reaktionen ab, die (mit wenigen Ausnahmen) alle von hochwirksamen Biokatalysatoren (Enzymen ) beschleunigt und gesteuert
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
2. Biochemie Seminar
 2. Biochemie Seminar Rezeptorvermittelte Signaltransduktion (Rezeptortypen und Prinzipien: nucleäre Rezeptoren (Steroid- und Schilddrüsenhormone) - Lipophile Signalmoleküle können durch die Plasmamembran
2. Biochemie Seminar Rezeptorvermittelte Signaltransduktion (Rezeptortypen und Prinzipien: nucleäre Rezeptoren (Steroid- und Schilddrüsenhormone) - Lipophile Signalmoleküle können durch die Plasmamembran
F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH
 B I O C H E M I S C H E S P R A K T I K U M F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH 2003 INHALTSVERZEICHNIS *) Zum Biochemischen Praktikum steht Ihnen
B I O C H E M I S C H E S P R A K T I K U M F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH 2003 INHALTSVERZEICHNIS *) Zum Biochemischen Praktikum steht Ihnen
Autotrophe und heterotrophe Organismen
 Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
4. Quantitative Analyse der Ligand-Bindungsstudien
 4. Quantitative Analyse der Ligand-Bindungsstudien Im folgenden apitel sollen die grundlegenden analytischen Methoden zur Interpretation der experimentell gewonnenen Bindungsdaten vorgestellt werden. ie
4. Quantitative Analyse der Ligand-Bindungsstudien Im folgenden apitel sollen die grundlegenden analytischen Methoden zur Interpretation der experimentell gewonnenen Bindungsdaten vorgestellt werden. ie
The Journal Club. Resistenzmechanismen unter antihormoneller Therapie des fortgeschrittenen Prostatakarzinoms
 The Journal Club Resistenzmechanismen unter antihormoneller Therapie des fortgeschrittenen Prostatakarzinoms Kastrationsresistentes metastasierendes P-Ca (mcrpca) Es gibt unterschiedliche Resistenzmechanismen
The Journal Club Resistenzmechanismen unter antihormoneller Therapie des fortgeschrittenen Prostatakarzinoms Kastrationsresistentes metastasierendes P-Ca (mcrpca) Es gibt unterschiedliche Resistenzmechanismen
Enzymhemmung I EI E. Reversible Hemmung Enzym- Inaktivierung (irreversibel) E I E-I E I EI E-I. Drug targets:
 Enzyheung Reversible Heung Enzy- Inaktivierung (irreversibel) E I E I E IEIE I E I E-I E I EI E-I Drug targets: 1 Pharakologisch wirksae Inhibitoren Aspirin het die Cyclooxygenase Behandlung von Scherz
Enzyheung Reversible Heung Enzy- Inaktivierung (irreversibel) E I E I E IEIE I E I E-I E I EI E-I Drug targets: 1 Pharakologisch wirksae Inhibitoren Aspirin het die Cyclooxygenase Behandlung von Scherz
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot
 Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Der Stoffwechsel: Konzepte und Grundmuster
 Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Genregulation bei Eukaryoten
 Genregulation bei Eukaryoten 1. Allgemeines über Genregulation 2. Aufbau der DNA 3. Enhancer 4. Aktivierung und Repression 5. System, das Östrogene wahrnimmt und auf sie anspricht - DNA- Bindungsdomäne
Genregulation bei Eukaryoten 1. Allgemeines über Genregulation 2. Aufbau der DNA 3. Enhancer 4. Aktivierung und Repression 5. System, das Östrogene wahrnimmt und auf sie anspricht - DNA- Bindungsdomäne
Expressionskontrolle in Eukaryonten
 Expressionskontrolle in Eukaryonten Warum muss Genexpression kontrolliert werden? 1. Gewebsspezifische Kontrolle - nicht jedes Genprodukt ist in allen Zellen erforderlich - manche Genprodukte werden ausschliesslich
Expressionskontrolle in Eukaryonten Warum muss Genexpression kontrolliert werden? 1. Gewebsspezifische Kontrolle - nicht jedes Genprodukt ist in allen Zellen erforderlich - manche Genprodukte werden ausschliesslich
Vorname: Frage 1. Nennen Sie drei Metalle, die :für den Menschen essentiell sind und als Mengenelemente Körper vorkommen (3 P) Frage 2
 1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
Peptide Proteine. 1. Aminosäuren. Alle optisch aktiven proteinogenen Aminosäuren gehören der L-Reihe an: 1.1 Struktur der Aminosäuren
 1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
