Trennung nach molekularer Größe
|
|
|
- Reinhardt Lange
- vor 6 Jahren
- Abrufe
Transkript
1 Chromatographische Untersuchungen von Proteinen und Immunoglobulinen Trennung nach molekularer Größe Dr. Christian Dauwe, Dr. Günter Reinhold, Polymer Standards Service GmbH, Mainz Die chromatographischen Trennung von Proteinen wird von der Art des Eluenten und der Porosität des Trenngels stark beeinflusst. Im Folgenden werden neue hydrophile Chromatographie-Phasen für die Trennung und Analyse von Proteinen nach molekularer Größe vorgestellt. Proteine sind aufgrund ihrer vielfältigen - häufig katalytischen - Einsatzfelder in der Lebensmitteltechnik, Pharmazie und Biotechnik von erheblicher wirtschaftlicher Bedeutung. Vor allem deshalb hat sich die Analytik von Proteinen zu einem wichtigen Betätigungsfeld von Naturwissenschaftlern im Bereich Qualitäts- und Prozesskontrolle sowie in Forschungsabteilungen entwickelt. Häufig verfährt man bei Proteinuntersuchungen in zwei Schritten, denen sich gegebenenfalls weitere Schritte, wie z. B. Eigenschafts/Funktionsprüfung der Proteine anschließen können. Die Proteine sollen während der Aufarbeitung und während der chromatographischen Trennung nicht denaturieren, damit gegebenenfalls anschließende Eigenschafts und Funktiosprüfungen aussagekräftig bleiben. Deshalb sollen die Chromatographiesysteme (Säulenmaterial, Eluent,...) biokompatibel sein, d. h. sie sollen die Wirksamkeit des Proteins nicht verändern. Die zwei wichtigsten Schritte einer Proteinanalytik sind: 1) Trennung/Fraktionierung nach Löslichkeit (Probenvorbereitung) Fällung des Proteins, z. B. aus wässriger Lösung mit Ammoniumsulfat oder mit Alkohol. 2) Chromatographische Trennung Hydrophobe Wechselwirkungs- Chromatographie (HIC) Reversed Phase Chromatographie (RP) Ionenaustauschchromatographie (IC) Größenausschlusschromatographie (GPC bzw. SEC). Die Fülle chromatographischer Separationsmethoden für Proteintrennungen/-analysen liegt in den komplexen Eigenschaften dieser Moleküle begründet. Bei den Proteinen handelt es sich um polykondensierte Aminosäuren. Die Molmassen reichen von wenigen D bis zu mehreren D. Die Seitengruppen der Aminosäureeinheiten sind aliphatisch lipophil, aromatisch lipophil, Phenole, Carbonsäuren oder Basen. Durch Einstellungen des Eluenten im Bezug auf Ionenstärke und des ph-wertes oder mit organischen Zusätzen, auch Modifier genannt, (z. B. Alkohole oder Acetonitril) werden die äußere Ladung (Polyanion-, Betain- oder Polykation-Struktur), die molekulare Größe (z. B. gemessen in Å) und die Löslichkeit dieser komplex aufgebauten Biopolymere eingestellt. Zugleich werden diese Parameter zur Steuerung der chromatographischen Trennung der Proteine verwendet. Im hier vorliegenden Artikel werden wir auf die Trennung von Proteinen nach deren molekularer Größe eingehen. Hierfür müssen die zu untersuchenden Proteine gut löslich im chromatographischen Eluenten sein. Die Wechselwirkungen mit der stationären Phase werden durch entsprechende Eluenteinstellungen ausgeschlossen (Einstellung einer hohen Ionenstärke zur Unterdrückung ionischer Wechselwirkungen mit der stationären Phase oder Verwendung organischer Modifier zur Unterdrückung lipophiler Adsorption an der stationären Phase). Abb. 1: GPC-Trennmechanismus unterschiedlich großer/voluminöser Proteine an porösen Gelmaterialien. GPC-Trennungen von Proteinen GPC-Trennungen von Proteinen gelingen mit Proteinfraktionen, die im GPC-Eluenten bzw. GPC-Laufmittel gut löslich sind. Diese Trennungen erfolgen streng nach molekularer Größe, sofern Wechselwirkungen mit der stationären Phase ausgeschlossen werden (Abb. 1). Die molekulare Größe der Proteine korreliert 176 CLB Chemie in Labor und Biotechnik, 52. Jahrgang, Heft 5/2001
2 zwar mit deren Molmasse, diese Übereinstimmung ist aber aufgrund des komplexen Charakters der Proteine weniger ausgeprägt als bei Polysacchariden oder technischen Polymeren. Zudem lässt sich die molekulare Größe bzw. die Tertiärstruktur von Proteinen durch die Wahl des Lösungsmittels stark beeinflussen. Somit erwarten wir für unterschiedliche Lösungsmittel/Eluenten auch unterschiedliche chromatographische Ergebnisse. Die Untersuchung der Abhängigkeit der GPC-Separationsleistung vom gewählten Eluenten und der Porosität des GPC-Materials sind damit Ziele, auf die wir im Folgenden eingehen werden. Stand der Technik und Entwicklungsziele Für GPC-Proteintrennungen haben sich Polysaccharidphasen, Polymerphasen und hydrophil modifizierte Silicaphasen etabliert. Polysaccharidphasen weisen häufig eine geringe Druckstabilität auf. Dies bedingt teilweise geringe Lebensdauern der Säulen. Die benötigten geringen Flussraten (wegen der geringen Druckstabilität) bedingen häufig lange Analysenzeiten. Allerdings zeigen diese Polysaccharid-Gele häufig sehr hohe chromatographische Auflösungen. Bei einigen etablierten Polymer- und Silicaphasen treten aufgrund geringer Druckstabilität ebenfalls häufig verkürzte Lebensdauern der GPC-Säulen auf. Hydrophil modifizierte Silicaphasen können bei hohen ph-werten durch Silica-Abbau verändert werden. Die Auswahl des geeigneten Eluenten für Protein-GPC-Analysen ist häufig schwierig. Es gilt, Wechselwirkungen zwischen dem Protein und der Säulenoberfläche auszuschalten. Etabliert haben sich insbesondere folgende Eluenten: Puffermischungen (ph 5-8) mit 0,1 oder 0,2 M NaCl, Puffermischungen mit SDS, sowie Wasser mit unterschiedlich hohen Anteilen organischer Eluenten (Acetonitril, Methanol). Aufgrund der Empfindlichkeit zahlreicher GPC- Säulenmaterialien und wegen der sehr unterschiedlichen chemischen bzw. Lösungseigenschaften von Proteinen kann die Methodenentwicklung dieser GPC-Trennungen komplex verlaufen. Ziel unserer Untersuchung war die Entwicklung eines einfach handhabbaren und zudem robusten GPC-Materials für Proteinuntersuchungen inklusive der dazugehörigen Trennmethodenentwicklung. Die Entwicklungsziele in Stichworten: hohe Druckstabilität (>80 bar) geringer Säulen-Gegendruck durch monodisperse Gelpartikel AUFSÄTZE geringer bzw. nicht feststellbarer Scherabbau großer Proteine durch monodisperse Gelpartikel hohe theoretische Bodenzahl durch 10-µm-Gelpartikel ( theoret. Böden/m) große zugängliche Porenvolumina (>50 %) für hohe GPC-Separationsleistungen definierte Porengrößen zur Trennung unterschiedlich großer Proteine hohe ph-wert-stabilität GPC-Proteintrennungen in sauren Eluenten und auch bei hoher Salzfracht des Eluenten Diese Ziele wurden mit der Neuentwicklung des GPC-Säulenmaterials für Proteintrennungen (PSS Novema TM ) erreicht. Details werden den folgenden Abschnitten präsentiert. Experimentelles GPC-System: Die Software PSS WinGPC 6.20 steuerte das iskokratische HP-1100-HPLC-System mit Abb. 2: Porositäten von PSS- Novema TM 8 x 300mm (Pullulan Kalibrationskurven, D); Eluent: 0.05% NaN 3 in Wasser, Injektionsvolumen: 20 µl, Probenkonzentration: 5mg/ml, Fluss: 1ml/min, Detektion: RI. Porositäten: 30 Å, 300 Å, 1000 Å, 3000 Å (aufgezählt von der unteren zur oberen Kalibrationskurve). CLB Chemie in Labor und Biotechnik, 52. Jahrgang, Heft 5/
3 GPC von Proteinen Abb. 3: Zusammenhang zwischen Protein-Molmasse und Elutionsvolumen: PSS Novema TM 300Å, 8 x 300 mm; Eluent: 40 % Acetonitril, 60 % Wasser mit 0.5 % TFA, Injektionsvolumen: 20µl, Probenkonzentration: 5 mg/ml, Fluss: 1ml/min, Detektion: UV 230 nm. UV-Detektor (230 nm), extern: Shodex RI 71 Detektor, Injektionsvolumen: 20 µl. Probenkonzentration: 5 g Protein/l Eluent, Flussrate (sofern nicht anders beschrieben): 1,0 ml/min, Temperatur: 20 C. PSS Novema TM Säulen (8 x 300 mm): 30, 300, oder Å, 10 µm. Eluenten: 0,0667 M NaKHPO 4 - Puffer ph 6,8 + 0,1 M NaCl (9,078g KH 2 PO ,876g Na 2 HPO ,68g NaCl gelöst in 2000 g kochendem Wasser) oder 0,5 % Vol.% Trifluoressigsäure in Wasser/Acetonitril (60/40 // Vol./Vol.). Enzyme: Vitamin B 12 (1,355 kd), Insulin bovine pancreas (5,733 kd), Lactalbumin-bovine-Milk (14,2 kd), Lysozym hen egg (14,6 kd), Trypsin bovine pancreas (23 kd), Trypsin hog pancreas (24 kd), Proteinase Bacillus licheniformis (27 kd), Albumin hen egg (45 kd), Albumin bovine (67- kd-monomer, 134-kD-Dimer), Amylase sweet potato (200 kd), Ferritin horse (450 kd), Thyroglobulin bovine thyroid glands (660 kd) (Firma Fluka oder Aldrich). Immunoglobulin: Host: Rabbit Anti-, Antigen: Human IgG (Fc), Label: Horseradish Peroxidase; Pierce company. Ergebnisse Porenvolumina und Porengrößen von PSS Novema TM Porenvolumina und Porengrößen bzw. GPC-Trennbereiche von PSS Novema TM wurden mittels GPC-Kalibrationskurven von Pullulanen unverzweigten Zuckern dargestellt (Abb. 2). Deutlich erkennt man die gute Separationsleistung von PSS Novema TM 30 Å im Bereich vom Oligomer bis zu Molmassen von D. PSS Novema 300 Å erlaubt die Trennung von Oligomeren bis hin zu Molmassen von D. Dieses Material weist für den untersuchten Bereich einen nahezu linearen Zusammenhang auf zwischen dem Logarithmus der Molmasse und dem Elutionsvolumen. Das größerporige Gelmaterial mit Å-Porosität trennt den Bereich vom Monomer bis D, und das Gel mit Å-Porosität trennt den Bereich bis über D. Die größerporigen Säulen PSS Novema TM und Å verfügen allerdings über eine geringe chromatographische Auflösung für Oligomere. GPC-Trennungen in wässrig-organischen Lösungsmittelgemischen Das neue PSS Novema TM wurde in einer Eluentenmischung untersucht, die sich für zahlreiche Protein-GPC- Trennungen auf unterschiedlichen Säulenmaterialien bewährt hat: 0,5 % Trifluoressigsäure in Wasser/Acetonitril (60/40 // v/v). Untersucht wurden PSS Novema TM 30-Åund PSS Novema TM 300-Å-Säulen. Die größerporige GPC-Säule PSS Novema TM 300-Å-Säule eignet sich hervorragend für Protein-GPC-Trennungen. Es zeigt sich ein sehr guter Zusammenhang zwischen dem Elutionsvolumen und der Molmasse der Proteine. Die Ergebnisse sind in Abb. 3 dargestellt. Das kleinerporige Material PSS Novema TM 30 Å zeigte in dieser organisch/wässrigen Eluentenmischung für zahlreiche untersuchte Proteine GPC-Trennungen. Einige kleinere Proteine mit Molmassen von < 24 kd erscheinen allerdings auf der PSS Novema TM 30-Å-Säule (oberflächenreiches Material) an der GPC-Trennschwelle (geringe Adsorption). Deshalb ist für diese Eluentenmischung PSS Novema TM 300 Å vorzuziehen, da Adsorptionseffekte hier nicht unter diesen Messbedingungen beobachtet werden (weniger oberflächenreiches Material). Es zeigte sich bei den Untersuchungen, dass die größenchromatographische Auflösung (Peakschärfe bzw. Peakseparation) mit Verringerung der Flussgeschwindigkeit zunimmt. Für hochauflösende GPC-Trennungen mehrerer Proteine an PSS Novema TM sollte ein Fluss von 0,5 ml/min oder weniger anstatt der GPC-üblichen 1 ml/min verwendet werden. Diese geringeren Flüsse erlauben eine bessere Zugänglichkeit der Poren für die häufig sehr großen und langsam diffundierenden Proteine. GPC-Trennungen in wässrigen Eluenten mit Puffern GPC-Untersuchungen in gepufferten wässrigen Systemen in Abwesenheit organisch/wässriger Mischlösungsmittel bieten die Möglichkeit, die GPC-Separationsmethode mit der Lichtstreudetektion zu koppeln. Bei bekanntem Brechungsinkrement (dn/dc-wert) des Proteins kann die Molmasse unbekannter Proteine aus dem Lichtstreusignal berechnet werden. Zudem erlaubt diese Methode die Bestimmung der Proteinstruktur in Lösung. 178 CLB Chemie in Labor und Biotechnik, 52. Jahrgang, Heft 5/2001
4 GPC-Untersuchungen von Proteinen in wässrigen Eluenten mit Puffern gelingen, wenn Wechselwirkungen zwischen dem Protein und der stationären Phase ausgeschlossen werden. Am häufigsten treten bei Proteinen aufgrund ihrer Struktur hydrophobe und auch ionische Wechselwirkungen auf. Die Einstellung eines geeigneten ph-wertes (5 8) und die Zugabe einer geeigneten Salzfracht (bzw. Ionenstärke) zum Eluenten, z. B. 0,1 oder 0,2 M NaCl erlaubt in den meisten Fällen die Unterdrückung dieser beiden störenden Wechselwirkungen. Sehr viel stärkere Salzkonzentrationen (>1 M NaCl) bewirken hydrophobe Wechselwirkungen mit der GPC-Gel-Oberfläche, geringere Salzkonzentrationen (< 0,1 M NaCl) bewirken häufig das Auftreten ionischer Wechselwirkungen. Insbesondere bei kleinporigen Säulenmaterialien, die große Oberflächen aufweisen, sind diese adsorptiven Wechselwirkungen bekannt. Bei großporigen Säulenmaterialien werden diese Phänomene seltener beobachtet. Die Einstellung der geeigneten Ionenstärke im Eluenten ist daher wichtig für eine gute GPC- Trennung von Proteinen, insbesondere an kleinporigen Säulenmaterialien. Der ph-wert des Eluenten sollte sich bei der GPC-Trennung vom isoelektrischen Punkt (pi) des Proteins unterscheiden. Am isoelektrischen Punkt ist ein Protein nach außen neutral, d. h. es kompensieren sich die negativen und positiven Ladungen. Günstig für die GPC-Trennung ist ein ph-wert des Eluenten, der sich vom isoelektrischen Punkt (pi) unterscheidet. Dabei tritt eine äußere Nettoladung für das Protein auf. Es wurden folgende Puffer/Salz- Lösungen als Eluenten für die Proteintrennungen untersucht: 1) 0,0667 M NaKHPO 4 -Puffer ph 6,8 in Wasser 2) 0,0667 M NaKHPO 4 -Puffer ph 6,8 + 0,1 M NaCl in Wasser 3) 0,0667 M NaKHPO 4 -Puffer ph 6,8 + 0,2 M NaCl in Wasser. AUFSÄTZE lysen an den untersuchten Proteinen. Die 300-Å-Säule war zu großporig für eine hohe chromatographische Auflösung für die untersuchten Proteine in diesen rein wässrigen, gepufferten salzhaltigen Eluenten. PSS Novema TM 30 Å zeigte bei Verwendung des Eluenten (2) und ebenso bei Verwendung des Eluenten (3) gute und vergleichbare GPC-Separationen für die untersuchten Proteine. Der Zusatz von 0,1 M NaCl zum Phosphatpuffer war ausreichend zur Unterdrückung der ionischen Wechselwirkungen mit dem (kleinporigen) Säulenmaterial. Die Verwendung des Phosphatpuffers ohne NaCl-Zusatz führte allerdings zur Adsorption zahlreicher Proteine, so dass sich Eluent (1) nicht zur GPC-Trennung der untersuchten Proteine an PSS Novema TM 30 Å empfiehlt. Für Proteintrennungen sollte nach unseren Erfahrungen als erster Schritt der Methodenentwicklung Eluent (2) eingesetzt werden, falls rein wässrig gepufferte Systeme zur Anwendung kommen sollen. Eluent (2) hat im Vergleich zu Eluent (3) den Vorteil, dass dieser den geringeren (HPLC-System verschleißenden) Salzgehalt aufweist. Abb. 4 zeigt die Ergebnisse. Zur Erhöhung der Lebensdauer des HPLC/GPC System (Pumpen, Kapillaren,...) sollte man nach Verwendung der Pufferlösungen (z. B. bei Messpausen am Wochenende) in jedem Fall das Gesamtsystem auf reines Wasser bzw. auf 0,05 % NaN 3 in Wasser umstellen. Diskussion der Proteinuntersuchungen Wässrige Eluenten mit erhöhter Ionenstärke ergeben für die von uns untersuchten Proteine auf dem kleinporigen PSS Novema TM 30-Å-Material gute GPC-Trennungen. Die Porengröße ist den molekularen Größen der Proteine unter diesen Bedingungen angepasst und Adsorptionen treten nicht auf. Hingegen erzielen wir für die gleichen Proteine in dem von uns verwendeten sauren organisch/wässrigen Eluenten eine vergleichbar gute Trennung, wenn die größerporige PSS Novema TM 300-Å- Säule verwendet wird. Der Grund für dieses unterschiedliche Verhalten wird einleuchtend bei näherer Betrachtung der Proteine Abb. 4: Zusammenhang zwischen Protein-Molmasse und Elutionsvolumen: PSS Novema TM 30Å 8 x 300 mm, Eluent: 0,07 M Na/K/HPO 4 -Puffer ph ,1 M NaCl in Wasser, Injektionsvolumen: 20 µl, Probenkonzentration: 5 mg/ml, Fluss: 1ml/min, Detektion: UV 230nm. PSS Novema TM 30-Å- und 300-Å- Säulen wurden getestet. Die kleinporige PSS Novema TM 30Å-Säule erwies sich als geeignet für GPC-Ana- CLB Chemie in Labor und Biotechnik, 52. Jahrgang, Heft 5/
5 GPC von Proteinen Detector Response 0,0100 0,0075 0,0050 0,0025 0, und des GPC-Trennmechanismus: Proteine sind Polykondensate von Aminosäuren, tragen somit eine Polyamid-Hauptkette. Die Seitenketten sind lipophil, sauer oder basisch. Proteine verhalten sich wegen ihrer äußeren Ladung als Polyelektrolyte. Im sauren Eluenten mit organischem Modifier geschieht Folgendes: Das Protein liegt als Polykation vor (die basischen Seitenketten sind protoniert und tragen positive Ladungen). Gleiche Ladungen unterliegen der elektrostatischen Abstoßung. Damit streckt sich das Protein und nimmt für sich einen großen Raum ein. Da bei GPC-Trennungen die Analyte primär nach molekularer Größe getrennt werden, benötigen wir in diesem Fall für die groß erscheinenden Proteine ein größerporiges GPC-Material (PSS Novema TM 300 Å). Im nahezu neutralen gepufferten Eluenten mit hoher Salzfracht liegt folgender Fall vor: Die Proteine tragen partiell positive (Ammonium- Gruppen) und auch negative (Carboxylat-Gruppen) Ladungen. Eine geringe Nettoladung positiv oder negativ erscheint nach außen. Das Protein wird weniger gestreckt, als wenn es als reines Polykation vorläge. Zudem führt die hohe Salzkonzentration des Eluenten zu einem Schrumpfungsprozess des Proteins Volume [ml] RI UV 230nm Abb. 5: GPC-Analyse des Antikörperkomplexes Rabbit Anti Human IgG. 1,0 ml/min 0,0667 M NaKHPO4- Puffer ph 6,8 in Wasser, PSS-Novema TM 300 Å Säule, 8x300 mm, Detektor: UV 230 nm + RI, Injektionsvolumen: 20 µl 0,5 %ige Antikörperlösung im Eluenten. (normales Verhalten eines Polyelektrolyten). Die Proteine erscheinen als kleine Moleküle. Somit eignet sich hier insbesondere das kleinporige PSS Novema TM 30-Å-Material für die GPC-Untersuchungen. Immunoglobuline Immunoglobuline (IgGs) sind von zentraler Bedeutung für das Immunsystem und somit auch von erheblichem therapeutischem Interesse. Immunoglobuline weisen Strukturelemente auf, welche spezifisch über Nebenvalenzen mit den Antigenen reagieren. Die Bildung von Immunoglobulinen erfolgt durch Reaktion von z. B. Fremdproteinen auf den Organismus eines Menschen oder eines Wirbeltieres. Es bilden sich Antikörper gegen diese Fremdstoffe (Antigene). Antigen und Antikörper reagieren miteinander zu einem Komplex. Die Antikörper sind die Proteine des Blutplasmas und gehören zu den gamma-globulinfraktionen. Sie werden auch Immunoglobuline genannt. Untersuchungen an Immunoglobulinen erfolgen durch Funktions- bzw. Eigenschaftsprüfungen, aber auch mittels Chromatographie. Insbesondere die Größenausschlusschromatographie ist geeignet, strukturelle Informationen über das Gesamtmolekül zu erhalten. Eine entsprechendes Elugramm des kommerziell erhältlichen Antikörperkomplexes Rabbit Anti Human IgG an PSS Novema TM 300 Å wird in Abb. 5 vorgestellt. Deutlich erkennbar ist der UV-aktive Peak bei einem Elutionsvolumen von 7,6 ml, die der UV-aktiven Globulinfraktion zugeschrieben werden kann. Die Kombination von UV und RI-Detektion deckt auf, dass das untersuchte Immunoglobulin aus unterschiedlichen chemischen Strukturelementen aufgebaut ist, UV- (230nm) und nicht-uv-aktive Bestandteile. Das im Immunoglobulin enthaltene Globulin entspricht unter den Untersuchungsbedingungen (Art des Puffers, Ionenstärke) der Größe eines Pullulans mit der Molmasse D (vgl. Abb. 2). Die Kopplung der GPC mit der Viskositäts- oder Lichtstreudetektion sollte zur Ermittlung weiterer struktureller Informationen dieses Komplexes führen. Zusammenfassung und Ausblick PSS Novema TM -GPC-Säulen sind geeignet für GPC-Untersuchungen an Proteinen. Es können organisch/wässrige Eluentensysteme mit Trifluoressigsäure für die Trennungen verwendet werden, aber auch wässrige gepufferte Systeme mit ausreichend hoher Ionenstärke. Die Abschätzung des Zusammenhangs zwischen räumlicher Größe (Tertiärstruktur) der Proteine und der Art des Lösungsmittels kann durch den Vergleich der entsprechenden Protein-Kalibrationskurven getroffen werden. Die Kopplung dieser GPC-Trennungen mit Viskositäts- oder Lichtstreudetektoren führt zur deutlichen Erhöhung der Genauigkeit der Größen- und Strukturbestimmung von Proteinen in Lösung (im Eluenten). Referenzen K. K. Unger, Handbuch der HPLC, GIT-Verlag Darmstadt (1989). C.S. Wu, Column Handbook for Size Exclusion Chromatography, Academic Press, San Diego (1999). B. J. Hunt, S. R. Holding, Size Exclusion Chromatography, Blackie Publisher, Glasgow (1989). Kontakt: Dr. Christian Dauwe, Dr. Günter Reinhold, Polymer Standards Service GmbH, Postfach 3368, Mainz. cdauwe@polymer.de und greinhold@polymer.de 180 CLB Chemie in Labor und Biotechnik, 52. Jahrgang, Heft 5/2001
Im Blickpunkt: PSS Schulungen. Inhalt: Aktuelle Nachrichten von PSS Polymer Standards Service GmbH. Ausgabe: Herbst 2001
 Aktuelle Nachrichten von PSS Polymer Standards Service GmbH Ausgabe: Herbst 2001 Im Blickpunkt: SIE PSS, dieser Name steht seit über 15 Jahren für Qualität, Innovation, Wissen und Erfahrung in der GPC.
Aktuelle Nachrichten von PSS Polymer Standards Service GmbH Ausgabe: Herbst 2001 Im Blickpunkt: SIE PSS, dieser Name steht seit über 15 Jahren für Qualität, Innovation, Wissen und Erfahrung in der GPC.
Agilent AdvanceBio Oligonucleotide-Säulen und Oligonukleotidstandards ERHÖHTE ZUVERLÄSSIGKEIT. GERINGERE KOSTEN. GRÖSSERE FLEXIBILITÄT.
 Agilent AdvanceBio Oligonucleotide-Säulen und Oligonukleotidstandards ERHÖHTE ZUVERLÄSSIGKEIT. GERINGERE KOSTEN. GRÖSSERE FLEXIBILITÄT. AGILENT ADVANCEBIO OLIGONUCLEOTIDE-SÄULEN UND OLIGONUKLEOTIDSTANDARDS
Agilent AdvanceBio Oligonucleotide-Säulen und Oligonukleotidstandards ERHÖHTE ZUVERLÄSSIGKEIT. GERINGERE KOSTEN. GRÖSSERE FLEXIBILITÄT. AGILENT ADVANCEBIO OLIGONUCLEOTIDE-SÄULEN UND OLIGONUKLEOTIDSTANDARDS
Wichtige (Säulen-)chromatographische Trennmethoden in der Proteinanalytik: Adsorptions-/Verteilungschromatographie
 Wichtige (Säulen-)chromatographische Trennmethoden in der Proteinanalytik: Gelfiltration Trennung nach Molekülgröße Ionenaustauschchromatographie Trennung nach Ladung Adsorptions-/Verteilungschromatographie
Wichtige (Säulen-)chromatographische Trennmethoden in der Proteinanalytik: Gelfiltration Trennung nach Molekülgröße Ionenaustauschchromatographie Trennung nach Ladung Adsorptions-/Verteilungschromatographie
High Performance Liquid Chromatography
 Was ist? Was ist das Besondere? Aufbau Auswertung Möglichkeiten & Varianten der Zusammenfassung High Performance Liquid Chromatography () Systembiologie - Methodenseminar WS 08/09 FU Berlin 10. November
Was ist? Was ist das Besondere? Aufbau Auswertung Möglichkeiten & Varianten der Zusammenfassung High Performance Liquid Chromatography () Systembiologie - Methodenseminar WS 08/09 FU Berlin 10. November
Proteine I. Fällung Konzentrationsbestimmung. Dr. Richard Weiss
 Proteine I Fällung Konzentrationsbestimmung Dr. Richard Weiss Praktikumsaufbau Tag 1: Konzentrieren Denaturierende und native Fällung Protein Konzentrationsbestimmung Tag 2: Entsalzen Gelchromatographie
Proteine I Fällung Konzentrationsbestimmung Dr. Richard Weiss Praktikumsaufbau Tag 1: Konzentrieren Denaturierende und native Fällung Protein Konzentrationsbestimmung Tag 2: Entsalzen Gelchromatographie
Als "normale" Adsorptionschromatographie bezeichnet man Systeme, bei denen die stationäre Phase polarer ist als das Elutionsmittel.
 Chromatographie: Bei der Reinigung von Stoffen durch chromatographische Verfahren werden die Komponenten eines Gemisches nach bestimmten Gesetzmäßigkeiten zwischen einer stationären Phase und einer mobilen
Chromatographie: Bei der Reinigung von Stoffen durch chromatographische Verfahren werden die Komponenten eines Gemisches nach bestimmten Gesetzmäßigkeiten zwischen einer stationären Phase und einer mobilen
1 Grundlagen der Chromatographie
 1 1 Grundlagen der Chromatographie Chromatographie für Einsteiger. Karl Kaltenböck Copyright 2008 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ISBN: 978-3-527-32119-3 1389vch01.indd 1 22.06.2008 20:39:43
1 1 Grundlagen der Chromatographie Chromatographie für Einsteiger. Karl Kaltenböck Copyright 2008 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ISBN: 978-3-527-32119-3 1389vch01.indd 1 22.06.2008 20:39:43
Einlasssystem oder Voraussetzung für optimale Datenqualität Die Rolle des LC in der LC/MS Analytik
 Einlasssystem oder Voraussetzung für optimale Datenqualität Die Rolle des LC in der LC/MS Analytik Dr. Udo Huber Produktspezialist LC Agilent Technologies 1 Braucht man eine gute chromatographische Trennung
Einlasssystem oder Voraussetzung für optimale Datenqualität Die Rolle des LC in der LC/MS Analytik Dr. Udo Huber Produktspezialist LC Agilent Technologies 1 Braucht man eine gute chromatographische Trennung
Gerinnung von Proteinen
 V11 Gerinnung von Proteinen Fach Klasse Überthema Feinthema Zeit Chemie Q2 Aminosäuren, Peptide, Polypeptide Proteine 20 Minuten Zusammenfassung: Die Gerinnung von Eiklar wird durch Zugabe von gesättigter
V11 Gerinnung von Proteinen Fach Klasse Überthema Feinthema Zeit Chemie Q2 Aminosäuren, Peptide, Polypeptide Proteine 20 Minuten Zusammenfassung: Die Gerinnung von Eiklar wird durch Zugabe von gesättigter
Proteine II Chromatographie und Dialyse. Dr. Sandra Scheiblhofer
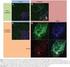 Proteine II Chromatographie und Dialyse Dr. Sandra Scheiblhofer Isolierung von Proteinen > 30.000 Proteine im menschlichen Organismus, beträchtlicher Teil davon nicht oder nur über die biologische Aktivität
Proteine II Chromatographie und Dialyse Dr. Sandra Scheiblhofer Isolierung von Proteinen > 30.000 Proteine im menschlichen Organismus, beträchtlicher Teil davon nicht oder nur über die biologische Aktivität
TICKER. » Lesen Sie weiter auf Seite 2. Sie brauchen sichere und intelligente GPC/SEC Lösungen? Die Top-Themen
 Aktuelle Nachrichten Ausgabe erbst 2007 TICKER Sie brauchen sichere und intelligente GPC/SEC Lösungen? Intelligente Detektion mit PSS SECcurity Das modulare PSS SECcurity GPC1200-System unterstützt die
Aktuelle Nachrichten Ausgabe erbst 2007 TICKER Sie brauchen sichere und intelligente GPC/SEC Lösungen? Intelligente Detektion mit PSS SECcurity Das modulare PSS SECcurity GPC1200-System unterstützt die
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch/ Elektrophorese 2 Elektrophorese
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch/ Elektrophorese 2 Elektrophorese
Einfache Tipps und Wege zur Erhöhung der Lebensdauer von HPLC-Säulen. Dr. Frank Michel
 Einfache Tipps und Wege zur Erhöhung der Lebensdauer von HPLC-Säulen Dr. Frank Michel 1 Übersicht Methode Apparatives Generelles 2 Methode Mobile Phase Organischer Modifier Wässriger Anteil Verwendung
Einfache Tipps und Wege zur Erhöhung der Lebensdauer von HPLC-Säulen Dr. Frank Michel 1 Übersicht Methode Apparatives Generelles 2 Methode Mobile Phase Organischer Modifier Wässriger Anteil Verwendung
1. HPLC-Pumpe (2-Kanal Gradient) Überprüfung der Flussrate und der Gradientenzusammensetzung. Einstellungen Mobile Phase entgastes Wasser
 Geräte im Labor Pharmafirma Qualifizierungsplan (OQ) Seite 1 von 7 Inhalt 1. HPLC-Pumpe (2-Kanal Gradient) 1.a Überprüfung der 1.b Überprüfung der Gradientenzusammensetzung und des Rauschens des Gradientenmischers
Geräte im Labor Pharmafirma Qualifizierungsplan (OQ) Seite 1 von 7 Inhalt 1. HPLC-Pumpe (2-Kanal Gradient) 1.a Überprüfung der 1.b Überprüfung der Gradientenzusammensetzung und des Rauschens des Gradientenmischers
Proteinanalyse mittels SDS-PAGE (SDS Polyacrylamid Gel-Elektrophorese)
 Praktikum IV, SS 07 Biologieversuch 2-23.05.2007 Proteinanalyse mittels SDS-PAGE (SDS Polyacrylamid Gel-Elektrophorese) Zahner Michele (zahnerm@student.ethz.ch) Büchi Luca (lbuechi@student.ethz.ch) Reibisch
Praktikum IV, SS 07 Biologieversuch 2-23.05.2007 Proteinanalyse mittels SDS-PAGE (SDS Polyacrylamid Gel-Elektrophorese) Zahner Michele (zahnerm@student.ethz.ch) Büchi Luca (lbuechi@student.ethz.ch) Reibisch
Im Blickpunkt: Qualität
 PSS-Ticker_Final 20.09.2000 1:55 Uhr Seite 6 Aktuelle Nachrichten von PSS Polymer Standards Service GmbH Ausgabe: Herbst 2000 Im Blickpunkt: Qualität Die neueste Ausgabe des PSS-Tickers befasst sich mit
PSS-Ticker_Final 20.09.2000 1:55 Uhr Seite 6 Aktuelle Nachrichten von PSS Polymer Standards Service GmbH Ausgabe: Herbst 2000 Im Blickpunkt: Qualität Die neueste Ausgabe des PSS-Tickers befasst sich mit
Quantitative Analyse des Polysaccharides Sinistrin in Serum mittels HPLC und elektrochemischer Detektion
 Quantitative Analyse des Polysaccharides Sinistrin in Serum mittels HPLC und elektrochemischer Detektion D. Payerl, K. Öttl und G. Reibnegger Institut für Medizinische Chemie & Pregl-Laboratorium Harrachgasse
Quantitative Analyse des Polysaccharides Sinistrin in Serum mittels HPLC und elektrochemischer Detektion D. Payerl, K. Öttl und G. Reibnegger Institut für Medizinische Chemie & Pregl-Laboratorium Harrachgasse
Veronika R. Meyer Praxis der Hochleistungs- Flüssigchromatographie
 Jnv. - Mr. 1 I l ~ L 0100 Dar^is".^, Peters^netrsi'?-';-18 Veronika R. Meyer Praxis der Hochleistungs- Flüssigchromatographie Verlag Moritx Diesterweg Frankfurt am Main Verlag Sauerländer Aarau Frankfurt
Jnv. - Mr. 1 I l ~ L 0100 Dar^is".^, Peters^netrsi'?-';-18 Veronika R. Meyer Praxis der Hochleistungs- Flüssigchromatographie Verlag Moritx Diesterweg Frankfurt am Main Verlag Sauerländer Aarau Frankfurt
Biochromatografie. Bioline
 Biochromatografie Bioline Solide Basis KNAUER Systeme für die Biochromatografie verwenden durchdachte Geräte- und Software-Lösungen, um effektive Trennungen hoher Qualität zu erzielen. Das Bioline Start
Biochromatografie Bioline Solide Basis KNAUER Systeme für die Biochromatografie verwenden durchdachte Geräte- und Software-Lösungen, um effektive Trennungen hoher Qualität zu erzielen. Das Bioline Start
8 Better Peakshape. min
 ProntoSIL Hypersorb ODS Die Alternative zu Hypersil ODS Keine Revalidierung der HPLC-Methode erforderlich Breite Palette an Säulendimensionen Höchste Qualität der Säulenpackung Refill Service Preisvorteil
ProntoSIL Hypersorb ODS Die Alternative zu Hypersil ODS Keine Revalidierung der HPLC-Methode erforderlich Breite Palette an Säulendimensionen Höchste Qualität der Säulenpackung Refill Service Preisvorteil
KOFFEINBESTIMMUNG IN KAFFEEBOHNEN
 1 Lebensmittelanalytisches Praktikum für Ernährungswissenschaftler KOFFEIBESTIMMUG I KAFFEEBOHE Einleitung: Struktur von Koffein: H 3 C O O CH 3 CH 3 1,3,7-Trimethylxanthin atürliches Vorkommen: Kaffeebohnen
1 Lebensmittelanalytisches Praktikum für Ernährungswissenschaftler KOFFEIBESTIMMUG I KAFFEEBOHE Einleitung: Struktur von Koffein: H 3 C O O CH 3 CH 3 1,3,7-Trimethylxanthin atürliches Vorkommen: Kaffeebohnen
PSS TICKER. GPC / SEC - Service. Ausgabe Herbst 2010
 Ausgabe Herbst 2010 PSS TICKER GPC / SEC - Service In den vergangenen Jahre wurden in der chemischen und pharmazeutischen Industrie immer mehr Laborarbeitsplätze eingespart. Immer weniger Fachleute müssen
Ausgabe Herbst 2010 PSS TICKER GPC / SEC - Service In den vergangenen Jahre wurden in der chemischen und pharmazeutischen Industrie immer mehr Laborarbeitsplätze eingespart. Immer weniger Fachleute müssen
Analytische Chemie II Modul 1
 Analytische Chemie II Modul 1 1. a) Ein Stoff A und seine Verunreinigung B beide mit Masse m A = m B = 1 sind durch Extraktion voneinander zu trennen. Berechnen Sie, wie viele Extraktionsschritte notwendig
Analytische Chemie II Modul 1 1. a) Ein Stoff A und seine Verunreinigung B beide mit Masse m A = m B = 1 sind durch Extraktion voneinander zu trennen. Berechnen Sie, wie viele Extraktionsschritte notwendig
Typische Fragen für den Gehschul-Teil: Typ 1: Mengen und Konzentrationen:
 Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Aus organisatorischen Gründen wird dieser Test gleichzeitig mit der Prüfung aus Grundlagen der Biochemie angeboten. Das Abschneiden
Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Aus organisatorischen Gründen wird dieser Test gleichzeitig mit der Prüfung aus Grundlagen der Biochemie angeboten. Das Abschneiden
HPLC im Spannungsfeld zwischen Auflösung und Probedurchsatz
 HPLC im Spannungsfeld zwischen Auflösung und Probedurchsatz Thomas Welsch, v. Universität Ulm, Institut für Analytische und Bioanalytische Chemie, Ulm, Deutschland thomas.welsch@uni-ulm.de TZ ekolampad,
HPLC im Spannungsfeld zwischen Auflösung und Probedurchsatz Thomas Welsch, v. Universität Ulm, Institut für Analytische und Bioanalytische Chemie, Ulm, Deutschland thomas.welsch@uni-ulm.de TZ ekolampad,
Schnelle Optimierung in der HPLC ein Vorschlag. Stavros Kromidas, Saarbrücken
 Schnelle Optimierung in der HPLC ein Vorschlag Stavros Kromidas, Saarbrücken 29. September 2009, Jena NOVIA GmbH Seite 1 Das 5 - oder genauer, das 3+2-Schritte-Modell Ein Konzept für eine effektive Methodenentwicklung
Schnelle Optimierung in der HPLC ein Vorschlag Stavros Kromidas, Saarbrücken 29. September 2009, Jena NOVIA GmbH Seite 1 Das 5 - oder genauer, das 3+2-Schritte-Modell Ein Konzept für eine effektive Methodenentwicklung
Herstellung monolithischer Säulen zur LC/MS/MS Analyse von Proteinen und Arzneistoffen
 Herstellung monolithischer Säulen zur LC/MS/MS Analyse von Proteinen und Arzneistoffen Jens Sproß Pharmazeutische Chemie und Bioanalytik Martin-Luther-Universität Halle-Wittenberg - und wie stellt man
Herstellung monolithischer Säulen zur LC/MS/MS Analyse von Proteinen und Arzneistoffen Jens Sproß Pharmazeutische Chemie und Bioanalytik Martin-Luther-Universität Halle-Wittenberg - und wie stellt man
Applikation. Bestimmung von Kohlenwasserstofftypen in Grundölen. Zusammenfassung. Einleitung
 Applikation Bestimmung von Kohlenwasserstofftypen in Grundölen Kategorie Matrix Methode Schlagwort Analyten ID Chemische Analyse Mineralöle Normalphasen-HPLC Qualitätskontrolle, industrielle Nebenprodukte,
Applikation Bestimmung von Kohlenwasserstofftypen in Grundölen Kategorie Matrix Methode Schlagwort Analyten ID Chemische Analyse Mineralöle Normalphasen-HPLC Qualitätskontrolle, industrielle Nebenprodukte,
Chromatographie Version 04/2008
 Chromatographie Version 04/2008 1. Erläutern Sie das Prinzip der Chromatographie. 2. In der Dünnschichtchromatographie kann man mit der sogenannten eindimensionalen Mehrfachentwicklung bzw. der zweidimensionalen
Chromatographie Version 04/2008 1. Erläutern Sie das Prinzip der Chromatographie. 2. In der Dünnschichtchromatographie kann man mit der sogenannten eindimensionalen Mehrfachentwicklung bzw. der zweidimensionalen
Elektrophorese. Sommersemester 2012
 Elektrophorese Sommersemester 2012 Gliederung 1. Was ist Elektrophorese? Allgemeine Informationen 1. Anwendung 2. Physikalische Grundlagen 3. Arten der Elektrophorese 1. Trägerelektrophorese 1. Grundlagen
Elektrophorese Sommersemester 2012 Gliederung 1. Was ist Elektrophorese? Allgemeine Informationen 1. Anwendung 2. Physikalische Grundlagen 3. Arten der Elektrophorese 1. Trägerelektrophorese 1. Grundlagen
Spritzenfilter - Spritzenvorsatzfilter - zertifiziert für die HPLC
 - TITAN2 Spritzenfilter sind in Bezug auf Leistung und Reproduzierbarkeit für die HPLC zertifiziert. Jedes einzelne Batch wird einer sehr strengen Qualitätskontrolle unterzogen. Mittels einer Standard-Testlösung
- TITAN2 Spritzenfilter sind in Bezug auf Leistung und Reproduzierbarkeit für die HPLC zertifiziert. Jedes einzelne Batch wird einer sehr strengen Qualitätskontrolle unterzogen. Mittels einer Standard-Testlösung
ÖAB Report. Monographie Sulfadimidin-Natrium. Betreff: A. Mayrhofer, 23.05.2013 ------------------------------------------------------
 BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report Betreff: Monographie Sulfadimidin-Natrium VORWORT Die Basis-Monographie Sulfadimidin ist in der Ph. Eur. enthalten und wurde kürzlich
BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report Betreff: Monographie Sulfadimidin-Natrium VORWORT Die Basis-Monographie Sulfadimidin ist in der Ph. Eur. enthalten und wurde kürzlich
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Tropfenkonturanalyse
 Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Arbeiten mit Membranproteinen. Rupert Abele
 Arbeiten mit Membranproteinen Rupert Abele Überblick Solubilisierung Reinigung Liposomenpräparation Rekonstitution Selbstorganisation von Detergenzien und Lipiden Detergenz Bildung von Mizellen (a) Phospholipiden
Arbeiten mit Membranproteinen Rupert Abele Überblick Solubilisierung Reinigung Liposomenpräparation Rekonstitution Selbstorganisation von Detergenzien und Lipiden Detergenz Bildung von Mizellen (a) Phospholipiden
Bedeutung von Hydrokolloiden bei der Herstellung und Stabilisierung von Emulsionen
 Bedeutung von Hydrokolloiden bei der Herstellung und Stabilisierung von Emulsionen G. Muschiolik Food Innovation Consultant, Potsdam www.muschiolik.de 1 Gliederung 1. Was ermöglichen Hydrokolloide (Proteine,
Bedeutung von Hydrokolloiden bei der Herstellung und Stabilisierung von Emulsionen G. Muschiolik Food Innovation Consultant, Potsdam www.muschiolik.de 1 Gliederung 1. Was ermöglichen Hydrokolloide (Proteine,
Vom Ei zum Proteinkristall. Reinigung und Kristallisation von Lysozym
 Vom Ei zum Proteinkristall Reinigung und Kristallisation von Lysozym Isolierung von Lysozym aus Hühnereiweiß (Protokoll adaptiert von www.biochemie.uni-jena.de/files/praktikum/lysozym.pdf) Einführung in
Vom Ei zum Proteinkristall Reinigung und Kristallisation von Lysozym Isolierung von Lysozym aus Hühnereiweiß (Protokoll adaptiert von www.biochemie.uni-jena.de/files/praktikum/lysozym.pdf) Einführung in
12. Schülerpraktikum 2014
 12. Schülerpraktikum 2014 Am 04., 05. und 06. März absolvierten ca. 50 Schüler aus den ostsächsichen Gymnasien das diesjährige BioAnalytik-Praktikum Ein besonderer Dank gilt den Organisatoren und Betreuern
12. Schülerpraktikum 2014 Am 04., 05. und 06. März absolvierten ca. 50 Schüler aus den ostsächsichen Gymnasien das diesjährige BioAnalytik-Praktikum Ein besonderer Dank gilt den Organisatoren und Betreuern
Protokoll zur Übung Gelelektrophorese
 Protokoll zur Übung Gelelektrophorese im Rahmen des Praktikums Labor an der TU Wien Durchgeführt bei Univ.Ass. Mag.rer.nat. Dr.rer.nat. Martina Marchetti-Deschmann Verfasser des Protokolls: Gwendolin Korinek
Protokoll zur Übung Gelelektrophorese im Rahmen des Praktikums Labor an der TU Wien Durchgeführt bei Univ.Ass. Mag.rer.nat. Dr.rer.nat. Martina Marchetti-Deschmann Verfasser des Protokolls: Gwendolin Korinek
Trennungsverfahren Techniken (in der Biologie)
 Trennungsverfahren Techniken (in der Biologie)? Biomoleküle können getrennt werden aufgrund ihrer - chemischen Eigenschaften: Ladung, Löslichkeit, Wechselwirkung mit spezifischen Reagenzen, Molmasse -
Trennungsverfahren Techniken (in der Biologie)? Biomoleküle können getrennt werden aufgrund ihrer - chemischen Eigenschaften: Ladung, Löslichkeit, Wechselwirkung mit spezifischen Reagenzen, Molmasse -
Proteinanalytik. Proteineigenschaften Proteinquellen Proteinisolierung Proteinnachweis Proteincharakterisierung
 PROTEINANALYTIK Proteinanalytik Proteineigenschaften Proteinquellen Proteinisolierung Proteinnachweis Proteincharakterisierung Aminosäuren Proteine Molekulare Eigenschaften Chemische Grundstruktur Größe
PROTEINANALYTIK Proteinanalytik Proteineigenschaften Proteinquellen Proteinisolierung Proteinnachweis Proteincharakterisierung Aminosäuren Proteine Molekulare Eigenschaften Chemische Grundstruktur Größe
Analyse trizyklischer Antidepressiva mit der Agilent Poroshell HPH C18- Säule
 Analyse trizyklischer Antidepressiva mit der Agilent HPH C18- Säule Application ote Small Molecule Pharmaceuticals Autor William Long Agilent Technologies, Inc. Einführung Trizyklische Antidepressiva wurden
Analyse trizyklischer Antidepressiva mit der Agilent HPH C18- Säule Application ote Small Molecule Pharmaceuticals Autor William Long Agilent Technologies, Inc. Einführung Trizyklische Antidepressiva wurden
Analytica. Die Top-Themen: Im Blickpunkt: Kundennähe. Neue Produkte. Aktuelle Nachrichten Ausgabe Frühjahr 2004 -TICKER. Referenz-Materialien
 Aktuelle Nachrichten Ausgabe Frühjahr 2004 -TICKER Im Blickpunkt: Kundennähe Neue Produkte Die kommende Analytica in München ist die ideale Plattform, neue und weiter entwickelte Produkte und Methoden
Aktuelle Nachrichten Ausgabe Frühjahr 2004 -TICKER Im Blickpunkt: Kundennähe Neue Produkte Die kommende Analytica in München ist die ideale Plattform, neue und weiter entwickelte Produkte und Methoden
Thermische Eigenschaften von Polymeren. Thermische Eigenschaften von Polymeren
 Thermische Eigenschaften von Polymeren Thermische Eigenschaften von Polymeren Vier wichtige Temperaturen/Temperaturintervalle charakterisieren teilkristalline Polymere: 1. Glastemperatur T g Beim Abkühlen
Thermische Eigenschaften von Polymeren Thermische Eigenschaften von Polymeren Vier wichtige Temperaturen/Temperaturintervalle charakterisieren teilkristalline Polymere: 1. Glastemperatur T g Beim Abkühlen
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers (4) Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Proteinreinigung Techniken & Methoden der Proteinreinigung
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers (4) Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Proteinreinigung Techniken & Methoden der Proteinreinigung
Peptid in Plasma: selektive und sensitive Analytik LC/MS-Diskussionstreffen, Wuppertal, 13.11.2007. Thomas Wirz, Roche Bioanalytik, Basel
 Peptid in Plasma: selektive und sensitive Analytik LC/MS-Diskussionstreffen, Wuppertal, 13.11.2007 Thomas Wirz, Roche Bioanalytik, Basel Ausgangslage: Synthetisches Peptid Molekulargewicht 3340 Da Dosis
Peptid in Plasma: selektive und sensitive Analytik LC/MS-Diskussionstreffen, Wuppertal, 13.11.2007 Thomas Wirz, Roche Bioanalytik, Basel Ausgangslage: Synthetisches Peptid Molekulargewicht 3340 Da Dosis
Identifizierung von Bindungspartnern der Acyl-Protein-Thioesterase 1 (APT 1) unter Verwendung eines anti-hapt 1 Antikörpers
 Präsentation zur Bachelorarbeit Identifizierung von Bindungspartnern der Acyl-Protein-Thioesterase 1 (APT 1) unter Verwendung eines anti-hapt 1 Antikörpers Michael Thomas Reinartz 28.3.2008 Übersicht Einführung
Präsentation zur Bachelorarbeit Identifizierung von Bindungspartnern der Acyl-Protein-Thioesterase 1 (APT 1) unter Verwendung eines anti-hapt 1 Antikörpers Michael Thomas Reinartz 28.3.2008 Übersicht Einführung
Bioanalytik von Arzneistoffen
 Bioanalytik von Arzneistoffen Seminar zum Praktikum Arzneimittelanalytik Agenda Gliederung!! Einführung!! Probenvorbereitung!! Analytische Verfahren!! spektroskopische Verfahren!! chromatographische Verfahren!!
Bioanalytik von Arzneistoffen Seminar zum Praktikum Arzneimittelanalytik Agenda Gliederung!! Einführung!! Probenvorbereitung!! Analytische Verfahren!! spektroskopische Verfahren!! chromatographische Verfahren!!
Quantitative Analytik -231- Elektrophorese. Bei dieser Gruppe von Methoden werden Ionen durch Anlegen eines elektrischen Feldes transportiert.
 Quantitative Analytik -231- Elektrophorese 9. ELEKTROPHORESE Bei dieser Gruppe von Methoden werden Ionen durch Anlegen eines elektrischen Feldes transportiert. Elektrophoretische Mobilität von Ionen in
Quantitative Analytik -231- Elektrophorese 9. ELEKTROPHORESE Bei dieser Gruppe von Methoden werden Ionen durch Anlegen eines elektrischen Feldes transportiert. Elektrophoretische Mobilität von Ionen in
Proteinbestimmung. Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der Proteinbestimmung mit den folgenden Lehrzielen:
 Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Chemisches Grundpraktikum für Ingenieure. 2. Praktikumstag. Andreas Rammo
 Chemisches Grundpraktikum für Ingenieure. Praktikumstag Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Das chemische Gleichgewicht Säure-Base-Reaktionen
Chemisches Grundpraktikum für Ingenieure. Praktikumstag Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Das chemische Gleichgewicht Säure-Base-Reaktionen
Reinigung rekombinant hergestellter Proteine
 Reinigung rekombinant hergestellter Proteine Dipl.-Biochem. Cord Hartmann / Dr. Benjamin Dälken Georg-Speyer-Haus Methodenseminar BCII-Praktikum 19. Januar 2009 / 9. Februar 2009 Reinigung rekombinant
Reinigung rekombinant hergestellter Proteine Dipl.-Biochem. Cord Hartmann / Dr. Benjamin Dälken Georg-Speyer-Haus Methodenseminar BCII-Praktikum 19. Januar 2009 / 9. Februar 2009 Reinigung rekombinant
Biochemisches Grundpraktikum
 Biochemisches Grundpraktikum Versuch Nummer G-06 06: Affinitätschromatographie und Charakterisierung von Immunglo- bulinen Gliederung: I. Das Immunsystem... 2 a) Einleitung... 2 b) Humorale Abwehr... 2
Biochemisches Grundpraktikum Versuch Nummer G-06 06: Affinitätschromatographie und Charakterisierung von Immunglo- bulinen Gliederung: I. Das Immunsystem... 2 a) Einleitung... 2 b) Humorale Abwehr... 2
Bestimmung des Paracetamolgehalts in Vivimed von Natalie Rotermel und Katharina Juhasz-Dora
 Bestimmung des Paracetamolgehalts in Vivimed von Natalie Rotermel und Katharina Juhasz-Dora Inhalt 1. Allgemeine Information zu den Chemikalien und den Bestandteilen einer Vivimed Tablette (Name, Wirkungsweise,
Bestimmung des Paracetamolgehalts in Vivimed von Natalie Rotermel und Katharina Juhasz-Dora Inhalt 1. Allgemeine Information zu den Chemikalien und den Bestandteilen einer Vivimed Tablette (Name, Wirkungsweise,
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 1
 Vom Molekül zur Zelle Block 3 Seminar / Praktikum 1 Diese Präsentation befindet sich auf der Homepage: http://www.meduniwien.ac.at/hp/medizinische-genetik/studium-lehre/seminare/ Helmut Dolznig, Ass. Prof.
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 1 Diese Präsentation befindet sich auf der Homepage: http://www.meduniwien.ac.at/hp/medizinische-genetik/studium-lehre/seminare/ Helmut Dolznig, Ass. Prof.
Dünnschichtchromatographie. - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie
 Dünnschichtchromatographie - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie Dünnschichtchromatographie (DC) Trennmethode mit vielen Vorteilen gegenüber klassischen Verfahren (Destillation,
Dünnschichtchromatographie - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie Dünnschichtchromatographie (DC) Trennmethode mit vielen Vorteilen gegenüber klassischen Verfahren (Destillation,
SDS-Polyacrylamidgelelektrophorese von Insulin
 Insulin ist ein Hormon der Bauchspeicheldrüse (Pankreas), das bei Wirbeltieren den Transport von Glukose aus dem Blut in die Körperzellen reguliert. Bei einem Ausfall (z.b. durch Autoimmunzerstörung der
Insulin ist ein Hormon der Bauchspeicheldrüse (Pankreas), das bei Wirbeltieren den Transport von Glukose aus dem Blut in die Körperzellen reguliert. Bei einem Ausfall (z.b. durch Autoimmunzerstörung der
Prüfungsfragenkatalog für Methoden der Chromatographie (Prof. Werner Seebacher)
 Prüfungsfragenkatalog für Methoden der Chromatographie (Prof. Werner Seebacher) Stand: Mai 2015 Termin: 28.05.2015 1. Zeigen Sie anhand einer einfachen Strukturformel einer Aminosäure wie sie im basischen,
Prüfungsfragenkatalog für Methoden der Chromatographie (Prof. Werner Seebacher) Stand: Mai 2015 Termin: 28.05.2015 1. Zeigen Sie anhand einer einfachen Strukturformel einer Aminosäure wie sie im basischen,
Western Blot. Zuerst wird ein Proteingemisch mit Hilfe einer Gel-Elektrophorese aufgetrennt.
 Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Schwermetalle Ph.Eur. 2.4.8 max. 20 ppm Methode F. Trocknungsverlust Ph.Eur. 2.2.32 max. 3,0% 80 C; 2 h. Sulfatasche Ph.Eur. 2.4.14 max.
 PRODUKT Dok.-Nr. S-3735-D Rev. 5 Seite 1/7 RETALAC DEFINITION: RetaLac ist ein co-processed Sprühagglomerat hergestellt aus 50 Teilen Lactose- Monohydrat (Ph.Eur./USP-NF/JP) und 50 Teilen Hypromellose
PRODUKT Dok.-Nr. S-3735-D Rev. 5 Seite 1/7 RETALAC DEFINITION: RetaLac ist ein co-processed Sprühagglomerat hergestellt aus 50 Teilen Lactose- Monohydrat (Ph.Eur./USP-NF/JP) und 50 Teilen Hypromellose
VDSpher. Erhöhte Druckstabilität garantiert: HPLC. UHPLC. LC-MS. HILIC. n präziseste Analyseergebnisse. n maximale Anwendungsdauer
 VDSpher Hochleistungs- Trennphasen HPLC. UHPLC. LC-MS. HILIC Erhöhte Druckstabilität garantiert: n präziseste Analyseergebnisse n maximale Anwendungsdauer n kürzeste Analysezeiten Hier trennt sich, was
VDSpher Hochleistungs- Trennphasen HPLC. UHPLC. LC-MS. HILIC Erhöhte Druckstabilität garantiert: n präziseste Analyseergebnisse n maximale Anwendungsdauer n kürzeste Analysezeiten Hier trennt sich, was
Versuch: Denaturierung von Eiweiß
 Philipps-Universität Marburg 29.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Denaturierung
Philipps-Universität Marburg 29.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Denaturierung
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen. Formaldehyd-Fixierung
 Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu
Biochemisches Grundpraktikum
 Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
ANALYTISCHE CHEMIE I Trennmethoden 2. Hochleistungsflüssigchromatographie (HPLC) WS 2007/2008
 ANALYTISCHE CHEMIE I Trennmethoden 2. Hochleistungsflüssigchromatographie (HPLC) WS 2007/2008 HPLC HPLC = hochauflösende Flüssigkeitschromatographie = high performance liquid chromatography Die HPLC ist
ANALYTISCHE CHEMIE I Trennmethoden 2. Hochleistungsflüssigchromatographie (HPLC) WS 2007/2008 HPLC HPLC = hochauflösende Flüssigkeitschromatographie = high performance liquid chromatography Die HPLC ist
Dissoziation, ph-wert und Puffer
 Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Agilent 1290 Infinity LC mit Intelligent System Emulation Technology. Infinitely better method transfer
 Agilent 129 Infinity LC mit Intelligent System Emulation Technology Infinitely better method transfer 129 Agilent 129 Infinity LC mit ISET Besserer Methodentransfer denn je. Nutzen Sie Methoden, die auf
Agilent 129 Infinity LC mit Intelligent System Emulation Technology Infinitely better method transfer 129 Agilent 129 Infinity LC mit ISET Besserer Methodentransfer denn je. Nutzen Sie Methoden, die auf
Referat : Aufbau v. Proteinen u. ihre Raumstruktur
 Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Johannes Gutenberg-Universität Mainz Fachbereich Biologie, Institut für Zoologie Leitung: Prof. Dr. Wolfrum Datum: 15. April 2005
 Johannes Gutenberg-Universität Mainz Fachbereich Biologie, Institut für Zoologie Leitung: Prof. Dr. Wolfrum Datum: 15. April 2005 F1 Molekulare Zoologie Teil II: Expressionsanalyse Proteinexpressionsanalyse
Johannes Gutenberg-Universität Mainz Fachbereich Biologie, Institut für Zoologie Leitung: Prof. Dr. Wolfrum Datum: 15. April 2005 F1 Molekulare Zoologie Teil II: Expressionsanalyse Proteinexpressionsanalyse
Elektrophorese. Zentrum für Mikro- und Nanotechnologien http://www.tu-ilmenau.de/nano
 Elektrophorese Die SDS- Polyacrylamidgelelektrophorese ist eine schnelle und empfindliche Methode, die zudem eine hohe Auflösung erlaubt. Schon 1 μg (2 pmol) eines Proteins ergeben eine erkennbare Bande.
Elektrophorese Die SDS- Polyacrylamidgelelektrophorese ist eine schnelle und empfindliche Methode, die zudem eine hohe Auflösung erlaubt. Schon 1 μg (2 pmol) eines Proteins ergeben eine erkennbare Bande.
nfoexpo 2011 10. November 2011: Zürich ConventionPoint - A Service of SIX Group Seminar Programm
 09:00-09:10 Begrüssung 09:15-09:45 TLC-MS als effektives Hilfsmittel im Syntheselabor Dr. Heinrich Luftmann, Organisch-Chemisches Institut der Universität Münster (Deutschland) 09:50-10:15 Die Bedeutung
09:00-09:10 Begrüssung 09:15-09:45 TLC-MS als effektives Hilfsmittel im Syntheselabor Dr. Heinrich Luftmann, Organisch-Chemisches Institut der Universität Münster (Deutschland) 09:50-10:15 Die Bedeutung
Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis o- Toluidin positiv, Glu-Oxidase-Peroxidase neg? Begründung!
 TEST1 Schreiben sie 2 saure Aminosäuren an! Was sind essentielle As geben sie 3 Beispiele an! Was versteht man unter Glykopyranose? Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis
TEST1 Schreiben sie 2 saure Aminosäuren an! Was sind essentielle As geben sie 3 Beispiele an! Was versteht man unter Glykopyranose? Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis
Ein modernes Analyselabor kann heute nicht mehr ohne chromatographische Analysetechniken
 g g g Chromatographie für alle In diesem Kapitel Was versteht man unter Chromatographie? In welche Gebiete teilt sich die Chromatographie auf? Was sind mobile und stationäre Phasen? 1 Ein modernes Analyselabor
g g g Chromatographie für alle In diesem Kapitel Was versteht man unter Chromatographie? In welche Gebiete teilt sich die Chromatographie auf? Was sind mobile und stationäre Phasen? 1 Ein modernes Analyselabor
Einzelmolekülfluoreszenzspektroskopie (EFS)
 Fortgeschrittenen Praktikum TU Dresden 29. Mai 2009 Einzelmolekülfluoreszenzspektroskopie (EFS) Klaus Steiniger, Alexander Wagner, Gruppe 850 klaus.steiniger@physik.tu-dresden.de, alexander.wagner@physik.tu-dresden.de
Fortgeschrittenen Praktikum TU Dresden 29. Mai 2009 Einzelmolekülfluoreszenzspektroskopie (EFS) Klaus Steiniger, Alexander Wagner, Gruppe 850 klaus.steiniger@physik.tu-dresden.de, alexander.wagner@physik.tu-dresden.de
F-I Molekulare Zoologie: Teil II: Expressionsanalysen. Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse
 F-I Molekulare Zoologie: Teil II: Expressionsanalysen Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse Inhalt: Seite I. Allgemeines 1 II. Durchführung der Elektrophorese
F-I Molekulare Zoologie: Teil II: Expressionsanalysen Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse Inhalt: Seite I. Allgemeines 1 II. Durchführung der Elektrophorese
Lösungsblatt zu Aufbau von Aminosäuren
 Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
AZURA Analytical HPLC. 2 Welche HPLC-Aufgaben meistern Sie heute?
 AZURA Analytical HPLC 2 Welche HPLC-Aufgaben meistern Sie heute? AZURA Analytical HPLC Flexibel und individuell anpassbar Autosampler mit Injektionsvolumen von 0,1 5000 µl Die neue AZURA Analytical HPLC
AZURA Analytical HPLC 2 Welche HPLC-Aufgaben meistern Sie heute? AZURA Analytical HPLC Flexibel und individuell anpassbar Autosampler mit Injektionsvolumen von 0,1 5000 µl Die neue AZURA Analytical HPLC
Hinweise zu den Prüfungen B17: März 2013
 Hinweise zu den Prüfungen B17: März 2013 Bestimmung von Art und Konzentration phenolischer und phosphitischer Antioxidantien in Dichtungsbahnen aus Polyethylen hoher Dichte (PEHD) herausgegeben vom Fachbereich
Hinweise zu den Prüfungen B17: März 2013 Bestimmung von Art und Konzentration phenolischer und phosphitischer Antioxidantien in Dichtungsbahnen aus Polyethylen hoher Dichte (PEHD) herausgegeben vom Fachbereich
Protokoll: Hochdruck-Flüssigkeits-Chromatographie (HPLC)
 Protokoll: Hochdruck-Flüssigkeits-Chromatographie (HPLC) Zielstellung: - Bestimmung der Retentionszeiten von Theobromin, Theophyllin und Coffein! - Ermittlung des Coffeingehalts verschiedener ahrungs-
Protokoll: Hochdruck-Flüssigkeits-Chromatographie (HPLC) Zielstellung: - Bestimmung der Retentionszeiten von Theobromin, Theophyllin und Coffein! - Ermittlung des Coffeingehalts verschiedener ahrungs-
4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd30-igg1-tnf- Fusionsproteins
 ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
SERVA IDA LD Agarose
 GEBRAUCHSANLEITUNG SERVA IDA LD Agarose Agarose zur Affinitätsreinigung von His-Tag-Fusionsproteinen (Kat.-Nr. 42144, 42145, 42146, 42147) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA IDA LD Agarose Agarose zur Affinitätsreinigung von His-Tag-Fusionsproteinen (Kat.-Nr. 42144, 42145, 42146, 42147) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach
 Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Fructose besitzt 5 Kohlenstoffatome. FALSCH, Fructose besitzt
Übungsklausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Fructose besitzt 5 Kohlenstoffatome. FALSCH, Fructose besitzt
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte)
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte) Lösungen, Konzentration Viele chemische Reaktionen werden
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte) Lösungen, Konzentration Viele chemische Reaktionen werden
Inhaltsverzeichnis. Geleitwort 5. Vorwort 7. 1 Einführung 19 1.1 Wissen ist gefragt 24
 Inhaltsverzeichnis «Geleitwort 5 Vorwort 7 1 Einführung 19 1.1 Wissen ist gefragt 24 2 Die Chromatographie und ihre Techniken 27 2.1 Historie 27 2.1.1 Der Weg bis heute 30 2.2 Prinzip 31 2.2.1 Einteilung
Inhaltsverzeichnis «Geleitwort 5 Vorwort 7 1 Einführung 19 1.1 Wissen ist gefragt 24 2 Die Chromatographie und ihre Techniken 27 2.1 Historie 27 2.1.1 Der Weg bis heute 30 2.2 Prinzip 31 2.2.1 Einteilung
Baldriantinktur, etherische Valerianae tinctura aetherea
 Baldriantinktur, etherische Valerianae tinctura aetherea ÖAB 2009/048 Definition Baldriantinktur, etherische, wird aus Etheralkohol (Ether + Ethanol: 1 + 3 V/V) und Baldrianwurzel (Valerianae radix) hergestellt.
Baldriantinktur, etherische Valerianae tinctura aetherea ÖAB 2009/048 Definition Baldriantinktur, etherische, wird aus Etheralkohol (Ether + Ethanol: 1 + 3 V/V) und Baldrianwurzel (Valerianae radix) hergestellt.
Löslichkeitsverhalten von Proteinen und Proteinbestimmung
 Löslichkeitsverhalten von Proteinen und Proteinbestimmung Proteine haben eine Primär-, Sekundär- und Tertiärstruktur. Die intakte Sekundär- und Tertiärstruktur ist verantwortlich für das Lösungsverhalten.
Löslichkeitsverhalten von Proteinen und Proteinbestimmung Proteine haben eine Primär-, Sekundär- und Tertiärstruktur. Die intakte Sekundär- und Tertiärstruktur ist verantwortlich für das Lösungsverhalten.
Proteinen. Zelle hergestellt, so sagt man, das entsprechende Gen werde exprimiert. Unterscheidung nach Form. Unterscheidung nach Funktion
 Proteine Die von den Peptiden bekannte Polykondensation der Aminosäuren ermöglicht die Bildung von Molekülen mit mehr als 10000 Aminosäuren. Enthält ein solches Makromolekül mehr als 100 (je nach Literaturquelle
Proteine Die von den Peptiden bekannte Polykondensation der Aminosäuren ermöglicht die Bildung von Molekülen mit mehr als 10000 Aminosäuren. Enthält ein solches Makromolekül mehr als 100 (je nach Literaturquelle
Bradford Reagent, 5x
 GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie
 HPLC 1 Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie 1. Aufgabe In diesem Versuch werden die Retentionszeiten der Substanzen Acetylsalicylsäure (ASS)
HPLC 1 Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie 1. Aufgabe In diesem Versuch werden die Retentionszeiten der Substanzen Acetylsalicylsäure (ASS)
ANALYTISCHE CHEMIE I Trennmethoden 6. Elektrophorese-Methoden Kapillarelektrophorese / Gelelektrophorese WS 2007/2008
 ANALYTISCHE CHEMIE I Trennmethoden 6. Elektrophorese-Methoden Kapillarelektrophorese / Gelelektrophorese WS 2007/2008 Definition Elektrophorese bezeichnet die Wanderung elektrisch geladener Teilchen durch
ANALYTISCHE CHEMIE I Trennmethoden 6. Elektrophorese-Methoden Kapillarelektrophorese / Gelelektrophorese WS 2007/2008 Definition Elektrophorese bezeichnet die Wanderung elektrisch geladener Teilchen durch
Titration einer Säure mit einer Base
 Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
Präparative HPLC-Säulen
 Preisübersicht 2015/16 Präparative HPLC- Eurospher II für semipräparative und präparative HPLC Axial komprimierbare hardware -> Langlebigkeit Unterschiedlichste Modifikationen verfügbar -> Flexibilität
Preisübersicht 2015/16 Präparative HPLC- Eurospher II für semipräparative und präparative HPLC Axial komprimierbare hardware -> Langlebigkeit Unterschiedlichste Modifikationen verfügbar -> Flexibilität
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Western-Analyse Protein-Elektrophorese ELISA Protein-Chip
 Western-Analyse Protein-Elektrophorese ELISA Protein-Chip DNA-RNA RNA-Protein Die Struktur der DNA Ebene der Proteinstruktur Die Gruppen der Aminosäuren Darstellung Räumliche R Proteinstrukturen (Röntgen
Western-Analyse Protein-Elektrophorese ELISA Protein-Chip DNA-RNA RNA-Protein Die Struktur der DNA Ebene der Proteinstruktur Die Gruppen der Aminosäuren Darstellung Räumliche R Proteinstrukturen (Röntgen
Immunologische Methoden und Enzymassays
 Immunologische Methoden und Enzymassays 1. Antikörper (Ak) Aufbau, Struktur monoklonale und polyklonale Ak 2. Immunpräzipitation 3. Affinitätschromatographie 4. Immundetektion 5. Immunblot 6. Immunhistochemie
Immunologische Methoden und Enzymassays 1. Antikörper (Ak) Aufbau, Struktur monoklonale und polyklonale Ak 2. Immunpräzipitation 3. Affinitätschromatographie 4. Immundetektion 5. Immunblot 6. Immunhistochemie
GPC/SEC Wir bringen s voran. Referenzmaterialien und LC-Säulen
 GPC/SEC Wir bringen s voran Referenzmaterialien und LC-Säulen PSS im Kurzporträt GPC/SEC - Wir bringen s voran PSS Polymer Standards Service GmbH wurde 1985 als Spin-Off Unternehmen der Universität Mainz
GPC/SEC Wir bringen s voran Referenzmaterialien und LC-Säulen PSS im Kurzporträt GPC/SEC - Wir bringen s voran PSS Polymer Standards Service GmbH wurde 1985 als Spin-Off Unternehmen der Universität Mainz
Erreichen Sie die neue Dimension in der präparativen HPLC
 Erreichen Sie die neue Dimension in der präparativen HPL... we Meet your Needs MHEREY-NGEL NULEODUR HTec Hauptmerkmale zuverlässige und langlebige Standard-RP-Phase für das Up-Scaling auf den präparativen
Erreichen Sie die neue Dimension in der präparativen HPL... we Meet your Needs MHEREY-NGEL NULEODUR HTec Hauptmerkmale zuverlässige und langlebige Standard-RP-Phase für das Up-Scaling auf den präparativen
Probenvorbereitung VARIAN, INC. Captiva ND Lipids DIE FILTRATIONSPLATTE ZUR ENTFERNUNG VON LIPIDEN UND PROTEINEN. www.varianinc.
 Probenvorbereitung VARIAN, INC. Captiva ND Lipids DIE FILTRATIONSPLATTE ZUR ENTFERNUNG VON LIPIDEN UND PROTEINEN www.varianinc.com VARIAN, INC. Bessere Analytik durch Entfernen von Phospholipiden Einleitung
Probenvorbereitung VARIAN, INC. Captiva ND Lipids DIE FILTRATIONSPLATTE ZUR ENTFERNUNG VON LIPIDEN UND PROTEINEN www.varianinc.com VARIAN, INC. Bessere Analytik durch Entfernen von Phospholipiden Einleitung
ANALYTISCHE CHEMIE I. Trennmethoden. 1. Grundlagen Chromatographie WS 2004/2005
 ANALYTISCHE CHEMIE I Trennmethoden 1. Grundlagen Chromatographie WS 2004/2005 Michael Przybylski Chromatographie Stoffgemisch Mobile Phase Stationäre Phase Unterschiedliche Adsorption Unterschiedliche
ANALYTISCHE CHEMIE I Trennmethoden 1. Grundlagen Chromatographie WS 2004/2005 Michael Przybylski Chromatographie Stoffgemisch Mobile Phase Stationäre Phase Unterschiedliche Adsorption Unterschiedliche
