Tumoren des Zentralnervensystems. Häufigste histologische Typen / Lokalisation CBTRUS
|
|
|
- Irmgard Fiedler
- vor 6 Jahren
- Abrufe
Transkript
1 Tumoren des Zentralnervensystems Häufigste histologische Typen / Lokalisation CBTRUS Intraaxial Kurs ZNS I Gliome (astroz./olig.) 33.6% Ependymome 2.1% Medulloblastome 1.5% Hämangioblastome 0.8% ZNS Lymphome 2.8% Extraaxial Kurs ZNS II Meningeome 32.1 % Hypophysenadenome 8.4% Kraniopharyngeome 0.7% Neurinome (Vestibularis) 4% Chordome / Dermoide 0.1%
2 Maligne Gliome Histologischer Grad / Überleben WHO II Oligodendrogliom Astrocytom Oligo-Astrozytom WHO III (anapl.) Oligodendrogliom Astrocytom Oligo-Astrozytom WHO IV Glioblastom Medianes ÜL 12 Mon. bis 12 Jahre 3 bis 5 Jahre 10 bis 15 Mon.
3 Maligne Gliome Gesichtsmaske und Lasersystem : präzise und reproduzierbare Bestrahlung
4 Maligne Gliome Bestrahlung der Tumorregion / moderne Technologien ventro-cranial Tisch 270 Gantry 327 Individueller Block Einfallender Strahl 2- Felder Technik non- coplanar Dosisverteilung links-lateral Tisch 0 Gantry 90 Individueller Block
5 Maligne Gliome Intensitätsmodulierte Radiotherapie (Reduktion der integralen Dosis außerhalb des Zielgebietes?) Hermanto et al., 2007
6 Niedriggradige Gliome Entscheidungskriterien Derzeitige Fragestellungen Zeitpunkt der Bestrahlung Dosis-Wirkungsbeziehungen Risikofaktoren Stellenwert der Chemotherapie Stratifikation nach molekulargenetischen Profilen?
7 Niedriggradige Gliome / Radiotherapie EORTC / RT versus wait and see Progression- free survival / up-date 2005 Van den Bent et al., 2005
8 Niedriggradige Gliome / Radiotherapie EORTC / RT versus wait and see Overall survival / up-date 2005 Van den Bent et al., 2005
9 Prozent progressionsfrei Niedriggradige Gliome / Radiotherapie Multizentrische Studien RTOG - Studie 9110 Dosis Wirkungsbeziehungen / Zeit zur Progression Jahre PFS : 55% Therapiezweig 50.4 Gy, n = Gy, n = Jahre PFS : 52% Jahre nach Randomisation Shaw et al., 2002
10 Prozent Nekrose Niedriggradige Gliome / Radiotherapie Multizentrische Studien RTOG - Studie 9110 Komplikationsrisiko : Nekrosebildungen Therapiezweig 50.4 Gy, n = Gy, n = 102 Nach 2 Jahren : 6% Nach 5 Jahren : 10% Nach 2 Jahren : 1% Nach 5 Jahren : 2% Jahre nach Randomisation Shaw et al., 2002
11 Niedriggradige Gliome / Radiotherapie Ansprechraten auf Radiotherapie 21 Patienten : MR Kontrollen und Evaluation neurologischer Defizite nach Bestrahlung Symptomkontrolle : 16 von 21 Patienten (76%) Mediane Zeit bis zum maximalen Ansprechen : 2,8 Monate (1,5-11 Monate) 5-Jahre progr.-freies ÜL : 43% Bauman et al., 1999
12 Niedriggradige Gliome / Radiotherapie Protonentherapie 7 Patienten 68.2 CGE (cobalt Gray equivalent) 5 x CGE 5 Jahre Überlebensrate : 71 % Dose escalation with conv. fractionation failed to improve outcome Fitzek et al., 2001
13 Niedriggradige Gliome / Radiotherapie Spätfolgen / Dosisverschreibung und Bestrahlungstechnik Moderne Techniken und moderate Dosisapplikationen RT bedingte Defizite Taphoorn, Pat. keine Defizite Vigliani, Pat. keine Defizite Lilja, Pat. keine Defizite Frühere Techniken und hohe Dosisapplikationen RT bedingte Defizite Kiebert, ,4 Gy Defizite Olson, 2000 bis 65 Gy Defizite Surma-aho, 2001 WB-RT, 60 Gy Defizite
14 Niedriggradige Gliome / Radiotherapie Therapieentscheidungen Resezierbar Nicht resezierbar Vollständig Partiell Biopsie Alter > 65 ; KI < 60?? Keine RT Risikoprofil! Postop. RT verlängert progr.-fr. ÜL Prim. RT verlängert ÜL* Keine RT * Med. ÜL 9.8 Jahre bei 35 Pat. Biopsie / RT wegen Progression Lunsford et al., 1995
15 Niedriggradige Gliome / Radiotherapie RTOG : Prospective studies in adult LGG Zwei Studien : Niedrig Risiko (Phase II) < 40 Jahre und komplette Resektion Observation = Arm 1 Hoch Risiko (Phase III) > / = 40 Jahre oder Teilresektion / Biopsie Arm 2 : alleinige RT (54 Gy / 5 x 1.8 Gy) versus Shaw, ASCO, 2005 Arm 3 : 6 x PCV (alle 8 Wo.) nach RT (54 Gy / 5 x 1.8 Gy)
16 Prozent überlebend ohne Progression Niedriggradige Gliome / Radiotherapie 100 RTOG : Prospective studies in adult LGG Risikogruppen : Progressionsfreies ÜL Progredient 5 Jahre PFÜL Arm 1 (Observ.) 49/11 48% p = n.s Arm 2 (RT) 70/126 42% Arm 3 (RT / PCV) 46/125 60% P = Jahre nach Registrierung Shaw, ASCO, 2005
17 Niedriggradige Gliome / Radiotherapie RTOG : Prospective studies in adult LGG Risikofaktoren Arm 1 (Observ.) : Progressionsfreies ÜL Gruppe Progression Log Rank p-wert Alle Patienten 44% Präop. Tumorgröße < 4 cm >/= 4 cm Histologie Oligodendrogliom Astrocytom Bildgebung / Resttumor < 1 cm 1 2 cm > 2 cm 27% 63% 32% 54% 16% 67% 89% < 0.05 Shaw, ASCO, 2005
18 Prozent überlebend ohne Progression Niedriggradige Gliome / Radiotherapie 100 RTOG : Prospective studies in adult LGG Progressionsfreies ÜL / up-date Progredient 5 Jahre PFÜL Arm 2 (RT) 74/126 46% Arm 3 (RT / PCV) 46/125 63% Shaw, ASCO, 2008 p = Jahre nach Registrierung
19 Prozent überlebend Niedriggradige Gliome / Radiotherapie 100 RTOG : Prospective studies in adult LGG Risikogruppen : Gesamtüberleben Verstorben 5 Jahre ÜL Arm 1 (Observ.) 8/11 93% Arm 2 (RT) 44/126 67% Arm 3 (RT / PCV) 32/125 67% p = < Jahre nach Registrierung Shaw, ASCO, 2005
20 Prozent überlebend Niedriggradige Gliome / Radiotherapie 100 RTOG : Prospective studies in adult LGG Gesamtüberleben / up-date Verstorben 5 Jahre ÜL Arm 2 (RT) 51/126 63% Arm 3 (RT / PCV) 37/125 72% Shaw, ASCO, 2008 p = Jahre nach Registrierung
21 Niedriggradige Gliome / Radiotherapie Arm 2 Alleinige RT RTOG : Prospective studies in adult LGG Toxizitätsprofile : alleinige RT versus RT + PVC Arm 3 RT + PVC Grad 3 Grad 4 Grad 3 Grad 4 7% 2% 53% 14% Rezidivtherapie Arm 1 Beobachtung n = 49 Arm 2 Alleinige RT n = 62 Operation 47% 26% 30% Radiotherapie 63% 21% 13% Chemotherapie 43% 66% 53% Arm 3 RT + PVC n = 40 Shaw, ASCO, 2005
22 Prozent Niedriggradige Gliome / Radiotherapie Multizentrische Studien NCCTG : Diagnostic and prognostic significance of 1p and 19q deletions in patients (pts) with low-grade oligo.-glioma and astrocytoma. Treatment : 50.4 Gy vs 64.8 Gy RTOG 9110, and NCCTG (RT+Chx) n = 62 n = 38 1p & 19q Verlust Kein Verlust Ansprechen auf RT (+Chx.) Jahre progr.-fr. ÜL 80% 47% p = 0.25 (logrank) Jahre Buckner et al., ASCO 2005
23 % Gesamtüberleben Niedriggradige Gliome / Radiotherapie Wirkung der Chemotherapie / neoadjuvant Temozolomide 1.0 Molekulargenet. Profil / Verlust 1p / 19q Gesamt ÜL - Prognostischer Faktor 0.8 1p / 19q Verlust n = 36 Patienten Kein 1p / 19q Verlust n = 50 Patienten p = Monate Kaloshi et al., 2007
24 Progr-freies Überleben Niedriggradige Gliome / Radiotherapie Natürlicher Verlauf / keine RT / Chx Einfluß 1p/19q Deletion auf progress.-fr. ÜL / Gliom Netzwerk n=76 Oligodendr. II 33 Oligo-Astr. II 30 Oligodendr. III 6 Oligo-Astr. III 5 Jahre Weller et al., 2007
25 Niedriggradige Gliome / Radiotherapie Histologie MR Ablauf Prüfung der Einschluß kriterien Registrierung Genetischer Test QoL Neuropsych Test (ausgew. Zentren) Temozolomide Randomisation Radiotherapie
26 Niedriggradige Gliome / Radiotherapie Randomisierung Randomisiert : 458 Patienten (Registrierung geschlossen ) Stand : Aktivierung : 12. Juli 2005
27 Niedriggradige Gliome / Radiotherapie Fazit / Ausblick Klinische prognostische Faktoren Therapieentscheidung / Zeitpunkt der Therapie Radiotherapie bei Progression oder Hoch-Risiko-Profil Molekulargenetische prognostische Faktoren 1p und 19q Verlust (MGMT Expression?) Auswahl der Therapiemodalitäten Stratifizierung nach Therapiebedarf / -profit Dosisfindung / Radiotherapie 50,4 54 Gy (5 x Gy) lokale RT Chemotherapie Stellenwert / Risikoprofile (progn. Faktoren, molek.- Muster) Auswahl der Protokolle (PFS und OS Vorteil / RTOG?) Endpunkt : Lebensqualität / neurokog. Leistung Integrierung in Studien (EORTC)
28 Hochmaligne Gliome / Radiotherapie Hochaggressive Tumoren Medianes Überleben ca 9-12 Monate Kurative oder palliative Therapie? Intensität der Therapie Nebenwirkungen Lebensqualität
29 Hochmaligne Gliome / Radiotherapie Resektionsausmass / 5 - Aminolaevulinsäurestudie Stummer et al., 2008
30 Hochmaligne Gliome / Radiotherapie Ziel der Radiotherapie Verbesserung der lokalen Tumorkontrolle Nutzung moderner RT - Techniken
31 Hochmaligne Gliome / Radiotherapie Rückfallmuster nach lokaler Bestrahlung Hess et al., 1993 Chan et al., 2002 Technik 2D konventionell 3D konformal (2 cm Sich.-saum) ( cm - Eskalation -) Dosis 60 Gy / 30 fr. 90 Gy / 45 Fr. Rate 58/66 23/34 Lokal 86% 91% Rand 9% 9% Ausserh. 5% 0%
32 Hochmaligne Gliome / Radiotherapie Glioblastom / Dosis-Wirkungsbeziehungen Studie / Autor Pat.-Zahl Gesamtdosis Medianes Überleben Signifikanz Walker et al., keine </= 45 Gy 50 Gy 55 Gy 60 Gy 18,0 Wo. 13,5 Wo. 28,0 Wo. 36,0 Wo. 42,0 Wo. niedrige Dosis : p= Gy <-> 60 Gy p=0.004 MRC, Gy 60 Gy 9 Mon. 12 Mon. p=0.007 Nelson et al., 1988 (RTOG 7401 / ECOG 1374) Gy (Ganzhirn) 60 Gy (Ganzhirn) +10 Gy Boost 9,3 Mon. 8,2 Mon.
33 Hochmaligne Gliome / Radiotherapie Glioblastom / Dosis-Wirkungsbeziehungen / hfx Autor / Studie Pat.- Zahl Gesamtdosis / Fraktionierung Medianes Überleben Signifikanz Fulton et al, ,4 Gy 71,2 Gy 80.0 Gy (3 x 0,89 Gy / Tag) 46 Wo. 38 Wo. 45 Wo. n.s Werner-Wasik et al., 1996 (RTOG 8302) (RT+ BCNU) ,8 Gy 72,0 Gy 76,8 Gy 81,6 Gy (2 x 1,2 Gy / Tag) 11,4 Mo. 12,7 Mo. 12,0 Mo. 11,7 Mo. n.s.
34 Hochmaligne Gliome / Radiotherapie Glioblastom / Dosis-Wirkungsbeziehungen / hfx mit Akzel. Autor / Studie Pat.-Zahl Gesamtdosis Frakt. Medianes Überleben Signif. Werner-Wasik et al, 1996 (RTOG 8302) Gy (BCNU) 2 x 1,6 Gy /Tag 54,4 Gy (BCNU) 2 x 1,6 Gy /Tag 11,9 Mon 10,8 Mon. n.s Gonzalez - Gonzalez, 1994 (EORTC) Gy 48 Gy 54 Gy 60 Gy (3 x 2Gy/Tag) 8,3 Mon. 8,1 Mon. 10,3 Mon. 7,2 Mon. n.s
35 Hochmaligne Gliome / Radiotherapie Dosiseskalation Patienten : 34 Pat / hochmaligne Gliome (33 Glioblastome, 1 anapl. Gliom) Medianes Alter : 55 Jahre Technik : 3 D konformal Dosisverschreibung : PTV 1 : (sichtb. Tumor + 0.5cm) : 90+/- 5 Gy PTV 2 : (sichtb. Tumor cm) : 60 Gy (biol. eff. : 70Gy) PTV 3 : (sichtb. Tumor cm) : 44 Gy (biol. eff. : 60 Gy) Ergebnis : medianes Überleben : 11.7 Mon. 1 / 2 Jahre Überl. : 47.1% / 12.9% Chan et al, 2002
36 Prozent Gesamt-ÜL Hochmaligne Gliome / Radiotherapie Dosiseskalation (70-80Gy, med. 78Gy) +/- Temoz. Retrospektive Analyse Medianes ÜL RT + Temoz (n=29) RT +/- and. Chx. (n=31) 12.7 Mon. 7.5 Mon. Kein ÜL- Vorteil durch Dosiseskalation Monate Watkins et al., 2009
37 Hochmaligne Gliome / Radiotherapie Externe fraktionierte RT + Brachytherapie ( boost ) Medianes ÜL Keine : 58.8 Wo. n = 137 Boost : 68.8 Wo. n = 133 p=0.101 (n.s.) Selker et al., 2002
38 Hochmaligne Gliome / Radiotherapie GliaSite Brachytherapie als Boost (50Gy) / lokale perk. RT 60Gy Retrospektive Analyse Welsh et al., 2007
39 Hochmaligne Gliome / Radiotherapie GliaSite Brachytherapie als Boost (50Gy) / lokale perk. RT 60Gy Retrospektive Analyse Med. Gesamt ÜL RTOG : 8,5 Mon. Boost GliaSite : 11,4 Mon Boost (n= 20) RTOG RPA data set Welsh et al., 2007
40 Hochmaligne Gliome / Radiotherapie RTOG / glioblastoma Phase III : conv. RT/BCNU versus conv. RT/BCNU+stereot. Boost (15-24Gy) Souhami et al., 2004
41 Hochmaligne Gliome / Radiotherapie Dosiseskalation (Protonen) / Glioblastom Phase I/II : hfx / concom. Proton boost GyE + ACNU 20 Pat. (17 RPA IV n. RTOG) Med. ÜL : 21.6 Mon. Med. ÜL RTOG IV : 11.1 Mon. 2 / 20 Pat. Spättoxizität Nekrose / Leukenceph. Mizumoto et al., 2010
42 Hochmaligne Gliome / Radiotherapie Dosiseskalation / Glioblastom Protonen / Carbon - Ionen Autor Pat.-Zahl Gesamtdosis / Fraktionierung Fitzek et al.,1999 Mizoe et al., 2007 Mizumoto Et al., (2 Oligo) 1 Epend. 1 Ries.zell-GBM 16 AA 32 GBM Photonen Gy Boost Protonen 90 CGE (kum) 50 Gy / 25 Fr. Boost Carbon-Ionen Gy ACNU Gy Phot,Prot. boost (hfx) 96.6 GyE (kumul.)/acnu Medianes Überleben Med. : 20 Mon. RPA-RTOG III-IV: 20 Mon. V : 14 Mon. Med. OS AA : 35 Mon. GBM : 17 Mon. Med. PFS Low dose : 4-7 Mon Med. dose : 7-19 Mon. High dose : Mon Med. ÜL : 21.6 Mon 17 Pat. RPA IV RTOG (med. ÜL) RPA IV Carb.-Ionen 13.7 Mon. RTOG 11.1 Mon. IV : 11.1 Mon.
43 Hochmaligne Gliome / Radiotherapie Glioblastom / Radiosensitivität Carbon - Ionen Combs et al., 2009
44 Hochmaligne Gliome / Radiotherapie Dosiseskalation / Glioblastom Carbon - Ionen Mizoe et al., 2007
45 Hochmaligne Gliome / Radiotherapie Einfluß der Wartezeit auf das Überleben N=182 / alleinige RT Medianes ÜL vom Zeitpunkt Beginn RT Keine Wartezeit 35.6 Wochen 1 Woche 2 Wochen 3 Wochen 4 Wochen 46 Wochen Do et al., 2000
46 Hochmaligne Gliome / Radiotherapie Einfluß der Wartezeit auf das Überleben Gesamtüberleben Intervall OP Start RT 16 RTOG-Studien /3052 Patienten Maximal 6 Wochen Bias? Anteil kompl Res : 15% 2 Wo. 26% > 4 Wo. Blumenthal, 2009
47 Hochmaligne Gliome / Radiotherapie Glioblastom / Alter als negativer prognostischer Faktor /cbtrus.org Alter (Jahre) Pat. 1 Jahr 2 Jahre 3 Jahre 4 Jahre 5 Jahre 10 Jahre , , , , , Total 15,793
48 Hochmaligne Gliome / Radiotherapie ANOCEF / Phase III : RT 50 Gy / 28 fr. versus best supportive care Pat. >/= 70 Jahre / KI >/= 70 (anapl. Glioma, Gliobl.) Keine Einschr. der LQ durch RT Medianes Überleben Op + RT (n=40) 28 Wochen nur Op. (n=44) 17 Wochen , 84 Pat., med. Alter : 73 Jahre (70-85 Jahre) Abbruch der Studie nach 1. Interimsanalyse Keime-Guibert, 2007
49 Autor Pat. Alter (Jahre) Bauman et al., 1994 Hochmaligne Gliome / Radiotherapie Glioblastom beim älteren Pat. / Überleben / Hypofraktionierung Gesamtdosis Fraktionierung Überleben 29 65,9-74,7 10 x 3.0 Gy (30 Gy ) 6 Mon Thomas et al., ,0 6 x 5.0 Gy (30 Gy) 6 Mon. Slotman et al., x 3.0 Gy (42 Gy) 36 Wochen Ford et al., x 3.0 Gy (36Gy) 16 Wochen Kleinberg et al., > x 3.0 Gy (51Gy) RPA V : 8.0 Mon. RPA VI : 5 Mon. Jeremic et al., > 60 or poor KPS 15 x 3.0 Gy (40Gy) 9 Mon. Philips et al., x 3.5 Gy (35 Gy) 8.7 Mon. Hulshof et al., McAleese et al., <65 - > x 2.0Gy (66 Gy) 8 x 5.0 Gy (40 Gy) 4 x 7.0 Gy (28 Gy) 7.0 Mon. 5.6 Mon. 6.6 Mon. 6 x 5.0 Gy (30 Gy) 5 Mon. Chang et al., x 2.5 Gy (50 Gy) 7 Mon. Lutterbach et al., x 3.5 Gy (42 Gy) 7.3 Mon.
50 Hochmaligne Gliome / Radiotherapie Phase III : 60 Gy in 30 Fraktionen versus 40 Gy in 15 Fraktionen Patienten >/= 60 Jahre Medianes ÜL 6 Wochen 5.1 Monate 3 Wochen 5.6 Monate Roa et al., 2004
51 Hochmaligne Gliome / Radiotherapie Radiotherapie / palliativer Effekt (neurologische Funktion) Autor Pat. Alter (Jahre) Dosis Fraktionierung Besser Stabil Schlechter Bauman et al., ,9-74,7 30 Gy / 10 Fr. 38% 38% 24% Thomas et al., ,0 30 Gy / 6 Fr. 78 % Besser / stabil 78 % Besser / stabil 22 % Slotman et al., Gy / 14 Fr. (3.0Gy) KPS 70 :11/15 KPS 80 : 3/6 KPS 90: /9 - Meckling et al., ,6 median 50 Gy median 35 Fr. 18 % 67 % 15% Jeremic et al., > 60 or poor KPS 45 Gy (15 x 3.0 Gy) 45% Keine Angaben Keine Angaben Hulshof et al., ,0 40 Gy (8 x 5.0 Gy) 28 Gy (4 x 7.0 Gy) 14% 31% Keine Angaben Keine Angaben McAleese et al., <65 - > Gy (6 x 5.0 Gy) 68% Besser / stabil 68% Besser / stabil 32%
52 Hochmaligne Gliome / Radiotherapie Palliativer Effekt der RT / KPS im Verlauf nach RPA Klassif. n = 7 n = 29 n = 19 Chang et al.,2003
53 Hochmaligne Gliome / Radiotherapie Palliativer Effekt der RT / Zeit ohne Rollstuhl / Bettlägerigkeit Chang et al.,2003
54 Hochmaligne Gliome / Radiotherapie Phase I, Radiosensitizer Motexaphin Gd, Glioblastom Gesamtüberleben / matched pair analyse RTOG data base (nur RT) Med. ÜL : 16,1 Mon P=0,03 n=33 n= k.a. Med. ÜL : 11,8 Mon Ford et al., 2007
55 Hochmaligne Gliome / Überleben nach Therapiearm 1 Hochmaligne Gliome / Radiotherapie Ü b e r l e b e n 0,8 0,6 0,4 0,2 Ereignis Gesamt Arm RT / PCV nur RT Medianes Überleben : RT / PCV : 10 Mon. Nur RT : 9,5 Mon. ÜL-Vorteil nach 2 Jahren : 1,7% p= nicht sign Jahre Med. Research Council Brain Tumour Working Party, 2001
56 Prozent Hochmaligne Gliome / Radiotherapie 100 Glioblastom / randomisierte Phase III Studie BCNU + RT versus BCNU + Cis vor RT BCNU + RT, n= 109 BCNU + Cis -> RT, n= BCNU/RT Cispl /RT Med. ÜL 11,2 Mon. 11,0 Mon Überleben (Monate) Grossman et al., 2003
57 Überleben (%) Hochmaligne Gliome / Radiotherapie Hochmaligne Gliome / NOA ,75 1 Gesamtüberlebenszeiten ACNU-VM26 : n = 183 ACNU-AraC : n = 179 0,5 0, ,34 Medianes Überleben (Monate) 18,79 Medianes Überleben (Monate) Zeit (Monate) NOA, J Clin Oncol 2003
58 Hochmaligne Gliome / Radiotherapie Intraop. Implantation von BCNU (Gliadel) Phase III Studie Gliadel : 120 Pat. Placebo : 120 Pat. Westphal, et al., 2006
59 Patienten (%) Hochmaligne Gliome / Radiotherapie Glioblastom / EORTC / 22981: progressionsfreies Überleben (PFS) RT TMZ/RT Medianes PFS (Monate) Jahres-PFS 27% 9% 2-Jahres-PFS 2% 11% HR [95% C.I.]: RT 0.54 TMZ/RT [ ] p < O N Anzahl der Patienten at risk : (Monate) RT TMZ/RT Stupp et al. New Engl. J. Med. 2005
60 Patienten (%) Hochmaligne Gliome / Radiotherapie Glioblastom / EORTC / 22981: Gesamtüberleben TMZ/RT RT Median (Monate) Jahres-Überleben 10% 26% HR [95% C.I.] 0.63 [ ] TMZ/RT p < RT O N Anzahl der Patienten at risk : (Monate) RT TMZ/RT Stupp et al. New Engl. J. Med. 2005
61 Hochmaligne Gliome / Radiotherapie MGMT Gen / Methylierungsstatus MGMT Ausschüttung MGMT Gen Kaum Ansprechen auf Behandlung MGMT Promotor Region aktiviert keine MGMT Ausschüttung MGMT Gen Ansprechen auf Behandlung Methyliert deaktiviert
62 Patienten (%) Hochmaligne Gliome / Radiotherapie Progressionsfreies Überleben Einfluss des MGMT-Status in den Studienarmen Overall Wald-Test: p<0.001 (df=3) Monate O N Anzahl der Patienten at risk : Meth - / RT Meth - / RT+TMZ Meth + / RT Meth + / RT+TMZ
63 Hochmaligne Gliome / Radiotherapie Glioblastom / Op / RT / Temoz. + Cilengitide (med. Überleben) Integrin Inhibitor (Anti-Tumoreffekt und Angiogenesehemmer) Methyl (n=23) Med. : nicht err. Unmethyl (n=22) Med. 12 Mon. Unbest (n=7) Cilengitide (n= 52) 12 Mon. : 67% Med. : nicht err. Histor. Kontr. (n=64) (Lausanne) 12 Mon.: 58% Stupp et al., ASCO 2007
64 Hochmaligne Gliome / Radiotherapie
65 Hochmaligne Gliome / Radiotherapie Treatment schema for (A) study group and (B) control group in which most patients received bevacizumab at recurrence. Lai A et al. JCO 2011;29:
66 Hochmaligne Gliome / Radiotherapie Kaplan-Meier analysis of (A) overall survival and (B) progression-free survival comparing current study group (gold; radiation therapy [RT] + temozolomide [TMZ] + bevacizumab [BV]) with control group (blue; RT + TMZ). Lai A et al. JCO 2011;29:
67 Hochmaligne Gliome / Radiotherapie Glioblastom / Op / RT / Temoz. + / - Bevac / Irinotecan GLARIUS
68 Hochmaligne Gliome / Radiotherapie Ältere Patienten / offene Fragen Alleinige postop. Bestrahlung (geeignetes Dosis-Frakt.-Schema) Alleinige Chemotherapie (RT bei Progression)? Primär kombinierte Therapie
69 Hochmaligne Gliome / Radiotherapie Nordic elderly trial (Sweden, Norway, Denmark, Finland) Phase III trial / role of up-front temozolomide + Assessment of appropriate RT schedule Group 1 Conventional radiotherapy 60 Gy in 30 fr./ 6 weeks Group 2 Short-term radiotherapy 34 Gy in 10 fr. / 2 weeks Group 3 Chemotherapy alone (RT upon progression) Temozolomide 200 mg/m 2 day 1-5, every 4 weeks for max. 6 cycles or until radiological and/or clinical progr.
70 Hochmaligne Gliome / Radiotherapie EORTC / Gesamt - ÜL RTOG class V (Alter >/= 50 / KPI ) p=0.054 Subgruppenanalyse der EORTC Alter (105 RT, 98 RT/TMZ), HR=0.63 p<0.05 Alter (58 RT, 57 RT/TMZ), HR=0.72 p=0.054 Alter (42 RT, 41 RT/TMZ), HR 0.8 p<0.096 p=0.34 Effekt von Temozolomide in der Kombination mit RT nimmt mit zunehmendem Alter ab (months) O N Number of patients at risk : Treatment RT TMZ/RT Mirimanoff et al., 2006
71 Hochmaligne Gliome / Radiotherapie
72 Hochmaligne Gliome / Radiotherapie Stand : 10.Jan 2011
73 Hochmaligne Gliome / Radiotherapie Temozolomide als Alternative zur RT 86 Patienten (Alter > 70): 60 Gy/30 Frakt. (54 Pat.) oder TMZ 5/28 (32 Pts.) (retrospective Analyse) Mittleres Alter: 73.8 Jahre Mittler KI: 70 98% (84/86) Glioblastom Medianes ÜL RT 4.1 Monate TMZ 6 Monate TMZ 150 mg/m 2 bei 11 und 200 mg/m 2 bei 21 Patienten Beherrschb. Toxizität bei 15.6% d. Pat. Glantz et al. 2003
74 Gesamtüberleben Operation (Resektion/Biopsie) Histologie: anaplastisches Astrozytom, Glioblastom Alter > 65 Jahre, Karnofsky Score? 60 Randomisierung Arm A Arm B NOA - 8 Strahlentherapie Gy in Fraktionen zu 1.8 bis 2 Gy an 4 bis 5 Tagen/Woche Dauer: ca. 6 Wochen Temozolomid 100 mg/m 2 KOF an Tag 1-7 und alle 28 Tage Dauer: bis zur Progression PD PD Chemotherapie(n) nach Maßgabe des Behandlers Strahlentherapie nach Maßgabe des Behandlers
75 Hochmaligne Gliome / Radiotherapie Anaplastische Oligodendrogliome / RTOG RT alone versus PCV anschl. RT (60 Gy) / Progressionsfreies Überleben Cairncross et al., 2006
76 Hochmaligne Gliome / Radiotherapie Anaplastische Oligodendrogliome / RTOG RT alone versus PCV anschl. RT (60 Gy) / Gesamtüberleben Cairncross et al., 2006
77 Hochmaligne Gliome / Radiotherapie Anaplastische Oligodendrogliome / RTOG RT alone v. PCV anschl. RT (60 Gy) / Progr.-fr. ÜL / 1p-19q Deletion Cairncross et al., 2006
78 Hochmaligne Gliome / Radiotherapie Anaplastische Oligodendrogliome / EORTC RT alone versus RT( 60Gy) anschl. PCV / Progressionsfreies Überleben RT/PCV RT (n=185) : RT/PCV (n=183): p= Mon Mon Nur RT Van den Bent et al., 2006
79 Hochmaligne Gliome / Radiotherapie Anaplastische Oligodendrogliome / EORTC RT alone versus RT( 60Gy) anschl. PCV / Gesamt - ÜL RT/PCV RT (n=185) : RT/PCV (n=183): p= Mon Mon. Nur RT Van den Bent et al., 2006
80 Hochmaligne Gliome / Radiotherapie Anaplastische Oligodendrogliome / EORTC RT alone versus RT( 60Gy) anschl. PCV / Progr.-fr. ÜL / 1p-19q Deletion Van den Bent et al., 2006
81 NOA-04: Randomisierte Phase-III-Studie der sequentiellen Radiochx. oligoastrozytärer Tumoren des WHO-Grads III mit PCV oder Temozolomid Resektion oder Biopsie Histologie: anaplastisches Oligodendrogliom, Oligoastrozytom, Astrozytom Arm A Arme B,C Strahlentherapie Primäre Chemotherapie B C PCV Temozolomid A1 PD A2 PD PD PCV Temozolomid Strahlentherapie Strahlentherapie PD PD PD PD Temozolomid PCV Temozolomid PCV
82 NOA-4 Hochmaligne Gliome / Radiotherapie
83 Anteil der überlebenden Patienten Hochmaligne Gliome / Radiotherapie NOA-4 / Gesamtüberleben n. histologischem Subtyp Monate
84 Anteil der überlebenden Patienten Hochmaligne Gliome / Radiotherapie NOA-4 / Gesamtüberleben n. Randomisationsarm A versus B1/2 Monate
85 Proportion of patients surviving Hochmaligne Gliome / Radiotherapie NOA 4 / Newly diagnosed anaplastic glioma: efficacy of RT improved in methylated tumors? Time, months Arm A: unmethylated (n = 35) Arm A: methylated (n = 56) Arm B1/2: unmethylated (n = 27) Arm B1/2: methylated (n = 58)
86 Hochmaligne Gliome / Radiotherapie
87 Hochmaligne Gliome / Radiotherapie
88 Hochmaligne Gliome / Radiotherapie Pseudoprogression nach RT Chx / Teilres. Astrozytom III präop post op.
89 Hochmaligne Gliome / Radiotherapie Pseudoprogression nach RT Chx / Teilres. Astrozytom III Mon. n.rt 3. Kurs ACNU VM Mon. n. RT 6. Kurs ACNU VM 26
90 Hochmaligne Gliome / Radiotherapie Pseudoprogression nach RT Chx / Teilres. Astrozytom III Mon. n.rt ACNU VM Mon. n. RT ACNU VM 26
91 Hochmaligne Gliome / Radiotherapie Bildgebung / Ansprechen auf Therapie / Pseudoprogression OP / RT 60 Gy / Temoz. Medianes Gesamt-ÜL Pseudoprogr. (n=32) frühe Progr. (n=18) weder / noch (n=53) 38 Mon Mon Mon. Brandes, et al. 2008
92 Hochmaligne Gliome / Radiotherapie Rezidivtherapie bei hochmalignen Gliomen - Operation - Erneute Bestrahlung? - Chemotherapie
93 Hochmaligne Gliome / Radiotherapie Strahlentherapie bei Rezidiv / hypofrakt. stereotakt. Autor Pat.-Zahl Technik / Dosierung Medianes Überleben Shepherd et al., Hypofrakt. Konvergenztherapie Einzeldosis 5 Gy, Eskal. 20 -> 50 Gy 11,0 Mon. Lederman et al., Stereotakt., hypofrakt. RT Med. 24 Gy in 4 Frakt. Voynov et al., Stereotakt. IMRT, med. 30 Gy (25-40 Gy), 5 Gy/Frakt. 7 Monate 10,1 Mon. Bartsch et al., Stereot. RT 14 Pat Gy, konv. Frakt. 8 Pat. 30 Gy hypofrakt. (6x5Gy) 7,0 Mon. Grosu et al., Stereotakt. RT, hypofrakt. 36 PET/SPECT, 30 Gy 8 CT/MRI (6 x 5 Gy) Vordermark et al Stereotakt. RT, hypofrakt. (4-10 Gy Einzeldosis) 30 Gy (20-30 Gy) 9,0 Mon. 5,0 Mon. 9,3 Mon.
94 Hochmaligne Gliome / Radiotherapie Strahlentherapie bei Rezidiv / konv. frakt. stereotakt. Autor Pat.- Zahl Technik / Dosierung Medianes Überleben Arcicasa et al., Frakt. Konvent. 2 D RT Einzeldosis 1,5 Gy, 34,5 Gy 13,7 Mon. Cho et al Konv. Frakt. RT, 37.5/15 Fraktionen 12,0 Mon. Hudes et al., 1999 Combs et al., 2005b 20 Stereot. RT Gy 24.0->35 Gy Eskalationsprotok. 54 GBM 39 WHO III Stereotakt. RT 36 Gy (15-62 Gy) 5 x 2.0 Gy konv. frakt Mon. 8,0 Mon. 12,0 Mon.
95 Re-Bestrahlung bei Rezidiv Effekt der Fraktionierung SRS / n = 46, med. ÜL : 11 Mon. FSRS / n = 25, med. ÜL : 12 Mon. Dosiskonzepte : 1. SRS : 17 Gy 50% Isodose 2. FSRT 37,5 Gy (ED 2,5 Gy) 85% Isodose Cho et al., 1999
96 Re-Bestrahlung bei Rezidiv Effekt der erneuten Operation Dosiskonzepte : 1. Frakt., konf. RT (n=14): Gy (ED 2-3 Gy) 2. FSRT (n=8) 30,0 Gy (ED 5,0 Gy) Überleben : 1. Re-Resektion (n=11): med. ÜL : 13 Monate 2. Keine Re-Resektion (n=11) med. ÜL : 5 Monate Bartsch et al., 2005
97 Überleben Re-Bestrahlung bei Rezidiv Fraktionierung (n = 31) 4 x 5 Gy 19 (61%) 5 x 4 Gy 10 (32%) 5 x 5 Gy 2 (7%) Med. ÜL : 10.2 Mon. 1,0 1,0 0,9 0,9 0,8 0,8 0,7 0,6 0,5 0,4 0,3 < 30 ml > 30 ml B p=0.01 0,7 0,6 0,5 0,4 0,3 < 50 Jahre =/> 50 Jahre p=0.05 0,2 0,2 0,1 0,1 0,0 0, Monate Henke et al., 2009
98 Surviving Re-Bestrahlung bei Rezidiv Überleben / Rezidivlokalisation 1,0 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0,0 Infield=1, border=2, outfield=3 Medianes Überleben: 12 vs.10 vs.6 Monate P= Überlebenszeit nach 2. Rt [Monate] Infield Border Exfield Henke et al., 2009
99 Hochmaligne Gliome / Radiotherapie Erneute RT 5 x 6Gy, 30.0Gy ZVD / Bevacizumab Alle 2 Wochen, 10mg /qm bis zur Progression n=25 (n=20 GBM, 5 AA) median. PFS 7.3 Mon. median. OS 12 Mon. Gutin et al., 2009
100 Re-Bestrahlung bei Rezidiv Hochmalignes Gliom / Re-Bestrahlung bei Rückfall / stereotaktische Konvergenztherapie Pat. 17 Jahre alt Hypofraktioniert, 4 x 5 Gy Vor RT 4 x 5 Gy CR 1 Jahr n. RT
101 Re-Bestrahlung bei Rezidiv 3 D konformale fraktionierte RT Rigide Fixierung Präzision : ca 1 mmm
102 Hochmaligne Gliome / Radiotherapie Targeting Methionin-PET bei hochmalignem Gliom zur Definition des klinischen Zielvolumens / z.b. Rezidivbestrahlungen
103 Hochmaligne Gliome / Radiotherapie Funktionelle Bildgebung in der Zielvolumenbestimmung Spektroskopie
104 Hochmaligne Gliome / Radiotherapie Postop. RT Tumorregion 60 Gy Dosiseskalation : kein Vorteil (Stereot. / Brachyth.) Dosiseskalation mit Hyperfraktionierung / Akzelerierung : kein Vorteil Ältere Patienten Fazit / Ausblick I lokale RT Überlebensvorteil alternativ hypofraktioniertes Konzept möglich Response Monitoring Pseudoprogression Funktionelle Bildgebung?
105 Hochmaligne Gliome / Radiotherapie Fazit / Ausblick II Integrierung von Systemtherapien Stratifizierung nach molekulargenetischem Profil 1p 19q Deletion (anapl. Gliome) MGMT Status (Glioblastom/anaplastische Gliome) Erneute Bestrahlung stereotaktische Techniken (geeign. Frakt.-Schema?) Integrierung funktioneller Bildgebung erneute Kombinationstherapie (RT-Chx.) Weitere Forschung notwendig
106 PZNSL - Radiotherapie Therapieziele Optimale Tumorkontrolle Verbesserung der Überlebenszeiten Kontrolliertes Nebenwirkungsrisiko Verbesserung der Lebensqualität
107 Wahrscheinlichkeit PZNSL - Radiotherapie Überlebensrate / Karnofsky-Index RTOG Alleinige RT Ganzhirn 40 Gy + boost 20 Gy verstorben KI (15/21) KI (20/20) Einsatzmöglichkeiten der Chx. unterschiedlich Therapieintensität Monate Nelson at al., 1992
108 Wahrscheinlichkeit PZNSL - Radiotherapie Überlebensrate / Alter RTOG Alleinige RT Ganzhirn 40 Gy + boost 20 Gy verstorben Alter < 60 Jahre (10/14) Alter 60 + Jahre (25/27) Einsatzmöglichkeiten der Chx. unterschiedlich Therapieintensität Monate Nelson at al., 1992
109 PZNSL - Radiotherapie Therapiekonzepte Prognostische Faktoren und Risikofaktoren für Therapiefolgen bestimmen die Auswahl der Therapie
110 PZNSL - Radiotherapie Zielvolumen Ganzhirn (unter Einschluß der Meningen) Aufsättigung der Tumorregion Nur Tumorregion
111 PZNSL - Radiotherapie Manifestationsmuster Immunkompetent HIV pos. Solitär 290 (72%) 87 (48%) Multipel 100 (25%) 94 (52%) Diffus 14 (3%) keine Ang. Gesamt Fine et al., 1993
112 PZNSL - Radiotherapie Intrakranielles pathobiol. Ausbreitungsmuster - Erhebung makroskopischer Tumorausbreitungen - Autopsie von 10 Patienten - Vergleich mit Bildgebung vor Exitus Ergebnis : MR : 7 Pat. lokalisierte Tumorbildung Autopsie : 10 Pat. : ausgedehnter Tumorbefall außerhalb der Regionen mit Befall im MR Bildgebung unterschätzt die reale Tumorausdehnung Lai et al., 2002
113 PZNSL - Radiotherapie Bestrahlung der erweiterten Tumorregion oder Ganzhirn-RT? 43 Pat., RT der Tumorregion +/- Chx., Gy, med. 50 Gy 21 Pat. : Sicherheitsabstand >/=4 cm 22 Pat. : Sicherheitsabstand <4 cm Ergebnis : 38 Rückfälle >/= 4cm < 4cm 20 Pat. 18 Pat. Innerhalb 8 6 Außerhalb 4 10 Med. ÜL 28,5 Mon. 15 Mon. p=0.057 Shibamoto et al., 2002
114 PZNSL - Radiotherapie RT Ganzhirn / Dosis - Wirkungsbeziehungen Autor Dosis Überleben P- Wert Pollack, Gy 5 J : 64% p= Gy 5 J.: 27% Hayekawa,1994 < 40 Gy med. 15 Mon. p=0.05 > 40 Gy med. 18 Mon. Reni, 2001 (< 60 Jahre) >/= 40 Gy < 40 Gy 3 J : 59% 3 J.: 62% n.s. Bessel, Gy < 45 Gy 3 J : 92% 3 J.: 60% p=0.04 Shibamoto, 2002 < 50 Gy 5 J : 18% n.s. (< 60 Jahre) >/= 50 Gy 5 J.: 12% DeAngelis, Gy med. 24,5 M. progr. frei RTOG Gy (2x1,2Gy) med. 23,3 M. p=0.81
115 Wahrscheinlichkeit PZNSL - Radiotherapie Dosis Wirkungsbeziehung 45 Gy versus < 45 Gy 1 0,8 RT 45 Gy (n=15) 0,6 0,4 0,2 0 RT < 45 Gy (n=10) Pat. 3 J. ÜLZ RT 45 Gy 15 92% RT< 45 Gy 10 60% p = 0.04 Land-mark : 6 Monate Monate Bessel et al., 2002
116 PZNSL - Radiotherapie Überleben / alleinige RT Autor Pat. Dosis Überleben Freeman Gy 2 Jahre 36 % Grangier med.46 Gy med. 24 Mon. De Angelis /60 Gy med. 21,7 Mon. Nelson /60 Gy med. 12,2 Mon. Mead /54 Gy med. 26 Mon.
117 PZNSL - Radiotherapie Überleben / Radio- / Chx. (ohne MTX) Autor Pat. Protokoll. RT Med. ÜLZ Lachance 1994 O Neill 1999 Schultz 1996 Shibamoto 1999 Mead CHOP (2-4x) 45 Gy + 53 CHOP (2x) AraC (2x) 46 CHOP (2-3x) 2x 12mg i.th.mtx 23 VEPA (VCR, Cycl,, Pred., Doxorub.) (6x) 10 Gy 8,5 Mon.O 50,4 Gy 9,6 Mon. 41,4 Gy+ 18 Gy Gy + 15 Gy 38 CHOP 1-6 x 40 Gy + 14 Gy 16,1 Mon. 25 Mon. 14 Mon.
118 PZNSL - Radiotherapie Überleben / Radio- / Chx. (mit MTX) Autor Pat. Protokoll RT Med. ÜLZ Glass 1994 De Angelis Abrey 1998 O Brien 2000 De Angelis 2002 Biron ,5 mg/m2 MTX (1-6x) 31 1g/m2 i.v 12mg i.th MTX (6x), AraC (2x) 46 1g/m2 MTX (2x) 102 2,5g/m2 MTX VCR,Proc. 12 mg i.th. MTX (5x) 42 3g/m2 MTX,VCR Dox., Cycloph.,AraC (5x) 30 Gy 33 Mon. 40/14 Gy 42 Mon. 45 Gy 33 Mon. 45 Gy 36 Gy 20 / 50 Gy 36,9 Mon. 96 Mon.
119 PZNSL - Radiotherapie Leukenzephalopathie Risiko RT/Chx. versus nur RT Autor RT / Chx. Nur RT Nelson, /51 (1,9%) De Angelis, /31 (9,7%) 0/16 Gragier, /12 (16,6%) 0/14 Kortmann, /7 0/10 Shibamoto, /30 (10%) - Sarazin, /17 (23,5%) - Schultz, /52 (3%) - Abray, /10 Pat > 60J. - Abray, 2000 <60 J. 1/18 (6%) >60 J. 10/12 ( 83%) Bessel, 2001 <60 J. 1/12 (8,3%) > 60 J. 5/8 (62%) - Patienten erlebten die Spättoxizität - nicht
120 PZNSL - Radiotherapie High-dose methotrexate with or without whole brain radiotherapy for primary CNS lymphoma (G-PCNSL-SG-1) *45 Gy Ganzhirn 5 x 1,5 Gy Randomisation A1 oder B1 versus A2 oder B2 CR 6 x MTX (4 mg/m2 alle 14d / 3 x 8mg Dex. /10d Kurs 1) PR/SD/PD Arm A Arm B A1 Sofortige RT* A2 RT* bei Rückfall B1 Sofortige RT* B2 : AraC 4x3mg/m2 in 48h alle 3 Wo. 4 Kurse
121 PZNSL - Radiotherapie High-dose methotrexate with or without whole brain radiotherapy for primary CNS lymphoma (G-PCNSL-SG-1) / PFS Chx. + RT Chx. ohne RT Med. ÜL Mon. Chx + RT 5.6 CHx RT 2.0 Med. ÜL Mon. Chx + RT 36.3 CHx RT 21.5 Thiel et al., 2011
122 PZNSL - Radiotherapie High-dose methotrexate with or without whole brain radiotherapy for primary CNS lymphoma (G-PCNSL-SG-1) / OS Chx. + RT Chx. ohne RT Med. ÜL Mon. Chx + RT 24.3 CHx RT 18.6 Med. ÜL Mon. Chx + RT 38.8 CHx RT 39.4 Thiel et al., 2011
123 Wahrscheinlichkeit PZNSL - Radiotherapie Überleben / sofortige RT versus RT bei Rückfall (Meta-Analyse, n = 288 Patienten, 19 prospektive Serien) Sof. RT (n=70) RT / Rückf. (n=49) 5 J. ÜL Sof. RT 61% RT / Rückf. 69% p= Monate Reni et al., 2001
124 PZNSL - Radiotherapie Leukenzephalopathie Risiko nur Chx. Autor Nur Chx. Substanzen Cher, /11 8g/m2 MTX Freilich, /13 (7,7%) MTX/Ara-C,Thiotepa Sandor, /14 (21,4%) 8,4g/m2 MTX, Thiotepa VCR, i.t. MTX/Ara-C Guha-Thakurta, /31 8g/m2 MTX Abrey, /22 (4,5%) 3,5mg/m2, Procarb, VCR Siobhan, /10 8g/m2 MTX Mc. Allister, /74 High-dose MTX i.a. VP-16 i.a./i.v., Cycloph.Procarb., Dexameth. Schlegel, /20 (5%) High-dose MTX, Ara-C VCR, Ifos., Cycloph., Dex.
125 PZNSL - Radiotherapie Kombiniertes Konzept : milde Chx. + intensive RT MTX i.v. 1g/m2 Tag 1 und 8 anschl. Ganzhirn 45 Gy / boost 5.4 Gy (5 x 1.8 Gy) (i.th MTX plus spinale RT bei pos. CSF) / Stand Med. ÜL 33 Mon. / 2 J. ÜL : 62% 46 Pat. (med. Alter 58 Jahre) (25 76 Jahre)) Pat. Demenz (13%) nach median 16 Monaten 3 von 6 verstarben (6.5%) Überleben / Monate Neurotoxizität / Monate O Brien, 2000
126 PZNSL - Radiotherapie Kombiniertes Konzept : milde Chx. + intensive RT MTX i.v. 1g/m2 Tag 1 und 8 anschl. Ganzhirn 45 Gy / boost 5.4 Gy (5 x 1.8 Gy) (i.th MTX plus spinale RT bei pos. CSF) / Stand Med. ÜL 36 Mon. / 5 J. ÜL : 37% 46 Pat. (med. Alter 58 Jahre (25 76 Jahre) Pat. Demenz (24%) nach median 30 Monaten 8 von 11 verstarben (17.4%) Pat =/> 65 Jahre Pat < 65 Jahre Überleben / Jahre Neurotoxizität / Jahre O Brien, 2006
127 PZNSL - Radiotherapie Spättoxizität / RTOG x MTX / 2.5 mg/m2 iv., 5 x 12 mg MTX Ommaya, VCR, Procarb. 45 Gy / 1.8 Gy versus 36 Gy hfx (2 x 1.2 Gy) bei CR Gy n = 66 (konv. frakt.) 36 Gy n = 16 (hfx.) Zeit bis zum Auftreten einer Grad 5 Neurotoxizität (Demenz) Gemessen am MMSE Neurotoxizität / Jahre Fisher et al.,2005
128 Risiko (%) Spätfolgen nach Therapie von Tumoren des ZNS Dosis - Wirkungsbeziehungen, n=536, Kinder 16 Publ. (ALL - + MTX) / FSIQ FSIQ<90 FSIQ< TD 50 TD TD 5 0 TD Dosis (Gy) Fuss et al., 2000
129 PZNSL - Radiotherapie Kombiniertes Konzept : intensivere Chx. + reduzierte RT 5-7 Zyklen R-MPV (Rituximab, MTX (3.5g/m2), VCR, Procarb. n = 27 n = 19 n = 8 Shah, et al. 2007
130 PZNSL - Radiotherapie Kaplan-Meier survival curves of the 19 patients treated with reduced-dose whole-brain radiotherapy showing OS; (solid line) and PFS; dashed line) 2 Jahre PFS : 79% 2 Jahre OS : 89% Shah, et al. 2007
131 PZNSL - Radiotherapie Neurokognitive Funktion n. Chx., 23.4 Gy Ganzhirn T1 : vor Therapie T2 : nach Chx. T3 : 6 Mon. n. RT T4 : 12 Mon. n. RT T5 : 18 Mon. n. RT T6 : 24 Mon. n. RT Correa et al., 2009
132 PZNSL - Radiotherapie Therapiefolgen / Bildgebung Risikofaktoren / 33 Patienten (immunkompetent) retrospektive Analyse, CT / MR Therapie : 22 Pat. alleinige RT, 11 Pat. RT / CHx. Risikofaktoren : Alter > 60 Jahre RT Dosis > 50 Gy (Anmerkung : > 30Gy?) Chemotherapie (MTX) Bereits vorliegende Bildveränderungen Multifokale Tumormanifestation Wassenberg et al., 2001
133 Wahrscheinlichkeit PZNSL - Radiotherapie Überleben / ältere Patienten (>/= 65 Jahre) SEER Daten Bank (stratifiziert nach Diagnosejahr / n = 579) Pat. : Supportivth. 211 Pat. : nur RT 101 Pat. : nur Chx. 152 Pat. : RT + Chx. Med. ÜL : 7 Monate Nur Chx./ RT + Chx. bei jüngeren Pat. nur RT bei älteren Pat. p = Monate Panageas et al., 2007
134 PZNSL - Radiotherapie Salvage RT nach MTX Versagen (nach median 3,9 Mon.) Ganzhirn (28-45 Gy, median 36 Gy) / Überleben nach Alter Gesamtüberleben / n = 27 (nach Beginn der RT) Median : 37.2 Mon. Median : 7.3 Mon. Nguyen et al., 2005
135 PZNSL - Radiotherapie Problem : Pat. über 65 J. bzw. KI < 70 Eingeschränkte Chemotherapieoptionen Niedrige Überlebensraten Bei Diagnose häufig bereits eingeschränkte neurokognitive Funktionen Bisherige kombinierte Therapien (MTX) mit hohem LE-Risiko verbunden Geeignetes Radiotherapiekonzept?
136 PZNSL - Radiotherapie Palliativer Effekt der Bestrahlung (alleinige RT bei HIV) Symptom Pat. Komplette Remission Fehlende Orientierung Ansprechrate (gesamt) 35 3 (8.6%) 17 (48.6%) Lethargie 20 1 (5%) 12 (60%) Erinnerungsverlust 17 1 (5.9%) 8 (47.1%) Kopfschmerzen 28 5 (17.9%) 17 (60.7%) Anfälle 46 1 (4.4%) 10 (43,4%) Neurol. Defizit 8 4 (8.7% 27 (58.7%) Sehstörungen (62.5%) Andere 1 (3.3%) 15 (50%) Corn et al., 1997
137 PZNSL - Radiotherapie Schlussfolgerungen Ganzhirnbestrahlung, kein boost Lokale Bestrahlung nicht ausreichend Dosis-Wirkungsbeziehung alleinige RT : Gy (Ganzhirn) (in Komb. mit Chx.?) Gy (Ganzhirn) hohe Spättoxizität Komb. Therapie ( intens. Chx und CR) : 23.4 Gy Ganzhirn ausreichend (?) 23.4 Gy Ganzhirn-RT niedriges Spätfolgenrisiko (?) (auch in Komb. mit Chx.) RT als Salvage-Therapie (Ganzhirn / Gy)
138 PZNSL - Radiotherapie Offene Fragen Ältere Patienten (> 65 Jahre) Geeignetes Radio-/Chemotherapie Schema Dosisreduktion (in Komb. mit Chx.) tolerables Chemotherapieprotokoll palliativer Effekt / Lebensqualität? Jüngere Patienten (= / < 65 Jahre) Radiotherapie als Salvagetherapie reduzierte Dosis? in Kombination mit einer weniger intensiven Salvage-Chemotherapie
139 Vielen Dank für Ihre Aufmerksamkeit
Tumoren des Zentralnervensystems. Häufigste histologische Typen / Lokalisation CBTRUS
 Tumoren des Zentralnervensystems Häufigste histologische Typen / Lokalisation CBTRUS 2000-2004 Intraaxial Gliome (astroz./olig.) 33.6% Ependymome 2.1% Medulloblastome 1.5% Hämangioblastome 0.8% ZNS Lymphome
Tumoren des Zentralnervensystems Häufigste histologische Typen / Lokalisation CBTRUS 2000-2004 Intraaxial Gliome (astroz./olig.) 33.6% Ependymome 2.1% Medulloblastome 1.5% Hämangioblastome 0.8% ZNS Lymphome
Erneute Strahlentherapie bei hochmalignen Gliomen
 Erneute Strahlentherapie bei hochmalignen Gliomen Therapieoptionen bei Rezidiv - Operation - Erneute Bestrahlung? - Chemotherapie Rückfallmuster nach lokaler Bestrahlung Hess et al., 1993 Chan et al.,
Erneute Strahlentherapie bei hochmalignen Gliomen Therapieoptionen bei Rezidiv - Operation - Erneute Bestrahlung? - Chemotherapie Rückfallmuster nach lokaler Bestrahlung Hess et al., 1993 Chan et al.,
Radiotherapie beim Prostatakarzinom Innovative Therapiestrategien
 KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie beim Prostatakarzinom Innovative Therapiestrategien Ziele der Strahlentherapie Verbesserung der
KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie beim Prostatakarzinom Innovative Therapiestrategien Ziele der Strahlentherapie Verbesserung der
Struktur der Clinical Pathways
 Gliome Verantwortlich: PD Dr. Machein, PD Dr. Schnell, Dr. Dr. Oehlke, Dr. Fritsch, Dr. Doostkam, Prof. Dr. Mader, Dr. Reinacher, Prof. Dr. Zentner, Prof. Dr. Grosu Freigabe: interdisziplinärer Qualitätszirkel
Gliome Verantwortlich: PD Dr. Machein, PD Dr. Schnell, Dr. Dr. Oehlke, Dr. Fritsch, Dr. Doostkam, Prof. Dr. Mader, Dr. Reinacher, Prof. Dr. Zentner, Prof. Dr. Grosu Freigabe: interdisziplinärer Qualitätszirkel
Aspekte zur Indikation und Auswahl der Radiotherapie
 Aspekte zur Indikation und Auswahl der Radiotherapie Kurative oder palliative Therapie (medianes Überleben 1 2 Jahre) Zielvolumen Sequenz Neoadjuvant (vor OP) Postoperativ adjuvant Definitiv bei Inoperabilität
Aspekte zur Indikation und Auswahl der Radiotherapie Kurative oder palliative Therapie (medianes Überleben 1 2 Jahre) Zielvolumen Sequenz Neoadjuvant (vor OP) Postoperativ adjuvant Definitiv bei Inoperabilität
Struktur der SOP. Zeichenerklärung. Entscheidungsfrage? Diagnostik. Therapie. Tumorboard. Nachsorge. individuelle Therapie. Studienfrage?
 Gliome Verantwortlich: PD Dr. Machein, PD Dr. Schnell, Dr. Oehlke, Dr. Fritsch, Dr. Doostkam, Prof. Dr. Mader, Dr. Reinacher, Prof. Dr. Zentner, Prof. Dr. Grosu Freigabe: interdisziplinärer Qualitätszirkel
Gliome Verantwortlich: PD Dr. Machein, PD Dr. Schnell, Dr. Oehlke, Dr. Fritsch, Dr. Doostkam, Prof. Dr. Mader, Dr. Reinacher, Prof. Dr. Zentner, Prof. Dr. Grosu Freigabe: interdisziplinärer Qualitätszirkel
Die stereotaktische Bestrahlung von Lungentumoren
 Hypofraktionierung Innovation oder Risiko? Die stereotaktische Bestrahlung von Lungentumoren Frank Zimmermann Institut für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch;
Hypofraktionierung Innovation oder Risiko? Die stereotaktische Bestrahlung von Lungentumoren Frank Zimmermann Institut für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch;
Neues und Altbewährtes in der Therapie der Glioblastome
 Neues und Altbewährtes in der Therapie der Glioblastome Christina Hofmann Standardtherapie für Neuerkrankungen 1. Resektion/ Biopsie, post-operatives cmrt 2. Kombinierte Radiatio (54-60 Gy/ ED 1,8-2 Gy)
Neues und Altbewährtes in der Therapie der Glioblastome Christina Hofmann Standardtherapie für Neuerkrankungen 1. Resektion/ Biopsie, post-operatives cmrt 2. Kombinierte Radiatio (54-60 Gy/ ED 1,8-2 Gy)
Medulloblastom Ependymom (spinale Ependymome) Kraniopharyngeom Niedriggradige Gliome Hochmaligne Gliome
 Tumorentitäten Medulloblastom Ependymom (spinale Ependymome) Kraniopharyngeom Niedriggradige Gliome Hochmaligne Gliome Unterschiede Kinder // Erwachsene Biologisches Verhalten, Obwohl histologisch identisch
Tumorentitäten Medulloblastom Ependymom (spinale Ependymome) Kraniopharyngeom Niedriggradige Gliome Hochmaligne Gliome Unterschiede Kinder // Erwachsene Biologisches Verhalten, Obwohl histologisch identisch
Therapeutische Strategien
 Spinale Tumoren Therapeutische Strategien Operation Strahlentherapie Chemotherapie? Astrocytome Ependymome Andere Lokalisation : intra / extramedullär Ependymom Pilocytäres Astrocytom Spinale Tumoren Wachstumsmuster
Spinale Tumoren Therapeutische Strategien Operation Strahlentherapie Chemotherapie? Astrocytome Ependymome Andere Lokalisation : intra / extramedullär Ependymom Pilocytäres Astrocytom Spinale Tumoren Wachstumsmuster
Chirurgische Kombinationstherapien: Nachbestrahlung von Resektionshöhlen
 Interdisziplinäres DGNC/DEGRO Update Symposium: Aktuelle Behandlung zerebraler Metastasen Chirurgische Kombinationstherapien: Nachbestrahlung von Resektionshöhlen 20. Oktober 2017, Frankfurt am Main Klinik
Interdisziplinäres DGNC/DEGRO Update Symposium: Aktuelle Behandlung zerebraler Metastasen Chirurgische Kombinationstherapien: Nachbestrahlung von Resektionshöhlen 20. Oktober 2017, Frankfurt am Main Klinik
Primäre Hirntumoren (maligne) Tumoren der Meningen (benigne und maligne) Tumoren des Rückenmarks Primär maligne Lymphome des ZNS Tumoren von
 Primäre Hirntumoren (maligne) Tumoren der Meningen (benigne und maligne) Tumoren des Rückenmarks Primär maligne Lymphome des ZNS Tumoren von Hirnnerven (benigne) sekundäre Hirntumoren (Metastasen) Tumoren
Primäre Hirntumoren (maligne) Tumoren der Meningen (benigne und maligne) Tumoren des Rückenmarks Primär maligne Lymphome des ZNS Tumoren von Hirnnerven (benigne) sekundäre Hirntumoren (Metastasen) Tumoren
SRH Wald-Klinikum Gera ggmbh
 SRH Wald-Klinikum Gera ggmbh PET-CT Bestrahlungsplanung bei Patienten mit Bronchialkarzinom Monat Jahr von Dr. med. J. Pagel Prof. Dr. med. R.P. Baum* Dipl.- Phys. M. Schöpe PD Dr. med. K.-H. Kloetzer
SRH Wald-Klinikum Gera ggmbh PET-CT Bestrahlungsplanung bei Patienten mit Bronchialkarzinom Monat Jahr von Dr. med. J. Pagel Prof. Dr. med. R.P. Baum* Dipl.- Phys. M. Schöpe PD Dr. med. K.-H. Kloetzer
Hirnmetastasen PRO Radiochirurgie: Indikation und Technik M. Kocher
 Hirnmetastasen PRO Radiochirurgie: Indikation und Technik M. Kocher Klinik für Stereotaxie und Funktionelle Neurochirurgie, UniKlinik Köln & Institut für Neurowissenschaften und Medizin 4, FZ Jülich Seite
Hirnmetastasen PRO Radiochirurgie: Indikation und Technik M. Kocher Klinik für Stereotaxie und Funktionelle Neurochirurgie, UniKlinik Köln & Institut für Neurowissenschaften und Medizin 4, FZ Jülich Seite
Molekularbasierte Therapie bei Gliomen
 Molekularbasierte Therapie bei Gliomen Interdisziplinäres onkologisches Kolloquium 09.05.2017 M. Nadji-Ohl Klinikum Stuttgart-Katharinenhospital Neurozentrum/Neurochirurgie Entwicklungen in der GBM Therapie
Molekularbasierte Therapie bei Gliomen Interdisziplinäres onkologisches Kolloquium 09.05.2017 M. Nadji-Ohl Klinikum Stuttgart-Katharinenhospital Neurozentrum/Neurochirurgie Entwicklungen in der GBM Therapie
Behandlungspfade Interdisziplinäres Onkologisches Zentrum Klinikum Ernst von Bergmann Potsdam. Neuroonkologie Stand September 2018
 Neuroonkologie Stand September 2018 Tumorkonferenz Klinisches Szenario Notwendige Diagnostik Entscheidungsgrundlage Procedere 1 Pathologie Weiteres Procedere Verdacht auf ein hochgradiges Gliom Anhand
Neuroonkologie Stand September 2018 Tumorkonferenz Klinisches Szenario Notwendige Diagnostik Entscheidungsgrundlage Procedere 1 Pathologie Weiteres Procedere Verdacht auf ein hochgradiges Gliom Anhand
Ototoxizität. Aspekte. Chemotherapieinduzierter Hörverlust (Cisplatin) Strahlentherapieinduzierter Hörverlust
 Aspekte Chemotherapieinduzierter Hörverlust (Cisplatin) Strahlentherapieinduzierter Hörverlust Kategorisierung (Grading) Hörverlust bei Kombination Radiotherapie Chx. Zeitpunkt (Radiotherapie, Chemotherapie)
Aspekte Chemotherapieinduzierter Hörverlust (Cisplatin) Strahlentherapieinduzierter Hörverlust Kategorisierung (Grading) Hörverlust bei Kombination Radiotherapie Chx. Zeitpunkt (Radiotherapie, Chemotherapie)
Aktuelle Aspekte zur Therapie und Prognose - Radiotherapie -
 Aktuelle Aspekte zur Therapie und Prognose - Radiotherapie - R.-D. Kortmann / Leipzig Besonderheiten Histologischer Typ pilocytäres Astrocytom Lokalisation supratentorielle Mittellinie ( Optikusgliome
Aktuelle Aspekte zur Therapie und Prognose - Radiotherapie - R.-D. Kortmann / Leipzig Besonderheiten Histologischer Typ pilocytäres Astrocytom Lokalisation supratentorielle Mittellinie ( Optikusgliome
Plattenepithelkarzinom Ösophagus Multimodale Therapie
 Plattenepithelkarzinom Ösophagus Multimodale Therapie Frank Zimmermann Institut für Radiologische Onkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch Grundlegende Überlegung
Plattenepithelkarzinom Ösophagus Multimodale Therapie Frank Zimmermann Institut für Radiologische Onkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch Grundlegende Überlegung
Glioblastome evidenzbasierte Therapie
 Glioblastome evidenzbasierte Therapie 5. NZW-Süd 8./9. September 2006 in Ravensburg Wolfgang Wagner Paracelsus-Strahlenklinik Osnabrück 1 Evidenzkategorien I : IIa : IIb : IIc : III : Randomisierte, kontrollierte
Glioblastome evidenzbasierte Therapie 5. NZW-Süd 8./9. September 2006 in Ravensburg Wolfgang Wagner Paracelsus-Strahlenklinik Osnabrück 1 Evidenzkategorien I : IIa : IIb : IIc : III : Randomisierte, kontrollierte
Palliative Chemotherapie First line 04.Februar 2006
 Klinikum der Johann Wolfgang Goethe Universität Zentrum für Innere Medizin Medizinische Klinik I Pneumologie/Allergologie Palliative Chemotherapie First line 04.Februar 2006 W. Gleiber Klinikum der Johann
Klinikum der Johann Wolfgang Goethe Universität Zentrum für Innere Medizin Medizinische Klinik I Pneumologie/Allergologie Palliative Chemotherapie First line 04.Februar 2006 W. Gleiber Klinikum der Johann
Datenevaluation von Hirnmetastasen: Bestrahlung der Resektionshöhle & Radiochirurgie von Hirnmetastasen
 Datenevaluation von Hirnmetastasen: Bestrahlung der Resektionshöhle & Radiochirurgie von Hirnmetastasen Prof. Dr. Stephanie E. Combs Professor and Chair Department of Radiation Oncology Institute of Innovative
Datenevaluation von Hirnmetastasen: Bestrahlung der Resektionshöhle & Radiochirurgie von Hirnmetastasen Prof. Dr. Stephanie E. Combs Professor and Chair Department of Radiation Oncology Institute of Innovative
Diagnostik und Therapie primärer und metastasierter Mammakarzinome
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome ZNS-Metastasen beim Mammakarzinom ZNS-Metastasen beim Mammakarzinom AGO e.v. in der DGGG e.v. Guidelines Breast Versionen 2003-2012: Bischoff
Diagnostik und Therapie primärer und metastasierter Mammakarzinome ZNS-Metastasen beim Mammakarzinom ZNS-Metastasen beim Mammakarzinom AGO e.v. in der DGGG e.v. Guidelines Breast Versionen 2003-2012: Bischoff
Radiochemotherapie des nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT
 Radiochemotherapie des Nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT W. Huhnt Ruppiner Kliniken GmbH, Klinik für Strahlentherapie und Radioonkologie, Neuruppin GLIEDERUNG Einleitung: Überblick
Radiochemotherapie des Nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT W. Huhnt Ruppiner Kliniken GmbH, Klinik für Strahlentherapie und Radioonkologie, Neuruppin GLIEDERUNG Einleitung: Überblick
Originalarbeit: James et al., N Engl J Med 2012; 366:
 Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Prostatakarzinom lokal Dr. med. J. Heß
 Prostatakarzinom lokal 30.11.2011 Dr. med. J. Heß Risiko für Prostatakarzinom: 40% Risiko für klinisch relevantem PCA: 10% Risiko für PCA-spezifischen Tod.: 3% Prostata, Lung, Colorectal and Ovarian Cancer
Prostatakarzinom lokal 30.11.2011 Dr. med. J. Heß Risiko für Prostatakarzinom: 40% Risiko für klinisch relevantem PCA: 10% Risiko für PCA-spezifischen Tod.: 3% Prostata, Lung, Colorectal and Ovarian Cancer
Strahlentherapie des Endometriumkarzinoms. Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg
 Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Strahlentherapie des Endometriumkarzinoms Aktuelle Studienlage
Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Strahlentherapie des Endometriumkarzinoms Aktuelle Studienlage
Was ist Strahlentherapie?
 Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Erhaltungstherapie mit Rituximab beim follikulären Lymphom
 Prof. Dr. med. Wolfgang Hiddemann: Non-Hodgkin-Lymphom - Erhaltungstherapie mit Rituximab beim fol Non-Hodgkin-Lymphom Erhaltungstherapie mit Rituximab beim follikulären Lymphom Prof. Dr. med. Wolfgang
Prof. Dr. med. Wolfgang Hiddemann: Non-Hodgkin-Lymphom - Erhaltungstherapie mit Rituximab beim fol Non-Hodgkin-Lymphom Erhaltungstherapie mit Rituximab beim follikulären Lymphom Prof. Dr. med. Wolfgang
QoL mit einem intrakraniellen Gliom DGNC, Seeheim 2014
 QoL mit einem intrakraniellen Gliom DGNC, Seeheim 2014 Oliver Heese HELIOS Klinken Schwerin W. Tönnis u. W. Walter Bericht über 2611 Fälle, Zürich 1958 1 2014 perfekte Patient: 20 Monate Durchschnitt:
QoL mit einem intrakraniellen Gliom DGNC, Seeheim 2014 Oliver Heese HELIOS Klinken Schwerin W. Tönnis u. W. Walter Bericht über 2611 Fälle, Zürich 1958 1 2014 perfekte Patient: 20 Monate Durchschnitt:
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom
 Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Radiotherapie sekundärer WS- Tumoren Seeheim D Schnell, AL Grosu
 Radiotherapie sekundärer WS- Tumoren 14.07.2016 Seeheim D Schnell, AL Grosu Palliative Strahlentherapie Konventionelle Strahlentherapie Stereotaxie/ Radiochirurgie Primäre Radiotherapie Adjuvante Radiotherapie
Radiotherapie sekundärer WS- Tumoren 14.07.2016 Seeheim D Schnell, AL Grosu Palliative Strahlentherapie Konventionelle Strahlentherapie Stereotaxie/ Radiochirurgie Primäre Radiotherapie Adjuvante Radiotherapie
Neues vom ASCO. P. Wimberger Carl-Gustav-Carus Universität Technische Universität Dresden. Neues vom ASCO 2013
 Neues vom ASCO 2013 Neues vom ASCO P. Wimberger Carl-Gustav-Carus Universität Technische Universität Dresden First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz
Neues vom ASCO 2013 Neues vom ASCO P. Wimberger Carl-Gustav-Carus Universität Technische Universität Dresden First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz
HIT 2000/ Ependymome/ Radiotherapie
 Präsentationsnummer: 14-08 / Themengebiet: Pädiatrische Tumoren, Sarkome, seltene Tumoren ZWISCHENAUSWERTUNG ZUM STAND DER PROSPEKTIVEN, KOOPERATIVEN STUDIE HIT 2000 FÜR NICHT METASTASIERTE EPENDYMOME
Präsentationsnummer: 14-08 / Themengebiet: Pädiatrische Tumoren, Sarkome, seltene Tumoren ZWISCHENAUSWERTUNG ZUM STAND DER PROSPEKTIVEN, KOOPERATIVEN STUDIE HIT 2000 FÜR NICHT METASTASIERTE EPENDYMOME
Radiotherapie epithelialer Hauttumoren
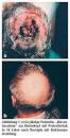 Radiotherapie epithelialer Hauttumoren 1. Basalzell Karzinom (ca. 80%) 100 Neuerkr. / 100.000 Einw./ Jahr (ca. 800 / 100.000 Einw. Nord-Austr.) 80 % im Kopf-Hals-Bereich Durchschn.-alter : 60 Jahre. (Tendenz
Radiotherapie epithelialer Hauttumoren 1. Basalzell Karzinom (ca. 80%) 100 Neuerkr. / 100.000 Einw./ Jahr (ca. 800 / 100.000 Einw. Nord-Austr.) 80 % im Kopf-Hals-Bereich Durchschn.-alter : 60 Jahre. (Tendenz
KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG. Radiotherapie in onkologischen Akutsituationen
 KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie in onkologischen Akutsituationen Neurologisches Defizit Schmerzen Obere Einflußstauung Atemnot
KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie in onkologischen Akutsituationen Neurologisches Defizit Schmerzen Obere Einflußstauung Atemnot
Diagnostik und Therapie primärer und metastasierter Mammakarzinome
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome ZNS-Metastasen beim Mammakarzinom ZNS-Metastasen beim Mammakarzinom AGO e.v. in der DGGG e.v. Guidelines Version 2010.1.1 Breast D Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome ZNS-Metastasen beim Mammakarzinom ZNS-Metastasen beim Mammakarzinom AGO e.v. in der DGGG e.v. Guidelines Version 2010.1.1 Breast D Versionen
RT CSA / Anapl. Ependymom Eineiige Zwillinge
 RT CSA / Anapl. Ependymom Eineiige Zwillinge M. Bamberg 6 Jaher alt Eineiige Zwillinge Kraniopharyngeom Z.n. mehrf. Op. s Keine Bestrahlung Spätfolgenprofile Neurokognitive Defizite Neurologische Ausfälle
RT CSA / Anapl. Ependymom Eineiige Zwillinge M. Bamberg 6 Jaher alt Eineiige Zwillinge Kraniopharyngeom Z.n. mehrf. Op. s Keine Bestrahlung Spätfolgenprofile Neurokognitive Defizite Neurologische Ausfälle
Neues vom ASCO beim metastasierten Mammakarzinom
 Neues vom ASCO 2008 beim metastasierten Mammakarzinom 04.07.2008 Dorit Lässig Medizinische Klinik und Poliklinik III (Direktor: Prof. Dr. med. W. Hiddemann) Universität München - Standort Großhadern Übersicht
Neues vom ASCO 2008 beim metastasierten Mammakarzinom 04.07.2008 Dorit Lässig Medizinische Klinik und Poliklinik III (Direktor: Prof. Dr. med. W. Hiddemann) Universität München - Standort Großhadern Übersicht
Primäre ZNS Lymphome Epidemiologie, Diagnostik und aktuelle Therapierichtlinien
 Primäre ZNS Lymphome Epidemiologie, Diagnostik und aktuelle Therapierichtlinien U Schlegel Neurologische Universitätsklinik Bochum 33. Fort- und Weiterbildungstagung der DGNC 19.-22.November 2014 M, 71
Primäre ZNS Lymphome Epidemiologie, Diagnostik und aktuelle Therapierichtlinien U Schlegel Neurologische Universitätsklinik Bochum 33. Fort- und Weiterbildungstagung der DGNC 19.-22.November 2014 M, 71
Journal: Journal of Clinical Oncology Publikationsjahr: 2012 Autoren: Paulo M. Hoff, Andreas Hochhaus, Bernhard C. Pestalozzi et al.
 Cediranib Plus FOLFOX/CAPOX Versus Placebo Plus FOLFOX/CAPOX in Patients With Previously Untreated Metastatic Colorectal Cancer: A Randomized, Double Blind, Phase III Study (HORIZON II) Journal: Journal
Cediranib Plus FOLFOX/CAPOX Versus Placebo Plus FOLFOX/CAPOX in Patients With Previously Untreated Metastatic Colorectal Cancer: A Randomized, Double Blind, Phase III Study (HORIZON II) Journal: Journal
PRO Ganzhirn: Indikation wann und mit welcher Technik?
 DKTK PRO Ganzhirn: Indikation wann und mit welcher Technik? Prof. Dr. med. Anca-L. Grosu Direktorin Klinik für Strahlenheilkunde Universitätsklinikum Freiburg 1. GHB (+/-RC) und Überlebenszeit These: GHB(+/-RC)
DKTK PRO Ganzhirn: Indikation wann und mit welcher Technik? Prof. Dr. med. Anca-L. Grosu Direktorin Klinik für Strahlenheilkunde Universitätsklinikum Freiburg 1. GHB (+/-RC) und Überlebenszeit These: GHB(+/-RC)
Strahlentherapie des Endometriumkarzinoms. Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg
 Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Übersicht Aktuelle Empfehlungen: risikoadaptierter Einsatz der
Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Übersicht Aktuelle Empfehlungen: risikoadaptierter Einsatz der
TAXOTERE (Docetaxel) Systemtherapie des Prostatakarzinoms: Taxotere, wann, wie lange und was dann? IX-1. Wann Wie lange Und was dann?
 TAXOTERE (Docetaxel) Wann Wie lange Und was dann? Gliederung Einleitung Evidenz für den Einsatz von Docetaxel Therapiebeginn Therapiedauer Zweitlinientherapien Zusammenfassung Ziel der Behandlung beim
TAXOTERE (Docetaxel) Wann Wie lange Und was dann? Gliederung Einleitung Evidenz für den Einsatz von Docetaxel Therapiebeginn Therapiedauer Zweitlinientherapien Zusammenfassung Ziel der Behandlung beim
St.Galler Ophtag. Felicitas Hitz Klinik für Onkologie und Hämatologie
 St.Galler Ophtag Felicitas Hitz Klinik für Onkologie und Hämatologie 31.5.2018 WHO 2017: Lymphoproliferative Erkrankungen Klinik, Morphologie, Immunphänotyp, Genetik Extranodale Lymphome mit Primärmanifestation
St.Galler Ophtag Felicitas Hitz Klinik für Onkologie und Hämatologie 31.5.2018 WHO 2017: Lymphoproliferative Erkrankungen Klinik, Morphologie, Immunphänotyp, Genetik Extranodale Lymphome mit Primärmanifestation
Hirntumore neue Therapien
 Hirntumore neue Therapien Peter Vajkoczy CHARITÉ - Universitätsmedizin Berlin (peter.vajkoczy@charite.de) U N I V E R S I T Ä T S M E D I Z I N B E R L I N THERAPIE MALIGNER GLIOME Langzeitüberleben beim
Hirntumore neue Therapien Peter Vajkoczy CHARITÉ - Universitätsmedizin Berlin (peter.vajkoczy@charite.de) U N I V E R S I T Ä T S M E D I Z I N B E R L I N THERAPIE MALIGNER GLIOME Langzeitüberleben beim
Relevante Aspekte. Wechselwirkungen zwischen Radiotherapie und Chemotherapie Histologie der Sekundärmalignome
 Relevante Aspekte Patientenfaktoren Alter bei Therapie, genet. Faktoren usw. Wechselwirkungen zwischen Radiotherapie und Chemotherapie Histologie der Sekundärmalignome Latenzzeiten bis zur Zweittumorentstehung
Relevante Aspekte Patientenfaktoren Alter bei Therapie, genet. Faktoren usw. Wechselwirkungen zwischen Radiotherapie und Chemotherapie Histologie der Sekundärmalignome Latenzzeiten bis zur Zweittumorentstehung
Hirntumoren. Christine Marosi. Klinik für Innere Medizin I Onkologie. Aufbaukurs Krebswissen Sommer Thema
 Aufbaukurs Krebswissen Sommer 2015 Hirntumoren Christine Marosi Klinik für Innere Medizin I Onkologie 1 Primäre Hirntumoren sind selten Hirnmetastasen (von einem anderen Primärtumor) sind 10x 1% der Krebsfälle
Aufbaukurs Krebswissen Sommer 2015 Hirntumoren Christine Marosi Klinik für Innere Medizin I Onkologie 1 Primäre Hirntumoren sind selten Hirnmetastasen (von einem anderen Primärtumor) sind 10x 1% der Krebsfälle
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
KML-Videoberichte. in Kooperation mit:
 KML-Videoberichte in Kooperation mit: Aggressive Lymphome in Kooperation mit: T-NHL Seite 3 CHOEP VERSUS CHOP ERZIELT BESSERE ERGEBNISSE BEI DER FIRSTLINE THERAPY VON T-CELL LYMPHOMEN A. Janikova für die
KML-Videoberichte in Kooperation mit: Aggressive Lymphome in Kooperation mit: T-NHL Seite 3 CHOEP VERSUS CHOP ERZIELT BESSERE ERGEBNISSE BEI DER FIRSTLINE THERAPY VON T-CELL LYMPHOMEN A. Janikova für die
Klinik für Dermatologie der Universität zu Köln. Metastasiertes Melanom Aktuelles vom amerikanischen Krebskongress 2015.
 Klinik für Dermatologie der Universität zu Köln Metastasiertes Melanom Aktuelles vom amerikanischen Krebskongress 2015 Cornelia Mauch ASCO 2014: Übersicht CTLA-4 AK in der adjuvanten Therapie Kombinationstherapien
Klinik für Dermatologie der Universität zu Köln Metastasiertes Melanom Aktuelles vom amerikanischen Krebskongress 2015 Cornelia Mauch ASCO 2014: Übersicht CTLA-4 AK in der adjuvanten Therapie Kombinationstherapien
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung. Universitäts- Klinikum Jena
 Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
Lokal radikale Radiotherapie von Hirnmetastasen: Luzerner Konzept und Resultate. Philipp Gut LUKS
 Lokal radikale Radiotherapie von Hirnmetastasen: Luzerner Konzept und Resultate Philipp Gut 1.5.2010-30.10.13 LUKS Number of Patients Lokal radikale Radiotherapie von Overall survival Patienten mit Hirnmetastasen
Lokal radikale Radiotherapie von Hirnmetastasen: Luzerner Konzept und Resultate Philipp Gut 1.5.2010-30.10.13 LUKS Number of Patients Lokal radikale Radiotherapie von Overall survival Patienten mit Hirnmetastasen
cyberknife center hamburg
 cyberknife center hamburg Interdisziplinäres DGNC / DEGRO Update Symposium: Aktuelle Behandlung zerebraler Metastasen Einfluss-Faktoren auf die Prognose von Patienten mit Hirnmetastasen Dr. med. Stefan
cyberknife center hamburg Interdisziplinäres DGNC / DEGRO Update Symposium: Aktuelle Behandlung zerebraler Metastasen Einfluss-Faktoren auf die Prognose von Patienten mit Hirnmetastasen Dr. med. Stefan
2nd surgery in recurrent glioblastoma: when and why?
 CAMPUS GROSSHADERN NEUROCHIRURGISCHE KLINIK UND POLIKLINIK INTERNET: NEUROCHIRURGIE.KLINIKUM.UNI-MUENCHEN.DE 2nd surgery in recurrent glioblastoma: when and why? Jörg-Christian Tonn Dept Neurosurgery University
CAMPUS GROSSHADERN NEUROCHIRURGISCHE KLINIK UND POLIKLINIK INTERNET: NEUROCHIRURGIE.KLINIKUM.UNI-MUENCHEN.DE 2nd surgery in recurrent glioblastoma: when and why? Jörg-Christian Tonn Dept Neurosurgery University
Einfluss der Niedrigdosisbelastung (V10) auf das Pneumonitisrisiko bei thorakaler Bestrahlung
 Einfluss der Niedrigdosisbelastung (V10) auf das Pneumonitisrisiko bei thorakaler Bestrahlung M. Becker-Schiebe 1, M. Renz 1, H. Christiansen 2, W. Hoffmann 1 1 Klinik für Radioonkologie und Strahlentherapie
Einfluss der Niedrigdosisbelastung (V10) auf das Pneumonitisrisiko bei thorakaler Bestrahlung M. Becker-Schiebe 1, M. Renz 1, H. Christiansen 2, W. Hoffmann 1 1 Klinik für Radioonkologie und Strahlentherapie
Thomas G. Wendt. Universitäts- Klinikum Jena
 Thomas G. Wendt 1. Meningeom 2. Hypophysenadenom, Craniopharyngeom 3. Akusticusneurinom = Vestibularisschwannom Diagnostik: Größe und Lage des Tumors sowie Beziehung zu Nachbarorganen: MRT, in Einzelfällen
Thomas G. Wendt 1. Meningeom 2. Hypophysenadenom, Craniopharyngeom 3. Akusticusneurinom = Vestibularisschwannom Diagnostik: Größe und Lage des Tumors sowie Beziehung zu Nachbarorganen: MRT, in Einzelfällen
Wintersemester 2014/2015
 Wintersemester 2014/2015 Weichteilsarkome Extremitäten, retroperitonäal, sehr selten Gesicht Sarkome Knochen und Knorpel (Osteosarkom, Chondrosakrom) Ewingsarkom (prädominant im Kindesalter) präoperativ
Wintersemester 2014/2015 Weichteilsarkome Extremitäten, retroperitonäal, sehr selten Gesicht Sarkome Knochen und Knorpel (Osteosarkom, Chondrosakrom) Ewingsarkom (prädominant im Kindesalter) präoperativ
Gliatumoren WHO-Klassifikation Malignitätsgrad III IV. Astrozytäre Tumoren Anaplastisches Astrozytom + Oligodendrogliom.
 Maligne Gliome Autor: Berthold Steinke 1. Definition und Basisinformation Als primäre Hirntumoren werden benigne und maligne Tumoren bezeichnet, die von Zellen des Gehirns oder der Meningen ausgehen, nicht
Maligne Gliome Autor: Berthold Steinke 1. Definition und Basisinformation Als primäre Hirntumoren werden benigne und maligne Tumoren bezeichnet, die von Zellen des Gehirns oder der Meningen ausgehen, nicht
Mesotheliom-therapeutische Optionen
 Mesotheliom-therapeutische Optionen Wolfgang Schütte Krankenhaus Martha-Maria Halle-Dölau Staging beim malignen Pleuramesotheliom International Mesotheliom Interest Group - IMIG 1 Erguß 2 Pleuratumor 3
Mesotheliom-therapeutische Optionen Wolfgang Schütte Krankenhaus Martha-Maria Halle-Dölau Staging beim malignen Pleuramesotheliom International Mesotheliom Interest Group - IMIG 1 Erguß 2 Pleuratumor 3
Lokalisiertes Prostatakarzinom: high risk Prostatakarzinom, nodal positives Prostatakarzinom. aus radioonkologischer Sicht
 November 2013 St.Gallen Lokalisiertes Prostatakarzinom: high risk Prostatakarzinom, nodal positives Prostatakarzinom aus radioonkologischer Sicht Gregor Goldner Medizinische Universität Wien lokalisiertes
November 2013 St.Gallen Lokalisiertes Prostatakarzinom: high risk Prostatakarzinom, nodal positives Prostatakarzinom aus radioonkologischer Sicht Gregor Goldner Medizinische Universität Wien lokalisiertes
University of Zurich. Strukturen neuroonkologischer Wissenschaft und Versorgung. Zurich Open Repository and Archive. Wick, W; Weller, M.
 University of Zurich Zurich Open Repository and Archive Winterthurerstr. 190 CH-8057 Zurich Year: 2010 Strukturen neuroonkologischer Wissenschaft und Versorgung Wick, W; Weller, M Wick, W; Weller, M (2010).
University of Zurich Zurich Open Repository and Archive Winterthurerstr. 190 CH-8057 Zurich Year: 2010 Strukturen neuroonkologischer Wissenschaft und Versorgung Wick, W; Weller, M Wick, W; Weller, M (2010).
Lokal ablative Therapieverfahren bei oligometastasiertem Pankreaskarzinom:
 DEGRO AG_Frankfurt_2017 Lokal ablative Therapieverfahren bei oligometastasiertem Pankreaskarzinom: Non sense oder Konsens? Dr. med. S. Gerum Klinik und Poliklinik für Strahlentherapie und Radioonkologie
DEGRO AG_Frankfurt_2017 Lokal ablative Therapieverfahren bei oligometastasiertem Pankreaskarzinom: Non sense oder Konsens? Dr. med. S. Gerum Klinik und Poliklinik für Strahlentherapie und Radioonkologie
F. Jentzmik, T. Wiegel, R. Hefty, A.J. Schrader, T.J. Schnöller Universitätsklinikum Ulm Urologie und Kinderurologie 1
 Salvage-Lymphadenektomie vs. Salvage- Lymphadenektomie in Kombination mit adjuvanter Radiatio und Androgenrezeptorblockade beim Prostatakarzinomrezidiv F. Jentzmik, T. Wiegel, R. Hefty, A.J. Schrader,
Salvage-Lymphadenektomie vs. Salvage- Lymphadenektomie in Kombination mit adjuvanter Radiatio und Androgenrezeptorblockade beim Prostatakarzinomrezidiv F. Jentzmik, T. Wiegel, R. Hefty, A.J. Schrader,
Biomarker beim KRK was kommt als nächstes in die Klinik?
 GI Oncology 2010 6. Interdisziplinäres Update 3. Juli 2010 Biomarker beim KRK was kommt als nächstes in die Klinik? Thomas Seufferlein Klinik für Innere Medizin I Martin-Luther-Universität Halle-Wittenberg
GI Oncology 2010 6. Interdisziplinäres Update 3. Juli 2010 Biomarker beim KRK was kommt als nächstes in die Klinik? Thomas Seufferlein Klinik für Innere Medizin I Martin-Luther-Universität Halle-Wittenberg
PRO Operation: Indikation, wann und mit welcher Technik?
 PRO Operation: Indikation, wann und mit welcher Technik? Prof. Dr. W. med. Stummer Neurochirurgische Klinik Hintumorzentrum Münster Univeristätsklinikum Münster Therapiemodalitäten: Konkurrenz oder Ergänzung?
PRO Operation: Indikation, wann und mit welcher Technik? Prof. Dr. W. med. Stummer Neurochirurgische Klinik Hintumorzentrum Münster Univeristätsklinikum Münster Therapiemodalitäten: Konkurrenz oder Ergänzung?
Medikamentöse Therapie der Neuroendokrinen Neoplasien
 Medikamentöse Therapie der Neuroendokrinen Neoplasien Medikamentöse Therapie der GIST und NET Einführung NET Prof. Dr. Tilo Andus Stuttgart, 21.02.2017 Therapierelevante Untergruppen Palliative Therapie:
Medikamentöse Therapie der Neuroendokrinen Neoplasien Medikamentöse Therapie der GIST und NET Einführung NET Prof. Dr. Tilo Andus Stuttgart, 21.02.2017 Therapierelevante Untergruppen Palliative Therapie:
Radio-(Chemo)-Therapie. des Rektumkarzinoms
 Radio-(Chemo)-Therapie des Rektumkarzinoms A. Liebmann 17.01.2012 Häufigkeitsverteilung Tumorausbreitung CT : tiefsitzendes Rektumkarzinom mit pararektaler LK-Metastase Chirurgie des Mesorektums Indikationen
Radio-(Chemo)-Therapie des Rektumkarzinoms A. Liebmann 17.01.2012 Häufigkeitsverteilung Tumorausbreitung CT : tiefsitzendes Rektumkarzinom mit pararektaler LK-Metastase Chirurgie des Mesorektums Indikationen
Kardiale Toxizität beim Mamma-Ca
 Kardiale Toxizität beim Mamma-Ca René Baumann, Jürgen Dunst Klinik für Strahlentherapie Christian-Albrechts-Universität Kiel/ UKSH Kiel seit 350 Jahren ganz weit oben 1. Daten aus historischen Studien
Kardiale Toxizität beim Mamma-Ca René Baumann, Jürgen Dunst Klinik für Strahlentherapie Christian-Albrechts-Universität Kiel/ UKSH Kiel seit 350 Jahren ganz weit oben 1. Daten aus historischen Studien
DIAGNOSTIK UND BEHANDLUNG VON NIERENTUMOREN. Norbert Graf
 DIAGNOSTIK UND BEHANDLUNG VON NIERENTUMOREN Norbert Graf Nierentumoren WT mit Metastasen 10% WT bilateral 7% Andere 11% CMN 3% CCSK 3% MRTK 1% WT lokalisiert 72% Andere 4% gutartig
DIAGNOSTIK UND BEHANDLUNG VON NIERENTUMOREN Norbert Graf Nierentumoren WT mit Metastasen 10% WT bilateral 7% Andere 11% CMN 3% CCSK 3% MRTK 1% WT lokalisiert 72% Andere 4% gutartig
Kolorektales Karzinom
 ASCO - Highlights Kolorektales Karzinom Henning Schulze-Bergkamen Nationales Centrum für Tumorerkrankungen (NCT) Abt. für Medizinische Onkologie Universitätsklinik Heidelberg ASCO Highlights Kolorektale
ASCO - Highlights Kolorektales Karzinom Henning Schulze-Bergkamen Nationales Centrum für Tumorerkrankungen (NCT) Abt. für Medizinische Onkologie Universitätsklinik Heidelberg ASCO Highlights Kolorektale
AGO-OVAR 19 / TRUST. (platinfreies Intervall 6-12 Monate) Intermediär-platinsensibles Rezidiv. Erstdiagnose FIGO IIIB-IV
 Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
Diagnostik und Therapie primärer und metastasierter Mammakarzinome
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome ZNS-Metastasen beim Mammakarzinom ZNS-Metastasen beim Mammakarzinom AGO e.v. in der DGGG e.v. Guidelines Version 2010.1.1 Breast D Version
Diagnostik und Therapie primärer und metastasierter Mammakarzinome ZNS-Metastasen beim Mammakarzinom ZNS-Metastasen beim Mammakarzinom AGO e.v. in der DGGG e.v. Guidelines Version 2010.1.1 Breast D Version
Radio-/Chemotherapie beim fortgeschrittenen Harnblasenkarzinom Blasenerhalt und Lebensqualität
 KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radio-/Chemotherapie beim fortgeschrittenen Harnblasenkarzinom Blasenerhalt und Lebensqualität T2 4a Harnblasenkarzinom
KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radio-/Chemotherapie beim fortgeschrittenen Harnblasenkarzinom Blasenerhalt und Lebensqualität T2 4a Harnblasenkarzinom
Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC
 SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Symptomatik bei Hirntumoren
 Symptomatik bei Hirntumoren fokal-neurologische Defizite sensomotorische Hemiparese, Hemianopsie Hirndrucksymptome Kopfschmerzen, Übelkeit/Erbrechen organisches Psychosyndrom Verlangsamung, reduzierte
Symptomatik bei Hirntumoren fokal-neurologische Defizite sensomotorische Hemiparese, Hemianopsie Hirndrucksymptome Kopfschmerzen, Übelkeit/Erbrechen organisches Psychosyndrom Verlangsamung, reduzierte
Update Radiotherapie beim Kleinzelligen Lungenkarzinom SCLC
 Klinik für Strahlentherapie und Radioonkologie Update Radiotherapie beim Kleinzelligen Lungenkarzinom SCLC Frank Zimmermann frank.zimmermann@usb.ch Universitätsspital Basel Übersicht Technik der Strahlentherapie
Klinik für Strahlentherapie und Radioonkologie Update Radiotherapie beim Kleinzelligen Lungenkarzinom SCLC Frank Zimmermann frank.zimmermann@usb.ch Universitätsspital Basel Übersicht Technik der Strahlentherapie
Aktuelle Therapiekonzepte bei GIST
 Aktuelle Therapiekonzepte bei GIST Sebastian Bauer Innere Klinik (Tumorforschung) Sarkomzentrum Übersicht Adjuvante Therapie Systemtherapie metastasierte Erkrankung Aktuelle Studien Folie 2 2 04.08.2014
Aktuelle Therapiekonzepte bei GIST Sebastian Bauer Innere Klinik (Tumorforschung) Sarkomzentrum Übersicht Adjuvante Therapie Systemtherapie metastasierte Erkrankung Aktuelle Studien Folie 2 2 04.08.2014
Erfolge der Immuntherapie beim Lungenkrebs. Martin Früh Klinik für Onkologie und Hämatologie Kantonsspital St. Gallen
 Erfolge der Immuntherapie beim Lungenkrebs Martin Früh Klinik für Onkologie und Hämatologie Kantonsspital St. Gallen Weltweite Krebsstatistik 2012 (Industrieländer) Neuerkrankungen/Jahr Mortalität/Jahr
Erfolge der Immuntherapie beim Lungenkrebs Martin Früh Klinik für Onkologie und Hämatologie Kantonsspital St. Gallen Weltweite Krebsstatistik 2012 (Industrieländer) Neuerkrankungen/Jahr Mortalität/Jahr
Lokale Therapie des Prostatatumors (durch OP oder RT) bei Patienten mit metastasiertem Prostata-Ca
 seit 350 Jahren ganz weit oben Lokale Therapie des Prostatatumors (durch OP oder RT) bei Patienten mit metastasiertem Prostata-Ca Prof. Dr. Jürgen Dunst & Dr. René Baumann Klinik für Strahlentherapie,
seit 350 Jahren ganz weit oben Lokale Therapie des Prostatatumors (durch OP oder RT) bei Patienten mit metastasiertem Prostata-Ca Prof. Dr. Jürgen Dunst & Dr. René Baumann Klinik für Strahlentherapie,
Neue Konzepte in der Strahlentherapie des Prostatakarzinoms
 KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Neue Konzepte in der Strahlentherapie des Prostatakarzinoms Anforderungen an eine optimale Radiotherapie Dosis
KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Neue Konzepte in der Strahlentherapie des Prostatakarzinoms Anforderungen an eine optimale Radiotherapie Dosis
Chemoimmuntherapie mit Rituximab: Standard bei der CLL sowie beim aggressiven und follikulären NHL
 Neue Maßstäbe in der Lymphomtherapie Chemoimmuntherapie mit Rituximab: Standard bei der CLL sowie beim aggressiven und follikulären NHL Mannheim (2. Oktober 2009) - Der monoklonale Antikörper Rituximab
Neue Maßstäbe in der Lymphomtherapie Chemoimmuntherapie mit Rituximab: Standard bei der CLL sowie beim aggressiven und follikulären NHL Mannheim (2. Oktober 2009) - Der monoklonale Antikörper Rituximab
Perioperative und paliative Therapie des Ösophaguskarzinoms - Standards und neue Studien -
 GI Oncology 2012 8. Interdisziplinäres Update, 7. Juli 2012 Perioperative und paliative Therapie des Ösophaguskarzinoms - Standards und neue Studien - Florian Lordick Klinikum Braunschweig Medizinische
GI Oncology 2012 8. Interdisziplinäres Update, 7. Juli 2012 Perioperative und paliative Therapie des Ösophaguskarzinoms - Standards und neue Studien - Florian Lordick Klinikum Braunschweig Medizinische
Radiotherapie des Mamma-Karzinom Konzepte Dr. med. Kirsten Steinauer
 Radiotherapie des Mamma-Karzinom Konzepte 2012 27.9.2012 Dr. med. Kirsten Steinauer 2 Wo befinden sich die Tumorzellen - und wie viele sind es? Radiotherapie bei brusterhaltender Therapie Standard: < 65
Radiotherapie des Mamma-Karzinom Konzepte 2012 27.9.2012 Dr. med. Kirsten Steinauer 2 Wo befinden sich die Tumorzellen - und wie viele sind es? Radiotherapie bei brusterhaltender Therapie Standard: < 65
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version 2002: Gerber / Friedrichs
Therapie der älteren Patientin
 Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
Management von Hirnmetastasen beim Lungenkarzinom
 Management von Hirnmetastasen beim Lungenkarzinom Roland Goldbrunner 01.10.2017 Jahrestagung DGHO Roland Goldbrunner Zentrum für Neurochirurgie Offenlegungen MagForce Advisory Board Glioblastome Bristol
Management von Hirnmetastasen beim Lungenkarzinom Roland Goldbrunner 01.10.2017 Jahrestagung DGHO Roland Goldbrunner Zentrum für Neurochirurgie Offenlegungen MagForce Advisory Board Glioblastome Bristol
Hirntumore - Was taugen MRT- Bilder und radiologische Befunde?
 Hirntumore - Was taugen MRT- Bilder und radiologische Befunde? G.Schuierer Zentrum Neuroradiologie des Universitätsklinikums und des Bezirksklinikums Regensburg Hirntumore - Was taugen MRT- Bilder und
Hirntumore - Was taugen MRT- Bilder und radiologische Befunde? G.Schuierer Zentrum Neuroradiologie des Universitätsklinikums und des Bezirksklinikums Regensburg Hirntumore - Was taugen MRT- Bilder und
Neue Standards der endokrinen Therapie Dr. Andreas Müller
 Neue Standards der endokrinen Therapie Dr. Andreas Müller Chefarzt Med. Onkologie (Speziell Brust- und Gynäkologische Onkologie) Ein alter Standard: wo ist die Grenze für ER-positiv? 0% 1% 10% 33% 66%
Neue Standards der endokrinen Therapie Dr. Andreas Müller Chefarzt Med. Onkologie (Speziell Brust- und Gynäkologische Onkologie) Ein alter Standard: wo ist die Grenze für ER-positiv? 0% 1% 10% 33% 66%
Bronchialkarzinom und Strahlentherapie: Downstaging, PCI, Radio-/Chemotherapie
 Bronchialkarzinom und Strahlentherapie: Downstaging, PCI, Radio-/Chemotherapie G. Klautke Klinik und Poliklinik für Strahlentherapie Universität Rostock Das kleinzellige Lungenkarzinom SCLC limited disease
Bronchialkarzinom und Strahlentherapie: Downstaging, PCI, Radio-/Chemotherapie G. Klautke Klinik und Poliklinik für Strahlentherapie Universität Rostock Das kleinzellige Lungenkarzinom SCLC limited disease
Second-line Chemotherapie
 Second-line Chemotherapie des metastasierten Urothelkarzinoms Übersicht First-line Standardtherapie Second-line Therapie: Vinflunin Second-line Therapie: Gemcitabin/Paclitaxel Second-line Therapie: Studie
Second-line Chemotherapie des metastasierten Urothelkarzinoms Übersicht First-line Standardtherapie Second-line Therapie: Vinflunin Second-line Therapie: Gemcitabin/Paclitaxel Second-line Therapie: Studie
kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ
 WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
Analyse von Ereignisdaten Univ.-Prof. DI Dr. Andrea Berghold Institut für Med. Informatik, Statistik und Dokumentation
 Analyse von Ereignisdaten Univ.-Prof. DI Dr. Andrea Berghold Institut für Med. Informatik, Statistik und Dokumentation Analyse von Ereigniszeiten Lebensdauer = Zeit zwischen einem Startpunkt (Anfangsdatum)
Analyse von Ereignisdaten Univ.-Prof. DI Dr. Andrea Berghold Institut für Med. Informatik, Statistik und Dokumentation Analyse von Ereigniszeiten Lebensdauer = Zeit zwischen einem Startpunkt (Anfangsdatum)
date Adjuvant Pegylated- Interferonalpha2b
 Organ/Bereich Krankheit Stadium Kurztitel Studie/ClinicalTrials.gov Identifier: Hauttumore Melanom ulzeriertes primäres kutanes Melanom T(2-4)b N0 M0) Hauttumore Melanom nicht vorbehandeltes, nicht reseziertes
Organ/Bereich Krankheit Stadium Kurztitel Studie/ClinicalTrials.gov Identifier: Hauttumore Melanom ulzeriertes primäres kutanes Melanom T(2-4)b N0 M0) Hauttumore Melanom nicht vorbehandeltes, nicht reseziertes
So gut wie noch nie und bei jedem Tumortyp: Heilung und Palliation mit perfekter Strahlentherapie
 So gut wie noch nie und bei jedem Tumortyp: Heilung und Palliation mit perfekter Strahlentherapie Klinik für Strahlentherapie und Radioonkologie und MVZ Lörrach Prof. Dr. Frank Zimmermann und Mitarbeiter
So gut wie noch nie und bei jedem Tumortyp: Heilung und Palliation mit perfekter Strahlentherapie Klinik für Strahlentherapie und Radioonkologie und MVZ Lörrach Prof. Dr. Frank Zimmermann und Mitarbeiter
Radiotherapie beim Prostatakarzinom. Teil 2 : Dosis-Wirkungsbeziehungen
 KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie beim Prostatakarzinom Teil 2 : Dosis-Wirkungsbeziehungen Schambein Tumor Fettgewebe Enddarm Harnblase
KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie beim Prostatakarzinom Teil 2 : Dosis-Wirkungsbeziehungen Schambein Tumor Fettgewebe Enddarm Harnblase
Palliative Therapien des Mammakarzinoms Neue Entwicklungen
 Wissenschaftliches Symposium der Sächsischen Krebsgesellschaft 13. November 2010, Machern Palliative Therapien des s Neue Entwicklungen Metastasiertes Behandlungsstrategie beim metastasierten * *Heinemann
Wissenschaftliches Symposium der Sächsischen Krebsgesellschaft 13. November 2010, Machern Palliative Therapien des s Neue Entwicklungen Metastasiertes Behandlungsstrategie beim metastasierten * *Heinemann
Aktuelle Aspekte zur Chemotherapie beim Ovarialkarzinomrezidiv
 Ovarialkarzinomrezidiv Aktuelle Aspekte zur Chemotherapie beim Ovarialkarzinomrezidiv M. Gropp-Meier Leitlinie: 5th OCCC November 2015 Entscheidungskriterien: Rezidivzeitpunkt in Relation zur letzten Therapie
Ovarialkarzinomrezidiv Aktuelle Aspekte zur Chemotherapie beim Ovarialkarzinomrezidiv M. Gropp-Meier Leitlinie: 5th OCCC November 2015 Entscheidungskriterien: Rezidivzeitpunkt in Relation zur letzten Therapie
