Antimikrobielle Therapie der Sepsis
|
|
|
- Sofia Vogel
- vor 7 Jahren
- Abrufe
Transkript
1 PEG-Empfehlungen Antimikrobielle Therapie der Sepsis Empfehlungen einer Arbeitsgruppe der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Klaus-Friedrich Bodmann und Friedrich Vogel unter Mitarbeit von Wolfgang Graninger, Michael Kresken, W. Dieter Paar, Georg Peters, Ernst Rietschel, Harald Seifert, Pramod Shah, Fritz Sörgel, Wolfgang Stille, Christian Tauchnitz, Matthias Trautmann, Uwe Ullmann, Hannes Wacha, Bernd Wiedemann Die Therapie der Sepsis stellt für den klinisch tätigen Arzt eine der größten Herausforderungen dar. Insbesondere im Bereich der Intensivmedizin kommt der Sepsis und dem septischen Schock aufgrund der unverändert hohen Letalität von 40 bis 60 % eine besondere Bedeutung zu. Die Inzidenz der Sepsis beträgt etwa 5 bis 15 Erkrankungen auf 1000 Krankenhauspatienten. Die Inzidenz der Sepsis-Fälle im Bereich der Intensivpatienten wird in der Literatur mit 3 bis 5 % angegeben. Es werden jedoch auch höhere Inzidenzzahlen genannt. Hierfür sind die unterschiedlichen Kriterien der Sepsis-Diagnose und -Definition sowie die Zusammensetzung des Krankengutes hinsichtlich der Grundleiden verantwortlich zu machen. Zu den prädisponierenden Erkrankungen gehören alle Formen der Abwehrschwäche, zum Beispiel Tumorleiden, Diabetes mellitus, Nieren-, Lebererkrankungen und Hämoblastosen, im Bereich der operativen Intensivmedizin zum Beispiel Polytraumen, Verbrennungen und große risikoreiche Eingriffe. Die wirksame antimikrobielle Therapie stellt die wichtigste Behandlungsoption dar. Sie wird ergänzt durch die allgemeine Intensivtherapie und gegebenenfalls durch eine Sanierung der Infektionsquelle. Die Erarbeitung eines antimikrobiellen Therapiekonzeptes der Sepsis war bereits das Ziel der Expertenkommission der Paul-Ehrlich-Gesellschaft (PEG) in ihrer Publikation zur parenteralen Antibiotika-Therapie aus dem Jahre In der vorliegenden Empfehlung sind die Ergebnisse einer Expertenkommission der PEG komplettiert und aktualisiert zusammengefasst. Es wurden die aktuelle Resistenzsituation sowie neue Antiinfektiva und Studienergebnisse berücksichtigt. Schlüsselwörter: Sepsis, Antiinfektiva, Therapie Einleitung Die klassische Definition der Sepsis geht auf Schottmüller aus dem Jahre 1914 zurück: Eine Sepsis liegt dann vor, wenn sich innerhalb des Körpers ein Herd gebildet hat, von dem konstant oder periodisch pathogene Bakterien in den Blutkreislauf gelangen und zwar derart, dass durch diese Invasion subjektive und objektive Krankheitserscheinungen ausgelöst werden. Spätere Sepsisdefinitionen haben die Erstdefinition Schottmüllers zwar variiert, aber nicht wesentlich verändert. Nach dem heutigen Kenntnisstand erscheint die mikrobielle Sepsis am besten in der Formulierung von Schuster beschrieben: Sepsis ist die Gesamtheit der lebensbedrohlichen klinischen Krankheitserscheinungen und pathophysiologischen Veränderungen als Reaktion auf die Aktion pathogener Erreger und ihrer Produkte, die aus einem Infektionsherd in den Blutstrom eindringen, die großen biologischen Kaskadensysteme und spezielle Zellsysteme aktivieren und die Bildung und Freisetzung humoraler und zellulärer Mediatoren auslösen. Diese Definition stützt sich auf die fünf Grundpfeiler des schweren septischen Krankheitsprozesses: Die septische Infektionsquelle als Ausgangspunkt, die Invasion von Mikroorganismen, die Freisetzung ihrer Bestandteile oder Toxine, die Ausschüttung von Mediatoren, Zellfunktionsstörungen und morphologische Destruktion von Zellmembranen und Konsensus-Konferenz Sepsis der PEG Die Empfehlungen zur antimikrobiellen Therapie der Sepsis wurden in mehreren Schritten erarbeitet. Organisation und Koordination lagen in den Händen von Klaus-Friedrich Bodmann und Friedrich Vogel. Am 8./9. September 2000 traf sich die Arbeitsgruppe bestehend aus Dr. Klaus- Friedrich Bodmann, Prof. Dr. Friedrich Vogel,Priv.-Doz. Dr. Dieter Paar und Prof. Dr. Matthias Trautmann zur Erarbeitung eines ersten Entwurfs, der Grundlage der großen Konsensuskonferenz am 20./21. Oktober 2000 in Bensberg war. Teilnehmer: Dr. med. Klaus-Friedrich Bodmann, Hildesheim, Dr. med. Josef Focht, Moers, Dr. med. Andreas Göpfert, Lahr, Dr. med. Beatrice Grabein, Eurasburg, Dr. Norbert Gustke, Hamburg, Dr. med. Matthias Heimesaat, Berlin, Dr. Kora Huber, Hamburg, Prof. Dr. med. Fritz H. Kayser, Zürich, Dr. Michael Kresken, Bonn, Dr. rer. nat. Cordula Lebert, Nürnberg, Dr. Matthias Liebscher, Dresden, Dipl.-Biol. Konstanze Machka, München, Priv.-Doz. Dr. med. Dieter Paar, Bonn, Priv.-Doz. Dr. med. Harald Seifert, Köln, Prof. Dr. med. Wolfgang Stille, Frankfurt, Hans-Joachim Stodt, Münster, Dr. rer. nat. Egid Strehl, Freiburg, Dr. med. Helmut Tassler, Dortmund, Prof. Dr. med. Christian Tauchnitz, Leipzig, Prof. Dr. med. Matthias Trautmann, Ulm, Prof. Dr. med. Uwe Ullmann, Kiel, Prof. Dr. med. Friedrich Vogel, Hofheim, Prof. Dr. med. Hannes Wacha, Frankfurt, Dr. med. Rudolf Weiss, Offenbach, Dr. med. Lutz Zabel, Tübingen Die bei der großen Konsensuskonferenz erarbeitete Fassung wurde nochmals allen Teilnehmern und Vorstandsmitgliedern der PEG zugesandt. Nach Einarbeitung weiterer Anregungen wurden zwei Gutachter hinzugezogen, deren Anregungen in der Endfassung ebenfalls berücksichtigt sind. Für die Verfasser: Dr. med. Klaus-Friedrich Bodmann, Medizinische Klinik I, Städtisches Krankenhaus, Weinberg 1, Hildesheim ChemotherapieJournal 10. Jahrgang Heft 2/
2 Zellstrukturen als Grundlage der Organschädigung und die Multiorganinsuffizienz, als deren klinischer Ausdruck das Multiorganversagen. Die allgemein anerkannten Kriterien zur Diagnose der Sepsis bestehen aus dem Nachweis einer Infektion und den vier nachfolgenden Kriterien: 1. Fieber über 38 C oder in seltenen Fällen Hypothermie unter 36 C 2. Tachypnoe über 20/min oder Hypokapnie mit einem PaCO 2 < 32 mm Hg 3. Tachykardie über 90/min 4. Leukozytose über oder Leukopenie unter 4 000/mm 3 Septische Zustandsbilder werden gemäß der amerikanischen Konsensus- Definition in verschiedene klinische Schweregrade eingeteilt. 1. SIRS (Systemic Inflammatory Response Syndrome): Das SIRS ist eine allgemeine, entzündliche Abwehrreaktion auf unterschiedliche Krankheitsbilder (z. B. Trauma, Hypoxie, Pankreatitis), die durch mindestens zwei der oben genannten Kriterien gekennzeichnet ist, ohne dass eine Infektion vorliegen muss. 2. Sepsis: Die Sepsis ist die systemische Reaktion auf eine Infektion. Wie beim SIRS müssen mindestens zwei der oben genannten Kriterien vorliegen. Der international erarbeitete Konsens definiert Sepsis somit ohne Vorliegen einer Organdysfunktion. 3. Schwere Sepsis: Hier liegen zusätzlich zur Sepsis Symptome eines Organversagens der Lunge (Hypoxie, respiratorische Azidose), Niere (Oligurie/Anurie, metabolische Azidose), Leber (z. B. Ikterus) und/oder des Herzens (Herzinsuffizienz) vor. Aber auch ZNS, Gastrointestinaltrakt, Knochenmark, Gerinnungs- und Immunsystem können betroffen sein. Aus intensivmedizinischer Sicht wird von einer Sepsis im Gegensatz zur internationalen Konsensusempfehlung erst dann gesprochen, wenn Symptome eines zusätzlichen Organversagen bestehen. Auch die vorliegenden Empfehlungen zur antimikrobiellen Therapie beziehen sich auf schwer kranke Patienten mit Organdysfunktion. 4. Septischer Schock: Der septische Schock geht mit anhaltendem Blutdruckabfall trotz ausreichender Flüssigkeitszufuhr einher. Ein therapierefraktärer septischer Schock liegt vor, wenn der Blutdruckabfall länger als eine Stunde dauert und sich durch Flüssigkeitszufuhr und Einsatz von Vasopressoren nicht beheben lässt. Die pathophysiologischen Erkenntnisse der vergangenen Jahre zeigen, dass septische Zustandsbilder durch ein kompliziertes Netzwerk pro- und antiinflammatorischer Zytokine bedingt sind. Im Anschluss an die proinflammatorische Phase des SIRS werden vermehrt Zytokine mit antiinflammatorischer Wirkung gebildet. Diese Phase wird als CARS (compensatory anti-inflammatory response syndrome) bezeichnet. Oftmals überlappen sich beim Patienten SIRSund CARS-Phasen, dann wird von einem mixed antagonistic response syndrome gesprochen (MARS). Das Sepsis-Geschehen ist ein dynamischer Prozess des Übergangs vom Stadium der einfachen Sepsis zur schweren Sepsis bzw. in den septischen Schock mit Organdysfunktion bzw. Organversagen, aber auch der Entwicklung von septischen Organabsiedlungen. Aufgrund der neuen Erkenntnisse zur Zytokin-Pathogenese septischer Zustandsbilder wurden umfangreiche Untersuchungen mit Anti-Zytokin-Behandlungsstrategien der Sepsis durchgeführt. Bisher konnte allerdings in keiner der zahlreichen großen kontrollierten Studien mit Mediatorblockade eine Reduktion der Letalität gezeigt werden. Auch Therapieansätze mit Endotoxin-bindenden Proteinen oder Endotoxin-Antikörpern waren trotz vielversprechender Ansätze bisher nicht in weitem Umfang klinisch erfolgreich. Auch die Gabe von Immunglobulinen kann trotz Hinweisen auf Effektivität in einer Metaanalyse derzeit nicht als gesichert angesehen werden. Große Hoffnungen wurden ebenfalls in die Gabe von Antithrombin-III als potentem Inhibitor der Fibringenerierung gesetzt. Aber auch erste Ergebnisse größerer kontrollierter Studien zeigen keinen eindeutigen Vorteil. Diese Ergebnisse verdeutlichen, dass die rasche Diagnose der Sepsis (Blutkultur) und eine unverzüglich eingeleitete, effektive antimikrobielle Therapie die entscheidende Bedeutung für das Überleben der Patienten haben. Standard-Verlaufsparameter ist das C- reaktive Protein (CRP). Neue diagnostische Marker septischer Zustandsbilder sind Procalcitonin und Komplementspaltprodukt C3a. Erste Befunde zur Differenzierung der Sepsis-Schweregrade und als Verlaufsparameter sind vielversprechend. Bis zur Vorlage großer kontrollierter Studien scheint die im Vergleich zur Bestimmung von CRP deutlich teurere routinemäßige Bestimmung von Procalcitonin allerdings noch nicht gerechtfertigt. Damit eine effektive kalkulierte Therapie im Sinne der Interventionstherapie eingeleitet werden kann, sind Kenntnisse über das Erregerspektrum, die Erregerhäufigkeit je nach Infektionslokalisation und die Resistenzsituation erforderlich. Mikrobiologie und aktuelle Resistenzsituation Die aktuellen Empfehlungen zur Blutkulturdiagnostik wurden kürzlich im Rahmen der MiQ-Richtlinien (Qualitätsstandard in der mikrobiologisch-infektiologischen Diagnostik der Deutschen Gesellschaft für Hygiene und Mikrobiologie, DGHM) publiziert. Dort finden sich genaue Angaben zum optimalen Zeitpunkt der Entnahme von Blutkulturen, zum Entnahmeort, zur Vorgehensweise bei der Venenpunktion sowie zum Probentransport und zur Verarbeitung mit und ohne automatisches Detektionssystem. Bei der Abnahme von Blutkulturen möglichst vor Beginn der Antibiotika- Therapie sind vor allem folgende Punkte zu beachten: Auswahl der Punktionsstelle Hygienische Händedesinfektion Wisch- oder Sprühdesinfektion der Haut auf einem mindestens 5 x 5 cm großen Areal mit alkoholischem Desinfektionsmittel, Einwirkzeit 1 min. Zweite Hautdesinfektion von innen nach außen mit sterilem Tupfer Anlegen von Einmalhandschuhen Keine erneute Palpation der Punktionsstelle Venenpunktion und Entnahme von 5 bis 10 ml Blut pro Blutkulturflasche Alkoholische Wischdesinfektion des Durchstichstopfens der Blutkulturflaschen Trocknung des Desinfektionsmittels abwarten Blutkulturflaschen mit jeweils frischer Kanüle beimpfen Keine Belüftung der aeroben Flasche vornehmen Blutkulturflaschen bis zum Transport ins Labor bei 37 C lagern Das aktuelle Spektrum der Sepsis-Erreger und Angaben zum Wandel des Erregerspektrum ergeben sich sowohl aus der MiQ-Richtlinie als auch aus aktuel Jahrgang Heft 2/2001
3 Tab. 1. Erregerspektrum der Sepsis: prozentualer Anteil einzelner Erregerspezies Spezies Rosenthal et al., Geerdes et al., Trautmann et al, Moser et al Staphylococcus aureus 20,4 17,4 18,8 15,1 Koagulase-negative Staphylokokken 9,3 9,5 23,9 14,1 Enterokokken 5,5 7,1 7,5 6,1 Streptococcus spp. 12,4 14,1 3,4 13,2 Escherichia coli 23,9 24,2 10,9 13,6 Enterobacter spp. 3,6 3,8 4,8 4,8 Klebsiella spp. 5,4 5,1 4,4 5,8 Pseudomonas aeruginosa 4,2 3,8 4,4 5,0 Stenotrophomonas maltophilia n.a. 0,3 2,0 1,7 Candida spp. 1,3 3,3 3,8 3,7 1 Blutkulturdaten, 2 Klinisch validierte Sepsis len Übersichten. Bei der Analyse der Daten ist jeweils zu berücksichtigen, dass in einigen Studien lediglich Blutkulturdaten ausgewertet wurden, während in anderen Studien nur Patienten eingeschlossen wurden, bei denen das Vorliegen einer klinischen Sepsis durch Anwendung der CDC-Kriterien oder anderer Sepsis-Kriterien definitiv bestätigt wurde. Tabelle 1 zeigt eine Übersicht über das aktuelle Erregerspektrum der Sepsis aus verschiedenen Studien der 90er Jahre. Aus diesen Daten ergibt sich, dass grampositive und gramnegative Erreger derzeit etwa gleich häufig vorkommen. Die in einigen Institutionen und Studien festgestellte Zunahme der grampositiven Sepsis-Erreger hängt stark von der Bewertung des Nachweises Koagulase-negativer Staphylokokken in Blutkulturen ab. In der Studie von Trautmann et al. wurde bereits der Nachweis von KNS in einer einzigen Blutkultur im Zusammenhang mit entsprechender klinischer Symptomatik im Sinne einer Sepsis bewertet. Dies entspricht den CDC-Kriterien, die keine differenzierte Bewertung zwischen ein- und mehrmaligem Nachweis bei Koagulase-negativen Staphylokokken vornehmen, wenn intravasale Fremdkörper vorliegen. Andere Autoren bewerten den Nachweis von KNS nur dann als signifikant, wenn Blutkulturisolate aus zu verschiedenen Zeitpunkten entnommenen Kulturproben vorliegen, die dann jeweils auch noch ein identisches Antibiogramm aufweisen müssen. Alternativ können die Isolate auch molekularbiologisch typisiert werden. Die MiQ-Richtlinie stellt fest, dass beim Nachweis von Bakterien der normalen Hautflora, wie Staphylococcus epidermidis oder anderen Koagulase-negativen Staphylokokken, Corynebacterium spp. oder Propionibakterien, die klinische Bedeutung des Befundes fraglich ist, insbesondere wenn diese Erreger in nur einer von mehreren Blutkulturen isoliert werden. Andererseits wird anerkannt, dass die genannten Erreger insbesondere bei immunsupprimierten und hämatologisch-onkologischen Patienten schwere Infektionen hervorrufen können. Zur aktuellen Resistenzsituation bei klinisch wichtigen Infektionserregern gegenüber antimikrobiellen Substanzen in Mitteleuropa liegen die von Kresken et al. zusammengestellten Daten der PEG- Studie vor (Details siehe Anhang Tab. 7 und 8). In dieser Untersuchung wurden die Erreger nicht nach Untersuchungsmaterialien aufgeschlüsselt. Es sind also keine gesonderten Daten von Blutkulturisolaten verfügbar. Dennoch gibt die Studie wertvolle Hinweise zur Entwicklung der Resistenzlage zwischen 1995 und 1998 sowie zum Vergleich der Resistenzsituation auf Allgemein- und Intensivstationen. Der Vergleich der Resistenzsituation bei Stämmen von Patienten auf Allgemein- und Intensivstationen erbrachte im Großen und Ganzen den Trend zu höheren Resistenzraten auf den Intensivstationen. Beispielsweise lag die MRSA-Rate auf Allgemeinstationen bei 15 % im Vergleich zu 20 % auf Intensivstationen. Nachdem die Resistenz im Zeitraum zwischen 1990 und 1995 bei vielen Bakterienspezies zum Teil erheblich angestiegen war, kam es zwischen 1995 und 1998 zu keinen wesentlichen Änderungen der Resistenzsituation (siehe Anhang Tab. 8). Zur Pharmakokinetik und -dynamik Wie weiter unten beschrieben, sollen Antibiotika bei Sepsis und vor allem bei septischem Schock hoch dosiert werden. Kliniker gehen im Einzelfall weit über die empfohlene Höchstdosis hinaus. Der konkrete Beitrag der Pharmakokinetik und Pharmakodynamik zur richtigen Auswahl und Dosierung eines Antibiotikums bei Vorliegen einer Sepsis und insbesondere bei einem septischen Schock ist gering. Zu wenig verwertbares Material und dann leider oft Widersprüchliches liegt vor. Das oben beschriebene pathophysiologische Geschehen bei einer Sepsis ist komplex. Es liegen praktisch keine Untersuchungen vor, die sich mit der Anpassung der Dosierung eines Antibiotikums an diese Veränderungen beschäftigen, die ein Patient beim Durchlaufen vom SIRS bis zum septischen Schock erfährt. Der Patient mit Sepsis ist deshalb aus pharmakokinetischer Sicht zunächst so zu behandeln wie andere schwer kranke Patienten. Bei Letzteren hat sich die Dosierung eines Antibiotikums in erster Linie an der Organfunktion und am Körpergewicht zu orientieren. Die zugelassene Höchstdosis kann aus der Fachinformation entnommen werden, aber gerade bei der Sepsis spielt die Erfahrung des Klinikers eine wesentliche Rolle. Ausführlichere Daten zur Pharmakokinetik und Pharmakodynamik findet man lediglich für Gentamicin, und tendenziell scheint man von einem höheren Verteilungsvolumen von Gentamicin bei einer Sepsis ausgehen zu können. Eine solche Veränderung führt zu einer niedri- ChemotherapieJournal 10. Jahrgang Heft 2/
4 Tab. 2. Pharmakodynamik von Antibiotika Substanzklasse C max /MHK AUC AUC/MHK t > MHK Beta-Lactame x Fluorchinolone x x Makrolide x x = Kein Zusammenhang x = Deutliche Hinweise auf einen Zusammenhang zwischen den Parametern und der klinischen Wirkung des Antibiotikums geren Spitzenkonzentration, was natürlich gerade für Aminoglykoside wegen der Abhängigkeit ihres Effekts vom Peak-zu-MHK-Verhältnis (Tab. 2) zumindest theoretisch von Bedeutung sein könnte. Eine Absicherung der Gentamicin-Dosis durch Drug-Monitoring wurde vorgeschlagen. Niemiec et al. berichteten 1987, dass bis zu 15 mg/kg Gentamicin pro Tag gegeben werden mussten, um Spitzenkonzentrationen von mehr als 5 µg/ml zu erhalten. Damals wurden die Tab. 3. Pharmakokinetische Charakteristika der parenteralen Antibiotika Aminoglykoside natürlich noch mehrmals täglich dosiert. Inwiefern ein höheres Verteilungsvolumen mit Empfehlungen zu höherer Dosis auch für andere Substanzgruppen abgeleitet werden kann, muss diskutiert werden. Für Substanzgruppen, wie die Beta-Lactame, die aus toxikologischer Sicht zumindest weniger problematisch zu sein scheinen als Aminoglykoside, könnte dies gelten. Ihre Wirkung hängt jedoch nach heutigem Kenntnisstand nicht von der Spitzenkonzentration ab. Ohne weitere Toleranzuntersuchungen wäre beispielsweise eine Erhöhung der derzeitig zugelassenen Höchstdosis eines Chinolons, z. B. auf 2,5 g/tag was mit der vorher beschriebenen Situation bei Aminoglykosiden vergleichbar wäre nicht vertretbar. Nach den Prinzipien der Pharmakodynamik sollte auch die Wirkung eines Chinolons von der Spitzenkonzentration abhängig sein. Aus pharmakokinetischer Sicht könnte die Vorsicht durchaus damit begründet werden, dass der Anteil des Extrazellulärvolumens am Gesamtverteilungsvolumen einzelner Chinolone geringer ist (< 20 % ) als bei Aminglykosiden (~ 100 %) oder Beta-Lactamen (~ 100 %). Bei einer Dosiserhöhung würde man den größten Teil (> 80 %) der Dosis im Intrazellularraum wiederfinden, was unter Toleranzgesichtspunkten problematisch sein könnte. So interessant die hier angestellten Überlegungen aus pharmakokinetischer und pathophysiologischer Sicht auch sein Plasma- t 1/2 Clearance Verteilungs- Fu Metaboli- C I /C E TS/TR/GFR spiegel volumen sierungs- (C max, AUC)* quote/extrarenale Ausscheidung Beta-Lactame Mittel hoch Niedrig mittel Niedrig hoch Niedrig Mittel hoch Niedrig CI << CE TS >>> TR Fluorchinolone Niedrig Mittel lang Mittel hoch Mittel hoch Niedrig hoch Niedrig mittel CI >> CE TS + TR Aminoglykoside Niedrig Niedrig Mittel Niedrig Hoch Niedrig CI << CE GFR Tetracycline Niedrig Mittel Mittel Mittel hoch Mittel Niedrig mittel CI > CE TR > TS Glykopeptide Mittel Mittel hoch Niedrig mittel Mittel Hoch Niedrig CI + CE GFR Parenterale Makrolide Niedrig Niedrig hoch Mittel hoch Mittel hoch Niedrig mittel Mittel hoch CI >> CE TR Verschiedene Niedrig mittel Niedrig mittel Mittel hoch Mittel Niedrig Hoch CI + CE TR > TS (Clindamycin, Metronidazol) Einteilung: Niedrig < 10 FE < 3 h < 50 ml/min < 0,3 l/kg < 10 % der Dosis < 10 % der Dosis Mittel FE 3 10 h ml/min 0,3 1,5 l/kg % der Dosis % der Dosis Hoch > 100 FE > 10 h > 150 ml/min > 1,5 l/kg > 50 % der Dosis > 50 % der Dosis *: Bei therapeutischer Dosis Fu: % der Dosis, die im Urin unverändert ausgeschieden wird FE: Flächeneinheiten C I /C E : Verteilung einer Substanz zwischen Intrazellulärraum (C I ) und Extrazellulärraum (C E ) TS/TR/GFR: Anteil an tubulärer Sekretion, tubulärer Rückresorption oder glomerulärer Filtration Jahrgang Heft 2/2001
5 Tab. 4. Bei Sepsis eingesetzte parenterale Antiinfektiva (BLI = Beta-Lactamase-Inhibitor) Gruppe INN Handelsnamen (Beispiele) Gruppe INN Handelsnamen (Beispiele) Penicilline Penicilline Benzylpenicillin Penicillin G Aminopenicilline/BLI Amoxicillin/ Augmentan Clavulansäure Ampicillin/ Unacid Sulbactam Acylaminopenicilline Mezlocillin Baypen Piperacillin Pipril Acylaminopenicillin/ Piperacillin/ Tazobac BLI Tazobactam Isoxazolylpenicilline Flucloxacillin Staphylex (Staphylokokken- Oxacillin Stapenor Penicilline) Cephalosporine Gruppe 1 Cefazolin Elzogram Cefamandol Mandokef Gruppe 2 Cefuroxim Zinacef Cefotiam Spizef Gruppe 3a Cefotaxim Claforan Ceftriaxon Rocephin Cefodizim Opticef Gruppe 3b Ceftazidim Fortum Cefepim Maxipime Cefpirom Cefrom (Österreich) mögen, die Organfunktion bleibt der entscheidende Parameter für die Dosierungsanpassung. Da viele Antiinfektiva überwiegend renal ausgeschieden werden, kann eine Anpassung der Dosis über die Creatinin-Clearance erfolgen. Für eine reduzierte Leberfunktion gibt es nach wie vor keinen Parameter, mit dem eine Dosisanpassung zuverlässig durchgeführt werden kann. Die Ausscheidungscharakteristika der wichtigsten Substanzgruppen können aus Tabelle 3 entnommen werden. Für jede Substanzgruppe müssen diese Veränderungen individuell betrachtet werden. Dabei muss jedoch darauf geachtet werden, dass es in jeder Gruppe Substanzen gibt, die nicht den typischen Charakteristika ihrer Substanzgruppe folgen. Carbapeneme Charakterisierung der Antiinfektiva-Gruppen im Rahmen der Sepsis-Therapie Die Therapie hat aufgrund der Schwere des Krankheitsbildes prinzipiell parenteral zu erfolgen. Aufgrund der derzeitigen Studienlage kann keine Empfehlung für die orale antibiotische Therapie im Rahmen einer Sequenztherapie gegeben werden. Parenterale Antiinfektiva, die für die Therapie der Sepsis eingesetzt werden, sind in Tabelle 4 aufgeführt. Carbapeneme Imipenem Zienam Meropenem Meronem Fluorchinolone Gruppe 2 Ofloxacin Tarivid Ciprofloxacin Ciprobay Gruppe 3 Levofloxacin Tavanic Aminoglykoside Aminoglykoside Amikacin Biklin Gentamicin Refobacin Netilmicin Certomycin Tobramycin Gernebcin Weitere Makrolide Erythromycin- Erythromycin Lactobionat Gykopeptide Vancomycin Vancomycin Teicoplanin Targocid Clindamycin Clindamycin Sobelin Streptogramine Quinupristin/ Synercid Dalfopristin Rifampicin Fosfomycin Eremfat Fosfocin Penicilline Benzylpenicillin (Penicillin G) gilt bei Monoinfektion durch empfindliche Streptokokken und Pneumokokken wegen seiner hohen intrinsischen Aktivität als Mittel der Wahl. Die Resistenzrate der Pneumokokken liegt in Deutschland unter 2 %, die Häufigkeit intermediärer Stämme liegt im Mittel bei etwa 5 %. Meningokokken sind gegenüber Benzylpenicillin zu 96 % empfindlich. Aminopenicilline: Ampicillin und Amoxicillin haben eine relevante hohe Wirksamkeit bei Enterokokken und Listerien. Dabei ist die unterschiedliche Häufigkeit der Ampicillin-Resistenz bei Enterococcus faecalis (< 1 %) und Enterococcus faecium (> 50 %) zu beachten. Die Wirksamkeit der Aminopenicilline gegen Beta-Lactamase-bildende Erreger wie Staphylococcus spp., Haemophilus influenzae und Moraxella catarrhalis ist durch ihre Empfindlichkeit gegen Beta- Lactamasen eingeschränkt. In Kombination mit einem Beta-Lactamase-Inhibitor (Clavulansäure, Sulbactam) sind sie dagegen auch gegen die Mehrzahl der Beta- Lactamase-produzierenden Stämme sehr gut wirksam. ChemotherapieJournal 10. Jahrgang Heft 2/
6 Acylaminopenicilline: Mezlocillin und Piperacillin zeichnen sich durch eine gute Wirkung gegen Enterokokken, Enterobacteriaceae und Pseudomonas aeruginosa (nur Piperacillin) aus. Acylaminopenicilline sind nicht säurestabil und können daher nur parenteral appliziert werden. In Kombination mit einem Beta-Lactamase- Inhibitor sind sie auch gegen die Mehrzahl der Beta-Lactamase-produzierenden Stämme wirksam. Zur Verfügung stehen freie Kombinationen mit Sulbactam oder die fixe Kombination von Tazobactam mit Piperacillin. Aufgrund der aktuellen Literaturdaten (mikrobiologische und pharmakokinetische Daten sowie klinisch dokumentierte Studien) und unter dem Aspekt der Therapiesicherheit ist die Kombination von Tazobactam mit Piperacillin bei septischen Patienten von großem Vorteil. Isoxazolylpenicilline: Isoxazolylpenicilline besitzen ein schmales Wirkungsspektrum, ihr Einsatzgebiet beschränkt sich auf Infektionen, die durch empfindliche Staphylococcus aureus und Koagulase-negative Staphylokokken verursacht werden. Oxacillin und Flucloxacillin sind parenteral verfügbar. Cephalosporine Die Cephalosporine zeichnen sich im Allgemeinen durch eine sehr gute Verträglichkeit aus. Allergische Reaktionen kommen seltener vor als bei den Penicillinen, eine Kreuzallergie ist jedoch möglich. Parenterale Cephalosporine werden nach der Empfehlung der Paul-Ehrlich- Gesellschaft entsprechend ihrem Wirkungsspektrum in Gruppen eingeteilt. Cephalosporine Gruppe 1: Das parenterale Cephalosporin der Gruppe 1 (Cefazolin) besitzt eine gute Wirksamkeit gegenüber Streptokokken und Staphylokokken einschließlich Penicillin-resistenter Stämme, aber nur eine schwache gegenüber den meisten gramnegativen Mikroorganismen. Wie alle Cephalosporine ist Cefazolin nicht wirksam gegen Enterokokken. Cephalosporine Gruppe 2: Parenterale Cephalosporine der Gruppe 2 (Cefuroxim und Cefotiam) zeigen eine deutlich bessere Wirksamkeit gegenüber gramnegativen Erregern als Cephalosporine der Gruppe 1 bei guter Wirksamkeit gegenüber grampositiven Erregern. Das Spektrum umfasst Streptokokken, einschließlich Pneumokokken, Staphylokokken, Haemophilus influenzae und Moraxella catarrhalis sowie Klebsiellen, Proteus mirabilis und Escherichia coli. Cephalosporine Gruppe 3: Cephalosporine der Gruppe 3 haben eine verbesserte Aktivität im gramnegativen Bereich. Die Aktivität gegen Staphylokokken ist schwächer, gegen Pneumokokken und Streptokokken jedoch gut. Je nach ihrer Wirksamkeit gegenüber Pseudomonaden können parenterale Cephalosporine der Gruppe 3 in zwei Untergruppen eingeteilt werden. Gruppe 3a zeigt keine, Gruppe 3b eine gute zusätzliche Pseudomonas-Wirksamkeit. Parenteral stehen aus der Gruppe 3a Cefotaxim, Ceftriaxon und Cefodizim zur Verfügung. Cephalosporine der Gruppe 3b sind Ceftazidim, Cefepim und Cefpirom (nur in Österreich). Sie besitzen ein breites Wirkungsspektrum mit zusätzlich guter Pseudomonas-Aktivität. Carbapeneme Carbapeneme sind Breitspektrum-Antibiotika mit einer guten Wirksamkeit gegenüber grampositiven und gramnegativen Bakterien einschließlich Anaerobiern. Im Handel sind Imipenem und Meropenem. Fluorchinolone Die Einteilung der Fluorchinolone erfolgt nach Gruppen auf der Grundlage des Wirkungsspektrums, der Pharmakokinetik und der Indikationen. Fluorchinolone Gruppe 1: Substanzen der Gruppe 1 sind ausschließlich in oraler Darreichungsform verfügbar und kommen für die Sepsis-Therapie nicht in Betracht. Fluorchinolone Gruppe 2: Fluorchinolone der Gruppe 2 haben eine gute Wirksamkeit gegen Enterobacteriaceae und Haemophilus influenzae, eine schwächere Wirkung gegen Staphylokokken, Pneumokokken und Enterokokken sowie Chlamydien, Legionellen und Mykoplasmen. Die Aktivität gegen Pseudomonas aeruginosa ist unterschiedlich, wobei Ciprofloxacin in vitro am aktivsten ist. Neben Ciprofloxacin sind aus dieser Gruppe Fleroxacin und Ofloxacin parenteral einsetzbar. Fluorchinolone Gruppe 3: Das Wirkungsspektrum dieser Fluorchinolone unterscheidet sich von dem der Gruppe 2 im Wesentlichen dadurch, dass die Aktivität gegen grampositive Erreger wie Staphylokokken, Streptokokken einschließlich Pneumokokken höher ist bei vergleichbarer Aktivität gegen gramnegative Erreger. Hinzu kommt die verbesserte Wirksamkeit gegen Chlamydien, Legionellen und Mykoplasmen. Zum klinischen Einsatz kommt aus der Gruppe 3 nur Levofloxacin. Makrolide Makrolide besitzen eine gute Wirksamkeit gegenüber Mykoplasmen, Chlamydien und Legionellen. Die Resistenzrate von Pneumokokken gegenüber Makrolid-Antibiotika liegt bei Blutkultur-Isolaten bei bis zu 20 %. Erythromycin ist in Deutschland als einziger Vertreter dieser Substanzgruppe parenteral verfügbar; in Österreich und in der Schweiz ist auch Clarithromycin zur intravenösen Applikation zugelassen. Glykopeptide Vancomycin und Teicoplanin sind wirksam gegen Staphylokokken (einschließlich Oxacillin-resistenter Stämme), Streptokokken, Enterokokken, Coryne- Bakterien, Clostridium difficile und andere grampositive Anaerobier. Bei etwa 10 % der KNS ist Teicoplanin nicht wirksam, bei Enterokokken wirkt es bakterizid. Ihre Verwendung ist indiziert bei Infektionen durch die oben genannten Erreger bei einer Allergie gegen andere mögliche Antiinfektiva, beim Vorliegen Ampicillin-resistenter Enterokokken oder Oxacillin-resistenter Staphylokokken sowie bei mehrfach resistenten Corynebakterien. Wegen der Gefahr der Selektion Glykopeptid-resistenter Enterokokken und Staphylokokken sollten Glykopeptide restriktiv verwendet werden. Insbesondere bei niereninsuffizienten Patienten sollte die Therapie durch Drug-Monitoring überwacht werden. Clindamycin Clindamycin zeigt eine gute Wirksamkeit gegen Staphylokokken (Staphylococcus aureus zu 10 %, Koagulase-negative Staphylokokken zu 30 % resistent) und Streptokokken, Anaerobier (Bacteroides fragilis zu 10 bis 20 % resistent), Cory Jahrgang Heft 2/2001
7 Tab. 5. Therapieempfehlungen zur Behandlung der Sepsis bei unbekanntem Erreger (BLI = Beta-Lactamase-Inhibitor, MRSA = Methicillin-resistente Staphylococcus aureus) Infektionsherd Nosokomial (+ = schwere Sepsis Ambulant erworben (+ = schwere Sepsis Häufigste Erreger und/oder Spektrumserweiterung) und/oder Spektrumserweiterung) Infektionsherd unbekannt Acylaminopenicillin/BLI ± Cephalosporin Gruppe 2/3a ± Staphylococcus aureus Fluorchinolon Gruppe 2/3 oder Aminoglykosid Fluorchinolon Gruppe 2/3 oder Aminoglykosid Streptococcus spp. Cephalosporin Gruppe 3b ± Aminopenicillin/BLI + E. coli Fluorchinolon Gruppe 2/3 oder Aminoglykosid Fluorchinolon Gruppe 2/3 oder Aminoglykosid Koagulase-negative Staphylokokken Fluorchinolon Gruppe 2/3 ± Acylaminopenicillin/BLI ± Enterokokken Cephalosporin Gruppe 3b Fluorchinolon Gruppe 2/3 oder Aminoglykosid Klebsiellen Carbapenem ± Pseudomonaden Fluorchinolon Gruppe 2/3 oder Aminoglykosid Bei Risikopatienten (Beatmung, vorhergehende Antibiotika-Therapie, großer chirurgischer Eingriff, langer Aufenthalt auf Intensivstation) jeweils in Kombination mit einem Glykopeptid bei hoher Rate an MRSA Atemwege Cephalosporin Gruppe 3b + Cephalosporin Gruppe 2/3 in Kombination mit Streptococcus pneumoniae Fluorchinolon Gruppe 2/3 oder Aminoglykosid Makrolid Haemophilus influenzae Acylaminopenicillin/BLI + Acylaminopenicillin/BLI in Kombination mit Staphylococcus aureus Fluorchinolon Gruppe 2/3 oder Aminoglykosid Makrolid Enterobacteriaceae Anaerobier Fluorchinolon Gruppe 2/3 + Fluorchinolon Gruppe 3a/b Pseudomonaden Cephalosporin Gruppe 3b Carbapenem ± Aminoglykosid Carbapenem in Kombination mit Makrolid (in besonders schweren Fällen) Harntrakt Fluorchinolon Gruppe 2/3 Fluorchinolon Gruppe 2/3 Escherichia coli Proteus mirabilis Cephalosporin Gruppe 3a/b Cephalosporin Gruppe 3a Pseudomonaden Enterobacteriaceae Acylaminopenicillin/BLI Carbapenem Darm, gynäkol. Organe Acylaminopenicillin/BLI Acylaminopenicillin/BLI Enterobacteriaceae Anaerobier Cephalosporin Gruppe 3a/b + Metronidazol Cephalosporin Gruppe 3a + Metronidazol Enterokokken Fluorchinolon Gruppe 2/3 + Metronidazol Carbapenem Pseudomonaden Carbapenem Gallenwege Acylaminopenicillin/BLI Acylaminopenicillin/BLI Enterobacteriaceae Enterokokken Fluorchinolon Gruppe 2/3 in Kombination mit Fluorchinolon Gruppe 2/3 eventuell in Anaerobier Aminopenicillin Kombination mit Aminopenicillin Pseudomonaden Cephalosporin Gruppe 3a in Kombination mit Cephalosporin Gruppe 3a eventuell in Aminopenicillin Kombination mit Aminopenicillin Haut/Weichteile Cephalosporin Gruppe 3b in Kombination mit Cephalosporin Gruppe 1/2 in Kombination mit Streptococcus pyogenes Clindamycin Clindamycin Staphylococcus aureus Anaerobier Enterobacteriaceae Pseudomonaden Acylaminopenicillin/BLI ± Clindamycin Fluorchinolon Gruppe 2/3 in Kombination mit Cephalosporin Gruppe 2 oder Clindamycin Katheter-assoziiert Koagulase-negative Staphylokokken Staphylococcus aureus Gramnegative Stäbchenbakterien Carbapenem Glykopeptid ± Acylaminopenicillin/BLI oder Cephalosporin Gruppe 3a/b oder Carbapenem ChemotherapieJournal 10. Jahrgang Heft 2/
8 Tab. 6. Empfehlungen zur gezielten Antibiotika-Therapie der Sepsis bei bekanntem Erreger (BLI = Beta-Lactamase-Inhibitor) Erreger Monotherapie Kombinationstherapie Staphylococcus aureus Nach Antibiogramm in Einzelfällen Quinupristin/Dalfopristin Cephalosporin Gruppe 1/2 + Rifampicin oder Clindamycin oder/und Aminoglykosid (5 Tage) Isoxazolylpenicillin + Rifampicin oder Clindamycin oder/und Aminoglykosid (5 Tage) Bei MRSA Vancomycin oder Teicoplanin in Kombination mit Rifampicin, Fosfomycin, Fusidinsäure oder Co-trimoxazol (nach Antibiogramm) Koagulase-negative Cephalosporin Gruppe 1/2 Cephalosporin Gruppe 1/2 oder Isoxazolylpenicillin Staphylokokken Isoxazolylpencillin + Aminoglykosid und/oder Rifampicin (nach Antibiogramm) (Nach Antibiogramm Glykopeptid ± Rifampicin bei MRSE (Teicoplanin nur nach Glykopeptid bei MRSE) Antibiogramm) Aminoglykosid oder Rifampicin nach Antibiogramm (Kombinationstherapie bei Endokarditis, infizierten Gefäßprothesen etc.) A-Streptokokken Benzylpenicillin Benzylpenicillin + Clindamycin Cephalosporin Gruppe 1/2 (bei Penicillin-Allergie) Pneumokokken Benzylpenicillin Vancomycin + Rifampicin (bei Beta-Lactam-Allergie oder Resistenz Cephalosporin Gruppe 3a gegen Penicilline und Cephalosporine) (bei Penicillin-Allergie oder -Resistenz) Enterococcus faecalis Enterococcus faecium Quinupristin/Dalfopristin (nach Antibiogramm) Escherichia coli Cephalosporin Gruppe 3 Klebsiella pneumoniae Acylaminopenicillin/BLI Proteus mirabilis Fluorchinolon Gruppe 2/3 Carbapenem Citrobacter freundii Carbapenem Enterobacter spp. Cephalosporin Gruppe 3b Serratia marcescens Fluorchinolon Gruppe 2/3 Acylaminopenicillin/BLI Pseudomonas aeruginosa Acinetobacter spp. Stenotrophomonas maltophilia Nach Antibiogramm! Carbapenem Fluorchinolon Gruppe 2/3 Trimethoprim/Sulfonamid Cephalosporin Gruppe 3b Fluorchinolon Gruppe 2/3 Aminopenicillin + Aminoglykosid Acylaminopenicillin + Aminoglykosid Bei Penicillin-Allergie Teicoplanin + Aminoglykosid Aminopenicillin + Aminoglykosid Acylaminopenicillin + Aminoglykosid Teicoplanin + Aminoglykosid Cephalosporin Gruppe 3b + Fluorchinolon Gruppe 2/3 oder Aminoglykosid Acylaminopenicillin/BLI + Fluorchinolon Gruppe 2/3 oder Aminoglykosid Carbapenem + Fluorchinolon Gruppe 2/3 oder Aminoglykosid Fluorchinolon Gruppe 2/3 + Pseudomonas-wirksames Beta-Lactam-Antibiotikum Jahrgang Heft 2/2001
9 Tab. 6. Empfehlungen zur gezielten Antibiotika-Therapie der Sepsis bei bekanntem Erreger (BLI = Beta-Lactamase-Inhibitor) (Fortsetzung) Erreger Monotherapie Kombinationstherapie Haemophilus influenzae Cephalosporin Gruppe 3 Fluorchinolon Gruppe 2/3 (bei Beta-Lactam-Allergie) Bacteroides fragilis Carbapenem Metronidazol + Acylaminopenicillin/BLI oder Acylaminopenicillin/BLI Cephalosporin Gruppe 3 Clostridium perfringens nebakterien und Mycoplasma pneumoniae. Gegen Methicillin-resistente Staphylokokken ist Clindamycin meist nicht wirksam, doch werden sehr große regionale Unterschiede beschrieben. Eine Resistenzentwicklung unter der Therapie ist möglich. Rifampicin Rifampicin ist gut wirksam gegen grampositive Bakterien, hier insbesondere Staphylokokken, Streptokokken und Enterokokken. Es ist daher geeignet zur Therapie der Sepsis durch Staphylococcus aureus und Koagulase-negative Staphylokokken in Kombination mit Cephalosporinen der Gruppe 1/2, Isoxazolylpenicillinen und Glykopeptiden. Aminoglykoside Aminoglykoside (Gentamicin, Tobramycin, Amikacin, Netilmicin) haben eine geringe therapeutische Breite. Ihr Einsatz erfordert deshalb eine strenge Indikationsstellung und darf nur in Kombination mit einem anderen Antibiotikum (vorzugsweise mit einem Beta-Lactam-Antibiotikum zur Erzielung synergistischer Effekte) erfolgen. Sie sind unter anderem gut wirksam gegen Enterobacteriaceae und Pseudomonas aeruginosa, hier besonders Tobramycin und Amikacin. Während der Therapie, bei der das Aminoglykosid möglichst nur einmal täglich appliziert wird, sollten regelmäßige Talspiegel-Bestimmungen erfolgen. Bei septischen Patienten ist aufgrund des veränderten Verteilungsvolumens initial oft eine höhere Dosierung erforderlich. Metronidazol Metronidazol ist ausschließlich gegen anaerobe Bakterien wirksam, es darf bei septischen Patienten nur im Rahmen Benzylpenicillin Metronidazol (bei Penicillin-Allergie) einer Kombinationstherapie eingesetzt werden. Streptogramine Die Streptogramin-Kombination Quinupristin/Dalfopristin stellt bei Infektionen durch multiresistente Staphylokokken oder Enterococcus faecium nach vorheriger Austestung eine wichtige Therapieoption dar. Ausblick Fluorchinolone der Gruppe 4 besitzen ein ebenso breites Wirkungsspektrum wie die Fluorchinolone der Gruppe 3 und zusätzlich eine verbesserte Aktivität gegen Anaerobier. Derzeit ist in Deutschland kein parenterales Fluorchinolon der Gruppe 4 im Handel. Im Zulassungsverfahren befinden sich Gemifloxacin und Gatifloxacin sowie die parenterale Darreichungsform von Moxifloxacin. Eine neue Option ist das Antibiotikum Linezolid, ein Oxazolidinon, zur Behandlung von Infektionen durch grampositive Erreger einschließlich solcher mit Multiresistenz. Therapie-Empfehlungen Bei fast allen Patienten erfolgt die initiale antimikrobielle Therapie kalkuliert im Sinne der von der Paul-Ehrlich-Gesellschaft 1996 empfohlenen Interventionstherapie. Bei einem Teil der Patienten besteht durch einen Erregernachweis mit Antibiogramm die Möglichkeit, die initial begonnene Interventionstherapie zu modifizieren. Die initiale Antiinfektiva-Auswahl wird durch eine vermutete Infektionsquelle, die Tatsache, ob eine Infektion ambulant oder nosokomial erworben wurde, die Grunderkrankung und eine vorbestehende antimikrobielle Therapie beeinflusst. Tabelle 5 zeigt Therapie-Empfehlungen bei unbekanntem Erreger bezogen auf die Art und Lokalisation der Infektion, Tabelle 6 Therapie-Empfehlungen bei nachgewiesenem Erreger. Die Vielfalt der in den Tabellen 5 und 6 aufgeführten Therapieoptionen ist erstens durch unterschiedliche Schweregrade des Krankheitsbildes und zweitens durch die Therapiefreiheit des behandelnden Arztes bei nahezu äquipotent wirksamen Antiinfektiva begründet. Wenn in der Tabelle 6 in der Indikation Sepsis von mikrobiologischer Seite beim Nachweis von Staphylococcus aureus die Möglichkeit einer Monotherapie erwogen wird bzw. beim Nachweis von E. coli, Klebsiella pneumoniae, Proteus mirabilis, Citrobacter freundii, Enterobacter spp., Serratia marcescens, Acinetobacter spp., Stenotrophomonas maltophilia und Haemophilus influenzae grundsätzlich eine antimikrobielle Monotherapie empfohlen wird, muss aus klinisch-infektiologischer Sicht darauf hingewiesen werden, dass bei lebensbedrohlich erkrankten Patienten initial immer eine Kombinationstherapie durchgeführt werden muss. Dieses entspricht den Therapieempfehlungen der Tabelle 5 für eine schwere Sepsis. Traditionell sind Aminoglykoside die bevorzugten Kombinationspartner für Beta-Lactam-Antibiotika. Die neue Option, Fluorchinolone als Kombinationspartner für Beta-Lactam-Antibiotika einzusetzen, ist durch pharmakokinetische Vorteile, eine geringere Toxizität und die fehlende Notwendigkeit von regelmäßigen Spiegelbestimmungen trotz höherer direkter Therapiekosten begründet. In der Indikation Sepsis müssen alle Antiinfektiva parenteral und in hoher Do- ChemotherapieJournal 10. Jahrgang Heft 2/
10 sierung appliziert werden, da weder eine Sequenzialtherapie noch eine Dosisreduktion in dieser Indikation durch Studien belegt sind. Bei der Sepsis, die von den Atemwegen ausgeht, muss vor allem mit Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, und verschiedenen Enterobacteriaceae sowie bei Aspirationspneumonie zusätzlich mit Anaerobiern gerechnet werden. Bei schwer wiegenden Risikosituationen oder bei einer Verweildauer im Krankenhaus von mehr als fünf Tagen ist ferner mit Pseudomonas aeruginosa, Acinetobacter spp. und Stenotrophomonas maltophilia zu rechnen. Bei den Harnwegen als Sepsisquelle ohne vorausgegangene instrumentelle Intervention sind in erster Linie Escherichia coli und Proteus mirabilis als Sepsis-Erreger zu erwarten. Nach urologischen Eingriffen müssen außerdem Pseudomonas aeruginosa, andere Enterobacteriaceae, Enterokokken und Staphylokokken berücksichtigt werden. Ist die Quelle der Darm oder ein gynäkologisches Organ, muss mit folgenden Erregern gerechnet werden: Enterbacteriaceae, Anaerobiern, Enterokokken, Pseudomonaden, Staphylococcus aureus. Bei einer chologenen Sepsis nimmt die Erregerbesiedlung in den Gallenwegen und damit die Bakteriämie mit dem Grad der Abflussbehinderung zu. Beim Verschlussikterus werden bei mehr als 75 % der Patienten Erreger im Blut nachgewiesen. Das Spektrum umfasst Enterobacteriaceae, Enterokokken und Anaerobier. Bei postoperativen Bakteriämien, cholangitischer Sepsis und subhepatischen Abszessen sowie bei interventionellen Eingriffen (ERCP oder endoskopischer Papillotomie) lassen sich weitere gramnegative Problemerreger einschließlich Pseudomonas aeruginosa nachweisen. Ist die Quelle im Bereich der Haut oder der Weichteile, sind Infektionen durch Streptococcus pyogenes, Staphylococcus aureus sowie Mischinfektionen unter zusätzlicher Beteiligung von Non- A-Streptokokken, Anaerobiern, Enterobacteriaceae sowie Pseudomonas aeruginosa möglich. Das Erregerspektrum der Katheter-assoziierten Sepsis umfasst Koagulase-negative Staphylokokken, Staphylococcus aureus, gramnegative Stäbchenbakterien, Candida spp., Corynebacterium jeikeium sowie Propionibakterien. Literatur Alejandria MM, Lansang MA, Dans LF, Mantaring JB. Intravenous immunoglobulin for treating sepsis and septic shock. Cochrane Database Syst Rev 2000: CD Astiz ME, Rackow EC. Septic shock. Lancet 1998;351: Baden LR, Eisenstein BI. Impact of antibiotic resistance on the treatment of gramnegative Sepsis. Curr Inf Dis Rep 2000;2: Balk RA. Severe sepsis and septic shock. Definitions, epidemiology, and clinical manifestations. Critical Care Clinics 2000;16: Baxter F. Septic shock. Can J Anaesth 1997; 44: Bodmann KF. Antimikrobielle Therapie. In: Schuster HP. Intensivtherapie bei Sepsis und Multiorganversagen. Berlin/Heidelberg/New York: Springer-Verlag, Bone RC. Sir Isaac Newton, sepsis, SIRS, and CARS. Crit Care Med 1996;24: Bone RC, Grodzin CJ, Balk RA. Sepsis: a new hypothesis for pathogenesis of the disease process. Chest 1997;112: Bone RC, Balk RA, Cerra FB, Dellinger RP, et al. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. The ACCP/SCCM Consensus Conference Committee. American College of Chest Physicians/Society of Critical Care Medicine. Chest 1992;101: Brunkhorst R, Brunkhorst F. Procalcitonin und C3a: Nützlich zur Prognose und Verlaufsbeurteilung der Sepsis? Intensivmed 2000;37: Dellinger RP. Current therapy for sepsis. Infect Dis Clin North America 1999;13: Ehrhard I, Sonntag HG. Epidemiologie der Meningokokken-Infektionen. Mikrobiologe 1998;8: Fourrier F, Jourdain M, Tournoys A. Clinical trial results with antithrombin III in sepsis. Crit Care Med 2000;(S9):S Geerdes HF, et al.: Septicemia in 980 patients at an university hospital in Berlin: prospective studies during four selected years between 1979 and Clin Inf Dis 1992;15: Horn KD. Evolving strategies in the treatment of sepsis and systemic inflammatory response syndrome (SIRS). Qjm 1998;91: Jacobs MR. Drug-resistant Streptococcus pneumoniae: rational antibiotic choices. Amer J Med 1999;106:19S-25S; discussion 48S-52S. Kresken M, Hafner D, und die Studiengruppe. Resistenzsituation bei klinisch wichtigen Infektionserregern gegenüber Chemotherapeutika in Mitteleuropa. Chemotherapie Journal 2000; 9: Kresken M, Hafner D. Prävalenz der Antibiotikaresistenz bei klinisch wichtigen Infektionserregern in Mitteleuropa. Bericht über die Ergebnisse einer multizentrischen Studie der Arbeitsgemeinschaft Resistenz in der Paul-Ehrlich- Gesellschaft für Chemotherapie e.v. aus dem Jahre Chemotherapie J 1996;5: Mesters RM, Helterbrand J. Utterback BG, et al. Prognostic value of protein C concentrations in neutropenic patients at high risk of severe septic complications. Crit Care Med 2000;28: MiQ-Richtlinie Sepsis-Blutkulturdiagnostik 1997; 3:1-44. Gustav-Fischer-Verlag, Stuttgart Jena Moser S, Fätkenheuer G, Salzberger B, Seifert H. Die klinische Signifikanz positiver Blutkulturen an einem Universitätsklinikum: eine prospektive Untersuchung zur Mikrobiologie, Epidemiologie und Prognose. 50. Kongress der DGHM, Berlin, 4. bis 9. Oktober Naber K, Adam D, und die Expertengruppe der Paul-Ehrlich-Gesellschaft für Chemotherapie e.v. Einteilung der Fluorchinolone. Chemotherapie J 1998;7:66-8. Nathwani D, Davey P. Strategies to rationalize sepsis management a review of 4 years' experience in Dundee. J Inf 1998;37 Suppl 1:10-7. Niemiec PW, Allo MD, Miller CF. Effect of altered volume of distribution on aminoglycoside levels in patients in surgical intensive care. Arch Surg 1987;122: Reed RL. Contemporary issues with bacterial infection in the intensive care unit. Surgical Clinics of North America 2000;80: , ix-x. Rosenthal EJK: Epidemiologie von Septikämie- Erregern. Dtsch Med Wochenschr 1993;118: Schottmüller H. Wesen und Behandlung der Sepsis. Verh Dtsch Ges Inn Med 1914;31:257. Scholz H, Naber KG, und die Expertengruppe der PEG. Einteilung der Cephalosporine. Chemotherapie J 1999;6: Schuster HP, Werdan K. Intensivtherapie bei Sepsis und Multiorganversagen. Berlin Heidelberg: Springer Verlag, Simon D, Trenholme G. Antibiotic selection for patients with septic shock. Crit Care Clin 2000; 16: Smith AL. Treatment of septic shock with immunotherapy. Pharmacotherapy 1998;18: Steinbrecher E, Sohr D, Nassauer A, Daschner F, et al. Die häufigsten Erreger bei Intensivpatienten mit nosokomialen Infektionen. Ergebnisse des Krankenhaus-Infektions-Surveillance-Systems (KISS). Chemotherapie J 2000;9: Trautmann M, et al.: Computergestützte prospektive Erfassung nosokomialer Septikämien in einem Universitätsklinikum. Hygiene und Medizin 1997;22: Unertl K. Antimicrobial chemoprophylaxis of pneumonia in intensive care patients. Chemotherapie J 1996;5: Vincent JL, Preiser JC. Management of the critically ill patient with severe sepsis. J Chemother 1999;11: Vogel F, Stille W, Tauchnitz C, Stolpmann R, et al. Positionspapier zur Antibiotikatherapie in der Klinik. Chemotherapie J 1996;5:23-7. Vogel F, Naber K, Wacha H, Shah P. Parenterale Antibiotika bei Erwachsenen. Chemotherapie J 1999;1:3-49. Werdan K, Pilz G. Supplemental immune globulins in sepsis: a critical appraisal. Clin Exp Immunol 1996;104(Sl): Wheeler AP, Bernard GR. Treating patients with severe sepsis. N Engl J Med 1999;340: Wittmann DH, Wittmann-Tylor A. Scope and limitations of antimicrobial therapy of sepsis in surgery. Langenbecks Arch Surg 1998;383(1): Woltmann A, Hamann L, Ulmer AJ, Gerdes J, Bruch HP, Rietschel ET. Molecular mechanisms of sepsis. Langenbecks Arch Surg 1998; 383: Wood MJ. Chemotherapy for gram-positive nosocomial sepsis. J Chemother 1999;11: Zanetti G, Baumgartner JD, Glauser MP. Sepsis and septic shock. Schweizerische Med Wochenschr 1997;127: Jahrgang Heft 2/2001
11 Anhang: Tab. 7. Prozentualer Anteil empfindlicher Stämme von E. coli, K. pneumoniae, P. aeruginosa, S. aureus, Koagulase-negativen Staphylokokken (KNS) und E. faecalis auf Allgemein (A)- und Intensivstationen (I) im Untersuchungsjahr 1998 [mod. nach Kresken et al.] E. coli K. pneumoniae P. aeruginosa S. aureus KNS E. faecalis A I A I A I A I A I A I n Penicilline Penicillin G c) Ampicillin Amoxicillin/ Clavulansäure a) Piperacillin Piperacillin/ Tazobactam a) Oxacillin b) Cephalosporine Cefazolin Cefuroxim Cefotaxim Ceftriaxon > Ceftazidim Cefepim Carbapeneme Imipenem e) Meropenem Aminoglykoside Amikacin Gentamicin d) 75 d) Tobramycin Fluorchinolone Ciprofloxacin Levofloxacin MLS-Gruppe Erythromycin Clindamycin Quinupristin/ > Dalfopristin Glykopeptide Teicoplanin > Vancomycin > Weitere Fusidinsäure Rifampicin a) Die Endkonzentration der Beta-Lactamase-Inhibitoren im Testansatz betrug für Clavulansäure konstant 2 mg/l und für Tazobactam konstant 4 mg/l b) Oxacillin-resistente Staphylokokken werden unabhängig vom Testergebnis gegenüber allen Beta-Lactam-Antibiotika als resistent gewertet c) Penicillin-G-resistente Staphylokokken werden unabhängig vom Testergebnis gegenüber allen Aminopenicillinen, Carboxypenicillinen und Acylaminopenicillinen als resistent gewertet d) Anteil der Stämme ohne Hochresistenz (MHK 500 mg/l) e) Zwischenzeitlich Grenzwert-Änderung bei Imipenem sensibel < 1 mg/l, resistent 4 mg/l ChemotherapieJournal 10. Jahrgang Heft 2/
12 Anhang:Tab. 8. Prozentualer Anteil empfindlicher Stämme von 5 Enterobacteriaceae-Spezies, P. aeruginosa, Koagulase-negativen Staphylokokken (KNS), S. aureus und E. faecalis in den Untersuchungsjahren 1995 und 1998 [mod. nach Kresken et al.] Stämme Jahr E. coli P. mira- E. cloa- K. pneu- K. oxy- P. aeru- KNS S. aureus E. faebilis cae moniae toca ginosa calis n (95/98) 783/ / / / / / / / /757 Penicilline Penicillin G c) Ampicillin Amoxicillin/ Clavulansäure a) Piperacillin Piperacillin/ Tazobactam a) Oxacillin b) Cephalosporine Cefazolin Cefuroxim Cefotaxim Ceftriaxon Ceftazidim Cefepim Carbapeneme Imipenem f) Meropenem Aminoglykoside Amikacin Gentamicin e) e) Tobramycin Fluorchinolone Ciprofloxacin Jahrgang Heft 2/2001
13 Anhang: Tab. 8. Prozentualer Anteil empfindlicher Stämme von 5 Enterobacteriaceae-Spezies, P. aeruginosa, Koagulase-negativen Staphylokokken (KNS), S. aureus und E. faecalis in den Untersuchungsjahren 1995 und 1998 (Fortsetzung) Stämme Jahr E. coli P. mira- E. cloa- K. pneu- K. oxy- P. aeru- KNS S. aureus E. faebilis cae moniae toca ginosa calis n (95/98) 783/ / / / / / / / /757 MLS-Gruppe Erythromycin Clindamycin Quinupristin/ Dalfopristin > 99 Glykopeptide Teicoplanin Vancomycin d) Weitere Fusidinsäure Rifampicin a) Die Endkonzentration der Beta-Lactamase-Inhibitoren im Testansatz betrug für Clavulansäure konstant 2 mg/l und für Tazobactam konstant 4 mg/l b) Oxacillin-resistente Staphylokokken werden unabhängig vom Testergebnis gegenüber allen Beta-Lactam-Antibiotika als resistent gewertet c) Penicillin-G-resistente Staphylokokken werden unabhängig vom Testergebnis gegenüber allen Aminopenicillinen, Carboxypenicillinen und Acylaminopenicillinen als resistent gewertet d) Weil eine Nachtestung der Vancomycin-resistenten S.-aureus-Stämme nicht möglich war, ist nicht auszuschließen, dass es sich bei den Isolaten um Stämme einer anderen Staphylokokken-Spezies handelt e) Anteil der Stämme ohne Hochresistenz (MHK 500 mg/l) f) Zwischenzeitlich Grenzwert-Änderung bei Imipenem sensibel < 1 mg/l, resistent 4 mg/l ChemotherapieJournal 10. Jahrgang Heft 2/
14 Jahrgang Heft 2/2001
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST. Karlsruhe, im März Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege,
 EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im März 2019 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im März 2019 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST. Karlsruhe, im August Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege,
 EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im August 2018 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im August 2018 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
Empirische antibiotische Therapie bei schwerer Sepsis
 MEDIZINISCHE KLINIK TÜBINGEN Empirische antibiotische Therapie bei schwerer Sepsis Infektionsmedizin 2011 Reimer Riessen Internistische Intensivstation Bedeutung einer raschen Antibiotikatherapie Jede
MEDIZINISCHE KLINIK TÜBINGEN Empirische antibiotische Therapie bei schwerer Sepsis Infektionsmedizin 2011 Reimer Riessen Internistische Intensivstation Bedeutung einer raschen Antibiotikatherapie Jede
ANTIBIOGRAMME - Interpretationshilfe -
 Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik ANTIBIOGRAMME - Interpretationshilfe - Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik
Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik ANTIBIOGRAMME - Interpretationshilfe - Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik
Highlights der PEG- Resistenzstudie 2007
 Jahrestagung der PEG Sektion Grundlagen Bonn, 1. Oktober 28 Highlights der PEG- Resistenzstudie 27 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation,
Jahrestagung der PEG Sektion Grundlagen Bonn, 1. Oktober 28 Highlights der PEG- Resistenzstudie 27 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation,
Resistenzsituation im Krankenhausbereich -
 2. estagung der PEG Antibiotikaverbrauch und Resistenz Wo steht Deutschland Resistenzsituation im Krankenhausbereich - Datenquellen, Entwicklung und aktuelle Situation Michael Kresken Antiinfectives Intelligence
2. estagung der PEG Antibiotikaverbrauch und Resistenz Wo steht Deutschland Resistenzsituation im Krankenhausbereich - Datenquellen, Entwicklung und aktuelle Situation Michael Kresken Antiinfectives Intelligence
Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK.
 Antibiotika Dosierungen Stand:Januar 2017 Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK. Penicilline iv Standarddosierung Höhere Dosierung
Antibiotika Dosierungen Stand:Januar 2017 Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK. Penicilline iv Standarddosierung Höhere Dosierung
Antibiotikatherapie - Grundlagen
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Antibiotikatherapie - Grundlagen B. Salzberger Hemmung der Zellwandsynthese: Penicilline, Cephalosporine, Glykopeptid-AB, Fosfomycin Proteinsynthese (Translation)
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Antibiotikatherapie - Grundlagen B. Salzberger Hemmung der Zellwandsynthese: Penicilline, Cephalosporine, Glykopeptid-AB, Fosfomycin Proteinsynthese (Translation)
Resistenzbericht Manfred Fille
 Resistenzbericht 216 Manfred Fille gefährli hste Erreger ( a h WHO, Februar 217) Kritische Priorität: Acinetobacter baumannii, resistent gegen Carbapeneme Pseudomonas aeruginosa, resistent gegen Carbapeneme
Resistenzbericht 216 Manfred Fille gefährli hste Erreger ( a h WHO, Februar 217) Kritische Priorität: Acinetobacter baumannii, resistent gegen Carbapeneme Pseudomonas aeruginosa, resistent gegen Carbapeneme
Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 2016 für Urine
 Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 206 für Urine September 206 Sehr geehrte Kolleginnen und Kollegen, die klinische Leitlinie Unkomplizierte Harnwegsinfektionen
Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 206 für Urine September 206 Sehr geehrte Kolleginnen und Kollegen, die klinische Leitlinie Unkomplizierte Harnwegsinfektionen
Antibiotikaresistenzen in der Humanmedizin
 BVL-Symposium Herausforderungen 24: Tierarzneimittel im Fokus Nutzen, Risiken, Resistenzen 5./6. November 23, Berlin Antibiotikaresistenzen in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
BVL-Symposium Herausforderungen 24: Tierarzneimittel im Fokus Nutzen, Risiken, Resistenzen 5./6. November 23, Berlin Antibiotikaresistenzen in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
RESISTENZANALYSE Atemwegsinfekte
 RESISTENZANALYSE Atemwegsinfekte NEU - aktuelle Daten aus 2016 Die Daten geben einen Überblick der ausgebildeten Resistenzen bei den am häufigsten aufgetretenen Keimen Nur ambulante Patienten Antibiotika
RESISTENZANALYSE Atemwegsinfekte NEU - aktuelle Daten aus 2016 Die Daten geben einen Überblick der ausgebildeten Resistenzen bei den am häufigsten aufgetretenen Keimen Nur ambulante Patienten Antibiotika
UNIVERSALINSTRUMENT ANTIBIOTIKUM?
 CAMPUS GROSSHADERN CAMPUS INNENSTADT UNIVERSALINSTRUMENT ANTIBIOTIKUM? Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene 02.04.2014 B. Grabein DIE INSTRUMENTE Daptomycin Aminoglykoside
CAMPUS GROSSHADERN CAMPUS INNENSTADT UNIVERSALINSTRUMENT ANTIBIOTIKUM? Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene 02.04.2014 B. Grabein DIE INSTRUMENTE Daptomycin Aminoglykoside
Multiresistenz Erfahrungen aus der PEG-Studie
 Multiresistenz Erfahrungen aus der PEG-Studie Bad Honnef- Symposium 2001 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation, Bonn Bad Honnef
Multiresistenz Erfahrungen aus der PEG-Studie Bad Honnef- Symposium 2001 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation, Bonn Bad Honnef
Erregerhäufigkeit bei akuter bakterieller Meningitis
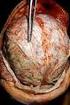 Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
Hier ist eine Zusammenstellung der vom RKI ermittelten Daten der Keime, bei denen jeweils mindestes 50 Proben auf Resistenzen getestet wurden.
 Keime und Resistenzen ARS 2011 oder Vorsicht, Antibiotika! Quelle: Robert Koch-Institut: ARS, https://ars.rki.de, Datenstand: 04.01.2012 Zusammenstellung und mehr zum Thema: www.krankenhhasser.de Die Datenbank
Keime und Resistenzen ARS 2011 oder Vorsicht, Antibiotika! Quelle: Robert Koch-Institut: ARS, https://ars.rki.de, Datenstand: 04.01.2012 Zusammenstellung und mehr zum Thema: www.krankenhhasser.de Die Datenbank
Antibiotikaresistenz und -einsatz in der Humanmedizin
 Europäischer Antibiotikatag Interdisziplinäres Symposium: Antibiotikaeinsatz - Wie wenig ist (noch) zu viel? 9. November 212, BVL, Berlin Antibiotikaresistenz und -einsatz in der Humanmedizin Michael Kresken
Europäischer Antibiotikatag Interdisziplinäres Symposium: Antibiotikaeinsatz - Wie wenig ist (noch) zu viel? 9. November 212, BVL, Berlin Antibiotikaresistenz und -einsatz in der Humanmedizin Michael Kresken
Antibiotika-Empfindlichkeit von HWI-Erregern
 Bad Honnef-Symposium 212, 16./17. April 212 Venerologische und urogenitale Infektionen Antibiotika-Empfindlichkeit von HWI-Erregern Michael Kresken Paul-Ehrlich-Gesellschaft für Chemotherapie e.v., Campus
Bad Honnef-Symposium 212, 16./17. April 212 Venerologische und urogenitale Infektionen Antibiotika-Empfindlichkeit von HWI-Erregern Michael Kresken Paul-Ehrlich-Gesellschaft für Chemotherapie e.v., Campus
1 Infektion der Atemwege
 1 Infektion der Atemwege 1.1 Infektexazerbation bei COPD Ca. 50% der Exazerbationen einer COPD werden durch Infektionserreger ausgelöst, überwiegend durch respiratorische Viren. Die häufigsten bakteriellen
1 Infektion der Atemwege 1.1 Infektexazerbation bei COPD Ca. 50% der Exazerbationen einer COPD werden durch Infektionserreger ausgelöst, überwiegend durch respiratorische Viren. Die häufigsten bakteriellen
ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH
 CAMPUS GROSSHADERN CAMPUS INNENSTADT ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene WANN KOMMT EIN IMPLANTATERHALTUNGSVERSUCH
CAMPUS GROSSHADERN CAMPUS INNENSTADT ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene WANN KOMMT EIN IMPLANTATERHALTUNGSVERSUCH
Übersicht der getesteten Antibiotika
 Übersicht der getesteten Antibiotika Penicilline (bakteriozid) Schmalspektrum-Penicilline Orale Penicilline (Penicillin V und Propicillin) sind bei Infektionen mit Keimen des "klassischen Penicillin-G-
Übersicht der getesteten Antibiotika Penicilline (bakteriozid) Schmalspektrum-Penicilline Orale Penicilline (Penicillin V und Propicillin) sind bei Infektionen mit Keimen des "klassischen Penicillin-G-
Resistenzepidemiologie 2015
 Resistenzepidemiologie 215 Arne C. Rodloff Erreger Chirurgie Escherichia coli 386 Staphylococcus aureus 39 Enterococcus faecalis 31 Staphylococcus epidermidis 227 Proteus mirabilis 134 Pseudomonas aeruginosa
Resistenzepidemiologie 215 Arne C. Rodloff Erreger Chirurgie Escherichia coli 386 Staphylococcus aureus 39 Enterococcus faecalis 31 Staphylococcus epidermidis 227 Proteus mirabilis 134 Pseudomonas aeruginosa
Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika
 Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika Fortbildungsveranstaltung Netzwerk MRE Landkreis Stendal 14.06.2017 Gramnegative Bakterien Enterobakterien* Pseudomonas aeruginosa
Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika Fortbildungsveranstaltung Netzwerk MRE Landkreis Stendal 14.06.2017 Gramnegative Bakterien Enterobakterien* Pseudomonas aeruginosa
Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie Außenstelle Großhadern. Béatrice Grabein
 Antibiotika als Tranquilizer und Antipyretika Der sinnvolle Einsatz von Antibiotika bei Knochen-, Gelenk- und Weichteilinfektionen Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und
Antibiotika als Tranquilizer und Antipyretika Der sinnvolle Einsatz von Antibiotika bei Knochen-, Gelenk- und Weichteilinfektionen Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und
Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion?
 Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion? Katja de With Medizinische Universitätsklinik Freiburg Entwicklung antibiotikaresistenter
Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion? Katja de With Medizinische Universitätsklinik Freiburg Entwicklung antibiotikaresistenter
Häufige Infektionen im Erwachsenalter: Diagnostik & DD
 Häufige Infektionen im Erwachsenalter: Diagnostik & DD Dr. Boris Ehrenstein Infektiologie / Rheumatologie Klinik und Poliklinik für Innere Medizin I Häufige ambulant erworbene Infektionen Sinusitis, Otitis
Häufige Infektionen im Erwachsenalter: Diagnostik & DD Dr. Boris Ehrenstein Infektiologie / Rheumatologie Klinik und Poliklinik für Innere Medizin I Häufige ambulant erworbene Infektionen Sinusitis, Otitis
Mikrobiologisches Labor Doz. Möst Erreger- und Resistenzstatistik Harnkulturen. Erregerspektrum
 Harnkulturen Harnproben gesamt: 13117 Erregerspektrum Enterobakterien Escherichia coli 3718 davon ESBL bildend 281 (=8,1%) Klebsiella sp. 3 davon ESBL bildend 10 (=2,2%) Proteus mirabilis 290 Enterobacter
Harnkulturen Harnproben gesamt: 13117 Erregerspektrum Enterobakterien Escherichia coli 3718 davon ESBL bildend 281 (=8,1%) Klebsiella sp. 3 davon ESBL bildend 10 (=2,2%) Proteus mirabilis 290 Enterobacter
Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf
 Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf - Effekte eines intensivierten MRSA screenings- J.Mattes 14 November 2012 Mühldorf The Epidemic of Antibiotic-Resistant Infections: A Call
Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf - Effekte eines intensivierten MRSA screenings- J.Mattes 14 November 2012 Mühldorf The Epidemic of Antibiotic-Resistant Infections: A Call
Bedeutung von Kreuzresistenz und Mehrfachresistenz bei bakteriellen Erregern für die Initialtherapie Michael Kresken. 21./22. März 2016, Königswinter
 Bad Honnef-Symposium 2016 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Empfehlungen zur kalkulierten Initialtherapie bakterieller Erkrankungen bei Erwachsenen 21./22. März 2016, Königswinter Bedeutung
Bad Honnef-Symposium 2016 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Empfehlungen zur kalkulierten Initialtherapie bakterieller Erkrankungen bei Erwachsenen 21./22. März 2016, Königswinter Bedeutung
Therapie von Infektionen beim alten Menschen
 Bad Honnef-Symposium 2011 Therapie von Infektionen beim alten Menschen 18./19. April 2011, Königswinter Resistenzsituation bei Harnwegsisolaten von älteren Patienten Ergebnisse aus der Resistenzstudie
Bad Honnef-Symposium 2011 Therapie von Infektionen beim alten Menschen 18./19. April 2011, Königswinter Resistenzsituation bei Harnwegsisolaten von älteren Patienten Ergebnisse aus der Resistenzstudie
Situation im Antibiotikaverbrauch und Erregerresistenz in der Humanmedizin
 Interdisziplinäres Symposium Antibiotikaresistenz Vom Wissen zum Handeln 19. / 20. September 2012 - Erlangen Situation im Antibiotikaverbrauch und Erregerresistenz in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
Interdisziplinäres Symposium Antibiotikaresistenz Vom Wissen zum Handeln 19. / 20. September 2012 - Erlangen Situation im Antibiotikaverbrauch und Erregerresistenz in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
Trends und Resistenzeckdaten 2010
 Trends und Resistenzeckdaten 21 21 hat sich die Resistenzsituation weiter verschlechtert. Diese Tatsache ist vor allem auf den Anstieg von gramnegativen Darmbakterien zurückzuführen, die in der Lage sind,
Trends und Resistenzeckdaten 21 21 hat sich die Resistenzsituation weiter verschlechtert. Diese Tatsache ist vor allem auf den Anstieg von gramnegativen Darmbakterien zurückzuführen, die in der Lage sind,
Antibiotikaverbrauch und Resistenzsituation in der ambulanten Versorgung
 Infektiologie Update 2012 23. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Symposium V: Infektionen in der Primärversorgung 13. Oktober 2012, Dresden Antibiotikaverbrauch und Resistenzsituation
Infektiologie Update 2012 23. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Symposium V: Infektionen in der Primärversorgung 13. Oktober 2012, Dresden Antibiotikaverbrauch und Resistenzsituation
Therapeutische Optionen bei Multiresistenten Erregern. OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel
 Therapeutische Optionen bei Multiresistenten Erregern OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel Themen Multiresistente Erreger MRSA MRGN VRE Therapeutische Optionen MRE-Netzwerk
Therapeutische Optionen bei Multiresistenten Erregern OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel Themen Multiresistente Erreger MRSA MRGN VRE Therapeutische Optionen MRE-Netzwerk
Mikrobiologisches Labor Doz. Möst Erreger- und Resistenzstatistik Harnkulturen
 Harnkulturen Harnproben gesamt: 10869 Erregerspektrum Enterobakterien Escherichia coli 2967 davon ESBL bildend 245 (=8,2%) Klebsiella sp. 380 davon ESBL bildend 12 (=3,2%) Proteus mirabilis 221 Enterobacter
Harnkulturen Harnproben gesamt: 10869 Erregerspektrum Enterobakterien Escherichia coli 2967 davon ESBL bildend 245 (=8,2%) Klebsiella sp. 380 davon ESBL bildend 12 (=3,2%) Proteus mirabilis 221 Enterobacter
Prävention der Ausbreitung von multiresistenten gramnegativen
 Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Prävention der Ausbreitung von multiresistenten gramnegativen Erregern (MRGNE) Internetversion ohne Photos
Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Prävention der Ausbreitung von multiresistenten gramnegativen Erregern (MRGNE) Internetversion ohne Photos
Zu unterscheiden ist zwischen Sepsis, schwerer Sepsis und septischem Schock.
 Sepsis in Deutschland Aktueller Stand und Perspektiven in Diagnose, Epidemiologie und Therapie der Sepsis Von Professor Dr. Michael Quintel München München (3. Mai 2007) - Der Verdacht auf eine Sepsis
Sepsis in Deutschland Aktueller Stand und Perspektiven in Diagnose, Epidemiologie und Therapie der Sepsis Von Professor Dr. Michael Quintel München München (3. Mai 2007) - Der Verdacht auf eine Sepsis
PEG-Blutkultur-Studien. Eberhard Straube, Jena Andrea Becker, Karlsruhe Erika J. K. Rosenthal, Wiesbaden Eberhard Kniehl, Karlsruhe Ines Noll, Berlin
 PEG-Blutkultur-Studien Eberhard Straube, Jena Andrea Becker, Karlsruhe Erika J. K. Rosenthal, Wiesbaden Eberhard Kniehl, Karlsruhe Ines Noll, Berlin PEG-Blutkultur-Studien Teilnehmer: Mikrobiologische
PEG-Blutkultur-Studien Eberhard Straube, Jena Andrea Becker, Karlsruhe Erika J. K. Rosenthal, Wiesbaden Eberhard Kniehl, Karlsruhe Ines Noll, Berlin PEG-Blutkultur-Studien Teilnehmer: Mikrobiologische
Pseudomonas aeruginosa. Pseudomonas aeruginosa. Optimales Wachstum
 Pseudomonas aeruginosa Pseudomonas aeruginosa Optimales Wachstum Kü/2002 10 Jahre DFS im Raum Trier Dr. med. Dipl. Biol. E. Kühnen, 13.12.20 in Mainz Diabetisches Fußsyndrom Infektionen der Haut und
Pseudomonas aeruginosa Pseudomonas aeruginosa Optimales Wachstum Kü/2002 10 Jahre DFS im Raum Trier Dr. med. Dipl. Biol. E. Kühnen, 13.12.20 in Mainz Diabetisches Fußsyndrom Infektionen der Haut und
Kommentare zur Resistenztestung
 Kommentare zur Resistenztestung Axel Hamprecht 19.02.2018 Warum Kommentare? Unsicherheit, wie Ergebnisse der Resistenztestung nach EUCAST am besten kommuniziert werden Hinweis auf diagnostische/therapeut.
Kommentare zur Resistenztestung Axel Hamprecht 19.02.2018 Warum Kommentare? Unsicherheit, wie Ergebnisse der Resistenztestung nach EUCAST am besten kommuniziert werden Hinweis auf diagnostische/therapeut.
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2018 INHALT
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2018 INHALT
Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik
 Workshop Wundzentrum Hamburg 20. August 2010 Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik Dr. J. Ungeheuer Tel.: 040-76696-103 www.labor-froreich.de
Workshop Wundzentrum Hamburg 20. August 2010 Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik Dr. J. Ungeheuer Tel.: 040-76696-103 www.labor-froreich.de
München. Zentrales Institut des Sanitätsdienstes der Bundeswehr. Rationale Antibiotikatherapie. OFA Bock. Text Stand: xx.xx.xxxx
 Zentrales Institut des Sanitätsdienstes der Bundeswehr München Rationale Antibiotikatherapie OFA Bock Einführung Schön wär`s gewesen wenn Einführung Bakterien sind schneller als die Menschen! Fragen für
Zentrales Institut des Sanitätsdienstes der Bundeswehr München Rationale Antibiotikatherapie OFA Bock Einführung Schön wär`s gewesen wenn Einführung Bakterien sind schneller als die Menschen! Fragen für
Multiresistente Erreger. Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen?
 Hygiene in der Arztpraxis 3MRGN/4MRGN was ist das nun wieder?? 17.04.2013 Multiresistente Erreger Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen? Multiresistente Erreger Welche sollen
Hygiene in der Arztpraxis 3MRGN/4MRGN was ist das nun wieder?? 17.04.2013 Multiresistente Erreger Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen? Multiresistente Erreger Welche sollen
Multiresistente Keime - Therapie
 Multiresistente Keime - Therapie Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Ted-Frage 1 Welche Erreger sind Ihrer Ansicht
Multiresistente Keime - Therapie Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Ted-Frage 1 Welche Erreger sind Ihrer Ansicht
Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I
 Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I Risikostratifizierung in der Praxis Definition individuelles Therapieziel Klinische Evaluation,
Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I Risikostratifizierung in der Praxis Definition individuelles Therapieziel Klinische Evaluation,
Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor. Dr. med. Arno Köster
 Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor Dr. med. Arno Köster Definition Multiresistenz (MRE) ICD-10-GM Version 2010 U81! Bakterien mit Multiresistenz gegen
Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor Dr. med. Arno Köster Definition Multiresistenz (MRE) ICD-10-GM Version 2010 U81! Bakterien mit Multiresistenz gegen
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim
 MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie
 Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie Ein Konsensuspapier der Deutschen Gesellschaft für Pneumologie DGP) und der Paul-Ehrlich-Gesellschaft für Chemotherapie PEG) unter Mitarbeit von
Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie Ein Konsensuspapier der Deutschen Gesellschaft für Pneumologie DGP) und der Paul-Ehrlich-Gesellschaft für Chemotherapie PEG) unter Mitarbeit von
Carbapeneme im Vergleich Stellenwert von Doripenem Mikrobiologie
 Carbapeneme im Vergleich Stellenwert von Doripenem Mikrobiologie Dr. med. Béatrice Grabein Klinische Mikrobiologie und Krankenhaushygiene am KUM Béatrice Grabein Einteilung der Carbapeneme* Allgemein:
Carbapeneme im Vergleich Stellenwert von Doripenem Mikrobiologie Dr. med. Béatrice Grabein Klinische Mikrobiologie und Krankenhaushygiene am KUM Béatrice Grabein Einteilung der Carbapeneme* Allgemein:
Antibiotika im Krankenhaus
 APOTHEKE ARZNEIMITTELINFORMATION Antibiotika im Krankenhaus Dr. Alexandra Weber, Apotheke Apotheke Klinikum der Universität München Wechselbeziehungen PATIENT ERREGER Resistenz Wirkung ANTIBIOTIKUM 2 1
APOTHEKE ARZNEIMITTELINFORMATION Antibiotika im Krankenhaus Dr. Alexandra Weber, Apotheke Apotheke Klinikum der Universität München Wechselbeziehungen PATIENT ERREGER Resistenz Wirkung ANTIBIOTIKUM 2 1
Harnkulturen. Resistenzraten von E.coli in Harnkulturen (n=3797)
 Harnkulturen Harnproben gesamt: 439 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 3797 davon ESBL bildend 239 (=6,3%) Klebsiella sp. 42 davon ESBL bildend 9 (=4,6%) Proteus mirabilis
Harnkulturen Harnproben gesamt: 439 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 3797 davon ESBL bildend 239 (=6,3%) Klebsiella sp. 42 davon ESBL bildend 9 (=4,6%) Proteus mirabilis
Vorschläge des NAK zur Kommentierung von Ergebnissen der Resistenztestung
 Vorschläge des NAK zur Kommentierung von Ergebnissen der Resistenztestung Version 1.1, Stand 21.07.2018 Änderung: H. alvei hinzugefügt; Änderungen im Text sind farblich gekennzeichnet. Spezies Indikator
Vorschläge des NAK zur Kommentierung von Ergebnissen der Resistenztestung Version 1.1, Stand 21.07.2018 Änderung: H. alvei hinzugefügt; Änderungen im Text sind farblich gekennzeichnet. Spezies Indikator
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2017 INHALT
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2017 INHALT
Tabelle 4-01: Absolute und relative Verteilung der Patienten nach Altersklassen
 Die in den XLS-Dateien vorhandene ATB-Streifen-Bezeichnungen sowie die Köpfe der einzelnen Spalten werden, da in der Access-Tabelle nicht gebraucht, verworfen. Um zu gewährleisten, daß keine neuen Streifen,
Die in den XLS-Dateien vorhandene ATB-Streifen-Bezeichnungen sowie die Köpfe der einzelnen Spalten werden, da in der Access-Tabelle nicht gebraucht, verworfen. Um zu gewährleisten, daß keine neuen Streifen,
Geld oder Leben? Antibiotikatherapie im Spannungsfeld zwischen Ökonomie und Resistenz
 Geld oder Leben? Antibiotikatherapie im Spannungsfeld zwischen Ökonomie und Resistenz Wiesbaden (15. April 2007 ) In Deutschland ist laut Prof. Dieter Adam aus München seit 1985 ein deutlicher Anstieg
Geld oder Leben? Antibiotikatherapie im Spannungsfeld zwischen Ökonomie und Resistenz Wiesbaden (15. April 2007 ) In Deutschland ist laut Prof. Dieter Adam aus München seit 1985 ein deutlicher Anstieg
Situation AB-Verbrauch & Erreger- Resistenz in der Humanmedizin
 Symposium I: Antibiotikaverbrauch und -resistenz Symposium der Initiative GERMAP Situation AB-Verbrauch & Erreger- Resistenz in der Humanmedizin Michael Kresken Antiinfectives Intelligence GmbH Campus
Symposium I: Antibiotikaverbrauch und -resistenz Symposium der Initiative GERMAP Situation AB-Verbrauch & Erreger- Resistenz in der Humanmedizin Michael Kresken Antiinfectives Intelligence GmbH Campus
Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de /
 Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de / mikro@labmed.de) seit April 2003 Akkreditierung (aktuell DIN EN ISO 15189; DACH) 1 1. Problematik multiresistenter
Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de / mikro@labmed.de) seit April 2003 Akkreditierung (aktuell DIN EN ISO 15189; DACH) 1 1. Problematik multiresistenter
Resistenzbericht Dorothea Orth-Höller Sektion für Hygiene und Medizinische Mikrobiologie Medizinische Universität Innsbruck
 Resistenzbericht 2017 Dorothea Orth-Höller Sektion für Hygiene und Medizinische Mikrobiologie Medizinische Universität Innsbruck Inhalt Überblick über Vorkommen von Multiresistenten Keimen in Tirol in
Resistenzbericht 2017 Dorothea Orth-Höller Sektion für Hygiene und Medizinische Mikrobiologie Medizinische Universität Innsbruck Inhalt Überblick über Vorkommen von Multiresistenten Keimen in Tirol in
Ergebnisse der PEG Resistenzstudie Resistenzsituation im stationären Versorgungsbereich
 Bad Honnef-Symposium 215 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Strategien zur Bekämpfung multiresistenter Erreger 3./31. März 215, Königswinter Ergebnisse der PEG Resistenzstudie 213 - Resistenzsituation
Bad Honnef-Symposium 215 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Strategien zur Bekämpfung multiresistenter Erreger 3./31. März 215, Königswinter Ergebnisse der PEG Resistenzstudie 213 - Resistenzsituation
Aktuelle Daten zur Resistenzsituation bei Bakterien gegenüber Antibiotika
 Jahrespressekonferenz der PEG Berlin, 29. November 2005 Aktuelle Daten zur Resistenzsituation bei Bakterien gegenüber Antibiotika Ergebnisse der PEG-Resistenzstudie 2004 Michael Kresken Antiinfectives
Jahrespressekonferenz der PEG Berlin, 29. November 2005 Aktuelle Daten zur Resistenzsituation bei Bakterien gegenüber Antibiotika Ergebnisse der PEG-Resistenzstudie 2004 Michael Kresken Antiinfectives
Rationale und rationelle Antibiotika-Therapie
 Rationale und rationelle Antibiotika-Therapie C. Berg Med. Klinik Abt. I = vernünftige nftige und zweckmäß äßige / wirtschaftliche Antibiotika-Therapie Vancomycin Zyvoxid Sobelin Penicilin G Staphylex
Rationale und rationelle Antibiotika-Therapie C. Berg Med. Klinik Abt. I = vernünftige nftige und zweckmäß äßige / wirtschaftliche Antibiotika-Therapie Vancomycin Zyvoxid Sobelin Penicilin G Staphylex
GERMAP-Ergebnisse: Antibiotikaverbrauch und Resistenzsituation im Humanbereich. Michael Kresken
 GERMAP-Ergebnisse: Antibiotikaverbrauch und Resistenzsituation im Humanbereich Michael Kresken Antiinfectives Intelligence GmbH Campus FH Bonn-Rhein-Sieg, Rheinbach GERMAP Humanbereich / 1 Verbrauch Antibiotikaverbrauch
GERMAP-Ergebnisse: Antibiotikaverbrauch und Resistenzsituation im Humanbereich Michael Kresken Antiinfectives Intelligence GmbH Campus FH Bonn-Rhein-Sieg, Rheinbach GERMAP Humanbereich / 1 Verbrauch Antibiotikaverbrauch
S3-Leitlinie. Kurzfassung. 1. Auflage. S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG.
 S3-Leitlinie Kurzfassung 1. Auflage S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Thieme 2005 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 133711 5 Inhaltsverzeichnis:
S3-Leitlinie Kurzfassung 1. Auflage S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Thieme 2005 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 133711 5 Inhaltsverzeichnis:
Mikrobiologische Surveillance oder nicht, das ist hier die Frage,. Heinz Burgmann
 Mikrobiologische Surveillance oder nicht, das ist hier die Frage,. Mikrobiologische Untersuchungen auf der ICU Diagnostisch: Klinische Indikation Material aus normalerweise sterilen Bereich (Blut, Blase,
Mikrobiologische Surveillance oder nicht, das ist hier die Frage,. Mikrobiologische Untersuchungen auf der ICU Diagnostisch: Klinische Indikation Material aus normalerweise sterilen Bereich (Blut, Blase,
Hygiene in der Arztpraxis
 Hygiene in der Arztpraxis 3MRGN/4MRGN Gefahr durch multiresistente Erreger? 22.04.2015 Multiresistente Erreger Welche sollen es denn diesmal sein? MRGN = Multiresistente Gramnegative Stäbchen Stäbchen?
Hygiene in der Arztpraxis 3MRGN/4MRGN Gefahr durch multiresistente Erreger? 22.04.2015 Multiresistente Erreger Welche sollen es denn diesmal sein? MRGN = Multiresistente Gramnegative Stäbchen Stäbchen?
Sepsis/Endokarditis im Alter. Bad Honnef Symposium der PEG April 2011
 Sepsis/Endokarditis im Alter Bad Honnef Symposium der PEG April 2011 Sepsis/Endokarditis im Alter Sind sie häufiger im Alter als es dem Anteil der Bevölkerung entspricht? Welche Risikofaktoren gibt es
Sepsis/Endokarditis im Alter Bad Honnef Symposium der PEG April 2011 Sepsis/Endokarditis im Alter Sind sie häufiger im Alter als es dem Anteil der Bevölkerung entspricht? Welche Risikofaktoren gibt es
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER
 Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
Umsetzung vorgezogene Regelung /5
 Hinweise zur Umsetzung der auf 2019 vorgezogenen Regelung zur Mitteilung des S nur gültig bei hoher Dosis als I, sensibel bei erhöhter Exposition NAK, 14.12.2018 Die Stellungnahme des NAK vom 26.10.2018
Hinweise zur Umsetzung der auf 2019 vorgezogenen Regelung zur Mitteilung des S nur gültig bei hoher Dosis als I, sensibel bei erhöhter Exposition NAK, 14.12.2018 Die Stellungnahme des NAK vom 26.10.2018
Dr. med. Stefan Schmitt MVZ Dr. Klein Dr. Schmitt & Kollegen, Kaiserslautern AGIL e.v. Grünstadt
 Passgenauigkeit in der Antibiotikatherapie Aktuelle regionale und bundesweite Daten zur Infektionslage bzw. Resistenzentwicklung als Grundlage einer rationellen Antibiotikatherapie Dr. med. Stefan Schmitt
Passgenauigkeit in der Antibiotikatherapie Aktuelle regionale und bundesweite Daten zur Infektionslage bzw. Resistenzentwicklung als Grundlage einer rationellen Antibiotikatherapie Dr. med. Stefan Schmitt
Tabelle 1.2 Antiinfektiva-Dosierungen (Auswahl)* Gruppe Appl. Patient Dosis in 24 Std. ED max. 1. Penicilline
 Allgemeines. Antiinfektiva und Dosierungen Tabelle. Antiinfektiva-Dosierungen (Auswahl)*. Penicilline Penicillin G Mo. hoch Penicillin V Mo. 0, 0, Mio. IE/kg 0, 0, Mio. IE/kg Mio. IE 8 Mio. IE 0, Mio.
Allgemeines. Antiinfektiva und Dosierungen Tabelle. Antiinfektiva-Dosierungen (Auswahl)*. Penicilline Penicillin G Mo. hoch Penicillin V Mo. 0, 0, Mio. IE/kg 0, 0, Mio. IE/kg Mio. IE 8 Mio. IE 0, Mio.
Resistenzentwicklung -international, national, regional
 Infektiologie Update 2014 24. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Workshop der Sektion Grundlagen: Antibiotikaresistenz - Epidemiologie, Detektion & Therapiestrategie 17.
Infektiologie Update 2014 24. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Workshop der Sektion Grundlagen: Antibiotikaresistenz - Epidemiologie, Detektion & Therapiestrategie 17.
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger. Prof. Dr. C. Wendt
 ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
Diagnostik und Therapie der Pneumonie
 Diagnostik und Therapie der Pneumonie H. Klinker Medizinische Klinik und Poliklinik II der Universität Würzburg Schwerpunkt Hepatologie/Infektiologie Infektionserkrankungen Zahl der Todesfälle 2000 bzw.
Diagnostik und Therapie der Pneumonie H. Klinker Medizinische Klinik und Poliklinik II der Universität Würzburg Schwerpunkt Hepatologie/Infektiologie Infektionserkrankungen Zahl der Todesfälle 2000 bzw.
Die neuen EUCAST Expert-Rules: Auswirkungen auf den mikrobiologischen Befund? Und was gibt es sonst noch Neues bei EUCAST?
 Die neuen EUCAST Expert-Rules: Auswirkungen auf den mikrobiologischen Befund? Und was gibt es sonst noch Neues bei EUCAST? Sören Gatermann Abteilung für Medizinische Mikrobiologie, Ruhr-Universität Bochum,
Die neuen EUCAST Expert-Rules: Auswirkungen auf den mikrobiologischen Befund? Und was gibt es sonst noch Neues bei EUCAST? Sören Gatermann Abteilung für Medizinische Mikrobiologie, Ruhr-Universität Bochum,
Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang
 WWW.INFEKTIO.DE Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang Register 2016 Heft 1 Heft 2 Heft 3 Heft 4 Heft 5 Heft 6 Seiten 1-10 Seiten 11-20 Seiten 21-30 Seiten
WWW.INFEKTIO.DE Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang Register 2016 Heft 1 Heft 2 Heft 3 Heft 4 Heft 5 Heft 6 Seiten 1-10 Seiten 11-20 Seiten 21-30 Seiten
Antibiotikatherapie bei Intensivpatienten - Mit Tigecyclin kalkuliert behandeln
 Antibiotikatherapie bei Intensivpatienten Mit Tigecyclin kalkuliert behandeln Neue Studienergebnisse, aktuelle ICAAC-Daten und das Update der PEG-Empfeh lungen unterstreichen den Stellenwert des ersten
Antibiotikatherapie bei Intensivpatienten Mit Tigecyclin kalkuliert behandeln Neue Studienergebnisse, aktuelle ICAAC-Daten und das Update der PEG-Empfeh lungen unterstreichen den Stellenwert des ersten
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA RESISTENZBERICHT 2016 INHALT Resistenzstatistik 2016....3 Einleitung....3
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA RESISTENZBERICHT 2016 INHALT Resistenzstatistik 2016....3 Einleitung....3
Antimikrobielle Resistenz: Eine grenzenlose Gefahr für Patienten
 Antimikrobielle Resistenz: Eine grenzenlose Gefahr für Patienten Prim. Univ. Prof. Dr. Petra Apfalter Nationales Referenzzentrum für nosokomiale Infektionen und Antibiotikaresistenz Institut für Hygiene,
Antimikrobielle Resistenz: Eine grenzenlose Gefahr für Patienten Prim. Univ. Prof. Dr. Petra Apfalter Nationales Referenzzentrum für nosokomiale Infektionen und Antibiotikaresistenz Institut für Hygiene,
Der Weg von CLSI zu EUCAST
 Der Weg von CLSI zu EUCAST Michael Lefmann, 25.03.2013 Von CLSI zu EUCAST Resistenztestung Entscheidung für EUCAST Implementierung Resistenzstatistik 1 Der wahre Breakpoint??? Kahlmeter et al. JAC2003(52):145-8
Der Weg von CLSI zu EUCAST Michael Lefmann, 25.03.2013 Von CLSI zu EUCAST Resistenztestung Entscheidung für EUCAST Implementierung Resistenzstatistik 1 Der wahre Breakpoint??? Kahlmeter et al. JAC2003(52):145-8
Ute Gritzka. Hämatologisch- Onkologisches. Speziallabor
 Sepsis Ute Gritzka Hämatologisch- Onkologisches Vivantes GmbH Klinikum Am Urban Dieffenbachstr. 1 10967 Berlin Tel. 030/ 130 222 130 UteGritzka@aol.com www.gritzka.de Speziallabor Inzidenz der Sepsis (USA)
Sepsis Ute Gritzka Hämatologisch- Onkologisches Vivantes GmbH Klinikum Am Urban Dieffenbachstr. 1 10967 Berlin Tel. 030/ 130 222 130 UteGritzka@aol.com www.gritzka.de Speziallabor Inzidenz der Sepsis (USA)
U N I V E R S I T Ä T S M E D I Z I N B E R L I N
 U N I V E R S I T Ä T S M E D I Z I N B E R L I N Intravenöse Medikamente - Antibiotika, Antimykotika, Virustatika - Immunsuppresiva - Schulung für Pflegepersonal Grundlagen Allgemeine Infektionszeichen:
U N I V E R S I T Ä T S M E D I Z I N B E R L I N Intravenöse Medikamente - Antibiotika, Antimykotika, Virustatika - Immunsuppresiva - Schulung für Pflegepersonal Grundlagen Allgemeine Infektionszeichen:
Sepsis Andrea Duppenthaler
 Sepsis 2012 Andrea Duppenthaler andrea.duppenthaler@insel.ch Universitätsklinik für Kinderheilkunde PEMS, 16.11.2012: SEPSIS 2012 Sepsis: Definitionen Sepsis: systemic inflammatory response syndrome (SIRS)
Sepsis 2012 Andrea Duppenthaler andrea.duppenthaler@insel.ch Universitätsklinik für Kinderheilkunde PEMS, 16.11.2012: SEPSIS 2012 Sepsis: Definitionen Sepsis: systemic inflammatory response syndrome (SIRS)
Antibiotikaverbrauch im ambulanten Versorgungsbereich. Königswinter, / 1
 Antibiotikaverbrauch im ambulanten Versorgungsbereich Königswinter, 14.4.14 / 1 Verordnungsdichte im ambulanten Bereich, 2006-2011 (in DDD pro 1.000 Versicherte und Tag) Königswinter, 14.4.14 / 2 Antibiotika-Verordnungsdichten
Antibiotikaverbrauch im ambulanten Versorgungsbereich Königswinter, 14.4.14 / 1 Verordnungsdichte im ambulanten Bereich, 2006-2011 (in DDD pro 1.000 Versicherte und Tag) Königswinter, 14.4.14 / 2 Antibiotika-Verordnungsdichten
49. Fortbildungsveranstaltung für Hals-Nasen- Ohrenärzte
 Multiresistente Keime: Mikrobiologie, Hygiene Autor: Prof. Dr. med. Wolfgang Pfister, Universitätsklinikum Jena, Institut für Medizinische Mikrobiologie, Erlanger Allee 101, 07747 Jena, E-Mail: Wolfgang.Pfister@med.uni-jena.de
Multiresistente Keime: Mikrobiologie, Hygiene Autor: Prof. Dr. med. Wolfgang Pfister, Universitätsklinikum Jena, Institut für Medizinische Mikrobiologie, Erlanger Allee 101, 07747 Jena, E-Mail: Wolfgang.Pfister@med.uni-jena.de
Erfassung von Erregern mit besonderen Resistenzen und Multiresistenzen - Die Umsetzung von 23 Infektionsschutzgesetz
 Erfassung von Erregern mit besonderen Resistenzen und Multiresistenzen - Die Umsetzung von 23 Infektionsschutzgesetz Veranstaltung: Fortbildungsveranstaltung für den öffentlichen Gesundheitsdienst Berlin,
Erfassung von Erregern mit besonderen Resistenzen und Multiresistenzen - Die Umsetzung von 23 Infektionsschutzgesetz Veranstaltung: Fortbildungsveranstaltung für den öffentlichen Gesundheitsdienst Berlin,
NEUE ANTIINFEKTIVA. Martin J. Hug Apotheke des Universitätsklinikums Freiburg
 NEUE ANTIINFEKTIVA Martin J. Hug Apotheke des Universitätsklinikums Freiburg Antiinfektivaentwicklung und Resistenzbildung PDR Acinetobacter u. Pseudomonas Ceftriaxon-R N. gonorrhoeae Ceftarolin-R Staphylococcus
NEUE ANTIINFEKTIVA Martin J. Hug Apotheke des Universitätsklinikums Freiburg Antiinfektivaentwicklung und Resistenzbildung PDR Acinetobacter u. Pseudomonas Ceftriaxon-R N. gonorrhoeae Ceftarolin-R Staphylococcus
Neue Wege zur Reduktion der Antibiotikaverordnung bei Atemwegsinfektionen.
 Neue Wege zur Reduktion der Antibiotikaverordnung bei Atemwegsinfektionen. Epidemiologie der antimikrobiellen Resistenzen in Deutschland und Europa Miriam Wiese-Posselt Institut für Hygiene und Umweltmedizin
Neue Wege zur Reduktion der Antibiotikaverordnung bei Atemwegsinfektionen. Epidemiologie der antimikrobiellen Resistenzen in Deutschland und Europa Miriam Wiese-Posselt Institut für Hygiene und Umweltmedizin
Agenda. Antibiotikaverbrauch und Resistenzsituation im ambulanten Versorgungsbereich. Antibiotikaverbrauch in der Humanmedizin Deutschland,
 Regionale Fortbildung Apothekerverband Nordrhein / Apothekerkammer Nordrhein 23. April 2012, Köln Antibiotikaverbrauch und Resistenzsituation im ambulanten Versorgungsbereich Michael Kresken Wissenschaftlicher
Regionale Fortbildung Apothekerverband Nordrhein / Apothekerkammer Nordrhein 23. April 2012, Köln Antibiotikaverbrauch und Resistenzsituation im ambulanten Versorgungsbereich Michael Kresken Wissenschaftlicher
Antibiotika im perioperativen Setting
 Antibiotika im perioperativen Setting Referent: Dr. Michael Sturm Mikrobiologe, Prüfstellenleiter und allg. beeideter gerichtlich beeideter SV für Hygiene und Mikrobiologie Hygienezentrum Dr. Sturm GmbH
Antibiotika im perioperativen Setting Referent: Dr. Michael Sturm Mikrobiologe, Prüfstellenleiter und allg. beeideter gerichtlich beeideter SV für Hygiene und Mikrobiologie Hygienezentrum Dr. Sturm GmbH
Mikrobiologie der Knocheninfektion mit Problematik der multiresistenten Erreger
 Mikrobiologie der Knocheninfektion mit Problematik der multiresistenten Erreger Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie Außenstelle Großhadern
Mikrobiologie der Knocheninfektion mit Problematik der multiresistenten Erreger Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie Außenstelle Großhadern
SARI http://www.antibiotika-sari.de 1
 Daten zum Verbrauch der teilnehmenden Intensivstationen im Zeitverlauf Antibiotikaverbrauch: n=116 Antimykotikaverbrauch: n=94 Institut für Umweltmedizin und Krankenhaushygiene Breisacher Str. 115 b 7916
Daten zum Verbrauch der teilnehmenden Intensivstationen im Zeitverlauf Antibiotikaverbrauch: n=116 Antimykotikaverbrauch: n=94 Institut für Umweltmedizin und Krankenhaushygiene Breisacher Str. 115 b 7916
Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie
 Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie Ein Konsensuspapier der Deutschen Gesellschaft für Pneumologie (DGP) und der Paul-Ehrlich-Gesellschaft für Chemotherapie (PEG) unter Mitarbeit
Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie Ein Konsensuspapier der Deutschen Gesellschaft für Pneumologie (DGP) und der Paul-Ehrlich-Gesellschaft für Chemotherapie (PEG) unter Mitarbeit
Antibiotika-Verbrauch und Antibiotika- Resistenzsituation in der Humanmedizin
 Europäischer Antibiotikatag, 18. November 2011 Paul Ehrlich gratuliert Gerhard Domagk 75 Jahre antibakterielle Therapie quo vadis Antibiotika? Brennpunkt Resistente Escherichia coli Antibiotika-Verbrauch
Europäischer Antibiotikatag, 18. November 2011 Paul Ehrlich gratuliert Gerhard Domagk 75 Jahre antibakterielle Therapie quo vadis Antibiotika? Brennpunkt Resistente Escherichia coli Antibiotika-Verbrauch
Zwischenbericht zur ESPED Studie. Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern
 Zwischenbericht zur ESPED Studie Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern Einleitung: Bei Routineabstrichen werden gelegentlich multiresistente bakterielle Infektionserreger
Zwischenbericht zur ESPED Studie Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern Einleitung: Bei Routineabstrichen werden gelegentlich multiresistente bakterielle Infektionserreger
Leitthema Antibiotikaresistenz. Universität, Düsseldorf 3 Praxis für Allgemeinmedizin, Ahlen
 Bundesgesundheitsbl - Gesundheitsforsch - Gesundheitsschutz 999 4: 7 Springer-Verlag 999 Leitthema Antibiotikaresistenz M. Kresken D. Hafner N. von Rosenstiel Rhône-Poulenc Rorer Arzneimittel GmbH, Köln
Bundesgesundheitsbl - Gesundheitsforsch - Gesundheitsschutz 999 4: 7 Springer-Verlag 999 Leitthema Antibiotikaresistenz M. Kresken D. Hafner N. von Rosenstiel Rhône-Poulenc Rorer Arzneimittel GmbH, Köln
Antibiotikaverbrauch in der Arztpraxis in Hessen
 Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Antibiotikaresistenzen vermeiden Antibiotikaverbrauch in der Arztpraxis in Hessen 2008-2015 Dr. med. Harald Herholz, MPH Kassenärztliche Vereinigung
Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Antibiotikaresistenzen vermeiden Antibiotikaverbrauch in der Arztpraxis in Hessen 2008-2015 Dr. med. Harald Herholz, MPH Kassenärztliche Vereinigung
Nationales Referenzzentrum für gramnegative Krankenhauserreger. MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke
 Nationales Referenzzentrum für gramnegative Krankenhauserreger MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke Was sind die Konsequenzen von Resistenz? Antibiotika gegen E. coli Ampicillin/Amoxicillin
Nationales Referenzzentrum für gramnegative Krankenhauserreger MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke Was sind die Konsequenzen von Resistenz? Antibiotika gegen E. coli Ampicillin/Amoxicillin
M. Mielke, N.-O. Hübner, RKI
 Nosokomiale und schwierig zu therapierende Infektionen IfSG und aktuelle Empfehlungen der KRINKO Aufmerksamkeit - Wissen - Verantwortung MRGN Was ist das? Was ist zu tun? M. Mielke, N.-O. Hübner, RKI Novellierung
Nosokomiale und schwierig zu therapierende Infektionen IfSG und aktuelle Empfehlungen der KRINKO Aufmerksamkeit - Wissen - Verantwortung MRGN Was ist das? Was ist zu tun? M. Mielke, N.-O. Hübner, RKI Novellierung
