a) Gegeben ist das folgende EI-Massenspektrum (M = 148 u). Wie entstehen die Signale bei m/z = 133, 105, 91, 77 und 43?
|
|
|
- Ralph Sven Busch
- vor 7 Jahren
- Abrufe
Transkript
1 Massenspektrometrie Übung 1: a) Gegeben ist das folgende EI-Massenspektrum (M = 148 u). Wie entstehen die Signale bei = 133, 15, 91, 77 und 43? ( m a in lib ) 2-Bu ta n o n e, 4-p h e n y l b) Gegeben ist das folgende EI-Massenspektrum (M = 197 u). Wie entstehen die Signale bei = 12, 92, 77 und 65? Welche Information zur Summenformel kann man direkt aus dem Molekülpeak entnehmen? H ( m a in lib ) Be n ze n a m in e, 2 -( p h e n y la zo
2 c) Gegeben ist das folgende EI-Massenspektrum (M 129 u). Wie entstehen die Signale bei = 112, 99, 85, 84 und 71? Tipp: 85 entsteht aus einer tautomeren Molekülstruktur H H ( m a in lib ) -M e th y lm a le a m ic a c id d) Gegeben ist das folgende EI-Massenspektrum (M 129 u). Wie entstehen die Signale bei = 114, 86 (zwei Signale), 58 (zwei Signale) und 3? ( m a in lib ) D ie th y la m in o a c e to n e
3 e) Gegeben ist das folgende EI-Massenspektrum (M 137 u). Wie entstehen die Signale bei = 121, 12, 93 und 92? (Intensitäten beachten!) 1 12 H 137 H ( m a in lib ) Sa lic y la m id e f) Gegeben ist das folgende EI-Massenspektrum (M 137 u). Wie entstehen die Signale bei = 16, 78, 51 und 31? Tipp: 31 entsteht aus einem nicht sichtbaren Fragment! H 2 H ( m a in lib ) Iso n ia zid
4 Massenspektrometrie Übung 2: a) Gegeben ist das folgende EI-Massenspektrum (M = 166 u). Cl = 35/37 u Wie entstehen die Signale bei = 131, 13, 77, 63 und 51? C l ( m a in lib ) 2-Pro p e n o y l c h lo rid e, 3-p h e n y l- b) Gegeben ist das folgende EI-Massenspektrum (M = 194 u). Br = 79/81 u Wie entstehen die Signale bei = 179, 165, 121, 93 und 57? ( m a in lib ) Bro m o a c e tic a c id, 2 -b u ty l e ste r Br 165
5 c) Gegeben ist das folgende EI-Massenspektrum (M 174 u). Br = 79/81 u Wie entstehen die Signale bei = 95, 81 (zwei Signale), 79 und 67? Wie kann man messtechnisch die Identität der Ionen bei 79 und 81 ganz einfach nachweisen? ( m a in lib ) C y c lo h e xe n e, 3 -( b ro m o m e th y l) - Br d) Gegeben ist das folgende EI-Massenspektrum (M 156 u). S = 32 u Wie entstehen die Signale bei = 141, 128, 111, 83 und 39? S ( m a in lib ) Th io p h e n e -2 -c a rb o xy lic a c id e th y l e ste r
6 e) Gegeben ist das folgende EI-Massenspektrum (M = 183 u). F = 19 u Wie entstehen die Signale bei = 165, 138, 19, 74? 1 74 H H 2 F ( m a in lib ) D,L-p -Flu o ro p h e n y la la n in e f) Gegeben ist das folgende EI-Massenspektrum (M = 268 u). Si = 28 u Wie entstehen die Signale bei = 253, 29, 135 und 73? Si ( m a in lib ) Be n ze n e a c e tic a c id, 4-m e th o xy -à -[( trim e th y lsily l) o xy ]-, m e th y l e ste r
7 Massenspektrometrie Übung 3: a) Welche Masse wird bei einer Massenfeinbestimmung gemessen und wofür liefert das Ergebnis entscheidende Hinweise? Welche andere Bezeichnung ist für so eine Messung noch üblich? b) Welche Elektronenenergie wird standardmäßig bei Elektronenstoß Ionisation (EI) verwendet und aus welchen zwei Gründen? Für welche datentechnische Auswertung ist einer Voraussetzung? c) Welche Chromatographie Methode ist ideal zur Kopplung mit Elektronenstoß Ionisation (EI)? Welche prinzipielle Art von Trennsäulen wird dabei verwendet und aus welchem Grund? d) Welche drei Ionensorten unterschiedlicher Lebensdauer erzeugt Elektronenstoß Ionisation (EI)? e) ennen Sie ein ein übliches Reaktandgas für Chemische Ionisation (CI) und dessen Reaktandgas Ion. Welches Problem kann bei Substanzen mit Hydroxylgruppen auftreten? f) Was ist das sogenannte Säulenbluten bei GC/MS und welche Verbindungen sind für moderne Gaschromatographie-Säulen besonders gefährlich? g) Eine Verbindung zeigt bei Elektronenstoß Ionisation (EI)-GC/MS im Massenspektrum keinen Molekülpeak. Welche alternative Ionisierungs-Methode ist für diese Kopplung geeignet? Welche Art von Ionen erwartet man dabei und durch welche Art von Reaktion werden sie erzeugt? h) ennen Sie zwei Einlass-Systeme, die gut für die Elektronenstoß Ionisation (EI) geeignet sind und jeweils deren Vorteil gegenüber anderen Einlass-Systemen. i) Welche massenspektrometrische Methode (Einlass-System und Ionisierung) ist geeignet, eine kleine leicht flüchtige Verbindung zu identifizieren und zu quantifizieren, die als Dopingmittel eingenommen wurde. Mit welchen Analysatoreigenschaften kann man diese Messung verbessern und welche zusätzlichen Substanzen braucht man noch für die Quantifizierung? j) Welche Proben-Eigenschaft ist die Voraussetzung dafür, ein Elektronenstoß Ionisations (EI) Massenspektrum zu erhalten? Anhand welcher anderen Proben-Eigenschaft kann man dieses einfach abschätzen? Welches Einlass-System kann diese Problematik teilweise umgehen? k) Skizzieren Sie das Innere einer Elektronenstoß (EI)-Ionenquelle im Moment der Ionisation.
8 Massenspektrometrie Übung 4: a) Welche typische Art von Ionen erwartet man bei Elektrospray (ESI) und welche Zahlen sind im Vergleich zu anderen Ionisierungs-Methoden dabei ungewöhnlich hoch? Welche sehr praktischen Vorteile hat das für die Auswahl eines entsprechenden Massenspektrometers und warum? b) ennen Sie zwei verschiedene Masse Analysatoren und jeweils einen ihrer Vorteile. c) Welche mit der Chemischen Ionisation (CI) verwandte Ionisierungs-Methode ist bei einer LC/MS Kopplung gebräuchlich? Wodurch ist der Anteil der mit diese Technik erfassbaren Substanzen immer noch eingeschränkt und bei welcher alternativen LC/MS Methode gilt die Einschränkung nicht mehr? Wodurch ergibt sich ein prinzipielles Problem bei solchen LC/MS Kopplungen? d) ennen Sie zwei der vier möglichen MS/MS Experimente und erklären Sie diese kurz. e) Was ist die prinzipielle Problematik bei einer Kopplung von Flüssigkeitschromatographie und Massenspektrometrie (1 P) und welche instrumentelle Lösung wird dagegen verwendet (1 P)? Welcher Ansatz begründet dabei die höhere Empfindlichkeit eines API-LC/MS Interfaces (1 P)? f) Welche oft als Verunreinigung auftauchende Verbindungsklasse kann Fast Atom Bombardment (FAB) Messungen empfindlich stören und warum? g) ennen Sie zwei, prinzipiell unterschiedliche, Ionisierungs-Methoden für polare schwer flüchtige Verbindungen mit der entsprechenden Abkürzung und einem geeigneten Einlass-System. h) Aus welchen zwei Gründen sind TF Analysatoren besonders geeignet für die Matrix Assisted Laser Desorption Ionisation (MALDI)? i) Welche 3 Schritte finden bei Produktionen MS/MS statt? Was ist der Unterschied zur unspezifischen Variante, die bei Atmosphärendruck Ionisationen möglich ist? j) ennen Sie die zwei Theorien, die zum Elektrospray (ESI) Ionisierungs-Mechanismus aufgestellt wurden und die andere Ionisierungs-Methode, auf die eine dieser Theorien angewendet wird. k) Skizzieren Sie den Aufbau eines LC/MS Interfaces für die Elektrospray Ionisation (ESI).
9 Massenspektrometrie Übung 1 Lösung: a) Gegeben ist das folgende EI-Massenspektrum (M = 148 u). Wie entstehen die Signale bei = 133, 15, 91, 77 und 43? ( m a in lib ) 2-Bu ta n o n e, 4-p h e n y l α V + -. CH 3 - C α -. R i -. R Bz -. R + + CH 3 C
10 b) Gegeben ist das folgende EI-Massenspektrum (M = 197 u). Wie entstehen die Signale bei = 12, 92, 77 und 65? Welche Information zur Summenformel kann man direkt aus dem Molekülpeak entnehmen? H ( m a in lib ) Be n ze n a m in e, 2 -( p h e n y la zo H H 2 H 2 α V + -. C 6 H 5-2 α -. C 6 H 4 H i -. 2 C 6 H 4 H 2 + WU 15 (kaum sichtbar) + V V H H 77 Stickstoffregel weist auf ungerade Zahl von Stickstoffen im Molekül hin (1 P). - CH 65 92
11 c) Gegeben ist das folgende EI-Massenspektrum (M 129 u). Wie entstehen die Signale bei = 112, 99, 85, 84 und 71? Tipp: 85 entsteht aus einer tautomeren Molekülstruktur H H ( m a in lib ) -M e th y lm a le a m ic a c id H +. + H α V + H H -. H - C H H H H α V + -. HCH 2 - C H H H Keto-Enol H Tautomerie. Mc +. H + H +. H H H - C 2 H H H H H
12 d) Gegeben ist das folgende EI-Massenspektrum (M 129 u). Wie entstehen die Signale bei = 114, 86 (zwei Signale), 58 (zwei Signale) und 3? ( m a in lib ) D ie th y la m in o a c e to n e α CH C 2 H 4 H + n α -. CCH 3 n - CH 2 C()CH 2 n - CH 2 C()CH 2 n + n H + - C 2 H 4 - C 2 H 4 [CH 2 =H 2 ] α -. CH 3 V - C + +. Mc +. - CH 3 -CH=-CH 2 -CH 3 inklusive folgender Keto-Enol Tautomerie 58
13 e) Gegeben ist das folgende EI-Massenspektrum (M 137 u). Wie entstehen die Signale bei = 121, 12, 93 und 92? (Intensitäten beachten!) 1 12 H 137 H ( m a in lib ) Sa lic y la m id e H H α = Bz H V H + -. H 2 - C (zu intensiv für 13 C!) (zu intensiv für 13 C!) WU achbargruppeneffekt + H El V - H 3 - C
14 f) Gegeben ist das folgende EI-Massenspektrum (M 137 u). Wie entstehen die Signale bei = 16, 78, 51 und 31? Tipp: 31 entsteht aus einem nicht sichtbaren Fragment! H 2 H ( m a in lib ) Iso n ia zid H2 +. H + + α V -. HH2 - C α -. R V - CH H2 H + - C + H2 V (nicht sichtbar) H
15 Massenspektrometrie Übung 2 Lösung: a) Gegeben ist das folgende EI-Massenspektrum (M = 166 u). Cl = 35/37 u Wie entstehen die Signale bei = 131, 13, 77, 63 und 51? C l ( m a in lib ) 2-Pro p e n o y l c h lo rid e, 3-p h e n y l- +. Cl α = i V -. Cl - C V 13 i - C 2 H 2 α -. R -. R + V - C 2 H 2 + Cl-C
16 b) Gegeben ist das folgende EI-Massenspektrum (M = 194 u). Br = 79/81 u Wie entstehen die Signale bei = 179, 165, 121, 93 und 57? ( m a in lib ) Bro m o a c e tic a c id, 2-b u ty l e st e r Br Br +. α 194 α -. CH α -. C 4 H 9 -. CH 2 CH Br Br + Br V Br - C + 93 Br +. i -. C()CH 2 Br auch ok durch α (-. CH 2 Br) plus V (- C 2 )
17 c) Gegeben ist das folgende EI-Massenspektrum (M 174 u). Br = 79/81 u Wie entstehen die Signale bei = 95, 81 (zwei Signale), 79 und 67? Wie kann man messtechnisch die Identität der Ionen bei 79 und 81 ganz einfach nachweisen? ( m a in lib ) C y c lo h e xe n e, 3 -( b ro m o m e th y l) - Br i RDA Br Br - C 2 H Allyl σ -. CH 2 Br + -. R Br + Br Br /81 Die Identität der Br-Ionen bei 81 und 79 kann man durch Bestimmung der exakten Masse mit einer Hochauflösungs-Messung nachweisen: 79 Br/ 81 Br 78.9/8.9
18 d) Gegeben ist das folgende EI-Massenspektrum (M 156 u). S = 32 u Wie entstehen die Signale bei = 141, 128, 111, 83 und 39? S ( m a in lib ) Th io p h e n e -2 -c a rb o xy lic a c id e th y l e ste r +. + S α S V S -. Et - C Mc - C 2 H 4 V - CHS α -. CH 3 +. S H S
19 e) Gegeben ist das folgende EI-Massenspektrum (M = 183 u). F = 19 u Wie entstehen die Signale bei = 165, 138, 19, 74? H 5 H 2 F ( m a in lib ) D,L-p -Flu o ro p h e n y la la n in e H CH 2 C 6 H 4 F + H 2 F α H 2 H = 183 = 74 α -. CH Bz -. CH(H 2 )CH 138 über α (-. H) + = 19 H F H2 + plus V (C) auch ok = 138 Wasserstoffumlagerung +. vom Ring aus auch ok F H 2 El + - H 2. = 183 = 165 H F F
20 f) Gegeben ist das folgende EI-Massenspektrum (M = 268 u). Si = 28 u Wie entstehen die Signale bei = 253, 29, 135 und 73? Si ( m a in lib ) Be n ze n e a c e tic a c id, 4-m e th o xy -à -[( trim e th y lsily l) o xy ]-, m e th y l e ste r Si α -. CH Si = 268 = 253 i -. R α = Bz -. C()CH 3 + Si = Si WU + V - HSi(CH 3 ) 3 = 29 = 135
21 Massenspektrometrie Übung 3 Lösung: a) Welche Masse wird bei einer Massenfeinbestimmung gemessen und wofür liefert das Ergebnis entscheidende Hinweise? Welche andere Bezeichnung ist für eine solche Messung noch üblich? 1. Exakte Masse 2. Summenformel 3. Hochauflösung b) Welche Elektronenenergie wird standardmäßig bei Elektronenstoß Ionisation (EI) verwendet und aus welchen zwei Gründen? Für welche datentechnische Auswertung ist einer Voraussetzung? 1. 7 ev 2. Ionenstrom ist maximal 3. Überschussenergie führt zu reproduzierbarer Fragmentierung 4. Bibliothekssuche c) Welche Chromatographie Methode ist ideal zur Kopplung mit Elektronenstoß Ionisation (EI)? Welche prinzipielle Art von Trennsäulen wird dabei verwendet und aus welchem Grund? 1. Gaschromatographie (GC) 2. Kapillarsäulen 3. Direkte Kopplung wegen geringem Gasstrom möglich d) Welche drei Ionensorten unterschiedlicher Lebensdauer erzeugt Elektronenstoß Ionisation (EI)? 1. Molekülionen 2. Fragmentionen 3. Metastabile Ionen
22 e) ennen Sie ein ein übliches Reaktandgas für Chemische Ionisation (CI) und dessen Reaktandgas Ion. Welches Problem kann bei Substanzen mit Hydroxylgruppen auftreten? 1. Ammoniak: H 4 + oder Methan: CH 5 + oder Isobutan: C 4 H Keine Quasimolekülionen durch Wasserverlust f) Was ist das sogenannte Säulenbluten bei GC/MS und welche Verbindungen sind für moderne Gaschromatographie-Säulen besonders gefährlich? 1. Zersetzung der stationären Phase 2. Starke Säuren oder Basen, sowie Verbindungen aus denen sie im Injektor entstehen g) Eine Verbindung zeigt bei Elektronenstoß Ionisation (EI)-GC/MS im Massenspektrum keinen Molekülpeak. Welche alternative Ionisierungs-Methode ist für diese Kopplung geeignet? Welche Art von Ionen erwartet man dabei und durch welche Art von Reaktion werden diese erzeugt? 1. Chemische Ionisation (CI) 2. [M+H] + 3. Protonentransfer Ion Molekül Reaktion h) ennen Sie zwei Einlass-Systeme, die gut für die Elektronenstoß Ionisation (EI) geeignet sind und jeweils deren Vorteil gegenüber anderen Einlass-Systemen. z. B. Reservoir Einlass (RI): gute Regulierbarkeit Direktinsertions Probe (DIP): Schutzgasverwendung Direktverdampfungs Probe (DEP): wenig Zersetzung Gaschromatographie (GC): Substanztrennung Flüssigkeitschromatographie (LC): Substanztrennung, aber schlechter als GC
23 i) Welche massenspektrometrische Methode (Einlass-System und Ionisierung) ist geeignet, eine kleine leicht flüchtige Verbindung zu identifizieren und zu quantifizieren, die als Dopingmittel eingenommen wurde. Mit welchen Analysatoreigenschaften kann man diese Messung verbessern und welche zusätzlichen Substanzen braucht man noch für die Quantifizierung? 1. GC/EI oder GC/CI 2. Hochauflösung 3. Isotopenmarkierte Standards j) Welche Proben-Eigenschaft ist die Voraussetzung dafür, ein Elektronenstoß Ionisations (EI) Massenspektrum zu erhalten? Anhand welcher anderen Proben-Eigenschaft kann man dieses einfach abschätzen? Welche Einlass-System kann diese Problematik teilweise umgehen? 1. Flüchtigkeit oder unzersetzte Verdampfbarkeit 2. Löslichkeit in unpolaren Lösungsmitteln 3. Direktverdampfungs Probe (DEP) k) Skizzieren Sie das Innere einer Elektronenstoß (EI)-Ionenquelle im Moment der Ionisation.
24 Massenspektrometrie Übung 4 Lösung: a) Welche typische Art von Ionen erwartet man bei Elektrospray (ESI) und welche Zahlen sind im Vergleich zu anderen Ionisierungs-Methoden dabei ungewöhnlich hoch? Welche sehr praktischen Vorteile hat das für die Auswahl eines entsprechenden Massenspektrometers und warum? 1. Mehrfach geladene Ionen 2. Sehr hohe Ladungszahlen z 3. Große Moleküle an Geräten mit geringem Massenbereich messbar 4. Bei hoher Ladungszahl z wird von großen Molekülen kleiner b) ennen Sie zwei verschiedene Masse Analysatoren und jeweils einen ihrer Vorteile. z. B. Sektorfeld: Massenfeinbestimmung, alternativ Hochauflösung FTMS: Massenfeinbestimmung, alternativ Hochauflösung, MS/MS rbitrap: Massenfeinbestimmung, alternativ Hochauflösung, MS/MS Quadrupol: Einfachheit, alternativ Kosten Flugzeit: hoher Massenbereich, alternativ Hochauflösung Ionenfalle: Einfachheit, alternativ MS/MS c) Welche mit der Chemischen Ionisation (CI) verwandte Ionisierungs-Methode ist bei einer LC/MS Kopplung gebräuchlich? Wodurch ist der Anteil der mit diese Technik erfassbaren Substanzen immer noch eingeschränkt und bei welcher alternativen LC/MS Methode gilt die Einschränkung nicht mehr? Wodurch ergibt sich ein prinzipielles Problem bei solchen LC/MS Kopplungen? 1. Atmosphärendruck Chemische Ionisation (APCI) 2. Probe muss unzersetzt verdampfbar sein 3. Elektrospray Ionisation (ESI) 4. Hohes Laufmittelvolumen <> Hochvakuum im Massenspektrometer
25 d) ennen Sie zwei der vier möglichen MS/MS Experimente und erklären Sie diese kurz. Produkt-Ionen: MS1: Selektion MS2: Scan Vorläufer-Ionen: MS1: Scan MS2: Selektion eutralverlust: MS1: Scan MS2: Scan mit negativer Massendifferenz eutralanlagerung: MS1: Scan MS2: Scan mit positiver Massendifferenz e) Was ist die prinzipielle Problematik bei einer Kopplung von Flüssigkeitschromatographie und Massenspektrometrie (1 P) und welche instrumentelle Lösung wird dagegen verwendet (1 P)? Welcher Ansatz begründet dabei die höhere Empfindlichkeit eines API-LC/MS Interfaces (1 P)? 1) Hohes Laufmittelvolumen <> Hochvakuum im Massenspektrometer 2) Mehrstufiges Vakuumpumpen- und Skimmersystem, Particle Beam war auch ok 3) Unter Atmosphärendruck erzeugte Ionen werden aktiv ins Massenspektrometer gezogen f) Welche oft als Verunreinigung auftauchende Verbindungsklasse kann Fast Atom Bombardment (FAB) Messungen empfindlich stören und warum? 1. Silikone, z. B. Schlifffett 2. Wegen ihrer hohen berflächenaktivität g) ennen Sie zwei, prinzipiell unterschiedliche, Ionisierungs-Methoden für polare schwer flüchtige Verbindungen mit der entsprechenden Abkürzung und einem geeigneten Einlass-System. z. B. Fast Atom Bombardment (FAB): Targetanalyse Matrix Assisted Laser Desorption Ionisation (MALDI): Targetanalyse Elektrospray (ESI): LC/MS
26 h) Aus welchen zwei Gründen sind TF Analysatoren besonders geeignet für die Matrix Assisted Laser Desorption Ionisation (MALDI)? 1. Sehr hoher erfassbarer Massenbereich 2. Gepulster TF Analysator passt zu gepulster MALDI Ionisierung i) Welche 3 Schritte finden bei Produktionen MS/MS statt? Was ist der Unterschied zur unspezifischen Variante, die bei Atmosphärendruck Ionisationen möglich ist? 1. a) Selektion einen Ions, b) Stoßaktivierung mit Stoßgas, c) Scan der Produktionen 2. Keine Selektion, alle vorhandenen Ionen werden gleichzeitig gestoßen j) ennen Sie die zwei Theorien, die zum Elektrospray (ESI) Ionisations-Mechanismus aufgestellt wurden und die andere Ionisierungs-Methode, auf die eine dieser Theorien angewendet wird. 1. Ionenverdampfung 2. Ladungsrückstand 3. Atmosphärendruck Chemische Ionisation (APCI): Ladungsrückstand k) Skizzieren Sie den Aufbau eines LC/MS Interfaces für die Elektrospray Ionisation (ESI).
27 Massenspektrometrie Übung 1 alt: 1. Welche Verbindungen zeigen folgende EI Massenspektren, ()? Isotopenmuster beachten! a) 27 (2.2), 26 (1), 25 (23), 24 (6.1), 13 (3.6), 12 (.9) b) 28 (1.6), 27 (1), 26 (17), 14 (1.6), 13.5 (.9), 13 (1.7), 12 (4.2) c) 31 (1.3), 3 (89), 29 (1), 28 (31), 16 (1.7), 14 (4.4), 13 (4.3), 12 (3.3) d) 35 (1.1), 34 (1), 33 (89), 32 (4.4), 31 (7.7), 16 (.1), 15 (12), 14 (3.1), 13 (1.2), 12 (.5) e) 38 (33), 37 (4.1), 36 (1), 35 (12) f) 66 (5.), 65 (.9), 64 (1), 5 (2.3), 49 (.4), 48 (49), 34 (.4), 33 (.1), 32 (1.), 16 (.5) g) 71 (3), 52 (1), 33 (36), 19 (8.4), 14 (5.2) h) 16 (.2), 14 (.7), 87 (5.9), 86 (.2), 85 (18), 7 (1.2), 69 (1), 5 (6.3), 37 (1.), 35 (3.) 2. Welche Substanzen ergeben folgende EI Massenspektren? Isotopen Peaks beachten! a) (6.8 ) b) Was ist die mittlere Molekülmasse von 1-Brom-4-iodbenzol, was die nominelle Masse und was die exakte Masse? Welche wird durch LR MS, HR MS und CHS Elementaranalyse bestimmt? 4. Ein aus Pflanzenmaterial isolierter Kohlenwasserstoff, der in der Literatur nach Elementaranalyse als C 3 H 62 beschrieben wurde, zeigt im oberen Bereich des EI Massenspektrums 436 (1 ), 421 (5 ), 48 (16 ) und 393 (8 ). Welche Schlüsse kann man daraus ziehen? 5. Wie groß ist der Unterschied der exakten Massen von Ionen der Summenformeln C 22 H 14 2 und C 18 H 16 4 in mmu? Wieviel in ppm? Welche Auflösung ist nötig um die Signale nach der 1 Tal Definition zu trennen? Wieviel nach der FWHM Definition?
28 Massenspektrometrie Übung 2 alt: 1. Wie entstehen die Signale bei = 55, 45, 27 im EI Massenspektrum von Acrylsäure (M 72 u)? H 2. Drei isomere Ketone (M 86 u) haben die Summenformel C 5 H 1. Welche EI Fragmente gehören zu welchen Strukturen? a) = 57, 29 b) = 71, 43 c) = 71, 58, Wie entstehen = 119, 15, 91, 77 im EI Massenspektrum von 2-Phenylbutan (M 134 u)? 4. Welche zwei Hauptfragmente sind im EI Spektrum von Cyclohexen (M 82 u) zu erwarten? 5. Gegeben ist das EI Massenspektrum von 4-,-Dimethylaminobenzoesäureethylester (M 193 u). Wie entstehen die Fragmente bei = 192, 178, 165, 164, 148?
29 Massenspektrometrie Übung 3 alt: 1. Warum zeigt Ethylthiol (M 62 u) im EI Spektrum = 29, Butylthiol (M 9 u) aber = 56? CH 3 -CH 2 -SH CH 3 -CH 2 -CH 2 -CH 2 -SH 2. Wie unterscheiden sich die folgenden Amine (M 73 u) in ihren EI Fragmentierungsmustern? a) (CH 3 ) 3 C-H 2 b) CH 3 -CH 2 -H-CH 2 -CH 3 c) CH 3 -CH 2 -CH 2 -CH 2 -H 2 d) CH 3 -CH 2 -CH(CH 3 )-H 2 3. Wie entstehen die Signale bei = 82, 81, 55 im EI Spektrum von Hydrochinon (M 11 u)? H H 4. p-toluylsäure und o-toluylsäure (M 136 u) zeigen verschiedene EI Fragmentierungen. Wieso? CH 3 H 3 C C 2 H C 2 H = 119, 91, 65 = 119, 118, 91, 9, Wie entstehen = 21, 136, 18 im EI Massenspektrum von 7-Hydroxyflavon (M 238 u)? H
30 Massenspektrometrie Übung 1 alt Lösung: 1. a) 27 (2.2), 26 (1), 25 (23), 24 (6.1), 13 (3.6), 12 (.9) 13 C -> Kohlenstoffanzahl CHCH: CHCH +., 26 CHCH +., 25 CHC +, 24 CC +., 13 CH +, 12 C + Acethylen b) 28 (1.6), 27 (1), 26 (17), 14 (1.6), 13.5 (.9), 13 (1.7), 12 (4.2) Stickstoffregel, 13.5 z=2 HC: 28 H 13 C +., 27 HC +., 26 C +, 14 +, 13.5 HC 2+, 13 CH +, 12 C + Blaus äure c) 31 (1.3), 3 (89), 29 (1), 28 (31), 16 (1.7), 14 (4.4), 13 (4.3), 12 (3.3) CH 2 : CH 2 +., 3 CH 2 +., 29 CH +, 28 C +., 16 +, 14 CH 2+, 13 CH +, 12 C + Formaldehyd d) 35 (1.1), 34 (1), 33 (89), 32 (4.4), 31 (7.7), 16 (.1), 15 (12), 14 (3.1), 13 (1.2), 12 (.5) CH 3 F: CH 3 F +., 34 CH 3 F +., 33 CH 2 F +, 32 CHF +., 31 CF +, CH 3+, 15 CH 3+, 14 CH 2+,... Methylfluorid e) 38 (33), 37 (4.1), 36 (1), 35 (12) Cl Isotopenmuster HCl: 38 H 37 Cl +., Cl +, 36 HCl +., 35 Cl + Salzäure f) 66 (5.), 65 (.9), 64 (1), 5 (2.3), 49 (.4), 48 (49), 34 (.4), 33 (.1), 32 (1.), 16 (.5) S 2 : S 2, S 2, 64 S 2, 5 34 S +, S +, 48 S +, S +, S +, 32 S +, 16 + Schwefeldioxid g) 71 (3), 52 (1), 33 (36), 19 (8.4), 14 (5.2) Stickstoffregel F 3 : 71 F +. 3, 52 F 2+, 33 F +., 19 F +, 14 + Stickstofftrifluorid keine Isotope! h) 16 (.2), 14 (.7), 87 (5.9), 86 (.2), 85 (18), 7 (1.2), 69 (1), 5 (6.3), 37 (1.), 35 (3.) ClCF 3 : ClCF 3 +., 14 ClCF 3 +., ClCF 2+, 86 Cl 13 CF 2+, 85 ClCF 2+, 7 13 CF 3+, 69 CF 3+, CF 2 + Chlortrifluormethan 2. a) Benzol (78 u) C -> 6 C 6 x 12 = = 6 79 (6.8 ) -> 6 C + 6 H => Benzol b) Trichlorbenzol (18 u) 18 Isotopenmuster 18 -> 3 Cl -Cl. - HCl -Cl. 3 x 35 = = > 75 = 78-3H => Trichlorbenzol 3. C 6 H 4 BrI -> mittlere Masse : CHS, nominelle Masse 282: LR, exakte Masse : HR 4. M (C 3 H 62 ) = 422 u --> u (CH 2 ) und u (CH 2 ) --> falsche Summenformel, weil Mittelwert zweier Substanzen in Elementaranalyse gemessen. Bestätigung durch zwei [M CH 3 ] Fragmente: 421 aus 436 und 393 aus 48. Lösungsansatz: GC/MS durchführen! 5. m1 = , m2 = , m =.85 u = 8.5 mmu (27 ppm) -> R = ( FWHM )
31 Massenspektrometrie Übung 2 alt Lösung: 1. Wie entstehen die Signale bei = 55, 45, 27 im EI Massenspektrum von Acrylsäure (M 72 u)? 55: [M H. ] + α 1 27: [55 C] + V H 45: [M CH 2 =CH. ] + α 2 2. Drei isomere Ketone (M 86 u) haben die Summenformel C 5 H 1. Welche EI Fragmente gehören zu welchen Strukturen? a) CH 3 -CH 2 -C()-CH 2 -CH 3 57: [M CH 3 -CH 2. ] + α 29: [57 C] + V b) CH 3 -C()-CH(CH 3 ) 2 71: [M CH 3. ] + α 1 43: [71 C] + V 43: [M CH(CH 3 ) 2. ] + α 2 15: [43 C/C 2 H 4 ] + V c) CH 3 -C()-CH 2 -CH 2 -CH 3 71: [M CH 3. ] + α 1 43: [71 C] + V 58: [M CH 2 =CH 2 ] +. Mc ----> [CH 3 -C()-CH 3 ] +. Keto Enol 43: [M CH 3 -CH 2 -CH 2. ] + α 2 43: [58 CH 3. ] + α 3 15: [43 C] + V 3. Wie entstehen die Peaks bei = 119, 15, 91, 77 im EI Massenspektrum von 2-Phenylbutan (M 134 u)? 119: [M CH 3. ] + Bz 1 15: [M. CH 2 -CH 3 ] + Bz 2 77: [M CH(CH 3 )(CH 2 -CH 3 ). ] + Ph 16: Mc (nicht zu sehen!) 79: [15 C 2 H 2 ] + V analog Aromatenabbau 91: [16 CH 3. ] + Bz 3 4. Welche zwei Hauptfragmente sind im EI Spektrum von Cyclohexen (M 82 u) zu erwarten?. 67: Al öffnet Ring --> WU analog Cyclohexanon -- α / -CH 3 --> [C 5 H 7 ] + 54: M RDA / - C 2 H 4 --> [C 4 H 6 ] +. 81: [M H. ] + α (sehr klein) 5. Gegeben ist das EI Massenspektrum von 4-,-Dimethylaminobenzoesäureethylester (M 193 u). Wie entstehen die Fragmente bei = 165, 164, 148? 148: [M -. CH 2 CH 3 ] + α am Ester 165: Mc vom Ethyl-CH 3 zum doppeltgebundenem : [(CH 3 ) 2 C 6 H 4 C 2 H] : [165 H. ] + α am Stickstoff: [CH 2 (CH 3 )C 6 H 4 C 2 H] + 192: [M H. ] + α möglich an Stickstoff-CH 3 oder Ethyl-CH 3 178: [M CH 3. ] + α am Ethylrest
32 Massenspektrometrie Übung 3 alt Lösung: 1. Warum zeigt Ethylthiol (M 62 u) im EI Spektrum = 29, Butylthiol (M 9 u) aber = 56? Ethylthiol 29: [M. SH] + i, kein 6 Ring Übergangszustand möglich Butylthiol 56: [M H 2 S] +. El, 5 und 6 Ring Übergangszustände möglich 2. Wie unterscheiden sich die folgenden Amine (M 73 u) in ihren EI Fragmentierungsmustern? a) (CH 3 ) 3 C-H 2 M α / - CH 3 --> [(CH 3 ) 2 C=H 2 ] + 58 b) CH 3 -CH 2 -H-CH 2 -CH 3 M α1 / - CH 3 --> [CH 3 CH 2 H=CH 2 ] n / - C 2 H 4 --> [H 2 =CH 2 ] + 3 M α2 / - H. --> [CH 3 CH 2 H=CHCH 3 ] n / - C 2 H 4 --> [H 2 =CHCH 3 ] + 44 c) CH 3 -CH 2 -CH 2 -CH 2 -H 2 M α1 / - C 3 H 7 --> [CH 2 =H 2 ] + 3 M α2 / - H. --> [CH 3 CH 2 CH 2 CH=H 2 ] n / - C 3 H 6 --> [CH 2 =H 2 ] Mc / - C 2 H 4 --> Tautomerie -o-> [CH 3 CH=H 2 ] + 44 d) CH 3 -CH 2 -CH(CH 3 )-H 2 M α1 / - CH 3 --> [CH 3 CH 2 CH=H 2 ] n / - C 2 H 4 --> [CH 2 =H 2 ] + 3 M α2 / - H. --> [CH 3 CH 2 CH(CH 3 )=H 2 ] n / - C 2 H 4 --> [CH 3 CH=H 2 ] + 44 M α3 / - C 2 H 5 --> [CH 3 CH=H 2 ] Wie entstehen die Signale bei = 82, 81, 55 im EI Spektrum von Hydrochinon (M 11 u)? H H 82: M WU+V / - C --> [C 5 H 6 ] +. 81: [C 5 H 6 ] Al / - H. --> [C 5 H 5 ] + Fünfring mit H 55: [C 5 H 5 ] + -- V / - C 2 H 2 --> [C 3 H 3 ] + Dreiring mit H 4. p-toluylsäure und o-toluylsäure (M 136 u) zeigen verschiedene EI Fragmentierungen. Wieso? p-tolylsäure: 119: [M H. ] + Bz o-tolylsäure: 119, 91, 65: Siehe p-tolylsäure 91: [119 C] + V 118: [M H 2 ] +. rtho Effekt 65: [91 C 2 H 2 ] + V 9: [118 C] +. V 5. Wie entstehen = 21, 136, 18 im EI Massenspektrum von 7-Hydroxyflavon (M 238 u)? 21: [M C] +. V aus dem Ketonring 136: RDA unter Verlust von CHCC 6 H 6 18: [RDA C] +. V aus dem RDA Fragment
Massenspektrometrie Eine Einführung
 Herbert Budzikiewicz, Mathias Schäfer Massenspektrometrie Eine Einführung Fünfte, vollständig überarbeitete und aktualisierte Auflage WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA Inhaltsverzeichnis Vorwort
Herbert Budzikiewicz, Mathias Schäfer Massenspektrometrie Eine Einführung Fünfte, vollständig überarbeitete und aktualisierte Auflage WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA Inhaltsverzeichnis Vorwort
Teil 4 Massenspektrometrie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
Literatur zur Massenspektrometrie
 Literatur zur Massenspektrometrie 1. M. Hesse, H. Meier, B. Zeeh: Spektroskopische Methoden in der organischen Chemie. Georg Thieme Verlag, Stuttgart, 8. Auflage 2012, 79.95; ISBN 9783135761084 Behandelt
Literatur zur Massenspektrometrie 1. M. Hesse, H. Meier, B. Zeeh: Spektroskopische Methoden in der organischen Chemie. Georg Thieme Verlag, Stuttgart, 8. Auflage 2012, 79.95; ISBN 9783135761084 Behandelt
Inhaltsverzeichnis. Vorwort zur 6. Auflage XI Aus dem Vorwort zur 1. Auflage XIII. Einleitung. Teil I Grundlagen 1.
 O:/Wiley/Budzikiewicz/3d/ftoc.3d from 13.06.2012 13:10:49 V Vorwort zur 6. Auflage XI Aus dem Vorwort zur 1. Auflage XIII Einleitung XV Teil I Grundlagen 1 1 Terminologie 3 2 Apparative Grundlagen 9 2.1
O:/Wiley/Budzikiewicz/3d/ftoc.3d from 13.06.2012 13:10:49 V Vorwort zur 6. Auflage XI Aus dem Vorwort zur 1. Auflage XIII Einleitung XV Teil I Grundlagen 1 1 Terminologie 3 2 Apparative Grundlagen 9 2.1
Teil 4 Massenspektrometrie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Funktionseinheiten eines Massenspektrometers Grundprinzip der MS: Trennung von Ionen nach
Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Funktionseinheiten eines Massenspektrometers Grundprinzip der MS: Trennung von Ionen nach
Schonende Ionisierungsmethoden
 Schonende Ionisierungsmethoden Warum? Zersetzung des Moleküls beim Erhitzen Instabiles Molekülion nicht verdampfbare Probensubstanz Zielsetzung/Möglichkeiten: Geringerer Energieeintrag in das entstehende
Schonende Ionisierungsmethoden Warum? Zersetzung des Moleküls beim Erhitzen Instabiles Molekülion nicht verdampfbare Probensubstanz Zielsetzung/Möglichkeiten: Geringerer Energieeintrag in das entstehende
~WILEY. Massenspektrometrie YCH. Herbert Budzikiewicz und Mathias Schäfer. Eine Einführung. 6., vollständig überarbeitete und aktualisierte Auflage
 Herbert Budzikiewicz und Mathias Schäfer Massenspektrometrie Eine Einführung 6., vollständig überarbeitete und aktualisierte Auflage ~WILEY YCH WILEY-VCH Verlag GmbH & Co. KGaA Vorwort zur 6. Auflage XI
Herbert Budzikiewicz und Mathias Schäfer Massenspektrometrie Eine Einführung 6., vollständig überarbeitete und aktualisierte Auflage ~WILEY YCH WILEY-VCH Verlag GmbH & Co. KGaA Vorwort zur 6. Auflage XI
Spektroskopie-Seminar SS 18 8 Massenspektrometrie Massenspektrometrie
 SS 18 Massenspektrometrie 1 8.1 Prinzip Methode zur Bestimmung der Masse von Molekülen Analyt wird in die Gasphase überführt Moleküle werden ionisiert und durch elektrisches Feld beschleunigt Auftrennung
SS 18 Massenspektrometrie 1 8.1 Prinzip Methode zur Bestimmung der Masse von Molekülen Analyt wird in die Gasphase überführt Moleküle werden ionisiert und durch elektrisches Feld beschleunigt Auftrennung
Spektroskopie in der Organischen Chemie. Massenspektren
 Massenspektren In der Frühzeit der MS wurden Spektren auf Fotopapier registriert, wobei das Spektrum mehrfach mit unterschiedlicher Ordinatenauslenkung ausgeschrieben wurde, um sehr schwache neben sehr
Massenspektren In der Frühzeit der MS wurden Spektren auf Fotopapier registriert, wobei das Spektrum mehrfach mit unterschiedlicher Ordinatenauslenkung ausgeschrieben wurde, um sehr schwache neben sehr
DISSERTATION. Diplom-Ingenieur Robert Koob. Darmstadt 2000 D 17
 Massenspektrometrische Methode zur Bestimmung der 13 C-Einbaurate und -position in Äpfelsäure bei der CO 2 -Aufnahme von CAM-Pflanzen Vom Fachbereich Chemie der Technischen Universität Darmstadt zur Erlangung
Massenspektrometrische Methode zur Bestimmung der 13 C-Einbaurate und -position in Äpfelsäure bei der CO 2 -Aufnahme von CAM-Pflanzen Vom Fachbereich Chemie der Technischen Universität Darmstadt zur Erlangung
Massenspektrometrie (MS)
 Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
2 Massenspektrometrie
 2 Massenspektrometrie 2.1 Grundlagen relative Atommasse Massenzahl Summe relative Molekülmasse M Isotope ein Element gleiche Protonenzahl, aber verschiedene Neutronenzahl Isobare Teilchen gleicher Masse,
2 Massenspektrometrie 2.1 Grundlagen relative Atommasse Massenzahl Summe relative Molekülmasse M Isotope ein Element gleiche Protonenzahl, aber verschiedene Neutronenzahl Isobare Teilchen gleicher Masse,
Massenspektrometrie (MS)
 Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Seminar WiSe 2015/2016
 Massenspektrometrie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Libi Leibniz Institut i für Naturstoff Forschung und Infektionsbiologie i E mail: markus.nett@hki jena.de Grundvorgänge
Massenspektrometrie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Libi Leibniz Institut i für Naturstoff Forschung und Infektionsbiologie i E mail: markus.nett@hki jena.de Grundvorgänge
1 Terminologie. 1) Die Bezeichnung Massenspektroskop wird praktisch nicht mehr verwendet; für Massenspektrograph siehe Abschnitt
 O:/Wiley/Budzikiewicz/3d/c01.3d from 13.06.2012 13:11:03 Teil I Grundlagen O:/Wiley/Budzikiewicz/3d/c01.3d from 13.06.2012 13:11:03 O:/Wiley/Budzikiewicz/3d/c01.3d from 13.06.2012 13:11:03 3 1 Terminologie
O:/Wiley/Budzikiewicz/3d/c01.3d from 13.06.2012 13:11:03 Teil I Grundlagen O:/Wiley/Budzikiewicz/3d/c01.3d from 13.06.2012 13:11:03 O:/Wiley/Budzikiewicz/3d/c01.3d from 13.06.2012 13:11:03 3 1 Terminologie
Schema einer Ionenquelle mit Elektronenstoßionisation Die dampfförmige Probe strömt senkrecht zur Bildebene in die Ionenquelle.
 Schema einer Ionenquelle mit Elektronenstoßionisation Die dampfförmige Probe strömt senkrecht zur Bildebene in die Ionenquelle. Ionenausbeute als Funktion der Primärenergie der Elektronen Reaktionen in
Schema einer Ionenquelle mit Elektronenstoßionisation Die dampfförmige Probe strömt senkrecht zur Bildebene in die Ionenquelle. Ionenausbeute als Funktion der Primärenergie der Elektronen Reaktionen in
Schema eines Massenspektrometer-Systems
 Vakuumsystem Probe - 8-5 Druck 10... 10 hpa Einlaßsystem Ionenquelle Massenanalysator Detektor Signalverarbeitung Ausgabe Schema eines Massenspektrometer-Systems Einlasssystem für direkte Probenaufgabe
Vakuumsystem Probe - 8-5 Druck 10... 10 hpa Einlaßsystem Ionenquelle Massenanalysator Detektor Signalverarbeitung Ausgabe Schema eines Massenspektrometer-Systems Einlasssystem für direkte Probenaufgabe
Teil 4 Massenspektrometrie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2015/16
 Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2015/16 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2015/16 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
Massenspektrometrie II
 Massenspektrometrie II (Bilder aus Hesse, Meier, Zeeh: Spektroskopische Methoden in der Organischen Chemie) Moderne Ionisationsmethoden Neuentwicklungen in der Massenspektrometrie erfolgten in den letzten
Massenspektrometrie II (Bilder aus Hesse, Meier, Zeeh: Spektroskopische Methoden in der Organischen Chemie) Moderne Ionisationsmethoden Neuentwicklungen in der Massenspektrometrie erfolgten in den letzten
Einführung in die Chromatographie
 Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/34 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/34 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Terminologie. Die Ausdrücke Massenspektrometer
 I Grundlagen Massenspektrometrie, Fünfte Auflage. H. Budzikiewicz, M. Schäfer Copyright 2005 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ISBN: 3-527-30822-9 7 1 Terminologie Ein Massenspektrometer ist
I Grundlagen Massenspektrometrie, Fünfte Auflage. H. Budzikiewicz, M. Schäfer Copyright 2005 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ISBN: 3-527-30822-9 7 1 Terminologie Ein Massenspektrometer ist
Schriftliche Prüfung BSc Frühling 2014
 Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
ZHAW / N / CH / Analytische Chemie
 Analytische Chemie Kurztest 3 Dauer: Minuten Erlaubte Hilfsmittel: Vorlesungsunterlagen, Lehrbücher, Taschenrechner und eigene Formelsammlungen Alle Berechnungen sind am Schluss zusammen mit diesen Aufgabenblättern
Analytische Chemie Kurztest 3 Dauer: Minuten Erlaubte Hilfsmittel: Vorlesungsunterlagen, Lehrbücher, Taschenrechner und eigene Formelsammlungen Alle Berechnungen sind am Schluss zusammen mit diesen Aufgabenblättern
Was bedeutet CH 3 OH?
 Was bedeutet CH 3 OH? 1 C 1 H H 17 O MS Einleitung 1 Worin unterscheiden sich diese Moleküle? MS Einleitung Richtig, sie unterscheiden sich in der Masse! MS Einleitung 3 Aber woher kommt unser Wissen über
Was bedeutet CH 3 OH? 1 C 1 H H 17 O MS Einleitung 1 Worin unterscheiden sich diese Moleküle? MS Einleitung Richtig, sie unterscheiden sich in der Masse! MS Einleitung 3 Aber woher kommt unser Wissen über
Fragmentierung geradelektronischer Ionen
 Fragmentierung geradelektronischer Ionen Problem: unterschiedliche Fragmentierungswege für geradelektronische Ionen [M+H] +, [M-H] - und Radikalionen [M] + umfangreiche Kenntnisse über die Fragmentierung
Fragmentierung geradelektronischer Ionen Problem: unterschiedliche Fragmentierungswege für geradelektronische Ionen [M+H] +, [M-H] - und Radikalionen [M] + umfangreiche Kenntnisse über die Fragmentierung
Funktionsweise von Flüssigkeitschromatographie und Massenspektrometrie
 Funktionsweise von Flüssigkeitschromatographie und Massenspektrometrie Die Kopplung von Massenspektrometrie mit der Flüssigchromatographie (LC-MS) ist eine relativ junge Entwicklung. In Verbindung mit
Funktionsweise von Flüssigkeitschromatographie und Massenspektrometrie Die Kopplung von Massenspektrometrie mit der Flüssigchromatographie (LC-MS) ist eine relativ junge Entwicklung. In Verbindung mit
Stichworte zu Inhalten
 Stichworte zu Inhalten API (atmospheric pressure ionisation) Methoden Ionisierung aus Lösungen ESI (electrospray ionisation) und APCI (atmospheric pressure chemical ionisation) ESI: Spray + Hochsp. > geladene
Stichworte zu Inhalten API (atmospheric pressure ionisation) Methoden Ionisierung aus Lösungen ESI (electrospray ionisation) und APCI (atmospheric pressure chemical ionisation) ESI: Spray + Hochsp. > geladene
Herbert Budzikiewicz und Mathias Schäfer. Massenspektrometrie
 Herbert Budzikiewicz und Mathias Schäfer Massenspektrometrie Beachten Sie bitte auch weitere interessante Titel zu diesem Thema Otto, M. Analytische Chemie 2011 ISBN: 978-3-527-32881-9 Schwedt, G., Vogt,
Herbert Budzikiewicz und Mathias Schäfer Massenspektrometrie Beachten Sie bitte auch weitere interessante Titel zu diesem Thema Otto, M. Analytische Chemie 2011 ISBN: 978-3-527-32881-9 Schwedt, G., Vogt,
SICRIT Ionenquelle. Produktinformation
 Einführung In den letzten Jahren sind viele LC-MS-Geräte auf den Markt gekommen, die in puncto Auflösung, Massenbereich, Massengenauigkeit und MS/MS-Funktionalitäten weit mehr bieten als klassische GC-MS-Systeme
Einführung In den letzten Jahren sind viele LC-MS-Geräte auf den Markt gekommen, die in puncto Auflösung, Massenbereich, Massengenauigkeit und MS/MS-Funktionalitäten weit mehr bieten als klassische GC-MS-Systeme
2. Mäuseburger Kaminabend
 www.papa-gey.de 2. Mäuseburger Kaminabend Marschner Str. 22 D 02763 Zittau Frau Dr. rer. nat. Monika Möder Helmholtz Zentrum, UFZ Leipzig Mittwoch, 09. 12.2015, 19.00 Uhr Ionen aus dem Feuer: Ionisierungstechniken
www.papa-gey.de 2. Mäuseburger Kaminabend Marschner Str. 22 D 02763 Zittau Frau Dr. rer. nat. Monika Möder Helmholtz Zentrum, UFZ Leipzig Mittwoch, 09. 12.2015, 19.00 Uhr Ionen aus dem Feuer: Ionisierungstechniken
1. Isotopie und Präzisionsmasse 2. Erkennung/Eigenschaften des Molekülions 3. Fragmentierung (ungeradelektronischer Ionen)
 Interpretation von Massenspektren 1. Isotopie und Präzisionsmasse 2. Erkennung/Eigenschaften des Molekülions 3. Fragmentierung (ungeradelektronischer Ionen) 1 EI-Massenspektrum (Acetophenon, M = 120):
Interpretation von Massenspektren 1. Isotopie und Präzisionsmasse 2. Erkennung/Eigenschaften des Molekülions 3. Fragmentierung (ungeradelektronischer Ionen) 1 EI-Massenspektrum (Acetophenon, M = 120):
Massenspektrometrie (MS)
 Massenspektrometrie (MS) Seite Stunde 1. Grundlagen 1.1 Probeneinlass I: RI, DIP, DEP; Quantifizierung 1.2 Ionenquelle I: EI, LEI; Verunreinigungen 1.3 Analysator I: BE + EB, SIM 1.4 Detektor I: FC, SEV,
Massenspektrometrie (MS) Seite Stunde 1. Grundlagen 1.1 Probeneinlass I: RI, DIP, DEP; Quantifizierung 1.2 Ionenquelle I: EI, LEI; Verunreinigungen 1.3 Analysator I: BE + EB, SIM 1.4 Detektor I: FC, SEV,
Massenspektrometrie. Die Faszination der chemischen Vielfalt gasförmiger Ionen. Aus der Sicht der allgemeinen Bedeutung
 cgi4you - Fotolia.com Massenspektrometrie Die Faszination der chemischen Vielfalt gasförmiger Ionen Aus der Sicht der allgemeinen Bedeutung und Anwendbarkeit ist die Massenspektrometrie wohl die wichtigste
cgi4you - Fotolia.com Massenspektrometrie Die Faszination der chemischen Vielfalt gasförmiger Ionen Aus der Sicht der allgemeinen Bedeutung und Anwendbarkeit ist die Massenspektrometrie wohl die wichtigste
Analytical Services Dr. Ralph Nussbaum
 Analytical Services Dr. Ralph Nussbaum Medizintechnisches Zentrum Pauwelsstrasse 19 D-52074 Aachen Tel.: +49 241 963 2150 Fax: +49 241 963 2154 www.analytical-services.com www.analytical-services.com 1
Analytical Services Dr. Ralph Nussbaum Medizintechnisches Zentrum Pauwelsstrasse 19 D-52074 Aachen Tel.: +49 241 963 2150 Fax: +49 241 963 2154 www.analytical-services.com www.analytical-services.com 1
Bioanalytik Zusatzinformation: Massenspektrometrie 012_001. BioAnalytik
 Bioanalytik 11.01.16 Zusatzinformation: Massenspektrometrie 012_001 Rev. 1.5 091206 - Standort Recklinghausen- Wintersemester 2015-16 2015-2016 : 1 Folienbasis: Prof. Beyer Massenspektrometrie Einführung
Bioanalytik 11.01.16 Zusatzinformation: Massenspektrometrie 012_001 Rev. 1.5 091206 - Standort Recklinghausen- Wintersemester 2015-16 2015-2016 : 1 Folienbasis: Prof. Beyer Massenspektrometrie Einführung
Massenspektrometrie I
 Forschungszentrum Karlsruhe In der Helmholtz-Gemeinschaft Universität Karlsruhe Institut für Organische Chemie Massenspektrometrie I Grundlagen Geräteaufbau ESI TOF MS LCMS Anwendungsbeispiele O. Zwernemann
Forschungszentrum Karlsruhe In der Helmholtz-Gemeinschaft Universität Karlsruhe Institut für Organische Chemie Massenspektrometrie I Grundlagen Geräteaufbau ESI TOF MS LCMS Anwendungsbeispiele O. Zwernemann
Schriftliche Prüfung BSc Herbst 2010
 Prüfungen Analytische Chemie Dienstag, 24. August 2010 Schriftliche Prüfung BSc Herbst 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 24. August 2010 Schriftliche Prüfung BSc Herbst 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
LCMS Single Quadrupole MS
 LCMS-2020 - Single Quadrupole MS Shimadzu http://www.shimadzu.de/lcms-2020-single-quadrupole-ms Home / Produkte / LCMS / LCMS-2020 - Single Quadrupole MS LCMS-2020 - Single Quadrupole MS LCMS 2020 - Single
LCMS-2020 - Single Quadrupole MS Shimadzu http://www.shimadzu.de/lcms-2020-single-quadrupole-ms Home / Produkte / LCMS / LCMS-2020 - Single Quadrupole MS LCMS-2020 - Single Quadrupole MS LCMS 2020 - Single
Instrumentierung 2/1
 Instrumentierung 2/1 Detektoren Elektronenvervielfacher (Electron Multiplier) Sekundärelektronenvervielfacher (SEM) + + + 2/2 Detektoren Elektronenvervielfacher (Electron Multiplier) Kanalelektronenvervielfacher
Instrumentierung 2/1 Detektoren Elektronenvervielfacher (Electron Multiplier) Sekundärelektronenvervielfacher (SEM) + + + 2/2 Detektoren Elektronenvervielfacher (Electron Multiplier) Kanalelektronenvervielfacher
DETEKTOREN. Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ ETH Zurich Dr.
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ ETH Zurich Dr.
2.2. Peptide. Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure
 2.2. Peptide Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure Peptid: bis zu ~30 linear über Peptidbindung verknüpfte Aminosäuren
2.2. Peptide Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure Peptid: bis zu ~30 linear über Peptidbindung verknüpfte Aminosäuren
Übersicht Massenanalysatoren
 Übersicht Massenanalysatoren Gerätetyp Trennprinzip Massenbereich Auflösung Sektorfeld-MS magnetisches u. elektrostatisches Feld max. 10000 Präzisionsmasse (max. 200000) ToF-MS Flugzeitmessung (theor.)
Übersicht Massenanalysatoren Gerätetyp Trennprinzip Massenbereich Auflösung Sektorfeld-MS magnetisches u. elektrostatisches Feld max. 10000 Präzisionsmasse (max. 200000) ToF-MS Flugzeitmessung (theor.)
Daniela Grotewahl (Autor) Entwicklung von Methoden zur Bestimmung von Chloramphenicol in Bienenprodukten mittels LC-MS
 Daniela Grotewahl (Autor) Entwicklung von Methoden zur Bestimmung von Chloramphenicol in Bienenprodukten mittels LC-MS https://cuvillier.de/de/shop/publications/2180 Copyright: Cuvillier Verlag, Inhaberin
Daniela Grotewahl (Autor) Entwicklung von Methoden zur Bestimmung von Chloramphenicol in Bienenprodukten mittels LC-MS https://cuvillier.de/de/shop/publications/2180 Copyright: Cuvillier Verlag, Inhaberin
Schriftliche Prüfung BSc Frühling 2006
 Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
2. Wiederholungsklausur OC1 (BA-Studiengang) :00 16:00 Uhr M1 C-Bau. Name: Punkte: Matrikel Nr. Note:
 2. Wiederholungsklausur C1 (BA-Studiengang) PI: 07.04.2011 13:00 16:00 Uhr M1 C-Bau ame: Punkte: Matrikel r. ote: otenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
2. Wiederholungsklausur C1 (BA-Studiengang) PI: 07.04.2011 13:00 16:00 Uhr M1 C-Bau ame: Punkte: Matrikel r. ote: otenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Schriftliche Prüfung BSc Frühling 2006 D CHAB/BIOL. Musterlösung. für den Teil Spektroskopie
 Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die
Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die
Schriftliche Prüfung BSc Herbst 2013
 Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Übung zu den Vorlesungen Organische und Anorganische Chemie
 Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 12.11.08 1. Stellen sie die Reaktionsgleichung für die Herstellung von Natriumsulfid aus den Elementen auf. Wieviel
Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 12.11.08 1. Stellen sie die Reaktionsgleichung für die Herstellung von Natriumsulfid aus den Elementen auf. Wieviel
Massenspektrometrie. Georg Pohnert
 Massenspektrometrie http://masspec.scripps.edu/ Georg Pohnert 1 Massenspektren OH Elektrospray-Ionisation + O HOOC O100 209 [M+H] + 100 rel. Int. (%) 0 41 55 70 83 Elektronenstoss-Ionisation 106 148 112
Massenspektrometrie http://masspec.scripps.edu/ Georg Pohnert 1 Massenspektren OH Elektrospray-Ionisation + O HOOC O100 209 [M+H] + 100 rel. Int. (%) 0 41 55 70 83 Elektronenstoss-Ionisation 106 148 112
Die Bedeutung der Massenspektrometrie in der Umweltanalytik
 Die Bedeutung der Massenspektrometrie in der Umweltanalytik Marc J-F J F Suter Umwelttoxikologie Juliane Hollender,, Heinz Singer Umweltchemie Eawag: Das Wasserforschungs-Institut des ETH-Bereichs 196
Die Bedeutung der Massenspektrometrie in der Umweltanalytik Marc J-F J F Suter Umwelttoxikologie Juliane Hollender,, Heinz Singer Umweltchemie Eawag: Das Wasserforschungs-Institut des ETH-Bereichs 196
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
URL: uni-leipzig.de/ bioanaly/sem6/vorlesungen%20ss%202014/vorlesung MS 1.pdf
 2014-04-08 Massenspektrometrie Vorlesung Prof. Dr. Ralf Hoffmann URL: http:// uni-leipzig.de/ bioanaly/sem6/vorlesungen%20ss%202014/vorlesung MS 1.pdf pw: 1 Einführung Massenspektrometrie ist kein spektroskopisches
2014-04-08 Massenspektrometrie Vorlesung Prof. Dr. Ralf Hoffmann URL: http:// uni-leipzig.de/ bioanaly/sem6/vorlesungen%20ss%202014/vorlesung MS 1.pdf pw: 1 Einführung Massenspektrometrie ist kein spektroskopisches
Pestizide im Warenkorb
 Ausgabe 10/2003 Pestizide im Warenkorb Heutzutage werden die Lebensmittel so gut überwacht wie nie zuvor. Und doch kommt es immer wieder zu Skandalen wie letzten Februar mit belasteten Erdbeeren aus Algerien.
Ausgabe 10/2003 Pestizide im Warenkorb Heutzutage werden die Lebensmittel so gut überwacht wie nie zuvor. Und doch kommt es immer wieder zu Skandalen wie letzten Februar mit belasteten Erdbeeren aus Algerien.
Proteomics. Analytik von humanen Serumproteinen durch massenspektrometrische Identifikation peptide mass fingerprint
 Proteomics Analytik von humanen Serumproteinen durch massenspektrometrische Identifikation peptide mass fingerprint 1. Theorie 1.1 Massenspektrometrie 1.1.1 Überblick Die Massenspektrometrie ist eine Untersuchungstechnik
Proteomics Analytik von humanen Serumproteinen durch massenspektrometrische Identifikation peptide mass fingerprint 1. Theorie 1.1 Massenspektrometrie 1.1.1 Überblick Die Massenspektrometrie ist eine Untersuchungstechnik
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Mas senspektrometrie in der Biochemie
 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Wolf D. Lehmann Mas senspektrometrie in der Biochemie Spektrum Akademischer
2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Wolf D. Lehmann Mas senspektrometrie in der Biochemie Spektrum Akademischer
Erratum im 3. Teil: Aminosäure, Folie Nr. 59
 Erratum im 3. Teil: Aminosäure, Folie Nr. 59 Gabriel Synthese O H N-Br O + R X Cl COOH O O N R COOH N 2 H 4 H 2 N R COOH N-Brom-Phthalimid O NH NH O Synthese von DL-Asp Synthese von DL-Glu COOH COOH Maleinsäure
Erratum im 3. Teil: Aminosäure, Folie Nr. 59 Gabriel Synthese O H N-Br O + R X Cl COOH O O N R COOH N 2 H 4 H 2 N R COOH N-Brom-Phthalimid O NH NH O Synthese von DL-Asp Synthese von DL-Glu COOH COOH Maleinsäure
Dr. Jürgen Zipfel. 15.03.2007 Chemisches Untersuchungslabor Dr. Zipfel 1 von 28. Neue Anforderungen im Auftragslabor
 LC-MS im Laboralltag Dr. Jürgen Zipfel 15.03.2007 Chemisches Untersuchungslabor Dr. Zipfel 1 von 28 Neue Anforderungen im Auftragslabor Matrix Trinkwasser: mit BG von PBSM 10 ng/l (Grenzwert TrinkwVO:
LC-MS im Laboralltag Dr. Jürgen Zipfel 15.03.2007 Chemisches Untersuchungslabor Dr. Zipfel 1 von 28 Neue Anforderungen im Auftragslabor Matrix Trinkwasser: mit BG von PBSM 10 ng/l (Grenzwert TrinkwVO:
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie)
 Übungen 24.01.2012 Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Aufgabe 1.1 Zeichnen Sie die Strukturformeln der folgenden Verbindungen (jeweils 1 Punkt pro Teilaufgabe).
Übungen 24.01.2012 Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Aufgabe 1.1 Zeichnen Sie die Strukturformeln der folgenden Verbindungen (jeweils 1 Punkt pro Teilaufgabe).
ANALYTISCHE CHEMIE I Trennmethoden 5. Prozess-Analytik GC-MS, LC-MS WS 2007/2008
 ANALYTISCHE CHEMIE I Trennmethoden 5. Prozess-Analytik GC-MS, LC-MS WS 2007/2008 Prozeßanalytik Analyse von Prozessen durch Messungen des zeitlichen Verlaufes physikalischer Probenveränderungen und von
ANALYTISCHE CHEMIE I Trennmethoden 5. Prozess-Analytik GC-MS, LC-MS WS 2007/2008 Prozeßanalytik Analyse von Prozessen durch Messungen des zeitlichen Verlaufes physikalischer Probenveränderungen und von
Übungen LÖSUNGEN
 Übungen 24.01.2012 - LÖSUNGEN Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Maximale Punktezahl: 20 Aufgabe 1.1 (5 Punkte) Zeichnen Sie die Strukturformeln der folgenden
Übungen 24.01.2012 - LÖSUNGEN Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Maximale Punktezahl: 20 Aufgabe 1.1 (5 Punkte) Zeichnen Sie die Strukturformeln der folgenden
Übungen zur Spektroskopie 2
 Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
3. Klausur OC1 (BSc-Studiengang) PIN: LÖSUNGEN :00 14:00 Uhr N6
 3. Klausur OC1 (BSc-Studiengang) PIN: LÖSUNGEN 17.03.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
3. Klausur OC1 (BSc-Studiengang) PIN: LÖSUNGEN 17.03.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Massenspektrometrie in der organischen Spurenanalytik
 Massenspektrometrie in der organischen Spurenanalytik Dr. Wolfgang Schulz, Dr. Wolfram Seitz und Thomas Lucke Einleitung Die Verfügbarkeit von Massenanalysatoren in Kopplung mit unterschiedlichen chromatographischen
Massenspektrometrie in der organischen Spurenanalytik Dr. Wolfgang Schulz, Dr. Wolfram Seitz und Thomas Lucke Einleitung Die Verfügbarkeit von Massenanalysatoren in Kopplung mit unterschiedlichen chromatographischen
Dissertation. zur Erlangung des akademischen Grades doctor rerum naturalium (Dr. rer. nat.) vorgelegt der
 Untersuchung der Ceramide des Stratum corneum in der nicht involvierten Haut bei Neurodermitis- und Psoriasis- Patienten mit Hilfe der AMD-HPTLC und der HPLC/APCI-MS Dissertation zur Erlangung des akademischen
Untersuchung der Ceramide des Stratum corneum in der nicht involvierten Haut bei Neurodermitis- und Psoriasis- Patienten mit Hilfe der AMD-HPTLC und der HPLC/APCI-MS Dissertation zur Erlangung des akademischen
Aus dem Institut fur Chemie und Technologie der Milch Bundesforschungsanstalt fur Ernahrung und Lebensmittel - Standort Kiel
 Aus dem Institut fur Chemie und Technologie der Milch Bundesforschungsanstalt fur Ernahrung und Lebensmittel - Standort Kiel Entwicklung von Methoden zur Bestimmung von Chloramphenicol in Bienenprodukten
Aus dem Institut fur Chemie und Technologie der Milch Bundesforschungsanstalt fur Ernahrung und Lebensmittel - Standort Kiel Entwicklung von Methoden zur Bestimmung von Chloramphenicol in Bienenprodukten
Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner Samstag, Uhr Allgemeine Chemie
 Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Organische Chemie 1 Teil 2
 Inhalte der 7. Vorlesung: 2.4. Bildung & Reaktion von Enolen und Enolaten 2.5 Chemie des Enolatanions 2.6 Enolat-Analoga 2.8 1,3-Dicarbonylverbindungen/ß-Dicarbonylverbindungen 2.9 α,β-ungesättigte Carbonylverbindungen
Inhalte der 7. Vorlesung: 2.4. Bildung & Reaktion von Enolen und Enolaten 2.5 Chemie des Enolatanions 2.6 Enolat-Analoga 2.8 1,3-Dicarbonylverbindungen/ß-Dicarbonylverbindungen 2.9 α,β-ungesättigte Carbonylverbindungen
P105. Konstitution. Massenspektrum 100 % m/z
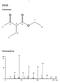 1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
Methoden der Proteomforschung. 2 D Gelelektrophorese
 Methoden der Proteomforschung 23.04.2003 Dr. Cornelia Kasper Geschichte der Proteomforschung Proteinforschung viel älter als Genomforschung Spektakuläre Analysenergebnisse sind jedoch viel schwieriger
Methoden der Proteomforschung 23.04.2003 Dr. Cornelia Kasper Geschichte der Proteomforschung Proteinforschung viel älter als Genomforschung Spektakuläre Analysenergebnisse sind jedoch viel schwieriger
Massenspektrometrie: ESI- und MALDI-MS
 Massenspektrometrie: ESI- und MALDI-MS 1. Massenspektrometrie Allgemeine Einführung Wichtige Komponenten Gerätetypen 2. Ionisierungstechniken Matrix-unterstützte Laser Desorption/Ionisierung (MALDI) Elektrospray-Ionisierung
Massenspektrometrie: ESI- und MALDI-MS 1. Massenspektrometrie Allgemeine Einführung Wichtige Komponenten Gerätetypen 2. Ionisierungstechniken Matrix-unterstützte Laser Desorption/Ionisierung (MALDI) Elektrospray-Ionisierung
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006
 Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Klausur zu Teil 1 des Wahlpflichtmoduls "Nanochemie" ( )
 1 ame... Matrikel-r.... Klausur zu Teil 1 des Wahlpflichtmoduls "anochemie" (13-121-0223) 20. Mai 2008 (9.00-9.50 Uhr, R. 014) Schreiben Sie sauber und ordentlich! Für nicht lesbare Ausdrücke können leider
1 ame... Matrikel-r.... Klausur zu Teil 1 des Wahlpflichtmoduls "anochemie" (13-121-0223) 20. Mai 2008 (9.00-9.50 Uhr, R. 014) Schreiben Sie sauber und ordentlich! Für nicht lesbare Ausdrücke können leider
Massenspektrometrie. Talián Csaba Gábor Universität Pécs Institut für Biophysik
 Massenspektrometrie Talián Csaba Gábor Universität Pécs Institut für Biophysik Grundprinzipien Bildung von Ionen aus irgendwelchem geeigneten Stoffe Trennung von Ionen anhand m/z Qualitative und Quantitative
Massenspektrometrie Talián Csaba Gábor Universität Pécs Institut für Biophysik Grundprinzipien Bildung von Ionen aus irgendwelchem geeigneten Stoffe Trennung von Ionen anhand m/z Qualitative und Quantitative
Schriftliche Prüfung J Analytische Chemie I&II Winter 2015
 Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Winter 2015 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Winter 2015 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Grundlagen der Chromatographie
 Grundlagen der Chromatographie Was ist Chromatographie? Trennung ähnlicher Moleküle aus komplexen Gemischen o Die Analyte werden in einer mobilen Phase gelöst und darin durch eine stationäre Phase transportiert.
Grundlagen der Chromatographie Was ist Chromatographie? Trennung ähnlicher Moleküle aus komplexen Gemischen o Die Analyte werden in einer mobilen Phase gelöst und darin durch eine stationäre Phase transportiert.
Chemisch reine Verbindungen ergeben ein Gemisch von Massenspektren -----> Isotopenmuster
 Cl B Cl 81 83 Cl 35 8 116 118 11 37 46 41 48 85 115 12 45 7 1 15 2 25 3 35 4 45 5 55 6 65 7 75 8 85 9 95 15 11 115 12 125 13 135 14 -Verhältnis Relative Intensität Basispeak Fragmentionen Molekülion Masse/Ladungsverhältnis
Cl B Cl 81 83 Cl 35 8 116 118 11 37 46 41 48 85 115 12 45 7 1 15 2 25 3 35 4 45 5 55 6 65 7 75 8 85 9 95 15 11 115 12 125 13 135 14 -Verhältnis Relative Intensität Basispeak Fragmentionen Molekülion Masse/Ladungsverhältnis
1. Klausur: Veranstaltung Allgemeine und Anorganische Chemie
 1. Klausur: Veranstaltung Allgemeine und Anorganische Chemie Geologie und Geophysik (Diplom), Geowissenschaften (BSc), Mathematik (Diplom), Informatik mit Anwendungsfach Chemie und andere Naturwissenschaften
1. Klausur: Veranstaltung Allgemeine und Anorganische Chemie Geologie und Geophysik (Diplom), Geowissenschaften (BSc), Mathematik (Diplom), Informatik mit Anwendungsfach Chemie und andere Naturwissenschaften
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2004
 Prüfungen Analytische Chemie Dienstag, 1. September 4 Schriftliche Prüfung. Vordiplom / BSc erbst 4 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 1. September 4 Schriftliche Prüfung. Vordiplom / BSc erbst 4 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 2. Klausur OC1 (BSc-Studiengang) PIN: 08.03.2017 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-75=1.0 74-71=1.3 70-67=1.7 66-63=2.0 62-59=2.3 58-53=2.7 52-50=3.0 49-48=3.3 47-42=3.7
2. Klausur OC1 (BSc-Studiengang) PIN: 08.03.2017 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-75=1.0 74-71=1.3 70-67=1.7 66-63=2.0 62-59=2.3 58-53=2.7 52-50=3.0 49-48=3.3 47-42=3.7
LMPG 3, Spek-ÜB-20 LÖSUNG Seite 1 von 6
 LMPG 3, Spek-ÜB-20 LÖSUG Seite 1 von 6 Aufgabe 1: a) Woran lässt sich aus dem MS-Spektrum auf die Zahl der -Atome schliessen? Molekülionenpeak ist ungerade, also ist auch die Zahl der -Atome ungerade.
LMPG 3, Spek-ÜB-20 LÖSUG Seite 1 von 6 Aufgabe 1: a) Woran lässt sich aus dem MS-Spektrum auf die Zahl der -Atome schliessen? Molekülionenpeak ist ungerade, also ist auch die Zahl der -Atome ungerade.
Produktinformation CombiFlash Rf + PurIon
 Stand: April 2015 Allgemein: Teledyne Isco hat das Portfolio erweitert und bietet zusätzlich zu den bekannten Detektoren UV, UV/VIS und ELSD, ein gekoppeltes Massenspektrometer an. Das PurIon besteht aus
Stand: April 2015 Allgemein: Teledyne Isco hat das Portfolio erweitert und bietet zusätzlich zu den bekannten Detektoren UV, UV/VIS und ELSD, ein gekoppeltes Massenspektrometer an. Das PurIon besteht aus
2D-NMR- Spektroskopie
 2. 2D-NMR-Spektroskopie 2D-NMR- Spektroskopie Organische Chemie Dr. I. Kempter - 28 - 2. 2D-NMR-Spektroskopie Überblick Der Einsatz von zweidimensionalen ermöglicht es die Nachteile eines eindimensionalen
2. 2D-NMR-Spektroskopie 2D-NMR- Spektroskopie Organische Chemie Dr. I. Kempter - 28 - 2. 2D-NMR-Spektroskopie Überblick Der Einsatz von zweidimensionalen ermöglicht es die Nachteile eines eindimensionalen
Herbert Budzikiewicz und Mathias Schäfer. Massenspektrometrie
 Herbert Budzikiewicz und Mathias Schäfer Massenspektrometrie Beachten Sie bitte auch weitere interessante Titel zu diesem Thema Otto, M. Analytische Chemie 2011 ISBN: 978-3-527-32881-9 Schwedt, G., Vogt,
Herbert Budzikiewicz und Mathias Schäfer Massenspektrometrie Beachten Sie bitte auch weitere interessante Titel zu diesem Thema Otto, M. Analytische Chemie 2011 ISBN: 978-3-527-32881-9 Schwedt, G., Vogt,
Schriftliche Prüfung 2. Vordiplom Herbst 2003
 Prüfungen Analytische hemie Mittwoch, 1. ktober 2003 Schriftliche Prüfung 2. Vordiplom erbst 2003 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische hemie Mittwoch, 1. ktober 2003 Schriftliche Prüfung 2. Vordiplom erbst 2003 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
4 Synthesen antiprionen-aktiver Verbindungen
 4 Synthesen antiprionen-aktiver Verbindungen Quinacrinanaloga (Grundstruktur C) 77 4 Synthesen antiprionen-aktiver Verbindungen 4.1 Synthesen der Quinacrinanaloga (Grundstruktur C) Die Synthesen der Quinacrinanaloga
4 Synthesen antiprionen-aktiver Verbindungen Quinacrinanaloga (Grundstruktur C) 77 4 Synthesen antiprionen-aktiver Verbindungen 4.1 Synthesen der Quinacrinanaloga (Grundstruktur C) Die Synthesen der Quinacrinanaloga
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 2. Klausur OC1 (BSc-Studiengang) PIN: 02.03.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
2. Klausur OC1 (BSc-Studiengang) PIN: 02.03.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
Schriftliche Prüfung Analytische Chemie I Sommer 2014
 Schriftliche Prüfung Analytische Chemie I Sommer 2014 Vorname: Name: Legi-Nr.: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut ein. Es sind
Schriftliche Prüfung Analytische Chemie I Sommer 2014 Vorname: Name: Legi-Nr.: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut ein. Es sind
Im Wasser sind ph-werte von ca bis 15 möglich.
 8 Superbasen 8.1 Basizität im System Wasser 2 H 2 O H 3 O + + OH pk =14 Säurestärken (pk S ): pk S HClO 4 10 saurer als H 3 O + HCl 7 H 2 SO 4 3 H 3 O + 0 H 3 PO 4 2.2 H 3.2 HCN 9.2 H 2 O 2 11.6 H 2 O
8 Superbasen 8.1 Basizität im System Wasser 2 H 2 O H 3 O + + OH pk =14 Säurestärken (pk S ): pk S HClO 4 10 saurer als H 3 O + HCl 7 H 2 SO 4 3 H 3 O + 0 H 3 PO 4 2.2 H 3.2 HCN 9.2 H 2 O 2 11.6 H 2 O
HPLC-MS in der Spurenanalytik
 Labor Seminar HPLC-MS in der Spurenanalytik Ein praxisnaher Überblick über Ionisationstechniken, praktische Probleme und Störfaktoren, Strukturaufklärung und Quantifizierung Termin/Ort 24. 25. Oktober
Labor Seminar HPLC-MS in der Spurenanalytik Ein praxisnaher Überblick über Ionisationstechniken, praktische Probleme und Störfaktoren, Strukturaufklärung und Quantifizierung Termin/Ort 24. 25. Oktober
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. Brückner
 eaktionsmechanismen nach dem gleichnahmigen ch von. Brückner Kap. 12 Chemie der Enole und Enamine Dr. ermann A. Wegner hermann.wegner@unibas.ch Keto/Enol-Tautomerie; Enolgehalt von Carbonyl- und Carboxylverbindungen
eaktionsmechanismen nach dem gleichnahmigen ch von. Brückner Kap. 12 Chemie der Enole und Enamine Dr. ermann A. Wegner hermann.wegner@unibas.ch Keto/Enol-Tautomerie; Enolgehalt von Carbonyl- und Carboxylverbindungen
Chemilumineszenz, MALDI TOF MS, DSC Vergleichende Messungen an Polymeren
 Chemilumineszenz, MALDI TF MS, DSC Vergleichende Messungen an Polymeren Urs von Arx und Ingo Mayer Berner Fachhochschule Architektur, Holz und Bau F+E, Werkstoffe und Holztechnologie Biel Problemstellung
Chemilumineszenz, MALDI TF MS, DSC Vergleichende Messungen an Polymeren Urs von Arx und Ingo Mayer Berner Fachhochschule Architektur, Holz und Bau F+E, Werkstoffe und Holztechnologie Biel Problemstellung
Erste Änderung der Studien- und Prüfungsordnung
 Amtliches Mitteilungsblatt Mathematisch-Naturwissenschaftliche Fakultät Erste Änderung der Studien- und Prüfungsordnung für das Bachelorstudium Chemie (AMB Nr. 42/2009) Kernfach und Beifach im Monostudiengang
Amtliches Mitteilungsblatt Mathematisch-Naturwissenschaftliche Fakultät Erste Änderung der Studien- und Prüfungsordnung für das Bachelorstudium Chemie (AMB Nr. 42/2009) Kernfach und Beifach im Monostudiengang
Kursus Medizinische Physik SS 2007
 Kursus Medizinische Physik SS 2007 Ablaufplan: Dienstag, 19. Juni (Vormittag): Vorlesung: Massenspektrometrische Lipidanalytik Dienstag, 19. Juni (Nachmittag): Praktikum: Lipidanalytik mittels MS und TLC
Kursus Medizinische Physik SS 2007 Ablaufplan: Dienstag, 19. Juni (Vormittag): Vorlesung: Massenspektrometrische Lipidanalytik Dienstag, 19. Juni (Nachmittag): Praktikum: Lipidanalytik mittels MS und TLC
