Finale Version Deutsche Zusammenfassung des Prüfplans
|
|
|
- Jobst Lenz
- vor 7 Jahren
- Abrufe
Transkript
1 Finale Version Deutsche Zusammenfassung des Prüfplans Randomisierte, multizentrische, offene Phase IIa Studie mit zwei Dosisstufen des intraperitoneal infundierten trifunktionalen bispezifischen Antikörpers Removab (anti-epcam x anti-cd3) an Patientinnen mit platinresistentem epithelialem Ovarialkarzinom zur Selektion der besseren Dosisstufe (Randomized, multicenter, 2-dose-level, open-label, phase IIa study with the intraperitoneally infused trifunctional bispecific antibody removab (anti-epcam x anti-cd3) to select the better dose level in platinum refractory epithelial ovarian cancer patients) Eine Phase IIa Studie der AGO Studiengruppe Ovarialkarzinom, Deutschland AGO-OVAR Dezember 2003 und Amendment Nr.1, vom 25 März 2004 Leiter der klinischen Prüfung Prof. Dr. Uwe Wagner Abteilung Gynäkologie und gynäkologische Onkologie Philipps-Universität Marburg Pilgrimstein 3 D Marburg Tel.: +49 (0) Fax +49 (0) uwe.wagner@med.uni-marburg.de Klinisches Monitoring Schantl Pharma Service GmbH Herderstr. 16 D Wiesbaden Tel.: +49 (0) Fax: +49 (0) peter_schantl@t-online.de Studiendaten: 1 Q 2004 to 3 Q 2005 AGO OVAR Studiensekretariat Marburg Prof. Dr. Uwe Wagner Helke Naujok, Ulrich Weitzel Abteilung Gynäkologie und gynäkologische Onkologie Philipps-Universität Marburg Pilgrimstein 3 D Marburg Tel.: +49 (0) /6491 Fax +49 (0) office-marburg@ago-ovar.de Statistik Dipl. Psych. Justine Rochon Koordinierungszentrum für klinische Studien Philipps-Universität Marburg Robert-Koch-Str. 5 D Marburg Tel.: +49 (0) Fax +49 (0) rochon@med.uni-marburg.de Die Studie einschließlich der Archivierung der Studienunterlagen wird gemäß des Prüfplans und unter Beachtung der Guten Klinischen Praxis, der Deklaration von Helsinki sowie anderen zutreffenden Regularien durchgeführt. keitserklärung Die Information in diesem Prüfplan ist vertraulich und ist für die Verwendung durch die Prüfer vorgesehen. Sie ist Eigentum der AGO Studiengruppe Ovarialkarzinom und darf nicht kopiert oder an Personen weitergegeben werden, die nicht in die Studie gemäß des AGO Prüfplans OVAR-2.10 involviert sind, es sei denn, diese Personen sind durch eine keitserklärung mit der AGO Studiengruppe Ovarialkarzinom zur Geheimhaltung verpflichtet.
2 AGO-OVAR Seite 2 von 10 Vorsitzender / Leiter der klinischen Prüfung: Prof. Dr. Uwe Wagner der Arbeitsgemeinschaft gynäkologische Onkologie (AGO) Studiengruppe Ovarialkarzinom, Universität Marburg Abteilung Gynäkologie und gynäkologische Onkologie Pilgrimstein 3 D Marburg Beratendes Gremium: Prof. Dr. H. G. Bender, Universitäts-Frauenklinik Düsseldorf Prof. Dr. G. Emons, Universitäts-Frauenklinik Göttingen Prof. Dr. W. Jonat, Klinik für Gynäkologie u. Geburtshilfe an der Christian-Albrechts- Universität Kiel Prof. Dr. M. Kaufmann, Universitäts-Frauenklinik Frankfurt Prof. Dr. R. Kreienberg, Universitäts-Frauenklinik Ulm Prof. Dr. H. Kühnle, Frauenklinik der Medizinischen Hochschule Hannover, Oststadtkrankenhaus Prof. Dr. W. Lichtenegger, Universitätsfrauenklinik und Poliklinik der Charité, Berlin Prof. Dr. H. Meden, Frauenklinik, Diakonissenkrankenhaus, Rotenburg/Wümme Prof. Dr. H.-G. Meerpohl, Frauenklinik der St.-Vincentius-Krankenhäuser Karlsruhe
3 AGO-OVAR Seite 3 von 10 Mitglieder der Studienkoordinationsgruppe Deutschland: Dr. A. Belau, Universitätsfrauenklinik der Ernst-Moritz-Arndt-Universität Greifswald Dr. A. Burges, Universitäts-Frauenklinik Klinikum Großhadern München Dr. U. Canzler, Universitäts-Frauenklinik Dresden Prof. Dr. A. du Bois, Klinik für Gynäkologie u. Gynäkol. Onkologie, Dr.-Horst-Schmidt-Kliniken GmbH Wiesbaden Dr. M. Gropp, Frauenklinik, Evangelisches Krankenhaus Düsseldorf Dr. V. Heilmann, Universitäts-Frauenklinik Ulm Dr. F. Hilpert, Universitätsfrauenklinik an der Christian-Albrechts-Universität zu Kiel PD Dr. J. Huober, Universitäts-Frauenklinik Tübingen PD Dr. C. Jackisch, Universitäts-Frauenklinik Marburg Prof. Dr. R. Kimmig, Universitäts-Frauenklinik Essen Dr. S. Loibl, Universitäts-Frauenklinik Frankfurt PD Dr. H.-J. Lück, Frauenklinik der Medizinischen Hochschule Hannover, Oststadtkrankenhaus Prof. Dr. W. Meier, Frauenklinik, Evangelisches Krankenhaus Düsseldorf Prof. Dr. J. Pfisterer, Universitätsfrauenklinik an der Christian-Albrechts-Universität zu Kiel Dr. B. Richter, Frauenklinik, Elblandkliniken Meißen-Radebeul Prof. Dr. B. Schmalfeldt, Universitäts-Frauenklinik, Klinikum rechts der Isar München Prof. Dr. W. Schröder, Frauenklinik, Zentralkrankenhaus St.-Jürgen-Straße Bremen Dr. J. Sehouli, Universitätsfrauenklinik und Poliklinik der Charité Berlin Dr. A. Stähle, Frauenklinik der St.-Vincentius-Krankenhäuser Karlsruhe Prof. Dr. U. Wagner, Universitäts-Frauenklinik Marburg Dr. K. Wollschlaeger, Klinik für Gynäkologie und Geburtshilfe der Med. Akademie Magdeburg
4 AGO-OVAR Seite 4 von 10 ZUSAMMENFASSUNG DES PRÜFPLANS Studientitel Studiennummer AGO Study OVAR Phase Sponsor LKP Randomisierte, multizentrische, offene Phase IIa Studie mit zwei Dosisstufen des intraperitoneal infundierten trifunktionalen bispezifischen Antikörpers Removab (anti-epcam x anti-cd3) an Patientinnen mit platinresistentem epithelialem Ovarialkarzinom zur Selektion der besseren Dosisstufe (Randomized, multicenter, 2-dose-level, open-label, phase IIa study with the intraperitoneally infused trifunctional bispecific antibody removab (anti-epcam x anti-cd3) to select the better dose level in platinum refractory epithelial ovarian cancer patients) IIa Arbeitsgemeinschaft gynäkologische Onkologie (AGO) Studiengruppe Ovarialkarzinom Prof. Dr. Uwe Wagner Studienbegründung Removab gehört zu einer neuen Generation monoklonaler Antikörper. Im Gegensatz zu den herkömmlichen mono- oder bispezifischen Antikörpern hat der trifunktionale bispezische Antikörper Removab zwei unterschiedliche Antigenbindungsstellen und eine (dritte) funktionale Bindungsstelle. Removab heftet sich mittels seiner EpCAM- (epithelial cell adhesion molecule) spezifischen Bindungsstelle effektiv an die Tumorzellen und mittels seiner CD3-spezifischen Bindungsstelle an die T-Zellen. EpCAM wird in mehr als 90% aller Ovarialkarzinome überexprimiert. Removab aktiviert zusätzlich die Fc-gamma Rezeptor I und III positiven (FcγR + ) Zellen mittels seiner speziellen Fc Region. Die intraperitoneale (i.p.) Infusion von Removab an Patienten mit malignem Aszites zeigte einen therapeutischen Nutzen in einer klinischen Studie und in Heilversuchen. Der maligne Aszites wurde stark verringert und ein signifikanter Rückgang der malignen Tumorzellen (>log 5) im Aszites gezeigt. Neben dem palliativen Effekt der Reduktion des Aszitesvolumens deuten die Ergebnisse auf einen direkten antitumoralen Effekt von Removab hin. Die lokale Anwendung von Removab in den malignen Aszites bringt den Vorteil einer zielgerichteten Immuntherapie mit sich, da die Tumorzellen direkt im Peritoneum angegriffen werden. Die Sicherheitsdaten der bisherigen Phase I/II Studie zur Behandlung des Aszites bei 23 Ovarialkarzinom Patientinnen sprechen einer weiteren i.p. Anwendung nicht entgegen. Alle 23 Patientinnen hatten jeweils mindestens ein unerwünschtes Ereignis, das laut Prüfarzt mindestens möglicherweise mit Removab zusammenhing. Fieber, Übelkeit und Erbrechen traten bei 19, 14 und 13 Patientinnen am häufigsten auf. 6 dieser Patientinnen hatten jeweils mindestens ein schwerwiegendes unerwünschtes Ereignis, das nach Ansicht des Prüfarztes mindestens möglicherweise mit Removab zusammenhing. Dies waren Hautinfektion und Darmverschluß bei jeweils 2 Patientinnen, sowie hämorrhagische Gastritis, Brustschmerz und abnorme Leberenzyme bei jeweils 1 Patientin. 6 Patientinnen starben, es wurde jedoch keiner dieser Todesfälle in Zusammenhang mit
5 AGO-OVAR Seite 5 von 10 Removab gebracht. Die maximal tolerierbare Dosis war laut Dose Steering Board bei µg erreicht. Studienzentren Fallzahl Studienziele Da in der Phase I keine klare Dosis-Wirkungsbeziehung und auch keine klare Dosis-Toxizitätsbeziehung festgestellt wurde, sind hierfür weitere Untersuchungen notwendig. Multizentrische europäische Studie (Deutschland, Belgien, Frankreich und Großbritannien) 44 Patientinnen (22 pro Arm). Primäres Studienziel: Selektion der besseren Dosisstufe basierend auf dem bestätigten Tumoransprechen. Ansprecher sind Patientinnen mit einem Gesamtansprechen (vollständiges Ansprechen [CR] und partielles Ansprechen [PR]) gemäß der Ansprech-Evaluationskriterien bei soliden Tumoren Response Evaluation Criteria in Solid Tumors [RECIST] Kriterien entsprechend der Beurteilung durch einen unabhängigen, verblindeten Gutachter. Sekundäre Studienziele: Beurteilung der Sicherheit und Verträglichkeit basierend auf: Unerwünschten Ereignissen (adverse events, AEs), Auftretenshäufigkeit und Gründen für die Verschiebung oder den endgültigen Abbruch der Removab Behandlung, Sicherheitslaborwerten (Hämatologie mit Differentialblutbild, klinische Chemie, Koagulation und Urinanalyse), Körperlicher Untersuchung, Vitalfunktionen, Röntgen Thorax, EKG. Beurteilung der Effekte von Removab basierend auf: Anteil der Patientinnen mit stabiler Krankheit (stable disease, SD) gemäß RECIST Qualitativem Ansprechen mittels Laparoskopie (nach Maßgabe des Prüfarztes an einwilligenden Patientinnen), Disseminierten Tumorzellen im Knochenmark (nach Maßgabe des Prüfarztes an Patientinnen nach gesonderter Einwilligungserklärung). Zeit bis zur Progression (TTP) (in der Post-Studien-Phase), Gesamtüberleben (in der Post-Studien-Phase). Beurteilung der nachfolgenden Krebstherapien (in der Post-Studien- Phase). Beurteilung der Human Anti-Maus Antikörper (HAMA)/human Anti- Ratten Antikörper (HARA) Serum Konzentration. Beurteilung der Pharmakokinetik basierend auf den Removab Serum Konzentrationen (optional und nur in der höheren Dosisgruppe). Beurteilung der Pharmakodynamik basierend auf der Serum Konzentration der Cytokine (optional). Beurteilung von CA 125 und Vergleich der CA 125 Ansprechkriterien
6 AGO-OVAR Seite 6 von 10 mit den RECIST Kriterien. Design Randomisierung Prüfmedikament Multizentrische randomisierte (1:1), offene Phase IIa Studie mit 2 Dosisstufen an Patientinnen mit platinresistentem epithelialem Ovarialkarzinom zur Selektion der besseren Dosisstufe. Removab wird pro Patientin einmal in einer Dosisserie von 4 Dosen verabreicht (intraperitoneale Infusionen an den Tagen 0, 3, 7, und 10). Die Patientinnen werden nach dem Studienende lebenslang alle 2 Monate telefonisch oder ambulant nachverfolgt und die Zeit bis zur Progression und das Gesamtüberleben sowie etwaige neue Krebsbehandlungen dokumentiert. Die Patientinnen werden per Randomisierung den beiden Dosisarmen im Verhältnis 1:1 zugewiesen. Removab (anti-epcam x anti-cd3) Dosis und Verabreichung Jede Patientin wird per Randomisierung einer der beiden folgenden Dosisstufen zugewiesen: Dosisreduktion oder Verschiebung der Infusion Studiendauer Niedriger Dosisarm: µg Hoher Dosisarm: µg Removab wird 4 Mal verabreicht (Tag 0, 3, 7 und 10). Um eine Behandlung am Wochenende zu vermeiden, muss die Studienbehandlung am Montag beginnen. Die 6-stündige i.p. Infusion wird mittels eines Katheters, einer Hohlnadel oder eines Port-Systems verabreicht. Vormedikation: 1000 mg Paracetamol 30 Minuten vor Beginn der Infusion. Zur besseren Verteilung des Antikörpers werden 500 ml NaCl Lösung 30 Minuten vor dem Beginn der Infusion i.p. verabreicht. An den Infusionstagen werden die Patientinnen für mindestens 24 Stunden hospitalisiert. Patientinnen, die weit entfernt vom Krankenhaus wohnen, können während der ganzen Verabreichungsdauer hospitalisiert bleiben. Die Verabreichung von Removab kann beim Auftreten relevanter unerwünschter Ereignisse (adverse events, AEs) verschoben werden: Lebertoxizität Grad 3, bis zur Besserung auf mindestens Grad 2, Fieber 39,0 C. Die gesamte Behandlungsdauer sollte 21 Tage nicht überschreiten. Dosisreduktionen sind nicht erlaubt. Nach der Voruntersuchung dauert die Studie für die Patientin 60 Tage im Falle von SD oder PD am Tag 60 und 90 Tage im Falle von CR oder PR am Tag 60. Nach Studienabschluss werden die Patientinnen lebenslang alle 2 Monate telefonisch oder ambulant nachverfolgt. Die Studie soll von Januar 2004 (erste Patientin erste Visite) bis Januar 2005 (letzte Patientin letzte Visite) stattfinden. Die folgenden Visiten finden statt: Voruntersuchung: Tag 14 bis Tag 1
7 AGO-OVAR Seite 7 von 10 Einschlusskriterien Removab Verabreichung: Tag 0, 3, 7 und 10 3, bzw. 4 Nachuntersuchungen: Tag 18 (±4), Tag 30 (±4), Tag 60 (±4) = Abschlußuntersuchung, Tag 90 (nur bei Patientinnen mit CR oder PR). Frauen, die 18 Jahre oder älter sind. Histologisch bestätigtes epitheliales Ovarialkarzinom. Meßbare Krankheit. Datierte und unterschriebene Einwilligungserklärung. Eine oder zwei vorausgegangene Chemotherapien, von denen die letzte auf Platin basierte. Platinresistenz nach der ersten und/oder zweiten Chemotherapie (definiert als Progression [progressive disease, PD] oder behandlungsfreies Intervall 6 Monate nach dem Ende einer Chemotherapie, die auf Platin basierte). Eastern Cooperative Oncology Group (ECOG) Status 0-2. Negativer Schwangerschaftstest bei gebärfähigen Frauen bei der Voruntersuchung.
8 AGO-OVAR Seite 8 von 10 Ausschlusskriterien Akute oder chronische Infektion, die nach Einschätzung des Prüfers eine Studienteilnahme nicht erlaubt. Behandlung mit einem Studienmedikament, einer Krebs Chemo- oder Radiotherapie innerhalb der letzten 28 Tage (vor der ersten Removab Infusion). Vorherige Behandlung mit einem monoklonalen Maus Antikörper. Bekannte oder vermutete Hypersensibilität gegenüber Removab oder ähnlichen Antikörper. Zweite Malignanz innerhalb der letzten 5 Jahre. Nicht-invasive, nicht-melanomatöse Hautkarzinome sind erlaubt. Unzureichende Nierenfunktion (Kreatinin >1,5 x ULN). Unzureichende Leberfunktion (ASAT, ALAT, GGT >2,0 x ULN, bei Vorliegen von Lebermetastasen >5,0 x ULN; Bilirubin >1,5 x ULN). Thrombozyten < Zellen/mm 3 ; Absolute Neutrophilenzahl <1.500 Zellen/mm 3. Kachektische Patientinnen mit einem Körpergewicht <45 kg. Patientinnen, die eine parenterale Ernährung benötigen. Patientinnen mit einem Ileus innerhalb der letzten 30 Tage. Patientinnen mit einer lebensbedrohlichen Krankheit oder einer anderen schweren Erkrankung, die die Patientinnen, nach Ansicht des Prüfers, im Falle der Studienteilnahme einem Risiko über Gebühr aussetzen würde. Jede andere Kondition, die nach Ansicht des Prüfers im Falle der Studienteilnahme für die Patientin zu einem Risiko über Gebühr führen würde. Schwangere oder stillende Frauen, bzw. gebährfähige Frauen, die keine zuverlässige Form der Verhütung während und in den 3 Monaten nach der letzten Infusion praktizieren. Statistische Methoden Vorgeschichte eines Myokardinfarktes, eines kongestiven Herzversagen oder einer signifikanten kardialen Arrhythmie innerhalb der letzten 6 Monate. Die Hauptanalyse des primären Zielkriteriums (bestätigtes Tumoransprechen gemäß RECIST) basiert auf der intent-to-treat Population (ITT). Das primäre Zielkriterium wird deskriptiv zusammengefasst. Eine inferenzstatistische Prüfung auf Unterschiede zwischen den beiden Armen ist nicht geplant. Die Selektion der besseren Dosisstufe basiert auf dem Phase II Selektionsdesign (Simon et al. 1985). Derjenige Arm, in dem eine höhere Tumoransprechrate (= Anteil an Patientinnen mit bestätigter CR und PR) beobachtet wird, wird als der bessere Arm gewählt, unabhängig davon wie groß der Unterschied zwischen den beiden Armen ausfällt. Alle sekundären Kriterien werden deskriptiv zusammengefasst. Das Gesamtüberleben und TTP werden mittels Kaplan-Meier Methoden geschätzt.
9 AGO-OVAR Seite 9 von 10 Das Ansprechen gemäß CA 125 und das Ansprechen gemäß RECIST werden mittels eines Standard-Konkordanzmaßes verglichen, wobei die RECIST Kriterien als Goldstandard dienen.
10 AGO-OVAR Seite 10 von 10 Übersicht über die Untersuchungen (Die Behandlung sollte am Montag beginnen) Removab Infusionen Voruntersuchung Nachfolgeuntersuchungen Post-Studien Untersuchungen Tag Nr. -14 bis ±4 30±4 60±4 90±4 Alle 2 Monate Visiten Nr Einwilligungserklärung X Demographie und Grundcharakteristik X Medizinische und Karzinom Vorgeschichte sowie ECOG X Frühere Medikamente X Körpergewicht X X X X Körperliche Untersuchung X X X EKG, Thorax Röntgen X EpCAM positive Tumorzellen (X) CT oder MRT für RECIST Kriterien 1 X X X 2 Tumormarker CA 125 X X 3 X X X 2 Laparoskopie (optional) (X) (X) Tumorzellen im Knochenmark (optional) (X) (X) 6-stündige Infusion (gemäß Randomisierung) X X X X Unerwünschte Ereignisse und Begleitmedikamente X X X X X X X X X X X X Sicherheitslabor X 4 X 3 X X 3 X X 3 X X 3 X X X X Vitalfunktionen (Temperatur, Puls und Blutdruck) X X 3 X X 3 X X 3 X X 3 X X X X HAMA / HARA X 3 X X X Pharmakodynamik (optional) 5 (X) (X) (X) (X) (X) (X) (X) (X) Pharmakokinetik (optional) 6 (X) (X) (X) (X) (X) (X) (X) (X) Gesamtüberleben, TTP und nachfolgende Krebstherapien X 1 Falls eine vergleichbare CT/MRT Untersuchung innerhalb von 28 Tagen vorliegt, braucht sie bei der Voruntersuchung nicht mehr durchgeführt werden. 2 CT/MRT Untersuchung und CA 125 im Falle einer vollständigen oder partiellen Remission gemäß RECIST werden auch an Tag 90 untersucht. 3 Immer kurz vor dem Beginn der Removab Infusion 4 Einschließlich Schwangerschaftstest bei gebärfähigen Frauen. 5 Pharmakodynamik (optional): An den Infusionstagen: kurz bevor und am Ende der Infusion (+ 1 h), und 24 h (±2 h) nach Beginn der Infusion zur Bestimmung der Cytokine im Serum. 6 Pharmakokinetik (Nur in der höheren Dosisgruppe, optional): kurz bevor und am Ende der Infusion (+ 1 h), und 24 h (±2 h) nach Beginn der Infusion zur Bestimmung der Removab Serum Konzentration. Unerwünschte Ereignisse und Begleitmedikation werden während der ganzen Studie bis Tag 60 (Abschlußvisite) bei jeder Visite dokumentiert.
Protokol ID: AGO-OVAR OP.4 (AGO DESKTOP OVAR III)
 EINE RANDOMISIERTE, MULTIZENTRISCHE STUDIE ZUM VERGLEICH DER WIRKSAMKEIT EINER ZUSÄTZLICHEN TUMORDEBULKING-OPERATION GEGEN EINE ALLEINIGE CHEMOTHERAPIE BEI PATIENTINNEN MIT EINEM PLATIN-SENSIBLEN OVARIALKARZINOM-REZIDIV
EINE RANDOMISIERTE, MULTIZENTRISCHE STUDIE ZUM VERGLEICH DER WIRKSAMKEIT EINER ZUSÄTZLICHEN TUMORDEBULKING-OPERATION GEGEN EINE ALLEINIGE CHEMOTHERAPIE BEI PATIENTINNEN MIT EINEM PLATIN-SENSIBLEN OVARIALKARZINOM-REZIDIV
AGO-OVAR OP.2 (AGO DESKTOP OVAR II)
 EVALUATION EINES PRÄDIKTORS FÜR DIE KOMPLETTE RESEKTION BEI PLATIN-SENSIBLEM OVARIALKARZINOMREZIDIV AGO-OVAR OP.2 (AGO DESKTOP OVAR II) Ein Projekt der AGO Kommission OVAR und der AGO Studiengruppe Ovarialkarzinom
EVALUATION EINES PRÄDIKTORS FÜR DIE KOMPLETTE RESEKTION BEI PLATIN-SENSIBLEM OVARIALKARZINOMREZIDIV AGO-OVAR OP.2 (AGO DESKTOP OVAR II) Ein Projekt der AGO Kommission OVAR und der AGO Studiengruppe Ovarialkarzinom
KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM
 KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM 11.11.02 RANDOMISIERTE, OFFENE, NICHT-KOMPARATIVE PHASE II STUDIE ZUR BEURTEILUNG DER WIRKSAMKEIT UND VERTRÄGLICHKEIT VON ZWEI DOSIERUNGEN ZD1839 BEI PATIENTEN
KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM 11.11.02 RANDOMISIERTE, OFFENE, NICHT-KOMPARATIVE PHASE II STUDIE ZUR BEURTEILUNG DER WIRKSAMKEIT UND VERTRÄGLICHKEIT VON ZWEI DOSIERUNGEN ZD1839 BEI PATIENTEN
Tätigkeitsbericht der Kommission Ovar der AGO
 Tätigkeitsbericht der Kommission Ovar der AGO 2007-2009 B. Schmalfeldt State of the Art Symposium 19.06.09 Mitglieder der Kommission Ovar Prof. Dr. A. du Bois, Wiesbaden Dr. A. Burges, München Prof. Dr.
Tätigkeitsbericht der Kommission Ovar der AGO 2007-2009 B. Schmalfeldt State of the Art Symposium 19.06.09 Mitglieder der Kommission Ovar Prof. Dr. A. du Bois, Wiesbaden Dr. A. Burges, München Prof. Dr.
Studienmeeting der AG Ovarialkarzinom Berlin, Predictor-study
 Studienmeeting der AG Ovarialkarzinom Berlin, 19.03.2009 Predictor-study Diagnostische Genauigkeit von In-vitro-Diagnostika für die Vorhersage eines Therapieansprechens bei Patientinnen mit Ovarialkarzinom-Rezidiv
Studienmeeting der AG Ovarialkarzinom Berlin, 19.03.2009 Predictor-study Diagnostische Genauigkeit von In-vitro-Diagnostika für die Vorhersage eines Therapieansprechens bei Patientinnen mit Ovarialkarzinom-Rezidiv
Eine Phase II Studie der AGO Studiengruppe Ovarialkarzinom (AGO-OVAR), Deutschland. Phase II Protokoll AGO-OVAR 2.11
 1 PHASE II STUDIE BEIM PLATINREFRAKTÄREN OVARIALKARZINOM: EINE RANDOMISIERTE MULTIZENTRISCHE STUDIE ZUR EVALUATION DER TOLERABILITÄT, TOXIZITÄT UND EFFEKTIVITÄT EINER MONOTHERAPIE MIT DEM ZIELGERICHTETEN
1 PHASE II STUDIE BEIM PLATINREFRAKTÄREN OVARIALKARZINOM: EINE RANDOMISIERTE MULTIZENTRISCHE STUDIE ZUR EVALUATION DER TOLERABILITÄT, TOXIZITÄT UND EFFEKTIVITÄT EINER MONOTHERAPIE MIT DEM ZIELGERICHTETEN
Eine Studie der Arbeitsgemeinschaft Gynäkologische Onkologie: AGO Studiengruppe. Deutsches Kurzprotokoll Phase II Protokoll AGO-GYN 7
 Phase II-Studie zum Einsatz der Kombinationschemotherapie PegLiposomales Doxorubicin (PLD) und Carboplatin bei gynäkologischen Sarkomen und gemischt epithelial-mesenchymalen Tumoren Eine Studie der Arbeitsgemeinschaft
Phase II-Studie zum Einsatz der Kombinationschemotherapie PegLiposomales Doxorubicin (PLD) und Carboplatin bei gynäkologischen Sarkomen und gemischt epithelial-mesenchymalen Tumoren Eine Studie der Arbeitsgemeinschaft
ABA-01 Menarini Ricerche S.p.A. Deutsches Kurzprotokoll AGO Studiengruppe Ovarialkarzinom (AGO-OVAR) Phase II/III Protokoll AGO-OVAR 10
 Eine randomisierte, doppelblinde, Placebo kontrollierte, multizentrische Studie mit Abagovomab als Erhaltungstherapie bei Patientinnen mit epithelialem Ovarialkarzinom und kompletter Remission nach erfolgter
Eine randomisierte, doppelblinde, Placebo kontrollierte, multizentrische Studie mit Abagovomab als Erhaltungstherapie bei Patientinnen mit epithelialem Ovarialkarzinom und kompletter Remission nach erfolgter
Verbessert eine palliative Chemotherapie die Symptome bei Patientinnen mit rezidivierten Ovarialkarzinom? Deutsches Kurzprotokoll
 Verbessert eine palliative Chemotherapie die Symptome bei Patientinnen mit rezidivierten Ovarialkarzinom? Deutsches Kurzprotokoll AGO-PO 1/Symptom Benefit Eine Studie der GCIG Internationaler Studienleiter
Verbessert eine palliative Chemotherapie die Symptome bei Patientinnen mit rezidivierten Ovarialkarzinom? Deutsches Kurzprotokoll AGO-PO 1/Symptom Benefit Eine Studie der GCIG Internationaler Studienleiter
Aktuelle Aspekte der PARP-Inhibition: Wer profitiert, wer nicht?
 Ovarialkarzinom State of the Art AGO-Symposium Aktuelle Aspekte der PARP-Inhibition: Wer profitiert, wer nicht? Pauline Wimberger Klinik und Poliklinik für Gynäkologie und Geburtshilfe Technische Universität
Ovarialkarzinom State of the Art AGO-Symposium Aktuelle Aspekte der PARP-Inhibition: Wer profitiert, wer nicht? Pauline Wimberger Klinik und Poliklinik für Gynäkologie und Geburtshilfe Technische Universität
Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid
 10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
Die Therapie des Ovarialkarzinoms in Deutschland. Die Therapie des Ovarialkarzinoms in Deutschland
 Die Therapie des Ovarialkarzinoms in Deutschland eine Qualitätssicherungserhebung tssicherungserhebung Q III 2004 A. du Bois 1, J. Rochon 2, C. Lamparter 3, J. Pfisterer 4 für r die AGO Organkommission
Die Therapie des Ovarialkarzinoms in Deutschland eine Qualitätssicherungserhebung tssicherungserhebung Q III 2004 A. du Bois 1, J. Rochon 2, C. Lamparter 3, J. Pfisterer 4 für r die AGO Organkommission
AGO-OVAR 19 / TRUST. (platinfreies Intervall 6-12 Monate) Intermediär-platinsensibles Rezidiv. Erstdiagnose FIGO IIIB-IV
 Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
Chronische lymphatische Leukämien - CLL2-BCG
 Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronische lymphatische Leukämien - CLL2-BCG Prüfplancode ISRCTN
Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronische lymphatische Leukämien - CLL2-BCG Prüfplancode ISRCTN
Verbessert eine palliative Chemotherapie die Symptome bei Patientinnen mit rezidiviertem Ovarialkarzinom? Deutsches Kurzprotokoll
 Verbessert eine palliative Chemotherapie die Symptome bei Patientinnen mit rezidiviertem Ovarialkarzinom? Deutsches Kurzprotokoll AGO-PO 1/Symptom Benefit Eine Studie der GCIG Internationaler Studienleiter
Verbessert eine palliative Chemotherapie die Symptome bei Patientinnen mit rezidiviertem Ovarialkarzinom? Deutsches Kurzprotokoll AGO-PO 1/Symptom Benefit Eine Studie der GCIG Internationaler Studienleiter
Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil
 CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
Die Therapie des Ovarialkarzinoms in Deutschland. Die Therapie des Ovarialkarzinoms in Deutschland
 Die Therapie des Ovarialkarzinoms in Deutschland eine Qualitätssicherungserhebung tssicherungserhebung Q III 2004 A. du Bois, J. Rochon 2, C. Lamparter 3, J. Pfisterer 4 für r die AGO Organkommission OVAR
Die Therapie des Ovarialkarzinoms in Deutschland eine Qualitätssicherungserhebung tssicherungserhebung Q III 2004 A. du Bois, J. Rochon 2, C. Lamparter 3, J. Pfisterer 4 für r die AGO Organkommission OVAR
Synopse AGO OVAR OP.7 TRUST/AGO OVAR 19 nationaler Part / Deutschland
 Synopse Protokolltitel Studie zur primären radikalen Operation bei fortgeschrittenem Ovarialkarzinom Erweiterung für Deutschland mit Evaluation von Fragilität und Langzeit Lebensqualität Protokollnummer
Synopse Protokolltitel Studie zur primären radikalen Operation bei fortgeschrittenem Ovarialkarzinom Erweiterung für Deutschland mit Evaluation von Fragilität und Langzeit Lebensqualität Protokollnummer
O f f e n e S t u d i e n - August 2013 -
 Sehr geehrte Patientinnen und Angehörige, sehr geehrte Ärztinnen und Ärzte, Klinische Studien zur Behandlung des Ovarial-, Tuben-, Endometrium- und Peritonealkarzinoms: bevor antihormonelle, chemotherapeutische
Sehr geehrte Patientinnen und Angehörige, sehr geehrte Ärztinnen und Ärzte, Klinische Studien zur Behandlung des Ovarial-, Tuben-, Endometrium- und Peritonealkarzinoms: bevor antihormonelle, chemotherapeutische
Eine Phase II Studie der AGO Studiengruppe Ovarialkarzinom (AGO-OVAR), Deutschland. (SPRI Protocol P02531)
 EINE MULTIZENTRISCHE RANDOMISIERTE PHASE II STUDIE ZUM VERGLEICH VON PACLITAEL/CARBOPLATIN UND LONAFARNIB VERSUS PACLITAEL/CARBOPLATIN IN DER PRIMÄRCHEMOTHERAPIE VON PATIENTINNEN MIT EINEM EPITHELIALEN
EINE MULTIZENTRISCHE RANDOMISIERTE PHASE II STUDIE ZUM VERGLEICH VON PACLITAEL/CARBOPLATIN UND LONAFARNIB VERSUS PACLITAEL/CARBOPLATIN IN DER PRIMÄRCHEMOTHERAPIE VON PATIENTINNEN MIT EINEM EPITHELIALEN
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
MICORYX Weitere Informationen
 MICORYX Weitere Informationen Im Rahmen der Micoryx-Studie wird eine neue Therapie getestet, die sich noch in der Erprobungsphase befindet. Es handelt sich dabei um eine Impfung gegen den Tumor mit Hilfe
MICORYX Weitere Informationen Im Rahmen der Micoryx-Studie wird eine neue Therapie getestet, die sich noch in der Erprobungsphase befindet. Es handelt sich dabei um eine Impfung gegen den Tumor mit Hilfe
Humira jetzt bei polyartikulärer juveniler idiopathischer Arthritis für Kinder ab vier Jahren zugelassen
 EU-Zulassungserweiterung für Adalimumab (Humira ) Humira jetzt bei polyartikulärer juveniler idiopathischer Arthritis für Kinder ab vier Jahren zugelassen Wiesbaden/Ludwigshafen (1. Juli 2011) Die Europäische
EU-Zulassungserweiterung für Adalimumab (Humira ) Humira jetzt bei polyartikulärer juveniler idiopathischer Arthritis für Kinder ab vier Jahren zugelassen Wiesbaden/Ludwigshafen (1. Juli 2011) Die Europäische
Eine Zusammenfassung des Studienprotokolls
 Eine Zusammenfassung des Studienprotokolls Datum: Dienstag, 27. September 2011 Studiennummer: FumadermAA01 EudraCT-Nr.: 2011-000659-18 Leiter der klinischen Prüfung: Professor Dr. Martin Röcken Universitäts-Hautklinik,
Eine Zusammenfassung des Studienprotokolls Datum: Dienstag, 27. September 2011 Studiennummer: FumadermAA01 EudraCT-Nr.: 2011-000659-18 Leiter der klinischen Prüfung: Professor Dr. Martin Röcken Universitäts-Hautklinik,
Dossierbewertung A16-10 Version 1.0 Ramucirumab (Kolorektalkarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Therapie der älteren Patientin
 Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
ASCO 2017: Highlights zur Therapie des metastasierten t t Mammakarzinoms
 Johannes Ettl Interdisziplinäres Brustzentrum und Frauenklinik rechts der Isar, Technische Universität München, Direktorin: Prof. Dr. M. Kiechle ASCO 2017: Highlights zur Therapie des metastasierten t
Johannes Ettl Interdisziplinäres Brustzentrum und Frauenklinik rechts der Isar, Technische Universität München, Direktorin: Prof. Dr. M. Kiechle ASCO 2017: Highlights zur Therapie des metastasierten t
Originalarbeit: James et al., N Engl J Med 2012; 366:
 Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
STUDIENSYNOPSIS. Randomisierte Phase-II-Studie. Art der Studie. Prof. Dr. Volker Heinemann (Leiter der klinischen Prüfung) Studienleitung
 STUDIENSYNOPSIS Randomisierte Studie zur Wirksamkeit von FOLFIRI in Kombination mit Cetuimab vs. Bevacizumab in der Erstlinien-Behandlung des metastasierten kolorektalen Karzinoms mit K- RAS-Wildtyp Art
STUDIENSYNOPSIS Randomisierte Studie zur Wirksamkeit von FOLFIRI in Kombination mit Cetuimab vs. Bevacizumab in der Erstlinien-Behandlung des metastasierten kolorektalen Karzinoms mit K- RAS-Wildtyp Art
HECTOR (Hycamtin plus Carboplatin versus Established Regimens for the Treatment of Ovarian Cancer Relapse) EudraCT Number: 2006-004628-34
 Topotecan plus Carboplatin im Vergleich zur Standardtherapie (Paclitaxel plus Carboplatin oder Gemcitabin plus Carboplatin) in der Therapie von Patientinnen mit Platin-sensitivem rezidivierten epithelialen
Topotecan plus Carboplatin im Vergleich zur Standardtherapie (Paclitaxel plus Carboplatin oder Gemcitabin plus Carboplatin) in der Therapie von Patientinnen mit Platin-sensitivem rezidivierten epithelialen
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Systemtherapie gynäkologischer Malignome was ist neu?
 Systemtherapie gynäkologischer Malignome was ist neu? Jörg B. Engel Frauenklinik der Julius-Maximilians Universität Würzburg Zielgerichtete Therapie Small molecules Antikörper Hybridmoleküle Magic bullets
Systemtherapie gynäkologischer Malignome was ist neu? Jörg B. Engel Frauenklinik der Julius-Maximilians Universität Würzburg Zielgerichtete Therapie Small molecules Antikörper Hybridmoleküle Magic bullets
Protokoll-Synopsis (deutsch) AGO Studiengruppe Ovarialkarzinom (AGO-OVAR), Protokoll AGO-OVAR 2.9
 CALYPSO Studiennummer: 1204 Originalprotokoll (Endversion) 01.Nov. 2004 S. 1 von 12 Multinationale, randomisierte klinische Prüfung der Phase III zum Vergleich von Pegyliertem Liposomalem Doxorubicin (Caelyx)
CALYPSO Studiennummer: 1204 Originalprotokoll (Endversion) 01.Nov. 2004 S. 1 von 12 Multinationale, randomisierte klinische Prüfung der Phase III zum Vergleich von Pegyliertem Liposomalem Doxorubicin (Caelyx)
Phase II-Studie zur Behandlung des nicht kleinzelligen Bronchialkarzinoms im Stadium III b und IV mit der Kombination Docetaxel und Carboplatin
 Aus der Universitätsklinik und Poliklinik für Innere Medizin II an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Herr Professor Dr. med. Bernd Osten) Phase II-Studie zur Behandlung des nicht
Aus der Universitätsklinik und Poliklinik für Innere Medizin II an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Herr Professor Dr. med. Bernd Osten) Phase II-Studie zur Behandlung des nicht
DAUER DER STUDIE: Läuft seit Nov mindestens bis 2017.
 KLINISCHE STUDIE: Swiss Inflammatory Bowel Disease Cohort Study (SIBDCS) Multizentrische Beobachtungsstudie in der ganzen Schweiz (Basel, Bern, Genf, Lausanne, St-Gallen, Zürich) mit Patient die an einem
KLINISCHE STUDIE: Swiss Inflammatory Bowel Disease Cohort Study (SIBDCS) Multizentrische Beobachtungsstudie in der ganzen Schweiz (Basel, Bern, Genf, Lausanne, St-Gallen, Zürich) mit Patient die an einem
Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC
 SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
SATURN-Studie: Erhaltungstherapie mit Erlotinib verlängert Gesamtüberleben bei fortgeschrittenem NSCLC Grenzach-Wyhlen (13. August 2009) - Aktuelle Daten der SATURN-Studie bestätigen eine signifikante
Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse -
 Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse - Franz Edler von Koch Klinikum Dritter Orden Klinik für Gynäkologie und Geburtshilfe Brustzentrum Gynäkologisches
Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse - Franz Edler von Koch Klinikum Dritter Orden Klinik für Gynäkologie und Geburtshilfe Brustzentrum Gynäkologisches
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer in der DGGG e.v. sowie Version 2009.1.0 2010.1.0D Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer in der DGGG e.v. sowie Version 2009.1.0 2010.1.0D Neoadjuvante
Charitè, Campus Benjamin Franklin Medizinische Klinik III Hämatologie, Onkologie und Transfusionsmedizin Direktor Prof. Dr. E.
 VERGLEICHENDE PROSPEKTIVE STUDIE FÜR DIE PROPHYLAXE VON INVASIVEN MYKOTISCHEN INFEKTIONEN BEI NEUTROPENISCHEN PATIENTEN MIT TOPISCHEN ANTIMYKOTIKA IM VERGLEICH ZU NIEDRIGDOSIERTEM, LIPOSOMALEM AMPHOTERICIN
VERGLEICHENDE PROSPEKTIVE STUDIE FÜR DIE PROPHYLAXE VON INVASIVEN MYKOTISCHEN INFEKTIONEN BEI NEUTROPENISCHEN PATIENTEN MIT TOPISCHEN ANTIMYKOTIKA IM VERGLEICH ZU NIEDRIGDOSIERTEM, LIPOSOMALEM AMPHOTERICIN
1 von :09
 1 von 5 09.06.2011 15:09 2 von 5 09.06.2011 15:09 Klinische Studien CAI Prüfplancode ISRCTN EudraCT Clinicaltrials.gov DRKS CAI n/a NCT00126321 Therapie von Patienten mit rezidivierter akuter myeloischer
1 von 5 09.06.2011 15:09 2 von 5 09.06.2011 15:09 Klinische Studien CAI Prüfplancode ISRCTN EudraCT Clinicaltrials.gov DRKS CAI n/a NCT00126321 Therapie von Patienten mit rezidivierter akuter myeloischer
Charitè, Campus Benjamin Franklin Medizinische Klinik III Hämatologie, Onkologie und Transfusionsmedizin Direktor Prof. Dr. E.Thiel Berlin Bonn, 04/05
 VERGLEICHENDE PROSPEKTIVE STUDIE FÜR DIE PRIMÄRE UND SEKUNDÄRE PROPHYLAXE VON MYKOTISCHEN INFEKTIONEN BEI PATIENTEN MIT LANGER NEUTROPENIEDAUER MIT TOPISCHEN ANTIMYKOTIKA IM VERGLEICH MIT SYSTEMISCHER
VERGLEICHENDE PROSPEKTIVE STUDIE FÜR DIE PRIMÄRE UND SEKUNDÄRE PROPHYLAXE VON MYKOTISCHEN INFEKTIONEN BEI PATIENTEN MIT LANGER NEUTROPENIEDAUER MIT TOPISCHEN ANTIMYKOTIKA IM VERGLEICH MIT SYSTEMISCHER
GBG 80 - SenSzi. Sherko Kümmel Interdisziplinäres Brustzentrum Kliniken Essen-Mitte
 GBG 80 - SenSzi Randomisierte, kontrollierte, multizentrische, operative Studie zur Evaluation der Rolle einer präoperativen Lymphszintigraphie vor axillärer Sentinel-Lymphonodektomie beim primären Mammakarzinom
GBG 80 - SenSzi Randomisierte, kontrollierte, multizentrische, operative Studie zur Evaluation der Rolle einer präoperativen Lymphszintigraphie vor axillärer Sentinel-Lymphonodektomie beim primären Mammakarzinom
Neues vom ASCO. P. Wimberger Carl-Gustav-Carus Universität Technische Universität Dresden. Neues vom ASCO 2013
 Neues vom ASCO 2013 Neues vom ASCO P. Wimberger Carl-Gustav-Carus Universität Technische Universität Dresden First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz
Neues vom ASCO 2013 Neues vom ASCO P. Wimberger Carl-Gustav-Carus Universität Technische Universität Dresden First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz First-line Therapie: Neoadjuvanz
DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen
 DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen Sponsor: Universitätsklinikum Ulm (AöR), Albert-Einstein-Allee 29, 89081
DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen Sponsor: Universitätsklinikum Ulm (AöR), Albert-Einstein-Allee 29, 89081
Up-Date zur adjuvanten endokrinen Therapie des Mammakarzinoms
 Up-Date zur adjuvanten endokrinen Therapie des Mammakarzinoms München 10. Januar 2008 Franz Edler von Koch Klinik und Poliklinik für Frauenheilkunde und Geburtshilfe Großhadern Ludwig-Maximilians-Universität
Up-Date zur adjuvanten endokrinen Therapie des Mammakarzinoms München 10. Januar 2008 Franz Edler von Koch Klinik und Poliklinik für Frauenheilkunde und Geburtshilfe Großhadern Ludwig-Maximilians-Universität
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben?
 Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
HIPEC noch Wissenschaft oder schon Routine in der Rezidivsituation? Walther Kuhn Universitätsfrauenklinik, Bonn
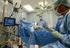 HIPEC noch Wissenschaft oder schon Routine in der Rezidivsituation? Walther Kuhn Universitätsfrauenklinik, Bonn Intraperitoneale Therapie: Rationale Ovarialkarzinom-Peritoneale Erkrankung Intraperitoneale
HIPEC noch Wissenschaft oder schon Routine in der Rezidivsituation? Walther Kuhn Universitätsfrauenklinik, Bonn Intraperitoneale Therapie: Rationale Ovarialkarzinom-Peritoneale Erkrankung Intraperitoneale
PROTOKOLL KURZFASSUNG deutsch
 PROTOKOLL KURZFASSUNG deutsch A multi-national randomized Phase III GCIG Intergroup Study comparing 1 st line chemotherapy with Gemcitabine, Paclitaxel and Carboplatin versus Paclitaxel and Carboplatin
PROTOKOLL KURZFASSUNG deutsch A multi-national randomized Phase III GCIG Intergroup Study comparing 1 st line chemotherapy with Gemcitabine, Paclitaxel and Carboplatin versus Paclitaxel and Carboplatin
Study of Letrozole Extension IBCSG BIG 1-07
 Study of Letrozole Extension IBCSG 35-07 BIG 1-07 Phase-III-Studie zur Untersuchung der Rolle einer fortlaufenden vs. intermittierenden Behandlung mit Letrozol nach vorangegangener 4- bis 6-jähriger adjuvanter
Study of Letrozole Extension IBCSG 35-07 BIG 1-07 Phase-III-Studie zur Untersuchung der Rolle einer fortlaufenden vs. intermittierenden Behandlung mit Letrozol nach vorangegangener 4- bis 6-jähriger adjuvanter
Second-line Chemotherapie
 Second-line Chemotherapie des metastasierten Urothelkarzinoms Übersicht First-line Standardtherapie Second-line Therapie: Vinflunin Second-line Therapie: Gemcitabin/Paclitaxel Second-line Therapie: Studie
Second-line Chemotherapie des metastasierten Urothelkarzinoms Übersicht First-line Standardtherapie Second-line Therapie: Vinflunin Second-line Therapie: Gemcitabin/Paclitaxel Second-line Therapie: Studie
Optimierung der Therapie des kolorektalen Karzinoms durch Panitumumab
 Neues und Wissenswertes aus der Onkologie Optimierung der Therapie des kolorektalen Karzinoms durch Panitumumab München (26. Juli 2012) - Deutliche Fortschritte in der Tumortherapie haben in den letzten
Neues und Wissenswertes aus der Onkologie Optimierung der Therapie des kolorektalen Karzinoms durch Panitumumab München (26. Juli 2012) - Deutliche Fortschritte in der Tumortherapie haben in den letzten
Dossierbewertung A17-24 Version 1.0 Nivolumab (Plattenepithelkarzinom des Kopf-Hals-Bereichs)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Nivolumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Nivolumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
Erbitux (Cetuximab) beim metastasierten kolorektalen Karzinom: Erstlinientherapie und Biomarker im Fokus
 Erbitux (Cetuximab) beim metastasierten kolorektalen Karzinom: Erstlinientherapie und Biomarker im Fokus Berlin (20. Februar 2008) Auch auf dem diesjährigen 28. Deutschen Krebskongress in Berlin überzeugte
Erbitux (Cetuximab) beim metastasierten kolorektalen Karzinom: Erstlinientherapie und Biomarker im Fokus Berlin (20. Februar 2008) Auch auf dem diesjährigen 28. Deutschen Krebskongress in Berlin überzeugte
WENN SOGAR UMARMUNGEN WEHTUN DIE NÄCHSTEN SCHRITTE. Informationen für Patienten. besuchen Sie
 DIE NÄCHSTEN SCHRITTE Wir danken Ihnen, dass Sie sich die Zeit genommen haben, sich über diese wichtige Studie zu informieren. Wenn Sie teilnehmen möchten, kontaktieren Sie uns bitte, damit wir einen Besuchstermin
DIE NÄCHSTEN SCHRITTE Wir danken Ihnen, dass Sie sich die Zeit genommen haben, sich über diese wichtige Studie zu informieren. Wenn Sie teilnehmen möchten, kontaktieren Sie uns bitte, damit wir einen Besuchstermin
HER2-positiver Rezeptorstatus als signifikanter Überlebensvorteil
 10 Jahre Herceptin HER2-positiver Rezeptorstatus als signifikanter Überlebensvorteil Frankfurt am Main (27. September 2010) - Die Entwicklung von Trastuzumab (Herceptin) hat die Brustkrebstherapie revolutioniert.
10 Jahre Herceptin HER2-positiver Rezeptorstatus als signifikanter Überlebensvorteil Frankfurt am Main (27. September 2010) - Die Entwicklung von Trastuzumab (Herceptin) hat die Brustkrebstherapie revolutioniert.
Klinik für Dermatologie der Universität zu Köln. Metastasiertes Melanom Aktuelles vom amerikanischen Krebskongress 2015.
 Klinik für Dermatologie der Universität zu Köln Metastasiertes Melanom Aktuelles vom amerikanischen Krebskongress 2015 Cornelia Mauch ASCO 2014: Übersicht CTLA-4 AK in der adjuvanten Therapie Kombinationstherapien
Klinik für Dermatologie der Universität zu Köln Metastasiertes Melanom Aktuelles vom amerikanischen Krebskongress 2015 Cornelia Mauch ASCO 2014: Übersicht CTLA-4 AK in der adjuvanten Therapie Kombinationstherapien
Version: V1.0 basierend auf Amendment 1 vom 15. Juli 2016
 Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and Trastuzumab or docetaxel, trastuzumab and, NCT02642458
Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and Trastuzumab or docetaxel, trastuzumab and, NCT02642458
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Herausforderungen in der individualisierten Therapie beim mcrc
 Erstlinientherapie des kolorektalen Karzinoms Herausforderungen in der individualisierten Therapie beim mcrc Berlin (2. Oktober 2010) Beim metastasierten kolorektalen Karzinom (mcrca) mit nicht-mutiertem
Erstlinientherapie des kolorektalen Karzinoms Herausforderungen in der individualisierten Therapie beim mcrc Berlin (2. Oktober 2010) Beim metastasierten kolorektalen Karzinom (mcrca) mit nicht-mutiertem
WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN
 CAMPUS INNENSTADT KOMM. DIREKTOR: PROF. DR: C. DANNEKER STELLV. DIREKTOR: PD DR. T. WEISSENBACHER WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN Informationsnachmittag- Leben mit Brustkrebs Was gibt es Neues?
CAMPUS INNENSTADT KOMM. DIREKTOR: PROF. DR: C. DANNEKER STELLV. DIREKTOR: PD DR. T. WEISSENBACHER WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN Informationsnachmittag- Leben mit Brustkrebs Was gibt es Neues?
Journal: Journal of Clinical Oncology Publikationsjahr: 2012 Autoren: Paulo M. Hoff, Andreas Hochhaus, Bernhard C. Pestalozzi et al.
 Cediranib Plus FOLFOX/CAPOX Versus Placebo Plus FOLFOX/CAPOX in Patients With Previously Untreated Metastatic Colorectal Cancer: A Randomized, Double Blind, Phase III Study (HORIZON II) Journal: Journal
Cediranib Plus FOLFOX/CAPOX Versus Placebo Plus FOLFOX/CAPOX in Patients With Previously Untreated Metastatic Colorectal Cancer: A Randomized, Double Blind, Phase III Study (HORIZON II) Journal: Journal
Dossierbewertung A15-13 Version 1.0 Ruxolitinib Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ruxolitinib gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ruxolitinib gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Erhaltungstherapie mit Rituximab beim follikulären Lymphom
 Prof. Dr. med. Wolfgang Hiddemann: Non-Hodgkin-Lymphom - Erhaltungstherapie mit Rituximab beim fol Non-Hodgkin-Lymphom Erhaltungstherapie mit Rituximab beim follikulären Lymphom Prof. Dr. med. Wolfgang
Prof. Dr. med. Wolfgang Hiddemann: Non-Hodgkin-Lymphom - Erhaltungstherapie mit Rituximab beim fol Non-Hodgkin-Lymphom Erhaltungstherapie mit Rituximab beim follikulären Lymphom Prof. Dr. med. Wolfgang
Neues aus Diagnostik und Therapie beim Lungenkrebs. Jürgen Wolf Centrum für Integrierte Onkologie Universitätsklinikum Köln
 Neues aus Diagnostik und Therapie beim Lungenkrebs Jürgen Wolf Centrum für Integrierte Onkologie Universitätsklinikum Köln Über was ich Ihnen heute berichten will: Lungenkrebs ist nicht gleich Lungenkrebs
Neues aus Diagnostik und Therapie beim Lungenkrebs Jürgen Wolf Centrum für Integrierte Onkologie Universitätsklinikum Köln Über was ich Ihnen heute berichten will: Lungenkrebs ist nicht gleich Lungenkrebs
GBG 80 - SenSzi. Johannes Holtschmidt Interdisziplinäres Brustzentrum Kliniken Essen-Mitte
 GBG 80 - SenSzi Randomisierte, kontrollierte, multizentrische, operative Studie zur Evaluation der Rolle einer präoperativen Lymphszintigraphie vor axillärer Sentinel-Lymphonodektomie beim primären Mammakarzinom
GBG 80 - SenSzi Randomisierte, kontrollierte, multizentrische, operative Studie zur Evaluation der Rolle einer präoperativen Lymphszintigraphie vor axillärer Sentinel-Lymphonodektomie beim primären Mammakarzinom
INHALT 1. EINLEITUNG: ZIEL DER STUDIE EPIDEMIOLOGIE VON NERVENWURZELREIZSYNDROMEN... 15
 INHALT 1. EINLEITUNG:... 14 1.1. ZIEL DER STUDIE... 14 1.2. EPIDEMIOLOGIE VON NERVENWURZELREIZSYNDROMEN... 15 1.3. ÄTIOLOGIE UND PATHOGENESE VON AKUTEN WURZELKOMPRESSIONSSYNDROMEN... 16 1.3.1. Degenerative
INHALT 1. EINLEITUNG:... 14 1.1. ZIEL DER STUDIE... 14 1.2. EPIDEMIOLOGIE VON NERVENWURZELREIZSYNDROMEN... 15 1.3. ÄTIOLOGIE UND PATHOGENESE VON AKUTEN WURZELKOMPRESSIONSSYNDROMEN... 16 1.3.1. Degenerative
Perjeta für die neoadjuvante Therapie zugelassen
 HER2-positives Mammakarzinom Perjeta für die neoadjuvante Therapie zugelassen Grenzach-Wyhlen (31. Juli 2015) - Die Europäische Arzneimittel-Agentur (EMA) hat Perjeta (Pertuzumab) in Kombination mit Herceptin
HER2-positives Mammakarzinom Perjeta für die neoadjuvante Therapie zugelassen Grenzach-Wyhlen (31. Juli 2015) - Die Europäische Arzneimittel-Agentur (EMA) hat Perjeta (Pertuzumab) in Kombination mit Herceptin
AGO-GYN 5 Deutsche Zusammenfassung des Prüfplans AEZS Æterna Zentaris
 Studientitel Studiennummer Studienphase VERTRAULICH Antitumorale Wirksamkeit und Verträglichkeit von AEZS-108, einem mit Doxorubizin gekoppelten LHRH-Agonisten, bei Frauen mit gynäkologischen Tumoren,
Studientitel Studiennummer Studienphase VERTRAULICH Antitumorale Wirksamkeit und Verträglichkeit von AEZS-108, einem mit Doxorubizin gekoppelten LHRH-Agonisten, bei Frauen mit gynäkologischen Tumoren,
Studien am Hauttumorzentrum Erfurt
 Studien am Hauttumorzentrum Erfurt Helios Klinikum Erfurt www.helios-gesundheit.de Melanom: adjuvant im Stadium IV Melanom: palliativ Immuned Nivolumab vs. Nivolumab + Ipilimumab Randomisierte, doppelt-verblindete,
Studien am Hauttumorzentrum Erfurt Helios Klinikum Erfurt www.helios-gesundheit.de Melanom: adjuvant im Stadium IV Melanom: palliativ Immuned Nivolumab vs. Nivolumab + Ipilimumab Randomisierte, doppelt-verblindete,
Dissertation zur Erlangung des akademischen Grades Doktor der Medizin (Dr. med.)
 Aus der Universitätsklinik und Poliklinik für Innere Medizin II (Direktor: Prof. Dr. med. habil. B. Osten) der Martin-Luther-Universität Halle-Wittenberg und der Klinik für Innere Medizin II (Chefarzt
Aus der Universitätsklinik und Poliklinik für Innere Medizin II (Direktor: Prof. Dr. med. habil. B. Osten) der Martin-Luther-Universität Halle-Wittenberg und der Klinik für Innere Medizin II (Chefarzt
STUDIEN PRO UND CONTRA
 V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms
 AMB 2006, 40, 89 Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms Mit Thalidomid, Lenalidomid und Bortezomib (Velcade ) stehen inzwischen neue Wirkstoffe für die
AMB 2006, 40, 89 Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms Mit Thalidomid, Lenalidomid und Bortezomib (Velcade ) stehen inzwischen neue Wirkstoffe für die
Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie
 Neue Studie zu Iscador Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie Schwäbisch-Gmünd (2. Dezember 2009) - Eine prospektive randomisierte offene Pilotstudie ergab eine Verbesserung
Neue Studie zu Iscador Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie Schwäbisch-Gmünd (2. Dezember 2009) - Eine prospektive randomisierte offene Pilotstudie ergab eine Verbesserung
Patienteninformation
 Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, Ihr Arzt hat Ihnen die Möglichkeit zur Teilnahme an einer klinischen Studie eröffnet. Vielleicht sind Sie auch durch eigene Initiative
Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, Ihr Arzt hat Ihnen die Möglichkeit zur Teilnahme an einer klinischen Studie eröffnet. Vielleicht sind Sie auch durch eigene Initiative
Kein Hand-Fuß-Syndrom unter Behandlung mit UFT (Tegafur Uracil)
 ESMO: Kein Hand-Fuß-Syndrom unter Behandlung mit UFT (Tegafur Uracil) Darmstadt (8. Oktober 2008) Auf der 33. Jahrestagung der European Society for Medical Oncology (ESMO) wurden die Ergebnisse einer Untersuchung
ESMO: Kein Hand-Fuß-Syndrom unter Behandlung mit UFT (Tegafur Uracil) Darmstadt (8. Oktober 2008) Auf der 33. Jahrestagung der European Society for Medical Oncology (ESMO) wurden die Ergebnisse einer Untersuchung
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom
 Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
AMLSG Amendment Nr. 3 vom zur Version der Protokollanhänge vom
 Studie: Randomisierte Phase II-Studie zu All-trans-Retinsäure bei der Induktions- und Konsolidierungstherapie sowie Pegfilgrastim in der Konsolidierungstherapie bei jüngeren Patienten mit neu diagnostizierter
Studie: Randomisierte Phase II-Studie zu All-trans-Retinsäure bei der Induktions- und Konsolidierungstherapie sowie Pegfilgrastim in der Konsolidierungstherapie bei jüngeren Patienten mit neu diagnostizierter
Dossierbewertung A16-11 Version 1.0 Ramucirumab (Lungenkarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Was gibt es Neues in der Therapie? YAEL Arzt-Patientenseminar, Hamburg Christoph Schramm I. Medizinische Klinik und Poliklinik, UKE
 Was gibt es Neues in der Therapie? YAEL Arzt-Patientenseminar, Hamburg 2011 Christoph Schramm I. Medizinische Klinik und Poliklinik, UKE Autoimmune Lebererkrankungen Autoimmune Lebererkrankungen Autoimmune
Was gibt es Neues in der Therapie? YAEL Arzt-Patientenseminar, Hamburg 2011 Christoph Schramm I. Medizinische Klinik und Poliklinik, UKE Autoimmune Lebererkrankungen Autoimmune Lebererkrankungen Autoimmune
Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2016.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2016.1D Endokrine und zielgerichtete Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten
Europac-2. Inhalte und aktueller Stand. Eckhard Weber. Klinik für Innere Medizin A Universitätsmedizin Greifswald
 Europac-2 Inhalte und aktueller Stand 1456 1856 Eckhard Weber Klinik für Innere Medizin A Universitätsmedizin Greifswald Was ist eine klinische Studie? Werkzeug der klinischen Forschung zur Untersuchung
Europac-2 Inhalte und aktueller Stand 1456 1856 Eckhard Weber Klinik für Innere Medizin A Universitätsmedizin Greifswald Was ist eine klinische Studie? Werkzeug der klinischen Forschung zur Untersuchung
Mitteilung an die Medien
 Mitteilung an die Medien Basel, 17 November 2014 FDA erteilt Zulassung für Roche-Medikament Avastin plus Chemotherapie für Frauen mit platinresistentem, rezidivierendem Eierstockkrebs Avastin plus Chemotherapie
Mitteilung an die Medien Basel, 17 November 2014 FDA erteilt Zulassung für Roche-Medikament Avastin plus Chemotherapie für Frauen mit platinresistentem, rezidivierendem Eierstockkrebs Avastin plus Chemotherapie
Rezidivchirurgie beim Ovarialkarzinom
 Rezidivchirurgie beim Ovarialkarzinom Die DESKTOP I - III Serie Philipp Harter für die Kommission OVAR Ovarialkarzinom - State of the Art München 19./20.Juni 2009 Rezidivchirurgie beim Ovarialkarzinom
Rezidivchirurgie beim Ovarialkarzinom Die DESKTOP I - III Serie Philipp Harter für die Kommission OVAR Ovarialkarzinom - State of the Art München 19./20.Juni 2009 Rezidivchirurgie beim Ovarialkarzinom
Deutsche Synopse. Studienphase und Titel:
 MEL001-Studie Seite 1 Deutsche Synopse Studienphase und Titel: Eine prospektive Phase I und fortlaufende Phase II, zweiarmige, randomisierte, multizentrische Studie von Temsirolimus in Kombination mit
MEL001-Studie Seite 1 Deutsche Synopse Studienphase und Titel: Eine prospektive Phase I und fortlaufende Phase II, zweiarmige, randomisierte, multizentrische Studie von Temsirolimus in Kombination mit
Kardio-CT im akuten Koronarsyndrom Gegenwart und Zukun. Hamburg Heart View,
 Kardio-CT im akuten Koronarsyndrom Gegenwart und Zukun. Hamburg Heart View, 05.11.2016 Prof. Dr. Gunnar Lund, Klinik und Poliklinik für diagnostische und interventionelle Radiologie, Universitätskrankenhaus
Kardio-CT im akuten Koronarsyndrom Gegenwart und Zukun. Hamburg Heart View, 05.11.2016 Prof. Dr. Gunnar Lund, Klinik und Poliklinik für diagnostische und interventionelle Radiologie, Universitätskrankenhaus
Onkologische Nachsorge
 Onkologische Nachsorge Dr. med. R. Dengler Schwerpunktpraxis und Tagesklinik für Hämatologie und Onkologie Dr. med. R. Dengler & Dr. med. A. Kröber Hildegard-von-Bingen-Str. 1, 93053 Regensburg Tel: 0941/566342
Onkologische Nachsorge Dr. med. R. Dengler Schwerpunktpraxis und Tagesklinik für Hämatologie und Onkologie Dr. med. R. Dengler & Dr. med. A. Kröber Hildegard-von-Bingen-Str. 1, 93053 Regensburg Tel: 0941/566342
Bildgebung vor Lebermetastasenresektion bei KRK: RECIST? - PET/CT?
 GI-Oncology 2009 5. Interdiziplinäres Update Bildgebung vor Lebermetastasenresektion bei KRK: RECIST? - PET/CT? Prof. Dr. med. Ernst J. Rummeny Institut für Röntgendiagnostik Klinikum rechts der Isar Technische
GI-Oncology 2009 5. Interdiziplinäres Update Bildgebung vor Lebermetastasenresektion bei KRK: RECIST? - PET/CT? Prof. Dr. med. Ernst J. Rummeny Institut für Röntgendiagnostik Klinikum rechts der Isar Technische
Bestrahlung der parasternalen LK beim Mamma-Ca Aktuelle Daten der dänischen Studiengruppe
 seit 350 Jahren ganz weit oben Bestrahlung der parasternalen LK beim Mamma-Ca Aktuelle Daten der dänischen Studiengruppe Jürgen Dunst Professor für Strahlentherapie, Christian-Albrechts-Universität zu
seit 350 Jahren ganz weit oben Bestrahlung der parasternalen LK beim Mamma-Ca Aktuelle Daten der dänischen Studiengruppe Jürgen Dunst Professor für Strahlentherapie, Christian-Albrechts-Universität zu
mit symptomatischen Knochenmetastasen beim CRPC
 Innovation aus der Bayer Onkologie-Entwicklung: Xofigo Eine neue Therapieoption für Patienten mit s Innovation aus der Bayer Onkologie-Entwicklung Xofigo Eine neue Therapieoption für Patienten mit symptomatischen
Innovation aus der Bayer Onkologie-Entwicklung: Xofigo Eine neue Therapieoption für Patienten mit s Innovation aus der Bayer Onkologie-Entwicklung Xofigo Eine neue Therapieoption für Patienten mit symptomatischen
Kontrolluntersuchungen Welche und wie oft?
 Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Dr. med. Christian Taverna Kantonsspital Münsterlingen Kontrolluntersuchungen
Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Dr. med. Christian Taverna Kantonsspital Münsterlingen Kontrolluntersuchungen
22. Onkologisches Symposium Große Fortschritte in der Leukämietherapie
 22. Onkologisches Symposium - 21.01.2017 Große Fortschritte in der Leukämietherapie Prof. Dr. Wolfgang Herr Klinik und Poliklinik für Innere Medizin III - Hämatologie und intern. Onkologie Leukämien (Patienten
22. Onkologisches Symposium - 21.01.2017 Große Fortschritte in der Leukämietherapie Prof. Dr. Wolfgang Herr Klinik und Poliklinik für Innere Medizin III - Hämatologie und intern. Onkologie Leukämien (Patienten
- eine Studie der GCIG - Deutsches Kurzprotokoll AGO Studiengruppe Ovarialkarzinom (AGO-OVAR) Phase III Protokoll AGO-OVAR 11
 Eine multizentrische randomisierte, zweiarmige Phase-III Studie zum Vergleich von Carboplatin/Paclitaxel und Bevacizumab versus Carboplatin/Paclitaxel in der Primärtherapie von Patientinnen mit epithelialem
Eine multizentrische randomisierte, zweiarmige Phase-III Studie zum Vergleich von Carboplatin/Paclitaxel und Bevacizumab versus Carboplatin/Paclitaxel in der Primärtherapie von Patientinnen mit epithelialem
Zweigbibliothek Medizin
 Sächsische Landesbibliothek - Staats- und Universitätsbibliothek Dresden (SLUB) Zweigbibliothek Medizin Diese Hochschulschrift finden Sie original in Printform zur Ausleihe in der Zweigbibliothek Medizin
Sächsische Landesbibliothek - Staats- und Universitätsbibliothek Dresden (SLUB) Zweigbibliothek Medizin Diese Hochschulschrift finden Sie original in Printform zur Ausleihe in der Zweigbibliothek Medizin
Endokrine Therapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Diagnostik und Therapie primärer und metastasierter Mammakarzinome AGO e. V. Version 2012.1D Endokrine Therapie des metastasierten Mammakarzinoms Endokrine Therapie des metastasierten Mammakarzinoms Version
Intraoperative Strahlentherapie bei Brustkrebs Patienteninformation zur intraoperativen Radiotherapie (IORT-Boost)
 Intraoperative Strahlentherapie bei Brustkrebs Patienteninformation zur intraoperativen Radiotherapie (IORT-Boost) Behandlung mit konventioneller Strahlentherapie Kein Grund für Verzweiflung Wenn die Diagnose
Intraoperative Strahlentherapie bei Brustkrebs Patienteninformation zur intraoperativen Radiotherapie (IORT-Boost) Behandlung mit konventioneller Strahlentherapie Kein Grund für Verzweiflung Wenn die Diagnose
Übersicht klinischer Studien im Onkologischen Zentrum Stand Juni 2014
 Übersicht klinischer Studien im Onkologischen Zentrum Stand Juni 2014 Studienzentrale Klinikum Aschaffenburg Studienbüro MKII: Fr. C. Klassert Telefon: 06021 / 32-2322 Fax: 06021 / 32-3020 christine.klassert@klinikum-aschaffenburg.de
Übersicht klinischer Studien im Onkologischen Zentrum Stand Juni 2014 Studienzentrale Klinikum Aschaffenburg Studienbüro MKII: Fr. C. Klassert Telefon: 06021 / 32-2322 Fax: 06021 / 32-3020 christine.klassert@klinikum-aschaffenburg.de
KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse
 Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Chronisch myeloproliferative Syndrome - CML-V TIGER
 Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
Perspektiven mit Tarceva und Avastin
 Fortgeschrittenes NSCLC: Perspektiven mit Tarceva und Avastin Mannheim (20. März 2009) - Die Behandlung des fortgeschrittenen nicht-kleinzelligen Lungenkarzinoms (Non Small Cell Lung Cancer, NSCLC) mit
Fortgeschrittenes NSCLC: Perspektiven mit Tarceva und Avastin Mannheim (20. März 2009) - Die Behandlung des fortgeschrittenen nicht-kleinzelligen Lungenkarzinoms (Non Small Cell Lung Cancer, NSCLC) mit
Projekte: Gutartige, boesartige und unspezifische Neubildungen (einschl. Zysten und Polypen)
 Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung eines VEGF-Rezeptor Hemmers Andere Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung Erstellung eines Dossiers für eine Nutzenbewertung
Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung eines VEGF-Rezeptor Hemmers Andere Erstellung einer Stellungnahme für den G-BA zur Nutzenbewertung Erstellung eines Dossiers für eine Nutzenbewertung
