CHE 102.1: Grundlagen der Chemie - Organische Chemie
|
|
|
- Rudolph Beltz
- vor 7 Jahren
- Abrufe
Transkript
1 C 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr.. Landau und Prof. Dr. J. A. Robinson 5. Aromatische Kohlenwasserstoffe Aufgrund des starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten. Aromatische Ringe kommen in vielen biologisch wirksamen Substanzen vor, z.b.: Cl arnsäure Benzen Benzol (Benzene) estron Diazepam (Valium) icotin Wir werden hier nur Benzol-Derivate betrachten, und nicht aromatische Ringe, die ein eteroatom enthalten (Kapitel-6), z.b., oder S. 5.1 Die Benennung von Benzolderivaten Der allgemeine Ausdruck für substituierte Benzolderivate lautet Arene. in Aren als Substituent heisst Arylgruppe, abgekürzt Ar-. Die einfachste Arylgruppe heisst Phenyl-, C 6 5 -, abgekürzt Ph-. inige Trivialnamen die häufig vorkommen:
2 2 C C Toluol (Sdp 110 o C) Anilin (Sdp 184 o C) Benzaldehyd (Sdp 178 o C) Anisol (Sdp 154 o C) Benzonitril (Sdp 188 o C) C Phenol (Smp 43 o C) Acetophenon (Smp 21 o C) Benzoesäure (Smp 122 o C) ortho-xylol (Sdp 144 o C) Styrol (Sdp 145 o C) Viele monosubstituierte Benzolderivate benennt man, indem man den Substituentennamen dem Wort "Benzol" voranstellt : 1-om-2,3-dimethylbenzol para-itrophenol meta-chlortoluol Bei disubstituierten Benzolderivaten können die Substituenten drei mögliche Stellungen zueinander einnehmen: benachbarte Substituenten 1,2- (ortho), für 1,3-disubstituierte Verbindungen 1,3- (meta), für 1,4-disubstituierte Verbindungen 1,4- (para). Die Substituenten werden in alphabetischer Reihenfolge genannt. 5.2 Die Struktur von Benzol : Aromatizität Im Jahr 1825 erhielt der englische Wissenschaftler Faraday eine farblose Flüssigkeit mit der empirischen Formel C. Diese Verbindung war mit der Theorie, nach der jeder Kohlenstoff vier Valenzen zu anderen Atomen ausbilden musste, nicht so einfach in inklang zu bringen. Besonders die ungewöhnliche Stabilität und chemische Trägheit dieser Substanz fiel auf. Man nannte die Verbindung Benzol und stellte schliesslich die Summenformel C 6 6 dafür auf. in Problem damals war, zu verstehen, warum nie zwei unterschiedliche Isomere von einem 1,2- disubstituierten Benzolderivat beobachtet werden konnten. Als Lösung schlug Kekulé im Jahre 1865 vor, dass Benzol aus sich rasch ineinander umwandelnden Isomeren von Cyclohexatrien bestehen
3 sollte. eute wissen wir, dasss diese ypothese nicht richtig ist. ach der modernen lektronentheorie kann man Benzol durch zwei äquivalente Resonanzstrukturen des Cyclohexatriens beschreiben: Benzol ist ungewöhnlich reaktionsträge. s geht keine Additionsreaktionen wie normale Alkene ein. Molekülorbital-Modell des Benzols Das Benzolmolekül bildet ein regelmässiges Sechseck aus sechs sp 2 -hybridisierten Kohlenstoffatomen. Die Abbildung unten zeigt die elektronische Struktur des Benzolrings. Alle Kohlenstoffatome sind sp 2 - hybridisiert, und jedes p-rbital steht senkrecht zur s-skellet und überlappt gleichmässig mit seinen beiden achbarn. Die sechs cyclisch angeordneten, überlappenden p-rbitale werden umhybridisiert zu einen Satz von sechs neue Molekülorbitalen (M), wobei drei als bindende Ms gelten und mit 6- lektronen besetzt sind, und drei anti-bindende Ms sind, und unbesetzt bleiben. Das π-bindende M mit der tiefsten nergie entspricht einer delokalisierten π-lektronen-wolke oberhalb und unterhalb der Ringebene.
4 Die Länge der aromatischen CC-Bindung liegt zwischen der einer infach- und der einer Doppelbindung. Valenz-Struktur-Beschreibung des Benzols Die Struktur von Benzol kann durch zwei gleichwertige Resonanzstrukturen von Cyclohexatrien wiedergegeben werden: Der wirkliche Zustand wird dann als "Zwischenzustand " oder "Resonanz-hybrid" zwischen diesen Grenzstrukturen wiedergegeben. Das Zeichen bedeutet, dass nicht etwa ein dynamisches Gleichgewicht zwischen zwei verschiedenen Molekülarten existiert, sondern dass der tatsächliche Zustand zwischen den Grenzstrukturen liegt und von diesen gewissermassen "umschrieben wird". Die Beschreibung einer wirklichen Struktur durch Kombination von nicht existierender Grenzstrukturen nennt man Resonanz. 5.3 Stabilität von Benzol Um ein Mass für die relative Stabilität einer Reihe von Alkenen zu bekommen, kann man ihre ydrierungswärmen bestimmen. in ähnliches xperiment können wir mit Benzol durchführen, und seine ydrierungswärme mit der von l,3 Cyclohexadien und Cyclohexen vergleichen :
5 bwohl Benzol nur schwer hydriert wird, kann die Reaktion katalytisch durchgeführt werden, und man erhält für die ydrierungswärme einen Wert von o -206 kj/mol. Der Unterschied zwischen den ydrierungswärmen (und den Bildungsenthalpien ) beträgt ungefähr 124 kj/mol und wird als Resonanzenergie von Benzol bezeichnet. Andere amen dafür sind Delokalisierungsenergie, aromatische Stabilisierug, oder einfach Aromatizität von Benzol. 5.4 Die ückel-regel Mit ilfe der M-Theorie lässt sich zeigen, dass ein monocyclisches konjugiertes Polyen (d.h. alle C-Atome sp 2 hybridisert) besonders stabil ist (d.h. Aromatizität besitzt), wenn es 4n+2 π-lektronen enthält (n ist ganzzahlig; d.h. ein p-system mit 2, oder 6, oder 10, oder... p-lektronen), z.b.: Aromatisch (4n + 2 π-lektronen) Benzol aphthalin Anthracen icht-aromatisch (4n π-lektronen) Phenanthren [14]-Annulen cyclobutadien cyclooctatetraen [16]-Annulen 5.5 lektrophile aromatische Substitution Aufgrund seiner π-lektronen besitzt das Benzol-Molekül nucleophile igenschaften und reagiert deshalb vorwiegend mit lektrophilen, z.b.:
6 2 itrierung Friedel-Crafts Acylierung S 3 Cl() Sulfonierung alogenierung Friedel-Crafts Alkylierung Im Gegensatz zu den Alkenen führt ein solcher Angriff zu einer Substitution eines -Atoms, nicht zu einer Addition. Z.B. ominierung in Gegenwart eines Katalysators: chanismus der elektrophilen aromatischen Substitution: Die π-lektronen aus dem Benzolring greifen + an
7 in Carbokation Zwischenprodukt wird gebildet Das Carbokation spaltet ein Proton ab Der erste Schritt ist thermodynamisch ungünstig, da die cyclische Delokalisierung und damit der aromatische Charakter dabei verloren geht. ach diesem Schritt wird der aromatische Ring wieder regeneriert, indem das Proton von dem sp 3 -hybridisierten Kohlenstoff abgespalten wird. Dies ist energetisch günstiger als eine Reaktion mit einem ukleophil, wodurch das Additionsprodukt entstünde : nergie + Reaktionskoordinat Die Änderung der potentiellen nergie während der Reaktion von Benzol mit einem lektrophil. Die Bildung des ersten Übergangszustand ist geschwindigkeitsbestimmend. Das Proton wird verhältnismässig rasch abgespalten.
8 Die Reaktion von Benzol mit k. 3 bei mässig erhöhter Temperatur führt zur itrierung des Benzolrings: 2 Konz. 2 S 4 reagiert bei RT nicht mit Benzol, sieht man von der Protonierung ab. "Rauchende Schwefelsäure" (leum) greift jedoch elektrophil an, da sie S 3 enthält. Aufgrund der stark elektronenziehenden Wirkung der drei Sauerstoffatome ist das S-Atom in S 3 so elektrophil, dass es Benzol direkt angreift : S 3 In Friedel-Crafts-Reaktionen entstehen neue C-C Bindungen. In Gegenwart einer Lewis Säure, gewöhnlich Aluminiumchlorid, greifen alogenalkane Benzol unter Bildung von Alkylbenzolderivaten an (Friedel-Crafts Alkylierung), Alkanoylhalogenide ergeben Alkanoylderivate (Friedel-Crafts Acylierung): + Cl C 3 C C 3 C 3 C C 3 C 3 C C 3 Die Reaktivität des alogenalkans nimmt in der Reihenfolge RF > RCl > R > RI ab. Typische Lewis- Säuren sind bei dieser Reaktion (nach abnehmender Reaktivität geordnet) Al 3, AlCl 3, FeCl 3, SbCl 5 und BF 3. Weitere Beispiele:
9 C 3 C 2 Cl AlCl 3, 25 o 3 C Cl AlCl 3, 0 o Cl AlCl 3, CS 2, 25 o Durch Friedel-Crafts-Acylierung entstehen Aryl-Alkyl-Ketone. Z.B. Benzol reagiert mit Acetylchlorid in Gegenwart von AlCl 3 und bildet Acetophenon : Die Bildung des Acylium-Kations geschieht allgemein durch die Reaktion von Alkanoylhalogeniden (Acylhaliden) mit AlCl 3. Ähnlich reagieren Carbonsäureanhydride mit Lewis-Säuren, z.b.: Allgemein R-C-Cl AlCl 3 R
10 5.6 Induktive- und Resonanz-ffekte im Benzolring in Substituent am Benzolring übt einen elektronischen ffekt aus, indem er entweder lektronendichte auf den Ring überträgt, oder lektronendichte abzieht. Auf diese Weise kann ein monosubstituierter Benzolring, verglichen mit Benzol, andere chemische und physikalische igenschaften aufweisen, z.b. kann eine elektrophile aromatische Substitutionsreaktion viel langsamer (d.h. wird desaktiviert) oder schneller (d.h. wird aktiviert) ablaufen als mit Benzol. Das Abziehen oder Liefern von lektronen kann durch Induktive- und durch Resonanz-ffekte zustandekommen. Induktive- und Resonanz-ffekte beeinflüssen viele chemische und physikalische igenschaften von Aromaten, nicht nur ihre Reaktivität bei elektrophilen Substitutionsreaktionen. Induktive- und Resonanz-ffekte Betrachten wir Beispiele von elektronenliefernden und elektronenziehenden Substituenten: = s-donator Relativ elektronenreicher Ring (reaktiver) CF 3 = s-akzeptor Relativ elektronenarmer Ring (weniger reaktiv) Induktive ffekte sind Polarisationseffekte, die über s-bindungen übertragen werden (siehe S.10). s ist auch möglich, dass ein Substituent an einen aromatischen Ring mit p-lektronen zu den p- lektronen des Ringes in Konjugation tritt und dadurch entweder negative Ladung aus dem ungesättigten System abzieht oder negative Ladung in dieses hineindrückt. äufig spricht man von
11 einem mesomeren ffekt oder Resonanzeffekt, was daherrührt, dass man in diesen Fällen die Ladungsdichteverteilung durch Kombination verschiedener Grenzstrukturen beschreiben kann, da eine Delokalisation der p-lektronen eintritt, z.b. ein π-akzeptor Ihre Akzeptorwirkung (die Stärke des mesomeren ffektes) steigt mit der Bereitschaft des Substituenten, negative Ladung aufzunehmen. R R R R Andere π-akzeptorgruppen: In der folgenden Reihe nimmt er darum nach rechts zu: R C R π-donorgruppen
12 Da elektronegativer ist als C, übt die - 2 Gruppe einen leicht elektronenziehenden ffekt aus (induktiver ffekt). Das freie lektronenpaar des -Atoms kann jedoch in das aromatische π-system miteingebracht werden, sodass die Ladungsdichte des Ringes erhöht wird: Dieser Resonanzeffekt überwiegt den induktiven ffekt bei weitem. Anilin ist deshalb für eine weitere Substitution reaktiver als Benzol. Das elektronegative -Atom in Phenol wirkt ebenfalls elektronenziehend (induktiver ffekt). Aber auch hier überwiegt der influss der Resonanz (p-donoreffekt), sodass der Benzolkern elektronenreicher wird: π-donorgruppen: 5.7 rientierung und relative Geschwindigkeit einer Zweitsubstitution Übt ein bereits vorhandener Substituent einen influss darauf aus, an welcher Stelle im Ring ein lektrophil angreift, und wie schnell die Reaktion abläuft (im Vergleich zu Benzol)? Schauen wir zuerst Toluol an, das die induktiv aktivierende thylgruppe trägt:
13 + + Die elektrophile itrierung von Toluol führt hauptsächlich zu ortho und para-substitution. Die itrierung ist kein Spezialfall: o-itrotoluol m-itrotoluol p-itrotoluol 2 Fe 3 o-omtoluol m-omtoluol p-omtoluol Trifluormethylbenzol ist gegenüber dem elektrophilen Angriff desaktiviert und reagiert deshalb nur zögernd. Unter energischen Bedingungen aber erhält man Substitution, jedoch nur in meta-stellung: + 40% <1% 60% + CF 3 CF 3 Für einen elektrophilen Angriff auf einen resonanz-aktivierten Benzolring ist oft nicht einmal ein Katalysator notwendig. Die Reaktion verläuft rasch und vollständig regioselektiv zu den (oft mehrfach) substituierten ortho- und para-produkten:
14 2 S 4 / 3 Ac Ac Ac % spüren 79% 2 o-itroacetanilid m-itroacetanilid 2 p-itroacetanilid 2 S 4 / % 2% 58% Anisol 2 o-itroanisol m-itroanisol p-itroanisol Anisol reagiert ungefähr 1000x schneller als Benzol! Wenden wir uns nun Benzolderivaten zu, die durch Resonanz desaktivierende Gruppen tragen. ierher gehört die Benzoesäure, bei der die itrierung 1000x langsamer verläuft als bei Benzol: C C C C 2 S 4 / % 80% 2 2% 2 o-itrobenzoesäure m-itrobenzoesäure p-itrobenzoesäure Die itrierung führt überwiegend zum meta-produkt. Die alogene (-F, -Cl, -, -I) als Substituenten bilden eine dritte Gruppe, die den Ring desaktivieren (Chlorbenzol reagiert 15-fach langsamer als Benzol), jedoch hauptsächlich ortho- und parasubstituierte Produkte bilden : Cl Cl Cl Cl 3 / 2 S % 2% 68% Dirigierende Wirkung von Substituenten bei der elektrophilen aromatischen Substitution: rtho- und para-dirigierend rtho- und para-dirigierend ta-dirigierend
15 aktivierend desaktivierend desaktivierend (s und p-donorgruppen) (s und p-akzeptorgruppen) - 2, -R, -R 2 -Cl, -, -I - 2 -CF 3 --CR -R 3 + -C -, -R -CR -C-R -R (Alkyl, Aryl) -S 3 -C 5.8 chanistische rklärung Können wir chanismen aufstellen, die diese Selektivitäten erklären können? Dazu wollen wir die möglichen Resonanzstrukturen des Kations zeichnen, das nach dem Angriff des lektrophils ( + ) entsteht. Dabei stellen wir fest, das s und p-donorsubstituenten, die ortho- oder para- stehen, das Zwischenprodukt (und den dazu führenden Übergangszustand) stabilisieren: Besonders stabile Resonanzstruktur Besonders stabile Resonanzstruktur
16 ur durch den Angriff in ortho- und para-stellung entsteht ein Kation mit einer Resonanzstruktur, die eine positiven Ladung neben der Alkylgruppe trägt. Da diese Struktur etwas vom Charakter eines 3 o - Carbenium-Ions hat, kommt ihr mehr Bedeutung zu (d.h. ist stabiler) als anderen, die die positive Ladung an einem 2 o C-Atom tragen. Durch einen meta-angriff entsteht dagegen eine Zwischenstufe, in der keine der möglichen Resonanzstrukturen von der Stabilität eines 3 o -Carbenium-Ions profitiert. Der elektrophile Angriff auf ein C-Atom ortho- oder para- zu einer thyl(alkyl)-gruppe führt deshalb zu einer Zwischenstufe, die stabiler ist als die, welche durch einen meta-angriff entstehen würde. Sie entsteht daher relativ schnell über einen Übergangszustand mit relativ niedriger nergie. Auch beim elektrophilen Angriff auf einen Resonanz-aktivierten Benzol-Ring kann man die beobachtete Regioselektivitäten durch Resonanzstrukturen der verschiedenen intermediären Kationen erklären. z.b.: Besonders stabile Resonanzstruktur Besonders stabile Resonanzstruktur rtho- und para-substitutionen sind bevorzugt, da sie über Zwischenprodukte verlaufen, für die man vier Resonanzstrukturen aufstellen kann, während bei der Zwischenstufe eines meta-angriffs nur drei zu formulieren sind. Wenn wir nun Benzolderivate betrachten, die Resonanz desaktivierende Gruppen tragen:
17 δ- Cδ+ Besonders instabile Resonanzstruktur C C C C C C Besonders instabile C C Resonanzstruktur C Der Angriff auf die meta-position vermeidet hier, dass eine positive Ladung neben der elektronenziehenden Carboxygruppe entsteht. Bei ortho- und para- Angriff hingegen ist dies nicht der Fall, d.h. hier müssen recht energiereiche Resonanzstrukturen formuliert werden. Bei anderen desaktivierenden Substituenten ist die Situation analog. alogenatome wie Cl und sind räumlich viel grösser als - und -Atome. bwohl ein p-donor- ffekt von -Cl noch vorhanden ist, ist der Resonanz-ffekt nicht so wirksam (wie bei - und - Atomen), weil das p-rbital am -Cl schlechter mit den benachbarten p-rbitale des Benzolringes überlappt. -, -, und Cl-Atome sind alle elektronegativ (s-akzeptorwirkung), aber mit - und - Atomen ist der Resonanz-ffekt (p-donor) viel stärker. Das heisst, Chlorbenzol ist weniger reaktiv, bezorzugt aber immer noch Substitutionsreaktionen in ortho- und para-positionen. Z.B. Cl Cl Cl Cl Cl in Resonanzeffekt führt nochmals bevorzugt zu ortho- und para-produkte. 5.9 lektrophiler Angriff auf disubstituierte Benzole Die Wirkungen zweier Substituenten auf die relative Geschwindigkeit und auf die rientierung der elektrophilen Substitution des Benzolrings addieren sich. Z.B.:
18 thyl dirigiert hier itro dirigiert hier 2 2 Wenn zwei in entgegengesetzte Richtung lenkende Gruppen vorhanden sind, sie üben ihren influss gewöhnlich unabhängig voneinander aus. Konkurrieren die Substituenten miteinander um den rt der Substitution, setzt sich die stärker aktivierende (oder desaktivierende) Gruppe durch. Resonanz- ffekte sind normalerweise stärker als Induktive-ffekte. Z.B.: thyl dirigiert hier dirigiert hier Wenn räumlich ausgedehnte Gruppen vorhanden sind, ist eine Stellung zwischen diesen Substituenten oft aus sterischen Gründen ungünstig: Z.B. Sterisch gehindert Cl Cl In den meisten anderen Fällen ergeben sich Produktgemische Synthetische Aspekte Benzol fällt bei verschiedenen technischen Prozessen an, z.b. in der aromatischen Fraktion von Rohöl- Destillat. Jährlich werden weltweit etwa 35 Millionen Tonnen Benzol hergestellt. Von 1940 bis
19 ungefähr 1960 wurde das meiste Benzol auf der Basis der Steinkohle hergestellt. Seit 1950 wird es auch aus rdöl gecrackt. Synthese Planung Bei der Synthese eines spezifischen Benzolderivats hängt alles davon ab, ob der erste eingeführte Substituent weitere Substituenten in die richtige Position dirigiert: Chlorbenzol Cl 2 2 Cl itrobenzol Aromatische-Carbonsäuren s gibt bestimmte Reaktionen, welche die dirigierende Wirkung eines Substituenten umkehren können. z.b. der Benzolring ist wegen seiner Resonanzenergie oxidationsbeständig. Aber eine Alkyl Seitenkette kann zu einer Carbonsäure oxidiert werden: z.b. für die Synthese von para-ombenzoesäure : C p-ombenzoesäure
20 Aromatische-Amine ine meta-dirigierende itrogruppe kann in die ortho- und para-dirigierende Aminogruppe umgewandelt werden. itrogruppen können zu Aminogruppen reduziert werden: Für eine Synthese von p-aminobenzoesäure (ein Bestandteil des Vitamins Tetrahydrofolsäure) : C C Toluol Aufpassen: Friedel-Crafts Reaktionen an itrobenzol sind nicht möglich: - 2 wirkt zu stark desaktivierend! 5.11 hrkernige benzoide Kohlenwasserstoffe Durch Kondensation oder Annelierung mehrerer Benzolringe ergibt sich eine Verbindungsklasse, die man als mehrkernige benzoide Kohlenwasserstoffe bezeichnet. z.b.
21 aphthalin Anthracen Tetracen (aphthacen) Phenanthren Triphenylen Pyren Benzo[a]pyren An diesen Ringen kann man, wie zu erwarten ist, elektrophile Substitutionen durchführen, die nach demselben chanismus wie die entsprechenden Reaktionen an Benzol und seinen Derivaten verlaufen. Der neue auptschwerpunkt liegt auf der Regioselektivität solcher Prozesse, die wir aber hier nicht betrachten werden. Viele der mehrkernigen benzoiden Kohlenwasserstoffe sind karzinogen (krebserregend). in besonders gut erforschtes Molekül ist Benz[a]pyren. Benz[a]pyren entsteht bei der Verbrennung organischer Materie, wie Automobiltreibstoff und rdöl, bei der Müllverbrennung, bei Waldbränden, man findet es in Zigaretten und im Zigarrenrauch und sogar in gegrilltem Fleisch. Wodurch kommt nun die karzinogene Wirkung von Benz[a]pyren zustande? Man nimmt an, dass ein oxidierendes nzym (eine xidase) aus der Leber den Kohlenwasserstoff in das C7/C8 -poxid überführt. in anderes nzym (poxid-ydratase) katalysiert die ydratisierung des Produkts zum trans-diol (vgl. Abschnitt 4.5). Durch weitere xidation entsteht dann das eigentliche Karzinogen, ein neues C9/C10 -poxid: Benzo[a]pyren Karzinogen Vermutlich erfolgt das krebsauslösende reignis dann, wenn der Aminstickstoff des Guanins, einer der Basen im DA-Strang, das poxid ukleophil angreift:
22 2 DA DA Bei dieser Reaktion wird die Struktur eines Basenpaare der DA geändert, was zu Fehlern und Störungen bei der DA-Replikation führt. Diese Fehler können zu einer Veränderung (Mutation) des genetischen Information führen, wodurch dann unter Umstände das Wachstum einer Linie von rasch und undifferenziert wuchernden Zellen ausgelöst wird, was typisch für Krebs ist. Benzo[a]pyren+DA Graphene Graphen ist die Bezeichnung für eine Modifikation des Kohlenstoffs mit zweidimensionaler Struktur, in der jedes Kohlenstoffatom von drei weiteren umgeben ist, so dass sich ein bienenwabenförmiges Muster ausbildet (Vgl. ben). Graphen hat ungewöhnliche igenschaften, die es sowohl für die Grundlagenforschung als auch für Anwendungen interessant machen, und zwar vor allem in der Physik (wie auch der obelpreis zeigt, der 2010 vergeben wurde). Beispielsweise sind Graphen- Flächeneinkristalle innerhalb der Flächen außerordentlich steif und fest. Wegen der hohen elektrischen Leitfähigkeit von Graphen wird derzeit an der Frage geforscht, ob Graphen Silicium als Transistormaterial ablösen könnte.
23 Als Fullerene (inzahl: das Fulleren; engl. Buckminsterfullerene or Bucky-balls) werden hohle, geschlossene Moleküle (mit häufig hoher Symmetrie, z. B. Ih-Symmetrie für C 60 ) aus Kohlenstoffatomen, die sich in Fünf- und Sechsecken anordnen, bezeichnet. Sie stellen (neben Diamant, Graphit, Lonsdaleit, Chaoit, Kohlenstoffnanoröhren und Graphen) eine weitere Modifikation des chemischen lements Kohlenstoff dar.
Wir werden hier nur Benzol-Derivate betrachten, und nicht aromatische Ringe, die ein Heteroatom enthalten (Kapitel-6), z.b. N, O oder S.
 5. Aromatische Kohlenwasserstoffe 36 Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten. Aromatische
5. Aromatische Kohlenwasserstoffe 36 Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten. Aromatische
5. Aromatische Kohlenwasserstoffe
 Inhalt Index 5. Aromatische Kohlenwasserstoffe Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten.
Inhalt Index 5. Aromatische Kohlenwasserstoffe Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten.
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Inhaltsverzeichnis zu Kapitel 6. Aromaten
 Inhaltsverzeichnis zu Kapitel 6. Aromaten 6. Aromaten 6.1 Aromatizität 73 6.2 omenklatur 75 6.3 Darstellung 76 6.4 lektrophile Substitution am Aromaten 76 6.5 Beispiele für S -Reaktionen (was ist?) 77
Inhaltsverzeichnis zu Kapitel 6. Aromaten 6. Aromaten 6.1 Aromatizität 73 6.2 omenklatur 75 6.3 Darstellung 76 6.4 lektrophile Substitution am Aromaten 76 6.5 Beispiele für S -Reaktionen (was ist?) 77
1. a) Geben sie den Reaktionsmechanismus für die Nitrierung und die Sulfonierung von Benzol an. Beginnen sie mit der Erzeugung des Elektrophils.
 Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
3. Aromatische Verbindungen Benzol(en)
 3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
Arene (Benzolderivate)
 Arene (Benzolderivate) Im Verlauf der Vorlesung haben wir bereits einige kennengelernt: DDT, DIXI, Cumol... hier nun weitere wichtige Vertreter: Acetylsalicylsäure (Aspirin) Synthese über die Kolbe-Schmitt-Synthese
Arene (Benzolderivate) Im Verlauf der Vorlesung haben wir bereits einige kennengelernt: DDT, DIXI, Cumol... hier nun weitere wichtige Vertreter: Acetylsalicylsäure (Aspirin) Synthese über die Kolbe-Schmitt-Synthese
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2016
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Aromatische Substitution. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
Aromatische Kohlenwasserstoffe
 Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. Brückner
 Reaktionsmechanismen nach dem gleichnahmigen Buch von R. ückner Kap. 5 Substitutionsreaktionen am Aromaten Dr. ermann A. Wegner hermann.wegner@unibas.ch lektrophile aromatische Substitution Wheland-Komplex
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. ückner Kap. 5 Substitutionsreaktionen am Aromaten Dr. ermann A. Wegner hermann.wegner@unibas.ch lektrophile aromatische Substitution Wheland-Komplex
Bundesrealgymnasium Imst. Chemie Klasse 8. Aromaten und deren Reaktionen
 Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
N N. Chinolin. Pyridin. Imidazol
 6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
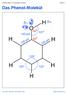 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
5 Chemie aromatischer Verbindungen
 5 hemie aromatischer Verbindungen Benzol wurde 1825 von Faraday entdeckt. bwohl das Verhältnis : = 1:1 stark ungesättigten harakter anzeigte, reagierte es weder mit Br 2 noch mit KMn 4 wie gewöhnliche
5 hemie aromatischer Verbindungen Benzol wurde 1825 von Faraday entdeckt. bwohl das Verhältnis : = 1:1 stark ungesättigten harakter anzeigte, reagierte es weder mit Br 2 noch mit KMn 4 wie gewöhnliche
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1
CE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1
Organische Chemie im Überblick
 Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Chemie für Biologen SS Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 11: Alkine / Polyene / Aromaten)
 hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
Beispiele. Polysubstituierte Benzole. Chapter 16. Organic Chemistry. Reaktionen of Substituierter Benzole. Bezeichnung durch Numerierung oder Präfix
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Beispiele Chapter 16 Reaktionen of Substituierter Benzole Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Bezeichnung durch
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Beispiele Chapter 16 Reaktionen of Substituierter Benzole Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Bezeichnung durch
Name, Vorname: Matrikelnummer: Studienrichtung: Fragen auf den folgenden Seiten: Musterlösung zur Klausur zur Experimentalvorlesung Organische Chemie
 rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhaltsverzeichnis. Teil I Volle Kraft voraus: Die Chemie des Kohlenstoffs 23. Einführung 17. Kapitel 1 Die wundervolle Welt der organischen Chemie 25
 Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
σ-bindung beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
 VIII. Alkine Die C/C-Dreifachbindung als funktionelle Gruppe erste π-bindung σ-bindung zweite π-bindung orthogonal zur ersten beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
VIII. Alkine Die C/C-Dreifachbindung als funktionelle Gruppe erste π-bindung σ-bindung zweite π-bindung orthogonal zur ersten beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
3. Gruppe: Aromatische Substitution
 1 1) Zum chanismus der elektrophilen aromatischen Substitution Aromatischer Charakter Antiaromatischer Charakter (4 n 2)π-lektronen 4 nπ e 3 C C 3 2 C C 2 1.48Å 1.54Å 1.34Å 1.39Å ingstrom-ffekte δ = 5
1 1) Zum chanismus der elektrophilen aromatischen Substitution Aromatischer Charakter Antiaromatischer Charakter (4 n 2)π-lektronen 4 nπ e 3 C C 3 2 C C 2 1.48Å 1.54Å 1.34Å 1.39Å ingstrom-ffekte δ = 5
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
Organische Experimentalchemie
 PD Dr. Alexander eder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 rganische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und Biologie
PD Dr. Alexander eder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 rganische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und Biologie
Aromatische Verbindungen (Vollhardt, 3. Aufl., S. 671 ff, 4. Aufl., S. 749 ff; Hart, S. 137ff; Buddrus, S. 333 ff)
 Vorlesung 27 Aromatische Verbindungen (Vollhardt, 3. Aufl., S. 671 ff, 4. Aufl., S. 749 ff; art, S. 137ff; Buddrus, S. 333 ff) ntdeckung von Benzol durch M. Faraday 1825 im Rückstand von Leuchtgas, das
Vorlesung 27 Aromatische Verbindungen (Vollhardt, 3. Aufl., S. 671 ff, 4. Aufl., S. 749 ff; art, S. 137ff; Buddrus, S. 333 ff) ntdeckung von Benzol durch M. Faraday 1825 im Rückstand von Leuchtgas, das
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - rganische hemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 4. Alkene: eaktionen und erstellung 4.1. Elektrophile Additionen an Alkene: egioselektivität Das Proton einer
E 102.1: Grundlagen der hemie - rganische hemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 4. Alkene: eaktionen und erstellung 4.1. Elektrophile Additionen an Alkene: egioselektivität Das Proton einer
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
3. Klausur zum Praktikum Organische Chemie I für Studierende der Chemie und der Biochemie im SS 2000
 Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und Nebenfächer (
 Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-OC-II Prof. R. Peters
 Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
Zusammenfassung 2. Teil
 Zusammenfassung 2. Teil Aromaten Wichtigste Vertreter: C 3 Vorkommen und Isolation: rdöl Verwendung: Lösungsmittel, Ausgangsmaterial für Synthesen Benzol (krebserregend) Toluol Bestandteil im Benzin, Benzolfreie
Zusammenfassung 2. Teil Aromaten Wichtigste Vertreter: C 3 Vorkommen und Isolation: rdöl Verwendung: Lösungsmittel, Ausgangsmaterial für Synthesen Benzol (krebserregend) Toluol Bestandteil im Benzin, Benzolfreie
Organische Chemie I Molekül der Woche - Azulen
 I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Gruppe 4 Pflichtversuch. Bromierung des Kerns von Toluol 40 % Menge R-Sätze S-Sätze Gefahrensymbole. 2 ml /
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 Pflichtversuch omierung des Kerns von Toluol
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 Pflichtversuch omierung des Kerns von Toluol
10. Die Carbonylgruppe : Aldehyde und Ketone - Nucleophile Addition
 Inhalt Index 10. Die Carbonylgruppe : Aldehyde und Ketone - Nucleophile Addition Die C=O Doppelbindung der Carbonylgruppe ist die wichtigste funktionelle Gruppe der organischen Chemie. Dieses Kapitel befasst
Inhalt Index 10. Die Carbonylgruppe : Aldehyde und Ketone - Nucleophile Addition Die C=O Doppelbindung der Carbonylgruppe ist die wichtigste funktionelle Gruppe der organischen Chemie. Dieses Kapitel befasst
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231
 Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
8 Carbonsäuren und Derivate
 8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
10. Die Carbonylgruppe : Aldehyde und Ketone - Nucleophile Addition
 Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 10. Die Carbonylgruppe : Aldehyde und Ketone - Nucleophile Addition Die C=O Doppelbindung der Carbonylgruppe ist die wichtigste funktionelle
Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 10. Die Carbonylgruppe : Aldehyde und Ketone - Nucleophile Addition Die C=O Doppelbindung der Carbonylgruppe ist die wichtigste funktionelle
Zweite Klausur zum Organisch-Chemischen Grundpraktikum
 Prof. Dr. Jens Christoffers 12. Juni 2006 Universität ldenburg Zweite Klausur zum rganisch-chemischen Grundpraktikum Vorname: Name: Matrikelnummer: Studiengang: Falls Sie zusätzliche Seiten verwenden,
Prof. Dr. Jens Christoffers 12. Juni 2006 Universität ldenburg Zweite Klausur zum rganisch-chemischen Grundpraktikum Vorname: Name: Matrikelnummer: Studiengang: Falls Sie zusätzliche Seiten verwenden,
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
OC 4 Aromaten / Heterocyclen. Aromatizität 1
 OC 4 Aromaten / Heterocyclen Aromatizität 1 Benzol Der Modellaromatt Historische Entwicklung 1825 1833 Entdeckung durch Michael Faraday (Pyrolyse) Mitscherlich: Erste Benzolsynthese Entdeckung der Summenformel
OC 4 Aromaten / Heterocyclen Aromatizität 1 Benzol Der Modellaromatt Historische Entwicklung 1825 1833 Entdeckung durch Michael Faraday (Pyrolyse) Mitscherlich: Erste Benzolsynthese Entdeckung der Summenformel
Br 1. Auch bei der folgenden Kombination, sind die Strukturen nicht identisch, sie lassen sich durch Drehung nicht ineinander überführen.
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Abschlussklausur zur Grundvorlesung Organische Chemie im SS 2007 Nachholtermin -
 Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Basisprüfung Allgemeine Chemie (Teil OC) Montag, 3. September 2007
 Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Die Strukturabhängigkeit der chemischen Verschiebung
 Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
1. Die folgenden Alkene liefern bei der elektrophilen Addition von Brom unterschiedliche kationische Zwischenstufen.
 Professor Lindhorst rganische Chemie 1: rganisch-chemische Reaktionsmechanismen chem303 WS 2008/09 ÜUNG 4 Addition an CC-hrfachbindungen - LÖSUNGEN - 1. Die folgenden Alkene liefern bei der elektrophilen
Professor Lindhorst rganische Chemie 1: rganisch-chemische Reaktionsmechanismen chem303 WS 2008/09 ÜUNG 4 Addition an CC-hrfachbindungen - LÖSUNGEN - 1. Die folgenden Alkene liefern bei der elektrophilen
Arzneistoff der Woche. Alkohole. Eliminierungen. Organische Chemie Agenda. Johann Wolfgang Goethe -Universität Frankfurt am Main
 Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
8 Zusammenfassung und Ausblick
 8 Zusammenfassung und Ausblick Im Rahmen der vorliegenden Dissertation wurden die LEWIS-aciden Eigenschaften diverser Übergangsmetallverbindungen in unterschiedlichen Reaktionen untersucht. Das Augenmerk
8 Zusammenfassung und Ausblick Im Rahmen der vorliegenden Dissertation wurden die LEWIS-aciden Eigenschaften diverser Übergangsmetallverbindungen in unterschiedlichen Reaktionen untersucht. Das Augenmerk
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
