Anlage zur Akkreditierungsurkunde D-PL nach DIN EN ISO/IEC 17025: und nach Richtlinien 93/42/EWG 2 und 90/385/EWG 3
|
|
|
- Herta Petra Meinhardt
- vor 6 Jahren
- Abrufe
Transkript
1 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL nach DIN EN ISO/IEC 17025: und nach Richtlinien 93/42/EWG 2 und 90/385/EWG 3 Gültigkeitsdauer: bis Ausstellungsdatum: Urkundeninhaber: HygCen Germany GmbH Bornhövedstraße 78, Schwerin Bereich: Medizinprodukte /-gegenstände: biologische, chemische, mikrobiologisch-hygienische und physikalische von Medizinprodukten einschließlich Desinfektionsmitteln und mikrobiologisch-hygienische einschließlich physikalischer von Reinigungs- und Desinfektionsgeräten (RDG) und Reinigungs- und Desinfektionsverfahren sowie Sterilisatoren und Sterilisationsverfahren; Umgebungsüberwachung verwendete Abkürzungen: siehe letzte Seite Seite 1 von 27
2 Biologische Medizinprodukte auf Zytotoxizität DIN EN ISO Zellvitalitätstest nach Kontakt mit Extrakten (Colorimetrische Messung der Vitalität (Neutralrot) SOP Test auf Membranintegrität nach Kontakt mit Extrakten (LDHe-Freisetzung) DIN EN ISO DIN EN ISO Gültigkeitsdauer: bis Ausstellungsdatum: Seite 2 von 27
3 Biologische Medizinprodukte auf Gentoxizität, Karzinogenität und Reproduktionstoxizität DIN EN ISO SOP in vitro-gentoxizitätsprüfungen - Bakterien-Rückmutationstest (Ames-Test) OECD-Guidelines 471 DIN EN ISO DIN EN ISO im Rahmen der Wechselwirkung mit Blut DIN EN ISO SOP Hämolysetest - Bestimmung der PTT - Thrombozytenzahl - Test auf Komplementaktivierung (TCC) DIN EN ISO DIN EN ISO im Rahmen der Beurteilung von Irritation und Allergien vom verzögerten Typ DIN EN ISO SOP In vivo-irritationsprüfung auf der menschlichen Haut (Primary Skin Irritationtest) DIN EN ISO DIN EN ISO Gültigkeitsdauer: bis Ausstellungsdatum: Seite 3 von 27
4 Biologische Medizinprodukte Quantitativer Nachweis pyrogener Verunreinigungen im humanen Vollblutmodell mittels ELISA SOP (DIN EN ) Chemische Medizinprodukte Nachweis bluthaltiger Restanschmutzungen SOP Wasser und wässrige Lösungen Bestimmung der Gesamthärte SOP Quantitative Bestimmung von freien NH2-Gruppen der Proteine durch die OPA Methode Bestimmung des Proteingehaltes von Flüssigkeiten mit dem BCA Protein Assay Kit SOP (DIN ISO/TS ) DIN EN ISO 3071 SOP SOP (DIN ISO/TS ) Chemische und physikalische Medizinische Einmalhandschuhe von Produkteigenschaften - Bestimmung der löslichen Proteine - Bestimmung des entfernbaren Oberflächenpuders DIN EN SOP DIN EN ISO ISO SOP Bestimmung des ph Wertes des wässrigen Extraktes von Fasermaterial Mikrobiologischhygienische Medizinprodukte auf Sterilität DIN EN ISO SOP Zählung der gesamten vermehrungsfähigen aeroben Keime Ph. Eur. 8, Gültigkeitsdauer: bis Ausstellungsdatum: Seite 4 von 27
5 Mikrobiologischhygienische Desinfektionsmittel der viruziden Wirksamkeit chemischer Desinfektionsverfahren in vitro DIN EN R-DVV/RKI SOP SOP SOP SOP Quantitativer Suspensionsversuch zur Bestimmung der bakteriziden, fungiziden oder levuroziden oder sporiziden Wirkung chemischer Desinfektionsmittel und Antiseptika (Basistest Phase 1) DIN EN 1040 DIN EN 1275 DIN EN SOP EN Quantitativer Suspensionsversuch zur Bestimmung der bakteriziden, fungiziden, mycobakteriziden oder sporiziden Wirkung chemischer Desinfektionsmittel im Bereich der Humanmedizin (Phase 2, Stufe1) DIN EN DIN EN DIN EN SOP EN Praxisnahe Versuche zur Bestimmung der bakteriziden, fungiziden, mycobakteriziden oder sporiziden Wirkung chemischer Desinfektionsmittel und Antiseptika im Bereich Instrumente für den humanmedizinischen Bereich (Phase 2, Stufe2) DIN EN DIN EN DIN EN DGHM 15 SOP EN der bakteriostatischen und fungistatischen Wirksamkeit chemischer Desinfektionsverfahren DGHM Standardmethode 7 SOP SOP der bakteriziden und fungiziden Wirksamkeit chemischer Desinfektionsverfahren im qualitativen Suspensionsversuch DGHM Standardmethode 8 SOP SOP Gültigkeitsdauer: bis Ausstellungsdatum: Seite 5 von 27
6 Mikrobiologischhygienische Desinfektionsmittel der bakteriziden und fungiziden Wirksamkeit chemischer Desinfektionsverfahren im quantitativen Suspensionsversuch DGHM Standardmethode 9 - mit Bakterien und Pilzen DGHM Standardmethode 9.1 SOP SOP mit Mykobakterien DGHM Standardmethode 9.2 SOP der bakteriziden und fungiziden Wirksamkeit im Flächenversuch unter praxisnahen Bedingungen DGHM Standardmethode 14 - nicht poröse Oberflächen DGHM Standardmethode 14.1 SOP auf rohem Holz DGHM Standardmethode 14.2 SOP der Wirksamkeit von Desinfektionsmitteln für die chemische Instrumentendesinfektion bei Tuberkulose BGBl 11/94 SOP der Wirksamkeit von Flächendesinfektionsmitteln für die Desinfektion bei Tuberkulose BGBl 04/94 SOP der Wirksamkeit von Desinfektionsmitteln bei der chemothermischen Wäschedesinfektion DGHM Standardmethode 16 Standardmethode 17 SOP Gültigkeitsdauer: bis Ausstellungsdatum: Seite 6 von 27
7 Mikrobiologischhygienische Desinfektionsmittel der bakteriziden und fungiziden Wirksamkeit von Kollagen-Antiseptica- Präparationen im quantitativen Suspensionsversuch SOP der fungiziden Wirksamkeit chemischer Desinfektionsverfahren im Flächendesinfektionsversuch mit Tupfer-Abschwemm-Methode ÖGHMP SOP Quantitative Bestimmung der Keimreduktion durch antibakterielle Wundauflagen SOP Quantifizierung der Reinigungsleistung Nachweis der Abreicherung von praxisrelevanten Prüfanschmutzungen in Abhängigkeit des Trägermaterials und den Reinigungsbedingungen SOP Desinfektionsmittel- Dosiergeräte von dezentralen Desinfektionsmittel- Dosiergeräten BgndhBl 1, 2004 SOP Endoskope (aufbereitet) Kontrolle der Aufbereitung - mikrobiologische von Endoskopspüllösungen Endoskope (aufbereitet) Kontrolle der Endoskop- Aufbereitung Hyg.Med 1995; 20 (1) SOP SOP KRINKO/BfArM- Empfehlung Aufbereitung MP MIC-Instrumente (aufbereitet) der maschinellen Reinigung und Desinfektion von Instrumenten für minimal invasive Chirurgie DGKH SOP Gültigkeitsdauer: bis Ausstellungsdatum: Seite 7 von 27
8 Mikrobiologischhygienische Sterilbarriere- und Verpackungs-systeme, Materialien im Rahmen des Nachweises der Übereinstimmung DIN EN ISO Mikrobielle Barriere ASTM F 1608 bei Feuchte bei Luftdurchgang SS SOP Antimikrobiell ausgerüstete Materialien der antimikrobiellen Wirkung JIS Z 2801 JIS L 1902 DIN EN ISO SOP Mikrobiologischhygienische, einschließlich physikalischer Reinigungs- und Desinfektions-verfahren Reinigungs- und Desinfektionsgeräte (RDG) - mit thermischer Desinfektion für chir. Instrumente, Anästhesiegeräte, Gefäße, Utensilien, Glasgeräte - mit thermischer oder chemo-thermischer Desinfektion für Behälter für menschliche Ausscheidungen - mit chemischer oder thermischer Desinfektion für thermolabile Endoskope Anschmutzung von Prüfkörpern DIN ISO/TS SOP Geräteprüfung DIN EN ISO (ohne IEC ) Typprüfung DIN EN ISO SOP SOP Typprüfung DIN EN ISO SOP SOP Typrüfung DIN EN ISO SOP SOP DIN ISO/TS RKI-Richtlinie thermischer Desinfektionsverfahren in Reinigungsautomaten Gültigkeitsdauer: bis Ausstellungsdatum: Seite 8 von 27
9 Mikrobiologischhygienische, einschließlich physikalischer Reinigungs- und Desinfektions-verfahren Validierung DIN EN ISO (ohne IEC ) - mit thermischer Desinfektion für chir. Instrumente, Anästhesiegeräte, Gefäße, Utensilien, Glasgeräte - mit thermischer oder chemo-thermischer Desinfektion für Behälter für menschliche Ausscheidungen - mit chemischer oder thermischer Desinfektion für thermolabile Endoskope Installationsqualifikation Betriebsqualifikation Leistungsqualifikation Installationsqualifikation Betriebsqualifikation Leistungsqualifikation Installationsqualifikation Betriebsqualifikation Leistungsqualifikation DIN EN ISO SOP SOP DIN EN ISO SOP SOP DIN EN ISO SOP SOP DIN ISO/TS RKI-Richtlinie thermischer Desinfektionsverfahren in Reinigungsautomaten Reinigungs- und Desinfektions-verfahren - mit thermischer Desinfektion für chir. Instrumente, Anästhesiegeräte, Gefäße, Utensilien, Glasgeräte - mit chemischer oder thermischer Desinfektion für thermolabile Endoskope im Rahmen der Validierung Leistungsqualifikation Leistungsqualifikation Leitlinie von DGKH, DGSV und AKI, thermostabile Instrumente SOP Leitlinie von DGKH, DGSV und AKI, thermolabile Endoskope SOP Gültigkeitsdauer: bis Ausstellungsdatum: Seite 9 von 27
10 Mikrobiologischhygienische einschließlich physikalischer Dampf-Sterilisatoren Typprüfung Werksprüfung Abnahmeprüfung DIN EN 285 (ohne EN ) SOP SOP Dampf-Klein- Sterilisatoren Typprüfung Werksprüfung Abnahmeprüfung DIN EN (ohne EN , EN , EN 61326) SOP Sterilisations- verfahren Validierung mit feuchter Hitze Installationsqualifikation DIN EN ISO Betriebsqualifikation SOP Leistungsqualifikation DIN EN DIN EN 285 mit Ethylenoxid Installationsqualifikation DIN EN ISO Betriebsqualifikation Leistungsqualifikation DIN EN 1422 (ohne EN , IEC ) SOP mit Niedertemperatur Dampf-Formaldehyd (NTDF) Installationsqualifikation Betriebsqualifikation Leistungsqualifikation DIN EN (ohne EN , EN , EN 61326) SOP mit Wasserstoffperoxid (H 2 O 2 ) Installationsqualifikation Betriebsqualifikation Leistungsqualifikation DIN EN ISO (ohne EN , EN , EN 61326) SOP Informationen für die Aufbereitung von Medizinprodukten im Rahmen der Validierung DIN EN ISO Reinigung SOP Desinfektion Trocknung Sterilisation - mit feuchter Hitze - mit Ethylenoxid Gültigkeitsdauer: bis Ausstellungsdatum: Seite 10 von 27
11 Mikrobiologischhygienische, physikalische und physikalisch mechanische Masken Atmungs-Eignungsprüfung, Differentialer Druck (Luft- Austauschdruck) DIN EN ASTM F SOP in Übereinstimmung mit MIL-M C der Filterwirksamkeit für Bakterien (BFE) DIN EN ASTM F EDANA WSP SOP der Flüssigkeitsresistenz DIN EN SOP textile und nicht textile Medizinprodukte auf Keimdurchtritt im feuchten Zustand (Wet-Penetration) auf bakterielle Penetration im trockenen Zustand (DRY Penetration) Widerstand gegen Durchdringung von unterschiedlichen Flüssigkeiten Widerstand gegen Durchdringung von Bakteriophagen Widerstand gegen das Durchdringen von Wasser Weiterreißkraft von textilen Flächengeweben der Flusenfreisetzung von Vliesstoff-Oberflächen DIN EN ISO SS SOP DIN EN DIN EN ISO EDANA SOP DIN EN ISO ASTM F 1670 SOP (DIN EN 20811) ISO ASTM F 1671 SOP (DIN EN 20811) DIN EN DIN EN SOP DIN EN ISO SOP EDANA SOP Gültigkeitsdauer: bis Ausstellungsdatum: Seite 11 von 27
12 Mikrobiologischhygienische, physikalische und physikalisch mechanische textile und nicht textile Medizinprodukte auf lose haftende Partikel: Flusenbildung bei Vliesstoffen DIN EN ISO EDANA SOP Wasseraufnahme-vermögen ISO SOP Bestimmung des Ablaufverhaltens (Run-Off) ISO EDANA SOP Linting feucht DIN EN INDA IST SOP DIN EN DIN EN ISO von Produkteigenschaften DIN EN ISO Streifen-Zugversuch SOP Zugeigenschaft von textilen Flächengeweben DIN EN ISO SOP Physikalische und physikalischmechanische Medizinische Einmalhandschuhe von Produkteigenschaften - auf Dichtheit (Wasserhalteprüfung) - physikalischer Eigenschaften Länge Breite Reißkraft DIN EN SOP DIN EN SOP DIN ISO Gültigkeitsdauer: bis Ausstellungsdatum: Seite 12 von 27
13 Mikrobiologischhygienische Umgebungsüberwachung in der Herstellung und der Sauberkeit der Produkte gemäß DIN EN ISO : 2012, Abs. 6.4 und Abs Medizinprodukte Bettgestelle, Nachttische, Matratzen (aufbereitet) Schätzung der Population von Mikroorganismen auf Produkten (Bioburdenbestimmung) Beurteilung der quantitativen und qualitativen Verteilung von Hausstaubmilben in einem Biotop mittels Wärmefluchtverfahren und Mobilitätstest auf Bakterien - Endotoxine (LAL Test) auf maschinelle Dekontamination von Bettgestellen, Nachttischen, Matratzen DIN EN ISO SOP SOP DIN EN ISO Ph. Eur. 6, USP 32 : 2009, <85> FDA- Guideline 1987 SOP AK BWA 1997 SOP Wasser und wässrige Lösungen Nachweis spezifizierter Mikroorganismen BGBl 04/96 DIN EN ISO 6222 DIN EN DIN EN DIN DIN Legionellen BGBI 04/93 - Clostridium perfringens (einschl. Sporen) DVGW, Arbeitsblatt SOP SOP Pseudomonas aeruginosa DIN EN ISO SOP intestinalen Enterokokken DIN EN ISO SOP Gültigkeitsdauer: bis Ausstellungsdatum: Seite 13 von 27
14 Mikrobiologischhygienische Umgebungsüberwachung in der Herstellung und der Sauberkeit der Produkte gemäß DIN EN ISO : 2012, Abs. 6.4 und Abs Wasser und wässrige Lösungen Raumlufttechnische Anlagen Sicherheitswerkbänke Umgebungssicherung Nachweis spezifizierter Mikroorganismen - Escherichia coli und coliformen Bakterien - Bestimmung der Gesamtkeimzahl Überprüfung raumlufttechnischer Anlagen Messung von Mikroorganismen und Endotoxin in der Luft (Arbeitsplatzatmosphäre) auf Einhaltung der Leistungskriterien von Sicherheitswerkbänken für mikrobiologische und biotechnologische Arbeiten Hygienische Umgebungsuntersuchungen von Abfalldesinfektionsanlagen auf Wirksamkeit der mikrobiellen Emission sowie Keimzahländerung im Kühlwasser der Zusammensetzung des Kühlturmschwadens BGBl 04/96 DIN EN ISO 6222 DIN EN DIN EN DIN DIN ISO SOP DIN EN ISO 6222 SOP TVO 2011 DIN SOP DIN EN SOP DIN EN SOP SOP EN SOP BGBI SOP VGB F 301 P SOP VGB F 301 P SOP Gültigkeitsdauer: bis Ausstellungsdatum: Seite 14 von 27
15 Mikrobiologischhygienische Umgebungsüberwachung in der Herstellung und der Sauberkeit der Produkte gemäß DIN EN ISO : 2012, Abs. 6.4 und Abs Wäsche (aufbereitet) der desinfizierenden Wirkung chemothermischer Wäschereiverfahren DGHM 4.2 R-RKI SOP e 5 DIN EN 285 : Sterilisaton; Dampf-Sterilisatoren; Groß-Sterilisatoren DIN EN : Medizinische Handschuhe zum einmaligen Gebrauch; Teil 1: Anforderungen und auf Dichtheit DIN EN : Medizinische Handschuhe zum einmaligen Gebrauch; Teil 2: Anforderungen und der physikalischen Eigenschaften DIN EN : Medizinische Handschuhe zum einmaligen Gebrauch; Teil 3: Anforderungen und für die biologische Bewertung DIN EN 1040 : DIN EN 1275 : DIN EN 1422 : DIN EN : DIN EN : DIN : DIN EN ISO : DIN EN ISO 3071 : DIN EN ISO 6222 : DIN EN ISO : DIN EN ISO : Chemische Desinfektionsmittel und Antiseptika; Bakterizide Wirkung (Basistest); und Anforderungen (Phase 1) Chemische Desinfektionsmittel und Antiseptika - Fungizide Wirkung (Basistest) - Prüfmethode und Anforderungen (Phase 1); Sterilisatoren für medizinische Zwecke; Ethylenoxid Sterilisatoren; Anforderungen und für medizinische Vliesstoffkompressen - Teil 1: Vliesstoffe zur Herstellung von Kompressen für medizinische Vliesstoffkompressen - Teil 2: Kompressen Raumlufttechnik; Raumlufttechnische Anlagen in Gebäuden und Räumen des Gesundheitswesens Annahmestichprobenprüfung anhand der Anzahl fehlerhafter Einheiten oder Fehler (Attributprüfung) - Teil 1: Nach der annehmbaren Qualitätsgrenzlage (AQL) geordnete Stichprobenpläne für die einer Serie von Losen Textilien - Bestimmung des ph des wässrigen Extraktes Wasserbeschaffenheit - Quantitative Bestimmung der kultivierbaren Mikroorganismen - Bestimmung der Koloniezahl durch Einimpfen in ein Nähragarmedium Wasserbeschaffenheit - Nachweis und Zählung von intestinalen Enterokokken - Teil 2: Verfahren durch Membranfiltration Textilien - für Vliesstoffe - Teil 6: Absorption Gültigkeitsdauer: bis Ausstellungsdatum: Seite 15 von 27
16 DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN ISO : Bildung von Flusen und anderen Teilchen im trockenem Zustand Textilien - für Vliesstoffe - Teil 11: Bestimmung des Ablaufverhaltens (ISO :2002); Wasserbeschaffenheit - Nachweis und Zählung von Escherichia coli und coliformen Bakterien - Teil 1: Membranfiltrationsverfahren Biologische Beurteilung von Medizinprodukten - Teil 1: Beurteilung und im Rahmen eines Risikomanagements Biologische Beurteilung von Medizinprodukten - Teil 3: auf Genotoxizität, Karzinogenität und Reproduktionstoxizität Biologische Beurteilung von Medizinprodukten - Teil 4: Auswahl von zur Wechselwirkung mit Blut DIN EN ISO : Biologische Beurteilung von Medizinprodukten; Teil 5: auf In Vitro-Zytotoxizität DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN ISO : Biologische Beurteilung von Medizinprodukten - Teil 10: auf Irritation und Hautsensibilisierung Biologische Beurteilung von Medizinprodukten - Teil 11: auf systemische Toxizität Sterilisation von Medizinprodukten; Validierung und Routineüberwachung für die Sterilisation mit Ethylenoxid Verpackungen für in der Endverpackung zu sterilisierende Medizinprodukte - Teil 1: Anforderungen an Materialien, Sterilbarrieresysteme und Verpackungssysteme DIN EN ISO : Sterilisation von Medizinprodukten - Mikrobiologische Verfahren - Teil 1: Bestimmung der Population von Mikroorganismen auf Produkten DIN EN ISO : Sterilisation von Medizinprodukten - Mikrobiologische Verfahren - Teil 2: Sterilitätsprüfungen bei der Validierung und Aufrechterhaltung eines Sterilisationsverfahrens DIN EN : DIN EN : DIN EN : DIN EN : DIN EN : Biotechnik - Leistungskriterien für mikrobiologische Sicherheitswerkbänke Dampf-Klein-Sterilisatoren Arbeitsplatzatmosphäre - Leitlinien für die Messung von Mikroorganismen und Endotoxin in der Luft Chemische Desinfektionsmittel und Antiseptika Quantitativer Suspensionsversuch zur der fungiziden Wirkung chemischer Desinfektionsmittel für Instrumente im humanmedizinischen Bereich - und Anforderungen (Phase 2, Stufe1) Chemische Desinfektionsmittel und Antiseptika - Quantitativer Suspensionsversuch zur der bakteriziden Wirkung chemischer Desinfektionsmittel für Instrumente im humanmedizinischen Bereich - und Anforderungen (Phase 2, Stufe 1); Gültigkeitsdauer: bis Ausstellungsdatum: Seite 16 von 27
17 DIN EN ISO : Operationsabdecktücher, -mäntel und Rein-Luft-Kleidung zur Verwendung als Medizinprodukte für Patienten, Klinikpersonal und Geräte - Allgemeine Anforderungen für Hersteller, Wiederaufbereiter und Produkte, und Gebrauchsanforderungen DIN EN ISO : Textilien - Zugeigenschaften von textilen Flächengebilden - Teil 1: Bestimmung der Höchstzugkraft und Höchstzugkraft-Dehnung mit dem Streifen-Zugversuch DIN EN ISO : Textilien - Zugeigenschaften von textilen Flächengebilden - Teil 2: Bestimmung der Höchstzugkraft mit dem Grab-Zugversuch DIN EN ISO : Textilien - Weiterreißeigenschaften von textilen Flächengebilden - Teil 2: Bestimmung der Weiterreißkraft mit dem Schenkel-Weiterreißversuch (einfacher Weiterreißversuch) DIN EN : DIN EN : DIN EN : DIN EN : DIN EN : DIN EN : DIN EN : DIN EN : DIN EN : DIN EN : Schutzkleidung - Leistungsanforderungen und für Schutzkleidung gegen Infektionserreger Sterilisatoren für medizinische Zwecke - Niedertemperatur-Dampf- Formaldehyd-Sterilisatoren - Anforderungen und Chemische Desinfektionsmittel und Antiseptika - Sporizide Wirkung (Basistest) - und Anforderungen (Phase 1) Chemische Desinfektionsmittel und Antiseptika Quantitativer Suspensionsversuch zur der mykobakteriziden Wirkung chemischer Desinfektionsmittel im humanmedizinischen Bereich einschließlich der Instrumentendesinfektionsmittel - und Anforderungen (Phase 2, Stufe 1) Chemische Desinfektionsmittel und Antiseptika Quantitativer Suspensionsversuch Viruzidie für in der Humanmedizin verwendete chemische Desinfektionsmittel und Antiseptika - und Anforderungen (Phase 2, Stufe 1) Chemische Desinfektionsmittel und Antiseptika Quantitativer Keimträgerversuch zur der bakteriziden Wirkung für Instrumente im humanmedizinischen Bereich, und Anforderungen Phase 2, Stufe 2 Chemische Desinfektionsmittel und Antiseptika Quantitativer Keimträgerversuch zur der fungiziden oder levuroziden Wirkung für Instrumente im humanmedizinischen Bereich, und Anforderungen Phase 2, Stufe 2 Chemische Desinfektionsmittel und Antiseptika Quantitativer Keimträgerversuch zur der mykobakteriziden oder tuberkuloziden Wirkung chemischer Desinfektionsmittel für Instrumente im humanmedizinischen Bereich, und Anforderungen Phase 2, Stufe 2 Chemische Desinfektionsmittel und Antiseptika - Anwendung Europäischer Normen für chemische Desinfektionsmittel und Antiseptika Chirurgische Masken: Anforderungen und Gültigkeitsdauer: bis Ausstellungsdatum: Seite 17 von 27
18 DIN EN ISO : Reinräume und zugehörige Reinraumbereiche - Biokontaminationskontrolle - Teil 1: Allgemeine Grundlagen DIN EN ISO : Reinräume und zugehörige Reinraumbereiche - Biokontaminationskontrolle - Teil 2: Auswertung und Interpretation von Biokontaminationsdaten DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN ISO : Sterilisation von Produkten für die Gesundheitsfürsorge - Allgemeine Anforderungen an die Charakterisierung eines sterilisierenden Agens und an die Entwicklung, Validierung und Lenkung der Anwendung eines Sterilisationsverfahrens für Medizinprodukte Reinigungs-Desinfektionsgeräte - Teil 1: Allgemeine Anforderungen, Begriffe und Reinigungs-Desinfektionsgeräte - Teil 2: Anforderungen und von Reinigungs-Desinfektionsgeräten mit thermischer Desinfektion für chirurgische Instrumente, Anästhesiegeräte, Gefäße, Utensilien, Glasgeräte usw. Reinigungs-Desinfektionsgeräte - Teil 3: Anforderungen und von Reinigungs-Desinfektionsgeräten mit thermischer Desinfektion für Behälter für menschliche Ausscheidungen Reinigungs-Desinfektionsgeräte - Teil 4: Anforderungen und für Reinigungs-Desinfektionsgeräte mit chemischer Desinfektion für thermolabile Endoskope; DIN ISO/TS : Reinigungs-Desinfektionsgeräte - Teil 5: Prüfanschmutzungen und - verfahren zum Nachweis der Reinigungswirkung DIN EN ISO : Wasserbeschaffenheit - Nachweis und Zählung von Pseudomonas aeruginosa - Membranfiltrationsverfahren ISO : Kleidung zum Schutz gegen Kontakt mit Blut und Körperflüssigkeiten - Bestimmung des Widerstandes von Material für Schutzkleidung gegen Durchdringung von Blut und Körperflüssigkeiten - bei der Benutzung synthetischen Bluts ISO : Kleidung zum Schutz gegen Kontakt mit Blut und Körperflüssigkeiten - Bestimmung des Widerstandes von Material für Schutzkleidung gegen Durchdringung von Krankheitskeimen, die durch Blut übertragen werden - bei der Benutzung von Bakterium Phi-X-174 DIN EN ISO : Sterilisation von Medizinprodukten - Vom Hersteller bereitzustellende Informationen für die Aufbereitung von resterilisierbaren Medizinprodukten DIN EN ISO : Sterilisation von Produkten für die Gesundheitsfürsorge - Feuchte Hitze - Teil 1: Anforderungen an die Entwicklung, Validierung und Lenkung der Anwendung eines Sterilisationsverfahrens für Medizinprodukte DIN : DIN EN : Aufbereitung von Schwimm- und Badebeckenwasser; Teil 1: Allgemeine Anforderungen Textilien; Bestimmung des Widerstandes gegen das Durchdringen von Wasser; Hydrostatischer Druckversuch Gültigkeitsdauer: bis Ausstellungsdatum: Seite 18 von 27
19 DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN ISO : DIN EN : DIN EN : DIN 53124: IEC : IEC : EN : DIN EN : DIN EN : EN : AK BWA 1997 ASTM F 1670 : 2007 ASTM F 1671 : 2007 Textilien - Bestimmung der antibakteriellen Wirkung antibakteriell behandelter Erzeugnisse Medizinische Handschuhe Bestimmung des entfernbaren Oberflächenpuders Operationsabdecktücher, -mäntel und Rein-Luft-Kleidung zur Verwendung als Medizinprodukte für Patienten, Klinikpersonal und Geräte - für die Widerstandsfähigkeit gegen Keimdurchtritt im feuchten Zustand (Wet bacterial Penetration) Schutzkleidung gegen infektiöse Agenzien - zur Beständigkeit gegen mikrobielle Penetration im trockenen Zustand (Dry bacterial Penetration) Wasserbeschaffenheit; Nachweis und Zählung der Sporen sulfitreduzierender Anaerobier (Chlostridien); Teil 1: Flüssigkeitsanreicherung Wasserbeschaffenheit; Nachweis und Zählung der Sporen sulfitreduzierender Anaerobier (Chlostridien); Teil 2: Membranfiltrationsverfahren Bestimmung des ph-wertes in wässrigen Extrakten Safety requirements for electrical equipment for measurement, control, and laboratory use - Part 2-045: Particular requirements for washer disinfectors used in medical, pharmaceutical, veterinary and laboratory fields Safety requirements for electrical equipment for measurement, control, and laboratory use - Part 2-042: Particular requirements for autoclaves and sterilizers using toxic gas for the treatment of medical materials, and for laboratory processes Sicherheitsbestimmungen für elektrische Meß-, Steuer-, Regel- und Laborgeräte - Teil 1: Allgemeine Anforderungen (IEC :2001) Safety requirements for electrical equipment for measurement, control, and laboratory use - Part 2-040: Particular requirements for sterilizers and washer-disinfectors used to treat medical materials (IEC 66/467/CD:2012) Safety requirements for electrical equipment for measurement, control and laboratory use - Part 2-041: Particular requirements for autoclaves using steam for the treatment of medical materials and for laboratory processes (IEC :1995) Electrical equipment for measurement, control and laboratory use - EMC requirements - Part 1: General requirements (IEC :2012) auf maschinelle Dekontamination von Bettgestellen, Nachttischen, Matratzen, Transportwagen und Umlaufbehältern Standard Test Method for Resistance of Materials Used in Protective Clothing to Penetration by Synthetic Blood Standard Test Method for Resistance of Materials Used in Protective Clothing to Penetration by Blood-Borne Pathogens Using Phi-X174 Bacteriophage Penetration as a Test System Gültigkeitsdauer: bis Ausstellungsdatum: Seite 19 von 27
20 ASTM F 1608 : 2004 ASTM F 1862: 2007 ASTM F BGBI BGBI 04/93, S. 162 : BGBl 04/94, S : BGBl 11/94, S : BGBl 04/96, S : DGHM : DVGW, Arbeitsblatt: EDANA WSP 80.9 (152.2 (02)) EDANA WSP (190.1 (02)) EDANA WSP 160.1(220.1(02)) EDANA : EDANA WSP (05) Hyg.Med 1995; 20 (1) : Japanese Industrial Standard, JIS Z 2801: Japanese Industrial Standard, JIS L 1902: KRINKO/BfArM-Empfehlung Aufbereitung MP Standard test method for microbial ranking of porous packaging materials Standard Test Method for Resistance of Medical Face Masks to Penetration by Synthetic Blood (Horizontal Projection of Fixed Volume at a Known Velocity Standard Test Method for Evaluating the Bacterial Filtration Efficiency (BFE) of Medical Face Mask Materials, Using a Biological Aerosol of Staphylococcus aureus von Abfalldesinfektionsverfahren auf Wirksamkeit (Sonderdruck des BGBl) Mitteilung des Bundesgesundheitsamtes über den Nachweis von Legionellen in erwärmtem Trinkwasser der Wirksamkeit von Flächendesinfektionsmitteln für die Desinfektion bei Tuberkulose der Wirksamkeit von Desinfektionsmitteln für die chemische Instrumentendesinfektion bei Tuberkulose Badewasserkomission des Umweltbundesamtes (1996): Hygienische Überwachung öffentlicher und gewerblicher Bäder durch die Gesundheitsämter (Amtsarzt) Standardmethoden der DGHM zur chemischer Desinfektionsverfahren Trinkwassererwärmungs- und Leitungsanlagen, Technische Maßnahmen zur Verminderung des Legionellenwachstums; Sanierung und Betrieb RUN OFF Bestimmung der Flüssigkeitsaufnahmemenge Dry bacterial Penetration von Vliesstoffen auf lose haftende Partikel: Flusenbildung Linting tendency (dry state) Standard Test Metod for Nonwovens Bacterial Filtration Efficiency und Bewertung der Reinigungs- und Desinfektionswirkung von Endoskopie-Dekontaminationsautomaten sowie - Desinfektionsautomaten; Hyg.Med 1995; 20 (1): Antimicrobial products Tests for antimicrobial activity and efficacy Testing for antibacterial activity and efficacy on textile products Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten, Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut (RKI) und des Bundesinstitutes für Arzneimittel und Medizinprodukte (BfArM) Bundesgesundheitsbl. 2012, 55 : Gültigkeitsdauer: bis Ausstellungsdatum: Seite 20 von 27
21 Leitlinie von DGKH, DGSV und AKI: Leitlinie von DGKH, DGSV und AKI : Leitlinie DVV und RKI: ÖGHMP : 1983 Ph. Eur. 6, Ph. Eur. 8, Robert Koch Institut Empfehlung: R-RKI : R-RKI BGBl 4, 2002 R-RKI-BAM BGBl : SS : TrinkW VGB F 301 P : SOP SOP SOP SOP Leitlinie von DGKH, DGSV und AKI für die Validierung und Routineüberwachung maschineller Reinigungs- und Desinfektionsprozesse für thermostabile Medizinprodukte und zu Grundsätzen der Geräteauswahl Leitlinie von DGKH, DGSV, DEGEA, DGVS und AKI für die Validierung maschineller Reinigungs- und Desinfektionsprozesse zur Aufbereitung thermolabiler Endoskope Leitlinie der Deutschen Vereinigung zur Bekämpfung der Viruskrankheiten (DVV)e.V und des Robert-Koch-Instituts (RKI) zur von chemischen Desinfektionsmitteln auf Wirksamkeit gegen Viren in der Humanmedizin Methodik der Wirksamkeitsprüfung von Flächendesinfektionsverfahren auf Bakterien-Endotoxine Mikrobiologische nicht steriler Produkte: Zählung der gesamten vermehrungsfähigen Keime Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten Anforderungen der Hygiene an die Wäsche aus Einrichtungen des Gesundheitsdienstes, die Wäscherei und den Waschvorgang und Bedingungen für die Vergabe von Wäsche an gewerbliche Wäschereien Anforderungen an die Hygiene bei der Aufbereitung flexibler Endoskope und endokopischen Zusatzinstrumentariums Anforderungen an Gestaltung, Eigenschaften und Betrieb von dezentralen Desinfektionsmittel-Dosiergeräten Richtlinie der Bundesanstalt für Materialforschung und prüfung, des Robert Koch-Institutes und der Kommission für Krankenhaushygiene und Infektionsprävention. Health care textiles - bakterial penetration - Wet Trinkwasserverordnung Mikrobielle Emission sowie Keimzahländerung im Kühlwasser beim Betrieb von Naß-Kühltürmen Bestimmung der bakteriostatischen und fungistatischen Wirksamkeit chemischer Desinfektionsverfahren sowie geeigneter Inaktivierungsmittel (DGHM) Bestimmung der bakteriostatischen und fungistatischen Wirksamkeit chemischer Desinfektionsverfahren im qualitativen Suspensionstest (DGHM) Bestimmung der bakteriziden Wirksamkeit chemischer Desinfektionsverfahren im quantitativen Suspensionstest (DGHM) Bestimmung der fungiziden Wirksamkeit chemischer Desinfektionsverfahren im Flächendesinfektionsversuch unter praxisnahen Bedingungen (DGHM) Gültigkeitsdauer: bis Ausstellungsdatum: Seite 21 von 27
22 SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP Bestimmung der bakteriziden Wirksamkeit chemischer Desinfektionsverfahren im Flächendesinfektionsversuch unter praxisnahen Bedingungen (DGHM) der Wirksamkeit von Desinfektionsmitteln für die chemische Instrumentendesinfektion, Teil c (DGHM) Quantitativer Suspensionstest mit M. terrae für die der Wirksamkeit von Instrumentendesinfektionsmitteln (DGHM) der Wirksamkeit von Desinfektionsmitteln für die chemische Instrumentendesinfektion bei Tuberkulose (Robert-Koch-Institut) der Wirksamkeit von Flächendesinfektionsmitteln für die Desinfektion bei Tuberkulose (Robert-Koch-Institut) Chemothermische Wäschedesinfektion (DGHM) der Wirksamkeit von Hautdesinfektionsmitteln Bestimmung der bakteriziden und fungiziden Wirksamkeit von Kollagen- Antiseptica-Präparationen im quantitativen Suspensionstest Bestimmung der fungiziden Wirksamkeit chemischer Desinfektionsmittelverfahren im Flächendesinfektionsversuch mit Tupfer- Abschwemm-Methode (ÖGHMP) Bestimmung der bakteriziden Wirksamkeit chemischer Wäschedesinfektionsmittelverfahren gegen Mykobakterien im Keimträgerversuch (DGHM) Quantitative Bestimmung der Keimreduktion durch antibakterielle Wundauflagen der desinfizierenden Wirkung chemothermischer Wäschedesinfektionsverfahren in den Wäschereien Quantifizierung der Reinigungsleistung Nachweis der Abreicherung von praxisrelevanten Prüfanschmutzungen in Abhängigkeit des Trägermaterials und den Reinigungsbedingungen Quantitativer Suspensionsversuch zur Bestimmung der bakteriziden, fungiziden oder sporiziden Wirkung chemischer Desinfektionsmittel und Antiseptika (Basistest Phase 1) Quantitativer Suspensionsversuch zur Bestimmung der bakteriziden, fungiziden, mycobakteriziden oder sporiziden Wirkung chemischer Desinfektionsmittel und Antiseptika im Bereich der Humanmedizin (Phase 2, Stufe 1) Praxisnahe Versuche zur Bestimmung der bakteriziden, fungiziden, mycobakteriziden oder sporiziden Wirkung chemischer Desinfektionsmittel und Antiseptika im Bereich der Humanmedizin (Phase 2, Stufe 2) der antimikrobiellen Wirkung von Oberflächen im Flächenversuch Gültigkeitsdauer: bis Ausstellungsdatum: Seite 22 von 27
23 SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP Bestimmung der bakteriostatischen und fungistatischen Wirksamkeit chemischer Desinfektionsverfahren sowie Auswahl geeigneter Inaktivierungsmittel Bestimmung der bakteriziden und fungiziden Wirksamkeit chemischer Desinfektionsverfahren im qualitativen Suspensionstest Bestimmung der bakteriziden Wirksamkeit im quantitativen Suspensionsversuch Quantitativer Suspensionsversuch Viruzidie für in der Humanmedizin verwendeten chemischen Desinfektionsmittel und Antiseptika (Phase 2, Stufe 1) Chemische Desinfektionsmittel und Antiseptika Quantitativer Suspensionsversuch zur Bestimmung der viruziden Wirkung chemischer Desinfektionsmittel und Antiseptika im Veterinärbereich und Anforderungen (Phase 2, Stufe 1) Quantitativer Suspensionsversuch begrenzte Viruzidie für in der Humanmedizin verwendeten chemischen Desinfektionsmittel und Antiseptika entsprechend der Leitlinie von RKI und DVV Quantitative der viruziden Wirksamkeit chemischer Desinfektionsmittel auf Oberflächen (Phase 2, Stufe 2) Mikrobiologische Untersuchung von Nutzwasser von Abfalldesinfektionsanlagen auf Wirksamkeit Biologische von Groß-Dampfsterilisatoren mit Prüfbeladung ( auf Wirksamkeit nach DIN Teil 3) Sterilisation von Medizinprodukten - Validierung und Routineüberwachung für Sterilisation mit Ethylenoxid DIN EN ISO Sterilisation für medizinische Zwecke Validierung und Routineüberwachung für Sterilisation mit Niedertemperatur-Dampf- Formaldehyd-Sterilisatoren nach DIN EN von Dosierzumischanlagen nach RKI Verpackungsmaterialien und systeme für zu sterilisierende Medizinprodukte Bestimmung der Population von Mikroorganismen auf einem Produkt (DIN EN ISO ) Sterilisation mit feuchter Hitze; Anforderungen und entsprechend DIN EN 285, DIN EN 13060, DIN EN ISO Niedertemperatur Sterilisation; Anforderungen und entsprechend ISO 14937, EN 14180, EN ISO 11135, EN 1422 SOP Überprüfung Raumlufttechnischer Anlagen DIN SOP SOP Sicherheitswerkbänke für mikrobiologische und biotechnologische Arbeiten; Anforderungen, (DIN Teil 10) Arbeitsplatzatmosphäre - Leitlinie für die Messung von Mikroorganismen und Endotoxin in der Luft Gültigkeitsdauer: bis Ausstellungsdatum: Seite 23 von 27
24 SOP Biologische Beurteilung von Medizinprodukten ISO Zytotoxizität SOP Biologische Beurteilung von Medizinprodukten ISO auf Gentoxizität, Karzinogenität und Reproduktionstoxizität SOP Biologische Beurteilung von Medizinprodukten ISO Auswahl von zur Wechselwirkung von Blut mit Fremdoberflächen SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP Quantitativer Nachweis pyrogener Verunreinigungen im humanen Vollblutmodell mittels ELISA Beurteilung der quantitativen und qualitativen Verteilung von Hausstaubmilben in einem Biotop mittels Wärmefluchtverfahren und Mobilitätstest Quantitativer Nachweis von Endotoxin in Flüssigkeiten und Eluaten mittels LAL-Test (Limulus Amöbozyten - Lysat Test). auf mikrobielle Verunreinigung bei nicht sterilen Produkten: Zählung der gesamten, vermehrungsfähigen, aeroben Keime nach Europäischem Arzneibuch (Ph.-Eur ) auf mikrobielle Verunreinigung bei sterilen Produkten: Zählung der gesamten, vermehrungsfähigen, aeroben und anaerobe Keime nach Europäischem Arzneibuch (Ph.-Eur ) Epikutantest, auf Irritation Hygienische Umgebungsuntersuchungen RABC Wet-Penetration EN und Penetration Schwedischer Standard SS Bestimmung der Zugeigenschaften von textilen Flächengeweben nach EN ISO und 2 Bestimmung des Widerstandes gegen das Durchdringen von Wasser Hydrostatischer Drucktest EN Bestimmung der Weiterreißkraft von textilen Flächengeweben nach EN ISO SOP von Textilien im Streifen-Zugversuch EN ISO SOP SOP Dry-Penetration nach EN SOP SOP SOP Bestimmung der Flusenfreisetzung von der Fliesstoff-Oberfläche (EDANA) auf lose haftende Partikel : Linting nach EDANA /ISO Widerstand gegen Durchdringung von unterschiedlichen Flüssigkeiten (ASTM )Modifiziert mit Widerstand gegen Durchdringung von Bakteriophagen (ASTM b) Modifiziert nach DIN EN Gültigkeitsdauer: bis Ausstellungsdatum: Seite 24 von 27
25 SOP Wasseraufnahmevermögen SOP RUN OFF-Bestimmung der Flüssigkeitsaufnahmemenge EDANA SOP Linting feucht entsprechend INDA IST und EN 1644 SOP SOP SOP SOP SOP Atmungs-Eignungsprüfung, Differentialer Druck, in Übereinstimmung mit U.S.Militär-Spezifikation-MIL-M C (Luft-Austauschdruck) und EN der Filterwirksamkeit für Bakterien (BFE) für Masken nach EN der Flüssigkeitsresistenz Masken gegen das Durchdringen von Flüssigkeitsspritzern nach EN Medizinische Handschuhe zum einmaligen Gebrauch Teil 1: Anforderungen und auf Dichtheit Medizinische Handschuhe zum einmaligen Gebrauch Teil 2: Anforderungen und der physikalischen Eigenschaften SOP Medizinische Handschuhe zum einmaligen Gebrauch Teil 3: Anforderungen und für die biologische Beurteilung SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP Annahmestichprobenprüfung anhand der Anzahl fehlerhafter Einheiten oder Fehler (Attributprüfung) Medizinische Handschuhe Bestimmung des entfernbaren Oberflächenpuders, ISO 21171:2006 Mikrobielle Emission sowie Keimzahländerungen im Kühlwasser beim Betrieb von Naß- und Hybrid-Kühltürmen Zusammensetzung des Kühlturmschwadens Typprüfung von Wash-/Desinfektionsgeräten Allgemeine Anforderungen, Definitionen und DIN EN ISO Anforderungen und von Wasch-Desinfektionsgeräten für OP- Instrumentarium, Anästhesie-Ausrüstungen, Hohlkörper, Utensilien, Glasgerätschaften usw. Anforderungen und von Steckbecken-Wasch-Desinfektionsgeräten Anforderungen und von Endoskop-Wasch-Desinfektionsgeräten und Bewertung der Reinigungs- und Desinfektionswirkung von Endoskopie-Dekontaminationsautomaten sowie -Desinfektionsautomaten (Arbeitskreis Endoskopie, Projektgruppe Flexible Endoskope ; DGKH) auf maschinelle Dekontamination von Bettgestellen, Nachttischen, Matratzen, Transportwagen und Umlaufbehältern (AK BWA) Empfehlungen und Prüfmethode zur maschinellen Reinigung und Desinfektion von Instrumenten für minimal invasive Chirurgie Anschmutzung von Prüfkörpern mit laborinternen Prüfanschmutzungen Gültigkeitsdauer: bis Ausstellungsdatum: Seite 25 von 27
26 SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP SOP : und Anschmutzungen gemäß EN ISO der Reinigungsleistung von Reinigungs- und Desinfektionsgeräten für thermostabile Medizinprodukte entsprechend der Leitlinie von DGKH, DGSV und AKI Hygienisch-mikrobiologische Kontrolle der Endoskop-Aufbereitung gemäß RKI-Empfehlungen Bestimmung der Gesamthärte des Wassers Bestimmung von anionischen Tensiden in Wässern und wäßrigen Lösungen Quantitative Bestimmung von freien NH2-Gruppen der Blutproteine durch die modifizierte OPA-Methode (1,2) Bestimmung des ph Wertes des wässrigen Extraktes von Fasermaterial Nachweis bluthaltiger Restanschmutzungen von Medizinprodukten Orientierende Untersuchung des anionischen Tensidgehalt Orientierende Untersuchung des kationischentensidgehalt Orientierende Untersuchung des nichtionischen Tensidgehalt Enzymatischer Test zur Bestimmung von nativer Stärke und von Stärkepartialhydrolysaten in Lebensmitteln und anderen Probenmaterialien Bestimmung des Proteingehaltes von Flüssigkeiten mit dem BCA Protein Assay Kit Bestimmung von Formaldehyd Spektrophotometrische Methode mit Chromotopsäure Vom Hersteller bereitzustellende Informationen für die Aufbereitung von Medizinprodukten (ISO 17664) Anschmutzung von Produkten mit Prüfanschmutzungen zur der Reinigung und Desinfektion und Rückgewinnung der Prüfanschmutzung in Anlehnung an EN ISO Anschmutzung von Produkten mit Prüfanschmutzungen zur der Sterilisation und Rückgewinnung der Prüfanschmutzung Abkürzungen AK BWA ASTM BGBl CEN CEN/TC DGHM Arbeitskreis Bettgestell- und Wagen-Dekontaminationsanlagen der DGKH American Society for Testing and Materials Bundesgesundheitsblatt Europäische Normungsorganisation Technisches Komitee des CEN Deutsche Gesellschaft für Hygiene und Mikrobiologie Gültigkeitsdauer: bis Ausstellungsdatum: Seite 26 von 27
27 DIN DVGW DVV DGKH EDANA EN Hyg.Med IEC ISO OECD ÖGHMP Ph. Eur. R-DGHM R-RKI SOP SS TS TVO VAH Deutsches Institut für Normung Deutscher Verein des Gas- und Wasserfaches e.v. Deutsche Vereinigung zur Bekämpfung der Viruskrankheiten e.v. Deutsche Gesellschaft für Krankenhaushygiene European disposibles and nonwovens association Europäische Norm Zeitschrift Hygiene und Medizin International Electrotechnical Commission International Organization for Standardization Organization for Economic Cooperation and Development Österreichische Gesellschaft für Hygiene, Mikrobiologie und Präventivmedizin European Pharmacopoeia Richtlinie der Deutschen Gesellschaft für Hygiene und Mikrobiologie für die und Bewertung chemischer Desinfektionsverfahren Richtlinie für Krankenhaushygiene und Infektionsprävention des Robert-Koch Instituts Arbeitsanweisung der HygCen GmbH Swedish Standard Technical Standard Trinkwasserverordnung Verbund für angewandte Hygiene 1 DIN EN ISO/IEC : Allgemeine Anforderungen an die Kompetenz von Prüf- und Kalibrierlaboratorien 2 Richtlinie 93/42/EWG des Rates vom 14. Juni 1993 über Medizinprodukte, ABl. Nr. L 169 vom 12. Juli 1993, S. 1; zuletzt geändert durch Richtlinie 2007/47/EG vom 05. September 2007, ABl. Nr. L 247 vom 21. September 2007, S Richtlinie 90/385/EWG des Rates vom 20. Juni 1990 zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über aktive implantierbare medizinische Geräte, ABl. Nr. L 189 vom 20. Juli 1990, S. 17; zuletzt geändert durch Richtlinie 2007/47/EG vom 05. September 2007, ABl. Nr. L 247 vom 21. September 2007, S DIN EN ISO 13485: Medizinprodukte Qualitätsmanagementsysteme Anforderungen für regulatorische Zwecke 5 Zu den Übergangsfristen vergl. die Liste harmonisierter Normen auf der Homepage der EU Gültigkeitsdauer: bis Ausstellungsdatum: Seite 27 von 27
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten über die Akkreditierung der HygCen Centrum für Hygiene und Medizinische Produktsicherheit GmbH Bornhövedstraße 78 19055
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten über die Akkreditierung der HygCen Centrum für Hygiene und Medizinische Produktsicherheit GmbH Bornhövedstraße 78 19055
Akkreditierungsumfang der Prüfstelle (EN ISO/IEC 17025:2005) HygCen Austria GmbH / (Ident.Nr.: 0196)
 1 2 3 4 5 6 7 8 02-030 11-001 16-009 16-010 17-008 DGHM Kapitel 14 DGHM Kapitel 15 DGHM Kapitel 17 2008-05 Prüfung der Reinigungswirkung chemothermischer Wäschedesinfektionsverfahren in den Wäschereien
1 2 3 4 5 6 7 8 02-030 11-001 16-009 16-010 17-008 DGHM Kapitel 14 DGHM Kapitel 15 DGHM Kapitel 17 2008-05 Prüfung der Reinigungswirkung chemothermischer Wäschedesinfektionsverfahren in den Wäschereien
Deutsche Akkreditierungsstelle GmbH
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14103-01-02 nach DIN EN ISO/IEC 17025:2005 1 und den Richtlinien 90/385/EWG 2 und 93/42/EWG 3 als Prüflaboratorium Gültigkeitsdauer:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14103-01-02 nach DIN EN ISO/IEC 17025:2005 1 und den Richtlinien 90/385/EWG 2 und 93/42/EWG 3 als Prüflaboratorium Gültigkeitsdauer:
Anlage zur Akkreditierungsurkunde D-PL-18176-01-02 nach DIN EN ISO/IEC 17025:2005 1 und nach Richtlinien 90/385/EWG 2 und 93/42/EWG 3
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18176-01-02 nach DIN EN ISO/IEC 17025:2005 1 und nach Richtlinien 90/385/EWG 2 und 93/42/EWG 3 Gültigkeitsdauer: 18.09.2014 bis
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18176-01-02 nach DIN EN ISO/IEC 17025:2005 1 und nach Richtlinien 90/385/EWG 2 und 93/42/EWG 3 Gültigkeitsdauer: 18.09.2014 bis
Anlage zur Akkreditierungsurkunde D-PL-18398-02-00 nach DIN EN ISO/IEC 17025:2005 3 und Richtlinie 93/42/EWG 1 und 90/385/EWG 2
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18398-02-00 nach DIN EN ISO/IEC 17025:2005 3 und Richtlinie 93/42/EWG 1 und 90/385/EWG 2 Gültigkeitsdauer: 17.12.2015 bis 04.03.2018
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18398-02-00 nach DIN EN ISO/IEC 17025:2005 3 und Richtlinie 93/42/EWG 1 und 90/385/EWG 2 Gültigkeitsdauer: 17.12.2015 bis 04.03.2018
Beliehene gemäß 8 Absatz 1 AkkStelleG i.v.m. 1 Absatz 1 AkkStelleGBV
 . { DÄkkS Deutsche Akkreditierungsstelle Deutsche Akkreditierungsstelle GmbH Beliehene gemäß 8 Absatz 1 AkkStelleG i.v.m. 1 Absatz 1 AkkStelleGBV Akkreditierung Die Deutsche Akkreditierungsstelle GmbH
. { DÄkkS Deutsche Akkreditierungsstelle Deutsche Akkreditierungsstelle GmbH Beliehene gemäß 8 Absatz 1 AkkStelleG i.v.m. 1 Absatz 1 AkkStelleGBV Akkreditierung Die Deutsche Akkreditierungsstelle GmbH
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten über die Überwachung der Anerkennung der Medical Device Services - DR. ROSSBERGER GmbH Lilienthalstraße 4 82205 Gilching
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten über die Überwachung der Anerkennung der Medical Device Services - DR. ROSSBERGER GmbH Lilienthalstraße 4 82205 Gilching
Akkreditierungsumfang der Prüfstelle (ISO/IEC 17025) W.H.U. GmbH / (Ident.Nr.: 0289)
 W.H.U. GmbH / (Ident.: 0289) Titel 1 2 3 4 5 5 6 6 4210 4240 4250 6020 6030 6040 DGHM-Kapitel 10 DGHM-Kapitel 2008-04 Bestimmung von Formaldehyd in Wasser mittels Chromotropsäure (VWR Spektroquant) 2008-04
W.H.U. GmbH / (Ident.: 0289) Titel 1 2 3 4 5 5 6 6 4210 4240 4250 6020 6030 6040 DGHM-Kapitel 10 DGHM-Kapitel 2008-04 Bestimmung von Formaldehyd in Wasser mittels Chromotropsäure (VWR Spektroquant) 2008-04
Anhang B: Normen. Tabelle - Normen. 93/42/EWG DIN EN 285 Sterilisation Dampf-Sterilisatoren Groß- Sterilisatoren
 Anhang B: Normen Bei Befolgung der Angaben der aufgeführten Normen kann von der Erfüllung der anerkannten Regeln der Technik ausgegangen werden. Diese Zusammenstellung umfasst die unter dem Aspekt der
Anhang B: Normen Bei Befolgung der Angaben der aufgeführten Normen kann von der Erfüllung der anerkannten Regeln der Technik ausgegangen werden. Diese Zusammenstellung umfasst die unter dem Aspekt der
Anlage zur Akkreditierungsurkunde D-PL-18084-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18084-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 28.11.2012 bis 27.11.2017 Urkundeninhaber: Waltraud Niedermann Institut
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18084-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 28.11.2012 bis 27.11.2017 Urkundeninhaber: Waltraud Niedermann Institut
Anlage zur Akkreditierungsurkunde D-PL-13366-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13366-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 07.10.2014 bis 26.06.2016 Ausstellungsdatum: 07.10.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13366-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 07.10.2014 bis 26.06.2016 Ausstellungsdatum: 07.10.2014 Urkundeninhaber:
Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen
 Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen F. H. H. Brill Dr. Brill + Partner GmbH Institut für Hygiene und Mikrobiologie, Hamburg, www.brillhygiene.com
Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen F. H. H. Brill Dr. Brill + Partner GmbH Institut für Hygiene und Mikrobiologie, Hamburg, www.brillhygiene.com
Anlage zur Akkreditierungsurkunde D-ZM-16002-06-00 nach DIN EN ISO/IEC 17021:2011
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZM-16002-06-00 nach DIN EN ISO/IEC 17021:2011 Gültigkeitsdauer: 15.12.2014 bis 14.12.2019 Ausstellungsdatum: 15.12.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZM-16002-06-00 nach DIN EN ISO/IEC 17021:2011 Gültigkeitsdauer: 15.12.2014 bis 14.12.2019 Ausstellungsdatum: 15.12.2014 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-PL-13168-04-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13168-04-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 22.07.2013 bis 21.07.2018 Ausstellungsdatum: 22.07.2013 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13168-04-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 22.07.2013 bis 21.07.2018 Ausstellungsdatum: 22.07.2013 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ZE-16029-04-00 nach DIN EN ISO/IEC 17065:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZE-16029-04-00 nach DIN EN ISO/IEC 17065:2013 Gültigkeitsdauer: 27.04.2016 bis 14.12.2019 Ausstellungsdatum: 27.04.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZE-16029-04-00 nach DIN EN ISO/IEC 17065:2013 Gültigkeitsdauer: 27.04.2016 bis 14.12.2019 Ausstellungsdatum: 27.04.2016 Urkundeninhaber:
Leistungsverzeichnis. 1. Januar. Hygiene Nord GmbH c/o BioTechnikum Walther-Rathenau-Straße 49 A D-17489 Greifswald http://www.hygiene-nord.
 Leistungsverzeichnis 1. Januar 2007 Hygiene Nord GmbH c/o BioTechnikum Walther-Rathenau-Straße 49 A D-17489 Greifswald http://www.hygiene-nord.de Ihr Ansprechpartner Torsten Koburger Tel + 49 (0)3834 515520
Leistungsverzeichnis 1. Januar 2007 Hygiene Nord GmbH c/o BioTechnikum Walther-Rathenau-Straße 49 A D-17489 Greifswald http://www.hygiene-nord.de Ihr Ansprechpartner Torsten Koburger Tel + 49 (0)3834 515520
Tübinger Forum 2011. 05. November 2011
 05. November 2011 Desinfektion immer ein aktuelles Thema Dipl.-Biol. Verona Schmidt Leitung Abteilung Mikrobiologie und Hygiene Chem. Fabrik Dr. Weigert, Hamburg 1 Inhalt: Grundlagen der Desinfektion Prüfung
05. November 2011 Desinfektion immer ein aktuelles Thema Dipl.-Biol. Verona Schmidt Leitung Abteilung Mikrobiologie und Hygiene Chem. Fabrik Dr. Weigert, Hamburg 1 Inhalt: Grundlagen der Desinfektion Prüfung
Anlage zur Akkreditierungsurkunde D-PL-18029-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18029-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 24.09.2012 bis 23.09.2017 Urkundeninhaber: BMA-Labor GbR Biologisches
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18029-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 24.09.2012 bis 23.09.2017 Urkundeninhaber: BMA-Labor GbR Biologisches
EUROPÄISCHE KOMMISSION
 24.1.2013 Amtsblatt der Europäischen Union C 22/1 IV (Informationen) INFORMATIONEN DER ORGANE, EINRICHTUNGEN UND SONSTIGEN STELLEN DER EUROPÄISCHEN UNION EUROPÄISCHE KOMMISSION Mitteilung der Kommission
24.1.2013 Amtsblatt der Europäischen Union C 22/1 IV (Informationen) INFORMATIONEN DER ORGANE, EINRICHTUNGEN UND SONSTIGEN STELLEN DER EUROPÄISCHEN UNION EUROPÄISCHE KOMMISSION Mitteilung der Kommission
Anlage zur Akkreditierungsurkunde D-PL-19327-01-01 nach DIN EN ISO/IEC 17025:2005 und nach Richtlinie 93/42/EWG und 98/79/EG
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-19327-01-01 nach DIN EN ISO/IEC 17025:2005 und nach Richtlinie 93/42/EWG und 98/79/EG Gültigkeitsdauer: 20.02.2015 bis 26.05.2019
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-19327-01-01 nach DIN EN ISO/IEC 17025:2005 und nach Richtlinie 93/42/EWG und 98/79/EG Gültigkeitsdauer: 20.02.2015 bis 26.05.2019
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen
 Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
Anlage zur Akkreditierungsurkunde D-PL-19339-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-19339-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 22.07.2014 bis 21.07.2019 Ausstellungsdatum: 22.07.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-19339-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 22.07.2014 bis 21.07.2019 Ausstellungsdatum: 22.07.2014 Urkundeninhaber:
(Veröffentlichung der Titel und der Bezugsnummern der harmonisierten Normen im Sinne der Harmonisierungsrechtsvorschriften
 C 14/36 DE Amtsblatt der Europäischen Union 16.1.2015 Mitteilung der Kommission im Rahmen der Durchführung der Richtlinie 90/385/EWG des Rates vom 20. Juni 1990 zur Angleichung der Rechtsvorschriften der
C 14/36 DE Amtsblatt der Europäischen Union 16.1.2015 Mitteilung der Kommission im Rahmen der Durchführung der Richtlinie 90/385/EWG des Rates vom 20. Juni 1990 zur Angleichung der Rechtsvorschriften der
Anlage zur Akkreditierungsurkunde D-PL-11020-03-02 nach DIN EN ISO/IEC 17025: 2005 4 und nach Richtlinien 93/42/EWG 1, 90/385/EWG 2 und 98/79/EWG 3
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-11020-03-02 nach DIN EN ISO/IEC 17025: 2005 4 und nach Richtlinien 93/42/EWG 1, 90/385/EWG 2 und 98/79/EWG 3 Gültigkeitsdauer:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-11020-03-02 nach DIN EN ISO/IEC 17025: 2005 4 und nach Richtlinien 93/42/EWG 1, 90/385/EWG 2 und 98/79/EWG 3 Gültigkeitsdauer:
Anlage zur Akkreditierungsurkunde D-PL-12049-01-01 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-12049-01-01 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 25.06.2014 bis 24.06.2019 Ausstellungsdatum: 25.06.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-12049-01-01 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 25.06.2014 bis 24.06.2019 Ausstellungsdatum: 25.06.2014 Urkundeninhaber:
( DAkkS Deutsche Akkreditierungsste e
 Akkreditierungsste e GmbH Anlage zur Akkreditierungsurkunde D-PL-13348-01-00 nach DIN EN 150/IEC 17025:2005 Urkundeninhaber: Medizinisches Versorgungszentrum Clotten Labor Dr. Englert, Dr. Raif & Kollegen
Akkreditierungsste e GmbH Anlage zur Akkreditierungsurkunde D-PL-13348-01-00 nach DIN EN 150/IEC 17025:2005 Urkundeninhaber: Medizinisches Versorgungszentrum Clotten Labor Dr. Englert, Dr. Raif & Kollegen
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis
 Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Umgebungs- und Hygieneprüfungen im Rahmen des Hygienemonitorings im Krankenhaus Prüfverfahren und Akzeptanzkriterien
 Umgebungs- und Hygieneprüfungen im Rahmen des Hygienemonitorings im Krankenhaus Prüfverfahren und Akzeptanzkriterien Dr. Julia Okpara-Hofmann Vortrag auf dem 115. Hygiene und Steri-Treff am 4. November
Umgebungs- und Hygieneprüfungen im Rahmen des Hygienemonitorings im Krankenhaus Prüfverfahren und Akzeptanzkriterien Dr. Julia Okpara-Hofmann Vortrag auf dem 115. Hygiene und Steri-Treff am 4. November
Reinigung, Desinfektion, Pflege und Sterilisation von Turbinen, Hand- und Winkelstücken
 Reinigung, Desinfektion, Pflege und Sterilisation von Turbinen, Hand- und Winkelstücken Mikrobielle Kontamination von Übertragungsinstrumenten Nach Behandlung sind diese innen wie außen kontaminiert! Kontamination
Reinigung, Desinfektion, Pflege und Sterilisation von Turbinen, Hand- und Winkelstücken Mikrobielle Kontamination von Übertragungsinstrumenten Nach Behandlung sind diese innen wie außen kontaminiert! Kontamination
Verpackungen für in der Endverpackung zu sterilisierende Medizinprodukte
 ÖNORM EN ISO 11607-1 Ausgabe: 2014-11-15 Verpackungen für in der Endverpackung zu sterilisierende Medizinprodukte Teil 1: Anforderungen an Materialien, Sterilbarrieresysteme und Verpackungssysteme (konsolidierte
ÖNORM EN ISO 11607-1 Ausgabe: 2014-11-15 Verpackungen für in der Endverpackung zu sterilisierende Medizinprodukte Teil 1: Anforderungen an Materialien, Sterilbarrieresysteme und Verpackungssysteme (konsolidierte
Hygienisch-mikrobiologische Überprüfung von flexiblen Endoskopen nach ihrer Aufbereitung
 » DGKH Hygienisch-mikrobiologische Überprüfung von flexiblen Endoskopen nach ihrer Aufbereitung Diese Empfehlung wird als Anlage in der noch nicht abgeschlossenen Leitlinie von DGKH, DGSV, DEGEA und AKI
» DGKH Hygienisch-mikrobiologische Überprüfung von flexiblen Endoskopen nach ihrer Aufbereitung Diese Empfehlung wird als Anlage in der noch nicht abgeschlossenen Leitlinie von DGKH, DGSV, DEGEA und AKI
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit?
 Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Hygiene-Gutachten zur Medigenic TM Tastatur/Maus-Kombination der Firma Esterline Advanced Input Systems aus Coeur d Alene, USA
 Institut für Medizinische Mikrobiologie und Krankenhaushygiene Krankenhaushygiene Universitätsklinikum Giessen und Marburg GmbH Philipps-Universität Marburg Rein EDV GmbH Jakob-Krebs-Strasse 124 47877
Institut für Medizinische Mikrobiologie und Krankenhaushygiene Krankenhaushygiene Universitätsklinikum Giessen und Marburg GmbH Philipps-Universität Marburg Rein EDV GmbH Jakob-Krebs-Strasse 124 47877
Nutzen der EN-Prüfungen von Desinfektionsmitteln
 Nutzen der EN-Prüfungen von Desinfektionsmitteln Im Rahmen der FDA-Richtlinie für die pharmazeutische Industrie Production hygiene is of major importance in many areas, as it is directly related to the
Nutzen der EN-Prüfungen von Desinfektionsmitteln Im Rahmen der FDA-Richtlinie für die pharmazeutische Industrie Production hygiene is of major importance in many areas, as it is directly related to the
Medizinprodukteaufbereitung aus Sicht der Bezirksregierung
 Medizinprodukteaufbereitung aus Sicht der Bezirksregierung Dr. Arno Terhechte Dezernat 24 Pharmazeutische Angelegenheiten Themen: Warum werden Betreiber inspiziert? Welche Betreibertypen werden überwacht?
Medizinprodukteaufbereitung aus Sicht der Bezirksregierung Dr. Arno Terhechte Dezernat 24 Pharmazeutische Angelegenheiten Themen: Warum werden Betreiber inspiziert? Welche Betreibertypen werden überwacht?
DGSV-Kongress vom 3.- 5. Oktober 2011. Neue Kompetenzen der ZSVA: Aufbereitung von flexiblen Endoskopen
 DGSV-Kongress vom 3.- 5. Oktober 2011 Neue Kompetenzen der ZSVA: Aufbereitung von flexiblen Endoskopen - Unterschiede in der Aufbereitung - Aufbereitungsverfahren mit chemo-thermischer Desinfektion - Materialveränderungen,
DGSV-Kongress vom 3.- 5. Oktober 2011 Neue Kompetenzen der ZSVA: Aufbereitung von flexiblen Endoskopen - Unterschiede in der Aufbereitung - Aufbereitungsverfahren mit chemo-thermischer Desinfektion - Materialveränderungen,
Kriterien zur Auswahl von Desinfektionsmitteln für Flächen und Personal
 Wissenschaft und Technik pharmind Kriterien zur Auswahl von Desinfektionsmitteln für Flächen und Personal Dr. Jörg Siebert und Dipl. Ing. Margarete Witt-Mäckel Schülke & Mayr GmbH, Norderstedt Korrespondenz:
Wissenschaft und Technik pharmind Kriterien zur Auswahl von Desinfektionsmitteln für Flächen und Personal Dr. Jörg Siebert und Dipl. Ing. Margarete Witt-Mäckel Schülke & Mayr GmbH, Norderstedt Korrespondenz:
Dieser Rahmenlehrplan ersetzt den Rahmenlehrplan für den Sachkundelehrgang in der bisher vorliegenden Fassung. Präambel
 Erwerb der Sachkenntnis gemäß 4(3) der Medizinproduktebetreiberverordnung (MPBetreibV) für die Instandhaltung von Medizinprodukten in der ärztlichen Praxis gültig ab Erscheinungsdatum und spätestens umzusetzen
Erwerb der Sachkenntnis gemäß 4(3) der Medizinproduktebetreiberverordnung (MPBetreibV) für die Instandhaltung von Medizinprodukten in der ärztlichen Praxis gültig ab Erscheinungsdatum und spätestens umzusetzen
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Sterile Medizinprodukte
 Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Sterile Medizinprodukte Geltungsbereich: Diese Regeln legen Anforderungen fest an Zertifizierungsstellen, die Zertifizierungsverfahren
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Sterile Medizinprodukte Geltungsbereich: Diese Regeln legen Anforderungen fest an Zertifizierungsstellen, die Zertifizierungsverfahren
Anlage zur Akkreditierungsurkunde D-PL-11125-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-11125-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 02.05.2014 bis 26.04.2017 Ausstellungsdatum: 02.05.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-11125-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 02.05.2014 bis 26.04.2017 Ausstellungsdatum: 02.05.2014 Urkundeninhaber:
Regulative Aspekte der Aufbereitung chirurgischer Implantate
 Regulative Aspekte der Aufbereitung chirurgischer Implantate 35.Veranstaltung des Arbeitskreis Infektionsprophylaxe 16. Oktober 2012 in Potsdam 17.Oktober 2012 in Leipzig 1 Person Anja Fechner Dipl.-Ing.
Regulative Aspekte der Aufbereitung chirurgischer Implantate 35.Veranstaltung des Arbeitskreis Infektionsprophylaxe 16. Oktober 2012 in Potsdam 17.Oktober 2012 in Leipzig 1 Person Anja Fechner Dipl.-Ing.
Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels
 Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm der DGSV zur Einstufung
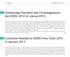 64 DGSV Zentralsterilisation 1/2013 Notwendige Korrektur des Flussdiagramms der DGSV 2012 im nuar 2013 In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm
64 DGSV Zentralsterilisation 1/2013 Notwendige Korrektur des Flussdiagramms der DGSV 2012 im nuar 2013 In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm
Die Deutsche Akkreditierungsstelle GmbH bestatigt hiermit, dass das PrOflaboratorium
 Akkreditierungsstelle Deutsche Akkreditierungsstelle GmbH Beliehene gemab 8 Absatz 1 AkkStelleG LV.m. 1 Absatz 1 AkkStelleGBV Unterzeichnerin der Multilateralen Abkommen von EA, ILAC und IAF zur gegenseitigen
Akkreditierungsstelle Deutsche Akkreditierungsstelle GmbH Beliehene gemab 8 Absatz 1 AkkStelleG LV.m. 1 Absatz 1 AkkStelleGBV Unterzeichnerin der Multilateralen Abkommen von EA, ILAC und IAF zur gegenseitigen
Softwarevalidierung aus Anwendersicht. DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009
 Softwarevalidierung aus Anwendersicht DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009 Softwarevalidierung aus Anwendersicht Geräte mit automatischen Prozessabläufen zur Aufbereitung von Medizinprodukten
Softwarevalidierung aus Anwendersicht DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009 Softwarevalidierung aus Anwendersicht Geräte mit automatischen Prozessabläufen zur Aufbereitung von Medizinprodukten
(Text von Bedeutung für den EWR) 9.8.2007 7.7.2010 9.10.1999. EN 12322:1999/A1:2001 31.7.2002 Anmerkung 3 Datum abgelaufen (30.4.2002) 19.8.
 C 22/30 Amtsblatt der Europäischen Union 24.1.2013 Mitteilung der Kommission im Rahmen der Durchführung der Richtlinie 98/79/EG des Europäischen Parlaments und des Rates vom 27. Oktober 1998 über In-vitro-Diagnostika
C 22/30 Amtsblatt der Europäischen Union 24.1.2013 Mitteilung der Kommission im Rahmen der Durchführung der Richtlinie 98/79/EG des Europäischen Parlaments und des Rates vom 27. Oktober 1998 über In-vitro-Diagnostika
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ)
 Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
OP- Hygiene, Desinfektion und Sterilisation
 OP- Hygiene, Desinfektion und Sterilisation Studenten-Vorlesung, Bochum, 8. Juni 2010 Prof. Dr. Walter Popp Krankenhaushygiene Universitätsklinikum Essen Hufelandstr. 55, 45122 Essen Tel. 0201-723-4577
OP- Hygiene, Desinfektion und Sterilisation Studenten-Vorlesung, Bochum, 8. Juni 2010 Prof. Dr. Walter Popp Krankenhaushygiene Universitätsklinikum Essen Hufelandstr. 55, 45122 Essen Tel. 0201-723-4577
NORMEN Wunschvorstellung und Realität Ein Blick hinter die Kulissen
 NORMEN Wunschvorstellung und Realität Ein Blick hinter die Kulissen Mag. Dr. Tillo Miorini Institut für angewandte Hygiene ÖGSV Wozu Normen? Normen sollen den Stand der Technik repräsentieren Definieren
NORMEN Wunschvorstellung und Realität Ein Blick hinter die Kulissen Mag. Dr. Tillo Miorini Institut für angewandte Hygiene ÖGSV Wozu Normen? Normen sollen den Stand der Technik repräsentieren Definieren
Übersicht. Normung von Software in der Medizin. Vorstellung der DKE. Vorstellung der Normungsgremien. Normen im Bereich Software.
 Normung von Software in der Medizin Übersicht Vorstellung der DKE Vorstellung der Normungsgremien Normen im Bereich Software Zukunftstrends 20.09.2013/1 Vorstellung der DKE Gemeinnütziger Verband ohne
Normung von Software in der Medizin Übersicht Vorstellung der DKE Vorstellung der Normungsgremien Normen im Bereich Software Zukunftstrends 20.09.2013/1 Vorstellung der DKE Gemeinnütziger Verband ohne
Umsetzung der Hygienerichtlinien
 Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
Leitlinie zur Validierung maschineller Reinigungs- Desinfektionsprozesse. Aufbereitung thermolabiler Endoskope. supplement 3
 D 2596 F 19. Jahrgang 2011 3 supplement 3 Leitlinie zur Validierung maschineller Reinigungs- Desinfektionsprozesse zur Aufbereitung thermolabiler Endoskope D e u t s c h e G e s e l l s c h a f t f ü r
D 2596 F 19. Jahrgang 2011 3 supplement 3 Leitlinie zur Validierung maschineller Reinigungs- Desinfektionsprozesse zur Aufbereitung thermolabiler Endoskope D e u t s c h e G e s e l l s c h a f t f ü r
Anlage zur Akkreditierungsurkunde D-PL-15018-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-15018-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 26.11.2015 bis 25.11.2020 Ausstellungsdatum: 26.11.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-15018-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 26.11.2015 bis 25.11.2020 Ausstellungsdatum: 26.11.2015 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ZM-16007-01-00 nach DIN EN ISO/IEC 17021:2011
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZM-16007-01-00 nach DIN EN ISO/IEC 17021:2011 Gültigkeitsdauer: 02.06.2016 bis 14.10.2018 Ausstellungsdatum: 02.06.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZM-16007-01-00 nach DIN EN ISO/IEC 17021:2011 Gültigkeitsdauer: 02.06.2016 bis 14.10.2018 Ausstellungsdatum: 02.06.2016 Urkundeninhaber:
Prof. Dr. Reinier Mutters Institut für Medizinische Mikrobiologie und Hygiene Philipps-Universität Marburg Universitätsklinikum Gießen und Marburg
 Prof. Dr. Reinier Mutters Institut für Medizinische Mikrobiologie und Hygiene Philipps-Universität Marburg Universitätsklinikum Gießen und Marburg GmbH Bett ist eine der direkten Kontaktflächen kontaminiert
Prof. Dr. Reinier Mutters Institut für Medizinische Mikrobiologie und Hygiene Philipps-Universität Marburg Universitätsklinikum Gießen und Marburg GmbH Bett ist eine der direkten Kontaktflächen kontaminiert
Technische Normen für Medizinprodukte
 Medizinprodukteverordnung (MepV) Technische Normen für Medizinprodukte Gestützt auf Artikel 4 Absatz 3 der Medizinprodukteverordnung vom 17. Oktober 2001 (MepV) 1 werden die im Anhang aufgeführten technischen
Medizinprodukteverordnung (MepV) Technische Normen für Medizinprodukte Gestützt auf Artikel 4 Absatz 3 der Medizinprodukteverordnung vom 17. Oktober 2001 (MepV) 1 werden die im Anhang aufgeführten technischen
ViFlow Prozessnetz als QM Handbuch in elektronischer Form
 ViFlow Prozessnetz als QM Handbuch in elektronischer Form Verpflichtung zur Qualitätssicherung 135a SGB V regelt die Verpflichtung zur Qualitätssicherung im Gesundheitswesen. Die Leistungserbringer sind
ViFlow Prozessnetz als QM Handbuch in elektronischer Form Verpflichtung zur Qualitätssicherung 135a SGB V regelt die Verpflichtung zur Qualitätssicherung im Gesundheitswesen. Die Leistungserbringer sind
ZSVA. gestern, heute, morgen
 ZSVA gestern, heute, morgen Folgen des Haarschnittes Zentralisierung der Instrumentenaufbereitung Neuer Namen Zentrale Sterilgutversorgungsabteilung ZSVA Lange Aufbereitungszeiten durch! Maschinenlaufzeiten
ZSVA gestern, heute, morgen Folgen des Haarschnittes Zentralisierung der Instrumentenaufbereitung Neuer Namen Zentrale Sterilgutversorgungsabteilung ZSVA Lange Aufbereitungszeiten durch! Maschinenlaufzeiten
Anforderungen an die Hygiene in der Zahnmedizin
 Fortbildungsveranstaltung 2005 für den Öffentlichen Gesundheitsdienst Anforderungen an die Hygiene in der Zahnmedizin Prof. Dr. Jürgen Becker Poliklinik für Zahnärztliche Chirurgie und Aufnahme Westdeutsche
Fortbildungsveranstaltung 2005 für den Öffentlichen Gesundheitsdienst Anforderungen an die Hygiene in der Zahnmedizin Prof. Dr. Jürgen Becker Poliklinik für Zahnärztliche Chirurgie und Aufnahme Westdeutsche
Gutachtenliste. Mikrobiologie
 Mikrobiologie MB 1 Bakterien und Pilze 09/84 Untersuchungen zur bakteriziden und fungiziden Wirk samkeit von Dr.U. Eigener, H. Nolte, S&M MB 2 Bakterien und Pilze Kurzzeit 06/85 Untersuchungen zur bakteriziden
Mikrobiologie MB 1 Bakterien und Pilze 09/84 Untersuchungen zur bakteriziden und fungiziden Wirk samkeit von Dr.U. Eigener, H. Nolte, S&M MB 2 Bakterien und Pilze Kurzzeit 06/85 Untersuchungen zur bakteriziden
Neueste Entwicklungen in der Wiederaufbereitung von Medizinprodukten
 Neueste Entwicklungen in der Wiederaufbereitung von Medizinprodukten Freiburg, 11. Juni 2008 Andreas Schneider Steris AG, Pieterlen European Marketing Manager ZSVA Um was geht es?? Neuste Entwicklung bei
Neueste Entwicklungen in der Wiederaufbereitung von Medizinprodukten Freiburg, 11. Juni 2008 Andreas Schneider Steris AG, Pieterlen European Marketing Manager ZSVA Um was geht es?? Neuste Entwicklung bei
biosanitizer der neue umweltfreundliche Desinfektionsreiniger auf Wasserbasis
 biosanitizer der neue umweltfreundliche Desinfektionsreiniger auf Wasserbasis Umweltfreundliche Zusammensetzung, zerfällt in Wasser und Sauerstoff alkoholfrei, VOC-, quat-, aldehyd- und phenolfrei ohne
biosanitizer der neue umweltfreundliche Desinfektionsreiniger auf Wasserbasis Umweltfreundliche Zusammensetzung, zerfällt in Wasser und Sauerstoff alkoholfrei, VOC-, quat-, aldehyd- und phenolfrei ohne
Mitteilung der Kommission im Rahmen der Durchführung der Richtlinie 93/42/EWG des Rates vom 14. Juni 1993 über Medizinprodukte
 16.5.2014 DE Amtsblatt der Europäischen Union C 149/3 Mitteilung der Kommission im Rahmen der Durchführung der Richtlinie 93/42/EWG des Rates vom 14. Juni 1993 über Medizinprodukte (Veröffentlichung der
16.5.2014 DE Amtsblatt der Europäischen Union C 149/3 Mitteilung der Kommission im Rahmen der Durchführung der Richtlinie 93/42/EWG des Rates vom 14. Juni 1993 über Medizinprodukte (Veröffentlichung der
Hygiene im Sanitärbereich im Gesundheitswesen
 Hygiene im Sanitärbereich im Gesundheitswesen Vortrag im Rahmen der Themenreihe Wohlfühlraum Patientenzimmer, KALDEWEI Creative Care Day am 6. Mai 2015 in Ahlen Mehr wissen. Weiter denken. Übersicht Rechtliche
Hygiene im Sanitärbereich im Gesundheitswesen Vortrag im Rahmen der Themenreihe Wohlfühlraum Patientenzimmer, KALDEWEI Creative Care Day am 6. Mai 2015 in Ahlen Mehr wissen. Weiter denken. Übersicht Rechtliche
Termine Nord. Lehrgang Fachkunde 1-1: 1. Woche 19.01. - 23.01.2015 2. Woche 26.01. - 30.01.2015 3. Woche 09.02. - 13.02.2015
 MMM Akademie Nord Termine Nord HH-Barmbek Lehrgang Fachkunde 1-1: 1. Woche 19.01. - 23.01.2015 2. Woche 26.01. - 30.01.2015 3. Woche 09.02. - 13.02.2015 Neu MMM Akademie Nord MMM Akademie Süd Informationen
MMM Akademie Nord Termine Nord HH-Barmbek Lehrgang Fachkunde 1-1: 1. Woche 19.01. - 23.01.2015 2. Woche 26.01. - 30.01.2015 3. Woche 09.02. - 13.02.2015 Neu MMM Akademie Nord MMM Akademie Süd Informationen
Texcare Forum 2014 Forum für moderne Textilpflege
 Texcare Forum 2014 Forum für moderne Textilpflege Aktuelle Entwicklungen in der Wäschereihygiene Dr. Manuel Heintz Kap Europa, November 2014 Revision der EN 14065 Europäischer Standard Das primäre Ziel
Texcare Forum 2014 Forum für moderne Textilpflege Aktuelle Entwicklungen in der Wäschereihygiene Dr. Manuel Heintz Kap Europa, November 2014 Revision der EN 14065 Europäischer Standard Das primäre Ziel
Medizin. Reinigung, Desinfektion, Prionen-Inaktivierung. neodisher der multifunktionelle Reiniger
 Medizin Reinigung, Desinfektion, Prionen-Inaktivierung neodisher der multifunktionelle Reiniger Steigende Anforderungen an Qualität und Sicherheit Neue Herausforderungen wie z.b. Prionen als Erreger von
Medizin Reinigung, Desinfektion, Prionen-Inaktivierung neodisher der multifunktionelle Reiniger Steigende Anforderungen an Qualität und Sicherheit Neue Herausforderungen wie z.b. Prionen als Erreger von
Bekanntmachungen der Departemente und der Ämter
 Bekanntmachungen der Departemente und der Ämter Technische Normen für Medizinprodukte Medizinprodukteverordnung (MepV) vom 19. Oktober 1999 Gestützt auf Artikel 4 Absatz 3 der Medizinprodukteverordnung
Bekanntmachungen der Departemente und der Ämter Technische Normen für Medizinprodukte Medizinprodukteverordnung (MepV) vom 19. Oktober 1999 Gestützt auf Artikel 4 Absatz 3 der Medizinprodukteverordnung
Leitfaden zu Gewinnung, Lagerung und Transport von Hygieneproben
 Leitfaden zu Gewinnung, Lagerung und Transport von Hygieneproben medizinisch chemisches Labor Dr. Mustafa, Dr. Richter OG Abteilung für Hygiene 5020 Salzburg, Bergstraße 14 tel: 0662 2205 fax: 0662 2205-421
Leitfaden zu Gewinnung, Lagerung und Transport von Hygieneproben medizinisch chemisches Labor Dr. Mustafa, Dr. Richter OG Abteilung für Hygiene 5020 Salzburg, Bergstraße 14 tel: 0662 2205 fax: 0662 2205-421
Anlage zur Akkreditierungsurkunde D ZE 12007 01 06
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ZE 12007 01 06 nach DIN EN ISO/IEC 17065:2013 Gültigkeitsdauer: 06.05.2014 bis 05.05.2019 Ausstellungsdatum: 06.05.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ZE 12007 01 06 nach DIN EN ISO/IEC 17065:2013 Gültigkeitsdauer: 06.05.2014 bis 05.05.2019 Ausstellungsdatum: 06.05.2014 Urkundeninhaber:
institut Im Dienste der Wirtschaft
 institut Im Dienste der Wirtschaft Das wfk - Institut für Angewandte Forschung erbringt Dienstleistungen in den Bereichen der anwendungstechnischen Prüfungen und Ana ly sen von Wasch-, Reinigungs- und
institut Im Dienste der Wirtschaft Das wfk - Institut für Angewandte Forschung erbringt Dienstleistungen in den Bereichen der anwendungstechnischen Prüfungen und Ana ly sen von Wasch-, Reinigungs- und
Prüfbericht. Bestimmung der mikrobioziden Inaktivierungsleistung des DIOSOL-Verfahrens im quantitativen Suspensionsversuch mit praxisnahen Keimträgern
 Universitätsmedizin Göttingen Abteilung Medizinische Mikrobiologie Akkreditiertes Trinkwasser- und Hygienelabor Dr.med. Dipl.-Chem. Dipl.-Ing.(FH) Ulrich Schmelz Ärztl. Leiter des akkred. Labors www.hygiene-goettingen.de
Universitätsmedizin Göttingen Abteilung Medizinische Mikrobiologie Akkreditiertes Trinkwasser- und Hygienelabor Dr.med. Dipl.-Chem. Dipl.-Ing.(FH) Ulrich Schmelz Ärztl. Leiter des akkred. Labors www.hygiene-goettingen.de
Sterilisatoren für medizinische Zwecke Niedertemperatur-Dampf-Formaldehyd- Sterilisatoren Anforderungen und Prüfung
 ÖNORM EN 14180 Ausgabe: 2014-09-15 Sterilisatoren für medizinische Zwecke Niedertemperatur-Dampf-Formaldehyd- Sterilisatoren Anforderungen und Prüfung Sterilizers for medical purposes Low temperature steam
ÖNORM EN 14180 Ausgabe: 2014-09-15 Sterilisatoren für medizinische Zwecke Niedertemperatur-Dampf-Formaldehyd- Sterilisatoren Anforderungen und Prüfung Sterilizers for medical purposes Low temperature steam
Synopse der eingegangenen Stellungnahmen durch das Sekretariat der KRINKO und das BfArM
 Synopse der eingegangenen Stellungnahmen durch das Sekretariat der KRINKO und das BfArM (Bericht an die KRINKO 2008) Verschiedene Kreise stellen zum Teil konträre Forderungen, wie z.b. die Forderung nach
Synopse der eingegangenen Stellungnahmen durch das Sekretariat der KRINKO und das BfArM (Bericht an die KRINKO 2008) Verschiedene Kreise stellen zum Teil konträre Forderungen, wie z.b. die Forderung nach
Akkreditierungsumfang der Prüfstelle (ISO/IEC 17025) Amt der Tiroler Landesregierung, Chemisch-technische Umweltschutzanstalt / (Ident.Nr.
 Amt der Tiroler Landesregierung, Chemisch-technische Umweltschutzanstalt / (Ident.: 0100) Titel 1 BGBl. II 292/2001 2001-08 Verordnung des Bundesministers für Land- und Forstwirtschaft, Umwelt und Wasserwirtschaft
Amt der Tiroler Landesregierung, Chemisch-technische Umweltschutzanstalt / (Ident.: 0100) Titel 1 BGBl. II 292/2001 2001-08 Verordnung des Bundesministers für Land- und Forstwirtschaft, Umwelt und Wasserwirtschaft
Inhaltsverzeichnis Medizinprodukte in Europa Online (die Normen der Pakete sind hier nicht enthalten)
 Medizinprodukte in Europa Online www.medizinprodukte-europa.de Inhaltsverzeichnis Medizinprodukte in Europa Online (die Normen der Pakete sind hier nicht enthalten) DIN EN 285 2009-08 DIN EN 455-1 2001-01
Medizinprodukte in Europa Online www.medizinprodukte-europa.de Inhaltsverzeichnis Medizinprodukte in Europa Online (die Normen der Pakete sind hier nicht enthalten) DIN EN 285 2009-08 DIN EN 455-1 2001-01
Anlage zur Akkreditierungsurkunde D-PL-14549-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14549-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 07.08.2014 bis 21.08.2016 Ausstellungsdatum: 07.08.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14549-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 07.08.2014 bis 21.08.2016 Ausstellungsdatum: 07.08.2014 Urkundeninhaber:
MPG und VO zum 94. N. Buchrieser
 MPG und VO zum 94 N. Buchrieser Gesetze und Regelwerke EU-Direktive 93/42/EWG Medizinproduktegesetz Verordnung zum 94 MPG (ÖGSV-LL 11) RDG-Normen (ÖNORM EN ISO 15883 Teil 1-7) Sterilisatornormen (EN 285,
MPG und VO zum 94 N. Buchrieser Gesetze und Regelwerke EU-Direktive 93/42/EWG Medizinproduktegesetz Verordnung zum 94 MPG (ÖGSV-LL 11) RDG-Normen (ÖNORM EN ISO 15883 Teil 1-7) Sterilisatornormen (EN 285,
Infektionsgefahren im Einsatzdienst. Prof. Dr. Walter Popp, Krankenhaushygiene, Universitätsklinikum Essen Jörg Spors, Berufsfeuerwehr Essen
 Infektionsgefahren im Einsatzdienst Prof. Dr. Walter Popp, Krankenhaushygiene, Universitätsklinikum Essen Jörg Spors, Berufsfeuerwehr Essen 1 Themen Einige Zahlen RKI-Empfehlungen zur Reinigung und Desinfektion
Infektionsgefahren im Einsatzdienst Prof. Dr. Walter Popp, Krankenhaushygiene, Universitätsklinikum Essen Jörg Spors, Berufsfeuerwehr Essen 1 Themen Einige Zahlen RKI-Empfehlungen zur Reinigung und Desinfektion
Zertifizierungsstellen für Qualitätsmanagementsysteme
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 15.08.2009 Hinweis:
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 15.08.2009 Hinweis:
UV-Desinfektion von Ultraschallköpfen: Praxistestung
 UV-Desinfektion von Ultraschallköpfen: Praxistestung Priv. Doz. Dr. Magda Diab-El Schahawi Universitätsklinik für Krankenhaushygiene und Infektionskontrolle Med Uni Wien Literatur zu mangelnder Aufbereitung
UV-Desinfektion von Ultraschallköpfen: Praxistestung Priv. Doz. Dr. Magda Diab-El Schahawi Universitätsklinik für Krankenhaushygiene und Infektionskontrolle Med Uni Wien Literatur zu mangelnder Aufbereitung
Hygiene/Gesundheit: Notwendigkeit von Desinfektionsmaßnahmen auch in der Prophylaxe
 Hygiene/Gesundheit: Notwendigkeit von Desinfektionsmaßnahmen auch in der Prophylaxe Cornelia Wegemund Desinfektions- und Reinigungsmittel IHO-Mitglied Hygieneschulung Pflege 1 Warum Hygiene? Warum Desinfektion?
Hygiene/Gesundheit: Notwendigkeit von Desinfektionsmaßnahmen auch in der Prophylaxe Cornelia Wegemund Desinfektions- und Reinigungsmittel IHO-Mitglied Hygieneschulung Pflege 1 Warum Hygiene? Warum Desinfektion?
Grundlagen der Desinfektion und Sterilisation
 Grundlagen der Desinfektion und Sterilisation Desinfektion, Sterilisation: Ziele Arbeitssicherheit und Gesundheitsschutz Umweltsicherheit Produktesicherheit Merke: Es gibt kein universelles Sterilisationsverfahren.
Grundlagen der Desinfektion und Sterilisation Desinfektion, Sterilisation: Ziele Arbeitssicherheit und Gesundheitsschutz Umweltsicherheit Produktesicherheit Merke: Es gibt kein universelles Sterilisationsverfahren.
Mindestinhalte von Validierungsberichten für Peroxid/ Peroxid-Plasma-Sterilisationsverfahren für Medizinprodukte
 Antworten und Beschlüsse des HAK Reinigung, Desinfektion u. Sterilisation Sterilisation RDS 004 Mindestinhalte von Validierungsberichten für Peroxid/ Peroxid-Plasma-Sterilisationsverfahren für Medizinprodukte
Antworten und Beschlüsse des HAK Reinigung, Desinfektion u. Sterilisation Sterilisation RDS 004 Mindestinhalte von Validierungsberichten für Peroxid/ Peroxid-Plasma-Sterilisationsverfahren für Medizinprodukte
Hygiene im Alltag. Massnahmen bei Patienten mit cystischer Fibrose (CF)
 Hygiene im Alltag Massnahmen bei Patienten mit cystischer Fibrose (CF) Luzia Vetter, Rolf Kuhn Spitalhygiene LUKS 1 0 2 Bakterien - Pseudomonas aeruginosa - Burkholderia cepacia - Staphylococcus aureus
Hygiene im Alltag Massnahmen bei Patienten mit cystischer Fibrose (CF) Luzia Vetter, Rolf Kuhn Spitalhygiene LUKS 1 0 2 Bakterien - Pseudomonas aeruginosa - Burkholderia cepacia - Staphylococcus aureus
Übersicht über die Updates von Medizinprodukte in Europa
 Medizinprodukte in Europa Online www.medizinprodukte-europa.de Übersicht über die Updates von Medizinprodukte in Europa Update Mai 2016 98/79/EG ersetzt durch 98/79/EG 2016-05 DIN 58953-1*) 2010-05 entnommen
Medizinprodukte in Europa Online www.medizinprodukte-europa.de Übersicht über die Updates von Medizinprodukte in Europa Update Mai 2016 98/79/EG ersetzt durch 98/79/EG 2016-05 DIN 58953-1*) 2010-05 entnommen
Zertifizierungsstellen für Qualitätsmanagementsysteme
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 30.12.2009 Hinweis:
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 30.12.2009 Hinweis:
Kassenärztliche Vereinigung Sachsen-Anhalt Abteilung Qualitätssicherung und management Doctor-Eisenbart-Ring 2 39120 Magdeburg
 Ansprechpartner: Anke Schmidt Tel.: 0391 627-6453 Christin Richter Tel.: 0391 627-7454 oder per E-Mail: Hygiene@kvsa.de Anschaffung eines Reinigungs- und Desinfektionsgerätes (RDG) Reinigungs- und Desinfektionsgeräte
Ansprechpartner: Anke Schmidt Tel.: 0391 627-6453 Christin Richter Tel.: 0391 627-7454 oder per E-Mail: Hygiene@kvsa.de Anschaffung eines Reinigungs- und Desinfektionsgerätes (RDG) Reinigungs- und Desinfektionsgeräte
DGSV-Kongress 2014. Einbau eines validierten RDG-E Programms in ein RDG zur Aufbereitung thermolabiler MP. 18 Jahre DGSV: vom 8. bis 10.
 Einbau eines validierten RDG-E Programms in ein RDG zur Aufbereitung thermolabiler MP DGSV-Kongress 2014 vom 8. bis 10. Oktober 2014 18 Jahre DGSV: Volljährig und verantwortungsbewusst Bruno Amann 1 1.
Einbau eines validierten RDG-E Programms in ein RDG zur Aufbereitung thermolabiler MP DGSV-Kongress 2014 vom 8. bis 10. Oktober 2014 18 Jahre DGSV: Volljährig und verantwortungsbewusst Bruno Amann 1 1.
Gesetzliche Grundlagen für die Wiederaufbereitung von Medizinprodukten
 Gesetzliche Grundlagen für die Wiederaufbereitung von Medizinprodukten Markus Weiss Inspektor Swissmedic, Abteilung Medizinprodukte Hallerstrasse 7 3000 Bern 9 markus.weiss@swissmedic.ch www.swissmedic.ch/md.asp
Gesetzliche Grundlagen für die Wiederaufbereitung von Medizinprodukten Markus Weiss Inspektor Swissmedic, Abteilung Medizinprodukte Hallerstrasse 7 3000 Bern 9 markus.weiss@swissmedic.ch www.swissmedic.ch/md.asp
Patienten- und Personalschutz
 Patienten- und Personalschutz Produktübersicht 01/13 Isolator-Plus Maske FFP 2 Mund-Nasenschutz mit hoher Filterleistung Schutzstufe FFP 2 (z.b. bei TBC oder Influenza) Best.-Nr.: 8002 Verkaufseinheit:
Patienten- und Personalschutz Produktübersicht 01/13 Isolator-Plus Maske FFP 2 Mund-Nasenschutz mit hoher Filterleistung Schutzstufe FFP 2 (z.b. bei TBC oder Influenza) Best.-Nr.: 8002 Verkaufseinheit:
Antimikrobielle Produkte im Haushalt eine Betrachtung zu Auswirkungen auf Gesundheit und Umwelt sowie zum Nutzen für den Anwender
 Schlüsselwörter Desinfektion Biozidprodukte Biozidzulassung Desinfektionsmittel Häusliches Umfeld Haushalt Resistenz Keywords Disinfection Biocidal products Biocidal product authorisation Disinfectants
Schlüsselwörter Desinfektion Biozidprodukte Biozidzulassung Desinfektionsmittel Häusliches Umfeld Haushalt Resistenz Keywords Disinfection Biocidal products Biocidal product authorisation Disinfectants
Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien STERILGUTVERSORGUNG
 Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien 18 Stand: 16.03.2016 STERILGUTVERSORGUNG Die internationale Normenreihe ÖNORM EN
Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien 18 Stand: 16.03.2016 STERILGUTVERSORGUNG Die internationale Normenreihe ÖNORM EN
Abschnitt 1 Anwendungsbereich und Allgemeine Anforderungen an die Konformitätsbewertung 1 Anwendungsbereich
 13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
Wo liegt der Hygienelevel höher? OP Pharmaindustrie
 Wo liegt der Hygienelevel höher? OP Pharmaindustrie HFK Petra Dorfner HFK Susanna Grabmayer Wo liegt der Hygienelevel höher? Ziel Vorgaben Anforderungen Kontrollmöglichkeiten Gemeinsamkeiten/Unterschiede
Wo liegt der Hygienelevel höher? OP Pharmaindustrie HFK Petra Dorfner HFK Susanna Grabmayer Wo liegt der Hygienelevel höher? Ziel Vorgaben Anforderungen Kontrollmöglichkeiten Gemeinsamkeiten/Unterschiede
Medizinprodukte-Sicherheitsplanverordnung
 Hygieneforum Sande 19.06.2014 Meldung von Vorkommnissen nach der Medizinproduke-Sicherheitsplanverordnung www.klinikum-bremen-ldw.de Klinikum Links der Weser Senator-Weßling-Str. 1 28277 Bremen Meldung
Hygieneforum Sande 19.06.2014 Meldung von Vorkommnissen nach der Medizinproduke-Sicherheitsplanverordnung www.klinikum-bremen-ldw.de Klinikum Links der Weser Senator-Weßling-Str. 1 28277 Bremen Meldung
Anlage zur Akkreditierungsurkunde D-PL-13451-01-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13451-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 25.09.2013 bis 01.07.2017 Ausstellungsdatum: 25.09.2013 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13451-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 25.09.2013 bis 01.07.2017 Ausstellungsdatum: 25.09.2013 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-PL-11267-04-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-11267-04-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 17.02.2015 bis 18.03.2017 Ausstellungsdatum: 24.04.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-11267-04-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 17.02.2015 bis 18.03.2017 Ausstellungsdatum: 24.04.2015 Urkundeninhaber:
ZSVA & ISO 13485 (9001:2008) Anforderungen und Praxislösungen in der ZSVA
 & ISO 13485 (9001:2008) Anforderungen und Praxislösungen in der Iljias Mislimi Zentrale Sterilgutversorgungsabteilung () Diakonie-Klinikum Schwäbisch Hall ggmbh Oktober 2014 & ISO 13485 (9001:2008) Anforderungen
& ISO 13485 (9001:2008) Anforderungen und Praxislösungen in der Iljias Mislimi Zentrale Sterilgutversorgungsabteilung () Diakonie-Klinikum Schwäbisch Hall ggmbh Oktober 2014 & ISO 13485 (9001:2008) Anforderungen
