Amphiphile Moleküle vereinen zwei inkompatible Molekülteile mit unterschiedlicher Löslichkeit (meist: hydrophil + hydrophob)
|
|
|
- Florian Kappel
- vor 5 Jahren
- Abrufe
Transkript
1 3. Amhihile 3.1. Allgemeines Amhihile Moleküle vereinen zwei inkomatible Molekülteile mit unterschiedlicher Löslichkeit (meist: hydrohil + hydrohob) Tenside, Detergentien, surfactant, Liide, Blockcoolymere,... Charakteristisch: Anreicherung an der Grenzfläche + herabsetzen der Oberflächensannung Bildung von Mizellen und Mesohasen
2 3.2. Amhihile Moleküle (hydrohob + hydrohil) Ionische Tenside (anionisch, kationisch) Zwitterionische Tenside Amhotere Tenside Nichtionische Tenside Liide Blockcoolymere Proteine
3 3.3. Grenzflächen - / Oberflächensaktivität Oberflächensannung Moleküle an Oberflächen haben eine geringere Anzahl an Nachbarn! Amhihile reichern sich an der Grenzfläche zur Luft an und setzen die Oberflächensannung herab! Kann man dies quantifizieren? Charakteristische Funktionen hängen auch von der Oberfläche A ab! dg = G T,A dt + G T,A d + G A,T da + G n i,t,a dn i dg = SdT +Vd +??da + µ i dn i
4 Oberflächensannung ( G/ A),T beschreibt die Eigenschaften einer 2D-Schicht [Nm/m 2 oder N/m] In 3D: N/m 2 = Sannung! Oberflächensannung g Energie, die man aufwenden muss, um in einem isothermen und isobaren Prozess neue Oberfläche zu erzeugen! G A,T = γ d.h.: dg = SdT +Vd +γda + µ i dn i
5 Oberflächensannung Bs: g [Nm -1 ] (Oberflächensannung) Wasser 7.275*10-2 Methanol 2.26*10-2 Benzol 2.888*10-2 Quecksilber 47.2*10-2 Wechselwirkungen der Moleküle /Atome beeinflussen stark die Oberflächensannung! (z.b. H-Brücken, Metall mit dislokalisierten Elektronen,...) Die Oberflächensannung g ist die artielle Ableitung der freien Enthalie G nach der Fläche A ( und T konstant!)
6 Wo wirkt sich die Oberflächensannung g aus? Blasen, Hohlräume, Trofen Hohlräume in einer Flüssigkeit befinden sich im Gleichgewicht, wenn die Tendenz der Oberfläche sich zu verkleinern, durch einen Überdruck im Innern des Hohlraumes komensiert wird. Kraft nach aussen: Kraft nach innen: 4πr 2 i 4πr 2 a Energie der Oberfläche A des Hohlraumes : Aγ 4πr 2 γ Vergrösserung des Radius um dr, erfordert die Kraft: Im Gleichgewicht: 4πr 2 i = 4πr 2 a + 8πγr d( Aγ) dr = 8πrγ i = a + 2γ r Lalace- Gleichung!
7 Damfdruck kleiner, kugelförmiger Teilchen (Tröfchen) Betrachte: Geschlossenes System, das aus kleinen, flüssigen Tröfchen (flüssige Phase a) und Damf (Phase b) besteht! Wenn,T = const., lautet die Gleichgewichtsbedingung: dg,t = µ β dn β + µ α dn α + γda = 0 Die Aenderung der Stoffmenge in Damf und Flüssigkeit sind abhängig in einem geschlossenen System: dn β = dn α & µ β = µ α + γ A ) ( + ' n α *,T Chem. Potential Damf Chem. Potential Flüssigkeit
8 Damfdruck kleiner, kugelförmiger Teilchen (Tröfchen) Die Flüssigkeit besteht aus z gleich grossen, kugelförmigen Tröfchen (mit Radius r!) Oberfläche der flüssigen Phase: Volumen der flüssigen Phase A = z 4πr 2 n α V α = z 4 3 πr3 A = 3nα V α r n a : Molzahl oder Stoffmenge Flüssigkeit V a : Molvolumen Flüssigkeit $ A ' & ) % n α ( T, = 3V α r 3nα V α r 2 $ r ' & ) % n α ( z Da n α = z 4 $ n α ' V α 3 πr3 ist & ) % r ( z = z V α 4πr2 = 3nα r
9 Damfdruck kleiner, kugelförmiger Teilchen (Tröfchen) Damit: $ A ' & ) % n α ( T, = 3V α r 3nα V α r 2 r 3n α = 2V α r µ β = µ α + 2γV α r µ a : chemisches Potential der Flüssigkeit, bei normalem, nicht durch Teilchengrösse beeinflusstem Druck r=oo µ b : chemisches Potential des Damfes, bezogen auf den Damfdruck r der kleinen Trofen (Druckabhängigkeit des chemischen Potentials: µ i = µ 0 i + RT ln ) 0 D.h. hier: µ β = µ α + RT ln r r= Vergleich: µ β = µ α + 2γV α r RT ln r = 2γV α r= r
10 d.h.: Damfdruck kleiner, kugelförmiger Teilchen (Tröfchen) & r = r= ex 2γV α ) ' * ( rrt + Kelvin-Gleichung! kleine Tröfchen mit Radius r stehen unter erhöhtem Druck haben auch höheren Damfdruck! Bs.: Damfdruck flüssiger Tröfchen, mit Radius r = 10-6 cm g [10-3 Nm -1 ] V a [10-6 m 3 mol -1 ] r / r=oo Hg ,8 1,78 H 2 O 72,75 18,0 1,11 Benzol 23,4 88,9 1,23 Et 2 O 17,0 103,9 1,18
11 Kaillarkräfte Flüssigkeiten haben die Tendenz in engen Kaillaren emor zu steigen Kaillarwirkung als Folge der Oberflächensannung Bs: Glaskaillare in Wasser 2 r h 2γ r Druck, den eine Flüssigkeit der Dichte r und der Höhe h ausübt: = πr2 hρg πr 2 = ρgh = 2γ r h = 2γ ρgr r: Dichte der Flüssigkeit g= 9.81 ms -2 Erdbeschleunigung
12 Flüssigkeit in Kontakt mit Festkörer: 3 Grenzflächensannungen müssen berücksichtigt werden! gas flüssig g lv q s: solid l: liquid v:,vaour fest g sl g sv q: Kontaktwinkel Gleichgewicht der Fläche: γ sl +γ lv cosθ = γ sv cosθ = γ sv γ sl γ lv z.b. cosq > 1: vollständige Benetzung cosq < -1: keine Benetzung
13 Benetzung einer rauhen Oberfläche A A rauh A = r ( 1) A rauh r: Rauhigkeit A: Projektion auf eine glatte Fläche rγ sl +γ lv cosθ rauh = rγ sv cosθ rauh = r γ sv γ sl γ lv = r cosθ glatt Bs.: q glatt = 60 und r = 2 q rauh = 0 (vollständige Benetzung!) q glatt = 100 und r = 5 q rauh = 150 Rauhigkeit macht hydrohile Oberflächen hydrohiler und hydrohobe Oberflächen hydrohober!
14 Thermodynamik der Grenzflächen in Mehrstoffsystemen Es mögen 2 Phasen (a und b) aneinandergrenzen! Physikalische Eigenschaften innerhalb einer Phase sollen sich nicht srunghaft ändern. Aber: Grenzflächenschichten haben andere Eigenschaften als das Innere der Phasen! Phase a A S B Grenzflächenhase g Phase b A S B Begrenzungsebenen: AA und BB! Abstand der Ebenen: einige Moleküldurchmesser (ca cm!) Innerhalb der Grenzschicht ändern sich die Eigenschaften kontinuierlich von denen der Phase a zu denen der Phase b! Ebene SS: Grenzflächenhase g
15 Thermodynamik der Grenzflächen in Mehrstoffsystemen Annahme: Zusammensetzung der homogenen Phasen a und b soll bis zur Grenzfläche SS konstant sein! Stoffmenge n ig in der Grenzflächenhase g n ig = n i (n ia + n ib ) mit n i : Stoffmenge der Komonente i im gesamten System n ia ( n ib ) : Stoffmenge der Komonente i in Phase a (Phase b) n ia und n ib berechnet man aus analytisch bestimmbaren Volumenkonzentrationen c ia oder c ib, multiliziert mit den Volumen V a bzw. V b (. z.b.: n ia = c ia * V a ) Die Konzentration zwischen AA und BB ist zunächst unbekannt! Willkürlich werden V a und V b bis SS gerechnet, d.h. im Bereich AA-SS gilt die Konzentration c ia und im Bereich BB-SS die Konzentration c ib :
16 Thermodynamik der Grenzflächen in Mehrstoffsystemen Hat sich die Komonente i in der Grenzschicht angereichert, so erhält man mit (n ia + n ib ) eine zu kleine Stoffmenge : n ig > 0 Ist die Grenzfläche an i verarmt, so ist das berechnete (n ia + n ib ) zu gross: n ig < 0! Die Konzentrationen in den Phasen a und b sind durch n ia /V ia und n ib /V ib gegeben [mol/l] Konzentrationsangabe in der zweidimensionalen Grenzflächenhase A: Γ i n γ i A Die Grenzflächenkonzentration G i ist eine Flächenkonzentration! Sie kann, je nach dem Vorzeichen von n ig ositiv oder negativ sein, gibt also an, ob die Grenzflächenhase bezüglich der Komonente i gegenüber einer der Phasen a oder b angereichert oder verarmt ist!
17 Freie Energie der Grenzflächenhase g Es gilt: dg γ = S γ dt +V γ d +γda + γ µ i dn i Annahme:, T = const.!! dg γ = γda + γ µ i dn i * Integration bei konstantem g und µ i : G γ = γ A + Differentiation: γ µ i n i dg γ = γda + Adγ + Vergleich mit * Adγ + γ n i dµ i = 0 µ i dn γ i + γ n i dµ i Vgl.: Gibbs-Duhem Gleichung!!! (Ohne Berücksichtigung der Oberflächensannung!)
18 Berücksichtige: Γ i n γ i A Grenzflächen n i γ dγ = dµ i = Γ i dµ i A Gibbs sche Gleichung für Grenzflächen! Aenderung der Grenzflächensannung Grenzflächenkonzentration Aenderung des chemischen Potentials Für ein binäres System gilt: dγ = Γ 1 dµ 1 Γ 2 dµ 2 d.h. direkte Beziehung zwischen der Grenzflächensannung und der Grenzflächenkonzentration Da µ 1 und µ 2 nicht unabhängig voneinander gewählt werden können (Gibbs-Duhem!), kann man G 1 und G 2 nicht unabhängig voneinander bestimmen! Annahme: Grenzfläche SS liege so, dass die Grenzflächenkonzentration G 1 des Lösungsmittels gleich 0 ist! G 1 = 0!
19 Für eine ideale Lösung: µ 2 = µ 2 + RT ln x 2 und damit: dγ = Γ # Γ&* 2 dµ # = 2 = Γ Γ # $%&'() 2# drt ln x # 2# d.h. Γ 2 = 1 RT γ ln x 2,T = x 2 RT γ x 2,T Gibbs sche Adsortionsisotherme Dies ermöglicht es, die Anreicherung oder Verarmung der Grenzfläche an gelöstem Stoff aus der Konzentrationsabhängigkeit der Grenzflächensannung ( g/ x 2 ) zu ermitteln!
20 Oberflächensanung [mnm -1 ] Al 2 (SO 4 ) 3 CH 3 CH(CH 3 )CH 2 OH Konzentartion [g L -1 ] - Stoffe, die die Grenzflächensannung herabsetzen, nennt man kaillaraktiv, - Stoffe, die sie heraufsetzen, kaillarinaktiv Man kann also Grenzflächensannung von wässrigen Lösungen quantitativ erfassen Verhalten wasserlöslicher Substanzen Bildung von Mizellen bei Amhihilen
21
22 g I Mizellbildung II cmc III ln c I : Oberflächensannung nimmt linear mit zunehmender Konzentration ab! γ = γ 0 kc 2 mit π = γ 0 γ = kc 2 $ γ ' & ) = k % c 2 ( (Oberflächendruck) Damit: Γ 2 = c 2 RT & γ ) ( + = c 2 ' c 2 * RT k ( ) kc 2 = π = Γ 2 RT Γ i = n γ i Da : A πa = n 2 γ RT Tenside verhalten sich wie ein ideales, 2D Gas!
23 II: g nimmt näherungsweise linear mit ln c ab Γ 2 = 1 RT & γ ) ( + ' lnc 2 * Mizellbildung G 2 ist konstant, d.h. gesättigt an Oberfläche! aber: Packungsdichte im Oberflächenfilm nimmt zu (ändert sich gleich, wie in der Lösung!)) Gibbs sche Adsortionsisotherme erlaubt in diesem Bereich die Berechnung des Flächenbedarfs ro Molekül! III: g const.! Ursache: sehr geringe Aenderung des chemischen Potentials mit der Konzentration µ s = µ s 0 + RT lnc
Die Eigenschaften einfacher
 Die Eigenschaften einfacher ischungen Lernziele: Thermodynamische eschreibung von ischungen Partielle molare Grössen, TD von Ischhasen Chemisches Potenzial flüssiger Phasen Eigenschaften von Lösungen,
Die Eigenschaften einfacher ischungen Lernziele: Thermodynamische eschreibung von ischungen Partielle molare Grössen, TD von Ischhasen Chemisches Potenzial flüssiger Phasen Eigenschaften von Lösungen,
Adsorption an Festkörpern
 Adsortion an Festkörern Anreicherung eines Stoffes findet im wesentlichen nur an der Festköreroberfläche statt. Die Lage der Grenzfläche ist damit sehr genau bestimmt. Nicht nur die Größe der für die Adsortion
Adsortion an Festkörern Anreicherung eines Stoffes findet im wesentlichen nur an der Festköreroberfläche statt. Die Lage der Grenzfläche ist damit sehr genau bestimmt. Nicht nur die Größe der für die Adsortion
1 I. Thermodynamik. 1.1 Ideales Gasgesetz. 1.2 Vereinfachte kinetische Gastheorie. 1.3 Erster Hauptsatz der Thermodynamik.
 1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Van der Waals-Theorie und Zustandsgleichung
 Van der Waals-Theorie und Zustandsgleichung Eine verbesserte Zustandsgleichung für klassische Gase bei höheren Dichten liefert die Van der Waals-Gleichung. Diese Gleichung beschreibt auch den Phasenübergang
Van der Waals-Theorie und Zustandsgleichung Eine verbesserte Zustandsgleichung für klassische Gase bei höheren Dichten liefert die Van der Waals-Gleichung. Diese Gleichung beschreibt auch den Phasenübergang
PC I Thermodynamik und Transportprozesse
 20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
4. Grenzflächenspannung 1
 4. Grenzflächenspannung 1 4. GRENZFLÄCHENSPANNUNG 1. Aufgabe Mit Hilfe der Ringmethode soll die Grenzflächenspannung als Funktion der Konzentration einer grenzflächenaktiven Substanz gemessen werden. Für
4. Grenzflächenspannung 1 4. GRENZFLÄCHENSPANNUNG 1. Aufgabe Mit Hilfe der Ringmethode soll die Grenzflächenspannung als Funktion der Konzentration einer grenzflächenaktiven Substanz gemessen werden. Für
3.5.2 Thermodynamik der Grenzflächengleichgewichte reiner Stoffe Thermodynamik der Grenzflächengleichgewichte von Mehrstoffsystemen
 Inhalt von Abschnitt 3.5 3.5-0 3.5 Thermodynamik der Grenzflächen 3.5.1 Einführung 3.5.2 Thermodynamik der Grenzflächengleichgewichte reiner Stoffe 3.5.3 Thermodynamik der Grenzflächengleichgewichte von
Inhalt von Abschnitt 3.5 3.5-0 3.5 Thermodynamik der Grenzflächen 3.5.1 Einführung 3.5.2 Thermodynamik der Grenzflächengleichgewichte reiner Stoffe 3.5.3 Thermodynamik der Grenzflächengleichgewichte von
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser links) und Ethanol rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser links) und Ethanol rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme Lernziele: Phasen, Komonenten, Freiheitsgrade Die Phasenregel Zweikomonentensysteme: Damfdruckdiagramme, Hebelgesetz Zweikomonentensysteme: Siedediagramme (die Destillation von Mischungen,
Phasendiagramme Lernziele: Phasen, Komonenten, Freiheitsgrade Die Phasenregel Zweikomonentensysteme: Damfdruckdiagramme, Hebelgesetz Zweikomonentensysteme: Siedediagramme (die Destillation von Mischungen,
Tropfenkonturanalyse
 Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Grenzflächenüberschuss
 Grenzflähenübershuss β α Grenzshiht G = G( α) + G( β) GA ( ) = G ( G( α) + G( β) ) ( A) ( α β ) n ( A) n n ( ) n ( ) = Γ = n A Definition: Grenzflähenübershuß Da sih Moleküle in der Grenzshiht anreihern
Grenzflähenübershuss β α Grenzshiht G = G( α) + G( β) GA ( ) = G ( G( α) + G( β) ) ( A) ( α β ) n ( A) n n ( ) n ( ) = Γ = n A Definition: Grenzflähenübershuß Da sih Moleküle in der Grenzshiht anreihern
Die Zusammensetzung am Ausgang der 1. Verdampfereinheit (0) kann aus dem beigefügten T, x-diagramm abgelesen werden zu
 Fragenteil : Aufgabe 1 Phasengleichgewichte 15 P a Eine binäre Mischung wird in einer Verdamfereinheit kontinuierlich teilweise verdamft. Messtechnisch wurden für die Ausgangsströme der Temeratur, der
Fragenteil : Aufgabe 1 Phasengleichgewichte 15 P a Eine binäre Mischung wird in einer Verdamfereinheit kontinuierlich teilweise verdamft. Messtechnisch wurden für die Ausgangsströme der Temeratur, der
IV T H E R M I S C H E V E R F A H R E N S T E C H N I K A G R U N D L A G E N
 -IV A.1- IV T H E R M I S C H E V E R F A H R E N S T E C H N I K A G R U N D L A G E N 1 Einleitung Während heterogene Stoffgemische sich häufig durch mechanische Trennverfahren in ihre homogenen Phasen
-IV A.1- IV T H E R M I S C H E V E R F A H R E N S T E C H N I K A G R U N D L A G E N 1 Einleitung Während heterogene Stoffgemische sich häufig durch mechanische Trennverfahren in ihre homogenen Phasen
[ ε] = J m Phänomene an Flüssigkeitsgrenzflächen. ε = ΔW. Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf.
![[ ε] = J m Phänomene an Flüssigkeitsgrenzflächen. ε = ΔW. Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf. [ ε] = J m Phänomene an Flüssigkeitsgrenzflächen. ε = ΔW. Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf.](/thumbs/77/76332734.jpg) 6.4 Phänomene an Flüssigkeitsgrenzflächen Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf. effektive Kräfte nur in Grenzschichten. Oberflächenspannung Energie nötig, um Molekül von innen
6.4 Phänomene an Flüssigkeitsgrenzflächen Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf. effektive Kräfte nur in Grenzschichten. Oberflächenspannung Energie nötig, um Molekül von innen
5. Die Thermodynamischen Potentiale
 5. Die hermodynamischen Potentiale 5.1. Einführung der Potentiale Gibbs'sche Fundamentalgleichung. d = du + d, du + d δ Q d = = Ist die Entroie als Funktion von U und bekannt, = ( U, ) dann lassen sich
5. Die hermodynamischen Potentiale 5.1. Einführung der Potentiale Gibbs'sche Fundamentalgleichung. d = du + d, du + d δ Q d = = Ist die Entroie als Funktion von U und bekannt, = ( U, ) dann lassen sich
Physikalische Aspekte der Respiration
 Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
8. Vorlesung EP. EPI WS 2007/08 Dünnweber/Faessler
 8. Vorlesung EP I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik (Fortsetzung: Auftrieb) c) Oberflächenspannung und Kapillarität Versuche:
8. Vorlesung EP I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik (Fortsetzung: Auftrieb) c) Oberflächenspannung und Kapillarität Versuche:
[ ε] = J m Phänomene an Flüssigkeitsgrenzflächen. ε = ΔW. Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf.
![[ ε] = J m Phänomene an Flüssigkeitsgrenzflächen. ε = ΔW. Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf. [ ε] = J m Phänomene an Flüssigkeitsgrenzflächen. ε = ΔW. Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf.](/thumbs/77/76332817.jpg) 6.4 Phänomene an Flüssigkeitsgrenzflächen Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf. effektive Kräfte nur in Grenzschichten. Oberflächenspannung Energie nötig, um Molekül von innen
6.4 Phänomene an Flüssigkeitsgrenzflächen Kräfte von Nachbarmolekülen heben sich in der Flüssigkeit auf. effektive Kräfte nur in Grenzschichten. Oberflächenspannung Energie nötig, um Molekül von innen
Oberflächenspannung. Abstract. 1 Theoretische Grundlagen. Phasen und Grenzflächen
 Phasen und Grenzflächen Oberflächenspannung Abstract Die Oberflächenspannung verschiedener Flüssigkeit soll mit Hilfe der Kapillarmethode gemessen werden. Es sollen die mittlere Abstand der einzelnen Moleküle
Phasen und Grenzflächen Oberflächenspannung Abstract Die Oberflächenspannung verschiedener Flüssigkeit soll mit Hilfe der Kapillarmethode gemessen werden. Es sollen die mittlere Abstand der einzelnen Moleküle
Thermodynamik II. G 0 Ed = G 0 A + G 0 B = n A,st g 0. = n A,st
 Thermodynamik II Lösung ufgabe 89 sgleichgewicht a us der efinition der Freien Enthalie H T S ergibt sich bei Referenzdruck Index aus den molaren ildungsenthalien und den absoluten Entroien die Freie Enthalie
Thermodynamik II Lösung ufgabe 89 sgleichgewicht a us der efinition der Freien Enthalie H T S ergibt sich bei Referenzdruck Index aus den molaren ildungsenthalien und den absoluten Entroien die Freie Enthalie
D r H Entropie-Änderungeng. D rs Arbeit, maximale (Nicht Volumen) D r G
 REP Was schon behandelt wurde: 1. Hauptsatz 2. Hauptsatz Enthalpie-Änderungen D r H Entropie-Änderungeng D rs Arbeit, maximale (Nicht Volumen) D r G REP D r G = D r H - TDD r S Gleichgewicht: D r G = 0
REP Was schon behandelt wurde: 1. Hauptsatz 2. Hauptsatz Enthalpie-Änderungen D r H Entropie-Änderungeng D rs Arbeit, maximale (Nicht Volumen) D r G REP D r G = D r H - TDD r S Gleichgewicht: D r G = 0
1. Thermodynamische Potentiale, Maxwellgleichungen
 69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
Die innere Energie and die Entropie
 Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
Probeklausur STATISTISCHE PHYSIK PLUS
 DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
6.2 Zweiter HS der Thermodynamik
 Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Typische Grundbausteine weicher Materialien
 Typische Grundbausteine weicher Materialien Polymere 1-100 nm Kolloide 10-1000 nm Amphiphile 1-10 nm Flüssigkristalle 1-10 nm Supramoleküle 1 10 nm 1.1. Zwischenmolekulare Wechselwirkungen - meist schwache
Typische Grundbausteine weicher Materialien Polymere 1-100 nm Kolloide 10-1000 nm Amphiphile 1-10 nm Flüssigkristalle 1-10 nm Supramoleküle 1 10 nm 1.1. Zwischenmolekulare Wechselwirkungen - meist schwache
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
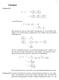 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
Physikalische Chemie II
 Physikalische Chemie II Molekulare Quantenmechanik Kondensierte Materie S. Willitsch + W. Meier Quantentheorie, Molekülstruktur Makroskopische Eigenschaften der Materie auf Basis der Thermodynamik Physikalische
Physikalische Chemie II Molekulare Quantenmechanik Kondensierte Materie S. Willitsch + W. Meier Quantentheorie, Molekülstruktur Makroskopische Eigenschaften der Materie auf Basis der Thermodynamik Physikalische
T 1 T T Zustandsverhalten einfacher Systeme (Starthilfe S ) - Prozess und Zustandsänderung. Prozess (Q 12
 . Zustandserhalten einfacher Systeme (Starthilfe S. 9-38) - Prozess und Zustandsänderung Zustandsänderung δq Prozess (Q ) - thermodynamisch einfache Systeme reiner Stoff feste flüssige damfförmige Phase
. Zustandserhalten einfacher Systeme (Starthilfe S. 9-38) - Prozess und Zustandsänderung Zustandsänderung δq Prozess (Q ) - thermodynamisch einfache Systeme reiner Stoff feste flüssige damfförmige Phase
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Kolligative Eigenschaften
 Prof. Dr. Norbert Hampp 1/8 11. Kolligative Eigenschaften Kolligative Eigenschaften Unter kolligativen Eigenschaften versteht man die Eigenschaften eines Systems die auf der Mischung unterschiedlicher
Prof. Dr. Norbert Hampp 1/8 11. Kolligative Eigenschaften Kolligative Eigenschaften Unter kolligativen Eigenschaften versteht man die Eigenschaften eines Systems die auf der Mischung unterschiedlicher
Ideale Gase. Abb.1: Versuchsanordnung von Torricelli
 Ideale Gase 1 Empirische Gasgesetze, Einblick in die Geschichte der Naturwissenschaften. Wie hängt das Volumen eines Gases von Druck, Temperatur und Stoffmenge ab? Definition Volumen V: Das Volumen V ist
Ideale Gase 1 Empirische Gasgesetze, Einblick in die Geschichte der Naturwissenschaften. Wie hängt das Volumen eines Gases von Druck, Temperatur und Stoffmenge ab? Definition Volumen V: Das Volumen V ist
Abbildung 1: Dichtegradient im Gleichgewicht (rechte Achse) und Hierbei sind neben einer Dichteverteilung auch die ungefähren Molmas-
 UZ-Dichtegradient Ziel des Experiments Häufig ist die Dichte eines sedimentierenden Partikels nicht bekannt oder sogar Hauptgegenstand der Untersuchung. Zur ausschließlichen Bestimmung der Teilchendichte
UZ-Dichtegradient Ziel des Experiments Häufig ist die Dichte eines sedimentierenden Partikels nicht bekannt oder sogar Hauptgegenstand der Untersuchung. Zur ausschließlichen Bestimmung der Teilchendichte
Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H 2 O von
 Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11
 Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Knoch, Anastasiya Petri, Guido. (Gruppe C11) Praktikum Physikalische Chemie. III Phasen und Grenzflächen. Oberflächenspannung
 Knoch, Anastasiya 10.11.2015 Petri, Guido (Gruppe C11) Praktikum Physikalische Chemie III Phasen und Grenzflächen Oberflächenspannung 1. Aufgabenstellung Es soll mit Hilfe der Kapillarmethode die Oberflächenspannung
Knoch, Anastasiya 10.11.2015 Petri, Guido (Gruppe C11) Praktikum Physikalische Chemie III Phasen und Grenzflächen Oberflächenspannung 1. Aufgabenstellung Es soll mit Hilfe der Kapillarmethode die Oberflächenspannung
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13. Klausur PC 1. Sommersemester :15 bis 11:45.
 Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13 Klausur PC 1 Sommersemester 2009 03.08.2007 10:15 bis 11:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13 Klausur PC 1 Sommersemester 2009 03.08.2007 10:15 bis 11:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die
5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht
 5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht Ein Teilchen, oder auch ein ganzes System von Teilchen, befindet sich im Gleichgewicht, falls sich "nichts" mehr ändert. Bei
5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht Ein Teilchen, oder auch ein ganzes System von Teilchen, befindet sich im Gleichgewicht, falls sich "nichts" mehr ändert. Bei
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
8.6 Thermodynamik der Grenzflächen
 8.6 Thermodynamik der Grenzflächen 8.6.1 Einführung Innerhalb jeder homogenen Phase erfährt ein Molekül allseitige Anziehungskräfte durch die nächsten Nachbarn Isotropie. Diese Anziehungskräfte heben sich
8.6 Thermodynamik der Grenzflächen 8.6.1 Einführung Innerhalb jeder homogenen Phase erfährt ein Molekül allseitige Anziehungskräfte durch die nächsten Nachbarn Isotropie. Diese Anziehungskräfte heben sich
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test
 PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
Karlsruher Institut für Technologie Festkörperphysik. Übungen zur Theoretischen Physik F SS 10
 Karlsruher Institut für Technologie Institut für Theoretische Festkörperphysik Übungen zur Theoretischen Physik F SS 10 Prof. Dr. G. Schön Lösungsvorschlag zu Blatt 2 Dr. J. Cole 30.04.2010 1. Van-der-Waals
Karlsruher Institut für Technologie Institut für Theoretische Festkörperphysik Übungen zur Theoretischen Physik F SS 10 Prof. Dr. G. Schön Lösungsvorschlag zu Blatt 2 Dr. J. Cole 30.04.2010 1. Van-der-Waals
4.5 KLASSISCHE FLÜSSIGKEITEN 85
 4.5 KLASSISCHE FLÜSSIGKEITEN 85 σ / 2 σ / 2 Abbildung 4.9: Modell der harten Scheiben Wie wir sehen werden, besitzt dieses Modell mehrere Phasen und ist damit ideal zum Studium gewisser Eigenschaften solcher
4.5 KLASSISCHE FLÜSSIGKEITEN 85 σ / 2 σ / 2 Abbildung 4.9: Modell der harten Scheiben Wie wir sehen werden, besitzt dieses Modell mehrere Phasen und ist damit ideal zum Studium gewisser Eigenschaften solcher
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Gefrierpunktserniedrigung
 Knoch, Anastasiya Datum der Durchführung: Petri, Guido 05.01.2016 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Gefrierpunktserniedrigung 1. Aufgabenstellung
Knoch, Anastasiya Datum der Durchführung: Petri, Guido 05.01.2016 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Gefrierpunktserniedrigung 1. Aufgabenstellung
Kolligative Eigenschaften
 Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Prof. Dr. Peter Vogl, Thomas Eissfeller, Peter Greck. Übung in Thermodynamik und Statistik 4B Blatt 8 (Abgabe Di 3. Juli 2012)
 U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
Lernziele: Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme,
 Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009)
 Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
3.2 Thermodynamische Gleichgewichte in Mehrkomponentensystemen
 Inhalt Kapitel 3 3.0-1 3. Mehrkomponentensysteme 3.1 Partielle molare Zustandsgrößen 3.2 Thermodynamische Gleichgewichte in Mehrkomponentensystemen Das Chemische Potential reiner Stoffe und von Stoffen
Inhalt Kapitel 3 3.0-1 3. Mehrkomponentensysteme 3.1 Partielle molare Zustandsgrößen 3.2 Thermodynamische Gleichgewichte in Mehrkomponentensystemen Das Chemische Potential reiner Stoffe und von Stoffen
Theorie der Wärme Musterlösung 11.
 Theorie der Wärme Musterlösung. FS 05 Prof. Thomas Gehrmann Übung. Edelgas im Schwerefeld Berechne den Erwartungswert der Energie eines monoatomaren idealen Gases z. B. eines Edelgases in einem zylindrischen
Theorie der Wärme Musterlösung. FS 05 Prof. Thomas Gehrmann Übung. Edelgas im Schwerefeld Berechne den Erwartungswert der Energie eines monoatomaren idealen Gases z. B. eines Edelgases in einem zylindrischen
Physikalische Chemie II
 Prof.Dr.M.Bredol / FB01 Physikalische Chemie II Modulprüfung PC-II (Klausur) 16.3.2016 Name, Vorname Aufgabe 1 2 3 4 5 Punkte maximal 20 20 20 18 22 Erreichte Punktzahl Matrikel-Nr. Gesamtpunktzahl Note
Prof.Dr.M.Bredol / FB01 Physikalische Chemie II Modulprüfung PC-II (Klausur) 16.3.2016 Name, Vorname Aufgabe 1 2 3 4 5 Punkte maximal 20 20 20 18 22 Erreichte Punktzahl Matrikel-Nr. Gesamtpunktzahl Note
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Grundlagen der Physiologie
 Grundlagen der Physiologie Bioenergetik www.icbm.de/pmbio Energieformen Von Lebewesen verwertete Energieformen o Energie ist etwas, das Arbeit ermöglicht. o Lebewesen nutzen nur zwei Formen: -- Licht --
Grundlagen der Physiologie Bioenergetik www.icbm.de/pmbio Energieformen Von Lebewesen verwertete Energieformen o Energie ist etwas, das Arbeit ermöglicht. o Lebewesen nutzen nur zwei Formen: -- Licht --
Vorlesung Statistische Mechanik: Ising-Modell
 Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
Physikalische Chemie I
 Physikalische Chemie I J.P. Maier + W. Meier Untersuchung einzelner Atome und Moleküle mit den MiGeln der Quantenmechanik Makroskopische Eigenscha;en der Materie auf Basis der Thermodynamik Physikalische
Physikalische Chemie I J.P. Maier + W. Meier Untersuchung einzelner Atome und Moleküle mit den MiGeln der Quantenmechanik Makroskopische Eigenscha;en der Materie auf Basis der Thermodynamik Physikalische
PC-Übung Nr.3 vom
 PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
PC-Übung Nr.1 vom
 PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke)
 Freie Universität Berlin W 006/007 Fachbereich Physik 8..006 tatistische Physik - heorie der Wärme (PD Dr. M. Falcke) Übungsblatt 9: hermodynamische Identitäten, hermische/kalorische Zustandsgleichung,
Freie Universität Berlin W 006/007 Fachbereich Physik 8..006 tatistische Physik - heorie der Wärme (PD Dr. M. Falcke) Übungsblatt 9: hermodynamische Identitäten, hermische/kalorische Zustandsgleichung,
Musterlösung Übung 3
 Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Statistische Thermodynamik I Lösungen zur Serie 11
 Statistische Thermodynamik I Lösungen zur Serie Verschiedenes 20 Mai 206 Barometrische Höhenformel: Betrachte die rdatmosphäre im homogenen Gravitationspotential M gz der rde Unter der Annahme, dass sich
Statistische Thermodynamik I Lösungen zur Serie Verschiedenes 20 Mai 206 Barometrische Höhenformel: Betrachte die rdatmosphäre im homogenen Gravitationspotential M gz der rde Unter der Annahme, dass sich
4. Freie Energie/Enthalpie & Gibbs Gleichungen
 4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
I el U el. P el W V 23+W F23. Musterlösung SS Aufgabe (34 Punkte) a) Energiebilanz für die Kammer A im Zeitintervall t 12 :
 Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
= n + + Thermodynamik von Elektrolytlösungen. Wdhlg: Chemisches Potential einer Teilchenart: Für Elektrolytlösungen gilt: wobei : und
 Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Die Innere Energie U
 Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
1. Wärmelehre 1.1. Temperatur Wiederholung
 1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
Zustandsbeschreibungen
 Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
! #!! % & ( )! ! +, +,# # !.. +, ) + + /) # %
 ! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmetrie und physikalische Eigenschaften, Neumannsches Prinzip
 PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmeie und physikalische Eigenschaften, Neumannsches Prinzip 2. Thermodynamik fester Körper Phänomenologische Thermodynamik (Potentiale,
PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmeie und physikalische Eigenschaften, Neumannsches Prinzip 2. Thermodynamik fester Körper Phänomenologische Thermodynamik (Potentiale,
Ausscheidungsvorgänge
 9 Ausscheidungsvorgänge Die Kristallstruktur von Metallen kann sich auch im festen Zustand ändern. Sie muß nicht notwendigerweise unterhalb der Schmelztemperatur bei allen Temperaturen stabil sein. Diejenige
9 Ausscheidungsvorgänge Die Kristallstruktur von Metallen kann sich auch im festen Zustand ändern. Sie muß nicht notwendigerweise unterhalb der Schmelztemperatur bei allen Temperaturen stabil sein. Diejenige
Klausur Thermodynamik E2/E2p SoSe 2019 Braun. Formelsammlung Thermodynamik
 Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Die Eigenschaften einfacher
 Die Eigenschaften einfacher Mischungen Lernziele: hermodynamische eschreibung von Mischungen Partielle molare Grössen, D von MIschhasen Chemische Potenzial flüssiger Phasen Eigeschaften von Lösungen, flüssige
Die Eigenschaften einfacher Mischungen Lernziele: hermodynamische eschreibung von Mischungen Partielle molare Grössen, D von MIschhasen Chemische Potenzial flüssiger Phasen Eigeschaften von Lösungen, flüssige
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Thermodynamik gekrümmter Grenzflächen
 Thermodynamik gekrümmter Grenzflächen Kapillarität und Arbeit Wir schauen zuerst den Prozess an, dass mechanische Arbeit in einem kapillären System verrichtet wird: Die allgemeine Definition thermodynamischer
Thermodynamik gekrümmter Grenzflächen Kapillarität und Arbeit Wir schauen zuerst den Prozess an, dass mechanische Arbeit in einem kapillären System verrichtet wird: Die allgemeine Definition thermodynamischer
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Aufgabe: Es sind die kryoskopischen Konstante von Wasser und die Molmassen von darin löslichen Substanzen zu bestimmen.
 Versuchsanleitungen zum Praktikum Physikalische Chemie für nfänger 1 4 Kryoskopie ufgabe: Es sind die kryoskopischen Konstante von Wasser und die Molmassen von darin löslichen Substanzen zu bestimmen.
Versuchsanleitungen zum Praktikum Physikalische Chemie für nfänger 1 4 Kryoskopie ufgabe: Es sind die kryoskopischen Konstante von Wasser und die Molmassen von darin löslichen Substanzen zu bestimmen.
Zur Erinnerung. p isotherm. Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: Kreisprozesse:
 Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
3.2 Thermodynamische Gleichgewichte in Mehrkomponentensystemen
 Inhalt Kapitel 3 3.0-1 3. Mehrkomponentensysteme 3.1 Partielle molare Zustandsgrößen 3.2 Thermodynamische Gleichgewichte in Mehrkomponentensystemen Das Chemische Potential reiner Stoffe und von Stoffen
Inhalt Kapitel 3 3.0-1 3. Mehrkomponentensysteme 3.1 Partielle molare Zustandsgrößen 3.2 Thermodynamische Gleichgewichte in Mehrkomponentensystemen Das Chemische Potential reiner Stoffe und von Stoffen
1.2 Zustandsgrößen, Zustandsänderungen, Gleichgewichtszustand
 1.2 Zustandsgrößen, Zustandsänderungen, Gleichgewichtszustand Wie erfolgt die Beschreibung des Zustands eines Systems? über Zustandsgrößen (makroskopische Eigenschaften, die den Zustand eines Systems kennzeichnen)
1.2 Zustandsgrößen, Zustandsänderungen, Gleichgewichtszustand Wie erfolgt die Beschreibung des Zustands eines Systems? über Zustandsgrößen (makroskopische Eigenschaften, die den Zustand eines Systems kennzeichnen)
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
3. Mikrostruktur und Phasenübergänge
 3. Mikrostruktur und Phasenübergänge Definition von Mikrostruktur und Gefüge Gefüge bezeichnet die Beschaffenheit der Gesamtheit jener Teilvolumina eines Werkstoffs, von denen jedes hinsichtlich seiner
3. Mikrostruktur und Phasenübergänge Definition von Mikrostruktur und Gefüge Gefüge bezeichnet die Beschaffenheit der Gesamtheit jener Teilvolumina eines Werkstoffs, von denen jedes hinsichtlich seiner
ELEMENTE DER WÄRMELEHRE
 ELEMENTE DER WÄRMELEHRE 3. Elemente der Wärmelehre 3.1 Grundlagen 3.2 Die kinetische Gastheorie 3.3 Energieumwandlungen 3.4 Hauptsätze der Thermodynamik 2 t =? 85 ºC t =? 61.7 ºC Warum wird der Kaffe eigentlich
ELEMENTE DER WÄRMELEHRE 3. Elemente der Wärmelehre 3.1 Grundlagen 3.2 Die kinetische Gastheorie 3.3 Energieumwandlungen 3.4 Hauptsätze der Thermodynamik 2 t =? 85 ºC t =? 61.7 ºC Warum wird der Kaffe eigentlich
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Chemisches Potential und Nernstgleichung Carsten Stick
 Chemisches Potential und Nernstgleichung Carsten Stick Definition der mechanischen Arbeit: Kraft mal Weg W = F! ds W = Arbeit oder Energie; F = Kraft; s = Weg Diese Definition lässt sich auch auf die Kompression
Chemisches Potential und Nernstgleichung Carsten Stick Definition der mechanischen Arbeit: Kraft mal Weg W = F! ds W = Arbeit oder Energie; F = Kraft; s = Weg Diese Definition lässt sich auch auf die Kompression
Einführung in die Chromatographie
 Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/32 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/32 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Übungen zur Vorlesung Physikalische Chemie 2 (B. Sc.) Lösungsvorschlag zu Blatt 12
 Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
