5 Kernresonanzspektrometrie (NMR-Spektrometrie)
|
|
|
- Hermann Holzmann
- vor 7 Jahren
- Abrufe
Transkript
1 5 Kernresonanzspektrometrie (NMR-Spektrometrie) N171_KernresonanzSpektrometrie_c_BAneu.doc - 1/22 Die NMR-Spektrometrie beruht auf der Wechselwirkung des Eigendrehimpulses eines Atomkerns mit einem äußeren Magnetfeld B 0. Der mit dem Drehimpuls verbundene magnetische Dipol des Kerns wechselwirkt aber nicht nur mit dem äußeren Magnetfeld sondern auch mit den Elektronen, die das Atom umgeben chemische Verschiebung induktive Abschirmung mit den Elektronen der übrigen Atome chemische Verschiebung Entschirmung mit benachbarten Atomkernen im selben Molekül J-Kopplung Spin-Spin-Kopplung Diese verschiedenen Wechselwirkungen liefern ein sehr genaues Abbild über das Innere des Moleküls. Damit ist die NMR-Spektrometrie neben der Röntgenstrukturanalyse heute die wichtigste Methode zur Strukturaufklärung in der analytischen Chemie und Biologie. 5.1 Physikalische Grundlagen Grundlage der NMR-Spektrometrie ist das Verhalten von Atomkernen in einem äußeren Magnetfeld B 0. Atomkerne (Isotope, Symbol X) bestehen aus Protonen und Neutronen. Ordnungszahl Z = Anzahl der Protonen A 12 1 Massenzahl A = Anzahl von Protonen + Anzahl Neutronen Z X z.b.: 6 C, 1H Die meisten Atomkerne besitzen einen Kerndrehimpuls, den Kernspin J. In der klassischen Vorstellung ist dieser auf die Rotation der Kerne (Protonen und Neutronen) um eine Kernachse zurückzuführen. Wie viele andere atomare Größen auch, ist der Kernspin J quantisiert. J J I( I 1) I ist die Kernspinquantenzahl und kann halbzahlig oder ganzzahlig sein. Da mit einer rotierenden Ladung immer auch die Erzeugung eines Magnetfeldes verbunden ist, besitzt jeder Atomkern mit dem Kernspin J ein magnetisches Moment µ. J heißt gyromagnetisches Verhältnis und ist für die einzelnen Isotope unterschiedlich. Atomkern als Kompassnadel im Magnetfeld (klassisch) Kerne mit Ι = 0 als Kernspinquantenzahl, haben keinen Drehimpuls und kein magnetisches Moment. Vom gyromagnetischen Verhältnis γ hängt die Nachweisempfindlichkeit eines Kernes für das NMR-Experiment ab. Die Messmethode wird mit steigendem γ empfindlicher. N Regel: gg I = 0 ug I = halbz. gu I = halbz. uu I = ganzz. [T] = V s m -2
2 Kerne im äußeren Magnetfeld (I = ½) N171_KernresonanzSpektrometrie_c_BAneu.doc - 2/22 Ohne äußeres Magnetfeld sind die magnetischen Dipole der Kerne einer Probe alle zufällig ausgerichtet. In einem äußeren Magnetfelde B 0 richten sich die mag. Dipole aus. Dabei tritt Richtungsquantisierung nach den Gesetzen der Quantenmechanik auf: Die Komponente J z des Drehimpulses in Richtung des Magnetfeldes kann nur die (2I+1) Werte J z m einnehmen, wobei die magnetische Quantenzahl m = I, I-1, I-2,... -I sein kann. J z m z m Spin ½ - Kerne (I = ½ ) haben damit zwei Einstellmöglichkeiten, parallel (m = + ½, -Stellung) oder antiparallel (m = - ½, -St.) 1 J 2 3 Energie im Magnetfeld B 0 Die Energie eines magnetischen Dipols in einem Magnetfeld B 0 beträgt: W B 0 cos B 0 W zb m 0 B 0 Damit ergeben sich für einen Kern mit I = ½ zwei Energieniveaus, die sogenannten Kern-Zeeman-Niveaus, wobei die Orientierung mit der Spinquantenzahl m = +½ (parallele Ausrichtung) die energetisch günstigere ist. Der Energieunterschied der Energieniveaus beträgt: W W 1/ 2 W1/ 2 B0 Im Resonanzfall klappt das Proton von der parallelen in die antiparallele Orientierung um. Präzession im Magnetfeld Befindet sich der Atomkern mit dem mag. Moment in einem Magnetfeld, so präzediert der Vektor J und sein mag. Moment auf einem Kegelmantel um die Richtung von B 0. dj M Drehm. B0 dt J d B sin 0 sin dt B JB J 0 0 L B 0 L Die Larmor-Präzessionsfrequenz L entspricht der Energiedifferenz W L und ist proportional zum angelegten B 0 -Feld. B 0 = 0 W energiereich antiparallel m = - 1/2 energiearm parallel m = + 1/2
3 N171_KernresonanzSpektrometrie_c_BAneu.doc - 3/22 Die makroskopische Magnetisierung M Die einzelnen Kernmomente rotieren mit ihrer Larmor-Frequenz auf den beiden Kegelmänteln, jedoch mit statistisch verteilter Phase, so dass sich sämtliche transversalen Komponenten µ x und µ y der Spinvektoren senkrecht zu B 0 herausmitteln. Ebenso verhindert die Temperaturbewegung eine Einstellung aller Dipolmomente parallel zu B 0. Im thermischen Gleichgewicht sind die beiden Zustände entsprechend der Boltzmann-Verteilung besetzt, mit einem geringfügigen Besetzungsüberschuss im energieärmeren Niveau parallel zu B 0. Nantip.; β W exp( ) N kt parallel; α Zahlenbeispiel für Protonen ( 1 H): B 0 = 1,41 T Na (Ergebnis: 0, ) N p Die Addition sämtlicher mag. Dipolmomente ergibt dann eine makroskopische Magnetisierung M in Richtung von B 0. Sie resultiert aus dem geringen Besetzungsüberschuss im energieärmeren Spinniveau α. Spinanregung (Präparation des Spinzustandes) Mit einer Sendespule wird ein linear polarisiertes Wechselfeld B 1, z.b. in x-richtung eingestrahlt. Wenn die Frequenz des Wechselfeldes der Lamor- Frequenz L der anzuregenden Kerne entspricht, rotiert eine Komponente von B 1 genauso wie die Einzelspins der Kerne um das Feld B 0. 1 Der Vektor B 1 mit dem gleichen Drehsinn wie die Präzession der Kerne kann mit dem Vektor M in Wechselwirkung treten. Es erfolgt Resonanzabsorption ( ß), sodass sich die Population der Spins zugunsten ß verändert. Mikroskopisch werden einzelne Spins von der energiearmen Parallelstellung in die energiereichere Stellung umgeklappt und laufen synchron mit dem drehenden B 1 -Feld. Kerne werden so in einen kohärent, mit fester Phasenlage präzedierenden Zustand versetzt. Makroskopisch ist das Ergebnis ein Kippen des Magnetisierungsvektors M um den Winkel. Dadurch tritt nun auch in der transversalen xy-ebene senkrecht zu B 0 und senkrecht zu B 1 eine Komponente auf, die sogenannte transversale Magnetisierung M xy. 1 Das linear in x-richtung oszillierende B 1 -Feld in der Spule kann man durch zwei um die z-richtung rotierende Vektoren entgegengesetzter Drehrichtung beschreiben.
4 N171_KernresonanzSpektrometrie_c_BAneu.doc - 4/22 Das Kippen der makroskopischen Magnetisierung M kann anschaulich auch in einem rotierenden Koordinatensystem (RKS) erklärt werden, das sich um die z-achse mit der Larmorfrequenz dreht. Damit wird das (im Laborsystem sich drehende) B 1 -Feld im RKS zu einem statischen Magnetfeld: B 1 = const! Die transversalen Achsen bezeichnen wir dann mit x' und y'. Rotierendes System In dem mit L rotierenden System wirkt auf M ein Drehmoment M Drehm. M B1 (vom angelegten B 1 -Feld). Die makroskopische Magnetisierung M erfährt eine Präzession um die rotierende x'-achse und wird aus der senkrechten Stellung ausgelenkt. Es entsteht die transversale (Quer-)Magnetisierung M xy. Gleichzeitig wird die M z -Komponente gegenüber dem Ausgangszustand (M z = M 0 ) verkleinert. Laborsystem Insgesamt bewegt sich der Vektor M der Gesamtmagnetisierung dann im Laborsystem spiralförmig auf der Oberfläche einer Kugel. Während des B 1 -Pulses präzediert (dreht sich) M um die Richtung von B 1 (x ) für die analog gilt: ω 1 = γb 1 und erreicht bis zum Pulsende den sog. Flipwinkel α (t p ist die Pulsdauer). 1 1t p B1 t P x y Ist die Pulsdauer so gewählt, dass = π/2 (90 ; π/2-puls), liegt M gerade auf der y'-achse, d.h. es liegt eine maximale Quermagnetisierung vor, aber keine longitudinale Magnetisierung mehr. Die beiden Energiezustände sind dann gleich populiert! Free Induction Decay Schaltet man nun das B 1 -Feld (HF-Impuls) ab, so präzediert die Magnetisierung im Laborsystem weiterhin in der xy-ebene und induziert in der Empfängerspule eine Spannung, das Kernresonanzsignal ( FID). Dies ist der Prozess, der gemessen und letztlich als NMR-Spektrum dargestellt wird. Da die Dauer t P des B 1 -Pulses nur einige µs beträgt, ist die spektrale Breite ( f 1/t P ) ausreichend groß, um auch Kerne mit leicht unterschiedlichen Resonanzfrequenzen mit einem einzigen Hf-Impuls der Frequenz L anzuregen.
5 Free Induction Decay FID N171_KernresonanzSpektrometrie_c_BAneu.doc - 5/22 Nach dem Abschalten des B 1 -Impulses läuft die synchrone Magnetisierung wieder auseinander, um letztlich in ihren Gleichgewichtszustand zurückzukehren. Die Relaxation der Quermagnetisierung M xy wird als Free Induction Decay (FID) bezeichnet und bei der NMR-Spektrometrie primär gemessen. 90 -Impuls FID-Signal Die Ursache für das Abklingen des Signals sind im wesentlichen leicht unterschiedliche Umlaufzeiten der Spins aufgrund von Inhomogenitäten des lokalen B 0 -Feldes an den Kernorten ( T 2 *). Longitudinale und transversale Relaxation* Die Relaxation nach Abschalten des B 1 -Impulses wird von zwei unabhängigen Relaxationsprozessen bestimmt, der Spin-Gitter-Relaxation T 1 und der Spin-Spin-Relaxation T 2. Die Zeitkonstanten T 1 und T 2 sind erheblich langsamer als der Puls (µs), üblicherweise 0,1 bis 100s. Es gilt: T 2 T 1. 1) Longitudinale (Spin-Gitter-) Relaxation T 1 (Energie)-Relaxation ins thermodynamische Gleichgewicht entlang der z-achse. Das ursprüngliche Boltzmann-Gleichgewicht stellt sich wieder ein. Die Überschussenergie wird als thermische Energie an die Umgebung abgegeben. Dieser Vorgang ist aber nicht direkt beobachtbar, weil er in z-richtung, also senkrecht zum Detektor erfolgt. Die Längsrelaxationszeit T 1 ist abhängig von der sog. "Spin-Gitter"-Wechselwirkung, d.h. von der chemischen Umgebung des beobachteten Kerns.
6 N171_KernresonanzSpektrometrie_c_BAneu.doc - 6/22 Messung von T 1 Bei entsprechend doppelter Pulsdauer ist = π (180 ; π-puls). Die Boltzmannsche Spinverteilung wird damit umgekehrt und es gibt auch keine Quermagnetisierung (der ß-Zustand ist jetzt überpopuliert). M z 180 -Puls M z (t) Die Zeit T 1 misst man, indem man die relaxierende Magnetisierung M zu verschiedenen Zeiten mit einem 90 -Impuls umklappt und die Stärke des transversalen FID-Signals misst. Trifft man z.b. die Zeit t = 0,693 T 1 ist das FID Signal Null. t 2) Transversale (Spin-Spin-) Relaxation T 2 Durch den B 1 -Puls wurde die gleichmäßige Verteilung der Einzelspins auf den Kegelmänteln teilweise aufgehoben und so die Quermagnetisierung erzeugt (kohärent synchroner Umlauf der Einzelspins). Diese Störung wird beim Ausschalten des B 1 -Feldes rückgängig gemacht. Wegen der Spin-Spin-Wechselwirkung, bei der die Kerne eines Moleküls untereinander Spinenergie austauschen (Energieübertragung auf einen Nachbarspin) und aufgrund von Inhomogenitäten des B 0 -Feldes laufen die Spins mit leicht unterschiedlichen Geschwindigkeiten herum. Sie verlieren damit ihre Phasenkohärenz und laufen auseinander. Die Spins verteilen sich wieder gleichmäßig auf den Kegelmänteln. Damit verkleinert sich die transversale Magnetisierung M xy, bis sie zu Null zerfallen ist. Es ändert sich aber nicht der Besetzungsunterschied, d.h. die Magnetisierung in z-richtung. Messung von T 2 (Spinecho) Erst wird mit einem 90 -Impuls die Magnetisierung M in die x,y-ebene gedreht. Nach einer bestimmten Zeit t = t E /2 (t E = Echozeit) wird ein 180 -Impuls eingestrahlt, der die auseinanderlaufenden Spins um 180 umklappt. Nach der doppelten Zeit t = t E sind dann alle Spins wieder in Phase und erzeugen das Echo-Signal.
7 N171_KernresonanzSpektrometrie_c_BAneu.doc - 7/22 Zur Messung von T 2 strahlt man nun mehrere 180 -Impulse im Abstand von t E ein. Dabei können aber die aufgrund von Spin-Spin-Relaxation die (statistisch) dephasierten Spins nicht mehr refokussiert werden. Nur die Dispersion der Umlaufzeiten aufgrund der B 0 -Inhmogenitäten wird rückgängig gemacht (refokussiert). Die Abnahme der Echo-Signale wird dann nur durch die Spin-Spin-Relaxationszeit T 2 verursacht. T 2 beschreibt damit die zeitliche Auffächerung der Quermagnetisierung nach einem Auslenkungsimpuls, die auch durch 180 -Rephasierung nicht mehr rückgängig gemacht werden kann. Da T 2 auf intramolekularer Spin-Spin-Wechselwirkung beruht und nicht von der Umgebung abhängt, ist sie ein wichtiger Parameter für die Strukturaufklärung. 2 Ein Anwendungsbeispiel außerhalb der Analytik ist die Magnet-Resonanz-Tomografie (MRT), wo Unterschiede in den Relaxationszeiten T 1 und T 2 zur Bildgebung in der modernen Medizin genutzt werden. Abb. rechts: Typische Längsrelaxationszeiten T 1 in s von menschlichem Gewebe. Da T 1 in spezifischer Weise von der Art der Bindung des Wassers (Protonen) im Gewebe abhängig ist, kann so gesundes von krankem Gewebe unterschieden werden. Primär dient die T 1 -Messung zur Kontrast steigerung in der MRT. 2 Das FID-Signal fällt mit der sog T 2 *-Relaxationszeit ab. Dieser Abfall setzt sich aus zwei Beiträgen zusammen. Der erste Beitrag ist die Spin-Spin-Relaxation T 2. Der zweite Beitrag kommt dadurch zustande, dass die einzelnen Kerne wegen der Inhomogenität B 0 des B 0 -Feldes leicht unterschiedliche Umlaufzeiten, bzw. Larmorfrequenzen besitzen. Es gilt: 1 B0 1 T * 2 T 2 2
8 5.2 Messgrößen der NMR-Spektrometrie Einfluss der Umgebung des betrachteten Kerns N171_KernresonanzSpektrometrie_c_BAneu.doc - 8/22 Bei gegebener Magnetfeldstärke B 0 ist die Resonanzfrequenz für einen bestimmten Kern festgelegt. In einem realen Atom beeinflussen jedoch die Elektronen, die einen Kern umgeben und die Elektronenverteilung der übrigen Atome im Molekül das lokale Magnetfeld am Kernort. Die Elektronenbewegung verursacht nämlich kleine magnetische Zusatzfelder. Je nachdem, ob diese Zusatzfelder dem externen Feld B 0 am Atomkern entgegenwirken oder dieses verstärken, bezeichnet man dieses Phänomen als Abschirmung oder Entschirmung. Abschirmung: Das angelegte Feld B 0 bewirkt eine kreisförmige Bewegung der Elektronen um den Kern. Diese Ringströme induzieren im Bereich des Kerns ein sekundäres Feld B Ind, das dem äußeren entgegengesetzt ist (diamagnetischer Effekt ; Lenzsche Regel). Auf diese Weise wirkt am Kernort ein verringertes Magnetfeld Abschirmung Beff B 0 B Ind B eff B0 B0 ) B0(1 Damit ergibt sich eine Verminderung der Resonanzfrequenz. B 0(1 ) 0 B 0 0 Atom induzierte Elektronen - Die Abschirmkonstante liegt im ppm-bereich und ist eine typische Molekülkonstante (für einen bestimmten Kern), die durch die intramolekulare chemische Umgebung des jeweiligen Kerns bestimmt wird. ist um so größer, je größer die Elektronendichte um den Kern ist und hängt daher von den Bindungsverhältnissen ab - z.b. verstärken elektronenliefernde Nachbaratome die Abschirmung. Entschirmung: Befinden sich in der Nachbarschaft des Atomkerns elektronenziehende Gruppen (N, O, Halogene), so wird die Elektronendichte am Kern wieder verringert. Es erfolgt Entschirmung des Atoms wie man sagt und die Resonanzfrequenz wird wieder größer. Bedeutung für die Strukturanalytik: Die Kerne spüren ihre intramolekulare Umgebung. Mit der genauen Lage des Resonanz- Übergangs kann man verschiedenartig gebundene Kerne derselben Sorte im Molekül unterscheiden. Deshalb ist die Methode für die Strukturaufklärung so interessant. Chemisch äquivalente Kerne Chemisch äquivalente Kerne sind Kerne mit der gleichen elektronischen Umgebung. Sie ergeben im NMR-Spektrum nur ein Signal. Beispiel: Im Tetrametylsilan (TMS) haben alle Protonen die gleiche elektronische Umgebung nur ein NMR-Signal.
9 Chemisch nicht-äquivalente Kerne N171_KernresonanzSpektrometrie_c_BAneu.doc - 9/22 Chemisch nicht-äquivalente Kerne sind Kerne mit einer unterschiedlichen elektronischen Umgebung. Sie ergeben im NMR-Spektrum getrennte Signale. Beispiel: Methyl-methyl-sulfoxid Die Protonen der CH 3 - (rot), CH 3 - (blau) und CH 2 -Gruppe (grün) sind zueinander nicht-äquivalent, da deren elektronische Umgebung verschieden ist. CH 3 -Gruppe (rot): S(O)CH 2 -Gruppe in der Nachbarschaft CH 3 -Gruppe (blau): SCH 2 -Gruppe in der Nachbarschaft Dagegen sind die Protonen in den jeweiligen Gruppen in sich chemisch äquivalent, z.b. die 3 Protonen der CH 3 -Gruppe (rot). Im 1 H- Spektrum gibt es deshalb nur drei Signale: eins für die CH 3 -Gruppe (rot), eins für die CH 3 -Gruppe (blau) und eins für die CH 2 -Gruppe (grün) Chemische Verschiebung Die Frequenzverschiebung ist proportional zur Stärke des Magnetfeldes B 0 ( B 0 0 ). Die Angabe der absoluten Frequenzverschiebung als Molekülparameter ist aber ungeeignet, da die Spektren nicht einheitlich mit einer Feldstärke B 0 gemessen werden. Deshalb wurde eine relative Größe, die chemische Verschiebung δ eingeführt. fprobe freferenz 10 6 ppm Chemische Verschiebung in ppm f Referenz δ ist die relative Frequenzdifferenz der Resonanzsignale des betrachteten Kerns in der Probe (f Probe ) und in einer Referenzsubstanz (f Referenz ), geteilt durch die Referenzfrequenz f Referenz (bzw. f 0 ). TMS als Referenzsubstanz TMS (siehe Beispiel) hat aufgrund seiner chemischen Struktur (12 äquivalente Protonen) nur ein scharfes Signal, welches zudem von den meisten anderen Resonanzsignalen deutlich getrennt ist. Da die Protonen im TMS sehr stark abgeschirmt sind und es fast keine weiteren Gruppen mit derart hoher Abschirmung gibt, liegen die bekannten chemischen Verschiebungen fast alle im positiven Bereich. Die Entschirmung der Wasserstoffkerne ist hier kleiner als in den meisten anderen org. Verbindungen, da das zentrale Si-Atom eine geringe Elektronegativität besitzt. TMS wird meist der Probe beigemischt oder bei Lösungsmittelproblemen in einem Röhrchen in die Probe gebracht. Es wird deshalb als innerer Standard bezeichnet. Hinweis : chemische Verschiebung groß Abschirmung klein liegt bei der 1 H -NMR im Bereich von 0 ppm bis ca. 15 ppm. Die Frequenzverschiebung umfasst damit nur einen Bereich von 1/ der Messfrequenz. Hohe Anforderungen an die Messgenauigkeit.
10 N171_KernresonanzSpektrometrie_c_BAneu.doc - 10/22 Anisotropieeffekte Ursachen für die chemische Verschiebung: induktive Abschirmung der Elektronenhülle des Atoms (diamagnetisch Abschirmung) Elektronegativität (polare Bindungen) der Nachbargruppen (paramagnetisch Entschirmung) Weiterer Effekt: Richtungsabhängigkeit der chem. Verschiebung Anisotropie Protonen, die sich in bestimmten Bereichen um die π-systeme ungesättigter Verbindungen (Alkene, Alkine, Aromaten, Carbonyl-Verbindungen) befinden, werden durch Ringströme entschirmt oder abgeschirmt. - Protonen an C = C Doppelbindungen - Protonen an C C Dreifachbindungen - Protonen an Carbonylgruppen - Protonen an Aromaten - Ringstrommodell - Abschirmkegel Anisotropie bei Benzol: Das äußere Magnetfeld B 0 induziert einen Ringstrom im aromatischen -System, der seinerseits ein Magnetfeld hervorruft. Dieses verstärkt die magnetische Flußdichte am Ort der Protonen ( Entschirmung ). Anisotropie bei Mehrfachbindungen Anisotropieeffekte führen zu einer Entschirmung der Protonen von Alkenen und Carbonylverbindungen (Aldehyden), jedoch zu einer Abschirmung im Fall von Alkinen. Atome innerhalb der Abschirmungskegel sind stärker abgeschirmt (kleinere Entschirmung). zunehmende Entschirmung zunehmende Abschirmung B eff nimmt zu B eff nimmt ab Chemische Verschiebung einiger Verbindungen
11 N171_KernresonanzSpektrometrie_c_BAneu.doc - 11/22 Chemische Verschiebung verschiedener Arten von H-Atomen im 1 H-NMR-Spektrum Chemische Verschiebung von H-Atomen in Methylgruppen (-CH 2 -) mit unterschiedlicher Nachbarschaft Abhängigkeit der Entschirmung vom Abstand funktioneller Gruppen.
12 N171_KernresonanzSpektrometrie_c_BAneu.doc - 12/ Spin-Spin-Kopplung (Signalaufspaltung in Spinsystemen mit I = ½) Die benachbarten Kernspins (zu einem Kern X in Resonanz) in dem gleichen Molekül treten über die Polarisation der Bindungselektronen miteinander in Wechselwirkung (indirekte Spin-Spin-WW). Dadurch können Kopplungen über größere Abstände wirken, als durch die unmittelbare oder direkte räumliche Spin-Spin-WW möglich wäre. Dies führt in einer Probe mit mehr als einer chemisch äquivalenten Kernsorte (gleiche chemische Verschiebung) zu einer Feinstrukturaufspaltung der Resonanzlinien 3. Wegen der diskreten Einstellmöglichkeiten der Kerndipole ergeben sich nur diskrete Kombinationen von zusätzlichen Feldstärken an einem Kernort (Kern X). B eff - B A B eff + B A Kern X Kern A Kern X Kern A (in Resonanz) (nicht in Resonanz) Modellbeispiel: Aufgrund der beiden praktisch gleich wahrscheinlichen Orientierungen der Kerne A relativ zu X ist das Resonanzsignal der Kerne X in zwei Signale von gleicher Intensität aufgespalten (Dublett; gilt für I = ½) Aufspaltungsmuster von I = ½ Kernen Befinden sich nun zwei äquivalente Kerne (d.h. Kerne mit der gleichen chemischen Verschiebung, AA) in Nachbarschaft zum Kern X, so sind drei unterschiedliche Magnetfelder am Ort von X möglich. Daraus resultiert eine Aufspaltung des Resonanzsignals vom Kern X (oder untereinander äquivalenten X-Kernen) in ein Triplett. Intensitätsverhältnis 1:2:1, da gleichwertige mittlere Konfiguration doppelt so häufig ist. Für die beiden äquivalenten Kerne AA verändert sich die Situation jedoch im Vergleich zum AX- System nicht (AA-Kerne Duplett) X A A mögliche Orientierungen der Kerne A relativ zu X Bei drei koppelnden äquivalenten Kernen AAA ergibt sich ein Quartett mit dem Intensitätsverhältnis 1:3:3:1 (Pascalsches Dreieck). X A A A 3 Kerne eines Moleküls heißen chemisch äquivalent, wenn sie die gleiche Umgebung im Molekül besitzen. magnetisch äquivalent, wenn sie chemisch äquivalent sind und jeder Kern X in Resonanz dieselben Kopplungen zu jedem einzelnen chemisch äquivalenten Kern A im Molekül hat isochron, wenn sie dieselbe Resonanzfrequenz besitzen.
13 N171_KernresonanzSpektrometrie_c_BAneu.doc - 13/22 Die direkte Spin-Spin-WW zwischen magnetisch äquivalenten Kernen (z.b. zwischen den H-Atomen in -CH 3 ) tritt im NMR-Spektrum nicht in Erscheinung (obwohl vorhanden). Aufspaltungsregeln: (N+1) Regel: Bei N benachbarten A-Kernen spaltet die X-Linie in (N+1) Niveaus auf. Äquivalente Kerne (X) mit 1 benachbarten H-Atom (A) geben ein Duplett-Signal. Äquivalente Kerne (X) mit 2 benachbarten, untereinander äquivalenten H-Atomen (AA) geben ein Triplett-Signal. Äquivalente Kerne (X) mit 3 benachbarten, untereinander äquivalenten H-Atomen (AAA) geben ein Quartett-Signal. Beispiel: Tribrom-ethan Br-CH 2 -CHBr 2 Die Methylenprotonen sind chemisch äquivalent und ergeben ein Signal bei 4,10 ppm. Das Signal des Protons der CHBr 2 -Gruppe erscheint bei 5,67 ppm Das Signal der Methylenprotonen ist ein Dublett, da sich in der Nachbarschaft eine CH-Gruppe befindet. Das Proton der CH-Gruppe ergibt ein Triplett, hervorgerufen durch die CH 2 -Gruppe. Kopplungskonstante J Der Abstand zwischen den Resonanzlinien in einem durch Spin-Spin-Kopplung hervorgerufenen Multiplett heißt Kopplungskonstante J [Dimension Hz] und ist unabhängig vom angelegten Magnetfeld B 0. (skalare) Kopplung geminale Kopplung vacinale Kopplung Fernkopplung Kopplung über eine Bindung 1 J Kopplung über zwei Bindungen 2 J = -30 bis +6 Hz Kopplung über drei Bindungen 3 J = 0 bis 14 Hz Kopplung über mehr als drei Bindungen n J = 0 bis 10 Hz C H H H C H C H C C C H
14 N171_KernresonanzSpektrometrie_c_BAneu.doc - 14/22 Intensitätsregel Die Intensitäten der einzelnen Linien eines Multipletts lassen sich aus dem Pascalschen Dreieck herleiten. Die Intensität ergibt sich aus der Fläche unter der Resonanzlinie und ist proportional zur Anzahl der Protonen der betreffenden Sorte. Beispiel 1: Feinstruktur im 1 H-NMR-Spektrum von Ethanol in CDCl 3 Ethanol : Drei Sorten verschieden gebundener H-Atome in HO-CH 2 -CH 3 drei Signale plus Feinstruktur wegen J-Kopplung. Die Integration der Resonanzpeaks ergibt ein Zahlenverhältnis von 1:2: Spektren höherer Ordnung* Die in diskutierten einfachen Spinsysteme werden AX-Systeme genannt. Es handelt sich dann um Spektren erster Ordnung. Signalaufspaltung nach diesen einfachen Regeln nur, wenn der Unterschied der Resonanzfrequenzen (der koppelnden Kerne) f mindestens 10 mal größer ist als die Kopplungskonstante J. f ( AX ) 10 J AX Bei zu großer Kopplungskonstante, bzw. zu kleinem Frequenzunterschied ergeben sich Spektren höherer Ordnung mit komplizierten Aufspaltungsmustern (Feinstruktur). Eine Auswertung ist dann oftmals nicht mehr einfach möglich. Bei Kopplung eines Protons M mit zwei chemisch nicht äquivalenten Protonen A und X erhält man (vorausgesetzt Δf(MA)/J MA > 10 und Δf(MX)/J MX > 10) ein sog. AMX-System. Darin wird das Signal von M durch die Kopplung mit A zu einem Dublett aufgespalten und die beiden Linien dieses Dubletts werden durch die Kopplung mit X erneut aufgespalten. Als Resultat erhält man ein Dublett vom Dublett.
15 Beispiel 2: 1 H-NMR-Spektrum von Ethylbenzol (Spektrum 1. Ordnung) N171_KernresonanzSpektrometrie_c_BAneu.doc - 15/22 aus: Dominik, Steinhilber: Instrumentelle Analytik
16 5.3 Gerätetechnik N171_KernresonanzSpektrometrie_c_BAneu.doc - 16/ CW (Continuous Wave) Spektrometer CW-NMR-Spektrometer haben nur noch geringe Bedeutung. Prinzip: Kontinuierliche Einstrahlung mit konstanter Radiofrequenz (z.b. 60 MHz für 1 H) und langsame Erhöhung der angelegten Magnetfeldstärke B 0. Nur in dem Moment, wenn die eingestrahlte Frequenz mit der Larmorfrequenz ω L genau übereinstimmt, kommt es zur Resonanz. Detektiert wird die Absorption (Leistungsaufnahme in der hf Sender Sendespule) oder die Strahlung, die von den in Resonanz geratenen Atomen wieder emittiert wird. B-Scan: B f-scan: PFT-(Puls-Fourier-Transform) NMR-Spektrometrie Wichtige Kennzeichen: homogenes Magnetfeld. (große Polschuhe) Feldstärke ab 1-2 Tesla (supraleitend bis 18,8 T = 800 MHz für 1 H) Probenröhrchen dreht sich, um Feldinhomogenitäten auszumitteln Probenvolumen klein (0,5 ml) Deuterierte Lösungsmittel oder protonenfreie Lösungsmittel (CCl 4, CS 2, CDCl 3..) Messprinzip der PFT-NMR Bei konstantem Magnetfeld werden in der Probe sämtliche Kerne einer Sorte (z.b. 1 H) durch einen sehr kurzen Radiofrequenz-Impuls gleichzeitig angeregt. Durch den Anregungsimpuls werden die Kerne in einen kohärent präzedierenden Zustand versetzt und induzieren anschließend beim freien Induktionszerfall einen schwachen Wechselstrom in der Empfangsspule (A). Dieses FID-Signal wird durch mathematische FOURIER-Transformation in die entsprechende Frequenzdomäne (d.h. in das NMR-Spektrum) umgerechnet(b).
17 N171_KernresonanzSpektrometrie_c_BAneu.doc - 17/22 Wenn alle Kerne in der Probe dieselbe Frequenz (chemische Verschiebung) haben, dann enthält das detektierte Signal (Wechselstrom in der Empfängerspule) nur eine einzige Frequenz, d.h. es besteht aus einer einfachen, exponentiell abklingenden Sinuskurve (Free Induction Decay FID). Wenn mehrere Kerne mit unterschiedlichen Frequenzen vorliegen (unterschiedlichen chemischen Verschiebungen), besteht der FID aus mehreren sich überlagernden Frequenzen. Verbesserung des Signal-Rauschverhältnisses Akkumulation vieler FID-Signale und dann erst Fouriertransformation. (SNR n ½ ) Berechnung des B 1 -Feldes: Spektrale Breite des Anregungsimpulses Bei kurzer Pulsdauer (t P ) im µs-bereich entsteht ein kontinuierliches Anregungsfrequenzband mit einer Breite von 1/t P. Dieses deckt das gesamte Spektrum der leicht unterschiedlichen Frequenzen der Kerne ab. ( chemische Verschiebung) Vorteile der PFT-NMR-Spektrometrie Das gesamte Spektrum wird gleichzeitig erhalten: Mehrere FID-Signale können summiert werden: weitergehend (nicht Inhalt der VL): Zeitgewinn! besseres Signal-Rausch-Verhältnis Gepulste NMR erlaubt mehrdimensionale Spektren: Korrelationen zwischen Signalen Mehrdimensionale Spektren (homo / heteronuklear): Strukturaufklärung von Biomolekülen
18 N171_KernresonanzSpektrometrie_c_BAneu.doc - 18/22 Weitere Beispiele von 1 H-NMR-Spektren NMR-Spektrum der Propionsäure (Propansäure) Ganz rechts, im Nullpunkt der δ-skala, das mit TMS bezeichnete Signal des Tetramethylsilans. Zur Zuordnung sind die Protonengruppen in der chemischen Formel und die entsprechenden Liniengruppen im Spektrum mit Buchstaben gekennzeichnet. NMR-Spektrum von Propionsäuremethylester
19 N171_KernresonanzSpektrometrie_c_BAneu.doc - 19/22 NMR-Spektrum von Propionsäurechlorid (Warum ist die Gruppe (b) im Vergleich zur Propionsäure etwas nach links verschoben? bewirkt durch Austausch von -OH gegen -Cl) NMR-Spektrum von Propionsäureanhydrid NMR-Spektrometrie in der Praxis: Große Tabellenwerke bzw. Datenbanken erleichtern die Zuordnung der Peaks. Ebenso sind verschiedene Computerprogramme auf dem Markt, die dieses Puzzlespiel automatisieren. Beides ersetzt jedoch nicht die Erfahrung des Analytikers!
20 5.4 Grundlagen der Kernspin-Tomographie (ortsaufgelöste NMR) N171_KernresonanzSpektrometrie_c_BAneu.doc - 20/22 Mit Hilfe eines inhomogenen Magnetfeldes erfolgt eine räumliche Zuordnung des NMR-Signals. Dem statischen Magnetfeld B 0 wird ein Gradientenfeld überlagert, das linear in x-richtung zunimmt. B B B( x) B 0 x const. x x Die Präzessionsfrequenz bzw. die Resonanzfrequenz wird dann ortsabhängig. B L( x) ( B0 x) x Links ist die Resonanzfrequenz niedriger als rechts. Es erfolgt eine räumliche Zuordnung des Signals über die Frequenz des Signals (Frequenzkodierung). Die Fouriertransformation (Frequenzanalyse) ergibt dann unmittelbar die Zuordnung der Frequenzskala auf die Ortsskala. Die Signalhöhe wird bestimmt durch die Zahl der Kernspins, die sich senkrecht zur Achse x befinden. Alle Signale aus dieser Senkrechten werden auf einen Punkt auf x-achse projiziert. Man weiß deshalb nicht aus welcher Tiefe das Signal kommt (das Signal ist eindimensional). Projektions-Rekonstruktions-Verfahren (zweidimensionales Signal) Um ein zweidimensionales Bild zu erhalten, misst man das Kernsignal über mindestens zwei Richtungen. Dazu wird das Gradientenfeld gedreht, so dass der Gradient z.b. in y-richtung liegt. B L( y) ( B0 y) y Die Signale der so erhaltenen Projektionen werden überlagert und zu einem Bild rekonstruiert. 4 Phasenkodierung In modernen Kernspin-Tomographen wird mit Hilfe einer sog. Phasenkodierung des Kerninduktionssignals eine dreidimensionale Bildgebung erreicht. Dazu benutzt man Gradientenfelder in den drei Koordinatenrichtungen x, y und z. Die drei Gradientenfelder werden nacheinander kurz eingeschaltet und mit einem Hf-Impuls für jede Koordinate das richtungskodierte Kernresonanzsignal gemessen. 4 Dieses sog. Projektions-Rekonstruktions-Verfahren wurde auch von der Röntgen-Computertomographie übernommen.
21 N171_KernresonanzSpektrometrie_c_BAneu.doc - 21/22 Schema des Prinzips der Kernspin-Tomographie. Die Signale von vier Experimenten mit verschiedenen Feldgradienten-Richtungen (Pfeile) liefern vier verschiedene Projektionen der mit Wasser gefüllten Kapillaren. Diese spektralen Daten dienen zur Rekonstruktion einer zweidimensionalen Repräsentation. Zweidimensionales NMR-Bild, das mit der experimentellen Anordnung erhalten wurde. Zwei mit H 2 O gefüllte Kapillaren von 1 mm Durchmesser wurden in einer zylindrischen Messzelle von 4,2 mm Innendurchmesser, die als Medium eine Mischung von D 2 O und H 2 O enthielt, angebracht.
22 N171_KernresonanzSpektrometrie_c_BAneu.doc - 22/22 Aufgabe NMR (AMX-System)*: Ordnen Sie die Protonensignale im Spektrum der Substanz zu. Geben Sie die chemische Verschiebung der Wasserstoffkerne in Hz an, wenn die Spektren mit einer 100-MHz Anlage gemessen wurden (ein ppm ist dann genau 100 Hz).
Eigenschaften einiger für die NMR-Spektrometrie organischer Verbindungen wichtiger Kerne
 Der Zusammenhang zwischen dem magnetischen Moment eines Atomkerns und seines mechanischen Drehimpulses lautet: μ=γ J, wobei γ das gyromagnetische Verhältnis ist. Der mechanische Drehimpuls ist durch die
Der Zusammenhang zwischen dem magnetischen Moment eines Atomkerns und seines mechanischen Drehimpulses lautet: μ=γ J, wobei γ das gyromagnetische Verhältnis ist. Der mechanische Drehimpuls ist durch die
Das NMR-Experiment in der Vektordarstellung
 Das NMR-Experiment in der Vektordarstellung Kerne mit einer Spinquantenzahl I = ½ ( 1 H, 13 C) können in einem äußeren statischen homogenen Magnetfeld B 0 (Vektorfeld) zwei Energiezustände einnehmen: +½
Das NMR-Experiment in der Vektordarstellung Kerne mit einer Spinquantenzahl I = ½ ( 1 H, 13 C) können in einem äußeren statischen homogenen Magnetfeld B 0 (Vektorfeld) zwei Energiezustände einnehmen: +½
Spektroskopische Methoden in der Organischen Chemie (OC IV) NMR Spektroskopie 1. Physikalische Grundlagen
 NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ
 Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
NMR Spektroskopie. 1nm Frequenz X-ray UV/VIS Infrared Microwave Radio
 NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
NMR - Seite 1. NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie
 NMR - Seite 1 NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie Protonen besitzen ebenso wie Elektronen einen eigenen Spin (Drehung um die eigene Achse).Allerdings gibt es mehrere Möglichkeiten als
NMR - Seite 1 NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie Protonen besitzen ebenso wie Elektronen einen eigenen Spin (Drehung um die eigene Achse).Allerdings gibt es mehrere Möglichkeiten als
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden
 Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Zentralabstand b, Spaltbreite a. Dreifachspalt Zentralabstand b, Spaltbreite a. Beugungsgitter (N Spalte, N<10 4, Abstand a)
 Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Vorbereitung. µ z = mγ h (1) γ = gq 2m wobei q die Ladung und m die Masse des Teilchens beschreiben.
 Physikalisches Fortgeschrittenenpraktikum NMR-Spektroskopie Vorbereitung Armin Burgmeier Robert Schittny 1. Theoretische Grundlagen 1.1. Kerndrehimpuls und magnetisches Moment Nach der Quantentheorie besitzt
Physikalisches Fortgeschrittenenpraktikum NMR-Spektroskopie Vorbereitung Armin Burgmeier Robert Schittny 1. Theoretische Grundlagen 1.1. Kerndrehimpuls und magnetisches Moment Nach der Quantentheorie besitzt
Übungsaufgaben zur NMR-Spektrometrie
 Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Bestimmung der Struktur einer (un)bekannten Verbindung
 Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen
 Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen Seminar 5. 0. 200 Teil : NMR Spektroskopie. Einführung und Physikalische Grundlagen.2 H NMR Parameter: a) Chemische
Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen Seminar 5. 0. 200 Teil : NMR Spektroskopie. Einführung und Physikalische Grundlagen.2 H NMR Parameter: a) Chemische
Magnetresonanztomographie (MRT) * =
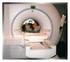 γ * γ π Beispiel: - Protonen ( H) Messung - konstantes B-Feld (T) in -Richtung - Gradientenfeld (3mT/m) in -Richtung - bei 0: f 00 4,6 MH Wie stark ist Frequenveränderung Df der Spins bei 0 mm? f (0mm)
γ * γ π Beispiel: - Protonen ( H) Messung - konstantes B-Feld (T) in -Richtung - Gradientenfeld (3mT/m) in -Richtung - bei 0: f 00 4,6 MH Wie stark ist Frequenveränderung Df der Spins bei 0 mm? f (0mm)
Physikalische Grundlagen der Magnetresonanz-Tomographie MRT
 Physikalische Grundlagen der Magnetresonanz-Tomographie MRT http://www.praxis-nuramed.de/images/mrt_3_tesla.png Seminarvortrag am 30.05.2016 von Nanette Range MRT Bilder Nanette Range 30.05.2016 2 Motivation
Physikalische Grundlagen der Magnetresonanz-Tomographie MRT http://www.praxis-nuramed.de/images/mrt_3_tesla.png Seminarvortrag am 30.05.2016 von Nanette Range MRT Bilder Nanette Range 30.05.2016 2 Motivation
Kernmagnetische Resonanzspektroskopie. N Nuclear M Magnetic R Resonance Beobachtung magnetisch aktiver Kerne in einem äußeren Magnetfeld
 NMR- SPEKTROSKOPIE Prüfungsfrage Radiospektroskopische Methode: NMR. Das Spin und magnetische Moment, die Bedingung der Resonanz, Spektralspaltung, chemische Verschiebung. Kernmagnetische Resonanzspektroskopie
NMR- SPEKTROSKOPIE Prüfungsfrage Radiospektroskopische Methode: NMR. Das Spin und magnetische Moment, die Bedingung der Resonanz, Spektralspaltung, chemische Verschiebung. Kernmagnetische Resonanzspektroskopie
Multipuls-NMR in der Organischen Chemie. Puls und FID
 Puls und FID Obwohl der Puls eine bestimmte, am NMR-Spektrometer vorab eingestellte Sendefrequenz ν 1 hat, ist er in der Lage, über einen relativ weiten Frequenzbereich von mehreren khz, den gesamten Resonanzbereich
Puls und FID Obwohl der Puls eine bestimmte, am NMR-Spektrometer vorab eingestellte Sendefrequenz ν 1 hat, ist er in der Lage, über einen relativ weiten Frequenzbereich von mehreren khz, den gesamten Resonanzbereich
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4.1 Allgemeines Spektroskopische Methode zur Untersuchung von Atomen: elektronische Umgebung Wechselwirkung
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4.1 Allgemeines Spektroskopische Methode zur Untersuchung von Atomen: elektronische Umgebung Wechselwirkung
Kernmagnetismus und Magnetfelder
 Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Einführung: NMR, was ist das? NMR = Nuclear Magnetic Resonance oder zu deutsch: Kernspinresonanz
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Einführung: NMR, was ist das? NMR = Nuclear Magnetic Resonance oder zu deutsch: Kernspinresonanz
2. Magnetresonanztomographie (MRT, MRI) 2.3. Spin und Magnetisierung
 2. Magnetresonanztomographie (MRT, MRI) 2.3. Spin und Magnetisierung Übergang zwischen den beiden Energieniveaus ω l = γb 0 γ/2π Larmor-Frequenz ν L 500 400 300 200 100 ν L = (γ/2π)b 0 [MHz/T] 1 H 42.57
2. Magnetresonanztomographie (MRT, MRI) 2.3. Spin und Magnetisierung Übergang zwischen den beiden Energieniveaus ω l = γb 0 γ/2π Larmor-Frequenz ν L 500 400 300 200 100 ν L = (γ/2π)b 0 [MHz/T] 1 H 42.57
NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz)
 NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz) Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p = ħ I, der ganz - oder halbzahlige Werte von ħ betragen
NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz) Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p = ħ I, der ganz - oder halbzahlige Werte von ħ betragen
NMR Spektroskopie I = 0 : C, 16 O (sogenannte gg-kerne haben immer I=0!) I = 1/2: 1 H, 13 C, 15 N, 19 F, 31 P,... I = 1: 2. H=D, 6 Li, 14 N I = 3/2: 7
 NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
Zusammenfassung des Seminarsvortrags Nuclear magnetic resonance
 Zusammenfassung des Seminarsvortrags Nuclear magnetic resonance Andreas Bünning 9. Januar 2012 Betreuer: Dr. Andreas Thomas Seite 1 3 PHYSIKALISCHE GRUNDLAGEN 1 Motivation Die nuclear magnetic resonance,
Zusammenfassung des Seminarsvortrags Nuclear magnetic resonance Andreas Bünning 9. Januar 2012 Betreuer: Dr. Andreas Thomas Seite 1 3 PHYSIKALISCHE GRUNDLAGEN 1 Motivation Die nuclear magnetic resonance,
Relaxation. Dominik Weishaupt. 2.1 T1: Longitudinale Relaxation T2/T2*: Transversale Relaxation 8
 2 Relaxation 7 7 2 Relaxation Dominik Weishaupt 2.1 T1: Longitudinale Relaxation 8 2.2 T2/T2*: Transversale Relaxation 8 D. Weishaupt, V. D. Köchli, B. Marincek, Wie funktioniert MRI?, DOI 10.1007/978-3-642-41616-3_2,
2 Relaxation 7 7 2 Relaxation Dominik Weishaupt 2.1 T1: Longitudinale Relaxation 8 2.2 T2/T2*: Transversale Relaxation 8 D. Weishaupt, V. D. Köchli, B. Marincek, Wie funktioniert MRI?, DOI 10.1007/978-3-642-41616-3_2,
Kernmagnetische Resonanz NMR
 Kernmagnetische Resonanz: NMR F. Bloch E.M. Purcell: NMR 195 Physik Standard-Technik zur Strukturanalyse in der Organischen Chemie Kernmagnetische Resonanz NMR Kern: Eigenschaft der Atomkerne wird Kernspin
Kernmagnetische Resonanz: NMR F. Bloch E.M. Purcell: NMR 195 Physik Standard-Technik zur Strukturanalyse in der Organischen Chemie Kernmagnetische Resonanz NMR Kern: Eigenschaft der Atomkerne wird Kernspin
Chemisches Grundpraktikum II (270002) Kernresonanzspektroskopie. NMR-Spektroskopie
 hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
Methodische Ansätze zur Strukturaufklärung: Rnt. - Kernmagnetische Resonanzspektroskopie (NMR)
 ? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
NMR Vortag im Rahmen des Fortgeschrittenen-Praktikums
 NMR Vortag im Rahmen des Fortgeschrittenen-Praktikums Martin Fuchs 1 Motivation Die Nuclear Magnetic Resonance, oder zu deutsch Kernspinresonanz ist vor allem durch die aus der Medizin nicht mehr wegzudenkende
NMR Vortag im Rahmen des Fortgeschrittenen-Praktikums Martin Fuchs 1 Motivation Die Nuclear Magnetic Resonance, oder zu deutsch Kernspinresonanz ist vor allem durch die aus der Medizin nicht mehr wegzudenkende
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische Chemie Prof. Dr. B. Dick
 UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische hemie Prof. Dr. B. Dick PHYSIKALISH-HEMISHES PRAKTIKUM (Teil Ic) (Spektroskopie) Versuch NMR Protonenresonanz 0 http://www-dick.chemie.uni-regensburg.de/studium/praktikum1c.html
UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische hemie Prof. Dr. B. Dick PHYSIKALISH-HEMISHES PRAKTIKUM (Teil Ic) (Spektroskopie) Versuch NMR Protonenresonanz 0 http://www-dick.chemie.uni-regensburg.de/studium/praktikum1c.html
Leibniz-Institut für Neurobiologie Speziallabor Nicht-Invasive Bildgebung
 Leibniz-Institut für Neurobiologie Speziallabor Nicht-Invasive Bildgebung Das Magnetische Feld als Folge von Ladungsverschiebungen Gerader stromdurchflossener Leiter Spulenförmiger Leiter Wichtige Kenngrößen
Leibniz-Institut für Neurobiologie Speziallabor Nicht-Invasive Bildgebung Das Magnetische Feld als Folge von Ladungsverschiebungen Gerader stromdurchflossener Leiter Spulenförmiger Leiter Wichtige Kenngrößen
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
Die chemische Verschiebung - 1
 Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
Bildbeispiele Physikalisches Prinzip Hounsfield-Einheiten Bilderzeugung. Strahlenbelastung Bildbeispiele. Hirn - Weichteilfenster
 Prof. Dr. med. P. Schramm Röntgen- Computer-Tomografie Magnet-Resonanz-Tomografie Physikalisches Prinzip Dr. rer. nat. Uwe H. Melchert Röntgen - Computer-Tomografie Bildbeispiele Physikalisches Prinzip
Prof. Dr. med. P. Schramm Röntgen- Computer-Tomografie Magnet-Resonanz-Tomografie Physikalisches Prinzip Dr. rer. nat. Uwe H. Melchert Röntgen - Computer-Tomografie Bildbeispiele Physikalisches Prinzip
MRT. Benoit Billebaut MTRA, Institut für Klinische Radiologie UKM
 MRT Benoit Billebaut MTRA, Institut für Klinische Radiologie UKM WARUM SIND RÖNTGEN UND CT NICHT GENUG? MAGNETRESONANZTOMOGRAPHIE Die Große Frage? "Image by AZRainman.com Wie schaffen wir das überhaupt?
MRT Benoit Billebaut MTRA, Institut für Klinische Radiologie UKM WARUM SIND RÖNTGEN UND CT NICHT GENUG? MAGNETRESONANZTOMOGRAPHIE Die Große Frage? "Image by AZRainman.com Wie schaffen wir das überhaupt?
NMR-Spektroskopie Nuclear Magnetic Resonance - Spektroskopie H2N HO2C CH3
 NMR-Spektroskopie Nuclear Magnetic Resonance - Spektroskopie anwendbar auf Atomkerne mit magnetischem Moment z.b. 1 H, 13 C, und andere Kerne O H 2 N NH HO 2 C Si CH 3 6. 5. 4. 3. 2. 1.. ppm Folie 1 Bedeutung
NMR-Spektroskopie Nuclear Magnetic Resonance - Spektroskopie anwendbar auf Atomkerne mit magnetischem Moment z.b. 1 H, 13 C, und andere Kerne O H 2 N NH HO 2 C Si CH 3 6. 5. 4. 3. 2. 1.. ppm Folie 1 Bedeutung
Kernresonanzspektroskopie
 Gleich geht s los! Kernresonanzspektroskopie 1. Geschichtliche Entwicklung 2. Physikalische Grundlagen 3. Das NMR-Spektrometer 4. Anwendung der 1 H-NMR-Spektren zur Analyse der Konstitution von Molekülen
Gleich geht s los! Kernresonanzspektroskopie 1. Geschichtliche Entwicklung 2. Physikalische Grundlagen 3. Das NMR-Spektrometer 4. Anwendung der 1 H-NMR-Spektren zur Analyse der Konstitution von Molekülen
Einführung in die NMR-Spektroskopie. NMR-Spektroskopie. Teil 1: Einführung und Grundlagen der 1 H NMR. Das NMR Spektrometer
 NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
Spektroskopische Methoden in der Organischen Chemie (OC IV)
 2 3 4 O 1 2 3 1 N 5 6 O 5 4 6 Probleme bei der Interpretation von NMR Spektren großer Moleküle Zuordnung der Resonanzen Bestimmung der geometrischen Beziehungen (Bindungen, Abstände, Winkel) zwischen den
2 3 4 O 1 2 3 1 N 5 6 O 5 4 6 Probleme bei der Interpretation von NMR Spektren großer Moleküle Zuordnung der Resonanzen Bestimmung der geometrischen Beziehungen (Bindungen, Abstände, Winkel) zwischen den
Ferienkurs Experimentalphysik Übung 2 - Musterlösung
 Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
4.57 ppm 1.45 ppm = 3.12 ppm 3.12 ppm * MHz = Hz Hz = rad/sec
 (1) Zwei Signale liegen im Protonenspektrum bei 1.45 und 4.57 ppm, das Spektrometer hat eine Frequenz von 400.13 MHz. Wieweit liegen die Signale in Hz bzw. in rad/sec auseinander? 4.57 ppm 1.45 ppm = 3.12
(1) Zwei Signale liegen im Protonenspektrum bei 1.45 und 4.57 ppm, das Spektrometer hat eine Frequenz von 400.13 MHz. Wieweit liegen die Signale in Hz bzw. in rad/sec auseinander? 4.57 ppm 1.45 ppm = 3.12
Wo ist der magnetische Nordpol der Erde?
 Wo ist der magnetische Nordpol der Erde? A B C D am geographischen Nordpol am geographischen Südpol Nahe am geographischen Südpol Nahe am geographischen Nordpol 3. Magnetische Phänomene 3.1. Navigation,
Wo ist der magnetische Nordpol der Erde? A B C D am geographischen Nordpol am geographischen Südpol Nahe am geographischen Südpol Nahe am geographischen Nordpol 3. Magnetische Phänomene 3.1. Navigation,
Spektroskopiemodul II. H-NMR und 13 C-NMR
 Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
Die Strukturabhängigkeit der chemischen Verschiebung
 Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Teil 3 2D-NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
Magnetische Resonanzmethoden
 Nuclear Magnetic Resonance (NMR) und Electron Spin Resonance (ESR) Kernspinresonanz und Elektronenspinresonanz Wichtige Technik in der organischen Chemie Zahlreiche Anwendungen in der Chemie, Medizin,
Nuclear Magnetic Resonance (NMR) und Electron Spin Resonance (ESR) Kernspinresonanz und Elektronenspinresonanz Wichtige Technik in der organischen Chemie Zahlreiche Anwendungen in der Chemie, Medizin,
Grundlagen der magnetischen Kernresonanz
 Grundlagen der magnetischen Kernresonanz 26.05.2014 Spin und gyromagnetisches Verhältnis Zeeman-Effekt Spin-Präzession Magnetisierung Teilchen haben Spin S Erfüllt Eigenwertgleichungen ˆ S 2 Ψ = s(s +
Grundlagen der magnetischen Kernresonanz 26.05.2014 Spin und gyromagnetisches Verhältnis Zeeman-Effekt Spin-Präzession Magnetisierung Teilchen haben Spin S Erfüllt Eigenwertgleichungen ˆ S 2 Ψ = s(s +
Spektroskopische Methoden in der Organischen Chemie (OC IV) C NMR Spektroskopie
 6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
2) In welcher Einheit wird die Energie (x-achse) im NMR-Spektrum angegeben und wie ist sie definiert?
 Aufgabe 1: Verständnisfragen 1) Welche Eigenschaften eines Atomkerns führen zu einem starken NMR-Signal? (man sagt der Kern hat eine große Empfindlichkeit) Ein Isotop eines Elements wird empfindlich genannt,
Aufgabe 1: Verständnisfragen 1) Welche Eigenschaften eines Atomkerns führen zu einem starken NMR-Signal? (man sagt der Kern hat eine große Empfindlichkeit) Ein Isotop eines Elements wird empfindlich genannt,
Polarisationstransfer
 Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Molekulare Biophysik. NMR-Spektroskopie (Teil 1)
 Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/94 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/94 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Physikalische Grundlagen der Pulsspektroskopie I = ½. I > 1 Komplexe Kopplungsmuster. 2 B Resonanz!
 4. Physikalische Grundlagen der Pulsspektroskopie Dieses Kapitel behandelt das ustandekommen des NMR-Signals sowie einige ausgewählte Messmethoden, die dem Verständnis der 2D-Techniken dienen. Am COS wird
4. Physikalische Grundlagen der Pulsspektroskopie Dieses Kapitel behandelt das ustandekommen des NMR-Signals sowie einige ausgewählte Messmethoden, die dem Verständnis der 2D-Techniken dienen. Am COS wird
Kernspinresonanz - NMR
 Kernspinresonanz - NMR Referent: Pierre Sissol 10. Mai 2010 Seminar in Kern- und Teilchenphysik zum Fortgeschrittenenpraktikum 2 im SoSe 2010 Johannes-Gutenberg-Universität Mainz Betreuer: Dr. Andreas
Kernspinresonanz - NMR Referent: Pierre Sissol 10. Mai 2010 Seminar in Kern- und Teilchenphysik zum Fortgeschrittenenpraktikum 2 im SoSe 2010 Johannes-Gutenberg-Universität Mainz Betreuer: Dr. Andreas
Fortgeschrittenenpraktikum
 Fortgeschrittenenpraktikum Nuclear Magnetic Resonance (NMR) Standort: Physikgebäude, Raum PHY D012 Versuchsdurchführung: - Donnerstag: 11-17 Uhr - Freitag: 8-16 Uhr - Im Sommersemester können die Anfangszeiten
Fortgeschrittenenpraktikum Nuclear Magnetic Resonance (NMR) Standort: Physikgebäude, Raum PHY D012 Versuchsdurchführung: - Donnerstag: 11-17 Uhr - Freitag: 8-16 Uhr - Im Sommersemester können die Anfangszeiten
Kernspinresonanztomographie (NMR)
 Kernspinresonanztomographie (NMR) Einleitung Physikalische Grundlagen: Makroskopische Kernmagnetisierung Präzession der Kernmagnetisierung Kernresonanzexperiment Blochsche Gleichungen/Relaxation Selektive
Kernspinresonanztomographie (NMR) Einleitung Physikalische Grundlagen: Makroskopische Kernmagnetisierung Präzession der Kernmagnetisierung Kernresonanzexperiment Blochsche Gleichungen/Relaxation Selektive
Homonukleare Korrelationsspektroskopie (COSY)
 Homonukleare Korrelationsspektroskopie (COSY) Hier wird ähnlich wie bei HETCOR in beiden Dimensionen die chemische Verschiebung abgebildet. Im homonuklearen Fall ( 1 H, 1 H COSY) jedoch, ist es in beiden
Homonukleare Korrelationsspektroskopie (COSY) Hier wird ähnlich wie bei HETCOR in beiden Dimensionen die chemische Verschiebung abgebildet. Im homonuklearen Fall ( 1 H, 1 H COSY) jedoch, ist es in beiden
Bericht zum Versuch Gepulste Kernspinresonanz
 Bericht zum Versuch Gepulste Kernspinresonanz Anton Haase, Michael Goerz 22. Januar 27 Freie Universität Berlin Fortgeschrittenenpraktikum Teil A Tutor: M. Brecht Inhalt 1 Einführung 2 1.1 Kernspin................................
Bericht zum Versuch Gepulste Kernspinresonanz Anton Haase, Michael Goerz 22. Januar 27 Freie Universität Berlin Fortgeschrittenenpraktikum Teil A Tutor: M. Brecht Inhalt 1 Einführung 2 1.1 Kernspin................................
Spin-Echo und J-Modulation; APT
 Spin-Echo und J-Modulation; APT Stellen wir uns ein PFT-Experiment vor, bei dem ν = ν 0 - ν 1 = 0 und der Puls ein 90 0 -Puls sein soll. Außerdem wollen wir der Einfachheit halber zunächst annehmen, dass
Spin-Echo und J-Modulation; APT Stellen wir uns ein PFT-Experiment vor, bei dem ν = ν 0 - ν 1 = 0 und der Puls ein 90 0 -Puls sein soll. Außerdem wollen wir der Einfachheit halber zunächst annehmen, dass
III. Strukturbestimmung organischer Moleküle
 III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
VL Spin-Bahn-Kopplung Paschen-Back Effekt. VL15. Wasserstoffspektrum Lamb Shift. VL16. Hyperfeinstruktur
 VL 16 VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2. Paschen-Back Effekt VL15. Wasserstoffspektrum 15.1. Lamb Shift VL16. Hyperfeinstruktur 16.1. Hyperfeinstruktur 16.2. Kernspinresonanz
VL 16 VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2. Paschen-Back Effekt VL15. Wasserstoffspektrum 15.1. Lamb Shift VL16. Hyperfeinstruktur 16.1. Hyperfeinstruktur 16.2. Kernspinresonanz
 Übungen zu Experimentalphysik 4 - Lösungsvorschläge Prof. S. Paul Sommersemester 005 Dr. Jan Friedrich Nr. 5 16.05.005 Email Jan.Friedrich@ph.tum.de Telefon 089/89-1586 Physik Department E18, Raum 3564
Übungen zu Experimentalphysik 4 - Lösungsvorschläge Prof. S. Paul Sommersemester 005 Dr. Jan Friedrich Nr. 5 16.05.005 Email Jan.Friedrich@ph.tum.de Telefon 089/89-1586 Physik Department E18, Raum 3564
1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie
 Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment
 Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
1. Allgemeine Grundlagen Quantenmechanik
 1. Allgemeine Grundlagen 1.3. Quantenmechanik Klassische Mechanik vs Quantenmechanik Klassische (Newton sche) Mechanik klassischer harmonischer Oszillator Quantenmechanik quantenmechanischer harmonischer
1. Allgemeine Grundlagen 1.3. Quantenmechanik Klassische Mechanik vs Quantenmechanik Klassische (Newton sche) Mechanik klassischer harmonischer Oszillator Quantenmechanik quantenmechanischer harmonischer
Spektroskopie-Seminar WS 17/18 5 NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
2.5 Evolution der Spins im Magnetfeld
 - 43-2.5 Evolution der Spins im Magnetfeld 2.5.1 Drehimpuls und Drehmoment Wenn wir die Bewegung eines Spins im Magnetfeld betrachten, so müssen wir zunächst den Einfluss des Magnetfeldes auf den assoziierten
- 43-2.5 Evolution der Spins im Magnetfeld 2.5.1 Drehimpuls und Drehmoment Wenn wir die Bewegung eines Spins im Magnetfeld betrachten, so müssen wir zunächst den Einfluss des Magnetfeldes auf den assoziierten
Edelgas-polarisierte. NMR- Spektroskopie. Jonas Möllmann Jan Mehlich. SoSe 2005
 Edelgas-polarisierte NMR- Spektroskopie Jonas Möllmann Jan Mehlich SoSe 2005 NMR Prinzip Aufspaltung der Kernspins in verschiedene Niveaus durch angelegtes Magnetfeld Messung des Besetzungs- unterschiedes
Edelgas-polarisierte NMR- Spektroskopie Jonas Möllmann Jan Mehlich SoSe 2005 NMR Prinzip Aufspaltung der Kernspins in verschiedene Niveaus durch angelegtes Magnetfeld Messung des Besetzungs- unterschiedes
Kernmagnetische Resonanz
 Strahlung Kernmagnetische Resonanz Die verschiedenen Arten der Spektroskopie nutzen die Adsorption, Emission oder Streuung von Strahlen an Atomen oder Molekülen. Die Kernresonanzspektroskopie im speziellen
Strahlung Kernmagnetische Resonanz Die verschiedenen Arten der Spektroskopie nutzen die Adsorption, Emission oder Streuung von Strahlen an Atomen oder Molekülen. Die Kernresonanzspektroskopie im speziellen
Seminar WiSe 2015/2016. PD Dr. Markus Nett. Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: jena.
 Kernresonanzspektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: markus.nett@hki jena.de NMR = nuclear
Kernresonanzspektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: markus.nett@hki jena.de NMR = nuclear
15.Magnetostatik, 16. Induktionsgesetz
 Ablenkung von Teilchenstrahlen im Magnetfeld (Zyklotron u.a.): -> im Magnetfeld B werden geladene Teilchen auf einer Kreisbahn abgelenkt, wenn B senkrecht zu Geschwindigkeit v Kräftegleichgewicht: 2 v
Ablenkung von Teilchenstrahlen im Magnetfeld (Zyklotron u.a.): -> im Magnetfeld B werden geladene Teilchen auf einer Kreisbahn abgelenkt, wenn B senkrecht zu Geschwindigkeit v Kräftegleichgewicht: 2 v
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
Grundlagen der Kernspintomographie (NMR) Richard Bauer, JLU Gießen
 Grundlagen der Kernspintomographie (NMR) Richard Bauer, JLU Gießen Physikalische Grundlagen der Bildgebung Röntgen, CT Ultraschall Szintigraphie MR-Tomographie Absorption von Röntgenstrahlen Änderung der
Grundlagen der Kernspintomographie (NMR) Richard Bauer, JLU Gießen Physikalische Grundlagen der Bildgebung Röntgen, CT Ultraschall Szintigraphie MR-Tomographie Absorption von Röntgenstrahlen Änderung der
NMR-Lösungsmittel. 1 H-NMR. Bei der Verwendung der normalen, nichtdeuterierten Lösungsmittel. Spektroskopie in der Organischen Chemie
 NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
Molekulare Biophysik. NMR-Spektroskopie (Teil 1)
 Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/93 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/93 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Bestimmung der Struktur einer (un)bekannten Verbindung
 Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektroskopie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie neue Produktlinie,
Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektroskopie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie neue Produktlinie,
Molekulare Biophysik. NMR-Spektroskopie (Teil 2)
 Molekulare Biophysik NMR-Spektroskopie (Teil 2) NMR-Parameter NMR-Parameter 3/88 Folgenden NMR-Parameter sind von Interesse chemische Verschiebung skalare Kopplung Relaxation / NOE-Effekt NMR-Parameter
Molekulare Biophysik NMR-Spektroskopie (Teil 2) NMR-Parameter NMR-Parameter 3/88 Folgenden NMR-Parameter sind von Interesse chemische Verschiebung skalare Kopplung Relaxation / NOE-Effekt NMR-Parameter
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
PD Para- und Diamagnetismus
 PD Para- und Diamagnetismus Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Magnetfeld in Materie............................ 2 1.2 Arten von Magnetismus...........................
PD Para- und Diamagnetismus Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Magnetfeld in Materie............................ 2 1.2 Arten von Magnetismus...........................
Spektroskopische Methoden in der Organischen Chemie (OC IV)
 H 3 C 10 O G F D E 8 5 I H GF E D CB A 10 8 5 3 2 1 125 MHz 13 C NMR Spektrum 500 MHz 1 H NMR Spektrum NMR -_1 32 1 H 3 C 10 8 5 10 O G F D E 8 5 Dieder-Winkel: H 10 -H : 5, H -H : 80 H H 8 : 2, H -H :
H 3 C 10 O G F D E 8 5 I H GF E D CB A 10 8 5 3 2 1 125 MHz 13 C NMR Spektrum 500 MHz 1 H NMR Spektrum NMR -_1 32 1 H 3 C 10 8 5 10 O G F D E 8 5 Dieder-Winkel: H 10 -H : 5, H -H : 80 H H 8 : 2, H -H :
Atome im elektrischen Feld
 Kapitel 3 Atome im elektrischen Feld 3.1 Beobachtung und experimenteller Befund Unter dem Einfluss elektrischer Felder kommt es zur Frequenzverschiebung und Aufspaltung in optischen Spektren. Dieser Effekt
Kapitel 3 Atome im elektrischen Feld 3.1 Beobachtung und experimenteller Befund Unter dem Einfluss elektrischer Felder kommt es zur Frequenzverschiebung und Aufspaltung in optischen Spektren. Dieser Effekt
Grundlagen der NMR-Spektroskopie
 Westfälische Wilhelms-Universität Münster Institut für Pharmazeutische und Medizinische Chemie 8. Semester Übersicht: Einleitung Physikalische Grundlagen Magnetische Kerne Resonanz Spektrometer 1 Chem.
Westfälische Wilhelms-Universität Münster Institut für Pharmazeutische und Medizinische Chemie 8. Semester Übersicht: Einleitung Physikalische Grundlagen Magnetische Kerne Resonanz Spektrometer 1 Chem.
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld
 Simon Lewis Lanz 2015 simonlanzart.de Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld Zeeman-Effekt, Paschen-Back-Effekt, Fein- und Hyperfeinstrukturaufspaltung Fließt elektrischer Strom
Simon Lewis Lanz 2015 simonlanzart.de Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld Zeeman-Effekt, Paschen-Back-Effekt, Fein- und Hyperfeinstrukturaufspaltung Fließt elektrischer Strom
3.7 Gekoppelte Spinsysteme
 - 47-3.7 Gekoppelte Spinsysteme 3.7. Matrixdarstellung von Operatoren in Systemen mit mehreren Spins Um Rechnungen für Systeme aus mehr als einem Spin durchführen zu können, müssen wir die Matrixdarstellungen
- 47-3.7 Gekoppelte Spinsysteme 3.7. Matrixdarstellung von Operatoren in Systemen mit mehreren Spins Um Rechnungen für Systeme aus mehr als einem Spin durchführen zu können, müssen wir die Matrixdarstellungen
Spinsysteme. AX 3 -Spinsystem
 Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Der Kern-Overhauser-Effekt (Nuclear Overhauser Effect, NOE)
 Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
Übungsaufgaben NMR-Spektroskopie (1)
 Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester # 29,30 11/12/2008 und 16/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Magnetische Kernresonanz Spins im Magnetfeld, Relaxation, Bildgebung Magnetische
Physik für Mediziner im 1. Fachsemester # 29,30 11/12/2008 und 16/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Magnetische Kernresonanz Spins im Magnetfeld, Relaxation, Bildgebung Magnetische
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil I. Peter Schmieder AG NMR
 Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil I Das Programm 2/108 Wintersemester 2007/2008 10 Termine: 24.10.07, 31.10.07, 07.11.07, 14.11.07,
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil I Das Programm 2/108 Wintersemester 2007/2008 10 Termine: 24.10.07, 31.10.07, 07.11.07, 14.11.07,
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III. Peter Schmieder AG NMR
 Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III Programm 2/92 Was haben wir uns letztes Mal angeschaut: Wie beschreibt man Experimente mit Produktoperatoren Wie funktioniert
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III Programm 2/92 Was haben wir uns letztes Mal angeschaut: Wie beschreibt man Experimente mit Produktoperatoren Wie funktioniert
Molekulare Biophysik. NMR-Spektroskopie (Teil 2)
 Molekulare Biophysik NMR-Spektroskopie (Teil 2) 3/96 Folgenden NMR-Parameter sind von Interesse chemische Verschiebung skalare Kopplung dipolare Kopplung Relaxation / NOE-Effekt 4/96 Chemische Verschiebung
Molekulare Biophysik NMR-Spektroskopie (Teil 2) 3/96 Folgenden NMR-Parameter sind von Interesse chemische Verschiebung skalare Kopplung dipolare Kopplung Relaxation / NOE-Effekt 4/96 Chemische Verschiebung
