Isomerie von Nickel(П)-komplexen. VI. Über zwei isomere Formen des Ni(NCS) 2 (Chinolin) 2 2H 2 0
|
|
|
- Julius Lenz
- vor 6 Jahren
- Abrufe
Transkript
1 Isomerie von Nickel(П)-komplexen. VI. Über zwei isomere Formen des Ni(NCS) 2 (Chinolin) 2 2H 2 0 E. JONA, T. ŠRAMKO und J. GAŽO Lehrstuhl für anorganische Chemie der SlowakiscJien Technischen Hochschule, S80 37 Bratislava Eingegangen am 20. Dezember 1971 Gewidmet dem Korrespondierenden Mitglied der Slowakischen Akademie der Wissenschaften M. Gregor zu seinem 70. Geburtstag Durch unterschiedliche Kristallisationstemperatur wurden aus einer wäßrig-alkoholischen Lösung zwei isomere Formen von Ni(NCS)2Q2 2H2O (Q = Chinolin) bereitet. Aus Diffrakt ions -Pulveraufnahmen wurde festgestellt, daß das Isomer /, das durch Kristallisation bei 70 C gebildet wurde, nach Zerreiben und Stehenlassen bei 20 C in das thermodynamisch stabilere Isomer II übergeht. Aus den Reflexionsspektren geht hervor, daß beide Komplexe eine hexakoordinierto. pseudooktaedrische Struktur aufweisen. Die Ultrarotabsorptionsspektren zeigen, daß beim Isomer I die NCS-Gruppe endständig gebunden ist, was die Zusammensetzung des Komplexes [Ni(NCS)2(H 2 0)2Q2] erforderlich macht, während beim Isomer II die NCS-Gruppe sowohl endständig gebunden als auch in Brückenbindung vorhanden ist, was wiederum die Zusammensetzung des Komplexes [Ni(NCS)2Q2] 2H2O notwendig macht. Aus den strukturellen Unterschieden kann man schließen, daß es sich hier um ein Paar von Hydrat isomeren handelt. Two isomerie forms of Ni(NCS)2Q2 2H2O (Q = quinoline) were prepared at different crystallization temperatures from aqueous-alcoholic solutions. It was found on the basis of diffraction powder patterns that the isomer I prepared by crystallization at 70 C turned to the thermodynamically more stable isomer II after trituration and standing at 20 C. It follows from the diffuse reflectance spectra that both complexes have a six-coordinate, pseudooctahedral structure. The infrared absorption spectra have shown that in the isomer / there are the terminal NCS groups what corresponds to the composition [Ni(NCS)2(H20)2Q2] while in the isomer II there are the terminal NCS groups as well as NCS bridges what requires the composition [Ni(NCS)2Q2] 2H2O. It ensues from structural differences that these two forms have the character of hydrate isomers. Wenn auch bisher schon eine große Zahl von Nickel(II)-komplexen mit verschiedenen Liganden bereitet wurde, so kommen in der Literatur doch nur selten Angaben über verschiedene Modifikationen dieser Stoffe vor. Das Auffinden von Arbeitsvorgängen, die zur Herstellung von verschiedenen isomeren Nickel(II)-verbindungen führen, würde 14c О
2 E. JÓNA, T. ŠRAMKO, J. GAŽO deren Anzahl erweitern, zur Erkenntnis des Mechanismus ihrer Entstehung und damit gleichzeitig auch des Mechanismus der Substitutionsreaktionen bei Nickel(II)-komplexen beitragen [1 3]. In den vorangegangenen Arbeiten [4 7] haben wir gezeigt, daß für Nickel(II)-komplexe am typischesten die Konfigurationsisomere sind, und daß für deren Bildung insbesondere Liganden mit delokalisierten n -Bindungen (NCS-Gruppe, Chinolin und dessen Derivate u. dgl.) geeignet erscheinen. Weiter haben wir festgestellt, daß es oft möglich ist, zwei Isomere durch Kombination einer homogenen und einer heterogenen Reaktion darzustellen, gegebenenfalls auch nur durch eine heterogene Reaktion unter verschiedenen Bedingungen [5, 8, 9]. Beim Studium der Konfigurationsisomere von Ni(NCS)2Q2 stellten wir zwei strukturell voneinander abweichende Komplexe von Ni(NCS)2Q2 2H2O dar. Die Erklärung für diese strukturellen Unterschiede (mit Hilfe indirekter physikalisch-chemischer Methoden) sowie der Bedingungen für ihre Entstehung hat sich die vorliegende Arbeit zum Ziel gesetzt. Experimenteller Teil Chemikalien und analytische, Methoden NiCb 6H2O p. a., KNCS p. a. und Chinolin p. a. waren tschechoslowakische Erzeugnisse. Das Chinolin wurde von der Verwendung durch Destillation bei vermindertem Druck gereinigt. Der Gehalt an Nickel wurde komplexometrisch gegen Murexid bestimmt. Der Gehalt an Stickstoff, Kohlenstoff und Wasserstoff wurde nach gebräuchlichen Methoden der organischen Elementaranalyse ermittelt. Darstellung der Verbindungen Bei der Darstellung der beiden Komplexe Ni(NCS)2Q2 2H2O (I und II) sind wir von den bei der Darstellung von Ni(NCS)2Q4 2H2O [5], sowie der analogen Komplexe mit Lepidin [6] gewonnenen Erkenntnissen ausgegangen. Bei der Darstellung des Komplexes / wurde folgendes Verfahren angewandt: 0,04 Mol NÍCI2 6H2O wurden in 80 ml Äthanol gelöst und 0,08 Mol zerriebene festes KNCS hinzugefügt. Das ausgeschiedene KCl wurde abfiltriert und zur klaren Lösung von Ni(NCS)2 wurden 10 ml Chinolin zugesetzt. Die entstandene Lösung wurde im Trockenschrank bei einer Temperatur von 70 C eingedickt. Die in 24 Stdn. ausgeschiedenen dunkelgrünen, stäbchenförmigen Kristallenen wurden mit Äthanol gewaschen und an der Luft getrocknet. Durch Zerreiben und Stehenlassen von Komplex I an der Luft für die Dauer von 7 10 Tagen entsteht der Komplex II. Dieser Komplex kann aber auch durch Kristallisation aus der Lösung (ein analoges Verfahren wie beim Komplex I, jedoch bei Laboratoriumstemperatur) während 14 Tagen bereitet werden. Zugleich mit diesem Komplex kristallisiert indessen auch der Komplex Ni(NCS)2Q4 2H2O aus, so daß für die Darstellung des Komplexes II in reiner Form der vorher geschilderte Vorgang vorteilhafter ist. Für Ni(NCS) 2 (Cc)H 7 N)2 2H2O (469,24) berechnet: 12,50% Ni, 12,15% N, 51,20% C, 3,87% H; gefunden: Komplex I: 12,49% Ni, 12,01% N, 50,80% C, 4,10% H; Komplex II: 12,40%JNii, 12,21% N, 51,42% C, 3,93% H. 146
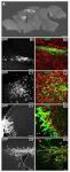
3 ISOMERIE VON NICKEL(II)-KOMPLEXEN. VI Apparatur Die Diffraktions-Pulveraufnahmen der zu untersuchenden Proben wurden mit dem Pulver-Diffraktographen GON II (Chirana) mit automatischer Registrierung der diffraktionierten Strahlung gemessen. CuK a -Strahlung wurde angewandt. Bedingungen des Röntgenaufnahmeverfahrens: Spannung 36 kv, Strom 10 ma, Zeitkonstante des Geräts 8, Empfindlichkeit 500. Die Schiobungsgeschwindigkeit des Schenkels und des Papiers betrug 1 /Minute. Die Reflexionsspektren der Pulverproben im sichtbaren Bereich wurden auf dem Spektralphotometer SF-10 sowjetischer Erzeugung gemessen. Die Ultrarotabsorptionsspektren der festen Proben wurden mittels KBr-Technik und in Nujol mit einem Doppelstrahl-Spektralphotometer UR-10 (Zeiss, Jena) im Bereich von , bzw cm -1 gemessen. Beide Techniken gaben übereinstimmende Absorptionsspektren. Ergebnisse und Diskussion Im Zusammenhang mit dem Studium der isomeren Koordinationsverbindungen tritt das Problem ihrer Darstellung und Identifizierung in den Vordergrund. Die Darstellung von Isomeren aus einer Lösung in reinem Zustand wird allgemein [10] durch die geringe Geschwindigkeit der Isomerisierung und durch die beträchtlich unterschiedliche Löslichkeit der einzelnen Isomere bedingt. Deshalb sind sehr wenige Arbeiten über die Darstellung von Isomeren kinetisch labiler Koordinationsverbindungen bekannt, zu denen auch die Komplexe von Ni(II) gehören. In der vorliegenden Arbeit sind wir vor allem von den Erkenntnissen ausgegangen, die wir bei der Darstellung analoger Komplexe mit Lepidin [6] erhalten haben, bei denen wir durch Änderung der Temperatur mehrere Hydrate der Isothiocyanatonickel(II)- -komplexe mit Lepidin darstellen konnten. Im Falle des Ni(NCS)2Q2 2H 2 0 haben wir in Abhängigkeit von der Temperatur zwei isomere Formen (/ und II) bereitet. Ihre Bildung kann schematisch folgend veranschaulicht werden: Kristallisation t = 70 C Ni(NCS) 2 Q 2 2H 2 0 (/) Lösung Ni(NCS) 2 : Q = 1 : 2 feste Phase, t = 20 C t = 20 C -> Ni(NCS) 2 Q 2 2H 2 0 (II) Kristallisation Zur Identifizierung dieser Verbindungen benutzten wir Diffraktions-Pulveraufnahmen, Reflexions- und Ultrarotabsorptionsspektren. Die Diffraktions-Pulveraufnahmen des Komplexes / in Abhängigkeit von der Zeit, und des Komplexes II sind in Abb. 1 dargestellt. Für den Komplex / sind insbesondere die Diffraktionslinien bei 2# = 8 30' (sehr intensiv); 10 24'; 11 30'; 16 54' und 22 30' charakteristisch. Nach Zerreiben der Probe und nach ihrem Stehenlassen an der Luft sinkt allmählich die Intensität der angeführten Banden und zwei neue Banden treten bei 2ů = 12 42' und 20 54' auf (Abb. 16), die wiederum für den Komplex II charakteristisch sind. Aus den angeführten Aufnahmen geht hervor, daß der Gehalt an dem Ausgangskomplex I nach und nach abnimmt und daß die einzig entstehende kristalline Komponente der strukturell abweichende Komplex II ist. 147
4 E. JÓNA, T. ŠRAMKO, J. GAŽO i i,2 2 Abb. 1. Diffraktogramme des Komplexes I (a); I und II. (b); II (с). l _L b illiiill ii LuiiL LL_L_LL 11 II in, H M L_L tf i! Information über die Gestalt des Koordinationspolyeders der beiden Komplexe haben wir aus den Reflexionsspektren und aus den Ergebnissen der magnetischen Messungen [1] erhalten. Wie aus Abb. 2 hervorgeht, sind die analogen Reflexionsspektren der beiden Komplexe durch eine zusammengesetzte Absorptionsbande mit einem Maximum bei cm -1 und einer Seiten-Schulter bei ~ cm- 1 (Komplex /), resp. bei und ~ cm -1 (Komplex II) charakterisiert. Die Absorptionsbande im Bereich von cm -1 (mit einem Maximum unterhalb 400 nm) wird teilweise durch die Bande der Ladungsübertragung [11, 12] überdeckt. Auf Grund der obigen Ausführungen sowie = der Ergebnisse der magnetischen Messungen des Komplexes II (^eff 3,23 B. M. bei Laboratoriumstemperatur) [4] besteht die Möglichkeit, diese beiden Isomere als paramagnetische, pseiidooktaedrische Komplexe zu betrachten. Nachdem die Messungen nicht bei Wellenzahlen durchgeführt wurden, die niedriger als cm -1 und höher als cm -1 lagen, ist es nicht möglich, die Absorptionsbanden eindeutig zu identifizieren, jedoch in Anbetracht der in Erwägung gezogenen heterogenen, primären Koordinationssphäre, wird bei den beiden Isomeren eine erhebliche tetragonale Distorsion angenommen und in Übereinstimmung mit den Ergebnissen anderer Autoren [13, 14] kann man die Absorptionsbanden bei ~13 800, resp. bei cm -1 und bei , resp cm -1 den Übergängen 3 J3i g -> M 2g, resp. 3 B íg -> 3 E g (F), und die Bande im Bereich von cm -1 dem Übergang 3 B ig -> 3 E g (P) im schwachen, tetragonalen Symmetriefeld D AH zuzuschreiben. Eine analoge Spaltung der ersten Bande im angeführten Bereich wird auch im Reflexionsspektrum des pseudooktaedrischen, paramagnetischen Isomers Ni(NCS) 2 Q 2 [5], Ni(NCS) 2 (Lepidin) 2 [6, 7] sowie auch des Ni(NCS) 2 (Thiosemicarbazid) 2 [15] wahrgenommen, bei welchem die tetragonale Distorsion des Grundpolyeders auch durch die Röntgenstrukturanalyse [16] bestätigt wurde. Die Reflexionsspektren und die magnetische Susceptibilität des Komplexes II [4] weisen auf eine pseudooktaedrische Konfiguration dieser Verbindungen hin. Aus den angeführten Angaben kann indessen nicht auf die Zusammensetzung ihrer Koordinationssphäre gefolgert werden. Bei den Erwägungen zu dieser Frage gingen wir von der Analogie mit dem Komplex Ni(NCS) 2 Q4 * 2H 2 0 aus, wo wir auf Grund eigener Ergebnisse mit Hilfe indirekter Methoden [8] sowie von Literaturangaben [17] resp. von Mißerfolgen bei der Darstellung der Komplexe NiX 2 Qa (X = Halogenid) aus sterischen Gründen [18] die Zusammensetzung der primären Koordinationssphäre des [Ni(NCS) 2 (H 2 0) 2 Q 2 ] 148
5 ISOMERIE VON :N T ICKEL(ID-KOMPLEXEN. VI \[nm] \ / ^ angenommen haben, wobei wir das verbleibende Chinolin, das außerhalb der Koordinationssphäre gebunden ist, als einen Bestandteil der kristallinen Phase [8] angesehen haben. Eine derartige Zusammensetzung der primären Koordinationssphäre anzimehmen wäre auch im Falle der Komplexe von Ni(NCS)2<32 2ШО möglich. Allerdings deuten die magnetischen Eigenschaften des thermodynamisch stabileren Komplexes II (G = = 18 K, das Anwachsen des magnetischen Moments mit dem Sinken der Temperatur) [4], die analog zu denen des grünen Isomers Ni(NCS)2Q2 sind, wiederum darauf hin, daß diese beiden Komplexe hinsichtlich der Funktion der Liganden eine analoge Struktur aufweisen. Es ist also durchaus angängig anzunehmen, daß im Komplex Ni(NCS)2Q2 " 2H2O (II) die Wassermoleküle nicht zum Ni(II) koordiniert, sondern in der sekundären Sphäre gebunden sind. Bei der Lösung des Problems der Zusammensetzung der primären Koordinationssphäre haben wir uns auf die Art und Weise der Bindung der NCS-Gruppe in diesen Komplexen eingestellt. Zu diesem Zweck benutzten wir Ultrarotabsorptionsspektren. Wir untersuchten insbesondere die Bereiche von cm -1 {v(c N)) und von cm-i (v(c S)). Beim Komplex / beobachtet man (Abb. 3a) bei 2125 cm -1 eine intensive Bande, die der Schwingung C N entspricht. Bei den analogen Komplexen mit 4-Methylchinolin (Lepidin) mit der primären Koordinationssphäre von [Ni(NCS)2(H20)2Lep2] wurden gleichermaßen [6] Banden erst bei 2122, resp cm -1 festgestellt. Die Verschiebung dieser Banden in Richtung der Wellenzahlen, die höher sind als für die Koordination M NCS [19, 20] angegeben wird, haben wir [6] durch die Anwesenheit von Wasser in der primären Koordinationssphäre zu erklären versucht. Bei weiteren Komplexen mit Lepidin, in denen in der primären Koordinationssphäre keine Wassermoleküle vorkommen, wurden nämlich Banden der Schwingungen C N unterhalb 2100 cm -1 wahrgenommen. Auf Grund dieser Angaben sowie auch der abgelesenen v(c S) bei 775 cm -1 (Abb. 36) ist es möglich, beim Komplex I anzunehmen, daß die NCS-Gruppe endständig über das Stickstoffatom gebunden ist, weil die Absorptionsbande im Bereich von cm- 1, die für die Konfiguration von Ni SCN angegeben wird, fehlt [19, 21]. Die endständig gebundene NCS-Gruppe beim Komplex I macht jedoch die Zu- J%- 80 ~ V-70" J [cm- 1 ] Abb. 2. Reflexionsspektren des Komplexes / (a) und II (b) /. V a ^ ^ 10' 2 [cn _l l I l l! ř Abb. 3. Ultrarotabs( rp t i onsspektr u m des Komplexes / (a. b) und II (c, d). i JQ
6 E. JÓNA, T. ŠBAMKO, J. GAŽO sammensetzung der primären Koordinationssphäre von [Ni(NCS)2(H20)2Q2] erforderlich. Bei der Koordination der Wassermoleküle zum Metallatom treten im Bereich von cm -1 weitere Banden in Erscheinung, die der Schwingung M О entsprechen. So wurde z. B. bei den Komplexen NÍ(H 2 0)GC12 und Ni(H20)eSC>4 * H2O eine entsprechende Bande bei 810 cm~i [22], beim Komplex [Ni(NCS) 2 (H 2 0)Q 2 ] 2Q bei 823 cm-* [6] beobachtet. Eine solche Bande haben wir jedoch beim Isomer I direkt nicht festzustellen vermocht, aller Wahrscheinlichkeit nach zufolge deren Überdeckung durch die Banden des Chinolins (in Abb. 36, d mit einem Ringlein bezeichnet), die die Interpretation des Spektrums im angeführten Bereich komplizieren. Es scheint, daß es sich hier um die Bande des Chinolins bei 823 cm -1 handelt, die in Richtung zu höheren Wellenzahlen, als die bei analogen Komplexen mit Chinolin [5] beobachtet wurden, verschoben ist. Beim Komplex II werden im Bereich der Schwingungen C N (Abb. 3c) zwei inten - Banden bei 2125 und 2158 cm -1 beobachtet, von denen die zweite Bande deutlich in Richtung zu höheren Wellenzahlen, als die bei analogen Komplexen des Typs Ni(NCS)2L2 [23] festgestellt wurden, verschoben ist. Auf Grund dieser Verschiebung sowie auch der Existenz von zwei Schwingungen C S bei 777 und 760 cm -1 (Abb. 3d) nehmen wir an, daß beim Komplex II zwei koordinativ verschiedenartig gebundene Rhodangruppen vorhanden sind, u. zw. eine endständig gebundene (über den Stickstoff) und eine mit Brückenbindung, wahrscheinlich tridentat, wie beim Ni(NCS)2 (v(c N) bei 2165 cm -1 ) [24]. Analog wurden beim pseudooktaedrischen Isomer von Ni(NCS)2Q2 zwei Banden der Schwingungen C N bei 2114 und 2153 cm -1 festgestellt und gleichermaßen interpretiert [5]. Die verschieden gebimdenen NCS-Gruppen beim Komplex II seil ließen das Vorhandensein von Wasser in der primären Koordinationssphäre aus, was mit den magnetischen Messungen [4] übereinstimmt. Beim Studium der thermischen Eigenschaften beider Isomere wurde festgestellt, daß die für das Ablösen der WassermoleküJe und für die Reorganisation des Aufbaues des Isomers I notwendige Energie wesentlich niedriger ist als jene beim Isomer II [25]. Dies ist im Einklang mit den Erkenntnissen [26] über das thermische Verhalten der Hydrate von Übergangsmetallen, die koordiniertes und Strukturwasser enthalten. Folglich kann abschließend konstatiert werden, daß man durch unterschiedliche Temperatur bei der Kristallisation aus wäßrig-alkoholischer Lösung zwei isomere Formen des Komplexes Ni(NCS)2Q2 * 2H2O (tetragonal-bipyramidaler Struktur) darzustellen vermag, die sich durch eine unterschiedliche Anordnung der primären Koordinations - Sphäre voneinander unterscheiden. Beim thermodynamisch weniger stabilen Isomer / ist die NCS-Gruppe endständig gebunden, was die Zusammensetzung des Komplexes [Ni(NCS)2(H 2 0)2Q2] erforderlich macht, wohingegen beim Isomer II die NCS-Gruppe end ständig gebunden und auch in Brückenbindung erscheint, was wiederum die Zusammensetzung des Komplexes [Ni(NCShQ2] ' 2H2O als notwendig erscheinen läßt. Der Fall dieser Isomere kann deshalb durch eine Hydratisomerie erklärt werden. Literatur 1. Jona, E., Sramko, T. und Gažo, J., Chem. Zvesti 22, 648 (1968). 2. Jona, E., Jesenak, V und Sramko, Т., Chem. Zvesti 23, 420 (1969). 3. Jona, E., Šramko, Т., Gažo, J. und Sirota, A., Proceedings of the III. Conference on Coordination Chemistry, S Smolenice Bratislava Kohout, J., Kohútová, M. und Jóna, E., Z. Naturforsch. 25, 1054 (1970). 5. Jóna, E., Šramko, Т., Kohout, J., Sirota, A. und Gažo, J., Chem. Zvesti 25, 241 (1971). 6. Jóna, E., Jamnický, M., Šramko, T. und Gažo, J., Collect. Czech. Chem. Commun. 37, 3679 (1972). 150
7 ISOMERIE VON NICKELUD-KOMPLEXEN. VI Šramko, Т., Jona, E. und Sirota, A., Proceedings of the II. Conference on Coordination Chemistry, S Smolenice Bratislava Šramko, Т. und Jóna, E., Collect. Czech. Chem. Commun. 37, 1645 (1972). 9. Sirota, A., Jóna, E. und Šramko, Т., Proceedings of the XIII. International Conference on Coordination Chemistry, S Cracow Zakopane Sirota, A., Dissertation, S. 11. Slowakische Technische Hochschule, Bratislava Nelson, S. M. und Shepherd, T. M., Inorg. Chem. 4, 813 (1965). 12. Di Sipio, L., Oleari, L. und De Michelis, G., Coord. Chem. Rev. 1, 7 (1966). 13. Maki, G., J. Chem. Phys. 29, 162 (1958). 14. Lever, A. B. P., Coord. Chem. Rev. 3, 119 (1968). 15. Sirota, A., Šramko, T. und Kohout, J., Chem. Zvesti 20, 752 (1966). 16. Garaj, J. und Dunaj-Jurčo, M., Chem. Commun. 1968, King, H. C. A., Koros, E. und Nelson, S. M., J. Chem. Soc. (A) 1964, Goodgame, D. M. L. und Goodgame, M., J. Chem. Soc. 1963, Poraj-Košic, M. A., Kristallochimija 1965, S Itogi nauki, Ser. Chim., VINITI, Moskau Nelson, S. M. und Shepherd, T. M., J. Inorg. Nucl. Chem. 27, 2123 (1965). 21. Burmeister, J. L. und Basolo, F., Inorg. Chem. 3, 1587 (1964). 22. Fujita, J., Nakamoto, K. und Kobayashi, M., J. Amer. Chem. Soc (1956). 23. Clark, R. J. H. und Williams, C. S., Spectrochim. Acta 22, 1081 (1966). 24. Flint, C. D. und Goodgame, M., J. Chem. Soc. (A) 1970, Jóna, E., Šramko, T. und Gažo, J., Chem. Zvesti, im Druck. 26. Garner, W. E., Chemistry of the Solid State. Russische Übersetzung: Chimija tverdogo sostojanija, S Izdateľstvo inostrannoj literatury, Moskau Übersetzt von К. Ullrich 151
LMPG 2, ÜB21, Molekülbau & UV/VIS-Absorption LÖSUNG 1 von 11
 LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
Diskussion der Ergebnisse
 5 Diskussion der Ergebnisse Die Auswertung der Basiseigenschaften der Gläser beider Versuchsreihen lieferte folgende Ergebnisse: Die optische Einteilung der hergestellten Gläser konnte in zwei Gruppen
5 Diskussion der Ergebnisse Die Auswertung der Basiseigenschaften der Gläser beider Versuchsreihen lieferte folgende Ergebnisse: Die optische Einteilung der hergestellten Gläser konnte in zwei Gruppen
Protokoll. Kombinierte Anwendung verschiedener Spektroskopischer Methoden
 Protokoll Kombinierte Anwendung verschiedener Spektroskopischer Methoden Zielstellung: Durch die Auswertung von IR-, Raman-, MR-, UV-VIS- und Massenspektren soll die Struktur einer unbekannten Substanz
Protokoll Kombinierte Anwendung verschiedener Spektroskopischer Methoden Zielstellung: Durch die Auswertung von IR-, Raman-, MR-, UV-VIS- und Massenspektren soll die Struktur einer unbekannten Substanz
Kombinierte Übungen zur Spektroskopie Beispiele für die Bearbeitung
 Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Spektroskopie in der Organischen Chemie. Massenspektren
 Massenspektren In der Frühzeit der MS wurden Spektren auf Fotopapier registriert, wobei das Spektrum mehrfach mit unterschiedlicher Ordinatenauslenkung ausgeschrieben wurde, um sehr schwache neben sehr
Massenspektren In der Frühzeit der MS wurden Spektren auf Fotopapier registriert, wobei das Spektrum mehrfach mit unterschiedlicher Ordinatenauslenkung ausgeschrieben wurde, um sehr schwache neben sehr
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013
 Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Grundlagen der Elektrotechnik: Wechselstromwiderstand Xc Seite 1 R =
 Grundlagen der Elektrotechnik: Wechselstromwiderstand Xc Seite 1 Versuch zur Ermittlung der Formel für X C In der Erklärung des Ohmschen Gesetzes ergab sich die Formel: R = Durch die Versuche mit einem
Grundlagen der Elektrotechnik: Wechselstromwiderstand Xc Seite 1 Versuch zur Ermittlung der Formel für X C In der Erklärung des Ohmschen Gesetzes ergab sich die Formel: R = Durch die Versuche mit einem
3.Präparat / Versuch 8.3
 .Präparat ersuch 8. Herstellung von Nitropentainkobalt(III)-chlorid ([NH ) 5 NO ]Cl ) 1. Herstellungsvorschrift: (Quelle 1, ) Es sollen g Nitropentainkobalt(III)-chlorid hergestellt werden. a) Herstellung
.Präparat ersuch 8. Herstellung von Nitropentainkobalt(III)-chlorid ([NH ) 5 NO ]Cl ) 1. Herstellungsvorschrift: (Quelle 1, ) Es sollen g Nitropentainkobalt(III)-chlorid hergestellt werden. a) Herstellung
Anorganische Chemie I/II
 Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 11. Februar 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 11. Februar 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
IR-Spektroskopie. Fachhochschule Bonn-Rhein-Sieg. Fachbereich Angewandte Naturwissenschaften
 Fachhochschule Bonn-Rhein-Sieg Fachbereich Angewandte Naturwissenschaften Einführung Elektromagnetische Strahlung kann mit Materie in Wechselwirkung treten. Moleküle können die Energie von elektromagnetischer
Fachhochschule Bonn-Rhein-Sieg Fachbereich Angewandte Naturwissenschaften Einführung Elektromagnetische Strahlung kann mit Materie in Wechselwirkung treten. Moleküle können die Energie von elektromagnetischer
Synthese von Essigsäureisopropylester (1) Präparat 1
 Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
8. Mehrkomponentensysteme. 8.1 Partielle molare Größen. Experiment 1 unter Umgebungsdruck p:
 8. Mehrkomponentensysteme 8.1 Partielle molare Größen Experiment 1 unter Umgebungsdruck p: Fügen wir einer Menge Wasser n mit Volumen V (molares Volumen v m =V/n) bei einer bestimmten Temperatur T eine
8. Mehrkomponentensysteme 8.1 Partielle molare Größen Experiment 1 unter Umgebungsdruck p: Fügen wir einer Menge Wasser n mit Volumen V (molares Volumen v m =V/n) bei einer bestimmten Temperatur T eine
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid
 Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Darstellung von Kaliumtetrachloroiodat(III) K[ICl 4 ]
![Darstellung von Kaliumtetrachloroiodat(III) K[ICl 4 ] Darstellung von Kaliumtetrachloroiodat(III) K[ICl 4 ]](/thumbs/25/6722537.jpg) Darstellung von Kaliumtetrachloroiodat(III) K[ICl 4 ] Andreas J. Wagner 29. Juli 2004 1 Theorie Die Elemente der 17.Gruppe, die Halogene, treten in organischen und vielen anorganischen Verbindungen fast
Darstellung von Kaliumtetrachloroiodat(III) K[ICl 4 ] Andreas J. Wagner 29. Juli 2004 1 Theorie Die Elemente der 17.Gruppe, die Halogene, treten in organischen und vielen anorganischen Verbindungen fast
Thema heute: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Katalyse. Martin Babilon 14/07/2011. Katalyse. Martin Babilon Universität Paderborn. 14 Juli Montag, 18. Juli 2011
 Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Universität der Pharmazie
 Universität der Pharmazie Institut für Pharmazie Pharmazie-Straße 1 12345 Pharmastadt Identitäts-, Gehalts- und Reinheitsbestimmung von Substanzen in Anlehnung an Methoden des Europäischen Arzneibuchs
Universität der Pharmazie Institut für Pharmazie Pharmazie-Straße 1 12345 Pharmastadt Identitäts-, Gehalts- und Reinheitsbestimmung von Substanzen in Anlehnung an Methoden des Europäischen Arzneibuchs
Dieter Suter Physik B3
 Dieter Suter - 421 - Physik B3 9.2 Radioaktivität 9.2.1 Historisches, Grundlagen Die Radioaktivität wurde im Jahre 1896 entdeckt, als Becquerel feststellte, dass Uransalze Strahlen aussenden, welche den
Dieter Suter - 421 - Physik B3 9.2 Radioaktivität 9.2.1 Historisches, Grundlagen Die Radioaktivität wurde im Jahre 1896 entdeckt, als Becquerel feststellte, dass Uransalze Strahlen aussenden, welche den
B Chemisch Wissenwertes. Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden.
 -I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
-I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
Thermodynamik & Kinetik
 Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Grundlagen der Chemie Verschieben von Gleichgewichten
 Verschieben von Gleichgewichten Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Prinzip des kleinsten Zwangs Das
Verschieben von Gleichgewichten Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Prinzip des kleinsten Zwangs Das
Demonstrationsversuche zur Lehrveranstaltung. Strukturaufklärung mit optischen Streuverfahren
 Demonstrationsversuche zur Lehrveranstaltung 19.06.08 Schwerpunkte: (a) Vergleich der Schwingungsbanden des Sulfations (SO 2 4 ) - in kristallinem CaSO 4 2 H 2 O - in kristallinem CaSO 4 - in wäßriger
Demonstrationsversuche zur Lehrveranstaltung 19.06.08 Schwerpunkte: (a) Vergleich der Schwingungsbanden des Sulfations (SO 2 4 ) - in kristallinem CaSO 4 2 H 2 O - in kristallinem CaSO 4 - in wäßriger
Zentralabitur 2011 Physik Schülermaterial Aufgabe I ga Bearbeitungszeit: 220 min
 Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Wie wirkt sich die Zugabe von Salz auf den Schmelz- und Siedepunkt von Wasser aus?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Versuchsprotokoll Kapitel 6
 Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
6. Welche der folgenden Anordnungen von vier gleich großen ohmschen Widerständen besitzt den kleinsten Gesamtwiderstand?
 1 1. Welche der folgenden Formulierungen entspricht dem ersten Newton schen Axiom (Trägheitsprinzip)? Ein Körper verharrt in Ruhe oder bewegt sich mit konstanter gleichförmiger Geschwindigkeit, wenn die
1 1. Welche der folgenden Formulierungen entspricht dem ersten Newton schen Axiom (Trägheitsprinzip)? Ein Körper verharrt in Ruhe oder bewegt sich mit konstanter gleichförmiger Geschwindigkeit, wenn die
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Grundwissen Chemie 9. Klasse SG
 Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Grundwissen 8.Klasse 1 Grundwissen 8.Klasse 1. Grundwissen 8.Klasse 2 Grundwissen 8.Klasse 2. Stoffebene. Teilchen -ebene
 Grundwissen 8.Klasse 1 Grundwissen 8.Klasse 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp., Löslichkeit,
Grundwissen 8.Klasse 1 Grundwissen 8.Klasse 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp., Löslichkeit,
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen
 Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol
![Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol](/thumbs/50/26795947.jpg) 2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
4 an Beispielen Energiefluss und Energieentwertung quantitativ darstellen.
 3.3 Konzeptbezogene Kompetenzen im Fach Kompetenzen zum Basiskonzept Energie" Jahrgang 9 Energiekonzept auf der Grundlage einfacher Beispiele so weit entwickelt, dass sie... 1 an Vorgängen aus ihrem Erfahrungsbereich
3.3 Konzeptbezogene Kompetenzen im Fach Kompetenzen zum Basiskonzept Energie" Jahrgang 9 Energiekonzept auf der Grundlage einfacher Beispiele so weit entwickelt, dass sie... 1 an Vorgängen aus ihrem Erfahrungsbereich
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Spektroskopische und theoretische Untersuchungen von Übergangsmetallkomplexen mit non-innocent Liganden
 Spektroskopische und theoretische Untersuchungen von Übergangsmetallkomplexen mit non-innocent Liganden Jurema Schmidt Vortrag im Seminar Moderne Anwendungen der magnetischen Resonanz 17.10.2013 Inhalt
Spektroskopische und theoretische Untersuchungen von Übergangsmetallkomplexen mit non-innocent Liganden Jurema Schmidt Vortrag im Seminar Moderne Anwendungen der magnetischen Resonanz 17.10.2013 Inhalt
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Universität Regensburg
 Universität Regensburg Fakultät für Chemie und Pharmazie 93040 Regensburg 14. März 2006 Institut für Anorganische Chemie Prof. Dr. R. Winter 1. Was besagt das Moseleysche Gesetz? Welche Größe kann man
Universität Regensburg Fakultät für Chemie und Pharmazie 93040 Regensburg 14. März 2006 Institut für Anorganische Chemie Prof. Dr. R. Winter 1. Was besagt das Moseleysche Gesetz? Welche Größe kann man
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
ALLGEMEINE CHEMIE - GRUNDLAGEN
 ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
Der lichtelektrische Effekt (Photoeffekt)
 Der lichtelektrische Effekt (Photoeffekt) Versuchsanordnung Zn-Platte, amalgamiert Wulfsches Elektrometer Spannung, ca. 800 V Knappe Erklärung des Versuches Licht löst aus der Zn-Platte Elektronen aus
Der lichtelektrische Effekt (Photoeffekt) Versuchsanordnung Zn-Platte, amalgamiert Wulfsches Elektrometer Spannung, ca. 800 V Knappe Erklärung des Versuches Licht löst aus der Zn-Platte Elektronen aus
Anorganische Chemie I
 Anorganische Chemie I PRÜFUNG B. Sc. Chemieingenieurwesen 14. Juli 2014 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie I PRÜFUNG B. Sc. Chemieingenieurwesen 14. Juli 2014 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Moderne Methoden der Chemie - die Differenz-Thermo- Analyse (DTA)
 Moderne Methoden der Chemie - die Differenz-Thermo- Analyse (DTA) Einleitung Moderne Anaylsemethoden haben die Chemie - insbesondere in den letzten 50 Jahren - stark verändert. Sie ermöglichen völlig neue
Moderne Methoden der Chemie - die Differenz-Thermo- Analyse (DTA) Einleitung Moderne Anaylsemethoden haben die Chemie - insbesondere in den letzten 50 Jahren - stark verändert. Sie ermöglichen völlig neue
Einführung in die Photochemie
 Einführung in die Photochemie Praktikum und Lernaufgaben von Roger Deuber Inhalt: Die Schüler/innen führen im Praktikum die thermische und photochemische Umlagerung von Azobenzen durch und erfahren dabei,
Einführung in die Photochemie Praktikum und Lernaufgaben von Roger Deuber Inhalt: Die Schüler/innen führen im Praktikum die thermische und photochemische Umlagerung von Azobenzen durch und erfahren dabei,
 www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
Physikalische Analytik
 Labor im Lehrfach Physikalische Analytik Studiengang Applied Life Sciences Versuch IR-Spektroskopie Standort Zweibrücken Gruppe: Teilnehmer: Verfasser: Semester: Versuchsdatum: Bemerkungen: Inhalt 1. Einführung
Labor im Lehrfach Physikalische Analytik Studiengang Applied Life Sciences Versuch IR-Spektroskopie Standort Zweibrücken Gruppe: Teilnehmer: Verfasser: Semester: Versuchsdatum: Bemerkungen: Inhalt 1. Einführung
3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) 93
 3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) 93 Abbildung 3.29 Ti 5 O 4 (PO 4 ). ORTEP-Darstellung eines Ausschnitts der "Ketten" aus flächenverknüpften [TiO 6 ]-Oktaedern einschließlich der in der Idealstruktur
3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) 93 Abbildung 3.29 Ti 5 O 4 (PO 4 ). ORTEP-Darstellung eines Ausschnitts der "Ketten" aus flächenverknüpften [TiO 6 ]-Oktaedern einschließlich der in der Idealstruktur
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 6 Kalorimetrie Aufgabe: Mittels eines Flüssigkeitskalorimeters ist a) die Neutralisationsenthalpie von säure b) die ösungsenthalpie
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 6 Kalorimetrie Aufgabe: Mittels eines Flüssigkeitskalorimeters ist a) die Neutralisationsenthalpie von säure b) die ösungsenthalpie
Chelatisierende Koordination von Glucopyranose an ein Metallzentrum.
 Lars Jessen Dissertation 3 Zusammenfassung Ziel der vorliegenden Arbeit war, die Möglichkeit der Koordination von Kohlenhydratbausteinen, insbesondere von Glucopyranosen, als Diolatoliganden an (IV)- und
Lars Jessen Dissertation 3 Zusammenfassung Ziel der vorliegenden Arbeit war, die Möglichkeit der Koordination von Kohlenhydratbausteinen, insbesondere von Glucopyranosen, als Diolatoliganden an (IV)- und
Verrechnungspunkte: Gesamtpunkte: Note:
 Säure-Base-Reaktionen: E. 5. 2 Die Base Ammoniak Bearbeitungszeit: zweimal 45 Minuten Hilfsmittel: Taschenrechner Verrechnungspunkte: Gesamtpunkte: Note: Aufgaben 1 Ammoniak wird heute großtechnisch nach
Säure-Base-Reaktionen: E. 5. 2 Die Base Ammoniak Bearbeitungszeit: zweimal 45 Minuten Hilfsmittel: Taschenrechner Verrechnungspunkte: Gesamtpunkte: Note: Aufgaben 1 Ammoniak wird heute großtechnisch nach
Übung 9. Allgemeine Chemie I Herbstsemester Vergleichen Sie die Abbildung 30.1 (MM., p. 515).
 Übung 9 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Vergleichen Sie die Abbildung 30.1 (MM., p. 515). 2. Aufgabe Der Chelateffekt beruht darauf, dass ein mehrzähniger Ligand (einer, der simultan
Übung 9 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Vergleichen Sie die Abbildung 30.1 (MM., p. 515). 2. Aufgabe Der Chelateffekt beruht darauf, dass ein mehrzähniger Ligand (einer, der simultan
NMR-spektroskopische Untersuchung der Lithiumaggregate von organischen Verbindungen und von Cyclosporin A
 Zusammenfassung der wissenschaftlichen Ergebnisse zur Dissertation NMR-spektroskopische Untersuchung der thiumaggregate von organischen Verbindungen und von Cyclosporin A Der Fakultät für Chemie und Mineralogie
Zusammenfassung der wissenschaftlichen Ergebnisse zur Dissertation NMR-spektroskopische Untersuchung der thiumaggregate von organischen Verbindungen und von Cyclosporin A Der Fakultät für Chemie und Mineralogie
Die chemische Natur der Pigmente aus photosynthetischen Reaktionszentren von Rhodospirillum ruhrum G-9+
 Diss. ETHNr.6106 Die chemische Natur der Pigmente aus hotosynthetischen Reaktionszentren von Rhodosirillum ruhrum G-9+ ABHANDLUNG zur Erlangung destitelseinesdoktorsder Naturwissenschaften der Eidgenössischen
Diss. ETHNr.6106 Die chemische Natur der Pigmente aus hotosynthetischen Reaktionszentren von Rhodosirillum ruhrum G-9+ ABHANDLUNG zur Erlangung destitelseinesdoktorsder Naturwissenschaften der Eidgenössischen
Karin Gehrich (Autor) Phasenverhalten einiger Zucker und Zuckeraustauschstoffe
 Karin Gehrich (Autor) Phasenverhalten einiger Zucker und Zuckeraustauschstoffe https://cuvillier.de/de/shop/publications/3633 Copyright: Cuvillier Verlag, Inhaberin Annette Jentzsch-Cuvillier, Nonnenstieg
Karin Gehrich (Autor) Phasenverhalten einiger Zucker und Zuckeraustauschstoffe https://cuvillier.de/de/shop/publications/3633 Copyright: Cuvillier Verlag, Inhaberin Annette Jentzsch-Cuvillier, Nonnenstieg
Kettenreaktionen. Kapitel 2. In diesem Kapitel sollen die folgenden Fragen beantwortet werden:
 Kapitel 2 Kettenreaktionen In diesem Kapitel sollen die folgenden Fragen beantwortet werden: Was versteht man unter einer Kettenreaktion? Welches sind die verschiedenen Typen von Reaktionsschritten, die
Kapitel 2 Kettenreaktionen In diesem Kapitel sollen die folgenden Fragen beantwortet werden: Was versteht man unter einer Kettenreaktion? Welches sind die verschiedenen Typen von Reaktionsschritten, die
= 6,63 10 J s 8. (die Plancksche Konstante):
 35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
Von Nadine Ufermann und Marcus Oldekamp
 Von Nadine Ufermann und Marcus Oldekamp Photosynthese: Allgemein und Lichtreaktion Photosysteme: PSI und PSII, Entdeckung und Funktion Mangan und Manganenzyme: Speziell sauerstoffentwickelnder Mn Cluster
Von Nadine Ufermann und Marcus Oldekamp Photosynthese: Allgemein und Lichtreaktion Photosysteme: PSI und PSII, Entdeckung und Funktion Mangan und Manganenzyme: Speziell sauerstoffentwickelnder Mn Cluster
Extraktion/Komplexbildung
 Extraktion/Komplexbildung Inhalte dieser Lerneinheit: Quantitativer Nachweis von Eisen mit o-phenanthrolin Quantitativer Nachweis von Kupfer mit Bichinolin Dabei werden Grundlagen der: Komplexbildung und
Extraktion/Komplexbildung Inhalte dieser Lerneinheit: Quantitativer Nachweis von Eisen mit o-phenanthrolin Quantitativer Nachweis von Kupfer mit Bichinolin Dabei werden Grundlagen der: Komplexbildung und
Verbrennungstechnik. 1. Brennstoffe. 1.Brennstoffe. 2.Heizwert. 2.1 Oberer Heizwert 2.2 Unterer Heizwert. 3.Verbrennungsvorgang
 Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
IR-Spektroskopie organischer Moleküle
 Die Infrarot-Spektroskopie dient in der Organischen Chemie der Ermittlung von Strukturelementen, funktionellen Gruppen und ggf. von Isomeren und Konformeren. Ein Schwingungsspektrum eines organischen Moleküls
Die Infrarot-Spektroskopie dient in der Organischen Chemie der Ermittlung von Strukturelementen, funktionellen Gruppen und ggf. von Isomeren und Konformeren. Ein Schwingungsspektrum eines organischen Moleküls
ZHW / CB / AnP SS 03. Quantitative Bestimmung von Co- und Ni-Ionen im Gemisch Kinetische Untersuchungen an Farbstoffen
 UV/VIS Methode: UV/VIS - Spektrometrie Themen: Analyte: Matrix: Quantitative Bestimmung von Co- und Ni-Ionen im Gemisch Kinetische Untersuchungen an Farbstoffen Ni 2+, 2+, Murexid Rostfreier Stahl, Wasser
UV/VIS Methode: UV/VIS - Spektrometrie Themen: Analyte: Matrix: Quantitative Bestimmung von Co- und Ni-Ionen im Gemisch Kinetische Untersuchungen an Farbstoffen Ni 2+, 2+, Murexid Rostfreier Stahl, Wasser
Gleichstromkreis. 2.2 Messgeräte für Spannung, Stromstärke und Widerstand. Siehe Abschnitt 2.4 beim Versuch E 1 Kennlinien elektronischer Bauelemente
 E 5 1. Aufgaben 1. Die Spannungs-Strom-Kennlinie UKl = f( I) einer Spannungsquelle ist zu ermitteln. Aus der grafischen Darstellung dieser Kennlinie sind Innenwiderstand i, Urspannung U o und Kurzschlussstrom
E 5 1. Aufgaben 1. Die Spannungs-Strom-Kennlinie UKl = f( I) einer Spannungsquelle ist zu ermitteln. Aus der grafischen Darstellung dieser Kennlinie sind Innenwiderstand i, Urspannung U o und Kurzschlussstrom
Darstellung des Messings Cu 2 Zn
 Darstellung des Messings Cu 2 Zn Andreas J. Wagner 7. Juli 2004 1 Theorie Legierungen sind intermetallische Verbindungen. Im beschriebenen Versuch war es das Ziel, ein Messing 1 der Zusammensetzung Cu
Darstellung des Messings Cu 2 Zn Andreas J. Wagner 7. Juli 2004 1 Theorie Legierungen sind intermetallische Verbindungen. Im beschriebenen Versuch war es das Ziel, ein Messing 1 der Zusammensetzung Cu
Studienverlaufsplan. des Bachelor-Studiengangs Chemie. der RWTH Aachen. Stand
 Studienverlaufsplan des Bachelor-Studiengangs Chemie der RWTH Aachen Stand 18.12.2014 INHALTSÜBERSICHT Schematische Darstellung des Bachelor-Studiengangs Chemie... 2 Übersichtstabellen des Bachelor-Studiengangs
Studienverlaufsplan des Bachelor-Studiengangs Chemie der RWTH Aachen Stand 18.12.2014 INHALTSÜBERSICHT Schematische Darstellung des Bachelor-Studiengangs Chemie... 2 Übersichtstabellen des Bachelor-Studiengangs
Nickelocen. Bis(cyclopentadienyl)-nickel
 Nickelocen Bis(cyclopentadienyl)-nickel Ni Zürich, 11.1.5 Anna Evans, 1 SYNTHESE 1.1 Methode [1], [] Die Synthese von Nickelocen verläuft über das Cracken von Dicyclopentadien und die Herstellung von Natriumcyclopentadien.
Nickelocen Bis(cyclopentadienyl)-nickel Ni Zürich, 11.1.5 Anna Evans, 1 SYNTHESE 1.1 Methode [1], [] Die Synthese von Nickelocen verläuft über das Cracken von Dicyclopentadien und die Herstellung von Natriumcyclopentadien.
3. Kapitel Der Compton Effekt
 3. Kapitel Der Compton Effekt 3.1 Lernziele Sie können erklären, wie die Streuung von Röntgenstrahlen an Graphit funktioniert. Sie kennen die physikalisch theoretischen Voraussetzungen, die es zum Verstehen
3. Kapitel Der Compton Effekt 3.1 Lernziele Sie können erklären, wie die Streuung von Röntgenstrahlen an Graphit funktioniert. Sie kennen die physikalisch theoretischen Voraussetzungen, die es zum Verstehen
Spektroskopie. im IR- und UV/VIS-Bereich. Raman-Spektroskopie. http://www.analytik.ethz.ch
 Spektroskopie im IR- und UV/VIS-Bereich Raman-Spektroskopie Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Raman-Spektroskopie Chandrasekhara Venkata Raman Entdeckung des
Spektroskopie im IR- und UV/VIS-Bereich Raman-Spektroskopie Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Raman-Spektroskopie Chandrasekhara Venkata Raman Entdeckung des
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
Applikationsfeld / Industriezweig:
 Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Lösungen zu den Übungen zur Einführung in die Spektroskopie für Studenten der Biologie (SS 2011)
 Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
O 3a O 3 (98.1) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.3 [4+2]-Cycloaddition von Cyclopentadien mit Maleinsäureanhydrid zum endobzw. exo-bicyclo[2.2.1]hept-5-en-2,3-dicarbonsäureanhydrid (3, Umwandlung in das exo-addukt 3b C 5 6 (66.1) + C 4 2 3 (98.1)
3.4.3 [4+2]-Cycloaddition von Cyclopentadien mit Maleinsäureanhydrid zum endobzw. exo-bicyclo[2.2.1]hept-5-en-2,3-dicarbonsäureanhydrid (3, Umwandlung in das exo-addukt 3b C 5 6 (66.1) + C 4 2 3 (98.1)
Praktikum Chemie für Biologen SS Kurse SS
 1 Praktikum Chemie für Biologen SS 2001 - Kurse SS Klausur in Organischer Chemie (KlOC) Sa 28.07.2001 Name:... Vorname:... Wenn Nachschreiber aus einem der Vorkurse, bitte eintragen: Matrikel-Nr. Semester
1 Praktikum Chemie für Biologen SS 2001 - Kurse SS Klausur in Organischer Chemie (KlOC) Sa 28.07.2001 Name:... Vorname:... Wenn Nachschreiber aus einem der Vorkurse, bitte eintragen: Matrikel-Nr. Semester
Homogenes Gleichgewicht
 Knoch, Anastasiya Datum der Durchführung: Petri, Guido 08.12.2015 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Homogenes Gleichgewicht 1. Aufgabenstellung
Knoch, Anastasiya Datum der Durchführung: Petri, Guido 08.12.2015 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Homogenes Gleichgewicht 1. Aufgabenstellung
3 Wahr oder Falsch? = 6.67 % Werkstoffe und Fertigung I, HS 2016 Prof. Dr. K. Wegener. Seminarübung 6 Musterlösung Diffusion, Erstarrung
 3 Wahr oder Falsch? a) Diamant, Graphit und Fullerene sind allotrope Modifikationen des Kohlenstoffatoms. Sie unterscheiden jedoch nur in ihrem strukturellem Aufbau. Falsch: Sie unterschieden sich auch
3 Wahr oder Falsch? a) Diamant, Graphit und Fullerene sind allotrope Modifikationen des Kohlenstoffatoms. Sie unterscheiden jedoch nur in ihrem strukturellem Aufbau. Falsch: Sie unterschieden sich auch
Schulcurriculum des Evangelischen Gymnasiums Siegen-Weidenau im Fache Chemie, Einführungsphase:
 Schulcurriculum des Evangelischen Gymnasiums Siegen-Weidenau im Fache Chemie, Einführungsphase: Inhaltsfeld_1 (Kohlenstoffverbindungen und Gleichgewichtsreaktionen) 1) Organische Kohlenstoffverbindungen
Schulcurriculum des Evangelischen Gymnasiums Siegen-Weidenau im Fache Chemie, Einführungsphase: Inhaltsfeld_1 (Kohlenstoffverbindungen und Gleichgewichtsreaktionen) 1) Organische Kohlenstoffverbindungen
D-(+)-Biotin (Vitamin H)
 D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
Standortbestimmung / Äquivalenzprüfung. Chemie. Mittwoch, 13. April 2016, Uhr
 Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Titration von Metallorganylen und Darstellung der dazu benötigten
 Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
FTIR-Absorptionsspektroskopie
 Institut für Physik Physikalisches Praktikum für Fortgeschrittene 2000 M 1 FTIR-Absorptionsspektroskopie 1. Versuchsziel Aus den Infrarotspektren erhält man Informationen über das Rotationsund Schwingungsverhalten
Institut für Physik Physikalisches Praktikum für Fortgeschrittene 2000 M 1 FTIR-Absorptionsspektroskopie 1. Versuchsziel Aus den Infrarotspektren erhält man Informationen über das Rotationsund Schwingungsverhalten
(Communlcated at the meeting of December ).
 Physics. - Die Anregungsfunktionen des atomaren Wasserstoffs. (VorIäufige Mitteilung.) Van L. S. ORNSTEIN und H. LINDEMAN. (Communlcated at the meeting of December 25. 1930). 1. Die Anregungsfunktionen
Physics. - Die Anregungsfunktionen des atomaren Wasserstoffs. (VorIäufige Mitteilung.) Van L. S. ORNSTEIN und H. LINDEMAN. (Communlcated at the meeting of December 25. 1930). 1. Die Anregungsfunktionen
Text Anlage. Heparin-Calcium
 Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Synthese von 1-(p-Tolyl)butan-1,4-diol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
Übungsaufgaben Chemie Nr. 3
 Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
0.1.1 Exzerpt von B. S. 414: Unendlich hoher Potenzialtopf
 1 15.11.006 0.1 119. Hausaufgabe 0.1.1 Exzerpt von B. S. 414: Unendlich hoher Potenzialtopf (Siehe 118. Hausaufgabe.) 0.1. Exzerpt von B. S. 414: Wellenlängen der Wellenfunktion im Fall stehender Wellen
1 15.11.006 0.1 119. Hausaufgabe 0.1.1 Exzerpt von B. S. 414: Unendlich hoher Potenzialtopf (Siehe 118. Hausaufgabe.) 0.1. Exzerpt von B. S. 414: Wellenlängen der Wellenfunktion im Fall stehender Wellen
LK Lorentzkraft. Inhaltsverzeichnis. Moritz Stoll, Marcel Schmittfull (Gruppe 2) 25. April Einführung 2
 LK Lorentzkraft Blockpraktikum Frühjahr 2007 (Gruppe 2) 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Magnetfeld dünner Leiter und Spulen......... 2 2.2 Lorentzkraft........................
LK Lorentzkraft Blockpraktikum Frühjahr 2007 (Gruppe 2) 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Magnetfeld dünner Leiter und Spulen......... 2 2.2 Lorentzkraft........................
Kleines Wasserlexikon
 Kleines Wasserlexikon Lösung von Kohlenstoffdioxid. Kohlenstoffdioxid CO 2 ist leicht wasserlöslich und geht mit manchen Inhaltsstoffen des Wassers auch chemische Reaktionen ein. In einem ersten Schritt
Kleines Wasserlexikon Lösung von Kohlenstoffdioxid. Kohlenstoffdioxid CO 2 ist leicht wasserlöslich und geht mit manchen Inhaltsstoffen des Wassers auch chemische Reaktionen ein. In einem ersten Schritt
3. Mikrostruktur und Phasenübergänge
 3. Mikrostruktur und Phasenübergänge Definition von Mikrostruktur und Gefüge Gefüge bezeichnet die Beschaffenheit der Gesamtheit jener Teilvolumina eines Werkstoffs, von denen jedes hinsichtlich seiner
3. Mikrostruktur und Phasenübergänge Definition von Mikrostruktur und Gefüge Gefüge bezeichnet die Beschaffenheit der Gesamtheit jener Teilvolumina eines Werkstoffs, von denen jedes hinsichtlich seiner
AnC I Protokoll: 6.1 Extraktionsphotometrische Bestimmung von Cobalt mit HDEHP! SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Extraktion. Arbeitstechnik der Extraktion
 1 Extraktion Die heute vielfach angewandte Trennung durch Extraktion basiert auf der unterschiedlichen Löslichkeit bestimmter Verbindungen in zwei nicht (od. begrenzt) mischbaren Lösungsmittel. (Das Lösungsmittesystem
1 Extraktion Die heute vielfach angewandte Trennung durch Extraktion basiert auf der unterschiedlichen Löslichkeit bestimmter Verbindungen in zwei nicht (od. begrenzt) mischbaren Lösungsmittel. (Das Lösungsmittesystem
Seminar zum Methodenkurs Christian Graßl
 Seminar zum Methodenkurs Christian Graßl Neue Typen von Wasserstoffbrückenbindungen in der Organometallchemie (Coord. Chem. Rev. 231 (2002) 165) http://upload.wikimedia.org/wikipedia/commons/d/dd/wasserstoffbr%c3%bcckenbindungen_des_wasser.png
Seminar zum Methodenkurs Christian Graßl Neue Typen von Wasserstoffbrückenbindungen in der Organometallchemie (Coord. Chem. Rev. 231 (2002) 165) http://upload.wikimedia.org/wikipedia/commons/d/dd/wasserstoffbr%c3%bcckenbindungen_des_wasser.png
Klausur 12/1 Physik LK Elsenbruch Di (4h) Thema: elektrische und magnetische Felder Hilfsmittel: Taschenrechner, Formelsammlung
 Klausur 12/1 Physik LK Elsenbruch Di 18.01.05 (4h) Thema: elektrische und magnetische Felder Hilfsmittel: Taschenrechner, Formelsammlung 1) Ein Kondensator besteht aus zwei horizontal angeordneten, quadratischen
Klausur 12/1 Physik LK Elsenbruch Di 18.01.05 (4h) Thema: elektrische und magnetische Felder Hilfsmittel: Taschenrechner, Formelsammlung 1) Ein Kondensator besteht aus zwei horizontal angeordneten, quadratischen
KZU Bio. KZU Bio. KZU Bio. KZU Bio
 Was wollte van Helmont mit "Weidenzweig-Versuch" herausfinden? Weshalb nahm van Helmont Regenwasser und nicht Leitungswasser? Was war das Resultat des Experimentes von van Helmont? Was konnte er aus seinem
Was wollte van Helmont mit "Weidenzweig-Versuch" herausfinden? Weshalb nahm van Helmont Regenwasser und nicht Leitungswasser? Was war das Resultat des Experimentes von van Helmont? Was konnte er aus seinem
