Schwierige endosonografische Differenzialdiagnosen am Pankreas zystische Läsionen
|
|
|
- Friedrich Dittmar
- vor 6 Jahren
- Abrufe
Transkript
1 Übersicht 253 Schwierige endosonografische Differenzialdiagnosen am Pankreas zystische Läsionen Difficult Pancreatic Diagnoses in Endosonography Cystic Lesions Autoren C. Jenssen 1, K. Möller 2 Institute Schlüsselwörter l" Endosonografie l" abdominelle Sonografie l" kontrastverstärkte Sonografie l" EUS l" EUS-FNA l" zystische Pankreasläsion l" seröse zystische l" Zystadenom l" muzinöse zystische l" intraduktale papillärmuzinöse Key words l" endoscopic ultrasound l" transabdominal ultrasound l" contrast-enhanced ultrasound l" EUS l" EUS-FNA l" cystic pancreatic lesion l" serous cystic neoplasm l" mucinous cystic neoplasm l" intraductal papillary mucinous neoplasm Bibliografie DOI /s Endo heute 2010; 23: Georg Thieme Verlag KG Stuttgart New York ISSN X Korrespondenzadresse Dr. med. Christian Jenssen Klinik für Innere Medizin Krankenhaus Märkisch Oderland Prötzeler Chaussee Strausberg Tel.: +49 /33 41 / Fax: +49 / / c.jenssen@khmol.de 1 Krankenhaus Märkisch Oderland GmbH, Klinik für Innere Medizin 2 Sana Klinikum Berlin-Lichtenberg, Klinik für Innere Medizin /Gastroenterologie Zusammenfassung! Zystische Läsionen des Pankreas sind häufig und werden zunehmend als Zufallsbefunde bildgebender Diagnostik entdeckt. Im Gegensatz zu anderen parenchymatösen Organen sind dysontogenetische Pankreaszysten sehr selten. Unter den Zufallsbefunden dominieren zystische n unterschiedlichen Malignitätsrisikos, bei symptomatischen zystischen Pankreasläsionen handelt es sich dagegen überwiegend um akute oder chronische Pseudozysten. Die Endosonografie spielt neben anamnestisch-klinischen Kriterien in der differenzialdiagnostischen und prognostischen Charakterisierung eine herausragende Rolle. In einer Sitzung sind morphologische Beurteilung, Darstellung der Vaskularisation und Feinnadelaspiration von Zysteninhalt, Zystenwandung und soliden Anteilen möglich. Dennoch können Differenzialdiagnose und Entscheidungsfindung über das weitere Vorgehen im Einzelfall erhebliche Probleme aufwerfen, die in dieser Übersicht diskutiert werden. Es wird ein evidenzbasierter diagnostischer Algorithmus für zystische Pankreasläsionen vorgestellt. Abstract! Pancreatic cystic lesions are common. They are increasingly detected as a finding of radiological imaging. In contrast to other parenchymal organs in the pancreas dysontogenetic cysts are extremely rare. The majority of incidental cystic lesions are neoplasms which own different risks of malignancy. In symptomatic patients the most frequent cystic pancreatic lesions are acute and chronic pseudocysts. In addition to clinical criteria endoscopic ultrasound has an outstanding role in the differential diagnosis and prognostic characterization of pancreatic cystic lesions. In one examination it is possible to perform morphological description, perfusion imaging, and fine-needle aspiration of cyst content, cyst wall and solid components. Nevertheless, in several cases differential diagnosis and management decisions may prove difficult. This review will discuss problems in and approaches to endosonographic diagnosis of cystic pancreatic lesions. An evidence-based algorithm for diagnosis of pancreatic cystic lesions is introduced. Einleitung! Zystische Pankreasläsionen sind häufig. In einer Autopsiestudie fanden sich in 24,3% der Fälle Pankreaszysten [1]. Mit zunehmender Häufigkeit sind sie Zufallsbefunde bildgebender Diagnostik und zwingen zu einer diagnostischen und prognostischen Bewertung. In aktuellen Analysen wurde die Prävalenz magnetresonanztomografisch detektierter inzidenteller zystischer Pankreasläsionen mit 13,5 % [2] bzw. 44,7% [3] angegeben. Ihre Häufigkeit nimmt mit dem Alter zu [1 3]. Während bei symptomatischen Patienten Pseudozysten dominieren, handelt es sich bei den Zufallsbefunden überwiegend um kleine zystische n [4]. Die in Niere oder Leber häufigen dysontogenetischen Zysten stellen im Pankreas ebenso wie andere nicht neoplastische Entitäten eine Seltenheit dar. Die WHO-Klassifikation kennt inzwischen mehr als 25 verschiedene zystische Pankreasläsionen. Es kann zwischen primär zystischen n und Tumoren mit sekundärer zystischer Degeneration (zystische neuroendokrine Tumoren, zystische Adenokarzinome, solid-pseudopapilläre ) unterschieden werden. Glücklicherweise entfallen 60 90% aller zystischen n auf nur 5Entitäten: seröszystische n (SCN), muzinös-zystische n (MCN) und die intraduktalen papillär-muzinösen n vom Seitengangtyp (BD-IPMN) oder Hauptgangtyp (MD-IPMN) sowie die solid-pseudopapilläre (SPN) [5 7].
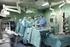
2 254 Übersicht Der Differenzierung dieser zystischen n untereinander und von non-neoplastischen Pankreaszysten kommt wegen der Unterschiede in Prognose und Therapie sehr große klinische Bedeutung zu. Während asymptomatische nicht neoplastische Pankreaszysten und SCN keiner Therapie bedürfen, besteht für MD- IPMN und MCN aufgrund des hohen Malignitätsrisikos unabhängig von einer Symptomatik prinzipiell die Indikation zum operativen Vorgehen. Bei BD-IPMN kann dagegen abhängig von patientenindividuellen und morphologischen Kriterien eine Verlaufsbeobachtung gerechtfertigt sein [8]. Von allen zur Verfügung stehenden diagnostischen Methoden hat der endoskopische Ultraschall (EUS) mit seiner hohen Ortsauflösung, der Möglichkeit von Perfusionsanalysen sowie der Option, in gleicher Sitzung eine Feinnadelaspiration (EUS-FNA) durchzuführen, prinzipiell das größte Potenzial. Sie wird daher im Regelfall ergänzend zur transkutanen Sonografie oder radiologischen Schnittbildgebung (Computertomografie, CT; Magnetresonanztomografie, MRT; Magnetresonanzcholangiopankreatografie, MRCP) eingesetzt, um zystische Pankreasraumforderungen zu charakterisieren und eine Entscheidung über das weitere Vorgehen herbeizuführen [9]. Endoskopische retrograde Pankreatografie (ERP) und Pankreatoskopie sind bei gangassoziierten Zysten eine komplementäre oder alternative Möglichkeit, eine zytologische oder histologische Diagnose zu erreichen. Trotz des breiten Spektrums diagnostischer Möglichkeiten sind jedoch selbst an Zentren mit hoher Fallzahl und großer Erfahrung, die EUS und EUS-FNA routinemäßig zur Abklärung zystischer Pankreasläsionen einsetzen, bis zu einem Drittel der präoperativen Diagnosen zystischer Pankreastumoren falsch. In einer retrospektiven Analyse von 136 operierten Patienten mit zufällig entdeckten zystischen Pankreasläsionen, die präoperativ als neoplastisch charakterisiert worden waren, erwiesen sich 5 % als nicht neoplastisch und damit die Operationsindikation als falsch. Umgekehrt stellte sich bei 20 % der als BD-IPMN diagnostizierten Läsionen eine Hauptgangbeteiligung heraus [10]. Es muss davon ausgegangen werden, dass im klinischen Alltag die diagnostische Treffsicherheit noch deutlich geringer ist. Nachdenklich stimmen auch kürzlich publizierte Ergebnisse einer Umfrage unter USamerikanischen Viszeralmedizinern und Endosonografikern [11]. Nur wenig mehr als ein Viertel aller Endosonografiker und knapp 10% der nicht spezialisierten Viszeralmediziner hatten Kenntnis von den Konsensus-Leitlinien der International Association for Pancreatology für das Managment muzinöser zystischer Pankreasneoplasien [8]. Die Akzeptanz und Umsetzung der Leitlinieninhalte war allenfalls mäßig ausgeprägt [11]. In einer Übersicht sollen daher die wichtigsten klinischen und endosonografischen Kriterien zystischer Pankreasläsionen dargestellt und ein leitliniengerechter diagnostischer Algorithmus abgeleitet werden. Übersicht über zystische Pankreasläsionen Pathologie, Biologie, Klinik, Therapie! Nicht-neoplastische Zysten Pseudozysten Unter den symptomatischen zystischen Pankreasläsionen dominieren mit etwa 75 % zweifelsohne die Pseudozysten. Aufgrund ihrer Genese besteht die unterschiedlich dicke Wandung aus extrazellulärer Matrix, Granulationsgewebe und im Zuge ihrer Ausreifung aus Bindegewebe, enthält aber keine Epithelzellen % aller Pseudozysten entstehen in Folge einer äthyltoxischen Pankreatitis. Die Häufigkeit von Pseudozysten bei akuter Pankreatitis ( akute Pseudozyste ) wird mit 5 16 % angegeben, bei chronischer Pankreatitis ( chronische Pseudozyste ) mit20 40%. Ca. 90% der Pseudozysten sind solitär, Lokalisation und Größe sind sehr variabel. Die Angaben zu einer Kommunikation von akuten Pseudozysten mit dem Pankreasgang variieren zwischen 6% und 60%. Chronische Pseudozysten weisen dagegen aufgrund ihrer Pathogenese (Gangruptur und vorgeschaltete Pankreasgangobstruktion) im Regelfall eine Kommunikation mit dem Pankreasgang auf, die jedoch nicht immer sicher dazustellen ist (37 72 %) [12 15]. Der flüssige Inhalt von Pseudozysten ist daher bis auf wenige Ausnahmen durch eine hohe Konzentration von Pankreasenzymen charakterisiert. Er kann wässrig-klar sein, ist jedoch aufgrund zurückliegender Nekrose und Blutungen häufig schmutzig-braun. Zytologisch dominieren amorphes gelbliches Pigment, Histiozyten und /oder Granulozyten sowie Cluster kernloser und nekrotischer Fettzellen [16]. In der Bildgebung kann nekrotisches Material solide Anteile vortäuschen (l" Abb. 1). Akute Pseudozysten haben insbesondere bei einer Größe <40 mm eine sehr hohe spontane Rückbildungsrate. Deutlich geringer ist dagegen die spontane Rückbildungsmöglichkeit chronischer Pseudozysten, insbesondere bei Lage im Pankreasschwanz und Obstruktion bzw. Kontinuitätsverlust des proximalen Pankreasgangs. Eine absolute Indikation zur dann meist endoskopischen (insbesondere endosonografisch gestützten) Therapie besteht bei symptomatischen Pseudozysten oder bei Komplikationen wie Gefäßkompression, intestinaler Obstruktion, obstruktiver Cholestase, Infektion oder Einblutung. Da bei einer Pseudozystengröße von mehr als 40 mm das Risiko von Komplikationen erhöht ist, sollte auch bei großen und größenprogredienten asymptomatischen Pseudozysten eine Therapie erwogen werden [12, 14, 15]. Epitheliale Zysten Die seltenen dysontogenetischen Pankreaszysten beruhen wahrscheinlich auf einer Sequestration duktaler Zellen. Sie weisen daher keine Kommunikation zum Gangsystem auf, sind mit normalen Gangepithelien ausgekleidet, mit klarer Flüssigkeit gefüllt und überwiegend klein und asymptomatisch. Ein gehäuftes Auftreten dysontogenetischer Pankreaszysten wird bei polyzystischer Erkrankung, von-hippel-lindau-syndrom und zystischer Fibrose beobachtet [5, 7, 17]. Abb.1 Große Pankreaspseudozyste der nicht echofreie Inhalt sprach im Zusammenhang mit der Klinik für eine infizierte Pseudozyste, bei der EUS-gestützten transgastralen Drainage entleerte sich Eiter.
3 Übersicht 255 Andere nicht-neoplastische Zysten Ebenfalls sehr selten sind lymphoepitheliale Zysten (LEC), Dermoidzysten (DC), Epidermoidzysten (ECISs), Retentionszysten (RC), muzinöse nichtneoplastische Zysten (MNC), Vorderdarm- Duplikaturzysten, zystische Hamartome und zystische Lymphangiome. Aufgrund ihrer epithelialen Auskleidung können sie zu differenzialdiagnostischen Problemen in der Abgrenzung zu zystischen n führen. Eine plattenepitheliale Auskleidung weisen LEC, DC und ECISs auf. RC, MNC und Duplikaturzysten zeichnen sich dagegen durch ein muzinöses Epithel aus [5, 6, 18 20]. Bei LEC ist die (teilweise verhornende) innere Plattenepithelschicht von einer subepithelialen Schicht lymphatischen Gewebes ausgekleidet, fokal kann das Epithel auch kubisch, flach, transitional oder in Einzelfällen muzinös sein. LEC treten in variabler Größe uni- oder multilokulär ohne anatomische Prädilektion bei Männern vierfach häufiger als bei Frauen (mittleres Alter: 56 Jahre) auf. Der Inhalt kann klar-wässrig, aber auch durch keratinösen Debris cremig oder käsig sein [19]. DC ähneln LEC, enthalten aber auch Haarfollikel, respiratorisches und muzinöses Epithel und treten eher bei jüngeren Patienten ohne Bevorzugung eines Geschlechts auf. Infektiöse Komplikationen sind häufig. ECISs sind als zystische Veränderungen intrapankreatischer Milzheterotopien durch rote Milzpulpa charakterisiert und fast ausschließlich im Pankreasschwanz anzutreffen [18]. RC entstehen als fokale zystische Erweiterung von Seitenästen des Pankreasgangs aufgrund einer duktalen Obstruktion durch Konkremente, fibrotische Striktur, Tumorwachstum oder Muzin. Sie sind durch muzinöses Epithel ausgekleidet [5, 6]. MNC finden sich überwiegend im Pankreaskopf, haben keine Gangkommunikation und treten bei Personen beiderlei Geschlechts mit einem mittleren Alter von 58 Jahren auf. Ihre Wandung besteht aus muzinösem Epithel ohne neoplastische Veränderungen [21]. Intrapankreatische Vorderdarm-Duplikaturzysten sind Raritäten und durch ein muzinöses Flimmerepithel charakterisiert. Die Zystenflüssigkeit enthält abgelöste Zilienbüschel [22, 23]. Nicht-neoplastische Pankreaszysten müssen nur dann einer operativen Therapie zugeführt werden, wenn sie symptomatisch sind. Neoplastische Zysten Zu unterscheiden ist zwischen echten zystischen n und soliden n mit durch Nekrose und Einblutung verursachter zystischer Degeneration. Etwa 8% der duktalen Adenokarzinome des Pankreas und 5 10% der neuroendokrinen Pankreastumoren weisen zystische Veränderungen auf (l" Abb.2, 3) [6, 24, 25]. Auch mesenchymale Tumoren und Pankreasmetastasen können als zystische oder solid-zystische Läsionen imponieren [26]. Ein typisches Beispiel für eine solide mit regelhaften zystisch-degenerativen Anteilen ist die solid-pseudopapilläre (SPN). Unter den echten zystischen n sind die intraduktalen papillär-muzinösen n (IPMN) am häufigsten, gefolgt von den serösen zystischen n (SCN) und den muzinösen zystischen n (MCN). Die relativen Häufigkeiten variieren in den publizierten Serien [5 7]. Sehr seltene echte zystische n sind zystische Azinuszelladenome, Azinuszelladenokarzinome und Lymphangiome [27, 28]. Seröse zystische (SCN) Unterteilt werden die SCN in das häufige mikrozystische Adenom (SMA, mit multiplen kleinen Zysten bis maximal 20 mm Einzeldurchmesser) sowie oligo- und makrozystische Varianten. Das Abb.2 Solid-zystischer Pankreasschwanztumor, die EUS-FNA ergab ein Adenokarzinom mit Nekrose. a b Abb.3a, b Kleiner zystischer neuroendokriner Tumor des Pankreas (a, 1,5 2cm), die soliden Anteile sind durch den Vaskularisationsnachweis mittels farbkodierter Duplexsonografie sicher von Debris oder Muzin zu differenzieren (b). SMA tritt bevorzugt bei Frauen im 7. Lebensjahrzehnt auf und wird vorwiegend im linksseitigen Pankreas gefunden. Die Zysten sind durch ein glykogenreiches kubisches oder flaches Epithel ausgekleidet und durch fibröse, gut durchblutete Septen voneinander separiert, die im Zentrum des Tumors zu einer zentralen,
4 256 Übersicht gelegentlich verkalkten Narbe zusammenlaufen. Durch die zahlreichen kleinen Zysten entsteht ein honigwabenartiges Bild. Der Zysteninhalt ist klar und serös. Sind die Zysten sehr klein, resultiert (in ca. 20 % der Fälle von SCN) bildgebend ein Honigwabenmuster (l" Abb. 4) oder sogar der Eindruck eines soliden echogenen Tumors. Die oligo- und makrozystischen Varianten der SCN mit einer Zystengröße >20 mm sind deutlich seltener als das SMA und bei Männern und Frauen annähernd gleich häufig. Anders als die mikrozystische Variante finden sie sich überwiegend im Pankreaskopf. Es handelt sich um lobulierte multizystische (multilokuläre) oder septierte Läsionen ohne zentrale Narbe (l" Abb. 5). Raritäten sind die morphologischen Extremvarianten des soliden und des unizystischen (unilokulären) SCA, das seröse Zystadenokarzinom sowie das multilokuläre SCA bei von-hippel- Lindau-Erkrankung [5, 7, 17, 29, 30]. Symptome bestehen lokalisations- und größenabhängig zum Diagnosezeitpunkt bei etwa der Hälfte aller Patienten mit SCN, meist handelt es sich um unspezifische Oberbauchbeschwerden [31 33]. SCN weisen eine mediane Größenzunahme von etwa 4 6mm pro Jahr auf. Tumoren 40 mm haben eine deutliche höhere jährliche Wachstumsrate (1,98 cm) als Tumoren < 40 mm (0,12 cm) [33]. Eine operative Therapie ist bei symptomatischen Tumoren und bei unklarer Differenzialdiagnose zu einer muzinösen indiziert und sollte auch bei asymptomatischen Patienten bei einer Tumorgröße ab 40 mm in Erwägung gezogen werden [33]. Muzinös-zystische (MCN) Betroffen sind nahezu ausschließlich Frauen im 2. bis 9. Lebensjahrzehnt (mittleres Alter: 48 Jahre). Die meisten Patientinnen sind symptomfrei oder haben uncharakteristische Oberbauchbeschwerden, bei jeder zehnten treten Pankreatitiden auf [34]. Mehr als 90 % der MCN sind in Pankreaskorpus oder -schwanz lokalisiert. Ein Ganganschluss liegt in >90 % der Fälle nicht vor und kommt allenfalls durch Fistelung zustande. MCN sind meist glatt konturiert, aber multilokulär mit perfundierten Septen ( cyst in cyst ) (l" Abb. 6). Eine dicke fibröse Kapsel ist typisch. Die Läsionen sind durch eine muzinöses Epithel ausgekleidet, das Stroma ist identisch zum ovariellen Stroma. Der Zysteninhalt ist klar und aufgrund des Muzingehaltes variabel viskös. Größenabhängig liegen fokale Atypien vor. Es besteht eine Adenom-Karzinom-Sequenz, sodass das Malignitätsrisiko mit dem Alter zunimmt [34 36]. In großen chirurgischen Serien fand sich zum Zeitpunkt der Diagnose eine maligne Entartung zum muzinösen Zystadenokarzinom in 17,5 % bis 27 % der Fälle. Prädiktiv für Malignität sind ein Durchmesser 40 mm und murale Noduli [34 36]. Daher wird unter Berücksichtigung des Alters der Patientinnen und der günstigen Lokalisation im linken Pankreas für alle MCN grundsätzlich eine operative Therapie vorgeschlagen [8]. Intraduktale papillär-muzinöse (IPMN) IPMN sind inzwischen die häufigsten zystischen Pankreasneoplasien. Morphologisch handelt es sich um durch Schleimproduktion verursachte zystische Dilatationen von Hauptgang (MD- IPMN, ca. 30 %) oder von Seitenästen (BD-IPMN, ca. 70 %). Mischtypen wurden beschrieben und machen in einzelnen Serien bis zu 38 % aller IPMN aus [37]. IPMN sind durch eine meist papilläre Proliferation neoplastischer muzinöser Gangepithelien charakterisiert. Es werden Adenome, Borderlineläsionen, in-situ-karzinome und invasive Karzinome unterschieden. Männer erkranken allenfalls geringfügig häufiger als Frauen, meist im Alter zwischen 40 und 80 Jahren. BD-IPMN und MD-IPMN unterscheiden sich hinsichtlich ihres Epitheltyps, des Muzinmusters, der Symptomatik und in der Prognose (l" Tab.1) [38 40]. Bei beiden Typen finden sich aufgrund der Pankreasgangobstruktion durch Muzin gehäuft (ca. 1 / 3 der Fälle) akut-rekurrierende oder obstruktive chronische Pankreatitiden [41, 42]. Weitere Symptome sind Oberbauchschmerzen, Gewichtsverlust, Diarrhö, Neuauftreten oder Verschlechterung eines Diabetes mellitus, seltener auch eine obstruktive Cholestase. Während Hauptgang-IPMN in einer großen Serie aus zwei chirurgischen Referenzzentren in den USA und in Italien nur in 27% der Fälle asymptomatisch waren [43], gilt dies für 86% der BD-IPMN [44], darunter für 40% der operativ behandelten [45]. BD-IPMN imponieren als meist polyzystische, traubenartig konfigurierte Zysten ( cyst by cyst ) mit Gangassoziation und treten nicht selten multifokal auf [46]. Ihre Hauptlokalisation ist der Processus uncinatus (l" Abb. 7, 8). BD-IPMN sind bei Diagnosestellung mit durchschnittlich 20 % (6 % 40 %; im Mittel 15 % mit invasivem Wachstum) wesentlich seltener maligne entartet als MD-IPMN [8]. Mit Malignität sind assoziiert eine Größe > 30 mm, ein Zystenwachstum > 2mm / Jahr, murale Noduli>6,5mm, eine dicke Wand und eine Pankreasgangweite> 5 6 mm [8, 47, 52]. BD-IPMN sind eine Präkursor- und Indikatorläsion für duktale Adenokarzinome des Pankreas [53]. Es besteht eine Assoziation mit dem Peutz-Jeghers-Syndrom, der Familiären Adenomatösen Polyposis und dem familiären Pankreaskarzinom. Im EUS-Screea b Abb.4a, b Typische mikrozystische SCN mit einem Durchmesser von knapp 4 cm (a), in der Powerdopplerdarstellung sind die echogenen Septen perfundiert (b).
5 Übersicht 257 a c b d Abb.5a d Makrozystische SCN, diagnostisch wegweisend sind Lokalisation im Pankreaskopf und die Lobulierung(a, Sternmarkierung: echoarme ventrale Anlage) sowie eine kleine Wandprotrusion (b, Pfeil). Nach Injektion des Ultraschallkontrastverstärkers SonoVue erweist sich die Wandprotrusion als perfundiert(c, Pfeil). Die EUS-FNA (d, Nadel durch Pfeile markiert) ergab ein zellarmes Aspirat ohne Epithelien, der CEA-Spiegel war 12 ng /ml, die Lipase lag im Bereich des Serumspiegels. Die postoperative Histologie zeigte, dass es sich bei der Wandprotrusion um Mikrozysten handelte. Abb.6 Typischer Befund einer muzinös-zystischen : Lokalisation im Pankreasschwanz einer 47-jährigen Patientin, glatte Kontur, Septen, 6mm kleine noduläre Wandprotrusion (zwischen den Messkreuzen). Abb.7 Intraduktale papillär-muzinöse vom Seitengangtyp (BD- IPMN): Lokalisation im Genua pancreatis einer 72-jährigen Patientin, rezidivierende Oberbauchschmerzen. Gut erkennbar: Kommunikation mit dem Pankreasgang (Pfeil=Seitengang, P=Pankreashauptgang) und nicht echofreies intrazystisches und intraduktales Muzin (Sternmarkierung).
6 258 Übersicht a Abb.8 BD-IPMN im kopfnahen Pankreaskorpus einer asymptomatischen 72-jährigen Patientin. Unmittelbar benachbarte mittelgroße und kleine Zyste (a), eine Gangkommmunikation war darstellbar (nicht abgebildet). Nach Injektion von SonoVue Darstellung der ausgeprägten Wandvaskularisation (b). CEA im zellarmen Aspirat 150 ng /ml, Lipase 45IU /ml, einzelne schleimproduzierende Epithelien ohne Atypie). Tab.1 b ning von Personen mit genetisch erhöhtem Risiko für ein Pankreaskarzinom sind sie daher ein relativ häufiger Befund [54]. Interessanterweise ist im Verlauf von Patienten mit BD-IPMN die Entwicklung duktaler Adenokarzinome an anderer Lokalisation des Pankreas ein wesentlich häufigeres Ereignis als die maligne Entartung der BD-IPMN selbst [55]. Zur BD-IPMN synchrone und metachrone duktale Adenokarzinome des Pankreas sind überzufällig häufig [48, 55, 56]. Risikofaktoren für die metachrone Entwicklung eines duktalen Adenokarzinoms sind ein Alter> 70 Jahre sowie das weibliche Geschlecht [55, 57, 58]. Klinische Prädiktoren für die Diagnose eines Pankreaskarzinoms bei Patienten mit BD-IPMN sind die Verschlechterung der Stoffwechsellage eines Diabetes mellitus, Ikterus und ein erhöhter Serumspiegel von CA19-9 [45, 48, 56]. Für die Verlaufskontrolle von BD-IPMN ergibt sich aus diesen Daten die Forderung, nicht nur die Entwicklung des BD-IPMN zu beobachten, sondern stets das gesamte Pankreas sorgfältig nach neuen Läsionen abzusuchen. Da auch extrapankreatische n (von Kolorektum, Prostata und Harnwegen, weiblicher Brust, Haut und Lunge sowie in Asien auch des Magens) gehäuft auftreten, können entsprechende Screeninguntersuchungen bei Patienten mit BD- IPMN sinnvoll sein [59 64]. MD-IPMN sind segmentale, zu 80 % im Pankreaskopf gelegene Dilatationen des muzingefüllten Dc. Wirsunganus, seltener auch des Dc. Santorini. Eine Muzinpapille ( Fischmaulpapille ) findet sich nur bei etwa der Hälfte der Patienten mit MD-IPMN. Bei Diagnosestellung besteht in etwa 70 % (60 92 %) eine maligne Entartung mit invasivem Wachstum in 2 / 3 dieser Fälle [8]. Prädiktoren für Malignität sind höheres Patientenalter, klinische Symptome (Ikterus, Verschlechterung der diabetischen Stoffwechsellage), eine Gangweite > 15 mm und murale Noduli (l" Abb. 9) [43, 65]. Die Indikationen für ein operatives Vorgehen wurden 2006 in einer Leitlinie der International Association of Pancreatology zusammengefasst, die zunächst überwiegend auf Erfahrungswissen fußte [8]. Patienten mit MD-IPMN soll grundsätzlich eine operative Therapie empfohlen werden, wenn Operationsrisiko und Lebenserwartung dies zulassen. Für BD-IPMN wird eine individualisierte Operationsentscheidung auf der Grundlage mindestens eines der folgenden Kriterien vorgeschlagen: Symptomatik, Merkmale und Prognose verschiedener Typen von intraduktalen papillär-muzinösen n (IPMN), Daten nach im Text zitierten Quellen. histologischer Typ relative Häufigkeit MD-IPMN intestinal 20% CDX2+ MUC2 + MUC5AC+ MUC1 pankreatobiliär 8% MUC1+ MUC5AC+ MUC2 CDX2 Immun- Invasivität Entartung und Prognose Phänotyp 1 36% muzinöses Adenokarzinom, Prognose günstiger als beim duktalen Adenokarzinom >50% duktales Adenokarzinom onkozytär sehr selten MUC6 + >50% duktales Adenokarzinom BD-IPMN gastrisch 70% MUC5AC + MUC6 + MUC1 MUC (15)% duktales Adenokarzinom 1 MUC2 (sekretorisches intestinales Muzin), MUC5AC (Muzin des gastralen Oberflächenschleims) und MUC6 (Muzin der gastralen Pylorus- und Fundusdrüsen) sind sekretorische Muzine und daher sowohl in epithelialen Tumorzellen als auch im sezernierten Schleim muzinöser n nachzuweisen; MUC1 (pan-epitheliales Membranmuzin) ist dagegen membrangebunden. CDX2 ist eintranskriptionsfaktor mit hoher Spezifität für intestinale n. Normales Pankreasgewebe exprimiert regelhaft MUC1, gelegentlich MUC6 und niemals MUC2 und MUC5AC. Duktale Pankreaskarzinome exprimieren MUC5AC und im Gegensatz zu IPMN mit Ausnahme des pankreatobiliären Typs MUC1. MCN haben kein spezifisches Muzinexpressionmuster [53].
7 Übersicht 259 a Abb.9a, b Typische MD-IPMN bei einem 70-jährigen Mann mit exokriner Pankreasinsuffizienz, Gewichtsabnahme und unspezifischen Oberbauchbeschwerden. Büschelartige, bei Schallkopfandruck mobile echogene Strukturen im stark erweiterten Pankreasgang (Pfeile), Wandung mit papillären Zystengröße > 30 mm, noduläre Wandläsionen, Hauptgangweite > 6 mm und positive Zytologie [8]. Auf der Grundlage dieser Kriterien müssen weniger als 20 % aller BD-IPMN operiert werden [44]. Arbeiten der letzten Jahre haben die Validität dieser Empfehlungen bestätigen können. Die Sensitivität der Leitlinienkriterien für die Diagnose maligner BD-IPMN lag in 3 Studien zwischen 97,3 % und 100 %, die Spezifität war dagegen niedrig (23 29,8 %) [66 68]. Für die Nachsorge von BD-IPMN < 10 mm sieht die Leitlinie radiologische Schnittbildmethoden vor, bei BD-IPMN von mm Größe EUS(-FNA) in Kombination mit MRCP oder ERCP. Bis zu einer Zystengröße von 20 mm werden Kontrollintervalle von 6 12 Monaten vorgeschlagen, bei BD- IPMN von mm von 3 6 Monaten. Nach 2 Jahren ohne Änderung können diese Intervalle verlängert werden. Umgekehrt sollte bei Auftreten von Symptomen, Größenzunahme auf > 30 mm oder Auftreten von Alarmkriterien (murale Noduli, Hauptgangdilatation >6 mm, atypische Zytologie) eine operative Therapie initiiert werden [8]. Solid-pseudopapilläre (SPN) Es handelt sich um meist sehr große, in Pankreaskorpus und -schwanz lokalisierte, glatt begrenzte solid-zystische Raumforderungen, die ganz überwiegend bei jungen Frauen (mittleres Lebensalter: 20 Jahre) diagnostiziert werden. Das Auftreten bei Männern wurde in Einzelfällen beschrieben. Die zystischen Anteile kommen durch Nekrose und Einblutung zustande und enthalten meist eine sanguiolente Flüssigkeit. Eine Gangassoziation besteht nicht. Die Tumorzellen exprimieren Sexualhormonrezeptoren, Vimentin, NSE und α1-antitrypsin. Bis zu 15 % der SPN rezidivieren oder metastasieren. Bei Nachweis einer SPN wird die operative Therapie empfohlen [69, 70]. Differenzialdiagnose! Anamnese und Klinik Schon die konsequente Anwendung anamnestischer und klinischer Kriterien (Alter, Geschlecht und Pankreatitis-Anamnese) führt zu einer relativ hohen Prätestwahrscheinlichkeit für die b Proliferationen (Sternmarkierung) (a). CELMI-EUS nach Injektion von Sono- Vue in einer späteren Untersuchung: Nachweis der ausgeprägten Vaskularisation der papillennahen neoplastischen Wandproliferationen (b, Pfeilmarkierungen). Differenzierung der häufigsten zystischen Pankreasläsionen (l" Tab. 2). Sehr deutlich wird dies an den Ergebnissen einer radiologischen Untersuchung. CT-morphologische Kriterien alleine erlaubten nur in 39 % der Fälle eine korrekte Diagnose zystischer Pankreasläsionen. Die Klassifikation in benigne und (potenziell) maligne Entitäten gelang in 61 % der Fälle, die Übereinstimmung von zwei Radiologen war gering (Kappa 0,28). Nach Entblindung der Untersucher gegenüber klinischen Informationen und weiteren Untersuchungsbefunden konnte das maligne Potenzial jedoch in 90 % der Fälle korrekt bestimmt werden, und die Untersucherübereinstimmung war nunmehr hoch (Kappa 0,73) [71]. Klinische Kriterien, die für Malignität zystischer Pankreasraumforderungen sprechen, sind fortgeschrittenes Alter, männliches Geschlecht, weiße Rasse, Gewichtsverlust, Ikterus, Oberbauchschmerzen, Neuentwicklung oder Verschlechterung eines Diabetes mellitus und erhöhte Serumspiegel von CA19 9 und CEA [44, 45, 48, 49, 56, 72 77]. EUS-Morphologie Bedeutsam für die Differenzierung zystischer n ist die Kenntnis ihrer Lokalisation (l" Tab. 2) sowie die Beurteilung der Morphologie von zystischer Läsion und Gesamtorgan (l" Tab. 3). Das wichtigste morphologische Einzelkriterium für die Beurteilung des Malignitätsrisikos einer zystischen Pankreasläsion ist zweifelohne deren Größe. Asymptomatische zystische Pankreasläsionen mit einem Durchmesser von 30 mm sind mit einer Wahrscheinlichkeit von % benigne [78, 79]. Eine Ausrichtung der Operationsindikation nur an der Zystengröße führt daher in bis zu einem Fünftel der Patienten zu einem inadäquaten Vorgehen. Eine bessere Differenzierung und prognostische Einschätzung ist möglich, wenn neben der Zystengröße weitere morphologische Kriterien Berücksichtigung finden. Der Stellenwert morphologischer EUS-Kriterien für die Charakterisierung und Differenzialdiagnose zystischer Pankreasläsionen wird in der Literatur allerdings unterschiedlich bewertet [80, 81]. Die Übereinstimmung erfahrener Endosonografiker in der Differenzierung neoplastischer von nicht-neoplastischen Pankreaszysten und in der Bewertung von Einzelkriterien erwies sich in einer
8 260 Übersicht Tab.2 Klinisch-anamnestische und morphologische Kriterien zystischer Pankreasneoplasien (Daten nach im Text zitierten großen Fallserien). Pseudozyste serös-zystische (SCN) Untersuchung als sehr gering (Kappa 0,24). Die 8 für klinische Informationen geblindeten Untersucher stimmten nur in der Diagnose von SCN (Kappa 0,46) und hinsichtlich des Vorhandenseins solider Anteile (Kappa 0,43) mäßig gut überein [82]. Problematisch kann die Differenzierung oligo-/ makrozystischer SCN von MCN sein. Allerdings sind diese im Gegensatz zu MCN überwiegend im Pankreaskopf lokalisiert und zeichnen sich durch eine nicht oder kaum erkennbare Zystenwand [83], eine Lobulierung und einen echofreien Zysteninhalt aus. In etwa der Hälfte der Fälle oligo-/makrozystischer SCN sind zusätzlich zu den Makrozysten auch winzige Mikrozysten erkennbar (l" Abb. 5) [84, 85]. Bei der im Einzelfall ebenfalls schwierigen Differenzialdiagnose von MCN und Pseudozysten hilft neben anamnestischen Informationen (Alkohol- und Pankreatitisnamnese; Geschlecht) vor allem muzinös zystische (MCN) intraduktal papillärmuzinöse (IPMN) solid-pseudopapilläre (SPN) Geschlecht m>w mikrozystisch w>>m(>20:1) m w w>>m(9:1) w>m(3:1) makrozystisch m w Alter variabel mittleres Alter 62 Jahre mittleres Alter 45Jahre mittleres Alter 65Jahre mittleres Alter 20Jahre Pankreatitis obligat nein selten > 30 %; akut-rekurrierend, nein chronisch Prädilektion variabel, meist unifokal >70%links, meist unifokal >70%links, meist unifokal >70%Caput BD-IPMN: überwiegend links, unifokal oft multifokal Gang-Kommunikation im Regelfall nein nein obligat nein Morphologie keine Septen oder soliden Anteile, evtl. Debris avaskulär mikrozystisch: Honigwabenmuster makrozystisch: lobuliert, unilokulär oder multilokulär (septiert) hypervaskulär oft septiert ( cyst in cyst ), dicke Wand, murale Noduli hypervaskulär Malignität nie <3% 25% MD: 70 % BD: 20% Tab.3 Bei der endosonografischen Charakterisierung und prognostischen Einschätzung zystischer Pankreasläsionen zu beantwortende Fragestellungen (modifiziert nach [9]). Bestehen duktale oder parenchymatöse Kriterien einer chronischen Pankreatitis? Ist der Pankreasgang (segmental) erweitert? Im Falle einer Gangerweiterung: liegt eine Gangobstruktion vor? In welchem Anteil des Pankreas ist die zystische Läsion lokalisiert? Ist die zystische Läsion uni- oder multilokulär? Wie groß ist zystische Läsion insgesamt? Wie groß sind die Einzelzysten? Ist die Läsion polyzystisch, oligozystisch oder unizystisch? Besteht eine Gangassoziation (Hauptgang, Seitengang)? Ist die Kontur glatt, lobuliert oder unscharf? Bestehen Infiltrationszeichen? Ist der Zysteninhalt echofrei oder fallen echogene Binnenstrukturen auf (Debris, Muzin)? Wie dick ist die Wandung? Ist die Wandung vaskularisiert? Liegt eine Septierung vor? Sind die Septen vaskularisiert? Bestehen murale Noduli? Wie groß sind die muralen Noduli? Sind diese vaskularisiert? Liegen solide Anteile vor? Sind diese vaskularisiert? MD-IPMN: zystische Gangdilatation, murale Noduli BD-IPMN: cyst bycyst hypervaskulär oft riesig, solide mit Nekrosen hypervaskulär <15% der Nachweis von Parenchym- und Gangkriterien einer chronischen Pankreatitis weiter. Eine nahezu runde Form, Septen, fokale Wandverdickungen und noduläre Wandprotrusionen sind typisch für MCN (l" Abb.6), können im Einzelfall aber auch bei Pseudozysten beobachtet werden. Multiple Zysten des Pankreas finden sich vorwiegend bei der BD-IPMN, aber auch bei dysontogenetischen Zysten im Kontext einer polyzystischen Leber- und Nierenerkrankung sowie bei der von-hippel-lindau-erkrankung. Entscheidend ist daher die gründliche Suche nach einer Gangkommunikation, die das entscheidende diagnostische Kriterium für eine BD-IPMN ist. Auch traubenartige Zystenkonglomerate und papilläre Wandprotrusionen sprechen für diese Diagnose. Die MD-IPMN sind im Regelfall endosonografisch sicher zu diagnostizieren. Schwierigkeiten können sich aber in der Abgrenzung zu einer chronischen Pankreatitis ergeben, zumal in Korpus und Kauda häufig neben der Gangerweiterung Parenchymkriterien einer (durch den chronischen Sekretstau) verursachten chronischen Pankreatitis auffallen. Im Gegensatz zum MD-IPMN, wo die Gangdilatation Ausdruck der Muzinproduktion ist, beruht die Gangerweiterung bei der chronischen Pankreatitis jedoch auf Gangobstruktionen durch Strikturen und / oder Pankreatolithen [86]. Muzin kann gelegentlich als echogenes intraduktales Substrat nachgewiesen werden, ist aber endosonografisch sehr gut von Pankreatolithen zu unterscheiden (l" Abb. 7, 9). Besonders wichtig ist die sorgfältige endosonografische (und endoskopische) Inspektion der Papille, um zwischen einer Stenose (obstruktive Pankreatitis) und einer durch Muzin klaffenden Papille zu differenzieren. Der Nachweis papillärer Wandproliferationen ist diagnostisch für eine IPMN (l" Abb. 9). Morphologische Kriterien, die für Malignität sprechen, wurden bereits weiter oben den verschiedenen Entitäten zugordnet. Kontrastverstärkte Endosonografie Der Einsatz der kontrastverstärkten Endosonografie (CE-EUS) scheint nach neueren Daten die Trennschärfe in der Differenzierung zystischer Pankreasläsionen zu erhöhen. Es können 2
9 Übersicht 261 unterschiedliche Techniken zum Einsatz gebracht werden die kontrastverstärkte Powerdopplersonografie oder Farbduplexsonografie mit hohem mechanischem Index oder die kontrastverstärkte harmonische Endosonografie mit niedrigem mechanischem Index (CELMI-EUS) [87]. Die erstgenannte Technik kann mit allen elektronischen Endosonografiesystemen unter Einsatz der Farbkodierung oder des Powerdopplers durchgeführt werden (l" Abb. 5 c, 8b). Sehr geringe Dosen von Ultraschall-Kontrastverstärker sind dazu ausreichend (z. B. 1 ml SonoVue, Bracco). CEL- MI-EUS ist nur mit der neuesten Generation von Endosonografiesystemen durchführbar und erfordert die Applikation vergleichweise hoher Dosen (z. B. 5 ml SonoVue, Bracco; l" Abb.9b). Zu achten ist insbesondere auf vaskularisierte Septen, papilläre Wandproliferationen und solide Anteile. Beyer-Enke et al. haben kürzlich an einer großen Anzahl zystischer Pankreasläsionen demonstrieren können, dass durch den Nachweis vaskularisierter Septen und Noduli mittels kontrastverstärkter transabdomineller Sonografie zystische n mit einer Sensitivität von 94 % und einer Spezifität von 97 % von Pseudozysten zu differenzieren sind [88]. Es ist davon auszugehen, dass diese Ergebnisse prinzipiell auch auf die Endosonografie übertragbar sind. Japanische Autoren konnten durch Nachweis und Charakterisierung muraler Noduli und solider Anteile mittels kontrastverstärkter Endosonografie das maligne Potenzial von IPMN mit einer hohen Genauigkeit charakterisieren [49]. Muzin kann im Grauwertbild nicht sicher von papillären Wandproliferationen unterscheidbar sein, der Nachweis oder Ausschluss einer Vaskularisation durch CE-EUS ist hier diagnostisch zielführend (l" Abb.9b). Endosonografische Feinnadelaspiration und Biopsie Die endosonografische Feinnadelaspiration (EUS-FNA) ist zur Charakterisierung zystischer Pankreasläsionen etabliert [81]. Sie ist nicht erforderlich und auch selten ergiebig, wenn ein pathognomischer Befund für eine mikrozystische SCN vorliegt [89, 90]. Auch IPMN können in vielen Fällen ohne EUS-FNA diagnostiziert werden. Hoch ist der Stellenwert dagegen in der Differenzierung makrozystischer Läsionen, bei denen zwischen non-neoplastischen und benignen Befunden und muzinösen n unterschieden werden muss (l" Abb. 5 d). Die EUS-FNA hat 2 Ziele: im Vordergrund steht die Gewinnung von Zysteninhalt zur makroskopischen und biochemischen, zusätzlich auch zur zytologischen und im klinisch definierten Einzelfall mikrobiologischen Analyse. Darüber hinaus sollte immer versucht werden, aus soliden Anteilen, papillären Wandproliferationen und der Wandung Material für die zytologische oder histologische Untersuchung zu gewinnen. Im Regelfall werden daher Aspirationsnadeln (22 Gauge, 19 Gauge) genutzt. Aufgrund des im Vergleich zur EUS-FNA solider Läsionen höheren Komplikationsrisikos (2 6%) [91, 92] durch Zysteninfektion, akute Pankreatitis und Blutung empfehlen wir die Durchführung einer periinterventionellen Antibiotikagabe (z. B. Gyrasehemmer unmittelbar präinterventionell intravenös, dann über 3 5 Tage oral), die möglichst komplette Aspiration des flüssigen Zyteninhalts und die Beschränkung auf nur 1 oder 2 Nadelpassagen. Blutungen werden immer wieder beobachtet, sistieren jedoch im Regelfall spontan und ohne klinische Folgen nach Koageltamponade der Zyste. Makroskopische Beurteilung Es sollte nie versäumt werden, die makroskopische Beurteilung des Zysteninhaltes in die differenzialdiagnostische Beurteilung einzubeziehen. Ein visköser, muzinreicher Zysteninhalt ist leicht daran zu erkennen, dass sich beim langsamen Anheben der Nadel aus dem Flüssigkeitsspiegel ein Schleimfaden ziehen lässt. Die maximal vor Abriss des Schleimfadens erreichbare Fadenlänge kann als Surrogatparameter für die Flüssigkeitsviskosität ( string sign ) genutzt werden, wenn die Viskositätsbestimmung mit einem Viskosimeter nicht möglich ist [93, 94]. Der Inhalt von Pseudozysten ist oft schmutzig-braun, der von LEC und CD, aber auch von kleinen Fettgewebsnekrosen gelegentlich weißgelb und milchig, schaumig oder cremig [95, 96]. Zytologie Im Gegensatz zu soliden Läsionen ist der Stellenwert für die Diagnose zystischer Pankreasläsionen begrenzt. Dies ist dem geringen Zellgehalt des Zysteninhalts und der oft geringen Größe solider Anteile geschuldet. Eine kürzlich veröffentlichte Metaanalyse, in die histologisch kontrollierten Ergebnisse der EUS- FNA-Zytologie von 376 Patienten aus 11 Studien eingingen, fand eine gepoolte Sensitivität und Spezifität für die Diagnose muzinöser zystischer Pankreasneoplasien von 63 % bzw. 88 % [97]. Pseudozysten konnten in einer Untersuchung nur in 10 % der Fälle anhand der Aspirationszytologie zweifelsfrei diagnostiziert werden [16]. Bei SCN gelang dies in 20 % bzw. 25 % der Fälle [89, 90], während für muzinöse n diagnostische Ausbeute und Genauigkeit der EUS-FNA-Zytologie besser sind. Eine negative oder nicht diagnostische Aspirationszytologie ist jedoch bei malignen und prämalignen zystischen Pankreasneoplasien nicht selten und darf bei Vorliegen klinischer, morphologischer und / oder biochemischer Kriterien für eine potenziell maligne Zyste nicht von den notwendigen operativen Konsequenzen abhalten [98]. Andererseits ist eine für eine neoplastische Zyste positive Aspirationszytologie bei Patienten mit asymptomatischen, kleinen, und morphologisch nicht suspekten Pankreaszysten für das Stellen der Operationsindikation von sehr großer Bedeutung. In diesem Kontext darf allerdings nicht übersehen werden, dass ein relevantes Risiko falsch positiver Befunde durch Kontamination des Aspirates mit gastralen oder duodenalen Epithelien aus dem Punktionsweg besteht [16, 89]. Diese gastroduodenalen Kontaminationen sind für den Zytologen auch unter Einsatz immunhistochemischer Methoden nur sehr schwer von muzinproduzierenden Zystenepithelien zu differenzieren [99 101] und können im Einzelfall zur Fehldiagnose einer muzinösen mit Atypie führen [16, 89]. Sinnvoll ist in jedem Fall die gezielte Punktion solider Anteile oder der Zystenwand (l" Abb.5d) [102]. Die Ausbeute der EUS-FNA-Zytologie kann auch durch Nutzung einer Zytologiebürste über das Lumen einer 19-Gauge-Aspirationsnadel [ ] gesteigert werden. Allerdings war der Einsatz der Zytologiebürste in 2Fallserien mit einer Rate klinisch relevanter Komplikationen von 8% bzw. 10% verbunden [103, 104]. Einen sehr hohen Stellenwert hat die Aspirationszytologie für die Diagnose seltener zystischer Pankreasläsionen wie der SPN [106, 107], lymphoepithelialer Zysten [95, 96], zystischer Lymphangiome [27, 108, 109], zystischer neuroendokriner Tumoren [110] und von Duplikaturzysten [22]. Immunzytochemische Untersuchungen (z. B. Muzinprofil, CD10, CK20, CDX2, E-cadherin, beta-catenin) sind an einem Teil der Feinnadelaspirate möglich und könnten zukünftig die Differenzierung muzinöser zystischer Läsionen erleichtern [ ]. Bei IPMN und MCN tragen zytologische Kriterien zur Diagnose von Dysplasie und maligner Entartung bei [51, 52, 77, ]. Finden sich im Aspirat aus einer Pankreaszyste keine epithelialen Zellen, dafür aber Entzündungszellen und vor allem Makrophagen und Histiozyten vor einem amorphen gelblichen Hintergrund, ist dieser Befund typisch für eine Pseudozyste [16].
10 262 Übersicht Biochemie Die biochemische Analyse der Zystenflüssigkeit hat möglicherweise einen höheren Stellenwert als die Aspirationszytologie. Zur Bestimmung der diagnostisch relevanten Parameter (Lipase, CEA, Muzin) ist weniger als 1 ml Flüssigkeit erforderlich. Eine hohe Lipasekonzentration spricht für eine Kommunikation mit dem Gangsystems und wird daher bei Pseudozyten und IPMN, nicht aber bei SCN, nichtneoplastischen Zysten und MCN angetroffen [94, 119, 120]. MCN zeichnen sich gegen (oligo-/ makrozystische) SCN und Pseudozysten durch hohe CEA-Spiegel in der Zystenflüssigkeit aus, wobei die Cut-off-Werte in verschiedenen Studien teilweise deutlich differieren. In der multizentrischen cooperative pancreatic cyst study konnten Brugge et al. die Überlegenheit von CEA gegenüber anderen Tumormarkern (CA19-9; CA72-4; CA125; CA15-3), der Morphologie und der Zytologie demonstrieren und einen Cut-off-Wert von 192 ng/ ml definieren (Sensitivität 73 %; Spezifität 84 % für die Diagnose einer muzinösen zystischen ) [121]. Ein optimaler Cut-off-Wert von etwa 150 bis 200 ng/ ml wurde inzwischen auch in weiteren Untersuchungen mit hohen Fallzahlen bestätigt [ ]. Höhere Cut-off-Werte von 480 ng/ ml [94] oder 800 ng/ ml [109, 120] erreichen eine Spezifität von >95 % zu Lasten einer deutlich reduzierten Sensitivität. Es muss darauf hingewiesen werden, dass erhöhte CEA-Werte auch in lymphoepithelialen Zysten, non-neoplastischen muzinösen Zysten und verschiedenen anderen zystischen Pankreasläsionen gemessen werden [96]. Die in einigen Studien nachgewiesene Assoziation extrem hoher CEA- Werte in der Zystenflüssigkeit mit einer malignen Entartung muzinöser Zysten [75, 94, 117] war in anderen Serien nicht reproduzierbar [122, 124]. Auch der Nachweis einer erhöhten Aspiratviskosität (>1,6) oder von Muzin im Zystenaspirat ist geeignet, zwischen muzinösen zystischen n und benignen zystischen Läsionen zu differenzieren [94, 125]. Die Differenzierung zwischen BD-IPMN und MCN kann möglicherweise durch Messung von PGE2 im Zystenaspirat erleichtert werden [126]. Tab.4 EUS-FNA-Kriterien für die Charakterisierung zystischer Pankreasläsionen (Daten nach im Text zitierten Quellen). Pseudozyste serös-zystische (SCN) Molekularbiologie Molekularbiologische Untersuchungen der Zystenflüssigkeit erfordern eine hohe Expertise des Labors und haben trotz vielversprechender Ergebnisse vor allem aus Studien mit kleiner Fallzahl bisher nicht in die klinische Routine Eingang gefunden. In einer prospektiven multizentrischen Studie hatten die Ergebnisse einer Untersuchung der Zystenflüssigkeit auf k-ras-mutation, Heterozygotie-Verlust und DNA-Quantität und -Qualität eine sehr hohe Genauigkeit. Insbesondere konnten alle malignen zystischen n richtig erkannt werden, bei deren Diagnose die Aspirationszytologie versagte [123]. Synthese Erwartungsgemäß kann durch die Kombination aus biochemischen Markern (CEA, Muzin) in der Zystenflüssigkeit und Aspiratzytologie die diagnostische Genauigkeit in der Differenzierung zystischer Pankreasläsionen deutlich gesteigert werden (l" Tab. 4). In einer Serie von 174 Patienten, die wegen zystischer Pankreasläsionen operiert wurde, lagen in 121 Fällen die Ergebnisse einer präoperativen EUS-FNA vor und konnten mit der endgültigen pathologisch-anatomischen Diagnose verglichen werden. Die Sensitivität bzw. Spezifität waren für den Nachweis von Muzin in der Zystenflüssigkeit 80 % bzw. 40 %, für den Nachweis von hohen CEA-Spiegeln 93 % bzw. 43 % und für die Zytologie 38 % bzw. 90 %. Waren die Ergebnisse von Muzin, CEA oder Zytologie typisch, wurde für die Diagnose einer muzinösen eine Sensitivität von 92 % bei einer Spezifität von 52 % erreicht [125]. Damit gelingt es, durch die kombinierte Anwendung biochemischer Marker und der Aspirationszytologie nahezu alle muzinösen zystischen Pankreasläsionen zu erfassen, allerdings zu Lasten einzelner falsch positiver Diagnosen. Es ist anzunehmen, jedoch bisher nicht durch Daten belegbar, dass das Risiko einer falsch positiven Diagnose durch Einbeziehung klinischanamnestischer Daten, der Lokalisation und EUS-morphologischer Kriterien noch erheblich reduziert werden kann. Schlussfolgerungen und Ausblick! Die Differenzialdiagnose zystischer n bleibt auch unter Ausschöpfung aller zur Verfügung stehenden Methoden einschließlich der (kontrastverstärkten) Endosonografie und der endosonografischen Feinnadelaspiration schwierig. Morphologische, biochemische und zytologische Einzelkriterien differenzieren im Regelfall nicht ausreichend sicher zwischen (potenziell) malignen und sicher benignen zystischen Pankreasläsionen. Fallstricke wie die Kontamination von endosonografisch gewonnenem Zysteninhalt durch Epithelien und Muzin aus dem gastralen muzinös zystische (MCN) intraduktal papillärmuzinöse (IPMN) solid pseudopapilläre (SPN) Flüssigkeit schmutzig, nonviskös klar, nonviskös klar-milchig, viskös klar-milchig, variabel blutig, nonviskös viskös Lipase oder hoch niedrig niedrig hoch niedrig Amylase CEA <5ng/ml <5ng/ ml > 200ng /ml variabel hoch niedrig Epithelien Histiozyten, Granulozyten Malignitätskriterien nein, amorphes gelblich pigmentiertes Material (31 %) ja, glykogenreich (nur in 20 25% nachweisbar) +++ hämosiderinbeladene Makrophagen (52%) ja, muzinös (PAS+) (Atypie) entfällt entfällt Nekrosen, zelluläre Atypien ja, muzinös (PAS+) (Atypie) (+) (+) nein Nekrosen, zelluläre Atypien ja, runde Kerne, schaumiges Zytoplasma, verzweigte Papillen, myxoides und fibrovaskuläres Stroma zelluläre Atypien
11 Übersicht 263 Abb.10 Endosonografische Differenzialdiagnose zystischer Pankreasläsionen. Abb.11 Evidenzbasierter Algorithmus für das Managment zystischer Pankreasraumforderungen (aus [130]). oder duodenalen Punktionsweg sowie seltene nonneoplastische Entitäten mit muzinösem Epithel müssen sowohl dem Kliniker als auch dem Zytopathologen bekannt sein. Die Synthese der Befunde unter Berücksichtigung weniger bedeutsamer klinischanamnestischer Daten (Alter, Geschlecht, Pankreatitisanamnese) und der Lokalisation sowie die kritische Wertung von Einzelbefunden ermöglichen eine deutliche Steigerung der diagnostischen Genauigkeit und ausreichend sichere therapeutische Entscheidungen (l" Abb. 11). Bei kleinen muzinösen Pankreaszysten ohne Alarmkriterien wird zunehmend ein konservatives Vorgehen favorisiert. Einer Liberalisierung der Leitlinienkriterien für eine operative Therapie von IPMN wird durch Untersuchungen unterstützt, die nicht nur bei Patienten mit einer Zystengröße >30 mm ohne Hauptgangerweiterung und ohne murale Noduli [51, 72, 73], sondern auch bei MD-IPMN mit muralen Noduli <10 mm ohne maligne Zytologie [74] die Sicherheit einer engmaschigen Überwachungsstrategie zeigen konnten. Zunehmend werden für Patienten mit hohem Operationsrisiko oder fehlendem Operationswunsch neue, nichtoperative Therapieansätze diskutiert. Das Konzept, mit der endosonografisch gestützten Äthanolablation eine minimalinvasive Therapiealternative zur Resektion kleiner prämaligner zystischer Pankreasläsionen zu etablieren, wird kontrovers diskutiert [127, 128]. Kürzlich publizierte Ergebnisse einer Pilotstudie weisen darauf hin, dass eine Chemoprävention mit dem nichtsteroidalen Antiphlogistikum Sulindac durch Hemmung der Glutathione-S-Transferase φ zur partiellen Rückbildung von muralen Noduli und Gangweite bei BD-IPMN führen kann [129]. Vor dem Hintergrund dieser Entwicklungen ist ein zunehmender Stellenwert der Endosonografie für die Überwachung von Patienten mit kleinen muzinösen Pankreaszysten, bei denen zugunsten eines konservativen Vorgehen entschieden wird, zu erwarten [131].
12 264 Übersicht Literatur 1 Kimura W, Nagai H, Kuroda A et al. Analysis of small cystic lesions of the pancreas. Int J Pancreatol 1995; 18: Lee KS, Sekhar A, Rofsky NM et al. Prevalence of incidental pancreatic cysts in the adult population on MR imaging. Am J Gastroenterol 2010; 105: Girometti R, Intini S, Brondani G et al. Incidental pancreatic cysts on 3D turbo spin echo magnetic resonance cholangiopancreatography: prevalence and relation with clinical and imaging features. Abdom Imaging 2010, published ahead of print 4 Edirimanne S, Connor SJ. Incidental pancreatic cystic lesions. World J Surg 2008; 32: Adsay NV. Cystic lesions of the pancreas. Mod Pathol 2007; 20: Basturk O, Coban I, Adsay NV. Pancreatic cysts: pathologic classification, differential diagnosis, and clinical implications. Arch Pathol Lab Med 2009; 133: Kosmahl M, Pauser U, Peters K et al. Cystic neoplasms of the pancreas and tumor-like lesions with cystic features: a review of 418 cases and a classification proposal. Virchows Arch 2004; 445: Tanaka M, Chari S, Adsay V et al. International consensus guidelines for management of intraductal papillary mucinous neoplasms and mucinous cystic neoplasms of the pancreas. Pancreatology 2006; 6: Dietrich CF, Jenssen C, Allescher HD et al. [Differential diagnosis of pancreatic lesions using endoscopic ultrasound]. Z Gastroenterol 2008; 46: Correa-Gallego C, Ferrone CR, Thayer SP et al. Incidental pancreatic cysts: do we really know what we are watching? Pancreatology 2010; 10: Buscaglia JM, Shin EJ, Giday SA et al. Awareness of guidelines and trends in the management of suspected pancreatic cystic neoplasms: survey results among general gastroenterologists and EUS specialists. Gastrointest Endosc 2009; 69: quiz 20 e Aghdassi A, Mayerle J, Kraft M et al. Diagnosis and treatment of pancreatic pseudocysts in chronic pancreatitis. Pancreas 2008; 36: Andren-Sandberg A, Dervenis C. Pancreatic pseudocysts in the 21 st century. Part II: natural history. JOP 2004; 5: Andren-Sandberg A, Dervenis C. Pancreatic pseudocysts in the 21 st century. Part I: classification, pathophysiology, anatomic considerations and treatment. JOP 2004; 5: Lerch MM, Stier A, Wahnschaffe U et al. Pancreatic pseudocysts: observation, endoscopic drainage, or resection? Dtsch Arztebl Int 2009; 106: Gonzalez Obeso E, Murphy E, Brugge W et al. Pseudocyst of the pancreas: the role of cytology and special stains for mucin. Cancer Cytopathol 2009; 117: Hammel PR, Vilgrain V, Terris B et al. Pancreatic involvement in von Hippel-Lindau disease. The Groupe Francophone d Etude de la Maladie de von Hippel-Lindau. Gastroenterology 2000; 119: Adsay NV, Hasteh F, Cheng JD et al. Squamous-lined cysts of the pancreas: lymphoepithelial cysts, dermoid cysts (teratomas), and accessory-splenic epidermoid cysts. Semin Diagn Pathol 2000; 17: Adsay NV, Hasteh F, Cheng JD et al. Lymphoepithelial cysts of the pancreas: a report of 12 cases and a review of the literature. Mod Pathol 2002; 15: Goh BK, Tan YM, Chung YF et al. Non-neoplastic cystic and cystic-like lesions of the pancreas: may mimic pancreatic cystic neoplasms. ANZ J Surg 2006; 76: Kosmahl M, Egawa N, Schroder S et al. Mucinous nonneoplastic cyst of the pancreas: a novel nonneoplastic cystic change? Mod Pathol 2002; 15: Dua KS, Vijayapal AS, Kengis J et al. Ciliated foregut cyst of the pancreas: preoperative diagnosis using endoscopic ultrasound guided fine needle aspiration cytology a case report with a review of the literature. Cytojournal 2009; 6: Woon CS, Pambuccian SE, Lai R et al. Ciliated foregut cyst of pancreas: cytologic findings on endoscopic ultrasound-guided fine-needle aspiration. Diagn Cytopathol 2007; 35: Adsay NV, Klimstra DS. Cystic forms of typically solid pancreatic tumors. Semin Diagn Pathol 2000; 17: Kosmahl M, Pauser U, Anlauf M et al. Pancreatic ductal adenocarcinomas with cystic features: neither rare nor uniform. Mod Pathol 2005; 18: Pauser U, Kosmahl M, Sipos B et al. [Mesenchymal tumors of the pancreas. Surprising, but not uncommon]. Pathologe 2005; 26: Dries AM, McDermott J. Diagnosis of cystic lymphangioma of the pancreas with endoscopic ultrasound-guided fine needle aspiration. Am J Gastroenterol 2008; 103: Zamboni G, Terris B, Scarpa A et al. Acinar cell cystadenoma of the pancreas: a new entity?. Am J Surg Pathol 2002; 26: Choi JY, Kim MJ, Lee JY et al. Typical and atypical manifestations of serous cystadenoma of the pancreas: imaging findings with pathologic correlation. AJR Am J Roentgenol 2009; 193: Lee SE, Kwon Y, Jang JY et al. The morphological classification of a serous cystic tumor (SCT) of the pancreas and evaluation of the preoperative diagnostic accuracy of computed tomography. Ann Surg Oncol 2008; 15: Bassi C, Salvia R, Molinari E et al. Management of 100 consecutive cases of pancreatic serous cystadenoma: wait for symptoms and see at imaging or vice versa? World J Surg 2003; 27: Galanis C, Zamani A, Cameron JL et al. Resected serous cystic neoplasms of the pancreas: a review of 158 patients with recommendations for treatment. J Gastrointest Surg 2007; 11: Tseng JF, Warshaw AL, Sahani DV et al. Serous cystadenoma of the pancreas: tumor growth rates and recommendations for treatment. Ann Surg 2005; 242: discussion Crippa S, Salvia R, Warshaw AL et al. Mucinous cystic neoplasm of the pancreas is not an aggressive entity: lessons from 163 resected patients. Ann Surg 2008; 247: Goh BK, Tan YM, Chung YF et al. A review of mucinous cystic neoplasms of the pancreas defined by ovarian-type stroma: clinicopathological features of 344 patients. World J Surg 2006; 30: Yamao K, Yanagisawa A, Takahashi K et al. Clinicopathological features and prognosis of mucinous cystic neoplasm with ovarian-type stroma: a multi-institutional study of the Japan Pancreas Society. Pancreas 2010, published ahead of print 37 Crippa S, Fernandez-Del Castillo C, Salvia R et al. Mucin-producing neoplasms of the pancreas: an analysis of distinguishing clinical and epidemiologic characteristics. Clin Gastroenterol Hepatol 2010; 8: Adsay NV, Merati K, Basturk O et al. Pathologically and biologically distinct types of epithelium in intraductal papillary mucinous neoplasms: delineation of an intestinal pathway of carcinogenesis in the pancreas. Am J Surg Pathol 2004; 28: Andrejevic-Blant S, Kosmahl M, Sipos B et al. Pancreatic intraductal papillary-mucinous neoplasms: a new and evolving entity. Virchows Arch 2007; 451: Belyaev O, Seelig MH, Muller CA et al. Intraductal papillary mucinous neoplasms of the pancreas. J Clin Gastroenterol 2008; 42: Pelletier AL, Hammel P, Rebours V et al. Acute pancreatitis in patients operated on for intraductal papillary mucinous neoplasms of the pancreas: frequency, severity, and clinicopathologic correlations. Pancreas 2010; 39: Ringold DA, Shroff P, Sikka SK et al. Pancreatitis is frequent among patients with side-branch intraductal papillary mucinous neoplasia diagnosed by EUS. Gastrointest Endosc 2009; 70: Salvia R, Fernandez-del Castillo C, Bassi C et al. Main-duct intraductal papillary mucinous neoplasms of the pancreas: clinical predictors of malignancy and long-term survival following resection. Ann Surg 2004; 239: discussion Salvia R, Crippa S, Falconi M et al. Branch-duct intraductal papillary mucinous neoplasms of the pancreas: to operate or not to operate? Gut 2007; 56: Rodriguez JR, Salvia R, Crippa S et al. Branch-duct intraductal papillary mucinous neoplasms: observations in 145 patients who underwent resection. Gastroenterology 2007; 13: quiz Salvia R, Partelli S, Crippa S et al. Intraductal papillary mucinous neoplasms of the pancreas with multifocal involvement of branch ducts. Am J Surg 2009; 198: Kang MJ, Jang JY, Kim SJ et al. Cyst growth rate predicts malignancy in patients with branch duct intraductal papillary mucinous neoplasms. Clin Gastroenterol Hepatol 2010, published ahead of print 48 Kanno A, Satoh K, Hirota M et al. Prediction of invasive carcinoma in branch type intraductal papillary mucinous neoplasms of the pancreas. J Gastroenterol 2010; 45: Ohno E, Hirooka Y, Itoh A et al. Intraductal papillary mucinous neoplasms of the pancreas: differentiation of malignant and benign tumors by endoscopic ultrasound findings of mural nodules. Ann Surg 2009; 249:
Zystische Pankreastumore und IPMN Systematik
 Systematik Zystische Pankreastumore (20% der Pankreastumore) Seröse Zystadenome 97% benigne (Seröse) Zystadenokarzinome selten Muzinöse cystische Neoplasien (Low-grade, borerline, High grade) 10-15% maligne
Systematik Zystische Pankreastumore (20% der Pankreastumore) Seröse Zystadenome 97% benigne (Seröse) Zystadenokarzinome selten Muzinöse cystische Neoplasien (Low-grade, borerline, High grade) 10-15% maligne
12. Gemeinsame Jahrestagung, September, Radebeul. Sächsische Radiologische Gesellschaft,
 12. Gemeinsame Jahrestagung, 09. 11. September, Radebeul Sächsische Radiologische Gesellschaft, Thüringische Gesellschaft für Radiologie und Nuklearmedizin Pankreas: Von der Morphe zur Funktion 1 Normales
12. Gemeinsame Jahrestagung, 09. 11. September, Radebeul Sächsische Radiologische Gesellschaft, Thüringische Gesellschaft für Radiologie und Nuklearmedizin Pankreas: Von der Morphe zur Funktion 1 Normales
Zystische Pankreasläsionen: Wann beobachten, wann resezieren?
 Zystische Pankreasläsionen: Wann beobachten, wann resezieren? Hana Algül II. Medizinische Klinik Klinikum rechts der Isar der Technischen Universität München München 17. Oktober 2015 Zystische Pankreasläsionen
Zystische Pankreasläsionen: Wann beobachten, wann resezieren? Hana Algül II. Medizinische Klinik Klinikum rechts der Isar der Technischen Universität München München 17. Oktober 2015 Zystische Pankreasläsionen
MRCP-rundum: IPMN u.a. (muzinöse) zystische Pankreasläsionen
 MRCP-rundum: IPMN u.a. (muzinöse) zystische Pankreasläsionen Kittner T, Klinik für Radiologie Krankenhaus Dresden-Friedrichstadt Städtisches Klinikum Akademisches Lehrkrankenhaus der TU Dresden nforderungen
MRCP-rundum: IPMN u.a. (muzinöse) zystische Pankreasläsionen Kittner T, Klinik für Radiologie Krankenhaus Dresden-Friedrichstadt Städtisches Klinikum Akademisches Lehrkrankenhaus der TU Dresden nforderungen
Das mikrozystische seröse Zystadenom des Pankreas
 298 Das mikrozystische seröse Zystadenom des Pankreas Serous Microcystic Cystadenoma of the Pancreas Autor Institut Schlüsselwörter l" seröses Zystadenom l" Pankreas l" mikrozystisches seröses Zystadenom
298 Das mikrozystische seröse Zystadenom des Pankreas Serous Microcystic Cystadenoma of the Pancreas Autor Institut Schlüsselwörter l" seröses Zystadenom l" Pankreas l" mikrozystisches seröses Zystadenom
Morphologische Varianten der IPMN. Die intraduktalen Neoplasien des Pankreas. Gangsystem ausgehen und durch übermäßige
 Chirurg 2012 DOI 10.1007/s00104-011-2182-9 Springer-Verlag 2012 H.J. Brambs M. Juchems Klinik für diagnostische und interventionelle Radiologie, Universitätsklinikum Ulm, Ulm Radiologische Diagnostik der
Chirurg 2012 DOI 10.1007/s00104-011-2182-9 Springer-Verlag 2012 H.J. Brambs M. Juchems Klinik für diagnostische und interventionelle Radiologie, Universitätsklinikum Ulm, Ulm Radiologische Diagnostik der
Diagnose und Management der fokalen benignen Leberläsion. Dirk Bareiss, Joachim Hohmann
 Diagnose und Management der fokalen benignen Leberläsion Dirk Bareiss, Joachim Hohmann Anamnese bei fokalen Leberläsionen Hat der Patient Symptome oder handelt es sich um einen Zufallsbefund? Patientencharakteristika:
Diagnose und Management der fokalen benignen Leberläsion Dirk Bareiss, Joachim Hohmann Anamnese bei fokalen Leberläsionen Hat der Patient Symptome oder handelt es sich um einen Zufallsbefund? Patientencharakteristika:
Diagnostisches Vorgehen bei Leberraumforderungen. H. Diepolder
 Diagnostisches Vorgehen bei Leberraumforderungen H. Diepolder Bei 20% aller Routinesonographien fällt eine Leberraumforderung auf Problem Problem Bei 20% aller Routinesonographien fällt eine Leberraumforderung
Diagnostisches Vorgehen bei Leberraumforderungen H. Diepolder Bei 20% aller Routinesonographien fällt eine Leberraumforderung auf Problem Problem Bei 20% aller Routinesonographien fällt eine Leberraumforderung
PANKREAS (( ( Sonographie Grundkurs DR. KLAUS DIRKS INTERDISZIPLINÄRES SONOZENTRUM REMS-MURR-KLINIKUM WINNENDEN
 PANKREAS Sonographie Grundkurs (( ( DR. KLAUS DIRKS INTERDISZIPLINÄRES SONOZENTRUM REMS-MURR-KLINIKUM WINNENDEN PANKREAS 1) Untersuchungstechnik 2) Normalbefunde / Varianten 3) Typische patholog. Befunde
PANKREAS Sonographie Grundkurs (( ( DR. KLAUS DIRKS INTERDISZIPLINÄRES SONOZENTRUM REMS-MURR-KLINIKUM WINNENDEN PANKREAS 1) Untersuchungstechnik 2) Normalbefunde / Varianten 3) Typische patholog. Befunde
Pankreas 2015 welche Bildgebung benötigt der Gastroenterologe? Prof. Dr. med. Stephan Hollerbach
 Pankreas 2015 welche Bildgebung benötigt der Gastroenterologe? Prof. Dr. med. Stephan Hollerbach Klinik für Gastroenterologie / Endoskopie / GI-Onkologie AKH Celle 11. Bremer MRT-Symposium, 3. Oktober
Pankreas 2015 welche Bildgebung benötigt der Gastroenterologe? Prof. Dr. med. Stephan Hollerbach Klinik für Gastroenterologie / Endoskopie / GI-Onkologie AKH Celle 11. Bremer MRT-Symposium, 3. Oktober
gastroenterologie
 Zystische Pankreastumoren: Klassifikation und malignes Potenzial Esposito I, Schlitter AM Klöppel G Journal für Gastroenterologische und Hepatologische Erkrankungen 2011; 9 (3), 30-36 Homepage: www.kup.at/
Zystische Pankreastumoren: Klassifikation und malignes Potenzial Esposito I, Schlitter AM Klöppel G Journal für Gastroenterologische und Hepatologische Erkrankungen 2011; 9 (3), 30-36 Homepage: www.kup.at/
Intraduktale papillär-muzinöse Neoplasie des Pankreas Aktueller Stand von Diagnostik, Therapie und Prognose
 ÜBERSICHTSARBEIT Intraduktale papillär-muzinöse Neoplasie des Pankreas Aktueller Stand von Diagnostik, Therapie und Prognose Robert Grützmann, Stefan Post, Hans Detlev Saeger, Marco Niedergethmann ZUSAMMENFASSUNG
ÜBERSICHTSARBEIT Intraduktale papillär-muzinöse Neoplasie des Pankreas Aktueller Stand von Diagnostik, Therapie und Prognose Robert Grützmann, Stefan Post, Hans Detlev Saeger, Marco Niedergethmann ZUSAMMENFASSUNG
Abklärung von Pankreaszysten
 Abklärung von Pankreaszysten Erstellt durch Rainer Schöfl & Andreas Maieron Innere Medizin 4, KH der Elisabethinen Linz Arbeitsgruppe Endoskopie Februar 2015 Dilemma - Pankreaszyste mehr Bildgebung produziert
Abklärung von Pankreaszysten Erstellt durch Rainer Schöfl & Andreas Maieron Innere Medizin 4, KH der Elisabethinen Linz Arbeitsgruppe Endoskopie Februar 2015 Dilemma - Pankreaszyste mehr Bildgebung produziert
3 ERGEBNISSE 19. Altersverteilung des gesamten Patientenkollektives Altersgruppen in Jahren
 3 ERGEBNISSE 9 3. ERGEBNISSE 3. Allgemeine Aussagen 3.. Alter 54 Patienten konnten in die Auswertung aufgenommen werden. Das mittlere Alter des gesamten Patientengutes lag zum Zeitpunkt der Diagnosestellung
3 ERGEBNISSE 9 3. ERGEBNISSE 3. Allgemeine Aussagen 3.. Alter 54 Patienten konnten in die Auswertung aufgenommen werden. Das mittlere Alter des gesamten Patientengutes lag zum Zeitpunkt der Diagnosestellung
Workshop Endosonographie
 Workshop Endosonographie Der interessante Fall Pankreaserkrankung Ch. Siebert Klinik für Innere Medizin Fallvorstellung/Rückschau 2/2003 S.G. 73 J. männl. peranale Blutabgänge/Gewichtsverlust Koloskopie:
Workshop Endosonographie Der interessante Fall Pankreaserkrankung Ch. Siebert Klinik für Innere Medizin Fallvorstellung/Rückschau 2/2003 S.G. 73 J. männl. peranale Blutabgänge/Gewichtsverlust Koloskopie:
Zufallsbefund zystischer Pankreastumor
 FORTBILDUNG_ÜBERSICHT Dr. med. Jan G. D Haese Klinik für Allgemeine, Viszeral-, Transplantations-, Gefäß- und Thoraxchirurgie am Klinikum der Universität München, Standort Großhadern Koautoren: Prof. Dr.
FORTBILDUNG_ÜBERSICHT Dr. med. Jan G. D Haese Klinik für Allgemeine, Viszeral-, Transplantations-, Gefäß- und Thoraxchirurgie am Klinikum der Universität München, Standort Großhadern Koautoren: Prof. Dr.
Die B3-Läsion. Veränderung mit unsicherem biologischen Potential. Prof. Dr. Michael Heine. Pathologisches Institut Bremerhaven
 Die B3-Läsion Veränderung mit unsicherem biologischen Potential Prof. Dr. Michael Heine Pathologisches Institut Bremerhaven Pathologisches Institut Bremerhaven im Mammographie-Screening seit 18.04. 2006
Die B3-Läsion Veränderung mit unsicherem biologischen Potential Prof. Dr. Michael Heine Pathologisches Institut Bremerhaven Pathologisches Institut Bremerhaven im Mammographie-Screening seit 18.04. 2006
Pankreas / Gallenwege Sonographie und EUS zum Staging
 Institut für Röntgendiagnostik KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Pankreas / Gallenwege Sonographie und EUS zum Staging Doris Schacherer 2 Vor- und Nachteile der Verfahren Sonographie + verfügbar
Institut für Röntgendiagnostik KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Pankreas / Gallenwege Sonographie und EUS zum Staging Doris Schacherer 2 Vor- und Nachteile der Verfahren Sonographie + verfügbar
5. Pankreastumoren und Pankreasläsionen
 5. Pankreastumoren und Pankreasläsionen Die meisten Tumoren des exokrinen Pankreas sind maligne, aber es existieren auch eine Reihen von benignen Pankreastumoren oder Tumoren mit ungewissem malignen Potential
5. Pankreastumoren und Pankreasläsionen Die meisten Tumoren des exokrinen Pankreas sind maligne, aber es existieren auch eine Reihen von benignen Pankreastumoren oder Tumoren mit ungewissem malignen Potential
Originaldokument gespeichert auf dem Publikationsserver der Philipps-Universität Marburg
 Originaldokument gespeichert auf dem Publikationsserver der Philipps-Universität Marburg http://archiv.ub.uni-marburg.de Dieses Werk bzw. Inhalt steht unter einer Creative Commons Namensnennung Keine kommerzielle
Originaldokument gespeichert auf dem Publikationsserver der Philipps-Universität Marburg http://archiv.ub.uni-marburg.de Dieses Werk bzw. Inhalt steht unter einer Creative Commons Namensnennung Keine kommerzielle
Radiologische Diagnostik von zystischen Pankreastumoren
 Universitätsklinikum Ulm Klinik für diagnostische und interventionelle Radiologie Ärztlicher Direktor: Prof. Dr. med. Hans - Jürgen Brambs Radiologische Diagnostik von zystischen Pankreastumoren Dissertation
Universitätsklinikum Ulm Klinik für diagnostische und interventionelle Radiologie Ärztlicher Direktor: Prof. Dr. med. Hans - Jürgen Brambs Radiologische Diagnostik von zystischen Pankreastumoren Dissertation
Maligner Polyp des Kolons/Rektums
 Wolfram Jochum Institut für Pathologie Kantonsspital St.Gallen wolfram.jochum@kssg.ch 1 2 1 Maligner Polyp Begriffsdefinitionen Maligner Polyp (= malignes Adenom): Adenom mit Übergang in ein invasives
Wolfram Jochum Institut für Pathologie Kantonsspital St.Gallen wolfram.jochum@kssg.ch 1 2 1 Maligner Polyp Begriffsdefinitionen Maligner Polyp (= malignes Adenom): Adenom mit Übergang in ein invasives
Die aktuelle S3-Leitlinie zur Diagnsotik, Therapie und Nachsorge des Ovarialkarzinoms. Diagnostik
 Die aktuelle S3-Leitlinie zur Diagnsotik, Therapie und Nachsorge des Ovarialkarzinoms Diagnostik Diagnostik: Zielsetzung und Fragestellungen Diagnostik (siehe Kapitel 3.3) Welche Symptome weisen auf ein
Die aktuelle S3-Leitlinie zur Diagnsotik, Therapie und Nachsorge des Ovarialkarzinoms Diagnostik Diagnostik: Zielsetzung und Fragestellungen Diagnostik (siehe Kapitel 3.3) Welche Symptome weisen auf ein
Fortschritte der radiologischen Diagnostik im abdomen
 Radiologisch-Internistische Schnittstellen in der Praxis Fortschritte der radiologischen Diagnostik im abdomen Gerhard Mostbeck Institut für diagn. und intervent. Radiologie, Wilhelminenspital and Röntgeninstitut,
Radiologisch-Internistische Schnittstellen in der Praxis Fortschritte der radiologischen Diagnostik im abdomen Gerhard Mostbeck Institut für diagn. und intervent. Radiologie, Wilhelminenspital and Röntgeninstitut,
INSTITUT FÜR ROENTGENDIAGNOSTIK. Pankreas/Gallenwege/Gallenblase. Computertomographie. M. Bachthaler
 INSTITUT FÜR ROENTGENDIAGNOSTIK Pankreas/Gallenwege/Gallenblase Computertomographie M. Bachthaler Ziele 2 Tumordetektion Differentialdiagnostik der Tumoren Abgrenzung Tumor vs. Entzündung Beurteilung der
INSTITUT FÜR ROENTGENDIAGNOSTIK Pankreas/Gallenwege/Gallenblase Computertomographie M. Bachthaler Ziele 2 Tumordetektion Differentialdiagnostik der Tumoren Abgrenzung Tumor vs. Entzündung Beurteilung der
Welcher Knoten muss weiter abgeklärt werden? Schilddrüsenknoten in der Praxis Fortbildung im Herbst, 8. Oktober 2016, Wels
 Welcher Knoten muss weiter abgeklärt werden? Schilddrüsenknoten in der Praxis Fortbildung im Herbst, 8. Oktober 2016, Wels Wolfgang Buchinger Institut für Schilddrüsendiagnostik und Nuklearmedizin Gleisdorf
Welcher Knoten muss weiter abgeklärt werden? Schilddrüsenknoten in der Praxis Fortbildung im Herbst, 8. Oktober 2016, Wels Wolfgang Buchinger Institut für Schilddrüsendiagnostik und Nuklearmedizin Gleisdorf
Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr
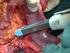 Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr Klinik für Allgemein-, Visceral- und Transplantationschirurgie Charité, Campus Virchow-Klinikum Universitätsmedizin
Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr Klinik für Allgemein-, Visceral- und Transplantationschirurgie Charité, Campus Virchow-Klinikum Universitätsmedizin
Neue Klassifikationssysteme in der Nierenpathologie
 Neue Klassifikationssysteme in der Nierenpathologie Kerstin Amann Abt. Nephropathologie Pathologisches Institut der Universität Erlangen-Nürnberg Krankenhausstr. 12 91054 Erlangen Histologische Klassifikationssysteme
Neue Klassifikationssysteme in der Nierenpathologie Kerstin Amann Abt. Nephropathologie Pathologisches Institut der Universität Erlangen-Nürnberg Krankenhausstr. 12 91054 Erlangen Histologische Klassifikationssysteme
Fokale Leberläsionen. Fall 1. Leberzyste. Fall 1 Diagnose? Leberzyste nativ. Fall jähriger Pat.
 Radiologische Diagnostik fokaler Leberläsionen Prof. Dr. Gerald Antoch Fokale Leberläsionen Bildgebende Verfahren Verschiedene Leberläsionen benigne maligne Fallbasierte Besprechung der bildgebenden Charakteristika
Radiologische Diagnostik fokaler Leberläsionen Prof. Dr. Gerald Antoch Fokale Leberläsionen Bildgebende Verfahren Verschiedene Leberläsionen benigne maligne Fallbasierte Besprechung der bildgebenden Charakteristika
Leitliniengerechte Abklärung vor einer Schilddrüsenoperation
 Leitliniengerechte Abklärung vor einer Schilddrüsenoperation Jointmeeting OGN & OSDG Standards in der Schilddrüsendiagnostik Zell 23.1.2015 Wolfgang Buchinger Institut für Schilddrüsendiagnostik und Nuklearmedizin,
Leitliniengerechte Abklärung vor einer Schilddrüsenoperation Jointmeeting OGN & OSDG Standards in der Schilddrüsendiagnostik Zell 23.1.2015 Wolfgang Buchinger Institut für Schilddrüsendiagnostik und Nuklearmedizin,
11. Radiologisch Internistisches Forum. Pankreas/Gallenwege: ERCP zur Diagnostik und zum Staging
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I 11. Radiologisch Internistisches Forum DIAGNOSE UND STAGING GASTROINTESTINALER TUMOREN WAS HAT SICH GEÄNDERT? Pankreas/Gallenwege: ERCP zur Diagnostik und zum
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I 11. Radiologisch Internistisches Forum DIAGNOSE UND STAGING GASTROINTESTINALER TUMOREN WAS HAT SICH GEÄNDERT? Pankreas/Gallenwege: ERCP zur Diagnostik und zum
1 EINLEITUNG Definition und Klassifikation neuroendokriner Tumoren des gastroenteropankreatischen Systems
 1 EINLEITUNG 6 1. EINLEITUNG 1.1 Definition und Klassifikation neuroendokriner Tumoren des gastroenteropankreatischen Systems Neuroendokrine Tumoren des Gastrointestinaltraktes stellen eine heterogene
1 EINLEITUNG 6 1. EINLEITUNG 1.1 Definition und Klassifikation neuroendokriner Tumoren des gastroenteropankreatischen Systems Neuroendokrine Tumoren des Gastrointestinaltraktes stellen eine heterogene
Klinikum Veterinärmedizin Klinik für Kleintiere - Chirurgie der Justus-Liebig-Universität Gießen. Bildgebung Prostata
 Klinikum Veterinärmedizin Klinik für Kleintiere - Chirurgie der Justus-Liebig-Universität Gießen Bildgebung Prostata Sebastian Schaub Res. ECVDI, FTA Klein- und Heimtiere Dr. K. Amort, Dr. N. Ondreka,
Klinikum Veterinärmedizin Klinik für Kleintiere - Chirurgie der Justus-Liebig-Universität Gießen Bildgebung Prostata Sebastian Schaub Res. ECVDI, FTA Klein- und Heimtiere Dr. K. Amort, Dr. N. Ondreka,
Der interessante Fall: Magen
 Klinik für Innere Medizin Der interessante Fall: Magen B. Schick Endosonographie Workshop 17./18. 09. 2004 Strausberg Fallvorstellung - 50jähriger Patient - rezidivierende peranale Blutungen seit 5 Jahren
Klinik für Innere Medizin Der interessante Fall: Magen B. Schick Endosonographie Workshop 17./18. 09. 2004 Strausberg Fallvorstellung - 50jähriger Patient - rezidivierende peranale Blutungen seit 5 Jahren
3.1 Ergebnisse des endoskopischen Screenings. Im Zeitraum von Mai 2000 bis August 2001 wurde bei insgesamt 148 Kopf-Hals-
 32 3. Ergebnisse 3.1 Ergebnisse des endoskopischen Screenings Im Zeitraum von Mai 2000 bis August 2001 wurde bei insgesamt 148 Kopf-Hals- Tumorpatienten eine einmalige Videoösophagoskopie mit routinemäßigen
32 3. Ergebnisse 3.1 Ergebnisse des endoskopischen Screenings Im Zeitraum von Mai 2000 bis August 2001 wurde bei insgesamt 148 Kopf-Hals- Tumorpatienten eine einmalige Videoösophagoskopie mit routinemäßigen
Pathologie des Ösophagus
 Pathologie des Ösophagus Cornelius Kuhnen Institut für Pathologie am Clemenshospital Münster Medical-Center Düesbergweg 128 48153 Münster www.patho-muenster.de Gastroösophageale Refluxkrankheit: Symptome
Pathologie des Ösophagus Cornelius Kuhnen Institut für Pathologie am Clemenshospital Münster Medical-Center Düesbergweg 128 48153 Münster www.patho-muenster.de Gastroösophageale Refluxkrankheit: Symptome
Gastroenterologe. Der. Elektronischer Sonderdruck für J. Werner. Resektion zystischer Pankreastumoren. Ein Service von Springer Medizin
 Der Gastroenterologe Zeitschrift für Gastroenterologie und Hepatologie Elektronischer Sonderdruck für J. Werner Ein Service von Springer Medizin Gastroenterologe 2014 9:31 37 DOI 10.1007/s11377-013-0821-z
Der Gastroenterologe Zeitschrift für Gastroenterologie und Hepatologie Elektronischer Sonderdruck für J. Werner Ein Service von Springer Medizin Gastroenterologe 2014 9:31 37 DOI 10.1007/s11377-013-0821-z
Früherkennung und Diagnostik
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Früherkennung und Diagnostik Früherkennung und Diagnostik Version 2005 2012: Albert / Blohmer / Junkermann / Maass / Scharl / Schreer
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Früherkennung und Diagnostik Früherkennung und Diagnostik Version 2005 2012: Albert / Blohmer / Junkermann / Maass / Scharl / Schreer
Darum liegt in mehr als der Hälfte der Fälle bereits bei Diagnosestellung ein fortgeschritteneres Stadium der Erkrankung vor.
 OVARIALKARZINOM EPIDEMIOLOGIE Das Ovarialkarzinom (Eierstockkrebs) stellt die häufigste Todesursache durch ein Malignom bei der Frau dar. In Österreich erkranken jährlich rund 936 Frauen an einem Eierstockkrebs.
OVARIALKARZINOM EPIDEMIOLOGIE Das Ovarialkarzinom (Eierstockkrebs) stellt die häufigste Todesursache durch ein Malignom bei der Frau dar. In Österreich erkranken jährlich rund 936 Frauen an einem Eierstockkrebs.
Magnetresonanz-Tomographie der Leber zugelassen
 Erste FDA-Zulassung für ein organspzifisches Kontrastmittel seit mehr als 10 Jahren Primovist in den USA für die Magnetresonanz-Tomographie der Leber zugelassen Berlin (8. Juli 2008) Die US-amerikanische
Erste FDA-Zulassung für ein organspzifisches Kontrastmittel seit mehr als 10 Jahren Primovist in den USA für die Magnetresonanz-Tomographie der Leber zugelassen Berlin (8. Juli 2008) Die US-amerikanische
Auf dem Boden einer Zirrhose oder einer chronischen Hepatitis B oder C Meist Entwicklung über Regeneratknoten und dysplastische Knoten
 Kurzdefinition " Epidemiologie Häufigster primärer maligner Tumor der Häufigkeit nimmt zu Erhöhte Inzidenz in Südostasien und Afrika Vorwiegend bei älteren Menschen (50 70 Jahre) Bei Männern 4-mal häufiger
Kurzdefinition " Epidemiologie Häufigster primärer maligner Tumor der Häufigkeit nimmt zu Erhöhte Inzidenz in Südostasien und Afrika Vorwiegend bei älteren Menschen (50 70 Jahre) Bei Männern 4-mal häufiger
Fall 2. Metachrones pleomorphes Adenom Parotis
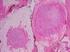 Fall 2 Metachrones pleomorphes Adenom Parotis Universitätsklinik für Hals-, Nasen- und Ohrenkrankheiten, Kopf- und Halschirurgie Schwerpunkttitel HNO 1 Anamnese 70-jährige Patientin mit progredienter,
Fall 2 Metachrones pleomorphes Adenom Parotis Universitätsklinik für Hals-, Nasen- und Ohrenkrankheiten, Kopf- und Halschirurgie Schwerpunkttitel HNO 1 Anamnese 70-jährige Patientin mit progredienter,
Konservative Therapie bei Kindern mit chronischer Pankreatitis. Heiko Witt Kinderklinik Schwabing & EKFZ, München
 Konservative Therapie bei Kindern mit chronischer Pankreatitis Heiko Witt Kinderklinik Schwabing & EKFZ, München Pankreatitis Therapie bei Kindern Pankreatitis Therapie Es gibt kaum prospektive, randomisierte
Konservative Therapie bei Kindern mit chronischer Pankreatitis Heiko Witt Kinderklinik Schwabing & EKFZ, München Pankreatitis Therapie bei Kindern Pankreatitis Therapie Es gibt kaum prospektive, randomisierte
Der pulmonale Rundherd. Hans-Stefan Hofmann Thoraxchirurgie Regensburg Universitätsklinikum Regensburg KH Barmherzige Brüder Regensburg
 Der pulmonale Rundherd Hans-Stefan Hofmann Thoraxchirurgie Regensburg Universitätsklinikum Regensburg KH Barmherzige Brüder Regensburg Definition rundliche Läsion Durchmesser: > 3 mm bis < 3 cm vollständig
Der pulmonale Rundherd Hans-Stefan Hofmann Thoraxchirurgie Regensburg Universitätsklinikum Regensburg KH Barmherzige Brüder Regensburg Definition rundliche Läsion Durchmesser: > 3 mm bis < 3 cm vollständig
Laparoskopische Pankreasresektion
 Rücksendung bitte an Chirurgische Klinik I Allgemein-, Thorax- und Gefäßchirurgie Chefarzt Prof. Dr. med. Marco Siech Ostalb-Klinikum Aalen 73430 Aalen Im Kälblesrain 1 Laparoskopische Pankreasresektion
Rücksendung bitte an Chirurgische Klinik I Allgemein-, Thorax- und Gefäßchirurgie Chefarzt Prof. Dr. med. Marco Siech Ostalb-Klinikum Aalen 73430 Aalen Im Kälblesrain 1 Laparoskopische Pankreasresektion
Innovative Diagnostik des Bronchialkarzinoms. Was leisten die neuen Methoden?
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN II Innovative Diagnostik des Bronchialkarzinoms. Was leisten die neuen Methoden? Christian Schulz Klinik und Poliklinik für Innere Medizin II Universität Regensburg
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN II Innovative Diagnostik des Bronchialkarzinoms. Was leisten die neuen Methoden? Christian Schulz Klinik und Poliklinik für Innere Medizin II Universität Regensburg
Tumor-Pathologie allgemeine
 Tumor-Pathologie allgemeine Systematisches Vorgehen bei der Diagnostik (1): Tumoren werden beurteilt anhand folgender Ebenen: - Gewebe-Ebene - Zell-Ebene - Klinisches Verhalten Systematisches Vorgehen
Tumor-Pathologie allgemeine Systematisches Vorgehen bei der Diagnostik (1): Tumoren werden beurteilt anhand folgender Ebenen: - Gewebe-Ebene - Zell-Ebene - Klinisches Verhalten Systematisches Vorgehen
Alternative Therapie infizierter Pankreaspseudozysten endoskopisch transmurale Nekrektomie/endoskopisches retroperitoneales Debridement
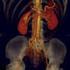 Alternative Therapie infizierter Pankreaspseudozysten endoskopisch transmurale Nekrektomie/endoskopisches retroperitoneales Debridement M. Hocke Interdisziplinäre re Endoskopie Klinik für f r Innere Medizin
Alternative Therapie infizierter Pankreaspseudozysten endoskopisch transmurale Nekrektomie/endoskopisches retroperitoneales Debridement M. Hocke Interdisziplinäre re Endoskopie Klinik für f r Innere Medizin
3 Ergebnisse 3.1 Charakterisierung der untersuchten Melanome
 3 Ergebnisse 3.1 Charakterisierung der untersuchten Melanome Untersucht wurden insgesamt 26 Melanome, die zwischen 1991 und 1997 in der Universitätsklinik und Poliklinik für Dermatologie und Venerologie
3 Ergebnisse 3.1 Charakterisierung der untersuchten Melanome Untersucht wurden insgesamt 26 Melanome, die zwischen 1991 und 1997 in der Universitätsklinik und Poliklinik für Dermatologie und Venerologie
Zytologie der Speicheldrüsen
 Zytologie der Speicheldrüsen 25. Tagung für klinische Zytologie 2017 Konstanz Dr. med. René Schönegg Institut für Pathologie Zytopathologie Häufigkeit der Neoplasien benigne pleom. Adenom: 60-70% Warthin-Tumor:
Zytologie der Speicheldrüsen 25. Tagung für klinische Zytologie 2017 Konstanz Dr. med. René Schönegg Institut für Pathologie Zytopathologie Häufigkeit der Neoplasien benigne pleom. Adenom: 60-70% Warthin-Tumor:
Pathologie Bochum Aktuelles zur Pathologie von Pankreastumoren (einschließlich NET)
 Pathologie Bochum Aktuelles zur Pathologie von Pankreastumoren (einschließlich NET) Andrea Tannapfel Institut für Pathologie Ruhr-Universität Bochum Andrea.Tannapfel@rub.de Neuroendokrine Tumoren (NET)
Pathologie Bochum Aktuelles zur Pathologie von Pankreastumoren (einschließlich NET) Andrea Tannapfel Institut für Pathologie Ruhr-Universität Bochum Andrea.Tannapfel@rub.de Neuroendokrine Tumoren (NET)
Notfall-ERCP Indikationen - Durchführung - Nachsorge
 Notfall-ERCP Indikationen - Durchführung - Nachsorge Frankfurt 02.05.2013 Jörg Bojunga Medizinische Klinik I Johann Wolfgang Goethe-Universität Frankfurt am Main Grundsätzliche Indikationen zur ERCP Diagnostisch
Notfall-ERCP Indikationen - Durchführung - Nachsorge Frankfurt 02.05.2013 Jörg Bojunga Medizinische Klinik I Johann Wolfgang Goethe-Universität Frankfurt am Main Grundsätzliche Indikationen zur ERCP Diagnostisch
Vorläuferläsionen FEA, LN, ADH
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Version 2009 1.0D Vorläuferläsionen FEA, LN, ADH Vorläuferläsionen LN, ADH Version 2005: Audretsch / Thomssen Version 2006-2008: Brunnert
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Version 2009 1.0D Vorläuferläsionen FEA, LN, ADH Vorläuferläsionen LN, ADH Version 2005: Audretsch / Thomssen Version 2006-2008: Brunnert
Malignitätshinweise bei der intraduktalen papillär muzinösen Neoplasie des Pankreas in der CT-Diagnostik
 Aus dem Institut für Diagnostische und Interventionelle Radiologie und Nuklearmedizin im St. Josef-Hospital Bochum - Universitätsklinik - der Ruhr-Universität Bochum Direktor: Prof. Dr. med. O. Köster
Aus dem Institut für Diagnostische und Interventionelle Radiologie und Nuklearmedizin im St. Josef-Hospital Bochum - Universitätsklinik - der Ruhr-Universität Bochum Direktor: Prof. Dr. med. O. Köster
Karzinoms. Die Unterscheidung des follikulären Karzinoms vom follikulären Adenom ist in der histologischen Untersuchung oft schwierig.
 1 Einleitung Die Erkrankungen der Schilddrüse erfordern im diagnostischen und therapeutischen Bereich eine interdiziplinäre Vorgehensweise. In Strumaendemiegebieten wie der Bundesrepublik Deutschland stellt
1 Einleitung Die Erkrankungen der Schilddrüse erfordern im diagnostischen und therapeutischen Bereich eine interdiziplinäre Vorgehensweise. In Strumaendemiegebieten wie der Bundesrepublik Deutschland stellt
Verbesserung des Tuberkulose-Screenings bei Patienten mit rheumatischen Erkrankungen vor Beginn einer Therapie mit TNFα-Blockern
 Rheumatologie / Klinische Immunologie Prof. Dr. H.P. Tony (Leiter des Schwerpunktes) Prof. Dr. med. Ch. Kneitz Medizinische Poliklinik Klinikstr. 6-8 97070 Würzburg Abstract: 1 / 10 Verbesserung des Tuberkulose-Screenings
Rheumatologie / Klinische Immunologie Prof. Dr. H.P. Tony (Leiter des Schwerpunktes) Prof. Dr. med. Ch. Kneitz Medizinische Poliklinik Klinikstr. 6-8 97070 Würzburg Abstract: 1 / 10 Verbesserung des Tuberkulose-Screenings
Berno Tanner. State of the Art Ovar 19.06.2009
 Pathologie und Konsequenzen für die Klinik Histologische Tumortypen Friedrich Kommoss Berno Tanner State of the Art Ovar 19.06.2009 Histologische Tumortypen benigne borderline maligne Histologische Tumortypen
Pathologie und Konsequenzen für die Klinik Histologische Tumortypen Friedrich Kommoss Berno Tanner State of the Art Ovar 19.06.2009 Histologische Tumortypen benigne borderline maligne Histologische Tumortypen
Lymphknotenzytologie t bei benignen Erkrankungen. Klinische Zytologie in der Pneumologie Grundlagenkurs Teil II Bernhard Opitz
 Lymphknotenzytologie t bei benignen Erkrankungen Klinische Zytologie in der Pneumologie Grundlagenkurs Teil II 31.05. Bernhard Opitz Lymphknotenzytologie tologie Simple Methode Wenig Traumatisch (fast)
Lymphknotenzytologie t bei benignen Erkrankungen Klinische Zytologie in der Pneumologie Grundlagenkurs Teil II 31.05. Bernhard Opitz Lymphknotenzytologie tologie Simple Methode Wenig Traumatisch (fast)
Pathologie des Ovars
 Pathologie des Ovars Cornelius Kuhnen Institut für Pathologie am Clemenshospital Münster Medical-Center Düesbergweg 128 48153 Münster www.patho-muenster.de Nichtneoplastische Zysten und tumorartige Läsionen
Pathologie des Ovars Cornelius Kuhnen Institut für Pathologie am Clemenshospital Münster Medical-Center Düesbergweg 128 48153 Münster www.patho-muenster.de Nichtneoplastische Zysten und tumorartige Läsionen
Dr. med. Ioannis Pilavas, Patientenuniversität Essen, 7. April Chronische Erkrankungen der Bauchspeicheldrüse Stent oder Operation?
 Dr. med. Ioannis Pilavas, Patientenuniversität Essen, 7. April 2015 Chronische Erkrankungen der Bauchspeicheldrüse Stent oder Operation? Häufigkeit der chronischen Pankreatitis (Bauchspeicheldrüsenentzündung)
Dr. med. Ioannis Pilavas, Patientenuniversität Essen, 7. April 2015 Chronische Erkrankungen der Bauchspeicheldrüse Stent oder Operation? Häufigkeit der chronischen Pankreatitis (Bauchspeicheldrüsenentzündung)
Diagnostik und Interventionen bei chronischer Pankreatitis: Chirurgische Therapie
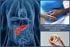 Diagnostik und Therapie bei chronischer Pankreatitis chirurgische Therapie Diagnostik und Interventionen bei chronischer Pankreatitis: Chirurgische Therapie Bruno Schmied Kantonsspital St. Gallen Diagnostik
Diagnostik und Therapie bei chronischer Pankreatitis chirurgische Therapie Diagnostik und Interventionen bei chronischer Pankreatitis: Chirurgische Therapie Bruno Schmied Kantonsspital St. Gallen Diagnostik
Kopf-Hals-Pathologie Teil II
 Kopf-Hals-Pathologie Teil II Kieferpathologie - neoplastisch PathoBasic 29.04.14 Daniel Baumhoer Pathologie Odontogenes Epithel mit reifem fibrösen Stroma Ameloblastom Plattenepithelialer odontogener Tumor
Kopf-Hals-Pathologie Teil II Kieferpathologie - neoplastisch PathoBasic 29.04.14 Daniel Baumhoer Pathologie Odontogenes Epithel mit reifem fibrösen Stroma Ameloblastom Plattenepithelialer odontogener Tumor
Allgemeine und spezielle klinische Untersuchung: Allgemeine Untersuchung: obb Orthopädische Untersuchung: Lahmheit Grad 1-2 vorne links Spezielle Unte
 Klinikum der Veterinärmedzin Klinik für Kleintiere Justus-Liebig-Universität Gießen Falldarstellung Gießener Kleintierabend 12. November 2008 M. Brückner Patient: Mischlingsrüde Rudi, 11 Jahre, mk Vorstellungsgrund:
Klinikum der Veterinärmedzin Klinik für Kleintiere Justus-Liebig-Universität Gießen Falldarstellung Gießener Kleintierabend 12. November 2008 M. Brückner Patient: Mischlingsrüde Rudi, 11 Jahre, mk Vorstellungsgrund:
Früherkennung und Diagnostik
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome in der DKG e.v Früherkennung und Diagnostik Früherkennung und Diagnostik Version 2005: Junkermann Version 2006-2009: Schreer / Albert
Diagnostik und Therapie primärer und metastasierter Mammakarzinome in der DKG e.v Früherkennung und Diagnostik Früherkennung und Diagnostik Version 2005: Junkermann Version 2006-2009: Schreer / Albert
Neuentwicklungen der Sonographie Möglichkeiten und Grenzen
 Neuentwicklungen der Sonographie Möglichkeiten und Grenzen Doris Schacherer GERÄTETECHNIK Gerätetechnik High-end Geräte Miniaturisierung von Ultraschallgeräten heute... 1964 Gerätetechnik Acuson P10 Taschenformatgerät
Neuentwicklungen der Sonographie Möglichkeiten und Grenzen Doris Schacherer GERÄTETECHNIK Gerätetechnik High-end Geräte Miniaturisierung von Ultraschallgeräten heute... 1964 Gerätetechnik Acuson P10 Taschenformatgerät
Ich habe einen Knoten in der Brust Wie weiter?
 EUSOMA akkreditiert Ich habe einen Knoten in der Brust Wie weiter? Dr. med. Claudia S. Hutzli Schaltegger Oberärztin Klinik für Gynäkologie UniversitätsSpital Zürich Dr. med. Franziska Zogg-Harnischberg
EUSOMA akkreditiert Ich habe einen Knoten in der Brust Wie weiter? Dr. med. Claudia S. Hutzli Schaltegger Oberärztin Klinik für Gynäkologie UniversitätsSpital Zürich Dr. med. Franziska Zogg-Harnischberg
Radiologische Veränderungen bei Pleuraerkrankungen
 Radiologische Veränderungen bei Pleuraerkrankungen Winfried Köpernik Radiologische Praxis am Krankenhaus St. Elisabeth und St. Barbara Themen Radiologische Verfahren Normalanatomie Pneumothorax Pleuraerguss,
Radiologische Veränderungen bei Pleuraerkrankungen Winfried Köpernik Radiologische Praxis am Krankenhaus St. Elisabeth und St. Barbara Themen Radiologische Verfahren Normalanatomie Pneumothorax Pleuraerguss,
EINLEITUNG 1.1 Allgemeine Einführung
 1 EINLEITUNG 1.1 Allgemeine Einführung Bei der vorliegenden Arbeit handelt es sich um eine retrospektive Studie an 141 Patienten mit zufällig diagnostiziertem Nebennierentumor. Es wurden mit Hilfe eines
1 EINLEITUNG 1.1 Allgemeine Einführung Bei der vorliegenden Arbeit handelt es sich um eine retrospektive Studie an 141 Patienten mit zufällig diagnostiziertem Nebennierentumor. Es wurden mit Hilfe eines
Tumoren der Schilddrüse
 456. Tutorial der Deutschen Abteilung der Internationalen Akademie für Pathologie e.v. Tumoren der Schilddrüse am 31. Oktober 2015 von Prof. Dr. med. Kurt Werner Schmid, Essen Tagungsort: Fortbildungszentrum
456. Tutorial der Deutschen Abteilung der Internationalen Akademie für Pathologie e.v. Tumoren der Schilddrüse am 31. Oktober 2015 von Prof. Dr. med. Kurt Werner Schmid, Essen Tagungsort: Fortbildungszentrum
abteilungsinterne Fortbildung ( )
 abteilungsinterne Fortbildung (12.06.2017) Gliederung/Themen 1) Lungenrundherde 2) BC-Screening / LungRads 3) BC / TNM 4) chronische Sinusitis 5) Gadolinium im ZNS 1) Lungenrundherde Rundherd (rund/oval)
abteilungsinterne Fortbildung (12.06.2017) Gliederung/Themen 1) Lungenrundherde 2) BC-Screening / LungRads 3) BC / TNM 4) chronische Sinusitis 5) Gadolinium im ZNS 1) Lungenrundherde Rundherd (rund/oval)
Dr. Edith Beck FA für Pathologie / ZF Zytologie
 Dr. Edith Beck FA für Pathologie / ZF Zytologie Ärztliche Leiterin Institut für Histologie Zytologie Bakteriologie Dr. Edith Beck Linz W a h l a r z t p r a x i s Hopfengasse 3 / 3 /2 A - 4020 L i n z
Dr. Edith Beck FA für Pathologie / ZF Zytologie Ärztliche Leiterin Institut für Histologie Zytologie Bakteriologie Dr. Edith Beck Linz W a h l a r z t p r a x i s Hopfengasse 3 / 3 /2 A - 4020 L i n z
Originalarbeit 43. Einleitung! Methoden! Ergebnisse des Video-Quiz!
 42 Schwierige endosonografische Differenzialdiagnosen am Pankreas chronische Pankreatitis Ergebnisse und Interpretation einer Interobserver-Variabilitätsuntersuchung Difficult Pancreatic Diagnoses in Endosonography
42 Schwierige endosonografische Differenzialdiagnosen am Pankreas chronische Pankreatitis Ergebnisse und Interpretation einer Interobserver-Variabilitätsuntersuchung Difficult Pancreatic Diagnoses in Endosonography
3 Eigene Untersuchungen
 3 Eigene Untersuchungen - 56-3.2.5.1.2 Zitzen Es werden 65 unveränderte, gesunde Zitzen sonographisch dargestellt. Diese stammen von 24 Hündinnen. Die Zitze stellt sich in allen Fällen als ein queroval
3 Eigene Untersuchungen - 56-3.2.5.1.2 Zitzen Es werden 65 unveränderte, gesunde Zitzen sonographisch dargestellt. Diese stammen von 24 Hündinnen. Die Zitze stellt sich in allen Fällen als ein queroval
Brustkrebs aktuell - OSP am Was ist eigentlich die Aufgabe des Pathologen in Diagnostik und Therapie des Mammakarzinoms?
 Brustkrebs aktuell - OSP am 21.10.2015 Was ist eigentlich die Aufgabe des Pathologen in Diagnostik und Therapie des Mammakarzinoms? Prof. Dr. German Ott, Institut für Pathologie Robert-Bosch-Krankenhaus
Brustkrebs aktuell - OSP am 21.10.2015 Was ist eigentlich die Aufgabe des Pathologen in Diagnostik und Therapie des Mammakarzinoms? Prof. Dr. German Ott, Institut für Pathologie Robert-Bosch-Krankenhaus
Nicht-epitheliale Tumore & Metastasen in der Schilddrüse
 Nicht-epitheliale Tumore & Metastasen in der Schilddrüse Prof. Dr.med.habil Andreas Zielke, MBA Klinik für Endokrine Chirurgie Endokrines Zentrum Diakonie Klinikum Stuttgart Fortbildungsveranstaltung OSP
Nicht-epitheliale Tumore & Metastasen in der Schilddrüse Prof. Dr.med.habil Andreas Zielke, MBA Klinik für Endokrine Chirurgie Endokrines Zentrum Diakonie Klinikum Stuttgart Fortbildungsveranstaltung OSP
Hat die Phlebographie in der Diagnose einer tiefen Venenthrombose noch einen Stellenwert?
 Hat die Phlebographie in der Diagnose einer tiefen Venenthrombose noch einen Stellenwert? 1.Ja 2.Nein 3.Weiss Nicht 4.Hab Angst Wieviele konventionelle Phlebographien, CT- Phlebographien oder MR- Phlebographien
Hat die Phlebographie in der Diagnose einer tiefen Venenthrombose noch einen Stellenwert? 1.Ja 2.Nein 3.Weiss Nicht 4.Hab Angst Wieviele konventionelle Phlebographien, CT- Phlebographien oder MR- Phlebographien
Voruntersuchungen. Klinik für Anästhesiologie und Intensivmedizin
 Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Diskrepante Befunde an der Cervix uteri bei wem liegt das Problem?
 Diskrepante Befunde an der Cervix uteri bei wem liegt das Problem? 25. Tagung für klinische Zytologie 23. März 2017 in Konstanz Katrin Marquardt, Schwerin Diskrepante Befunde Zytologie-Histologie 1. Falsch
Diskrepante Befunde an der Cervix uteri bei wem liegt das Problem? 25. Tagung für klinische Zytologie 23. März 2017 in Konstanz Katrin Marquardt, Schwerin Diskrepante Befunde Zytologie-Histologie 1. Falsch
Harnwegsinfekte nach Nierentransplantation Symposium 25 Jahre Transplantationszentrum Stuttgart
 Harnwegsinfekte nach Nierentransplantation Symposium 25 Jahre Transplantationszentrum Stuttgart Professor Dr. med. Andreas Kribben Klinik für Nephrologie Universitätsklinikum Essen 21. 5. 2011 Harnwegsinfektionen
Harnwegsinfekte nach Nierentransplantation Symposium 25 Jahre Transplantationszentrum Stuttgart Professor Dr. med. Andreas Kribben Klinik für Nephrologie Universitätsklinikum Essen 21. 5. 2011 Harnwegsinfektionen
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Onko Camp Gastroenterologie: November Speeding Update Pankreaskarzinom. F. Romeder
 Speeding Update Pankreaskarzinom F. Romeder 12.11.2016 Agenda Epidemiologie Diagnostik + Vorstufen kuratives Pankreaskarzinom Fortgeschrittenes/metastasiertes Pankreaskarzinom 1 Epidemiologie Siegel Ca
Speeding Update Pankreaskarzinom F. Romeder 12.11.2016 Agenda Epidemiologie Diagnostik + Vorstufen kuratives Pankreaskarzinom Fortgeschrittenes/metastasiertes Pankreaskarzinom 1 Epidemiologie Siegel Ca
Diagnostik des kalten Schilddrüsenknotens aus internistischer Sicht
 4. Endokrines Tumorsymposium 2009 Universitätsklinikum Düsseldorf Düsseldorf, 2. Dezember 2009 Diagnostik des kalten Schilddrüsenknotens aus internistischer Sicht Matthias Schott Klinik für Endokrinologie,
4. Endokrines Tumorsymposium 2009 Universitätsklinikum Düsseldorf Düsseldorf, 2. Dezember 2009 Diagnostik des kalten Schilddrüsenknotens aus internistischer Sicht Matthias Schott Klinik für Endokrinologie,
Gastro-Intestinalen-Stroma-Tumoren
 Erfassungsbogen zur Registrierung von Patienten mit Gastro-Intestinalen-Stroma-Tumoren in Österreich Zentrum: Patientennummer: 2 1 Stammdaten Geburtsdatum: Initialen (Vorname Nachname): - - - Geschlecht:
Erfassungsbogen zur Registrierung von Patienten mit Gastro-Intestinalen-Stroma-Tumoren in Österreich Zentrum: Patientennummer: 2 1 Stammdaten Geburtsdatum: Initialen (Vorname Nachname): - - - Geschlecht:
Neues aus Diagnostik und Therapie beim Lungenkrebs. Jürgen Wolf Centrum für Integrierte Onkologie Universitätsklinikum Köln
 Neues aus Diagnostik und Therapie beim Lungenkrebs Jürgen Wolf Centrum für Integrierte Onkologie Universitätsklinikum Köln Über was ich Ihnen heute berichten will: Lungenkrebs ist nicht gleich Lungenkrebs
Neues aus Diagnostik und Therapie beim Lungenkrebs Jürgen Wolf Centrum für Integrierte Onkologie Universitätsklinikum Köln Über was ich Ihnen heute berichten will: Lungenkrebs ist nicht gleich Lungenkrebs
MRT von Abdomen und Becken
 MRT von Abdomen und Becken Herausgegeben von Bernd Hamm Gabriel Paul Krestin Michael Laniado Volkmar Nicolas Matthias Taupitz Mit Beiträgen von P. Asbach D. Beyersdorff F. Dammann H.-B. Gehl B. Hamm C.
MRT von Abdomen und Becken Herausgegeben von Bernd Hamm Gabriel Paul Krestin Michael Laniado Volkmar Nicolas Matthias Taupitz Mit Beiträgen von P. Asbach D. Beyersdorff F. Dammann H.-B. Gehl B. Hamm C.
Nebenniere CT / MRT N. Zorger
 Institut für Röntgendiagnostik Nebenniere CT / MRT N. Zorger 2 Differentialdiagnose Allgemein Adenome Myelolipome Phaeochromozytome Karzinome Metastasen Nebennierenrindentumoren: Nebennierenmarktumoren:
Institut für Röntgendiagnostik Nebenniere CT / MRT N. Zorger 2 Differentialdiagnose Allgemein Adenome Myelolipome Phaeochromozytome Karzinome Metastasen Nebennierenrindentumoren: Nebennierenmarktumoren:
Plattenepithelkarzinom
 Hallesches Seminar Klinische Zytologie in der Pneumologie, Grundlagenkurs Teil II Plattenepithelkarzinom 31.Mai 01. Juni 2013, Halle KRANKENHAUS ST. ELISABETH & ST. BARBARA L. Welker Zytologisches Labor
Hallesches Seminar Klinische Zytologie in der Pneumologie, Grundlagenkurs Teil II Plattenepithelkarzinom 31.Mai 01. Juni 2013, Halle KRANKENHAUS ST. ELISABETH & ST. BARBARA L. Welker Zytologisches Labor
kontrolliert wurden. Es erfolgte zudem kein Ausschluss einer sekundären Genese der Eisenüberladung. Erhöhte Ferritinkonzentrationen wurden in dieser S
 5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN
 DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
12. Gemeinsame Jahrestagung, 09. 11. September, Radebeul. Sächsische Radiologische Gesellschaft,
 12. Gemeinsame Jahrestagung, 09. 11. September, Radebeul Sächsische Radiologische Gesellschaft, Thüringische Gesellschaft für Radiologie und Nuklearmedizin Leber: Von der Morphe zur (MR)-Funktion 1 Schlussfolgerungen
12. Gemeinsame Jahrestagung, 09. 11. September, Radebeul Sächsische Radiologische Gesellschaft, Thüringische Gesellschaft für Radiologie und Nuklearmedizin Leber: Von der Morphe zur (MR)-Funktion 1 Schlussfolgerungen
"In general, all solitary pulmonary nodules should be considered malignant until proven otherwise". Tan et al., Chest 123 (2003)
 "In general, all solitary pulmonary nodules should be considered malignant until proven otherwise". Tan et al., Chest 123 (2003) RELEVANZ Hohe Rate neu detektierter pulmonaler RH ca. 150.000 SRH / Jahr
"In general, all solitary pulmonary nodules should be considered malignant until proven otherwise". Tan et al., Chest 123 (2003) RELEVANZ Hohe Rate neu detektierter pulmonaler RH ca. 150.000 SRH / Jahr
MRT in der Gastroenterologie
 MRT in der Gastroenterologie MRT und bildgebende Differenzialdiagnose Bearbeitet von Henning Ernst Adamek, Thomas Lauenstein, Jörg Albert, Regina Beets-Tan, Jürgen Bunke, Siegbert Faiss, Lucas Greiner,
MRT in der Gastroenterologie MRT und bildgebende Differenzialdiagnose Bearbeitet von Henning Ernst Adamek, Thomas Lauenstein, Jörg Albert, Regina Beets-Tan, Jürgen Bunke, Siegbert Faiss, Lucas Greiner,
Sonographie und Endosonographie zum Staging von Ösophagus- und Magentumoren
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Sonographie und Endosonographie zum Staging von Ösophagus- und Magentumoren I. Zuber-Jerger Endosonographie zum Staging von Ösophagus- und Magenkarzinom EUS beste
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Sonographie und Endosonographie zum Staging von Ösophagus- und Magentumoren I. Zuber-Jerger Endosonographie zum Staging von Ösophagus- und Magenkarzinom EUS beste
Der Vergleich des Barrett-Spektrums im klinischen Bereich und den Arztpraxen
 Der Vergleich des Barrett-Spektrums im klinischen Bereich und den Arztpraxen ein Vortrag von Afag Aslanova > Präsentation > Bilder 54 Der Vergleich des Barrett-Spektrums im klinischen Bereich und den Arztpraxen
Der Vergleich des Barrett-Spektrums im klinischen Bereich und den Arztpraxen ein Vortrag von Afag Aslanova > Präsentation > Bilder 54 Der Vergleich des Barrett-Spektrums im klinischen Bereich und den Arztpraxen
Watchful waiting- Strategie
 Watchful waiting- Strategie Individualisierte Behandlung beim lokalisierten Prostatakarzinom- Welche Kriterien erlauben den Entscheid für eine watch und wait Strategie? Dr. Rudolf Morant, ärztlicher Leiter
Watchful waiting- Strategie Individualisierte Behandlung beim lokalisierten Prostatakarzinom- Welche Kriterien erlauben den Entscheid für eine watch und wait Strategie? Dr. Rudolf Morant, ärztlicher Leiter
