Leistungsverzeichnis. Institut für Virologie
|
|
|
- Mareke Grosse
- vor 8 Jahren
- Abrufe
Transkript
1 Leistungsverzeichnis Institut für Virologie Direktor: Univ.-Prof. Dr. Dr. h.c. Herbert Pfister UNIKLINIK KÖLN akkreditiert nach DIN EN ISO Nationales Referenzzentrum für Papillom- und Polyomaviren Version 4.1, August 2015
2 Herausgeber: Institut für Virologie Uniklinik Köln Prof. Dr. med. Ulrike Wieland Fürst-Pückler-Str Köln Layout: Thomas Müller Die jeweils aktuellste Version des Leistungsverzeichnisses finden Sie auf unserer Homepage unter Eine gedruckte Version des Leistungsverzeichnisses ist bei Herrn Thomas Müller anforderbar Tel ). 1
3 2
4 Inhaltsverzeichnis 1. Anschrift, Anfahrt und Lage 4 2. Öffnungszeiten, wichtige Telefonnummern, Notfalluntersuchungen 5 3. Ansprechpartner für die virologische Beratung 6 4. Handbuch für die Primärprobenentnahme 4.1 Hinweise zu Probenentnahme und Transport Leistungsanforderung Vorgehen bei V.a. Vogelgrippe Vorgehen bei V.a. eine Infektion mit hochinfektiösen Erregern Nationales Referenzzentrum für Papillom- und Polyomaviren Leistungsspektrum Einzeluntersuchungen (alphabetisch nach Erregernamen) 18 mit Angaben zu Testmethode, Untersuchungsmaterial, Probenmenge, Abnahme/Transport, Untersuchungsdauer, Indikation, Interpretation 7. Genotypisierung und Resistenztestung 7.1 HBV Hepatitis-B-Virus HCV Hepatitis-C-Virus HIV Humanes Immundefizienz-Virus Organbezogene klinische Symptomatik bei Virusinfektionen Auge 40 Bewegungsapparat, Muskulatur 41 Korpuskuläre Blutbestandteile, Blutbildung, Immunorgane 41 Gastrointestinaltrakt 42 Leber, Pankreas 42 Geschlechtsorgane 43 Haut und Schleimhaut 43 Herz und Gefäße 45 Mundhöhle, Rachen, Hals 45 Nase, Ohren 46 Niere, Harnwege, Nebenniere 46 Nervensystem 47 Respirationstrakt 48 Schwangerschaft HPV-Typen in klinischen Läsionen Literatur Meldepflicht ( 6-10 Infektionsschutzgesetz) Abkürzungsverzeichnis 58 3
5 1. Anschrift, Anfahrt und Lage Institut für Virologie, Uniklinik Köln Fürst-Pückler-Str. 56, Köln Straßenbahnhaltestellen: Linien 7 und 13 Haltestelle Wüllnerstr. Linien 1 und 7 Haltestelle Aachener Str./Gürtel Fahrplanauskunft: Aachener- Lindenthal Friedrich- Schmidt- Str. Kitsch- burger- Str. Lindenthal Fürst-Pückler-Str. H Str. H Aachener-Str./ Gürtel Zentrum Institut für Virologie A57 A1 Köln-Nord A3 Köln- Lövenich Aachener Str. Köln-Ost A4 Köln-West Dreieck-Heumar A4 A1 A555 Köln-Süd A59 4
6 2. Öffnungszeiten, Telefonnummern, Notfalluntersuchungen Öffnungszeiten: Montag Freitag 8:00 19:30 Samstag 8:00 16:00 Sonntag u. nachts (bis 2) Dienst-Handy für Notfallteste (s. u.) Wichtige Telefonnummern: Diagnostik-Sekretariat (Befundauskunft bis 16:15) 0221 / Karin Decker Anforderung von Transportröhrchen 0221 / , FAX 0221 / Diensthandy (bis 2, Mo-So) 0173 / Ansprechpartner für die virologische Beratung siehe Telefonnummern nächste Seiten Probentransport bei Notfällen (TAXI anfordern!!!) 0221 / Bitte fordern Sie bei Notfall-Untersuchungen immer ein TAXI an! Mit dem normalen Probentransport (Blutläufer) kann es mehrere Stunden dauern, bis die Probe unser Institut erreicht. Über das Diensthandy ist außerhalb der Öffnungszeiten bis 24 Uhr ein Wissenschaftlicher Mitarbeiter erreichbar, um in dringenden Fällen Notfalluntersuchungen für folgende Parameter durchzuführen: HIV-Antigen/Antikörper Suchtest HCV-Antikörper Suchtest Hepatitis B-Surface Antigen (HBs-Antigen) VZV-IgG Für Notfalluntersuchungen wenden Sie sich bitte an das Diagnostik-Sekretariat, nach 16:15 Uhr direkt an das Labor ( ) bzw. zwischen 19:00 und 24:00 Uhr an den diensthabenden wissenschaftlichen Mitarbeiter (Diensthandy 0173 / ). In dringenden Fällen versuchen wir jeden von uns angebotenen Parameter innerhalb der Öffnungszeiten sofort nach Eingang der Probe zu analysieren (bitte tel. Anmeldung). 5
7 3. Ansprechpartner für die virologische Beratung Über das Diagnostiksekretariat ( ) können Sie innerhalb der Dienstzeiten mit dem jeweils diensthabenden Wissenschaftlichen Mitarbeiter verbunden werden oder sich direkt an eine der unten genannten Personen wenden. Name Telefon Prof. Dr. Dr. h.c. Herbert Pfister 3900/3901 Institutsdirektor, Leiter des Nationalen Referenzzentrums für Papillom- und Polyomaviren Prof. Dr. med. Ulrike Wieland Oberärztin, Fachärztin für Mikrobiologie, Virologie und Infektionsepidemiologie 3910 Laborleitung Nationales Referenzzentrum für Papillom- und Polyomaviren Jun.-Prof. Dr. rer. nat. Baki Akgül 3911 Dipl. Biologe Dr. med. Sabine Awerkiew Fachärztin für Mikrobiologie, Virologie und Infektionsepidemiologie 3923 Funk 2050 Dr. med. Veronica Di Cristanziano Fachärztin für Mikrobiologie, Virologie und Infektionsepidemiologie 3927 (momentan in Elternzeit) 6
8 Name Telefon Dr. rer. nat. Rolf Kaiser Dipl. Biologe Bereichsleiter Molekularbiologie Ansprechpartner für HIV- und Hepatitis-Resistenztestung Dr. rer. nat. Elena Knops Dipl. Biologin Ansprechpartnerin für HIV- und Hepatitis-Resistenztestung Dr. rer. nat. Steffi Silling Dipl. Biologin 3928 Koordinatorin des Nationalen Referenzzentrums für Papillom- und Polyomaviren Linda Schroeder Assistenzärztin Dr. rer. nat. Gertrud Steger 3926 Dipl. Biologin Bitte wenden Sie sich bei Fragen, Unklarheiten, Beschwerden oder Problemen sofort an uns. Reklamationen können Sie an jeden der o.g. Ansprechpartner richten. 7
9 4. Handbuch für die Primärprobenentnahme 4.1. Hinweise zu Probenentnahme und Transport Während der Abnahme von Patientenproben müssen Einmalhandschuhe getragen werden. Besteht die Möglichkeit der Aerosolbildung/des Verspritzens bei der Probenabnahme, zusätzlich zu den Einmalhandschuhen Mundschutz und Schutzbrille tragen. Patientenproben müssen mit sterilem Abnahmebesteck entnommen und in sterilen Transportgefäßen befördert werden. Blutentnahmen sollten mit sicherem Blutentnahmebesteck (Sicherheits-Blutentnahmekanülen mit integrierter Kanülen- Schutzhülse; Sicherheitsflügel-Kanülen) erfolgen. Kanülen/Nadeln ohne integrierte Schutzmechanismen nach Probenabnahme niemals in die Schutzhülle zurückstecken (Verletzungsgefahr!), sondern direkt in den Sammelbehälter entsorgen. Das Abnahmebesteck (z.b. Kanülen, Skalpelle) muss sofort nach Abnahme in geeigneten Sammelgefäßen (z.b. Sharpsafe ) entsorgt werden, so dass sicher gestellt ist, dass andere Personen sich an dem Annahmebesteck nicht verletzten können. Die Sammelbehälter dürfen nicht überfüllt werden und dürfen nur geschlossen transportiert werden. Bitte bekleben Sie alle eingesandten Probengefäße (nicht die Hüllen oder Verpackungen) mit einem Proben- Etikett (siehe auch Leistungsanforderung) unseres Anforderungsformulars und beschriften Sie das Etikett (vor dem Abziehen vom Formular) mit dem Namen des Patienten. Ohne klinische Angaben ist eine sinnvolle Beurteilung der Testergebnisse oft nicht möglich. Bitte markieren Sie bei Z.n. aktueller Impfung, Nadelstichverletzungen, Immundefizienz, Bluttransfusion/ Immunglobulin- Gabe, etc. die entsprechenden Felder auf unserem Anforderungsformular. Fordern Sie bei Notfalluntersuchungen (siehe Abschnitt 2) unbedingt einen Sondertransport per TAXI an (Tel. 5492), da uns die Probe sonst eventuell (insbes. bei Abnahme am Nachmittag) nicht mehr am Tag der Abnahme erreicht. Der normale Uniklinik-Probentransport fährt unser Institut dreimal pro Tag an (gegen 11, 14 und 16 Uhr; Samstags nur einmal gegen 10 Uhr) und liefert dabei alle Proben an, die bis ca. 9:30/10:00 h, 13 h bzw. 15 h in der zentralen Probenannahme im Zentrallaboratorium (LFI-Gebäude) angelangt sind. Wir benötigen für die Virusdiagnostik folgende Materialien: (für weitere Angaben wie minimale Probenmenge siehe Kapitel "Leistungsspektrum") Serologische Untersuchungen 10 ml Blut ohne Zusatz in sterilem Röhrchen (braune Monovette). Neben Serum kann auch EDTA-Blut (rote Monovette) für serologische Untersuchungen eingesandt werden. Ggf. eine zweite Blutprobe im Abstand von 1-2 Wochen einsenden (Feststellung von Titer-Bewegungen). HIV-Testungen dürfen nur mit Einverständnis des Patienten durchgeführt werden. Influenzaviren- und RSV (Respiratory Syncytial Virus) Nachweis: Für den RSV-Antigennachweis wird Nasopharynx-Sekret benötigt (ideal > 0,5 ml). Am besten geeignet sind durch Absaugen (Katheter, Gummiball) oder Spülung (mit 2-3 ml physiologischer Kochsalzlösung) gewonnene Sekrete. Trachealsekret oder BAL können auch untersucht werden. Abstriche sind auch möglich, aber weniger gut geeignet (Tupfer mit Rayon- oder Dacron-Spitzen; keine Baumwoll-, keine Calciumalginat-Tupfer). Nach Abnahme wird der Tupfer in 'Transportmedium für die Virusisolierung (s.u.), gegeben und unverzüglich, idealer weise bei 2-8 C (auf Eis nicht einfrieren), eingesandt. Alle eingesandten Materialien sollten Epithelzellen enthalten und nach Abnahme so schnell wie möglich in das Labor gelangen. Mit Blut kontaminierte Materialien sind für RSV-Schnellteste nicht geeignet (falsch positive oder falsch negative Resultate möglich). Für den Nachweis von Influenza Viren haben sich Schnellteste wegen mangelnder Sensitivität nicht bewährt. Bitte fordern Sie zum Nachweis von Influenza Viren eine Influenza PCR-Untersuchung an. Sowohl 8
10 Influenzaviren, als auch RSV sind in unserem Untersuchungsblock "Respiratorischer Erregernachweis", welcher 10 Gruppen respiratorischer Viren umfasst (siehe Tabelle "Untersuchungsblöcke" im Kapitel "Leistungsanforderung"), enthalten, können aber auch als Einzeluntersuchung angefordert werden. PCR-Untersuchungen PCR-Untersuchungen sind aus zahlreichen Materialien möglich. Auf unserem Anforderungsformular (siehe unten) sind neben der Analyse die jeweils geeigneten Materialien in Klammern angegeben. Entsprechende Angaben finden Sie auch im Kapitel Leistungsspektrum bei den jeweiligen Erregern. HCV-RNA und HIV-1 RNA Bestimmungen Proben für den Nachweis von HCV-RNA, für die HCV-Typisierung (Serum oder EDTA-Blut) und für den quantitativen HIV-1 RNA Nachweis (EDTA-Blut; Heparinblut ist für PCR nicht geeignet!) müssen wegen der Instabilität der viralen RNA möglichst schnell nach Abnahme in unser Labor gelangen (Transportzeit max. 24 h). Bitte nehmen Sie bei gleichzeitiger Anforderung von HCV und HIV-1 RNA zwei separate Röhrchen ab. PCRs aus (Genital-)Abstrichen: Chlamydia trachomatis, HPV, HSV, VZV Chlamydia trachomatis, HPV-, HSV-, oder VZV-PCR-Untersuchungen können von Abstrichmaterialien nur durchgeführt werden, wenn diese in jeweils speziellen Abstrichröhrchen für Chlamydien- bzw. HPV-, HSV-, VZV-PCR abgenommen wurden. Das Transportmedium für Chlamydia trachomatis PCR (M4RT Transport Medium) ist nur für Chlamydia trachomatis PCR geeignet. Das Transportmedium für HPV-PCR ist auch für HSV- und VZV-PCR geeignet, jedoch nicht für Chlamydia trachomatis PCR (tel. Anforderung der Transportröhrchen unter ; Lagerung bei +2-8 C). Bei Abstrichen für die HPV-, HSV-, VZV oder Chlamydia trachomatis PCR muss der Tupfer nach der Probenabnahme unbedingt im Transportröhrchen verbleiben! Transportröhrchen, die keinen Tupfer enthalten, können nicht bearbeitet werden! Bitte nehmen Sie Abstriche für die Chlamydien-PCR mit den von uns versandten Tupfern mit Plastikstil ab (Swab Pack, Fa. Remel). Für Zervixabstriche benötigen Sie 2 Tupfer. Nur endozervikale Abstriche sind für die Chlamydien-PCR geeignet. Bei Männern bitte Urin einsenden (siehe unten). Abnahme von Zervixabstrichen für die Chlamydia trachomatis PCR: Zervixschleim mit dem ersten Tupfer entfernen und verwerfen. Den zweiten Tupfer in den endozervikalen Kanal einführen, bis die Tupferspitze nicht mehr sichtbar ist. Tupfer 3-5 Sekunden drehen (für die Abnahme von Zellen). Beim Zurückziehen des Tupfers Kontakt mit der Vaginalschleimhaut vermeiden! Tupfer in das Transportmedium (M4RT-Medium) geben und den Tupferstiel am Röhrchenrand abbrechen. Transportröhrchen fest verschließen und bei Raumtemperatur bzw C zum Labor transportieren lassen. Urin für die Chlamydia trachomatis PCR (Frauen und Männer) 2 Stunden vor Urinkollektion nicht urinieren und dann ml zu Beginn der Miktion in einem sauberen Polypropylen-Gefäß ohne Konservierungsmittel auffangen. Sammelgefäße, die Konservierungsmittel enthalten, dürfen NICHT benutzt werden. Die Probe muss innerhalb von 2 in das Labor gelangen (Transport bei Raumtemperatur bzw C). Biopsien für PCR-Untersuchungen Biopsien für PCR-Untersuchungen nativ (kein Einbett- oder Transportmedium) auf Trockeneis oder bei kurzem Transport auf Eis oder bei Raumtemperatur einsenden. Formalin-fixiertes paraffin-eingebettetes Gewebe ist ggf. auch geeignet. 9
11 Urin, Liquor, Kammerwasser, BAL, Tracheal- oder Nasopharynxsekret, Rachen-/Nasenspülung, Sputum, Punktate, Fruchtwasser, Stuhl für PCR-Untersuchungen nativ in sterilen Einmalgefäßen/Röhrchen versenden. Knochenmark kann in EDTA-Röhrchen transportiert werden. Für Liquor-Untersuchungen (viraler DNA/RNA-Nachweis mittels PCRs bzw. Liquor/Serum-Antikörper- Indizes) benötigen wir mindestens 750 ul, idealerweise 1 ml Liquor. Bei Kammerwasser benötigen wir mindestens ul. Für Stuhl-Untersuchungen senden Sie bitte eine erbsen- bis bohnengroße Menge ein (1-2 ml). Bei den übrigen o.g. Materialien senden Sie bitte 1 bis 10 ml ein. Virusisolierung Die Virusisolierung ist nur in Spezialfällen nach telefonischer Rücksprache möglich und in der Regel nur in den ersten (3) Krankheitstagen erfolgsversprechend. Soweit verfügbar, sind PCR-Untersuchungen vorzuziehen. Virusanzucht ist prinzipiell möglich für Adenoviren (Stuhl, Abstrich, resp. Sekrete, BAL, Urin), CMV (Urin), Enteroviren (Stuhl, Abstrich, Punktat, BAL, Liquor), HSV (Abstrich, Urin), Influenzaviren (Abstrich, BAL, TS, resp. Sekrete), VZV (Abstrich) Materialien für die Virusisolierung müssen so schnell wie möglich und nach Möglichkeit gekühlt (auf Eis - nicht einfrieren!) eingesandt werden. Proben möglichst frühzeitig abnehmen. Die Einsendung mehrerer aufeinanderfolgender Proben erhöht die Isolierungschance. Stuhl, Urin, Liquor, BAL, Punktat, Rachen- oder Trachelsekret nativ (ohne Zusätze) in sterilem Röhrchen/Transportgefäß einsenden. Für den Transport von Abstrichen (dürfen nicht austrocknen!) sind nur sterile Spezialröhrchen mit (rotem) Transportmedium für die Virusisolierung geeignet, die telefonisch bei uns bestellt werden können ( )(Lagerung bei +4 C für 4 Wochen oder bei -20 C für 12 Monate, vor Gebrauch auftauen). Für die Abstrichabnahme muss ein steriler Tupfer benutzt werden. Sofort danach wird der Tupfer in das Transportmedium überführt und der Tupferstiel am Röhrchenrand abgebrochen. Das Transportröhrchen, das nun den Tupfer in Transportmedium enthält, fest verschließen und sofort, wenn möglich gekühlt, einsenden. Für die Isolierung von Influenzaviren (Rachen- o. Nasenabstriche in den ersten drei Krankheitstagen) ist o.g. Transportmedium nicht geeignet. Ein Spezialtransportmedium für Influenzaviren ist notwendig (tel. Bestellung ). Materialien für die Influenzavirus-Isolierung sollten unbedingt gekühlt eingesandt werden (auf Eis - nicht einfrieren!) Bläscheninhalt kann mit einer Tuberkulinspritze, in die zuvor etwas physiologische Kochsalzlösung aufgezogen wurde, abgenommen werden und in der verschlossenen Spritze nach Abnahme der Kanüle eingesandt werden. 10
12 4.2. Leistungsanforderung Die Leistungsanforderung erfolgt durch unser maschinenlesbares Anforderungsformular (siehe Abbildung auf der übernächsten Seite). Die aktuelle Version unseres Anforderungsformulars ist in unserem Diagnostik-Sekretariat bestellbar (Kontaktdaten siehe Abschnitt 2). Falls Ihnen unser Anforderungsformular aktuell nicht vorliegt, können Sie in Ausnahmefällen eine Kopie von unserer Homepage herunterladen. Zur Markierung Ihrer Anforderungen auf unserem Formular kann ein Bleistift oder Kugelschreiber benutzt werden. Bitte waagrechte Striche, die das ganze Feld füllen anbringen (senkrechte Striche oder Kreuze werden von dem Belegleser u.u. nicht erkannt und die Parameter nicht bestimmt). Auf dem Formular bitte nicht radieren und das Formular nicht knicken! Einsender aus der Uniklinik Köln kleben bitte das Patienten-Etikett und das Stations-Etikett auf die entsprechenden Felder. Sollten bei Notfällen noch keine Patienten-Etiketten vorhanden sein, kann das entsprechende Feld auch handschriftlich ausgefüllt werden (unbedingt nötig: Name, Vorname, Geburtsdatum). Bitte keine beschädigten Etiketten benutzen. Externe Einsender füllen das Patienten- Etikett-Feld handschriftlich aus oder kleben ihre eigenen Patientenetiketten auf und geben dort zusätzlich die Einsenderadresse an. Bitte markieren Sie das entsprechende Feld (im oberen Drittel der Karte rechts), wenn ein Notfall vorliegt. Ihr Auftrag kann von dem Belegleser an die Labor-EDV nur vollständig weitergegeben werden, wenn auf dem Formular Materialart(en) (im Feld Eingesandte Materialien) und die gewünschte(n) Analyse(n) markiert sind! Nur wenn Sie Abnahmetag und Abnahmezeit markieren, können Verzögerungen beim Probentransport, die Einfluss auf die Untersuchungsergebnisse haben, erkannt werden (z.b. können Abbau viraler RNA oder Degradierung behüllter Viren bei zu langem Probentransport zu falsch negativen PCR- oder Virusisolierungs-Resultaten führen). Angaben zur Diagnose bzw. das Markieren von klinischen Angaben wie Nadelstichverletzung, Z.n. aktueller Impfung, Immundefizienz/-suppression, Dialyse, Gravidität, etc. erleichtern uns die Beurteilung der Testergebnisse. Wenn Sie das Feld Diagnostikprogramm markieren und eine Fragestellung angeben, erfolgt die Auswahl des Testprofils durch einen unserer Wissenschaftlichen Mitarbeiter entsprechend der Fragestellung (siehe auch: Tabellen zur organbezogenen klinischen Symptomatik bei Virusinfektionen). Probenetiketten Pro Formular können maximal sechs Probenröhrchen eingesandt werden (6 Proben-Barcode-Etiketten sind unten auf dem Formular angebracht). Für Liquor benutzen Sie bitte das Etikett mit dem grauen Randstreifen (untere Etiketten-Reihe rechts). Die restlichen fünf Etiketten (mit blauen Randstreifen) können für jedes Material (außer Liquor) benutzt werden. Beschriften Sie das Etikett vor dem Abziehen von dem Formular mit dem Patientennamen. Kleben Sie das Etikett längs auf das Probengefäß, so dass die Schmalseite des Etiketts parallel zum oberen Gefäßrand ist und die Auftragsnummer auf dem farbigen Etikettenrand lesbar ist. Die Barcodelinien müssen im rechten Winkel zur Röhrchen-Achse verlaufen (siehe Skizze unten links auf unserem Anforderungsformular). 11
13 Name Vorname Geb.-Datum Anschrift Patienten- Etikett Geschlecht Version: Institut für Virologie UNIKLINIK KÖLN Nationales Referenzzentrum für Papillom- und Polyomaviren Direktor: Prof. Dr. Dr. h. c. H. Pfister Fürst-Pückler-Str Köln Tel. (0221) Fax (0221) Dienst-Handy: (bis 2) Internet: 1 Kostenträger 2 3 Absender angeben! Einsender-Etikett Externe Einsender, bitte Adresse angeben! Ext. Einsenderadresse Tel.-Nr. f. Rückfragen: Fax-Nr.: Diagnose: Bemerkungen: Arzt / Ärztin (Name) / Funk-Nr. / Unterschrift Erstuntersuchung Folgeuntersuchung Therapiekontrolle Nadelstichverletzung Z. n. aktueller Impf. Immundefizienz/-suppr. Dialyse Prä-OP Prä-Tx Gravidität Bluttransf./Immunglob. 4 5 Bitte Untersuchungsmaterial 6 und Testanforderung so markieren: 7 8 nicht so 9 10 Montag Dienstag Mittwoch Donnerstag Freitag Samstag Sonntag Std Min. 13 stationär ambulant 14 Kasse privat Wissensch Bitte telefonische Anmeldung (Tel. s. o.) Notfall und Taxitransport (Tel ) 17 Eingesandte Materialien (zu Abnahme, Menge und Transport s. Rückseite) Serum (Se) EDTA-Blut (Ed) Heparin-Blut (He) Liquor (Li) Urin (Ur) Stuhl (St) Abstrich (Ab) von: BAL (Ba) Biopsie (Bi) von: Nasopharynxsekret (Np) Knochenmark (Km) Sputum (Sp) Sonstiges Feld bitte unbedingt ausfüllen! Fetalblut (Fe) Fruchtwasser (Fw) Kammerwasser (Kw) Punktat (Pu) Rachen/Nasenspül. (Ra) Trachealsekret (Ts) Diagnostikprogramm entsprechend der Fragestellung (Auswahl des Profils / Stufendiagnostik durch den Laborarzt) Antigennachweise Adenoviren (St) Astroviren (St) Rotavirus (St) CMV-pp65 (He, Ed, in separatem Röhrchen!) Schnellteste (Material siehe Rückseite) RSV Ag Hanta Puumala IgM (Se) CMV-Quantiferon (He) Virusanzucht (Zellkultur) Nur in Sonderfällen nach telefonischer Rücksprache Sonstiges Name Barcode-Etikett nur so auf die Monovetten kleben! Serologische Nachweise (Se) CMV IgM CMV IgG Dengue IgM/G/NS1 EBV-Screening (a-ebv-vca-igg/m + a-ebna1-igg) EBV VCA IgM EBV EA IgG Nur bei NPC: EBV VCA IgA FSME IgM FSME IgG Hantaviren-Screening (Puumala IgM Schnelltest, Hantaviren (5 Serotypen) IgG/IgM) Hantaviren IgM Hantaviren IgG HHV6-IgM a-hiv 1/2 a-hiv IB HSV IgM HSV IgG Sandfliegenfieber-Virus IgM Sandfliegenfieber-Virus IgG Name Name Name Virologie Name Name Name Virologie Influenza A IgA Influenza A IgG Influenza B IgA Influenza B IgG Masern IgM Masern IgG Mumps IgM Mumps IgG Parvov. B19 IgM Parvov. B19 IgG Röteln IgM Röteln IgG Toxoplasm. IgM Toxoplasm. IgG VZV IgM VZV IgG VZV-Reaktivierung (IgA + IgG) Für erregerspez. Liquor/ Serum- Antikörper-Indizes Einsendeschein Neurologische Labordiagnostik des Instituts für Klin. Chemie benutzen. Die Proben werden an uns weitergeleitet Hepatitis-Viren Virologie Virologie HAV IgM HAV IgG HBV-Screening (HBs-Ag, a-hbc) a-hbc a-hbc-igm HBs-Ag HBs-Ag quant. (Therapiekontrolle) a-hbs-titer HBe-Ag a-hbe HBV DNA quant. (Se, Ed) HBV Resistenz/ Genotyp. (Ed) a-hcv a-hcv IB HCV RNA quant. (Se, Ed) HCV Typisierung (Se, Ed) HCV Resistenz (Ed) HDV Gesamt-AK HDV RNA (Se, Ed) a-hev-igm a-hev-igg HEV RNA (St, Ed) Nukleinsäure-Nachw. (PCR) (Material) Separates Röhrchen! Adenov. (Ab, Ba, Bi, Ed, Km, Li, Np, Pu, Ra, St, Ts, Ur) BKV (Ed, Ur) Chlamydia trach. (Ab, Ur) CMV aus EDTA-Blut (quant.) CMV aus Urin CMV (Ab, Ba, Bi, Km, Kw, Li, Ts) EBV (Bi, Ed, Km, Li) Enteroviren (Li, Se, St, Pu) erfasste Typen s. Rückseite; Parechoviren s. unten HHV8 (KSHV) (Bi, Ed, Pu) HIV 1 RNA quant. (Ed, Li) HIV Resistenz RT/Protease (Ed) HIV Resistenz Integrase (Ed) HIV-1 Tropismus (Ed) HPV genital (Ab, Bi) HPV Haut (Bi) (Diagn. angeben) HSV (Ab, Bi, Ed, Kw, Li, Pu) Influenza A/B (Ab, Ba, Sp, Np) JCV (Li, Bi) Noroviren (St) MCPyV (Bi, Ab) Parechoviren (Ab, Ba, Ed, Li, Np, Se, Ts, St) Parvovirus B19 (Se, Fw, Bi, Km) Rötelnvirus (Se, Fw, Fe, Ur) VZV (Ab, Bi, Ed, Fw, Kw, Li, Pu) Virologie Liquor für Virologie Untersuchungsblöcke 23 Prä-OP Screening 24 (HBsAg, a-hbc, a-hcv, a-hiv) 25 Screening akute Hepatitis 26 (HAV+HEV IgM, HBs-Ag, a-hbc, a-hcv) 27 Nadelstichverletzung 28 ohne HBV-Impfung 29 (HBs-Ag, a-hbc, a-hcv, a-hiv) 30 Nadelstichverletzung 31 bei Z. n. HBV-Impfung 32 (a-hbs-titer, a-hcv, a-hiv) 33 Torch-Serologie 34 (Toxoplasmose IgM, Röteln IgM, 35 CMV IgM, HSV IgM) 36 Prae-Tx-Programm 37 Zwei (2!) Serumröhrchen einsenden! 38 (a-hbc, HBs-Ag, a-hcv, HCV-RNA, 39 a-hiv, HSV/VZV/CMV IgM/G, 40 EBV VCA IgM/G, EBNA1 IgG) 41 Post-Tx-Programm 42 1 Serum, 1 EDTA, 1 Urin! 43 (CMV IgM/G, CMV PCR [EDTA/Urin]) 44 Liquor-PCR auf 45 neurotrope Viren 46 (HSV, VZV, CMV, Entero) 47 Respirator. Erregernachweis 48 PCR aus Ab, Ba, Np, Pu, Ra, Sp, Ts (Influenza A/B, Parainfluenza, RSV, hmpv, Adeno-, Boca-, Corona-, Rhino/Enteroviren) Kardiotrope Viren 49 (Serum: Adeno-DNA, EBV-VCA IgG/M, 50 EBV-EBNA1 IgG, Entero-RNA, Influenza A/B IgA/G, Mumps IgM, Parvovirus B19 IgM/DNA, Röteln-IgM) Virale Durchfall-Erreger 51 (Adeno-, Astro-, Noro-, Rotaviren aus Stuhl) Wenn Sie einen der Untersuchungsblöcke (letzte Spalte) markieren, werden alle bei dem Untersuchungsblock aufgeführten Analysen durchgeführt: 12
14 Untersuchungsblock Prä-OP Screening Screening akute Hepatitis Nadelstichverletzung ohne HBV-Impfung Nadelstichverletzung bei Z.n. HBV-Impfung TORCH-Serologie Prä-Tx-Programm Bitte unbedingt zwei (2!) Serumröhrchen einsenden! Post-Tx-Programm Bitte 1 Serum-, 1 EDTA-, und 1 Urin- Röhrchen einsenden! Liquor-PCR auf neurotrope Viren Respiratorischer Erregernachweis aus Abstrich, BAL, Trachealsekret, Nasopharynxsekret, Rachen-/Nasen- Spülung, Sputum, Punktat (Abstrich in 1 ml Transportmedium für die Virusisolierung oder in 1 ml steriler Kochsalzlösung) Kardiotrope Viren Bitte 2 Serumröhrchen einsenden! Virale Durchfall-Erreger Analysen Hbs-Antigen, a-hbc, a-hcv, a-hiv HAV-IgM, HEV-IgM, Hbs-Antigen, a-hbc, a-hcv HBs-Antigen, a-hbc, a-hcv, a-hiv a-hbs-titer, a-hcv, a-hiv Toxoplasmose-, Röteln-, CMV-, HSV-IgM a-hbc, HBs-Antigen, a-hcv, HCV-RNA, a-hiv, HSV/VZV/CMV-IgM und IgG, EBV-VCA-IgM und -IgG, EBV-EBNA1-IgG CMV-IgM, -IgG, CMV-PCR aus EDTA-Blut und Urin HSV-, VZV-, CMV-, EBV-, Enteroviren-PCR Multiplex-PCR zum Nachweis folgender Viren: Influenza A/B, Parainfluenza, RSV, Metapneumo-, Adeno-, Boca-, Corona-, Rhino-/Enteroviren Adenoviren-DNA, EBV-VCA IgG/IgM, EBV-EBNA1-IgG, Enteroviren-RNA, Influenza A/B-IgA/IgG, Mumps-IgM, Parvovirus B19 IgM/DNA, Rötelnvirus-IgM Adeno-, Astro-, Noro-, Rotaviren im Stuhl Liquor/Serum IgG-Quotienten (Antikörper-Indizes) Wir bieten die Bestimmung von Liquor/Serum IgG-Quotienten für Masernvirus, Rötelnvirus, Varizella-Zoster- Virus, Mumpsvirus, Cytomegalie-Virus und Herpes simplex Virus an. Der Test dient dem Nachweis einer intrathekalen Antikörper-Synthese gegen die jeweiligen Viren. Diese ist frühestens 10 Tage nach Infektion nachweisbar, und somit nicht zur Akutdiagnostik geeignet. Für den Test wird ein am gleichen Tag entnommenes Probenpaar aus Serum und Liquor benötigt. Für die Anforderung von Antikörper-Indizes aus Liquor und Serum (relativer Liquor/Serum IgG-Quotienten) benutzen Sie bitte NICHT unser übliches Anforderungsformular, sondern das unten (siehe nächste Seite) gezeigte Anforderungsformular Neurologische Labordiagnostik des Instituts für Klinischen Chemie (Zentrallabor, Tel ). Liquor und Serum werden vom Institut für Klinische Chemie nach Ermittlung von Gesamt-IgG-/ und Albuminwerten an uns weitergeleitet. Wissenschaftliche Studien Vor Anforderung von virologischen Untersuchungen im Rahmen wissenschaftlicher Studien ist eine Rücksprache mit dem Institutsdirektor erforderlich (Tel ). Nachforderung von Untersuchungen Sofern genug Material eingesandt wurde, lagern wir nach der Durchführung der angeforderten Teste verbleibendes Probenmaterial für circa 1 Jahr bei 20 C (serologische Untersuchungen) oder 80 C 13
15 (Nukleinsäurenachweise). In diesem Zeitraum können ggf. zusätzliche Untersuchungen nachgefordert werden (Tel ) Wiederholungsuntersuchungen aufgrund analytischer Fehler werden kostenlos für die Einsender durchgeführt. Anforderungsformular Neurologische Labordiagnostik des Instituts für Klinische Chemie (siehe Abschnitt Liquor/Serum IgG-Quotienten): 14
16 4.3. Vorgehen bei V.a. Vogelgrippe (Aviäre Influenza, z.b. Influenza A H5N1) Der Verdacht auf Vogelgrippe beim Menschen besteht bei direktem Kontakt mit erkrankten/verstorbenen Tieren oder mit einem bestätigten menschlichen Erkrankungsfall oder mit einem menschlichen Verdachtsfall und akutem Krankheitsbeginn innerhalb von 7 Tagen nach dem Kontakt mit Fieber >38 C und Husten oder Dyspnoe. Bei Vorliegen eines Verdachtsfalls sollte umgehend ein labordiagnostischer Erregernachweis (PCR) angestrebt werden. Differentialdiagnostisch sollte immer eine Untersuchung auf aviäre und humane Influenzaviren erfolgen. Bei Nachweis von hochpathogenen aviären Influenzaviren wird empfohlen, den Patienten mit Neuraminidasehemmern, ggf. in erhöhter Dosierung (Oseltamivir/Tamiflu 2x150mg/d) zu behandeln. Personen, mit denen der Patient Kontakt hatte, sollen prophylaktisch mit Oseltamivir behandelt werden (75mg/d bis 5d nach Ende der letzten Exposition). Es muss eine Meldung an das zuständige Gesundheitsamt und eine Übermittlung an das Robert Koch-Institut erfolgen. Untersucht werden können Nasopharynxabstriche, Trachealsekret, und Bronchiallavage (BAL). Rachenabstriche, Nasopharynxsekret und Sputum sind weniger gut geeignet. Gelabstriche können NICHT untersucht werden. Die Probengewinnung sollte von geschultem Personal unter strikter Einhaltung der zu beachtenden hygienischen Aspekte (Atemschutzmaske, Schutzkittel, Einmalhandschuhe) erfolgen. Bei Probenentnahme mit möglicher Aerosolbildung (Trachealsekret, BAL) müssen eine eng anliegende FFP3- Atemschutzmaske und eine Schutzbrille getragen werden. Abstriche sollten idealer weise in speziellen Transportröhrchen für die Virusisolierung (rote Flüssigkeit) transportiert werden, die bei uns erhältlich sind (Tel. 3903). Falls diese Röhrchen nicht vorliegen, ist der Transport in physiologischer Kochsalzlösung (> 0,5 ml < 1 ml) möglich. Die PCR-Analyse nimmt etwa 4 Stunden in Anspruch. Wir bieten diesen Test während der normalen Dienstzeiten an. Um eine zügige Bearbeitung zu garantieren, bitten wir um telefonische Benachrichtigung und um Markierung der Einsendung als Notfall. Wir untersuchen nur Material von Menschen. Einsender von Untersuchungsmaterial von Tieren können sich an das Chemische und Veterinäruntersuchungsamt Rhein-Ruhr-Wupper wenden (Alte Gladbacher Str. 2-4, Krefeld, Tel ). Für aktuelle Informationen zu Influenzaviren siehe: und dort unter Infektionsschutz > RKI- Ratgeber für Ärzte > Influenza. 15
17 4.4. Vorgehen bei V.a. eine Infektion mit hochinfektiösen Erregern (Klasse IV-Erreger) Proben mit V.a. Klasse IV-Erreger werden an unserem Institut nicht untersucht und können nicht angenommen werden, da Klasse IV Erreger (Erreger von viralem hämorrhagischem Fieber, s.u.) nur in Instituten mit S4-Laboratorien untersucht werden dürfen. Bei entsprechendem klinischem Verdacht bitten wir unsere Einsender, direkt Kontakt mit u.g. S4-Einrichtungen aufzunehmen, die Probe anzukündigen und die Modalitäten des Transports zu besprechen. Institut für Virologie, Philipps-Universität Marburg Prof. Dr. S. Becker Hans-Meerwein-Str. 2, Marburg Tel.: (2), / 54 (Sekretariat), (Dr. Markus Eickmann, Leitung BSL-4 Labor), Fax Der Probentransport wird vom Institut für Virologie der Universität Marburg organisiert. Bernhard-Nocht-Institut für Tropenmedizin Bernhard-Nocht-Str. 74, Hamburg Tel (2 bei Verdacht auf virales hämorrhagisches Fieber) Liste der humanpathogenen viralen Klasse IV Erreger gemäß GenTR/BioMedR/ TRBA 462 Ebolavirus (hämorrhagisches Fieber) Guanaritovirus (Venezuelanisches hämorrhagisches Fieber) Hendravirus (Zoonose, Fledermäuse, Pferd; Resp.Trakt, Meningitis/Enzephalitis) Juninvirus (Argentinisches hämorrhagisches Fieber) Krim-Kongo-Fieber Virus (hämorrhagisches Fieber) Lassavirus (hämorrhagisches Fieber) Lujovirus (hämorrhagisches Fieber) Machupovirus (Bolivianisches hämorrhagisches Fieber) Marburgvirus (hämorrhagisches Fieber) Morbillivirus des Pferdes (Paramyxo-ähnliche Pferdeviren) Nipahvirus (Zoonose, Fledermäuse, Schweine; Resp. Trakt, Enzephalitis) Pockenviren (Variola-Major- und Variola-Minor-Virus) Sabiavirus (Brasilianisches hämorrhagisches Fieber) 16
18 5. Nationales Referenzzentrum für Papillom- und Polyomaviren Leitung: Univ. Prof. Dr. Herbert Pfister Laborleitung: Prof. Dr. med. Ulrike Wieland ( ) Koordination: Dr. Steffi Silling ( ) Leistungsangebot des NRZ: Beratung von Fachpersonal zu Fragen der Diagnostik, der Prophylaxe und der Therapie von Humanen Papillomvirus (HPV)- und Polyomavirus (PyV)-assoziierten Erkrankungen Beratung von Laboratorien bei der Diagnostik von Papillom- und Polyomavirus-Infektionen Typisierungen von HPV in diagnostischen Sonderfällen nach vorheriger Absprache Isolierung und Sequenzierung neuer HPV-Typen sowie Abgabe der Plasmide auf Anfrage Nachweis von BKPyV, JCPyV, MCPyV und weiterer humaner Polyomaviren in diagnostischen Sonderfällen nach vorheriger Absprache Führen einer Sammlung diagnostischer Referenzmaterialien für HPV und humane Polyomaviren sowie Abgabe auf Anfrage Durchführung von Fortbildungsveranstaltungen für Ärzte und Ärztinnen sowie Mitarbeiter/innen des öffentlichen Gesundheitsdienstes Evaluation von kommerziellen, diagnostischen Testsystemen für HPV und Polyomaviren Unterstützung von nationalen und internationalen Ringversuchen zu HPV und Polyomaviren. Hinweise zum Materialversand an das NRZ: Geeignete Materialien für die HPV- und Polyomavirus-DNA-Diagnostik sind Abstriche und Biopsien. Auch aus Paraffin-eingebettetem Gewebe kann virale DNA extrahiert werden. Abstriche für den DNA-Nachweis können in phosphat-gepufferter Kochsalzlösung (PBS) oder in Transportmedium für die Zytologie (z.b. PreservCyt, SurePath) versandt werden. Der Transport von Abstrichen und nativen Biopsien kann sofern nur DNA nachgewiesen werden soll - bei Raumtemperatur oder 4 C erfolgen. Biopsien können auch eingefroren (Trockeneis) versendet werden. Informationen zu Analen Dysplasien und Analkarzinom bei HIV- Infizierten finden Sie hier: 01.pdf Informationen zur HPV Impfung, herausgegeben von dem HPV Management Forum, finden Sie unter folgendem Link: Das NRZ für Papillom- und Polyomaviren ist Mitglied im Netzwerk für sexuell oder durch Blut übertragene Infektionen: 17
19 6. Leistungsspektrum Adenoviren (AV) Astroviren BK-Virus (BKV) Bocavirus Chlamydia trachomatis Cytomegalievirus (CMV) Coronaviren Dengue-Viren Epstein-Barr-Virus (EBV) Enteroviren Frühsommer-Meningoencephalitis (FSME) Virus Hantaviren Hepatitis-A-Virus (HAV) Hepatitis-B-Virus (HBV) Hepatitis-C-Virus (HCV) Hepatitis-D-Virus (HDV) Hepatitis-E-Virus (HEV) Herpes-simplex-Viren (HSV) Humanes Herpesvirus 6 (HHV-6) Humanes Herpesvirus 8 (HHV-8) Humanes Immundefizienz-Virus (HIV) Humane Papillomviren (HPV) Influenza-A-Viren Influenza-B-Viren Influenza A/B-Viren JC Virus (JCV) Masernvirus Merkelzell-Polyomavirus (MCPyV) Metapneumovirus (hmpv) Mumpsvirus Noroviren Parainfluenzaviren Parechoviren Parvovirus B Rhinoviren Rötelnvirus Rotaviren Respiratory-Syncytial-Virus (RSV) Sandfliegen-Fieber-Virus (SFV) Toxoplasma gondii Varizella-Zoster-Virus (VZV) Verschiedene Viren (Virusanzucht)
20 Einzeluntersuchungen alphabetisch nach Erregernamen mit Angaben zu Testmethode, Untersuchungsmaterial, Probenmenge, Abnahme/Transport, Untersuchungsdauer, Indikation, Interpretation Parameter Methode Material Probenmenge optimal (minimal) Besonderheiten bei Abnahme/ Transport Ergebnis/ Dimension Testfreq./ minimale Untersuchungsdauer Anmerkungen Adenoviren (AV) AG IC Stuhl 0,1 g erbsengr. DNA PCR Stuhl, Liquor, TS, BAL, Urin, Abstrich Nasen-/Rachensekret EDTA-Blut, Knochenmark DNA Multiplex -PCR Abstrich, BAL, TS, Nasopharynxsekret, Rachen/ Nasen- Spülung, Punktat, Sputum, erbsengr. 2 5 ml (750 ul; Blutproben: 1 ml) 1 2 ml (1 ml) Abstrich in 1-2 ml TM für die Virusisolierung Probe sollte 2 nach Abnahme im Labor sein. Probe sollte 2 nach Abnahme im Labor sein. Abstrich in TM für die Virus-isolierung oder in NaCl 0,9% (1 ml) pos/ neg Serum/ EDTA-Blut: Kopien/ml 0,5 h 4h bei V.a. virale GE V.a. Adenovirusinfektion (AV); virale Konjunktivitis, RT-Infekt., hämorrhag. Zystitis; Bei Immunsuppr. system. Infektionen möglich; Bei V.a. AV bei KM-TPL auch PCR aus EDTA-Blut: Intermediäres bzw. hohes Morbiditäts-Risiko ab 1000 bzw Kopien/ml. akute Infektion des RT; im Untersuchungsblock Respirator. Erregernachweis enthalten; auch als Einzeltest (siehe oben) anforderbar. Astroviren AG EIA Stuhl 0,1 g erbsengr Mo-Fr/ bei V.a. virale GE; 2.-häufigste Erreger der viralen infantilen GE BK-Virus (BKV) DNA PCR Urin EDTA 2 5 ml (750 ul; Blutproben: 1 ml) Probe sollte 2 nach Abnahme im Labor sein. Serum/EDT A-Blut: Kopien/ml Bei V.a. hämorrhag. Zystitis (KM- TPL, Leukämie), Ureterstenose (Kinder); Post-TPL-Nephropathie, selten Pneumonie, Meningoenzephalitits; asympt. Ausscheidung im Urin bei NTPL häufig; >10 7 Kopien/ml im Urin sind mit BKV- Nephropathie nach TPL bzw mit hämorrhag. Zystitis assoziiert. >10 4 Kopien/ml im EDTA-Blut (persistierend > 3 w) erhärten den V.a Post-TPL-Nephropathie (histologische Diagnosesicherung durch Nierenbiopsie). Bocavirus DNA Multiplex -PCR Abstrich, BAL, TS, Nasopharynxsekret, Rachen/ Nasen- Spülung, Punktat, Sputum 1 2 ml (1 ml) Probe sollte 2 nach Abnahme im Labor sein. Abstrich in TM für die Virus-isolierung oder in NaCl 0,9% (1 ml) 4h akute Infektion des RT; im Untersuchungsblock Respirator. Erregernachweis enthalten. 19
21 Parameter Methode Material Probenmenge optimal (minimal) Besonderheiten bei Abnahme/ Transport Ergebnis/ Dimension Testfreq./ minimale Untersuchungsdauer Anmerkungen Chlamydia trachomatis DNA PCR Zervix- Abstrich, Urin Trans- port max ml (1 ml) Chlamydien-TM! TM ohne Tupfer kann nicht bearbeitet werden! Urin: 2 h vor Kollektion nicht urinieren. 2 x pro w/ 6 h Schleim in zervikalen Proben kann die PCR beeinträchtigen und zu falsch-negativen Ergebnissen führen. Schleimfreie Proben empfohlen: einen (zu verwerfenden) Tupfer verwenden, um Zervixsekrete zu entfernen; Proben mit einem Blutanteil von mehr als 7% (v/v) können zu falsch-positiven Ergebnissen führen. Mutationen in den hochgradig konservierten Regionen der kryptischen Plasmid- DNA oder der Chromosomen-DNA von C. trachomatis, die durch die Primer bzw. Sonden des Tests abgedeckt sind, treten zwar selten auf, können jedoch zur Nichterkennung der Erreger führen. Nicht als Therapiemarker geeignet, da die nachgewiesene C. trachomatis Plasmid-DNA nach erfolgreicher Therapie noch vorliegen kann. Cytomegalievirus (CMV) IgG IgG Aviditäts -test CMIA Serum 5 ml (500 ul) IgM CMIA Serum 5 ml (500 ul) DNA PCR EDTA, Urin Liquor Kammerwasser BAL, TS Abstrich Biopsie Knochenm. 2 5 ml (750 ul; Blutproben: 1 ml; Biopsie: 2 mm 3 ) Probe sollte 2 nach Abnahme im Labor sein. U/ml Kopien/ml (Plasma, Serum) bzw. 1 h 1 h CMV-IgG positiv ab 6 U/ml (erfolgte CMV-Infektion); bei 6-15 U/ml empfiehlt der Testhersteller die Testung einer 2. Serumprobe zur Bestätigung des IgG Status; obere Nachweisgrenze: > 250 U/ml. Bei Serokonversion im Rahmen der Primärinfektion kann IgG zeitgleich mit IgM oder 1-2 (-3) w nach IgM nachweisbar sein. Bei positivem CMV-IgG u. V.a. Primärinfektion (IgM positiv) kann mittels CMV-IgG Aviditätstest zwischen einer kürzlich erworbenen Primärinfektion (niedrige Avidität) und einer Nicht- Primärinfektion (hohe Avidität) unterschieden werden. bei Primärinfekt. (ab 1 w nach Symptombeginn) 2 m bis 1 a nachweisbar (bei Immunsuppr. > 2 a); ein neg. Resultat schließt aktive Infektion/ Reaktiv. nicht sicher aus. TORCH: neg. IgM schließt konnatale Infekt. nicht sicher aus (bei bis zu 80% der kongenital Infizierten ist IgM nicht nachweisbar; CMV-PCR aus Urin o. Speichel empfohlen!). u.a. Monitoring nach TPL. CMV- DNA im Plasma korreliert mit erhöhtem Risiko einer systemischen CMV-Erkrankung (>1000 Kopien/ ml). Im Urin asymptomat. CMV-Ausscheidung möglich. Nachweis von CMV-DNA in Liquor, BAL etc. spricht für aktive CMV- Infektion. 20
22 Parameter pp65 Antigen* Quanti- feron- Test* Anti- körper- Index (AI) Methode Material IFT ELISA EDTA-, Heparin- Blut Heparin- Vollblut EIA Serum + + Liquor, zeitgleiche Entnahme Probenmenge optimal (minimal) 10 ml (5 ml) Besonderheiten bei Abnahme/ Transport Probe muss spätestens 2 nach Abnahme im Labor sein. Bitte separates Röhrchen abnehmen (d.h. für PCR + pp65 zwei Röhrchen!) 3 x 1 ml Nur die 3 testspezifischen Röhrchen (Fa. Qiagen) mit CMV- Antigen (blau), Mitogen (lila) und ohne Antigen (grau) sind geeignet! Röhrchen müssen bei Abnahme C haben. Röhrchen nach Befüllen 10x sanft schütteln. Die Probe muss sofort nach Abnahme bei RT in unser Labor transportiert werden oder vor Ort 16-24h bei 37 C stehend inkubiert werden (Röhrchen als inkubiert kennzeichnen). Serum 2 ml (120 ul) Liquor 0,75 ml (120 ul) Zeitgleiche Abnahme von Serum + Liquor Bitte nicht das normale Anforderungsformular für virologische Untersuchungen benutzen, sondern den Einsendeschein Neurologische Labordiagnostik (mittlere Spalte). Das Institut für Klinische Chemie leitet die Proben zur erregerspezif. AI-Bestimmung an uns weiter. Ergebnis/ Dimension semiquantitativ: pos. Zellen pro Zellen reaktiv/ nichtreaktiv/ nicht ermittelbar relativer Liquor/ Serum IgG- Quotient Testfreq./ minimale Untersuchungsdauer Mo-Fr/ 5 h Mo-Fr/ 28 h 3 x pro w/ 1d Anmerkungen u. a. Monitoring bei TPL; Bei KM- TPL ungeeignet; Bei pos. Befund disseminierte Infektion, die asymptomatisch bleiben o. symptomatisch werden kann; bei 50 pos. Zellen/ Zellen sympto-mat. Infektion/ Reaktivierung sehr wahrscheinlich. Kann bis zu 1 w vor Symptombeginn pos. sein. Der Test misst die zelluläre Immunität gegen CMV. Vollblut wird mit CMV-Antigenen und Kontrollantigenen stimuliert und die Interferon-gamma Sekretion im Plasma gemessen. Fehlende Stimulierbarkeit (Testresultat nichtreaktiv) ist wegen fehlender zellvermittelter Anti-CMV-Immunität mit einem erhöhten Risiko für eine CMV-Reaktivierung verbunden. < 1,5, normal (keine intrathekale IgG-Synthese gegen CMV). 1,5-1,9, AI mäßig erhöht; intrathekale IgG-Synthese gegen CMV möglich, sofern die Blut-Liquor- Schranke intakt ist (siehe Befunde der Klinischen Chemie). >= 2,0, intrathekale IgG-Synthese gegen CMV liegt vor, sofern die Blut-Liquor-Schranke intakt ist (siehe Befunde der Klin. Chemie). Der AI ist in der frühen Phase (1. Krankheitswoche) der Infektion unauffällig, da IgG im Liquor erst in der 2. Krankheitswoche an-steigt! Nach durchgemachter Infektion fällt der AI langsam (über Monate bis Jahre) ab. Im Rahmen chronisch entzündl. Erkrankungen des ZNS, wie z.b. Multipler Sklerose, können die AI für mehrere Erreger erhöht sein (unspezifische Stimulation virusspezifischer B-Zellen). Coronaviren RNA Multiplex -PCR Abstrich, BAL, TS, Nasopharynxsekret, Rachen/ Nasen- Spülung, Punktat, Sputum 1 2 ml (1 ml) Probe sollte 2 nach Abnahme im Labor sein. Abstrich in TM für die Virus-isolierung oder in NaCl 0,9% (1 ml) 4h akute Infektion des RT; im Untersuchungsblock Respirator. Erregernachweis enthalten. Umfasst die Coronaviren 229E, OC43 und NL63 21
23 Parameter Methode Material Probenmenge optimal (minimal) Besonderheiten bei Abnahme/ Transport Ergebnis/ Dimension Testfreq./ minimale Untersuchungsdauer Anmerkungen Dengue-Viren IgM+IgG EIA Serum 2 5 ml (100 ul) NS1-AG IC Serum 2 5 ml (150 ul) RNA PCR Serum, Liquor 2 5 ml (750 ul; Blutproben: 1 ml) 1 h Bei Fieber nach Tropenaufenthalt. IgM bei Primärinfektion frühestens 3-5 (-8) d nach Fieberbeginn für d (-8 m), bei Sekundärinfektion meist (aber nicht immer) ab d 20 positiv. IgG bei Primärinfektion meist ab d 14, bei Sekundärinfektion Titeranstieg ab d 1-2 nach Fieberbeginn. Bei neg. Test u. klinischem Verdacht: NS1-Antigen (s.u.) oder Kontrolleinsendung in 3-4 d oder PCR (Virämie 3 7 d). Kreuzreaktionen mit anderen Flaviviren sind möglich (Gelbfieber-, West Nil-, Japan. Enzephalitis-, FSME-Virus). Bei primärem oder sekundärem Dengue-Fieber von d1-d9 nach Fieberbeginn nachweisbar (Test- Spezifität 98,4%, Sensitivität 92,8%) Bei unklaren serologischen Dengue- Virus Befunden. Kurze Virämie (ca. 3-7 d). Epstein-Barr-Virus (EBV) VCA-IgA IFT Serum 5 ml (100 ul) VCA-IgG EIA Serum 5 ml (10 ul) VCA-IgM EIA Serum 5 ml (10 ul) EBNA1- IgG EIA Serum 5 ml (10 ul) EA-IgG EIA Serum 5 ml (10 ul) DNA PCR EDTA-Blut, Liquor, Biopsie, Knochenmark 2 5 ml (750 ul; Blutproben: 1 ml) Probe sollte 2 nach Abnahme im Labor sein. Titer bis > 1: 512 Kopien/ml (EDTA- Blut) bzw. pos./neg. 3x pro w/ Titer erhöht ( 1:160) bei Nasopharynx-Karzinom bei akuter Infektion pos., danach lebenslang akute EBV-Infektion o. Reaktivierung, nach Primärinfekt w nachweisbar (event. länger); bei Primärinfektion in 10% kein IgM (VCA-IgG pos., EBNA-IgG neg.) frühestens 4 w nach Primärinfektion nachweisbar, d.h. EBNA-1 IgG schließt Primärinfektion aus; bei Immunsuppr. oft Verlust von EBNA- 1 IgG; 5% der Infizierten bilden nie EBNA-1 IgG. Primärinfektion (bei 80% pos.) oder Reaktivierung Bei V.a. EBV-Reaktivierung; bei Immunsuppression o. EBVassoziiertem Lymphom; bei V.a. Primärinfektion (EDTA-Blut) und unklarer EBV-Serologie Enteroviren RNA PCR Liquor, Pu nktat, Serum, Stuhl RNA Multiplex -PCR Abstrich, BAL, TS, Nasopharynxsekret, Rachen/ Nasen- Spülung, Punktat, Sputum 2 5 ml (750 ul; Blutproben: 1 ml) 1 2 ml (1 ml) Probe sollte 2 nach Abnahme im Labor sein. Probe sollte 2 nach Abnahme im Labor sein. Abstrich in TM für die Virus-isolierung oder in NaCl 0,9% (1 ml) 4h V.a. Meningitis/Enzephalitis, Neugeborenen-Infekt.; erfasst Coxsackie A5, A7, A9, A10, A14, A16, B1-B6, Echovirus 4, 7, 9, 11, 13, 14, 20, 21, 24, 25, 30, Polio-Virus 1-3, Enterovirus 71 akute Infektion des RT; im Untersuchungsblock "Respirator. Erregernachweis" enthalten; auch als Einzeltest (siehe oben) anforderbar. 22
24 Parameter Methode Material Probenmenge optimal (minimal) Besonderheiten bei Abnahme/ Transport Ergebnis/ Dimension Testfreq./ minimale Untersuchungsdauer Anmerkungen Frühsommer-Meningoencephalitis (FSME) Virus IgG EIA Serum 5 ml (20 ul) IgM EIA Serum 5 ml (20 ul) Mo-Fr/ Mo-Fr/ Durchgemachte Infektion o. Z.n. Impfung; meist wie IgM bereits bei Krankheitsbeginn nachweisbar; AK gegen anderen Flaviviren (Dengue-, Gelbfieber-, West-Nil-Virus, Japan- Enzephalitis-V., HCV, u.a.) können kreuzreagieren. Diagnosesichernd ist ein Titeranstieg in einer 2. Serumprobe (Abstand 2-4 w). bei Krankheitsbeginn fast immer pos.; nach FSME-Impfung event. für einige w (schwach) positiv; Kreuzreaktivität s. FSME-IgG Hantaviren Puumala IgM IgG IgM IC Schnelltest Immunoblot Immunoblot Serum Serum Serum 2 5 ml (10 ul) 5 ml (50 ul) 5 ml (50 ul) pos/neg. 1 h Mo-Fr / 5 h Mo-Fr / 5 h Bei negativem Test u. klinischem V.a. Hanta-(Puumala-)Infektion Kontrolleinsendung in 3-7 d; Bei pos. Test sind Kreuzreaktionen zw. den versch. Hantavirus Serotypen möglich; IgM können einige Monate nach Infektion schwach positiv nachweisbar sein. akute o. durchgemachte Infektion. Der Test erfasst die 5 Hantavirus Serotypen Puumala (Europa), Dobrava (Europa), Hantaan (Asien), Seoul (Asien), Sin Nombre (Amerika); IgG sind kurz nach den IgM AK (s.u.) nachweisbar und bleiben wahrscheinlich lebenslang erhalten; Kreuzreaktionen zwischen den o.g. Serotypen sind möglich. frische Infektion; ab oder wenige d nach Krankheitsbeginn für 3-6 m positiv, in Einzelfällen 1-3 a nachweisbar; in Einzelfällen nur IgG nachweisbar; der Test erfasst die 5 Hantavirus Serotypen Puumala, Dobrava, Hantaan, Seoul, Sin Nombre; Kreuzreaktionen zwischen den o.g. Serotypen sind möglich. Bei negativem Test u. klinischem V.a. Hantavirus-Infektion bitte Kontrolleinsendung in 3-14 d; Bei pos. IgM und neg. IgG-Resultat sollte eine weitere Testung nach 1 w erfolgen. Hepatitis-A-Virus (HAV) IgG CMIA Serum 5 ml (500 ul) IgM CMIA Serum 5 ml (500 ul) pos. / neg. 1,5 h 1 h IgG nach durchgemachter Infektion oder Impfung (Immunität). Bei Krankheitsbeginn fast immer positiv und für ca. 12 w ( - 6m) nachweisbar, falsch positive Reaktionen sind (selten) möglich; ein positives Resultat sollte deshalb durch eine HAV-IgG-Bestimmung ergänzt werden. 23
25 Parameter Methode Material Probenmenge optimal (minimal) Besonderheiten bei Abnahme/ Transport Ergebnis/ Dimension Testfreq./ minimale Untersuchungsdauer Anmerkungen Hepatitis-B-Virus (HBV) a-hbc CMIA Serum 5 ml (500 ul) a-hbc- IgM CMIA Serum 5 ml (500 ul) HBs-AG CMIA Serum 5 ml (500 ul) HBs-AG quantitativ CMIA Serum 5 ml (500 ul) a-hbs CMIA Serum 5 ml (500 ul) HBe-AG CMIA Serum 5 ml (500 ul) a-hbe CMIA Serum 5 ml (500 ul) HBV- DNA Viruslast HBV- Genotypisierung/ Resistenz quant. PCR PCR u. Sequenz -analyse Serum EDTA EDTA-Blut (Serum) 5 ml (1 ml) 5 ml (2 ml) Das Serum sollte vor einer Heparintherapie entnommen werden, Probe sollte 2 nach Abnahme im Labor sein. Probe sollte 2 nach Abnahme im Labor sein IU/ml miu/ml IU/ml Nachweisgrenze = 10 IU/ml (1 IU =3,41 Kopien) Genotypisierung, Resistenzbestimmung 1 h 1 h 1 h 1 h 1,5 h 1 h 1 h 2 x pro w/ 6 h 1 x pro w/ >= 1 w Durchseuchungsmarker; Positiv nach HBV-Kontakt (akute, chron., abgelaufene Hepatitis B). Isoliert pos. a-hbc u.a. bei post-akuter HBV Infektion, HBV-Trägerstatus ohne nachweisbares HBsAG (Escape Mutanten, Immunkomplexe, sehr niedr. HBsAG Titer), passiver AK- Transfer, Anti-HBs-Verlust bei lange zurückliegender Primärinfektion, oder bei unspezifischer Reaktion akute HBV-Infektion, event. auch bei chron. Infekt. mit erhöhter Virusaktivität nachweisbar. Gelegentlich jahrelang und sogar länger als a-hbs nachweisbar. akute o. chronischr Infektion; frühester serolog. Marker (ca. 6 8 w p.i.); Infektiosität! Bei sog. Low Level Carriern (okkulte HBV-Infektion) nicht nachweisbar (PCR+,<200 IU/ml) Therapieüberwachung bei chronischer Hepatitis B; Biomarker für die Prognose und das Ansprechen auf die Therapie. Die Nachweisgrenze liegt bei 0,05 IU/ml. Dynamischer Bereich des Tests bis 250 bzw. (nach Verdünnung) 5000 IU/ml. Abgelaufene Infektion (bei pos. a-hbc) o. Z.n. Impfung (nur anti- HBs+); Immunität ab 10 miu/ml, lang anhaltende Immunität ab 100 miu/ml akute o. chronische Infektion; hohe Infektiosität Bei Präcore/ Core Mutanten trotz hoher Infektiosität nicht nachweisbar (HBV-DNA > 2000 IU/ml, hoch-virämisch) Abschätzung des Hepatitis- Aktivitätsgrads; Positivität schließt eine Lebererkrankung nicht aus, inbes. bei HBV-DNA-Last > 2000 IU/ml ab 4 Wochen p.i. nachweisbar; > 2000 IU/ml spricht für starke Infektiosität; Therapiemonitoring; prognost. Marker; Dynamischer Bereich des Tests bis 10 9 IU/ml Resistenzbestimmung bei V.a. Nukleos(t)idanaloga-Resistenz; Genotypisierung: prognostischer Marker für Erfolg einer Interferon- Therapie (A u. B günstiger als C u. D) Hepatitis-C-Virus (HCV) IgG CMIA Serum 5 ml (500 ul) IgG IB Serum 5 ml (20 ul) 1 h Mo-Fr/ 6 h HCV-Suchtest; in der Regel 7-8 w (Spannweite 2-26 w) nach Infektion positiv. Bei Immundefizienz/ suppression, Hämodialyse oder V.a. frische Infektion ist ein HCV-RNA- Nachweis vorzuziehen! Bestätigungstest bei erstmalig positivem Suchtest und fehlendem HCV-RNA Nachweis 24
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13253-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.08.2016 bis 31.07.2021 Ausstellungsdatum: 01.08.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13253-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.08.2016 bis 31.07.2021 Ausstellungsdatum: 01.08.2016 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.06.2015 bis 24.07.2017 Ausstellungsdatum: 11.06.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.06.2015 bis 24.07.2017 Ausstellungsdatum: 11.06.2015 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 18.05.2017 bis 29.03.2022 Ausstellungsdatum: 18.05.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 18.05.2017 bis 29.03.2022 Ausstellungsdatum: 18.05.2017 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13134-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.12.2017 bis 10.12.2022 Ausstellungsdatum: 11.12.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13134-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.12.2017 bis 10.12.2022 Ausstellungsdatum: 11.12.2017 Urkundeninhaber:
Virologische Diagnostik
 , Virologische Diagnostik (Version: 03/2015) 1. Überblick zu Diagnostik und Untersuchungsmaterial Erreger Untersuchungsmaterial Nachweisverfahren Bemerkungen Herpesviren [DNA-Viren] Herpes simplex- Virus
, Virologische Diagnostik (Version: 03/2015) 1. Überblick zu Diagnostik und Untersuchungsmaterial Erreger Untersuchungsmaterial Nachweisverfahren Bemerkungen Herpesviren [DNA-Viren] Herpes simplex- Virus
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13168-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.09.2017 bis 23.07.2018 Ausstellungsdatum: 01.09.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13168-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.09.2017 bis 23.07.2018 Ausstellungsdatum: 01.09.2017 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-14413-01-00 nach DIN EN ISO 15189:2014 Gültig ab: 30.10.2018 Urkundeninhaber: Ludwig-Maximilians-Universität München, Max von
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-14413-01-00 nach DIN EN ISO 15189:2014 Gültig ab: 30.10.2018 Urkundeninhaber: Ludwig-Maximilians-Universität München, Max von
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-05-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 30.08.2016 bis 29.08.2021 Ausstellungsdatum: 30.08.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-05-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 30.08.2016 bis 29.08.2021 Ausstellungsdatum: 30.08.2016 Urkundeninhaber:
Juni Ringversuche geschlossen. Information zu Probeneigenschaften. Prof. Dr. Heinz Zeichhardt. Dr. Martin Kammel
 Juni 2018 e geschlossen Information zu Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Juni 2018 e geschlossen Information zu Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13130-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 19.12.2016 bis 18.12.2021 Ausstellungsdatum: 19.12.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13130-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 19.12.2016 bis 18.12.2021 Ausstellungsdatum: 19.12.2016 Urkundeninhaber:
Interpretation von serologischen Befunden
 Interpretation von serologischen Befunden Cédric Hirzel Berner Infektiologie Symposium 2014 Hausärztliche serologische Fragen Borreliose EBV HBV Interpretation von serologischen Befunden Epstein Barr Virus
Interpretation von serologischen Befunden Cédric Hirzel Berner Infektiologie Symposium 2014 Hausärztliche serologische Fragen Borreliose EBV HBV Interpretation von serologischen Befunden Epstein Barr Virus
evademecum Analysenverzeichnis
 evademecum Analysenverzeichnis Analysen, Tarife, Durchführung Erreger: Analyse: AL-Pos.: TP: Durchführung: Kultur allg. für breites en, und/oder 3000.00 74 Virusspektrum Virus-Isolierung mittels Kurzkultur
evademecum Analysenverzeichnis Analysen, Tarife, Durchführung Erreger: Analyse: AL-Pos.: TP: Durchführung: Kultur allg. für breites en, und/oder 3000.00 74 Virusspektrum Virus-Isolierung mittels Kurzkultur
Juni Ringversuche geschlossen. Information zu Probeneigenschaften. Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel
 Juni 2017 e geschlossen Information zu Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Juni 2017 e geschlossen Information zu Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners. Dr. Thomas Berg, Berlin www.bergdoctor.de
 Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners Was untersucht der HIV-Antikörper- Schnelltest? (am Beispiel Vitest HIV) Der HIV-Antikörper-Schnelltest ist ein SUCHTEST, der untersucht, ob
Der HIV-Antikörper-Schnelltest aus Sicht des Labormediziners Was untersucht der HIV-Antikörper- Schnelltest? (am Beispiel Vitest HIV) Der HIV-Antikörper-Schnelltest ist ein SUCHTEST, der untersucht, ob
Auszug aus dem Strukturierten Qualitätsbericht
 Auszug aus dem Strukturierten Qualitätsbericht gemäß 137 Abs. 3 Satz 1 Nr. 4 SGB V für das Berichtsjahr 2010 Institut für Virologie B-37 Institut für Virologie B-37.1 Allgemeine Angaben : Institut für
Auszug aus dem Strukturierten Qualitätsbericht gemäß 137 Abs. 3 Satz 1 Nr. 4 SGB V für das Berichtsjahr 2010 Institut für Virologie B-37 Institut für Virologie B-37.1 Allgemeine Angaben : Institut für
evademecum Analysenverzeichnis
 evademecum Analysenverzeichnis Analysen, Tarife, Durchführung Erreger: Analyse: AL-Pos.: TP: Durchführung: Kultur allg. für breites en, und/oder 3000.00 74 Virusspektrum Virus-Isolierung mittels Kurzkultur
evademecum Analysenverzeichnis Analysen, Tarife, Durchführung Erreger: Analyse: AL-Pos.: TP: Durchführung: Kultur allg. für breites en, und/oder 3000.00 74 Virusspektrum Virus-Isolierung mittels Kurzkultur
Fallstricke in der HIV-Diagnostik. Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien
 Fallstricke in der HIV-Diagnostik Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien HIV-Infektion: Diagnostik- Zeitverlauf Nach Pilcher et al, 2004 HIV-Infektion: Diagnostik-
Fallstricke in der HIV-Diagnostik Elisabeth Puchhammer-Stöckl Department für Virologie Medizinische Universität Wien HIV-Infektion: Diagnostik- Zeitverlauf Nach Pilcher et al, 2004 HIV-Infektion: Diagnostik-
BIS Infobrief November 2014
 Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit BIS Infobrief November 2014 Sehr geehrte Kolleginnen und Kollegen, wir bedanken uns ganz herzlich bei Ihnen für Ihre aktive Teilnahme am
Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit BIS Infobrief November 2014 Sehr geehrte Kolleginnen und Kollegen, wir bedanken uns ganz herzlich bei Ihnen für Ihre aktive Teilnahme am
Cytomegalie & Co. Häufige Virusinfektionen in der Schwangerschaft. Deutsches Grünes Kreuz e.v.
 Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
evademecum Antikörpernachweis / Serologie
 evademecum Antikörpernachweis / Serologie 1. Einfachbestimmungen 2. Messunsicherheit bei quantitativen Bestimmungen 3. Bestimmung von IgG-, IgM- und IgA-Antikörpern 4. Methoden der Serologie 5. Liquor-Diagnostik
evademecum Antikörpernachweis / Serologie 1. Einfachbestimmungen 2. Messunsicherheit bei quantitativen Bestimmungen 3. Bestimmung von IgG-, IgM- und IgA-Antikörpern 4. Methoden der Serologie 5. Liquor-Diagnostik
Erkältung / Pharyngitis häufig: Adenoviren, EBV, Influenza-Viren, Parainfluenza-Viren, Picornaviren, RSV seltener: Bordetella pertussis
 Arthritis (Reaktiv) Borrelien, Campylobacter, Chlamydia trachomatis, Salmonellen, Streptokokken (ASL), Yersinien seltener: Brucellen, Hepatitis B-Virus, Mykoplasma hominis, Parvovirus B19, Röteln-Virus,
Arthritis (Reaktiv) Borrelien, Campylobacter, Chlamydia trachomatis, Salmonellen, Streptokokken (ASL), Yersinien seltener: Brucellen, Hepatitis B-Virus, Mykoplasma hominis, Parvovirus B19, Röteln-Virus,
Die Labordiagnose der Virushepatitis
 Seite 1 von 6 Die Labordiagnose der Virushepatitis Die primär hepatotropen Erreger HepatitisAVirus (HAV) HepatitisBVirus (HBV) HepatitisCVirus (HCV) HepatitisDVirus (HDV) (HepatitisDeltaVirus) HepatitisEVirus
Seite 1 von 6 Die Labordiagnose der Virushepatitis Die primär hepatotropen Erreger HepatitisAVirus (HAV) HepatitisBVirus (HBV) HepatitisCVirus (HCV) HepatitisDVirus (HDV) (HepatitisDeltaVirus) HepatitisEVirus
Liquor- und Punktatdiagnostik Inhaltsverzeichnis
 Inhaltsverzeichnis Liquordiagnostik...2 Albumin...2 Chlorid...2 Gesamteiweiß...2 Glucose...2 Immunglobulin A...2 Immunglobulin G...2 Immunglobulin M...2 Lactat...2 NSE...3 TPHA...3 Zellzahl / Zellart...3
Inhaltsverzeichnis Liquordiagnostik...2 Albumin...2 Chlorid...2 Gesamteiweiß...2 Glucose...2 Immunglobulin A...2 Immunglobulin G...2 Immunglobulin M...2 Lactat...2 NSE...3 TPHA...3 Zellzahl / Zellart...3
Leistungsverzeichnis. Institut für Virologie
 Leistungsverzeichnis Institut für Virologie Direktor: Univ.-Prof. Dr. med. Florian Klein UNIKLINIK KÖLN akkreditiert nach DIN EN ISO 15189 Nationales Referenzzentrum für Papillom- und Polyomaviren Version
Leistungsverzeichnis Institut für Virologie Direktor: Univ.-Prof. Dr. med. Florian Klein UNIKLINIK KÖLN akkreditiert nach DIN EN ISO 15189 Nationales Referenzzentrum für Papillom- und Polyomaviren Version
Schulungsunterlagen Zentrallabor
 Schulungsunterlagen Zentrallabor Institut für Klinische Chemie & Pharmakologie Zentrallabor Dr. med. Andreas Grigull Stand 10.02.2010 Lauris ist ein System zur elektronischen Anforderung von Laborbefunden.
Schulungsunterlagen Zentrallabor Institut für Klinische Chemie & Pharmakologie Zentrallabor Dr. med. Andreas Grigull Stand 10.02.2010 Lauris ist ein System zur elektronischen Anforderung von Laborbefunden.
Enterovirus/Parechovirus Infektionen. Daniela Huzly Institut für Virologie Freiburg
 Enterovirus/Parechovirus Infektionen Daniela Huzly Institut für Virologie Freiburg Virologie Beide gehören zur Familie der PICORNAVIRIDAE Enteroviren werden traditionell unterteilt in: Poliovirus 1 3 Echoviren
Enterovirus/Parechovirus Infektionen Daniela Huzly Institut für Virologie Freiburg Virologie Beide gehören zur Familie der PICORNAVIRIDAE Enteroviren werden traditionell unterteilt in: Poliovirus 1 3 Echoviren
Leistungsverzeichnis. Institut für Virologie
 Leistungsverzeichnis Institut für Virologie Direktor: Univ.-Prof. Dr. med. Florian Klein UNIKLINIK KÖLN akkreditiert nach DIN EN ISO 15189 Nationales Referenzzentrum für Papillom- und Polyomaviren Version
Leistungsverzeichnis Institut für Virologie Direktor: Univ.-Prof. Dr. med. Florian Klein UNIKLINIK KÖLN akkreditiert nach DIN EN ISO 15189 Nationales Referenzzentrum für Papillom- und Polyomaviren Version
Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e. V Düsseldorf Ubier- Str. 20, Postfach
 ...... cri 2362-1 ---------------------------.~----- ------ ---- ~ Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e. V. Virusimmunologie März 2010 ( Ausstellungsdatum 20.8.201
...... cri 2362-1 ---------------------------.~----- ------ ---- ~ Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e. V. Virusimmunologie März 2010 ( Ausstellungsdatum 20.8.201
Titer. französisch titre: Feingehalt
 Serologie Testverfahren (in der Mikrobiologie und Virologie) zur Bestimmung spezifischer Antikörper im Serum oder in anderen Körperflüssigkeiten gegen infektiöse Erreger Titer französisch titre: Feingehalt
Serologie Testverfahren (in der Mikrobiologie und Virologie) zur Bestimmung spezifischer Antikörper im Serum oder in anderen Körperflüssigkeiten gegen infektiöse Erreger Titer französisch titre: Feingehalt
Ringversuche geschlossen. Information zu Probeneigenschaften. INSTAND e.v. in Zusammenarbeit mit:
 Virologische e November/Dezember 2015 e geschlossen Information zu INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten (DVV) Gesellschaft für Virologie (GfV) Deutsche
Virologische e November/Dezember 2015 e geschlossen Information zu INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten (DVV) Gesellschaft für Virologie (GfV) Deutsche
Epstein-Barr-Virus-Infektion: Möglichkeiten und Grenzen der serologischen Diagnostik von Reaktivierungen und chronischen Verläufen
 Epstein-Barr-Virus-Infektion: Möglichkeiten und Grenzen der serologischen Diagnostik von Reaktivierungen und chronischen Verläufen Dr. Claudia Wolff Viramed Biotech AG 1 Akute EBV-Primärinfektion Erster
Epstein-Barr-Virus-Infektion: Möglichkeiten und Grenzen der serologischen Diagnostik von Reaktivierungen und chronischen Verläufen Dr. Claudia Wolff Viramed Biotech AG 1 Akute EBV-Primärinfektion Erster
Sinn und Unsinn der serologischen Virusdiagnostik. Dr. med. Daniela Huzly Abt. Virologie, Uniklinik Freiburg
 Sinn und Unsinn der serologischen Virusdiagnostik Dr. med. Daniela Huzly Abt. Virologie, Uniklinik Freiburg Historisches Louis Pasteur (1822-1895) Bis 1960 nur Erregeranzucht/Tiermodell Infektionsserologische
Sinn und Unsinn der serologischen Virusdiagnostik Dr. med. Daniela Huzly Abt. Virologie, Uniklinik Freiburg Historisches Louis Pasteur (1822-1895) Bis 1960 nur Erregeranzucht/Tiermodell Infektionsserologische
Leistungsverzeichnis. Institut für Virologie Leitung: Prof. Dr. Thomas F. Schulz. akkreditiert nach DIN EN ISO 15189
 Leistungsverzeichnis Leitung: Prof. Dr. Thomas F. Schulz akkreditiert nach DIN EN ISO 15189 16. Ausgabe Stand: Juli 2013 Herausgeber: Medizinische Hochschule Hannover Prof. Dr. med. Thomas F. Schulz Carl-Neuberg-Str.
Leistungsverzeichnis Leitung: Prof. Dr. Thomas F. Schulz akkreditiert nach DIN EN ISO 15189 16. Ausgabe Stand: Juli 2013 Herausgeber: Medizinische Hochschule Hannover Prof. Dr. med. Thomas F. Schulz Carl-Neuberg-Str.
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13130-03-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 13.10.2014 bis 15.04.2017 Ausstellungsdatum: 13.10.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13130-03-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 13.10.2014 bis 15.04.2017 Ausstellungsdatum: 13.10.2014 Urkundeninhaber:
Zentrum für Diagnostik Institut für Med. Mikrobiologie, Virologie und Hygiene
 Zentrum für Diagnostik Institut für Med. Mikrobiologie, Virologie und Hygiene Analyse/ Analyt Methode(n) Material Dauer Hintergrundinformation/ Interpretation Serologie/PCR 16S RNA-Gen (Bakterien) Liquor
Zentrum für Diagnostik Institut für Med. Mikrobiologie, Virologie und Hygiene Analyse/ Analyt Methode(n) Material Dauer Hintergrundinformation/ Interpretation Serologie/PCR 16S RNA-Gen (Bakterien) Liquor
Institut für Medizinische Virologie. Universitätsklinikum Tübingen. Untersuchungsverzeichnis Virusdiagnostik
 Institut für Medizinische Virologie Universitätsklinikum Tübingen Untersuchungsverzeichnis Virusdiagnostik Inhaltsverzeichnis Seite 1. Anschrift und Telefonverbindungen 3 2. Verzeichnis der untersuchten
Institut für Medizinische Virologie Universitätsklinikum Tübingen Untersuchungsverzeichnis Virusdiagnostik Inhaltsverzeichnis Seite 1. Anschrift und Telefonverbindungen 3 2. Verzeichnis der untersuchten
Text: Octapharma GmbH Illustrationen: Günter Hengsberg Layout: nonmodo, Köln
 Unser Immunsystem Text: Octapharma GmbH Illustrationen: Günter Hengsberg Layout: nonmodo, Köln Bakterien und Viren können uns krank machen. Wir bekommen dann Husten, Schnupfen oder Durchfall. Unser Körper
Unser Immunsystem Text: Octapharma GmbH Illustrationen: Günter Hengsberg Layout: nonmodo, Köln Bakterien und Viren können uns krank machen. Wir bekommen dann Husten, Schnupfen oder Durchfall. Unser Körper
Aufruf der Buchungssystems über die Homepage des TC-Bamberg
 Aufruf der Buchungssystems über die Homepage des TC-Bamberg Das Online-Buchungssystem erreichen Sie einfach über die Homepage des TC-Bamberg (www.tennis-club-bamberg.de).über den Link (siehe Bild 1) gelangen
Aufruf der Buchungssystems über die Homepage des TC-Bamberg Das Online-Buchungssystem erreichen Sie einfach über die Homepage des TC-Bamberg (www.tennis-club-bamberg.de).über den Link (siehe Bild 1) gelangen
Hantavirus-Diagnostik
 Hantavirus-Diagnostik A. Lucht, D. Münstermann, R. Geisel --------------------------------------------- Labor Dr. Krone & Partner Medizinaluntersuchungsstelle Bad Salzuflen, Herford Hanta-Virusstruktur
Hantavirus-Diagnostik A. Lucht, D. Münstermann, R. Geisel --------------------------------------------- Labor Dr. Krone & Partner Medizinaluntersuchungsstelle Bad Salzuflen, Herford Hanta-Virusstruktur
5. Isolierungsmaßnahmen
 5. Isolierungsmaßnahmen 5.8. Durch Blut- u. andere Körperflüssigkeiten übertragbare Erreger 5.8.1. HBV, HCV, HDV Hepatitis B Erreger: Hepatitis B-Virus (HBV) gehört zu der Gruppe der Hepadna-Viren Instrumente),
5. Isolierungsmaßnahmen 5.8. Durch Blut- u. andere Körperflüssigkeiten übertragbare Erreger 5.8.1. HBV, HCV, HDV Hepatitis B Erreger: Hepatitis B-Virus (HBV) gehört zu der Gruppe der Hepadna-Viren Instrumente),
Surveillance-Begleitforschungsprojekt des Robert Koch-Instituts: Diagnostik von gleichzeitigen Erkrankungen an HIV/AIDS und Tuberkulose
 Surveillance-Begleitforschungsprojekt des Robert Koch-Instituts: Diagnostik von gleichzeitigen Erkrankungen an HIV/AIDS und Tuberkulose Leitfaden zur Erhebung Ziel der Erhebung Ziel dieser Erhebung ist
Surveillance-Begleitforschungsprojekt des Robert Koch-Instituts: Diagnostik von gleichzeitigen Erkrankungen an HIV/AIDS und Tuberkulose Leitfaden zur Erhebung Ziel der Erhebung Ziel dieser Erhebung ist
Kapitel I: Registrierung im Portal
 Kapitel I: Registrierung im Portal Um zu unserem Portal zu gelangen, rufen Sie bitte die folgende Internetseite auf: www.arag-forderungsmanagement.de Bei Ihrem ersten Besuch des ARAG Portals ist es notwendig,
Kapitel I: Registrierung im Portal Um zu unserem Portal zu gelangen, rufen Sie bitte die folgende Internetseite auf: www.arag-forderungsmanagement.de Bei Ihrem ersten Besuch des ARAG Portals ist es notwendig,
Anleitung für die Lohnmeldung via ELM-Standard mittels PartnerWeb
 Ausgleichskasse Gewerbe St. Gallen Lindenstrasse 137 Postfach 245 9016 St. Gallen Telefon 071 282 29 29 Telefax 071 282 29 30 info@ahv-gewerbe.ch www.ahv-gewerbe.ch Anleitung für die Lohnmeldung via ELM-Standard
Ausgleichskasse Gewerbe St. Gallen Lindenstrasse 137 Postfach 245 9016 St. Gallen Telefon 071 282 29 29 Telefax 071 282 29 30 info@ahv-gewerbe.ch www.ahv-gewerbe.ch Anleitung für die Lohnmeldung via ELM-Standard
HIV1 /HIV2 Schnelltest In nur 60 Sekunden
 HIV1 /HIV2 Schnelltest In nur 60 Sekunden INSTI TM HIV Antikörper Test Features HIV 1 and HIV 2 Antikörpertest Human IgG Kontrolle Findet alle bekannten HIV 1 und HIV 2 Antikörpersubtypen, einschließlich
HIV1 /HIV2 Schnelltest In nur 60 Sekunden INSTI TM HIV Antikörper Test Features HIV 1 and HIV 2 Antikörpertest Human IgG Kontrolle Findet alle bekannten HIV 1 und HIV 2 Antikörpersubtypen, einschließlich
Erfahrungsbericht zur Eignung verschiedener ELISA Kits zum Nachweis von Antikörpern gegen Aviäre Influena für das Routinelabor
 Erfahrungsbericht zur Eignung verschiedener ELISA Kits zum Nachweis von Antikörpern gegen Aviäre Influena für das Routinelabor Dr. Hans-C. Philipp Lohmann Tierzucht GmbH Veterinär-Labor Abschnede 64 27472
Erfahrungsbericht zur Eignung verschiedener ELISA Kits zum Nachweis von Antikörpern gegen Aviäre Influena für das Routinelabor Dr. Hans-C. Philipp Lohmann Tierzucht GmbH Veterinär-Labor Abschnede 64 27472
Gene Control. Probenentnahme für DNA-Untersuchungen. Ein Unternehmen bayerischer Tierzuchteinrichtungen. Hinweise. Anleitung zur
 Hinweise Probenentnahme für DNA-Untersuchungen zur Haarwurzelentnahme Seite 2 Blutentnahme Seite 3 Gewebeentnahme Seite 4 Probenversand Seite 5 1 QMHAN19.03_Probenahme GeneControl GmbH Senator-Gerauer-Straße
Hinweise Probenentnahme für DNA-Untersuchungen zur Haarwurzelentnahme Seite 2 Blutentnahme Seite 3 Gewebeentnahme Seite 4 Probenversand Seite 5 1 QMHAN19.03_Probenahme GeneControl GmbH Senator-Gerauer-Straße
Stellen Sie bitte den Cursor in die Spalte B2 und rufen die Funktion Sverweis auf. Es öffnet sich folgendes Dialogfenster
 Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13102-03-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 09.12.2013 bis 08.12.2018 Ausstellungsdatum: 09.12.2013 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13102-03-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 09.12.2013 bis 08.12.2018 Ausstellungsdatum: 09.12.2013 Urkundeninhaber:
Eine Auflistung, der für die einzelnen klinischen Erkrankungen
 GEEIGNETES UNTERSUCHUNGSMATERIAL IM HINBLICK AUF KLINISCHE ERKRANKUNGEN Eine Auflistung, der für die einzelnen klinischen Erkrankungen in Frage kommenden Viren finden Sie auf unseren Zuweisungsscheinen
GEEIGNETES UNTERSUCHUNGSMATERIAL IM HINBLICK AUF KLINISCHE ERKRANKUNGEN Eine Auflistung, der für die einzelnen klinischen Erkrankungen in Frage kommenden Viren finden Sie auf unseren Zuweisungsscheinen
Zentraler Wertungsrichtereinsatz
 Zentraler Wertungsrichtereinsatz Anleitung zur erstmaligen Registrierung beim Online-System des zentralen Wertungsrichtereinsatzes des LTVB Zur Nutzung des Online-Systems des zentralen Wertungsrichtereinsatzes
Zentraler Wertungsrichtereinsatz Anleitung zur erstmaligen Registrierung beim Online-System des zentralen Wertungsrichtereinsatzes des LTVB Zur Nutzung des Online-Systems des zentralen Wertungsrichtereinsatzes
Schulungsunterlagen zur Version 3.3
 Schulungsunterlagen zur Version 3.3 Versenden und Empfangen von Veranstaltungen im CMS-System Jürgen Eckert Domplatz 3 96049 Bamberg Tel (09 51) 5 02 2 75 Fax (09 51) 5 02 2 71 Mobil (01 79) 3 22 09 33
Schulungsunterlagen zur Version 3.3 Versenden und Empfangen von Veranstaltungen im CMS-System Jürgen Eckert Domplatz 3 96049 Bamberg Tel (09 51) 5 02 2 75 Fax (09 51) 5 02 2 71 Mobil (01 79) 3 22 09 33
INSTAND e.v. in Zusammenarbeit mit:
 Vorauswertung zu den virologischen en Juni 2015 Korrigierte Version: 10. August 2015 (Siehe Tabelle 3; Programm 346) INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten
Vorauswertung zu den virologischen en Juni 2015 Korrigierte Version: 10. August 2015 (Siehe Tabelle 3; Programm 346) INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten
Teilnehmerlogin VHS Meppen Anleitung, Stand: 28.07.2015
 Volkshochschule Meppen Postfach 17 62 49707 Meppen Teilnehmerlogin VHS Meppen Anleitung, Stand: 28.07.2015 Ansprechpartner: Oliver Hankofer, Tel.: 05931 9373-35 oliver.hankofer@vhs-meppen.de Freiherr-vom-Stein-Str.
Volkshochschule Meppen Postfach 17 62 49707 Meppen Teilnehmerlogin VHS Meppen Anleitung, Stand: 28.07.2015 Ansprechpartner: Oliver Hankofer, Tel.: 05931 9373-35 oliver.hankofer@vhs-meppen.de Freiherr-vom-Stein-Str.
Tutorial. Wie kann ich meinen Kontostand von meinen Tauschpartnern in. übernehmen? Zoe.works - Ihre neue Ladungsträgerverwaltung
 Wie kann ich meinen Kontostand von meinen Tauschpartnern in Tutorial übernehmen? 1. Schritt : Legen Sie ein Startdatum fest Im ersten Schritt legen Sie für Ihr Unternehmen ein Startdatum fest, an dem Sie
Wie kann ich meinen Kontostand von meinen Tauschpartnern in Tutorial übernehmen? 1. Schritt : Legen Sie ein Startdatum fest Im ersten Schritt legen Sie für Ihr Unternehmen ein Startdatum fest, an dem Sie
Richtlinie zur Feststellung und Überwachung des PRRS-Status von Schweinebeständen (PRRS-Richtlinie) Rd. Erl. des MLU vom 27.
 Richtlinie zur Feststellung und Überwachung des PRRS-Status von Schweinebeständen (PRRS-Richtlinie) Rd. Erl. des MLU vom 27. Februar 2004 Anlagen 1. Einleitung Das PRRS-Virus wurde Anfang der 90-iger Jahre
Richtlinie zur Feststellung und Überwachung des PRRS-Status von Schweinebeständen (PRRS-Richtlinie) Rd. Erl. des MLU vom 27. Februar 2004 Anlagen 1. Einleitung Das PRRS-Virus wurde Anfang der 90-iger Jahre
Leistungsverzeichnis des Labordiagnostischen Zentrums / Uniklinik Aachen (LDZ)
 Adenovirus Antigen Stuhl FIA 0,5 3-5x wo Adenovirus DNA EDTA, Abstrich Kopien/ml PCR 0,5 2x wo Adenovirus IgA Serum VE ELISA 0,5 2x wo Adenovirus IgG Serum VE ELISA 0,5 2x wo Adenovirus IgM Serum VE ELISA
Adenovirus Antigen Stuhl FIA 0,5 3-5x wo Adenovirus DNA EDTA, Abstrich Kopien/ml PCR 0,5 2x wo Adenovirus IgA Serum VE ELISA 0,5 2x wo Adenovirus IgG Serum VE ELISA 0,5 2x wo Adenovirus IgM Serum VE ELISA
Leichte-Sprache-Bilder
 Leichte-Sprache-Bilder Reinhild Kassing Information - So geht es 1. Bilder gucken 2. anmelden für Probe-Bilder 3. Bilder bestellen 4. Rechnung bezahlen 5. Bilder runterladen 6. neue Bilder vorschlagen
Leichte-Sprache-Bilder Reinhild Kassing Information - So geht es 1. Bilder gucken 2. anmelden für Probe-Bilder 3. Bilder bestellen 4. Rechnung bezahlen 5. Bilder runterladen 6. neue Bilder vorschlagen
West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren
 West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren 100 nm HEV, Abb.: Center of Disease Control and Prevention WNV, Abb.: Dr. H. Gelderblohm, RKI Institut für Transfusionsmedizin
West-Nil-Virus und Hepatitis E-Virus: durch Bluttransfusion übertragbare Viren 100 nm HEV, Abb.: Center of Disease Control and Prevention WNV, Abb.: Dr. H. Gelderblohm, RKI Institut für Transfusionsmedizin
Real time RT-PCR Verfahren zur Detektion, Quantifizierung und Genotypisierung von Hepatitis-C-Virus
 Real time RT-PCR Verfahren zur Detektion, Quantifizierung und Genotypisierung von Hepatitis-C-Virus Seminar Molekulare Diagnostik 2011 30. November 2011, Wien AnDiaTec Kernkompetenz Entwicklung und Produktion
Real time RT-PCR Verfahren zur Detektion, Quantifizierung und Genotypisierung von Hepatitis-C-Virus Seminar Molekulare Diagnostik 2011 30. November 2011, Wien AnDiaTec Kernkompetenz Entwicklung und Produktion
Sie haben das Recht, binnen vierzehn Tagen ohne Angabe von Gründen diesen Vertrag zu widerrufen.
 Widerrufsbelehrung Nutzt der Kunde die Leistungen als Verbraucher und hat seinen Auftrag unter Nutzung von sog. Fernkommunikationsmitteln (z. B. Telefon, Telefax, E-Mail, Online-Web-Formular) übermittelt,
Widerrufsbelehrung Nutzt der Kunde die Leistungen als Verbraucher und hat seinen Auftrag unter Nutzung von sog. Fernkommunikationsmitteln (z. B. Telefon, Telefax, E-Mail, Online-Web-Formular) übermittelt,
Leitfaden zur Anlage einer Nachforderung. Nachforderung. 04.04.2013 Seite 1 von 11 RWE IT GmbH
 Leitfaden zur Anlage einer 04.04.2013 Seite 1 von 11 Inhaltsverzeichnis 1 Aufruf des RWE smanagements...3 2 Eingabe der Benutzerdaten...4 3 Erfassen der...5 4 Neue...6 4.1 Allgemeine Daten...7 4.2 Beschreibung...7
Leitfaden zur Anlage einer 04.04.2013 Seite 1 von 11 Inhaltsverzeichnis 1 Aufruf des RWE smanagements...3 2 Eingabe der Benutzerdaten...4 3 Erfassen der...5 4 Neue...6 4.1 Allgemeine Daten...7 4.2 Beschreibung...7
Anmeldung zum Triathlon Camp 2014 auf Fuerteventura Seite 1
 Anmeldung zum Triathlon Camp 2014 auf Fuerteventura Seite 1 Name: Adresse: Telefonnummer: E-Mail: Geburtsdatum: Bitte vollständig in Blockschrift ausfüllen! Pro Person eine Anmeldung ausfüllen! Ich buche
Anmeldung zum Triathlon Camp 2014 auf Fuerteventura Seite 1 Name: Adresse: Telefonnummer: E-Mail: Geburtsdatum: Bitte vollständig in Blockschrift ausfüllen! Pro Person eine Anmeldung ausfüllen! Ich buche
Leistungsverzeichnis. Institut für Virologie
 Leistungsverzeichnis Institut für Virologie Direktor: Univ.-Prof. Dr. med. Florian Klein UNIKLINIK KÖLN akkreditiert nach DIN EN ISO 15189 Nationales Referenzzentrum für Papillom- und Polyomaviren Version
Leistungsverzeichnis Institut für Virologie Direktor: Univ.-Prof. Dr. med. Florian Klein UNIKLINIK KÖLN akkreditiert nach DIN EN ISO 15189 Nationales Referenzzentrum für Papillom- und Polyomaviren Version
Erstellen von x-y-diagrammen in OpenOffice.calc
 Erstellen von x-y-diagrammen in OpenOffice.calc In dieser kleinen Anleitung geht es nur darum, aus einer bestehenden Tabelle ein x-y-diagramm zu erzeugen. D.h. es müssen in der Tabelle mindestens zwei
Erstellen von x-y-diagrammen in OpenOffice.calc In dieser kleinen Anleitung geht es nur darum, aus einer bestehenden Tabelle ein x-y-diagramm zu erzeugen. D.h. es müssen in der Tabelle mindestens zwei
Handbuch zum Excel Formular Editor
 Handbuch zum Excel Formular Editor Mit diesem Programm können Sie die Zellen von ihrer Excel Datei automatisch befüllen lassen. Die Daten können aus der Coffee Datenbank, oder einer weiteren Excel Datendatei
Handbuch zum Excel Formular Editor Mit diesem Programm können Sie die Zellen von ihrer Excel Datei automatisch befüllen lassen. Die Daten können aus der Coffee Datenbank, oder einer weiteren Excel Datendatei
Betroffenes Produkt: PRI Femureinschlägerkopf, 00-5901-032-00 (vollständige Liste der betroffenen Chargen siehe Anhang 1)
 22. Mai 2015 An: Betrifft: Risikomanager und Chirurgen DRINGENDER CHARGENSPEZIFISCHER RÜCKRUF EINES MEDIZINPRODUKTES Betroffenes Produkt: PRI Femureinschlägerkopf, 00-5901-032-00 (vollständige Liste der
22. Mai 2015 An: Betrifft: Risikomanager und Chirurgen DRINGENDER CHARGENSPEZIFISCHER RÜCKRUF EINES MEDIZINPRODUKTES Betroffenes Produkt: PRI Femureinschlägerkopf, 00-5901-032-00 (vollständige Liste der
Kapsch Carrier Solutions GmbH Service & Support Helpdesk
 Kapsch Carrier Solutions GmbH Kundenanleitung Tickets erstellen und bearbeiten 1 Das Helpdesk ist über folgende Webseite erreichbar https://support-neuss.kapschcarrier.com 2 Sie haben die Möglichkeit,
Kapsch Carrier Solutions GmbH Kundenanleitung Tickets erstellen und bearbeiten 1 Das Helpdesk ist über folgende Webseite erreichbar https://support-neuss.kapschcarrier.com 2 Sie haben die Möglichkeit,
Screening Das Programm. zur Früherkennung von Brustkrebs
 Mammographie Screening Das Programm zur Früherkennung von Brustkrebs das Mammographie Screening Programm Wenn Sie zwischen 50 und 69 Jahre alt sind, haben Sie alle zwei Jahre Anspruch auf eine Mammographie-Untersuchung
Mammographie Screening Das Programm zur Früherkennung von Brustkrebs das Mammographie Screening Programm Wenn Sie zwischen 50 und 69 Jahre alt sind, haben Sie alle zwei Jahre Anspruch auf eine Mammographie-Untersuchung
Installation der smart-q Terminal App
 Installation der smart-q Terminal App Zur Abrechnung per DTA benötigen Sie zusätzlich zu ISPC die smart-q Terminal App. Diese steht Ihnen als Download auf unserer Homepage http://www.smart-q.de/software/fallakte-palliativdokumentation-ispc-sapv-aapv/
Installation der smart-q Terminal App Zur Abrechnung per DTA benötigen Sie zusätzlich zu ISPC die smart-q Terminal App. Diese steht Ihnen als Download auf unserer Homepage http://www.smart-q.de/software/fallakte-palliativdokumentation-ispc-sapv-aapv/
Lieber SPAMRobin -Kunde!
 Lieber SPAMRobin -Kunde! Wir freuen uns, dass Sie sich für SPAMRobin entschieden haben. Mit diesem Leitfaden möchten wir Ihnen die Kontoeinrichtung erleichtern und die Funktionen näher bringen. Bitte führen
Lieber SPAMRobin -Kunde! Wir freuen uns, dass Sie sich für SPAMRobin entschieden haben. Mit diesem Leitfaden möchten wir Ihnen die Kontoeinrichtung erleichtern und die Funktionen näher bringen. Bitte führen
1. Einführung 2. 2. Erstellung einer Teillieferung 2. 3. Erstellung einer Teilrechnung 6
 Inhalt 1. Einführung 2 2. Erstellung einer Teillieferung 2 3. Erstellung einer Teilrechnung 6 4. Erstellung einer Sammellieferung/ Mehrere Aufträge zu einem Lieferschein zusammenfassen 11 5. Besonderheiten
Inhalt 1. Einführung 2 2. Erstellung einer Teillieferung 2 3. Erstellung einer Teilrechnung 6 4. Erstellung einer Sammellieferung/ Mehrere Aufträge zu einem Lieferschein zusammenfassen 11 5. Besonderheiten
Beispiel Shop-Eintrag Ladenlokal & Online-Shop im Verzeichnis www.wir-lieben-shops.de 1
 Beispiel Shop-Eintrag Ladenlokal & Online-Shop. Als Händler haben Sie beim Shop-Verzeichnis wir-lieben-shops.de die Möglichkeit einen oder mehrere Shop- Einträge zu erstellen. Es gibt 3 verschiedene Typen
Beispiel Shop-Eintrag Ladenlokal & Online-Shop. Als Händler haben Sie beim Shop-Verzeichnis wir-lieben-shops.de die Möglichkeit einen oder mehrere Shop- Einträge zu erstellen. Es gibt 3 verschiedene Typen
Erklärung zum Internet-Bestellschein
 Erklärung zum Internet-Bestellschein Herzlich Willkommen bei Modellbahnbau Reinhardt. Auf den nächsten Seiten wird Ihnen mit hilfreichen Bildern erklärt, wie Sie den Internet-Bestellschein ausfüllen und
Erklärung zum Internet-Bestellschein Herzlich Willkommen bei Modellbahnbau Reinhardt. Auf den nächsten Seiten wird Ihnen mit hilfreichen Bildern erklärt, wie Sie den Internet-Bestellschein ausfüllen und
Registrierungsanleitung ecom-system DARC e.v. OV Velbert
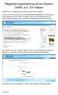 Willkommen zur Registrierung im ecom-system des OV Velbert! Dies ist eine kurze Einführung in die grundlegende Registrierung und Nutzung des ecom-systems des OV Velbert. Zu Beginn sollte man die Webseite
Willkommen zur Registrierung im ecom-system des OV Velbert! Dies ist eine kurze Einführung in die grundlegende Registrierung und Nutzung des ecom-systems des OV Velbert. Zu Beginn sollte man die Webseite
MS und Impfungen. DAS KLEINE IMPF-1x1. DAS KLEINE IMPF-1x1. Christian Lampl. Abteilung für Allgemeine Neurologie und Schmerzmedizin
 MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
CompassfaIrs. messehandbuch. 24. - 26. JanUar 2014. flensburg. flens-arena Campusallee 2 24943 flensburg. COMPASSFairs
 CompassfaIrs messehandbuch 24. - 26. JanUar 2014 flensburg flens-arena Campusallee 2 24943 flensburg COMPASSFairs nun ist es Zeit über die technik zu sprechen und Ihren Messestand so einzigartig wie möglich
CompassfaIrs messehandbuch 24. - 26. JanUar 2014 flensburg flens-arena Campusallee 2 24943 flensburg COMPASSFairs nun ist es Zeit über die technik zu sprechen und Ihren Messestand so einzigartig wie möglich
Kurzanleitung fu r Clubbeauftragte zur Pflege der Mitgliederdaten im Mitgliederbereich
 Kurzanleitung fu r Clubbeauftragte zur Pflege der Mitgliederdaten im Mitgliederbereich Mitgliederbereich (Version 1.0) Bitte loggen Sie sich in den Mitgliederbereich mit den Ihnen bekannten Zugangsdaten
Kurzanleitung fu r Clubbeauftragte zur Pflege der Mitgliederdaten im Mitgliederbereich Mitgliederbereich (Version 1.0) Bitte loggen Sie sich in den Mitgliederbereich mit den Ihnen bekannten Zugangsdaten
HESS-Shop. Handbuch. Etikettenformulare veredelte Produkte Garnituren Laserrollen Beipackzettel
 HESS-Shop 1 Handbuch 12. Mai 2011 2 Sehr geehrte Kundin, sehr geehrter Kunde Es freut uns sehr, dass Sie sich für unseren Online-Shop interessieren. Mit dem HESS-Shop können Sie schnell und unkompliziert
HESS-Shop 1 Handbuch 12. Mai 2011 2 Sehr geehrte Kundin, sehr geehrter Kunde Es freut uns sehr, dass Sie sich für unseren Online-Shop interessieren. Mit dem HESS-Shop können Sie schnell und unkompliziert
E-Government Sondertransporte (SOTRA) Registrierung von Benutzerkennung
 E-Government Sondertransporte (SOTRA) Registrierung von Benutzerkennung Projektteam Sondertransporte Land OÖ Version September 2012 Alle Rechte, insbesondere das Recht der Vervielfältigung, Verbreitung
E-Government Sondertransporte (SOTRA) Registrierung von Benutzerkennung Projektteam Sondertransporte Land OÖ Version September 2012 Alle Rechte, insbesondere das Recht der Vervielfältigung, Verbreitung
Hilfedatei der Oden$-Börse Stand Juni 2014
 Hilfedatei der Oden$-Börse Stand Juni 2014 Inhalt 1. Einleitung... 2 2. Die Anmeldung... 2 2.1 Die Erstregistrierung... 3 2.2 Die Mitgliedsnummer anfordern... 4 3. Die Funktionen für Nutzer... 5 3.1 Arbeiten
Hilfedatei der Oden$-Börse Stand Juni 2014 Inhalt 1. Einleitung... 2 2. Die Anmeldung... 2 2.1 Die Erstregistrierung... 3 2.2 Die Mitgliedsnummer anfordern... 4 3. Die Funktionen für Nutzer... 5 3.1 Arbeiten
Outlook. sysplus.ch outlook - mail-grundlagen Seite 1/8. Mail-Grundlagen. Posteingang
 sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
Version 1.0 Datum 05.06.2008. 1. Anmeldung... 2
 Anmeldung Wochenplatzbörse Spiez Version 1.0 Datum 05.06.2008 Ersteller Oester Emanuel Inhaltsverzeichnis 1. Anmeldung... 2 1.1. Anmeldeseite... 2 1.2. Anmeldung / Registrierung... 4 1.3. Bestätigungs-Email...
Anmeldung Wochenplatzbörse Spiez Version 1.0 Datum 05.06.2008 Ersteller Oester Emanuel Inhaltsverzeichnis 1. Anmeldung... 2 1.1. Anmeldeseite... 2 1.2. Anmeldung / Registrierung... 4 1.3. Bestätigungs-Email...
5. Isolierungsmaßnahmen
 5. Isolierungsmaßnahmen 5.1 Übertragungsweg-abhängige Isolierungsmaßnahmen Übertragungsweg-abhängige Isolierungsmaßnahmen Institut für Hygiene und Umweltmedizin Der Begriff Isolierung (engl. isolation)
5. Isolierungsmaßnahmen 5.1 Übertragungsweg-abhängige Isolierungsmaßnahmen Übertragungsweg-abhängige Isolierungsmaßnahmen Institut für Hygiene und Umweltmedizin Der Begriff Isolierung (engl. isolation)
Hygienemaßnahmen bei 3 und 4 MRGN Erreger in der stationären und ambulanten Versorgung
 Hygienemaßnahmen bei 3 und 4 MRGN Erreger in der stationären und ambulanten Versorgung Vortrag von Nicole Demuth-Werner HFK in der Kath. Krankenhaus Hagen gem. GmbH 2 3 Was Sie erwartet: Erregervorstellung
Hygienemaßnahmen bei 3 und 4 MRGN Erreger in der stationären und ambulanten Versorgung Vortrag von Nicole Demuth-Werner HFK in der Kath. Krankenhaus Hagen gem. GmbH 2 3 Was Sie erwartet: Erregervorstellung
Bitte leiten Sie diese Information an die zuständige Fachabteilung, bzw. die Anwender der oben genannten Produkte weiter.
 3. April 2013 cobas Software v1.x und v2.0 auf den Systemen cobas 4800 und cobas z 480: Seltener Channel Shift bei der Fluoreszenzauswertung führt zu invaliden Ergebnissen oder
3. April 2013 cobas Software v1.x und v2.0 auf den Systemen cobas 4800 und cobas z 480: Seltener Channel Shift bei der Fluoreszenzauswertung führt zu invaliden Ergebnissen oder
Liste der gültigen Prüfverfahren für den akkreditierten Bereich "Abteilung Infektionsdiagnostik", Basel
 Sämtliche n können täglich durchgeführt werden. nliste des EDI) 1 Adenovirus EDTA-Blut, Urin,, Konjuktivalabstrich, Liquor (Kit) PCR Genom qn E 195 2 Adenovirus Ig Serum KBR qn M 28 3 Adeno- und Rotavirus,
Sämtliche n können täglich durchgeführt werden. nliste des EDI) 1 Adenovirus EDTA-Blut, Urin,, Konjuktivalabstrich, Liquor (Kit) PCR Genom qn E 195 2 Adenovirus Ig Serum KBR qn M 28 3 Adeno- und Rotavirus,
Bedienungsanleitung. Matthias Haasler. Version 0.4. für die Arbeit mit der Gemeinde-Homepage der Paulus-Kirchengemeinde Tempelhof
 Bedienungsanleitung für die Arbeit mit der Gemeinde-Homepage der Paulus-Kirchengemeinde Tempelhof Matthias Haasler Version 0.4 Webadministrator, email: webadmin@rundkirche.de Inhaltsverzeichnis 1 Einführung
Bedienungsanleitung für die Arbeit mit der Gemeinde-Homepage der Paulus-Kirchengemeinde Tempelhof Matthias Haasler Version 0.4 Webadministrator, email: webadmin@rundkirche.de Inhaltsverzeichnis 1 Einführung
IN-OUT WEB ONLINE KALKULATIONS- UND BESTELLPROGRAMM BEDIENUNGSANLEITUNG
 IN-OUT WEB ONLINE KALKULATIONS- UND BESTELLPROGRAMM BEDIENUNGSANLEITUNG 1. Anmeldung Das Programm ist ein Online-Programm. Schreiben Sie den folgenden Link in Ihrem Browser ein: webkalkulator.eu/inoutweb,
IN-OUT WEB ONLINE KALKULATIONS- UND BESTELLPROGRAMM BEDIENUNGSANLEITUNG 1. Anmeldung Das Programm ist ein Online-Programm. Schreiben Sie den folgenden Link in Ihrem Browser ein: webkalkulator.eu/inoutweb,
Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren
 Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren Ziel der Anleitung Sie möchten ein modernes Firewallprogramm für Ihren Computer installieren, um gegen
Anleitung zum Computercheck Windows Firewall aktivieren oder eine kostenlose Firewall installieren Ziel der Anleitung Sie möchten ein modernes Firewallprogramm für Ihren Computer installieren, um gegen
Registrierung für eine Senioren IPIN www.itftennis.com/ipin. Ab 17. Mai 2011 können sich Spieler für eine Senioren IPIN (Lizenz) registrieren.
 Registrierung für eine Senioren IPIN www.itftennis.com/ipin Ab 17. Mai 2011 können sich Spieler für eine Senioren IPIN (Lizenz) registrieren. Um ab 2012 an den Turnieren des ITF Seniors Circuits teilnehmen
Registrierung für eine Senioren IPIN www.itftennis.com/ipin Ab 17. Mai 2011 können sich Spieler für eine Senioren IPIN (Lizenz) registrieren. Um ab 2012 an den Turnieren des ITF Seniors Circuits teilnehmen
Schritt für Schritt zur Krankenstandsstatistik
 Schritt für Schritt zur Krankenstandsstatistik Eine Anleitung zur Nutzung der Excel-Tabellen zur Erhebung des Krankenstands. Entwickelt durch: Kooperationsprojekt Arbeitsschutz in der ambulanten Pflege
Schritt für Schritt zur Krankenstandsstatistik Eine Anleitung zur Nutzung der Excel-Tabellen zur Erhebung des Krankenstands. Entwickelt durch: Kooperationsprojekt Arbeitsschutz in der ambulanten Pflege
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Internationales Altkatholisches Laienforum
 Internationales Altkatholisches Laienforum Schritt für Schritt Anleitung für die Einrichtung eines Accounts auf admin.laienforum.info Hier erklären wir, wie ein Account im registrierten Bereich eingerichtet
Internationales Altkatholisches Laienforum Schritt für Schritt Anleitung für die Einrichtung eines Accounts auf admin.laienforum.info Hier erklären wir, wie ein Account im registrierten Bereich eingerichtet
Leitfaden für die ersten Schritte im INIT-eCampus. mailto: ecampusadmin@init-software.de
 Leitfaden für die ersten Schritte im INIT-eCampus Version 1.0 (15.05.2013) Autor: INIT ecampus-team mailto: ecampusadmin@init-software.de Inhaltsverzeichnis Inhalt Leitfaden für die ersten Schritte im
Leitfaden für die ersten Schritte im INIT-eCampus Version 1.0 (15.05.2013) Autor: INIT ecampus-team mailto: ecampusadmin@init-software.de Inhaltsverzeichnis Inhalt Leitfaden für die ersten Schritte im
Online Schulung Anmerkungen zur Durchführung
 Online Schulung Anmerkungen zur Durchführung 1.0 Einleitung Vielen Dank, dass Sie sich für die Online Schulung von SoloProtect entschieden haben. Nachfolgend finden Sie Informationen für Identicomnutzer
Online Schulung Anmerkungen zur Durchführung 1.0 Einleitung Vielen Dank, dass Sie sich für die Online Schulung von SoloProtect entschieden haben. Nachfolgend finden Sie Informationen für Identicomnutzer
Ruhr-Universitä t Bochum. Modellregion West. Akute und chronische Hepatitis. Medizinische Universitätsklinik
 Ruhr-Universitä t Bochum Modellregion West Akute und chronische Hepatitis Medizinische Universitätsklinik HAV EBV CMV,... Ausheilung ASH DILD HBV HDV HCV Akute Hepatitis Chron. Hepatitis Zirrhose HCC,
Ruhr-Universitä t Bochum Modellregion West Akute und chronische Hepatitis Medizinische Universitätsklinik HAV EBV CMV,... Ausheilung ASH DILD HBV HDV HCV Akute Hepatitis Chron. Hepatitis Zirrhose HCC,
Juni Vorauswertung zu den virologischen Ringversuchen. Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel
 Juni 2017 zu den virologischen en Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Juni 2017 zu den virologischen en Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Hilfe zum Service Einzug
 Hilfe zum Service Einzug Schritt 1/8 Auswahl der vom Einzug betroffenen Verbrauchsstelle Bitte geben Sie uns das Datum Ihres Einzugs bekannt. Sie können das Datum entweder direkt in das Feld Einzugsdatum
Hilfe zum Service Einzug Schritt 1/8 Auswahl der vom Einzug betroffenen Verbrauchsstelle Bitte geben Sie uns das Datum Ihres Einzugs bekannt. Sie können das Datum entweder direkt in das Feld Einzugsdatum
