Lösungsblatt 13 zur Experimentalphysik I
|
|
|
- Karin Kneller
- vor 7 Jahren
- Abrufe
Transkript
1 Lösungsblatt 3 zur Exerimentalhysik I Sommersemester 04 - Übungsblatt 3 Letzte Hinweise zur Klausur: Die Klausur ist am Donnerstag, dem 3. Juli von 5:30 bis ca. 8:00 Uhr in S (In dem Hörsaal der orlesung). Thema ist der Stoff aus der orlesung und den Übungen. Erlaubte Hilfsmittel sind ein beidseitig beschriebenes DIN A4 Blatt als Formelsammlung sowie ein nicht rogrammierbarer Taschenrechner. Bitte bringen Sie daneben auch ausreichend Stifte und Schreibaier (mindestens 8 Blatt, da Sie jede Aufgabe auf einem searatem Blatt abgeben müssen) und einen Lichtbildausweis mit. Unsere Tutoren haben vor der Klausur noch Sondersrechstunden eingerichtet. Die Srechstunden von Alexander Bruns sind am Mittwoch 3.07 ab 5:00 und Montag 8.07 ab 3:00 jeweils im LZP. Die Srechstunden von Martin Baumann sind wie gehabt Donnerstags um 3:00 in S Srechstunden mit Daniel Kiefer und Maximilian Schilder können Sie er vereinbaren. Ansonsten wünsche ich Ihnen viel Erfolg bei der orbereitung. Hinweis: Da am.07. und.07. keine Übungen mehr stattfinden, gibt es in diesem Blatt keine Hausaufgaben. Sie werden in der Präsenzübung nicht alle Aufgaben schaffen. Lösen Sie die restlichen Aufgaben trotzdem zu Hause und vergleichen Sie Ihre Ergebnisse mit der Musterlösung, denn der Stoff dieses Blattes ist noch Klausurrelevant. Falls Sie danach noch Fragen haben, nutzen Sie die Srechstunden. Aufgabe 3. Neuer Sauerstoff Hubert lässt eine bis auf Atmoshärendruck (03 hpa) entleerte Sauerstoffflasche mit einem Innenvolumen von i bei einer Temeratur von 8 C isotherm neu befüllen. Die Füllung ist ein ideales Gas und würde bei Atmoshärendruck 6 m 3 einnehmen. a) Welcher Druck herrscht in der Flasche nach der Befüllung? N 03 hpa 6000 l b) Welche mechanische Arbeit muss die Firma zur Befüllung aufwenden? 5,95 Bar de d N d de N d E E N ln( ) ln( ) ln( ) E 0300 N m 6 m 3 ln c) Um wie viel nimmt die Masse der Flasche dabei zu? 6000 l 3,045 MJ M N m (v ) 0300 N 5,96 m3 0,03 m, J 0, ,03 7,958 K 9,5 K 6,0 0 3 d) Welches ist die wahrscheinlichste Geschwindigkeit der O -Moleküle in der Flasche? v ml kb T m, J K 9,5 K 0,03 6, ,9 m s e) Welcher Druck herrscht in der Flasche, wenn man den Sauerstoff als reales Gas betrachtet? Welcher Anteil entfällt auf das Eigenvolumen? Pa m6 5 m3 a 0,378 ; b 3,8 0 + a N ( bn) N k B T N a N a bn b 0300 Pa 0,378 m Pa 3, l 6,0 0 3, K J 9,5 K Pa m l (6,0 0 3 ) b a 0300 Pa, J K 9,5 K 35, Bar
2 Übungsblatt 3 zur Exerimentalhysik I Name, orname: Aufgabe 3. Wasserdamf Welches olumen nimmt Liter Wasser unter Normaldruck nach dem erdamfen ein? N k b T M k b T m, J K 373,5 K, m 3,700 m 3 Aufgabe 3.3 Eine Ballonfahrt, die ist Lustig Max und Moritz Taube Fridolin hat Flugangst und kann deswegen nicht alleine Fliegen. Damit Fridolin die Welt trotzdem von oben sehen kann haben Max und Moritz einen gelben quaderförmigen Ballon mit den Maßen 6 x 5 x 6 m 3 gebaut und wollen damit abheben. Die Temeratur beträgt 300 K und der Druck dank schönem Wetter 030 mbar. a) Wie viele e und wie viele Luft befinden sich in dem Ballon? Nehmen Sie an, dass Luft zu 78% aus Stickstoff (m 4,0 u), zu % aus Sauerstoff (m 6 u) und zu % aus Argon (m 39,95 u) besteht. N Pa 80 m3, J K 300 K 4, m Luft m x N m N + x O m O + x Ar m Ar x N m N + x O m O + x Ar m Ar 78% 4,0 u + % 6,00 u + % 39,95 u 8,98 u M mn 8,98 g ,4 b) Kann der Ballon abheben, wenn Max und Moritz die Innentemeratur des Ballons mit ihrem umgebauten Grill um 50 C erhöhen können? eranschlagen Sie für das Gewicht von Max, Moritz, Fridolin und dem Ballon 50, sowie 3 für den Grill und 7 für den Brennstoff A Paraffin Grillanzünder. M m N m m T T N M T 5,4 300 K 30,78 T T T 350 K So sehr Max und Moritz auch wedeln. Der Auftrieb reicht nicht und der Ballon bleibt am Boden. c) Wie viel darf der Ballon mit Antrieb, Max und Moritz wiegen, wenn Max und Moritz den Ballon nicht erhitzen und stattdessen komlett mit Wasserstoff füllen? M N m m H ,98 g, 0 g 00,4 Der Ballon hebt sogar, dann noch ab, wenn Max und Moritz ihre komlette Grillausrüstung mitnehmen. d) Mit welchen Gasen könnten Max und Moritz ihren Ballon ebenfalls füllen und wie viel kann er dann tragen? Mit welchen Gasen kann der Ballon abheben? Gas Summenformel m M Bemerkung Wasserstoff H,0 g 00,4 Bestes Ballongas, aber brennbar Helium He 4,00 g 85,69 In der Praxis verwendetes Gas Methan CH 4 6,05 g 96, Brennbar Ammoniak H 3 N 7,04 g 88,76 Ätzend, giftig Flourwasserstoff HF 0,0 g 66,68 Ätzend, giftig Neon Ne 0,8 g 65,4 Mäßiges Ballongas Ethin C H 6,04 g,85 Brennbar Blausäure HCN 7,03 g 4,50 Sehr giftig Kohlenmonoxid CO 8,0 g 7, Brennbar, giftig Stickstoff N 8,0 g 7,4 Schlechtes Ballongas Ethen C H 4 8,06 g 6,84 Brennbar Der Ballon hebt mit Wasserstoff und Helium ab. Da Wasserstoff aber ein brennbares Gas ist und der Ballon bei dem kleinsten Funken in die Luft fliegen würde, ist Helium das Gas der Wahl.
3 Übungsblatt 3 zur Exerimentalhysik I Name, orname: Aufgabe 3.4 Kai macht Eistee Da Kai zu lange an seinen Physikhausaufgaben gerechnet hat, hat er vergessen den Eistee für seine Freunde kalt zu stellen. Er gibt 0,5 Eis mit einer Temeratur von -0 C in seine Jumbo Thermoskanne und 3 Liter Tee mit einer Temeratur von 0 C. Welche Temeratur und Phase hat das Gemisch nachdem sich ein thermisches Gleichgewicht eingestellt hat. Da der Tee ungesüßt ist, können Sie ihn in guter Näherung als Wasser betrachten.. Phase: Das Eis erwärmt sich T. Phase T Anfang + T Wasser T Anfang + Q Wasser 0 C - 0 C 0,5 0 J K J K. Phase: Das Eis schmilzt T. Phase T. Phase 9, C Q Eis T. Phase M Eis L Eis 3. Phase: Mischen von Eiswasser und Tee T Ende M Wasser T. Phase +M Eis T Eis M Wasser +M Eis 3 5,87 C+0,5 0 C 3 + 0,5 T Anfang 5,03 C 9, C Q Eis T Anfang T Eis M Eis c Eis kj 0,5 333 J K 5,87 C Aufgabe 3.5 Benjamins Motor Um mit seinem Fahrrad besser voran zu kommen hat sich Benjamin folgende Wärmekraftmaschine gebaut: Ein ideales Gas, sagen wir mal Helium, das bei 900 K unter dem Anfangsdruck von, MPa steht, wird zunächst isotherm von Litern auf Litern exandiert. Im zweiten Schritt wird es isobar auf das Ausgangsvolumen komrimiert und im dritten und letzten Schritt isochor zurück in den Ausgangszustand gebracht. a) Zeichnen Sie das - -Diagramm dieses Prozesses. Image to be done. b) Berechnen Sie die in einem Zyklus aus dem Wärmereservoir aufgenommene Wärme und die abgegebene Arbeit. W d 0 0 P 0 ln( ) 0 0 N 0 d d N ln( ) ln( 0 ) + N kb T 0 ln( 0,00 m 3, MJ l ) l 300 J m 3 l l Q Q + Q + Q 3 Q + Q 3 (In Schritt wird keine Wärme aus den Wärmereservoir entnommen, dafür aber Wärme an das Kältereservoir abgegeben.) Q d + T 0 N k c Schritt dt B T f d + N k B dt N ln + f N k 0 B T0 T 0 T T 0 0 ln + f T 0 T 0 0 ln + f 0 MJ 0,00 m3, 0 0 m ln l 3 l + 3 l l 7300 J c) Welche Effizienz hat Benjamins Motor? ergleichen Sie diese mit der Effizienz des Carnot-Prozesses. η W 300 J 3,5%, ε η η 3,5% Q 7300 J η Carnot T 5 37,8% T0 6 Der Carnot-Prozess ist fast drei mal so effizient. Benjamins Motor hat also noch Otimierungsotential. d) Was würde sich ändern, wenn Benjamin statt Helium ( f 3) Kohlendioxid ( f 3) genommen hätte? An der abgegebenen Arbeit W ändert sich nichts, da diese durch die Mechanik gegeben ist und nicht von der Anzahl der Freiheitsgrade abhängt. Die aufgenommene Wärme ändert sich jedoch zu: 3
4 Übungsblatt 3 zur Exerimentalhysik I Name, orname: Q 0 0 ln + f 0 0 η W 300 J 3,9%, ε η η Q 7300 J η Carnot T 0,00 m 3, MJ m ln l 3 l + 3 l l J und damit sind 5,95% 3,9% 5 T0 6 Mit Kohlendioxid läuft Benjamins Motor also noch schlechter, abgesehen davon, dass T so niedrig ist, dass das Kohlendioxid gefrieren würde. Aufgabe 3.6 Barometrische Höhenformel Leiten Sie die barometrische Höhenformel unter Berücksichtigung des inhomogenen Schwerefelds der Erde (Gravitationsgesetz) her. Setzen Sie dazu an, der Druck in der Höhe h gleich der Schwerkraft ro Fläche ist, welche die Luft darüber aufbaut. Sie dürfen annehmen, dass die Atmoshäre homogen aus Atomen / Molekülen der Masse m besteht und die Temeratur T hat. Die Masse der Luft ist gegenüber der Masse der Erde vernachlässigbar. Man betrachte eine kleine Luftsäule der Fläche da und der Höhe dr. Durch den Druck der oberen Luftschichten liegt auf der Luftsäule eine Kraft df da. Unterhalb der Luftsäule wirkt zusätzlich die Schwerkraft der Luftsäule selbst. Diese ist d F dm a Gravitation ρdadr G m Erde r dadr (r) m Molekül G m Erde. Hieraus ergibt sich durch Division durch r da die Differentialgleichung d (r)g m Molekül m Erde dr. Durch Trennung der ariablen erhält man: r m G Erde dr d G m Erde k r B T ln() e r C m Molekül r m Molekül Mit der Bedingung, dass auf der Erdoberfläche (r 0 ) Normaldruck ( 0 ) herrscht erhält man (r 0 ) 0 C 0 e r (r) 0 e G m erde m Molekül r 0 r a) Welcher Druck herrscht im unendlichen? Was bedeutet es, dass dieser nicht 0 ist? P( ) P 0 e G m erde m Molekül 0 r 0 P 0 e G m erde m Molekül r 0 > 0 Das bedeutet, dass die Erde ständig Gas verliert, wenn der Weltraum leer ist. b) Berechnen Sie den Druck im unendlichen konkret mit folgenden Werten: G 6,674 0 m s m erde 5, k B, J K P( ) 03 hpa ex m3 6,674 0 s 5, ,080, J K 300 K m T 300 K r Erde 6, m 03 hpa e 703,5, hpa Aufgabe 3.7 Föhn Der Wind weht 0 C warme mit Wasser gesättigte Luft über einen Berg. Dabei kühlt sie sich auf 3 ab. Das überschüssige Wasser regnet über dem Berg ab. Auf der Rückseite des Berges weht die Luft wieder ins Tal hinab und erwärmt sich dabei wieder adiabatisch. Der Druck im Tal beträgt 000 hpa. Nehmen Sie Luft als ideales Gas mit 7 Freiheitsgraden an. 4 a) Der Sättigungsdamfdruck des Wassers ist gegeben durch (T) a e bt. Bestimmen Sie die Koeffizienten a und b aus dem Siedeunkt ((00 C) 03 hpa) und dem Trielunkt ((0,0 C) 6, hpa) des Wassers. Wie viel Wasser asst bei 0 C in einen Kubikmeter? ae bt aebt ae bt e b(t T ) b ln P P T T a e bt 6, hpa e 0,05 K 3,6 K 5, hpa M Tal N m Molekül m Molekül,58 g ae bt m Molekül ln 03 hpa 6, hpa 00 C 0,0 C 0,050 K 5,3 0 4 N m e 0,050 K 93,5 K m 3 8,0 g, J K 93,5 K b) Wie viel Wasser ist es auf dem Berg? Die Tatsache, dass sich die Luft beim Aufstieg ausdehnt dürfen Sie für diesen Teil der Aufgabe vernachlässigen. Wie viel latente Wärme wird bei dem Prozess frei?
5 Übungsblatt 3 zur Exerimentalhysik I Name, orname: M Berg ae bt m Molekül Q M L 3,538 g 56 J g 5,3 0 4 N m e 0,050 K 86,5 K 798 J m 3 8,0 g, J K 86,5 K 9,04 g c) Wie warm ist die Luft wenn sie wieder im Tal ankommt und welche relative Feuchte hat sie? T Q c Q f k B N f H rel M Tatsächlich M Potentiell QT ae b m Molekül Berg TTal ae bt Tal m Molekül Tal 798 J 93,5 K 0 5 J m 3 m 3 6,68 C T 0 C + 6,68 C 6,68 C e b( T Tal) 99,83 K 86,5 K e0,05 K (3 C 6,68 C) 5,08% d) Berechnen Sie den Luftdruck auf dem Berg und schließen Sie mit der barometrischen Höhenformel aus Aufgabe 3.6 auf die Höhe des Berges. κ + f T T 0 e G m erde m Molekül r 0 r r h r r 0 r hpa 9 N kb T ,5 K 99,83 K 7 N kb T 9 7 const. T 9 9 ln 0 r 0 TTal ln 6367 km, m 80,5 hpa 6367 km r 0 r 9 T 9 9 ln, K J 93,5 K m 6,674 0 m3 s 5, , T T T Tal ln 99,3 K 86,5 K r 0 Hier müsste man in die Formel eigentlich ein T(h) einsetzen, bzw. die barometrische Höhenformel für eine adiabatische Atmoshäre neu herleiten. Dies srengt aber den Rahmen der Aufgabe, daher ist es in Ordnung T als konstant zu nähern. 5
Ferienkurs Experimentalphysik 2 - Mittwoch-Übungsblatt. 1 Aufgabe: Adiabatengleichung fürs Ideale Gas
 Aufgabe: Gasrozess Ferienkurs Exerimentalhysik - Mittwoch-Übungsblatt 1 Aufgabe: Adiabatengleichung fürs Ideale Gas Aus dem 1. HS und den Wärmekaazitäten c und c olgt zusammen mit dem Adiabatenkoeffizienten
Aufgabe: Gasrozess Ferienkurs Exerimentalhysik - Mittwoch-Übungsblatt 1 Aufgabe: Adiabatengleichung fürs Ideale Gas Aus dem 1. HS und den Wärmekaazitäten c und c olgt zusammen mit dem Adiabatenkoeffizienten
Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt
 1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Übungen zu Experimentalphysik 2 für MSE
 Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
1. Klausur zur Vorlesung Physikalische Chemie I
 1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
Physikübungsaufgaben Institut für math.-nat. Grundlagen (IfG)
 Datei Alugefaess.docx Kapitel Thermodynamik ; thermische Ausdehnung Titel Aluminiumgefäß randvoll gefüllt Hinweise: Orear: Kap. 12.4, 12.5, Hering: Kap. 3.3.1 Dobrinski: Kap. 2.3 Alonso Finn: Kap. 13.7-9
Datei Alugefaess.docx Kapitel Thermodynamik ; thermische Ausdehnung Titel Aluminiumgefäß randvoll gefüllt Hinweise: Orear: Kap. 12.4, 12.5, Hering: Kap. 3.3.1 Dobrinski: Kap. 2.3 Alonso Finn: Kap. 13.7-9
Vorbemerkung. [disclaimer]
![Vorbemerkung. [disclaimer] Vorbemerkung. [disclaimer]](/thumbs/97/130802699.jpg) orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke)
 Freie Universität Berlin W 006/007 Fachbereich Physik 8..006 tatistische Physik - heorie der Wärme (PD Dr. M. Falcke) Übungsblatt 9: hermodynamische Identitäten, hermische/kalorische Zustandsgleichung,
Freie Universität Berlin W 006/007 Fachbereich Physik 8..006 tatistische Physik - heorie der Wärme (PD Dr. M. Falcke) Übungsblatt 9: hermodynamische Identitäten, hermische/kalorische Zustandsgleichung,
T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 8 Lösungsvorschlag
 T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
Aufgaben zur Wärmelehre
 Aufgaben zur Wärmelehre 1. Ein falsch kalibriertes Quecksilberthermometer zeigt -5 C eingetaucht im schmelzenden Eis und 103 C im kochenden Wasser. Welche ist die richtige Temperatur, wenn das Thermometer
Aufgaben zur Wärmelehre 1. Ein falsch kalibriertes Quecksilberthermometer zeigt -5 C eingetaucht im schmelzenden Eis und 103 C im kochenden Wasser. Welche ist die richtige Temperatur, wenn das Thermometer
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler
 TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Zur Erinnerung. Wärmetransport durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung. Planck sches Strahlungsgesetz. Stefan-Boltzman-Gesetz
 Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
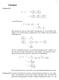 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
Institut für Thermodynamik Prof. Dr. rer. nat. M. Pfitzner Thermodynamik I - Lösung 8. Aufgabe kg Luft (perfektes Gas: κ = 1,4 ; R L = 287 J
 Aufgabe 3 0 kg Luft perfektes Gas: κ,4 ; R L 287 J von T 293 K und p 0,96 bar werden auf 0 bar verdichtet. Dies soll. isochor 2. isotherm 3. reversibel adiabat und 4. polytrop mit n,3 geschehen. a Skizzieren
Aufgabe 3 0 kg Luft perfektes Gas: κ,4 ; R L 287 J von T 293 K und p 0,96 bar werden auf 0 bar verdichtet. Dies soll. isochor 2. isotherm 3. reversibel adiabat und 4. polytrop mit n,3 geschehen. a Skizzieren
(b) Schritt I: freie adiabatische Expansion, also ist δw = 0, δq = 0 und damit T 2 = T 1. Folglich ist nach 1. Hauptsatz auch U = 0.
 3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
Physik 2 Hydrologen et al., SoSe 2013 Lösungen 3. Übung (KW 19/20) Carnot-Wärmekraftmaschine )
 3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
E2: Wärmelehre und Elektromagnetismus 8. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 8. Vorlesung 3.5.2018 Heute: - Boltzmann-Verteilung - Wärmekraftmaschinen - Carnot-Prozess und Wirkungsgrad - Kraftwärmemaschinen Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de
E2: Wärmelehre und Elektromagnetismus 8. Vorlesung 3.5.2018 Heute: - Boltzmann-Verteilung - Wärmekraftmaschinen - Carnot-Prozess und Wirkungsgrad - Kraftwärmemaschinen Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/hermodynamik Wintersemester 7 ladimir Dyakonov #3 am..7 Folien unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html.3 Ideales Gas Exerimentelle Bestimmung der
Einführung in die Physik I Wärmelehre/hermodynamik Wintersemester 7 ladimir Dyakonov #3 am..7 Folien unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html.3 Ideales Gas Exerimentelle Bestimmung der
Thermodynamik I Klausur 1
 Aufgabenteil / 100 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
Aufgabenteil / 100 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
Teilnehmer-Nr: Integrierter Kurs I. 2. Klausur, WiSe 2010/ März 2011
 Integrierter Kurs I 2. Klausur, WiSe 2010/2011 03. März 2011 Name: Gruppenleiter: Aufgabe Punkte 1 / 5 2 /16 3 /10 4 /13 5 /10 6 /12 7 / 8 8 / 6 insgesamt (max. 80) 1. Gravitationskraft (5 Punkte) Im Jahr
Integrierter Kurs I 2. Klausur, WiSe 2010/2011 03. März 2011 Name: Gruppenleiter: Aufgabe Punkte 1 / 5 2 /16 3 /10 4 /13 5 /10 6 /12 7 / 8 8 / 6 insgesamt (max. 80) 1. Gravitationskraft (5 Punkte) Im Jahr
Aufgaben zur Experimentalphysik II: Thermodynamik
 Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Thermodynamik 1 Klausur 03. März Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen.
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 03. März 2010 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 03. März 2010 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Vakuum - Mehr als Nichts? Was ist Vakuum? Luftdruck Vakuumpumpen Druckmessung Anwendungen
 Zum 400. Geburtstag von Otto von Guericke Vakuum - Mehr als Nichts? Was ist Vakuum? Luftdruck Vakuumpumpen Druckmessung Anwendungen Was ist Vakuum? Vakuum: Luftdruck geringer als Normaldruck Druck p
Zum 400. Geburtstag von Otto von Guericke Vakuum - Mehr als Nichts? Was ist Vakuum? Luftdruck Vakuumpumpen Druckmessung Anwendungen Was ist Vakuum? Vakuum: Luftdruck geringer als Normaldruck Druck p
Musterlösung Übung 3
 Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Die zugeführte Wärmemenge bei isochorer Zustandsänderung berechnet sich aus
 Ü 9. Aufheizung einer Preßluftflasche Eine Preßluftflasche, in der sich.84 kg Luft bei einem Druck on.74 bar und einer Temeratur on T 0 C befinden, heizt sich durch Sonneneinstrahlung auf 98 C auf. Gesucht
Ü 9. Aufheizung einer Preßluftflasche Eine Preßluftflasche, in der sich.84 kg Luft bei einem Druck on.74 bar und einer Temeratur on T 0 C befinden, heizt sich durch Sonneneinstrahlung auf 98 C auf. Gesucht
Allgemeine Gasgleichung und technische Anwendungen
 Allgemeine Gasgleichung und technische Anwendungen Ziele i.allgemeine Gasgleichung: Darstellung in Diagrammen: Begriffsdefinitionen : Iso bar chor them Adiabatische Zustandsänderung Kreisprozess prinzipiell:
Allgemeine Gasgleichung und technische Anwendungen Ziele i.allgemeine Gasgleichung: Darstellung in Diagrammen: Begriffsdefinitionen : Iso bar chor them Adiabatische Zustandsänderung Kreisprozess prinzipiell:
m T 1 0.5kg 8.6K = 7535 m T 2 0.5kg 10.4K = 6923 J
 3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
Thermodynamik 1 Klausur 06. März 2015
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 06. März 2015 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung:
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 06. März 2015 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung:
Versuch: Sieden durch Abkühlen
 ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
Thermodynamik 1 Klausur 08. September 2016
 Thermodynamik 1 Klausur 08. September 2016 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten Alle Unterlagen zur Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Thermodynamik 1 Klausur 08. September 2016 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten Alle Unterlagen zur Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
Thermodynamik 1 Klausur 02. März Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen.
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 02. März 2011 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 02. März 2011 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Physikalische Chemie I
 M.Bredol / MP Physikalische Chemie I / 10.3.16 1 Physikalische Chemie I Nachname orname Matrikel Aufgabe Punkte erreicht Note 1 20 2 20 3 20 4 22 5 18 Summe: 100 1. Gegeben seien 20 g Kohlendioxid, die
M.Bredol / MP Physikalische Chemie I / 10.3.16 1 Physikalische Chemie I Nachname orname Matrikel Aufgabe Punkte erreicht Note 1 20 2 20 3 20 4 22 5 18 Summe: 100 1. Gegeben seien 20 g Kohlendioxid, die
Thermodynamik 2 Klausur 23. Februar 2012
 Thermodynamik 2 Klausur 23. Februar 2012 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Thermodynamik 2 Klausur 23. Februar 2012 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Lösung. Nachholklausur zur Vorlesung Physikalische Chemie I - Sommersemester 2002
 Lösung Nachholklausur zur orlesung Physikalische hemie I - Sommersemester 00 6. Oktober 00, 9 5-5 Uhr Hineise - Bitte Namen auf jedes Blatt schreiben. - Auch Blatt-Rückseiten beschreiben. - Ggf. eitere
Lösung Nachholklausur zur orlesung Physikalische hemie I - Sommersemester 00 6. Oktober 00, 9 5-5 Uhr Hineise - Bitte Namen auf jedes Blatt schreiben. - Auch Blatt-Rückseiten beschreiben. - Ggf. eitere
Aufgaben zum Stirlingschen Kreisprozess Ein Stirling-Motor arbeite mit 50 g Luft ( M= 30g mol 1 )zwischen den Temperaturen = 350 C und T3
 Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Übung 2. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases. f=5 Translation + Rotation. f=7 Translation + Rotation +Vibration. Wiederholung
 1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
Thermodynamik 1 Klausur, 3. August Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen.
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur, 3. August 2009 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur, 3. August 2009 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Mitschrift Thermodynamik
 Mitschrift hermodynamik Herleitung für den Gasdruck Berechnung des oberen Kreisradius d cosϕ dϕ dψ d N eilchen im Gesamtvolumen dn d N Aufschlagswahrscheinlichkeit eines eilchens Fläche df df sinϕ Gesamte
Mitschrift hermodynamik Herleitung für den Gasdruck Berechnung des oberen Kreisradius d cosϕ dϕ dψ d N eilchen im Gesamtvolumen dn d N Aufschlagswahrscheinlichkeit eines eilchens Fläche df df sinϕ Gesamte
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc.
 Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc. Angaben zur Person: (bitte leserlich und in Druckbuchstaben) Name, Vorname: Geburtsdatum und ort: Matrikelnummer: Studienfach,
Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc. Angaben zur Person: (bitte leserlich und in Druckbuchstaben) Name, Vorname: Geburtsdatum und ort: Matrikelnummer: Studienfach,
Thermodynamik 1 Klausur 01. August 2011
 Thermodynamik 1 Klausur 01. August 2011 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als
Thermodynamik 1 Klausur 01. August 2011 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als
Klausur zur Vorlesung Thermodynamik
 Institut für Thermodynamik 18. März 2011 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Institut für Thermodynamik 18. März 2011 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Annahmen: Arbeitsmedium ist Luft, die spezifischen Wärmekapazitäten sind konstant
 Ü 11.1 Nachrechnung eines Otto-ergleichsprozesses (1) Annahmen: Arbeitsmedium ist Luft, die spezifischen Wärmekapazitäten sind konstant Anfangstemperatur T 1 288 K Anfangsdruck p 1 1.013 bar Maximaltemperatur
Ü 11.1 Nachrechnung eines Otto-ergleichsprozesses (1) Annahmen: Arbeitsmedium ist Luft, die spezifischen Wärmekapazitäten sind konstant Anfangstemperatur T 1 288 K Anfangsdruck p 1 1.013 bar Maximaltemperatur
Q i + j. dτ = i. - keine pot. und kin. Energien: depot. - adiabate ZÄ: Q i = 0 - keine technische Arbeit: Ẇ t,j = 0
 Institut für hermodynamik hermodynamik - Formelsammlung. Hauptsätze der hermodynamik (a. Hauptsatz der hermodynamik i. Offenes System de = de pot + de kin + du = i Q i + j Ẇ t,j + ein ṁ ein h tot,ein aus
Institut für hermodynamik hermodynamik - Formelsammlung. Hauptsätze der hermodynamik (a. Hauptsatz der hermodynamik i. Offenes System de = de pot + de kin + du = i Q i + j Ẇ t,j + ein ṁ ein h tot,ein aus
TU-München, Musterlösung. Experimentalphysik II - Ferienkurs Andreas Schindewolf
 TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
4 Hauptsätze der Thermodynamik
 I Wärmelehre -21-4 Hauptsätze der hermodynamik 4.1 Energieformen und Energieumwandlung Innere Energie U Die innere Energie U eines Körpers oder eines Systems ist die gesamte Energie die darin steckt. Es
I Wärmelehre -21-4 Hauptsätze der hermodynamik 4.1 Energieformen und Energieumwandlung Innere Energie U Die innere Energie U eines Körpers oder eines Systems ist die gesamte Energie die darin steckt. Es
Thermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden.
 Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
E2: Wärmelehre und Elektromagnetismus 8. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 8. Vorlesung 3.5.2018 Heute: - Boltzmann-Verteilung - Wärmekraftmaschinen - Kraftwärmemaschinen - Carnot-Prozess und Wirkungsgrad Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de
E2: Wärmelehre und Elektromagnetismus 8. Vorlesung 3.5.2018 Heute: - Boltzmann-Verteilung - Wärmekraftmaschinen - Kraftwärmemaschinen - Carnot-Prozess und Wirkungsgrad Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de
Übungen zu Experimentalphysik 1 für MSE
 Physik-Department LS für Funktionelle Materialien WS 2017/18 Übungen zu Experimentalphysik 1 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. Volker Körstgens, Dr. Neelima Paul, Sebastian Grott, Lucas Kreuzer,
Physik-Department LS für Funktionelle Materialien WS 2017/18 Übungen zu Experimentalphysik 1 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. Volker Körstgens, Dr. Neelima Paul, Sebastian Grott, Lucas Kreuzer,
Thermodynamik I PVK - Tag 2. Nicolas Lanzetti
 Thermodynamik I PVK - Tag 2 Nicolas Lanzetti Nicolas Lanzetti 05.01.2016 1 Heutige Themen Carnot; Wirkungsgrad/Leistungsziffer; Entropie; Erzeugte Entropie; Isentroper Wirkungsgrad; Isentrope Prozesse
Thermodynamik I PVK - Tag 2 Nicolas Lanzetti Nicolas Lanzetti 05.01.2016 1 Heutige Themen Carnot; Wirkungsgrad/Leistungsziffer; Entropie; Erzeugte Entropie; Isentroper Wirkungsgrad; Isentrope Prozesse
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 09. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 09. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 09. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 09. 07. 2007 Klausur Die Klausur
Klausur zur Vorlesung Thermodynamik
 Institut für Thermodynamik 7. März 2014 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Institut für Thermodynamik 7. März 2014 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch. Aufgabenstellung Thermodynamik I SS Aachen, den 22.
 Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch Aufgabenstellung Thermodynamik I SS 2014 Aachen, den 22. September 2014 Bachelorprüfung Thermodynamik I SS 2014 1/4 1 Aufgabe (25 Punkte)
Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch Aufgabenstellung Thermodynamik I SS 2014 Aachen, den 22. September 2014 Bachelorprüfung Thermodynamik I SS 2014 1/4 1 Aufgabe (25 Punkte)
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 ladimir Dyakonov #13 am 30.01.2007 Folien im PDF Format unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 ladimir Dyakonov #13 am 30.01.2007 Folien im PDF Format unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Thermodynamik 1 Klausur 12. März Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen.
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 12. März 2014 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung:
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 12. März 2014 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung:
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik II - Übung 1. Cornelius von Einem
 Thermodynamik II - Übung 1 Cornelius von Einem C. von Einem 05.03.2019 1 Hinweise zu der Übung Name: Cornelius von Einem 2. Semester Master Maschienenbau Mail: Raum: IFW A36 Zeit: Dienstag, 13:15-15:00
Thermodynamik II - Übung 1 Cornelius von Einem C. von Einem 05.03.2019 1 Hinweise zu der Übung Name: Cornelius von Einem 2. Semester Master Maschienenbau Mail: Raum: IFW A36 Zeit: Dienstag, 13:15-15:00
1. Klausur in "Technischer Thermodynamik II" (SoSe2014, ) - VERSION 1 -
 UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Al. Professor Dr.-Ing. K. Sindler. Klausur in "Technischer Thermodynamik II" (SoSe04, 03.06.04) - VERSION - Name: Fachr.: Matr.-Nr.: Es
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Al. Professor Dr.-Ing. K. Sindler. Klausur in "Technischer Thermodynamik II" (SoSe04, 03.06.04) - VERSION - Name: Fachr.: Matr.-Nr.: Es
Institut für Thermodynamik Prof. Dr. rer. nat. M. Pfitzner Thermodynamik I - Lösung 1. Einleitende Fragen
 Einleitende Fragen 1. Was versteht man unter Thermodynamik? Thermodynamik ist die Lehre von den Energieumwandlungen und den Zusammenhängen zwischen den Eigenschaften der Stoffe. 2. Erklären Sie folgende
Einleitende Fragen 1. Was versteht man unter Thermodynamik? Thermodynamik ist die Lehre von den Energieumwandlungen und den Zusammenhängen zwischen den Eigenschaften der Stoffe. 2. Erklären Sie folgende
PC-Übung Nr.3 vom
 PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
II. Wärmelehre. II.2. Die Hauptsätze der Wärmelehre. Physik für Mediziner 1
 II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009)
 Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
Klausur Thermodynamik E2/E2p SoSe 2019 Braun. Formelsammlung Thermodynamik
 Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Kapitel IV Wärmelehre und Thermodynamik
 Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas - makroskopisch e) Das reale Gas / Phasenübergänge f) Das ideale Gas mikroskopisch g)
Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas - makroskopisch e) Das reale Gas / Phasenübergänge f) Das ideale Gas mikroskopisch g)
Thermodynamik I Klausur SS 2010
 Thermodynamik I Klausur 00 Prof. Dr. J. Kuck, Prof. Dr. G. Wilhelms Aufgabenteil / 00 Minuten/eite Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und
Thermodynamik I Klausur 00 Prof. Dr. J. Kuck, Prof. Dr. G. Wilhelms Aufgabenteil / 00 Minuten/eite Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und
Grundlagen der Physik 3 Lösung zu Übungsblatt 1
 Grundlagen der Physik 3 Lösung zu Übungsblatt Daniel Weiss 0. Oktober 200 Inhaltsverzeichnis Aufgabe - Anzahl von Atomen und Molekülen a) ohlensto..................................... 2 b) Helium.......................................
Grundlagen der Physik 3 Lösung zu Übungsblatt Daniel Weiss 0. Oktober 200 Inhaltsverzeichnis Aufgabe - Anzahl von Atomen und Molekülen a) ohlensto..................................... 2 b) Helium.......................................
b ) den mittleren isobaren thermischen Volumenausdehnungskoeffizienten von Ethanol. Hinweis: Zustand 2 t 2 = 80 C = 23, kg m 3
 Aufgabe 26 Ein Pyknometer ist ein Behälter aus Glas mit eingeschliffenem Stopfen, durch den eine kapillarförmige Öffnung führt. Es hat ein sehr genau bestimmtes Volumen und wird zur Dichtebestimmung von
Aufgabe 26 Ein Pyknometer ist ein Behälter aus Glas mit eingeschliffenem Stopfen, durch den eine kapillarförmige Öffnung führt. Es hat ein sehr genau bestimmtes Volumen und wird zur Dichtebestimmung von
Thermodynamik I - Übung 7. Nicolas Lanzetti
 Thermodynamik I - Übung 7 Nicolas Lanzetti Nicolas Lanzetti 13.11.2015 1 Heutige Themen Zusammenfassung letzter Woche; Die Entropie; Die T ds-gleichungen; Die erzeugte Entropie; Isentroper Wirkungsgrad;
Thermodynamik I - Übung 7 Nicolas Lanzetti Nicolas Lanzetti 13.11.2015 1 Heutige Themen Zusammenfassung letzter Woche; Die Entropie; Die T ds-gleichungen; Die erzeugte Entropie; Isentroper Wirkungsgrad;
Fernerkundung der Erdatmosphäre
 Fernerkundung der Erdatmosphäre Dr. Dietrich Feist Max-Planck-Institut für Biogeochemie Jena Max Planck Institut für Biogeochemie Foto: Michael Hielscher Max Planck Institut für
Fernerkundung der Erdatmosphäre Dr. Dietrich Feist Max-Planck-Institut für Biogeochemie Jena Max Planck Institut für Biogeochemie Foto: Michael Hielscher Max Planck Institut für
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
Thermodynamik 1 Klausur 01. März Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen.
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 01. März 2013 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 1 Klausur 01. März 2013 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung:
Thermodynamik 2 Klausur 14. September 2011
 Thermodynamik 2 Klausur 14. September 2011 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Thermodynamik 2 Klausur 14. September 2011 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Technische Universität Hamburg
 NAME, Vorname Studiengang Technische Universität Hamburg ÈÖÓ º Öº¹ÁÒ º Ö Ö Ë Ñ ØÞ Prüfung am 16. 08. 2016 im Fach Technische Thermodynamik II Fragenteil ohne Hilfsmittel erreichbare Punktzahl: 20 Dauer:
NAME, Vorname Studiengang Technische Universität Hamburg ÈÖÓ º Öº¹ÁÒ º Ö Ö Ë Ñ ØÞ Prüfung am 16. 08. 2016 im Fach Technische Thermodynamik II Fragenteil ohne Hilfsmittel erreichbare Punktzahl: 20 Dauer:
Die Reise durch die Atmosphäre
 Die Reise durch die Atmosphäre Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung C2.2 Eigenschaften wichtiger Substanzen und Stoffklassen W1 Ich kann Vorgänge und Phänomene in Natur, Umwelt
Die Reise durch die Atmosphäre Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung C2.2 Eigenschaften wichtiger Substanzen und Stoffklassen W1 Ich kann Vorgänge und Phänomene in Natur, Umwelt
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik - hermodynamische Maschinen - Prof. Dr. Ulrich Hahn WS 2008/09 Folge von Prozessen mit Z Ende = Z Anfang rechtsläufig pro Umlauf verrichtete Arbeit: W r = W + W
Physik III im Studiengang Elektrotechnik - hermodynamische Maschinen - Prof. Dr. Ulrich Hahn WS 2008/09 Folge von Prozessen mit Z Ende = Z Anfang rechtsläufig pro Umlauf verrichtete Arbeit: W r = W + W
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Prof. Dr. U. Schollwöck Sommersemester 2013
 Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
Übungen zu Experimentalphysik 1 für MSE
 Physik-Department LS für Funktionelle Materialien WS 2014/15 Übungen zu Experimentalphysik 1 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. Volker Körstgens, Daniel Moseguí González, Pascal Neibecker, Nitin
Physik-Department LS für Funktionelle Materialien WS 2014/15 Übungen zu Experimentalphysik 1 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. Volker Körstgens, Daniel Moseguí González, Pascal Neibecker, Nitin
Abschlussprüfung an Fachoberschulen im Schuljahr 2002/2003
 Abschlussprüfung an Fachoberschulen im Schuljahr 00/00 Haupttermin: Nach- bzw. Wiederholtermin: 0.09.00 Fachrichtung: Technik Fach: Physik Prüfungsdauer: 10 Minuten Hilfsmittel: Formelsammlung/Tafelwerk
Abschlussprüfung an Fachoberschulen im Schuljahr 00/00 Haupttermin: Nach- bzw. Wiederholtermin: 0.09.00 Fachrichtung: Technik Fach: Physik Prüfungsdauer: 10 Minuten Hilfsmittel: Formelsammlung/Tafelwerk
0.1 Barometrische Höhenformel
 0. Barometrische Höhenformel Da, wie aus den bisherigen Überlegungen hervorgegeangen ist, Gase komressibel sind, kann deren Dichte nicht als konstant angesehen werden. Dies hat Konsequenzen auf den Schweredruck
0. Barometrische Höhenformel Da, wie aus den bisherigen Überlegungen hervorgegeangen ist, Gase komressibel sind, kann deren Dichte nicht als konstant angesehen werden. Dies hat Konsequenzen auf den Schweredruck
Thermodynamik 2 Klausur 19. September 2012
 Thermodynamik 2 Klausur 19. September 2012 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Thermodynamik 2 Klausur 19. September 2012 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
ST Der Stirling-Motor als Wärmekraftmaschine
 ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
Klausur Wärmelehre E2/E2p, SoSe 2012 Braun. Formelsammlung Thermodynamik
 Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Prof. Dr. Peter Vogl, Thomas Eissfeller, Peter Greck. Übung in Thermodynamik und Statistik 4B Blatt 8 (Abgabe Di 3. Juli 2012)
 U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
FAQ Entropie. S = k B ln W. 1.) Ist die Entropie für einen Zustand eindeutig definiert?
 FAQ Entroie S = k B ln W 1.) Ist die Entroie für einen Zustand eindeutig definiert? Antwort: Nein, zumindest nicht in der klassischen Physik. Es sei an die Betrachtung der Ortsraum-Entroie des idealen
FAQ Entroie S = k B ln W 1.) Ist die Entroie für einen Zustand eindeutig definiert? Antwort: Nein, zumindest nicht in der klassischen Physik. Es sei an die Betrachtung der Ortsraum-Entroie des idealen
Heissluftmotor ******
 luftmotor 8.3.302 luftmotor ****** 1 Motivation Ein luft- bzw. Stirlingmotor erzeugt mechanische Arbeit. Dies funktioniert sowohl mit einer Beheizung als auch mit einem Kältebad. Durch Umkehrung der Laufrichtung
luftmotor 8.3.302 luftmotor ****** 1 Motivation Ein luft- bzw. Stirlingmotor erzeugt mechanische Arbeit. Dies funktioniert sowohl mit einer Beheizung als auch mit einem Kältebad. Durch Umkehrung der Laufrichtung
Lösungen zu den Zusatzübungen zur Physik für Ingenieure (Maschinenbau) (WS 13/14)
 Lösungen zu den Zusatzübungen zur hysik für Ingenieure (Maschinenbau) (WS 13/14) rof. W. Meyer Übungsgruppenleiter: A. Berlin & J. Herick (NB 2/28) Zusatzübung (Lösung) alle Angaben ohne Gewähr Zusatzaufgabe
Lösungen zu den Zusatzübungen zur hysik für Ingenieure (Maschinenbau) (WS 13/14) rof. W. Meyer Übungsgruppenleiter: A. Berlin & J. Herick (NB 2/28) Zusatzübung (Lösung) alle Angaben ohne Gewähr Zusatzaufgabe
Probeklausur zur Vorlesung PN I Einführung in die Physik für Chemiker und Biologen Priv. Doz. Dr. P. Gilch
 Name: Martrikelnr.: Semester: Biologie Chemie Probeklausur zur Vorlesung PN I Einführung in die Physik für Chemiker und Biologen Priv. Doz. Dr. P. Gilch 12. 2. 2007 Bitte schreiben Sie Ihren Namen auf
Name: Martrikelnr.: Semester: Biologie Chemie Probeklausur zur Vorlesung PN I Einführung in die Physik für Chemiker und Biologen Priv. Doz. Dr. P. Gilch 12. 2. 2007 Bitte schreiben Sie Ihren Namen auf
Aufgabe 1 - Schiefe Ebene - (10 Punkte)
 - schriftlich Klasse: 4AW (Profil A) - (HuR) Prüfungsdauer: Erlaubte Hilfsmittel: Bemerkungen: 4h Taschenrechner TI-nspire CAS Der Rechner muss im Press-to-Test-Modus sein. Formelsammlung Beginnen Sie
- schriftlich Klasse: 4AW (Profil A) - (HuR) Prüfungsdauer: Erlaubte Hilfsmittel: Bemerkungen: 4h Taschenrechner TI-nspire CAS Der Rechner muss im Press-to-Test-Modus sein. Formelsammlung Beginnen Sie
Klausur Thermodynamik I ( )
 Klausur Thermodynamik I (14.09.2017) Musterlösung Aufgabe 1: 1 Atmosphären-Messsystem a) Stellen Sie die Zustandsänderungen 0 bis 4 in Kammer A in einem p, v - Diagramm dar. 0 1 : adiabate Kompression
Klausur Thermodynamik I (14.09.2017) Musterlösung Aufgabe 1: 1 Atmosphären-Messsystem a) Stellen Sie die Zustandsänderungen 0 bis 4 in Kammer A in einem p, v - Diagramm dar. 0 1 : adiabate Kompression
Klasse : Name : Datum :
 Gasgesetze (Boyle-Mariotte, Gay-Lussac, Amontons) Klasse : Name : Datum : Hinweis: Sämtliche Versuche werden vom Lehrer durchgeführt (Lehrerversuche). Die Protokollierung und Auswertung erfolgt durch den
Gasgesetze (Boyle-Mariotte, Gay-Lussac, Amontons) Klasse : Name : Datum : Hinweis: Sämtliche Versuche werden vom Lehrer durchgeführt (Lehrerversuche). Die Protokollierung und Auswertung erfolgt durch den
Ein Gedankenexperiment:
 Der thermische Wind Ein Gedankenexperiment: Dazu beginnen wir mit einer Luftsäule ule. Ein Gedankenexperiment: Der Fuß der Luftsäule ule befindet sich auf der Erdoberfläche che.. Dort herrscht ein Luftdruck
Der thermische Wind Ein Gedankenexperiment: Dazu beginnen wir mit einer Luftsäule ule. Ein Gedankenexperiment: Der Fuß der Luftsäule ule befindet sich auf der Erdoberfläche che.. Dort herrscht ein Luftdruck
V 1. pdv mit p = = p 0 V 0 ln p 1. m = C H2 O T ln p 1. = P a 150m J 8K ln P a
 2 Lösungen Lösung zu 46. Nutze den 1. Hauptsatz du = Q + W = Q pdv. Bei einem isothermen Prozess ändert sich die innere Energie nicht: du = 0, was wir schon in mehreren Aufgaben zuvor benutzt haben. Also
2 Lösungen Lösung zu 46. Nutze den 1. Hauptsatz du = Q + W = Q pdv. Bei einem isothermen Prozess ändert sich die innere Energie nicht: du = 0, was wir schon in mehreren Aufgaben zuvor benutzt haben. Also
