Thermodynamik 1 Klausur 08. September 2016
|
|
|
- Dörte Förstner
- vor 6 Jahren
- Abrufe
Transkript
1 Thermodynamik 1 Klausur 08. September 2016 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten Alle Unterlagen zur Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen. Geben Sie diese Aufgabenstellung bitte zusammen mit Ihren Lösungsblättern ab. Füllen Sie die Angaben zu Ihrer Person aus und versehen Sie jedes Lösungsblatt mit Ihrem Namen. Name: Vorname: Matrikelnummer: Unterschrift: Angaben zur Korrektur Aufgabe Maximale Punktzahl Erreichte Punkte Korrektor Zwischensumme Bonuspunkte Summe Bewertung
2 Aufgabe 1 (26 Punkte) Zur Erkundung der Venusatmosphäre soll eine Sonde mit einem Zweikammermesssystem eingesetzt werden. Die Kammer A wird auf der Erde mit Atmosphärenluft bei p = 1 bar und t = 20 C befüllt. Das System ist so konstruiert, dass die Wandung stets als ideal adiabat betrachtet werden kann. Eine Membrane, welche beide Kammern trennt, kann für Energie durchlässig gemacht werden, ist aber für Materie stets undurchlässig. Die Membrane kann zusätzlich an beliebigen Positionen entlang der z-achse arretiert werden. Die Kammer B ist zunächst evakuiert und dient der thermodynamischen Untersuchung unbekannter Gasproben. Sowohl die Luft in Kammer A als auch die unbekannte Gasprobe in Kammer B können stets als ideale Gase betrachtet werden. Beide Kammern bilden nach dem Befüllen und dem Schließen des Ventils separate geschlossene Systeme. Nach der Landung auf der Venus wird das Ventil geöffnet und bleibt zunächst offen. Die Kammer B füllt sich nun mit der unbekannten Gasprobe. Nach dem Lösen der Arretierung der Membrane verringert sich das Volumen der Kammer A auf 4 % des ursprünglichen Volumens. Die Membrane sei zunächst für Wärme undurchlässig. a) Bestimmen Sie den Druck in Kammer A. (4 P) Die Membrane wird nun für Wärme durchlässig gemacht und das Volumen der Kammer A verringert sich um weitere 31 %. b) Berechnen Sie die Temperatur in Kammer A. (3 P) c) Stellen die in a) und b) berechneten Größen auch die Temperatur und den Druck der Venusatmosphäre dar? Begründen Sie. (2 P) 2
3 Das Ventil wird nun geschlossen. Das Gesamtvolumen beider Kammern beträgt 1 dm 3. d) Berechnen Sie die Stoffmenge in den Kammern A und B, sowie die Masse der Luft in Kammer A, wenn das Volumen der Kammer A vor der Probennahme 0,5 dm 3 betrug und die Membrane kein Eigenvolumen hat. (4 P) Dem gesamten System werden nun von außen 45 J an Wärme zugeführt. Die Arretierung der Membrane ist gelöst und die Membrane ist für Wärme durchlässig. e) Welche Temperatur und welcher Druck stellen sich in den Kammern A und B ein, wenn für die molare isochore Wärmekapazität des Gases in Kammer B c v,m = 49, 9 J/(mol K) angenommen werden kann. (10 P) f) Geben Sie die jeweiligen Freiheitsgrade (Translation, Rotation, Vibration) der unbekannten Gasprobe in B an. Wie könnte die Molekülgeometrie demnach aussehen, unter der Annahme, dass alle Freiheitsgrade vollständig angeregt sind? (3 P) Universelle Gaskonstante: R m = 8,3145 J/(mol K) Stoffdaten der Atmosphärenluft in Kammer A: κ = 1, 4 ; c v = 0, 8 J/(g K) ; M = 28, 95 g/mol 3
4 Aufgabe 2 (28 Punkte) In einem Dampfkraftwerk durchläuft das Arbeitsmedium Wasser folgende Zustandsänderungen: 1 2: reversibel adiabate Druckerhöhung, am Punkt 2 liegt eine Enthalpie von h 2 = 167, 45 kj/kg vor 2 3: isobare unterkritische Wärmezufuhr bis zur Temperatur T 3 = 823, 15 K 3 4: irreversibel adiabate Entspannung auf das mittlere Drucknivau von p 4 = 4 bar, nach der realen Entspannung liegt der Dampf um 20 K überhitzt vor, nach einer reversibel adiabaten Entspannung würde ein Dampfgehalt von 92 % vorliegen 4 5: isobare Wärmezufuhr auf eine Temperatur T 5 = 773, 15 K 5 6: irreversibel adiabate Entspannung auf das untere Drucknivau von p 6 = 0, 06 bar, bei 20 K Überhitzung 6 1: isobare Wärmeabfuhr bis nur noch siedende Flüssigkeit vorliegt Beide Turbinen gemeinsam liefern eine Leistung von 120 MW. Die Umgebungstemperatur beträgt 25 C. a) Zeichnen Sie das Anlagenschema des Dampfturbinenprozesses mit allen zu- und abgeführten Wärmeströmen und Leistungen. (3 P) b) Stellen Sie den Prozess qualitativ in einem T, s-diagramm dar. Kennzeichen Sie im Diagramm den kritischen Punkt, sowie die Siede- und Taulinie. (5 P) c) Auf welchen Druck muss die Kesselspeisepumpe das Wasser fördern? (4 P) Wenn Sie Aufgabenteil c) nicht lösen konnten, rechnen Sie mit einem oberen Druckniveau von 14,5 MPa weiter. d) Berechnen Sie den isentropen Wirkungsgrad für beide Turbinen. Warum steigt die Entropie bei der Entspannung? (6 P) e) Bestimmen Sie den Massenstom Wasser im Dampfturbinenprozess, sowie die beiden aufzubringenden Wärmeströme. (4 P) f) Berechnen Sie den thermischen und exergetischen Wirkungsgrad des Dampfturbinenprozesses. Warum ist der exergetische Wirkungsgrad bei rechtsläufigen Kreisprozessen immer größer als der thermische? (6 P) 4
5 Stoffdaten Wasser: Zweiphasiger Zustand: T p h h s s K MPa kj / kg kj / kg kj / (kg K) kj / (kg K) 309,31 0, , ,6 0, , ,76 0,4 604, ,1 1,7765 6, , ,5 2800,8 2,7968 6, , ,1 2725,5 3,3606 5, , ,2 2610,7 3,6846 5, , ,2 2412,3 4,0156 4, ,10 22, ,6 2146,6 4,5033 4,5033 Gasförmiger Zustand: T p h s K MPa kj / kg kj / (kg K) 823, ,9 7, , ,3 7, , ,6 6, , ,8 6, , ,0 6, , ,0 6, , ,9 6, , ,7 6, , ,3 6, , ,9 6, , ,4 6, , ,8 6, , ,0 6, ,31 0, ,8 8, ,76 0,4 2783,1 7, ,15 0,4 3485,5 8,1933 5
6 Aufgabe 3 (26 Punkte) Im dargestellten Zylinder befindet sich 1 kg Wasser im thermischen Gleichgewicht mit der Umgebung (T a = 293 K, p a = 1 bar). Auf dem Kolben liegt eine Masse von 144,2 kg. Der Kolben ist bis zu den Anschlägen im oberen Teil des Zylinders frei beweglich. Die Masse und Höhe des Kolbens können vernachlässigt werden. Die Abmessungen des Zylinders sind der Skizze zu entnehmen. Der Zylinder ist über ein zunächst geschlossenes Ventil mit einem Tank verbunden. Dieser Tank enthält ebenfalls 1 kg Wasser, welches bei 5 bar im zweiphasigen Zustand vorliegt. a) Welcher Druck herrscht im Zylinder? In welchem Zustand liegt das Wasser darin vor und welches Volumen füllt es aus? (3 P) Der Druck im Zylinder soll durch Wärmezufuhr auf 3 bar erhöht werden. b) Welche Zustandsänderungen treten dabei auf? Zeichen Sie diese qualitativ in ein p, v-diagramm ein. Wieviel Wärme muss dem Wasser im Zylinder zugeführt werden? (12 P) Die Wärmeaufnahme durch Zylinder und Kolben ist zu vernachlässigen. c) Bestimmen Sie das Volumen des Tanks. (2 P) Nun wird das Ventil zwischen Zylinder und Tank geöffnet. d) Welcher neue Zustand (Dichte, Druck, Temperatur) stellt sich ein? Gehen Sie von einer nach außen hin adiabaten Zustandsänderung aus. (9 P) (Hinweis: Die innere Energie U und Enthalpie H sind extensive Zustandsgrößen, es gilt Massen- und Energieerhaltung.) 6
7 Stoffdaten Wasser: Kritischer Punkt: T c = 647,1 K ; p c = 22,064 MPa ; ρ c = 322,0 kg/m 3 Flüssiges Wasser bei 293 K ist als inkompressibel zu betrachten mit: ρ = 998,25 kg/m 3 ; u = 83,27 kj/kg ; h = 83,47 kj/kg Nassdampf-Gebiet: T p ρ ρ u u h h K MPa kg / m 3 kg / m 3 kj / kg kj / kg kj / kg kj / kg 293,00 0, ,19 0, , ,1 83, ,2 333,21 0,02 983,13 0, , ,0 251, ,9 349,01 0,04 974,30 0, , ,3 317, ,1 359,08 0,06 967,99 0, , ,0 359, ,9 366,64 0,08 962,93 0, , ,2 391, ,2 372,76 0,10 958,63 0, , ,6 417, ,9 377,93 0,12 954,86 0, , ,7 439, ,1 382,44 0,14 951,49 0, , ,9 458, ,0 386,45 0,16 948,41 0, , ,4 475, ,0 390,06 0,18 945,57 1, , ,5 490, ,4 393,36 0,20 942,94 1, , ,1 504, ,2 406,67 0,30 931,82 1, , ,2 561, ,9 416,76 0,40 922,89 2, , ,1 604, ,1 424,98 0,50 915,29 2, , ,7 640, ,1 431,98 0,60 908,59 3, , ,8 670, ,1 438,10 0,70 902,56 3, , ,8 697, ,8 443,56 0,80 897,04 4, , ,0 720, ,3 448,50 0,90 891,92 4, , ,6 742, ,0 453,03 1,00 887,13 5, , ,7 762, ,1 485,53 2,00 849,80 10, , ,1 908, ,3 507,00 3,00 821,90 15, ,7 2603,2 1008,3 2803,2 523,50 4,00 798,37 20, ,5 2601,7 1087,5 2800,8 537,09 5,00 777,37 25, ,2 2597,0 1154,6 2794,2 7
Kraft- und Arbeitsmaschinen Klausur zur Diplom-Hauptprüfung, 26. Juli 2006
 Kraft- und Arbeitsmaschinen Klausur zur Diplom-Hauptprüfung, 26. Juli 2006 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten; Die Foliensammlung, Ihre Mitschrift der Vorlesung
Kraft- und Arbeitsmaschinen Klausur zur Diplom-Hauptprüfung, 26. Juli 2006 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten; Die Foliensammlung, Ihre Mitschrift der Vorlesung
Thermodynamik 2 Klausur 17. Februar 2015
 Thermodynamik 2 Klausur 17. Februar 2015 Bearbeitungszeit: Umfang der Aufgabenstellung: 120 Minuten 5 nummerierte Seiten 2 Diagramme Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner
Thermodynamik 2 Klausur 17. Februar 2015 Bearbeitungszeit: Umfang der Aufgabenstellung: 120 Minuten 5 nummerierte Seiten 2 Diagramme Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Stickstoff kann als ideales Gas betrachtet werden mit einer spezifischen Gaskonstante von R N2 = 0,297 kj
 Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Klausur Thermische Kraftwerke (Energieanlagentechnik I)
 Klausur Thermische Kraftwerke (Energieanlagentechnik I) Datum: 09.03.2009 Dauer: 1,5 Std. Der Gebrauch von nicht-programmierbaren Taschenrechnern und schriftlichen Unterlagen ist erlaubt. Aufgabe 1 2 3
Klausur Thermische Kraftwerke (Energieanlagentechnik I) Datum: 09.03.2009 Dauer: 1,5 Std. Der Gebrauch von nicht-programmierbaren Taschenrechnern und schriftlichen Unterlagen ist erlaubt. Aufgabe 1 2 3
wegen Massenerhaltung
 3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 3. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 3 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3 Bilanzgleichungen 3.3.1 Massebilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 3 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3 Bilanzgleichungen 3.3.1 Massebilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K
![Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K](/thumbs/26/9282771.jpg) Fundamentalgleichung für die Entropie Entropie S [S] = J/K spezifische Entropie: s = S/m molare Entropie: s m = S/n Mit dem 1. Hauptsatz für einen reversiblen Prozess und der Definition für die Entropie
Fundamentalgleichung für die Entropie Entropie S [S] = J/K spezifische Entropie: s = S/m molare Entropie: s m = S/n Mit dem 1. Hauptsatz für einen reversiblen Prozess und der Definition für die Entropie
5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme
 5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme Für isotherme reversible Prozesse gilt und daher Dies
5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme Für isotherme reversible Prozesse gilt und daher Dies
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spindler
 UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spindler Prüfung "Technische Thermodynamik 1+2" 18. August 2014 Zeit: 180 min. zugelassen: für Aufgabe 1-4 Taschenrechner
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spindler Prüfung "Technische Thermodynamik 1+2" 18. August 2014 Zeit: 180 min. zugelassen: für Aufgabe 1-4 Taschenrechner
Klausur Wärmelehre E2/E2p, SoSe 2012 Braun. Formelsammlung Thermodynamik
 Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Übungsaufgaben zur Thermodynamik
 Übungsaufgaben zur Thermodynamik Übungsbeispiel 1 Ein ideales Gas hat bei einem Druck von 2,5 bar und ϑl = 27 C eine Dichte von ρ1 = 2,7 kg/m 3. Durch isobare Wärmezufuhr soll sich das Gasvolumen Vl verdoppeln
Übungsaufgaben zur Thermodynamik Übungsbeispiel 1 Ein ideales Gas hat bei einem Druck von 2,5 bar und ϑl = 27 C eine Dichte von ρ1 = 2,7 kg/m 3. Durch isobare Wärmezufuhr soll sich das Gasvolumen Vl verdoppeln
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Thermodynamik. oder Website der Fachhochschule Osnabrück
 Thermodynamik Prof. Dr.-Ing. Matthias Reckzügel Vorlesung, Übung und Praktikum im 3. Semester für die Studiengänge: Maschinenbau Fahrzeugtechnik Maschinenbauinformatik Integrierte Produktentwicklung EMS
Thermodynamik Prof. Dr.-Ing. Matthias Reckzügel Vorlesung, Übung und Praktikum im 3. Semester für die Studiengänge: Maschinenbau Fahrzeugtechnik Maschinenbauinformatik Integrierte Produktentwicklung EMS
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
Thermodynamik. Eine Einführung in die Grundlagen. Von. Dr.-Ing. Hans Dieter Baehr. o. Professor an der Technischen Hochschule Braunschweig
 Thermodynamik Eine Einführung in die Grundlagen und ihre technischen Anwendungen Von Dr.-Ing. Hans Dieter Baehr o. Professor an der Technischen Hochschule Braunschweig Mit 325 Abbildungen und zahlreichen
Thermodynamik Eine Einführung in die Grundlagen und ihre technischen Anwendungen Von Dr.-Ing. Hans Dieter Baehr o. Professor an der Technischen Hochschule Braunschweig Mit 325 Abbildungen und zahlreichen
Thermodynamik I. Sommersemester 2012 Kapitel 4, Teil 2. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 4, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 4, Teil 2: Übersicht 4 Zweiter Hauptsatz der Thermodynamik 4.5 Entropiebilanz 4.5.1 Allgemeine Entropiebilanz 4.5.2
Thermodynamik I Sommersemester 2012 Kapitel 4, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 4, Teil 2: Übersicht 4 Zweiter Hauptsatz der Thermodynamik 4.5 Entropiebilanz 4.5.1 Allgemeine Entropiebilanz 4.5.2
Ein Braunkohle-Kraftwerk arbeitet nach dem Clausius-Rankine-Prozess mit einfacher Zwischenüberhitzung
 Klausuraufgaben Thermodynamik (F 0 A) BRAUNKOHLE-KRAFTWERK Ein Braunkohle-Kraftwerk arbeitet nach dem Clausius-Rankine-Prozess mit einfacher Zwischenüberhitzung und Anzapf-Vorwärmung. Dabei wird der Wassermassenstrom
Klausuraufgaben Thermodynamik (F 0 A) BRAUNKOHLE-KRAFTWERK Ein Braunkohle-Kraftwerk arbeitet nach dem Clausius-Rankine-Prozess mit einfacher Zwischenüberhitzung und Anzapf-Vorwärmung. Dabei wird der Wassermassenstrom
Institut für Thermodynamik Prof. Dr. rer. nat. M. Pfitzner Thermodynamik I - Lösung 1. Einleitende Fragen
 Einleitende Fragen 1. Was versteht man unter Thermodynamik? Thermodynamik ist die Lehre von den Energieumwandlungen und den Zusammenhängen zwischen den Eigenschaften der Stoffe. 2. Erklären Sie folgende
Einleitende Fragen 1. Was versteht man unter Thermodynamik? Thermodynamik ist die Lehre von den Energieumwandlungen und den Zusammenhängen zwischen den Eigenschaften der Stoffe. 2. Erklären Sie folgende
Kleine Formelsammlung Technische Thermodynamik
 Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
Thermodynamik des Kraftfahrzeugs
 Cornel Stan Thermodynamik des Kraftfahrzeugs Mit 199 Abbildungen Inhaltsverzeichnis Liste der Formelzeichen... XV 1 Grundlagen der Technischen Thermodynamik...1 1.1 Gegenstand und Untersuchungsmethodik...1
Cornel Stan Thermodynamik des Kraftfahrzeugs Mit 199 Abbildungen Inhaltsverzeichnis Liste der Formelzeichen... XV 1 Grundlagen der Technischen Thermodynamik...1 1.1 Gegenstand und Untersuchungsmethodik...1
Projekt Aufgabensammlung Thermodynamik
 Projekt Aufgabensammlung Thermodynamik Nr. Quelle Lösungssicherheit Lösung durch abgetippt durch 1 Klausur 1 (1) OK Navid Matthes 2 Probekl. WS06 (1) / Kl.SS04 (1) 100% Prof. Seidel. (Nav.) Matthes (Nav)
Projekt Aufgabensammlung Thermodynamik Nr. Quelle Lösungssicherheit Lösung durch abgetippt durch 1 Klausur 1 (1) OK Navid Matthes 2 Probekl. WS06 (1) / Kl.SS04 (1) 100% Prof. Seidel. (Nav.) Matthes (Nav)
Klausur zur Vorlesung. Thermodynamik
 Institut für Thermodynamik 25. August 2010 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Institut für Thermodynamik 25. August 2010 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Inhaltsverzeichnis. Hans-Joachim Kretzschmar, Ingo Kraft. Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6
 Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
Formel X Leistungskurs Physik 2005/2006
 System: Wir betrachten ein Fluid (Bild, Gas oder Flüssigkeit), das sich in einem Zylinder befindet, der durch einen Kolben verschlossen ist. In der Thermodynamik bezeichnet man den Gegenstand der Betrachtung
System: Wir betrachten ein Fluid (Bild, Gas oder Flüssigkeit), das sich in einem Zylinder befindet, der durch einen Kolben verschlossen ist. In der Thermodynamik bezeichnet man den Gegenstand der Betrachtung
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seminar Thermische Abfallbehandlung - Veranstaltung 4 - Dampfkraftprozesse
 Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
Thermodynamik. Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur
 Thermodynamik Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur kann voraussagen, ob eine chemische Reaktion abläuft oder nicht kann nichts über den zeitlichen
Thermodynamik Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur kann voraussagen, ob eine chemische Reaktion abläuft oder nicht kann nichts über den zeitlichen
Übungsaufgabe. Bestimmen Sie das molare Volumen für Ammoniak bei einem Druck von 1 MPa und einer Temperatur von 100 C nach
 Übungsaufgabe Bestien Sie das olare Voluen für Aoniak bei eine Druck von 1 MPa und einer Teperatur von 100 C nach a) de idealen Gasgesetz b) der Van der Waals-Gleichung c) der Redlich-Kwong- Gleichung
Übungsaufgabe Bestien Sie das olare Voluen für Aoniak bei eine Druck von 1 MPa und einer Teperatur von 100 C nach a) de idealen Gasgesetz b) der Van der Waals-Gleichung c) der Redlich-Kwong- Gleichung
Dampfkraftprozess Dampfturbine
 Fachgebiet für Energiesysteme und Energietechnik Prof. Dr.-Ing. B. Epple Musterlösung Übung Energie und Klimaschutz Sommersemester 0 Dampfkraftprozess Dampfturbine Aufgabe : Stellen Sie den Dampfkraftprozess
Fachgebiet für Energiesysteme und Energietechnik Prof. Dr.-Ing. B. Epple Musterlösung Übung Energie und Klimaschutz Sommersemester 0 Dampfkraftprozess Dampfturbine Aufgabe : Stellen Sie den Dampfkraftprozess
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
HP 2003/04-3: Blockschaltbild eines Dampfkraftwerks:
 HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: Teilaufgaben: 1 Welche Energieformen werden den Bauteilen Dampferzeuger, Turbine, Generator und Verbraucher
HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: Teilaufgaben: 1 Welche Energieformen werden den Bauteilen Dampferzeuger, Turbine, Generator und Verbraucher
Übung 3. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) Verständnis des thermodynamischen Gleichgewichts
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Inhaltsverzeichnis XVII. Häufig verwendete Formelzeichen. 1 Allgemeine Grundlagen l
 Inhaltsverzeichnis Häufig verwendete Formelzeichen XVII 1 Allgemeine Grundlagen l 1.1 Thermodynamik 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 Was ist Thermodynamik? 9 1.2 System
Inhaltsverzeichnis Häufig verwendete Formelzeichen XVII 1 Allgemeine Grundlagen l 1.1 Thermodynamik 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 Was ist Thermodynamik? 9 1.2 System
Thermodynamik I. Sommersemester 2012 Kapitel 5, Teil 1. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 5, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 5, Teil 1: Übersicht 5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel isotherme
Thermodynamik I Sommersemester 2012 Kapitel 5, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 5, Teil 1: Übersicht 5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel isotherme
Aufgaben zum Stirlingschen Kreisprozess Ein Stirling-Motor arbeite mit 50 g Luft ( M= 30g mol 1 )zwischen den Temperaturen = 350 C und T3
 Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Aufgabe 1 : (10 + 6 + 4 = 20 Punkte)
 Aufgabe 1 : (10 + 6 + 4 = 20 Punkte) Wirtschaftlichkeitsbetrachtung Als Jungingenieur arbeiten Sie in einer mittleren Firma an der Auslegung eines neuen Produktionsprozesses. Bei der Planung haben Sie
Aufgabe 1 : (10 + 6 + 4 = 20 Punkte) Wirtschaftlichkeitsbetrachtung Als Jungingenieur arbeiten Sie in einer mittleren Firma an der Auslegung eines neuen Produktionsprozesses. Bei der Planung haben Sie
Energie- und Kältetechnik Klausur WS 2008/2009
 Aufgabenteil / 00 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
Aufgabenteil / 00 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
6.4.2 VerdampfenundEindampfen... 427 6.4.3 Destillieren und Rektifizieren... 430 6.4.4 Absorbieren... 436
 Inhaltsverzeichnis 1 Allgemeine Grundlagen... 1 1.1 Thermodynamik... 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 WasistThermodynamik?... 9 1.2 SystemundZustand... 11 1.2.1 SystemundSystemgrenzen...
Inhaltsverzeichnis 1 Allgemeine Grundlagen... 1 1.1 Thermodynamik... 1 1.1.1 Von der historischen Entwicklung der Thermodynamik 1 1.1.2 WasistThermodynamik?... 9 1.2 SystemundZustand... 11 1.2.1 SystemundSystemgrenzen...
EHW Seite. Bei einem Spritzeinsatz zur Schädlingsbekämpfung fliegt ein Flugzeug bei Windstille in 20 s über ein 500 m langes Feld.
 EHW Seite Bei einem Spritzeinsatz zur Schädlingsbekämpfung fliegt ein Flugzeug bei Windstille in 20 s über ein 500 m langes Feld. Welche Geschwindigkeit besitzt das Flugzeug? Wie lange benötigt es, wenn
EHW Seite Bei einem Spritzeinsatz zur Schädlingsbekämpfung fliegt ein Flugzeug bei Windstille in 20 s über ein 500 m langes Feld. Welche Geschwindigkeit besitzt das Flugzeug? Wie lange benötigt es, wenn
2.6 Zweiter Hauptsatz der Thermodynamik
 2.6 Zweiter Hauptsatz der Thermodynamik Der zweite Hauptsatz der Thermodynamik ist ein Satz über die Eigenschaften von Maschinen die Wärmeenergie Q in mechanische Energie E verwandeln. Diese Maschinen
2.6 Zweiter Hauptsatz der Thermodynamik Der zweite Hauptsatz der Thermodynamik ist ein Satz über die Eigenschaften von Maschinen die Wärmeenergie Q in mechanische Energie E verwandeln. Diese Maschinen
Thermodynamik I - Übung 1. Nicolas Lanzetti
 Thermodynamik I - Übung 1 Nicolas Lanzetti Nicolas Lanzetti 02.10.2015 1 Hinweise zu der Übung Name: Nicolas Lanzetti; 5. Semester Maschinenbau; Mail: Raum: CHN C14; Zeit: Freitag, 8:15-10:00; Alle Unterlagen:
Thermodynamik I - Übung 1 Nicolas Lanzetti Nicolas Lanzetti 02.10.2015 1 Hinweise zu der Übung Name: Nicolas Lanzetti; 5. Semester Maschinenbau; Mail: Raum: CHN C14; Zeit: Freitag, 8:15-10:00; Alle Unterlagen:
Schriftliche Prüfung aus VO Kraftwerke am Name/Vorname: / Matr.-Nr./Knz.: / V1 = 2,7 Liter
 Schriftliche Prüfung aus VO Kraftwerke am 10.11.2015 Name/Vorname: / Matr.-Nr./Knz.: / 1. Stirlingmotor (25 Punkte) Ein Stirlingmotor soll zur Stromerzeugung in einem 50 Hz Netz eingesetzt werden. Es wird
Schriftliche Prüfung aus VO Kraftwerke am 10.11.2015 Name/Vorname: / Matr.-Nr./Knz.: / 1. Stirlingmotor (25 Punkte) Ein Stirlingmotor soll zur Stromerzeugung in einem 50 Hz Netz eingesetzt werden. Es wird
Isotherme 3. 4 Adiabate 2 T 1. Adiabate Isotherme T 2. Arbeit nach außen = eingeschlossene Kurve
 Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht
 8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht
 8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
Übungen zur Vorlesung. Energiesysteme
 Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
Inhaltsverzeichnis. Gernot Wilhelms. Übungsaufgaben Technische Thermodynamik ISBN: 978-3-446-41512-6. Weitere Informationen oder Bestellungen unter
 Inhaltsverzeichnis Gernot Wilhelms Übungsaufgaben Technische Thermodynamik ISBN: 978-3-446-41512-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41512-6 sowie im Buchhandel.
Inhaltsverzeichnis Gernot Wilhelms Übungsaufgaben Technische Thermodynamik ISBN: 978-3-446-41512-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41512-6 sowie im Buchhandel.
Übungen. Vorlesung. Energietechnik
 Fachhochschule Münster Fachbereich Maschinenbau Motoren- und Energietechnik-Labor Prof. Dr. R. Ullrich Übungen zur Vorlesung Energietechnik Version 1/99 - 2 - Übung 1 1.) Die wirtschaftlich gewinnbaren
Fachhochschule Münster Fachbereich Maschinenbau Motoren- und Energietechnik-Labor Prof. Dr. R. Ullrich Übungen zur Vorlesung Energietechnik Version 1/99 - 2 - Übung 1 1.) Die wirtschaftlich gewinnbaren
J und κ =1, 4 behandelt werden. kg K. a) Berechnen Sie die fehlenden Temperaturen und Drücke!
 Übung 11 Aufgabe 7.6: Offene Gaturbine Eine Gaturbinenanlage untercheidet ich vom reveriblen oule-proze dadurch, da der Verdichter und die Turbine nicht ientrop arbeiten. E gilt vielmehr: η S,V =0, 85
Übung 11 Aufgabe 7.6: Offene Gaturbine Eine Gaturbinenanlage untercheidet ich vom reveriblen oule-proze dadurch, da der Verdichter und die Turbine nicht ientrop arbeiten. E gilt vielmehr: η S,V =0, 85
Aggregatzustände. Festkörper. Flüssigkeit. Gas
 Festkörper Festkörper: - weitreichend geordnetes Kristallgitter - feste Positionen, geringe Abstände - starke Wechselwirkung zwischen Atomen - Schwingungen um Positionen Flüssigkeit: - keine weitreichende
Festkörper Festkörper: - weitreichend geordnetes Kristallgitter - feste Positionen, geringe Abstände - starke Wechselwirkung zwischen Atomen - Schwingungen um Positionen Flüssigkeit: - keine weitreichende
wegen adiabater Kompression, d.h. kein Wärmeaustausch mit der Umgebung, gilt:
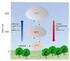 Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 1. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 1 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 1: Übersicht 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie 3.1.2 Innere Energie U 3.1.3 Energietransfer
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 1 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 1: Übersicht 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie 3.1.2 Innere Energie U 3.1.3 Energietransfer
Perpetuum Mobile I. Ein Perpetuum mobile erster Art wird durch den ersten Hauptsatz der Thermodynamik ausgeschlossen.
 Perpetuum Mobile I Perpetuum mobile erster Art: Unter einem perpetuum mobile erster Art versteht man eine Vorrichtung, deren Teile, einmal angeregt, nicht nur dauernd in Bewegung bleiben, sondern dabei
Perpetuum Mobile I Perpetuum mobile erster Art: Unter einem perpetuum mobile erster Art versteht man eine Vorrichtung, deren Teile, einmal angeregt, nicht nur dauernd in Bewegung bleiben, sondern dabei
Institut für Energiesysteme und Energietechnik. Vorlesungsübung 1. Musterlösung
 Institut für Energiesysteme und Energietechnik Vorlesungsübung 1 Musterlösung 3.1 Kohlekraftwerk Aufgabe 1 Gesucht: Aufgrund der Vernachlässigung des Temperaturunterschiedes des Luft-, Rauchgas- und Brennstoffstromes
Institut für Energiesysteme und Energietechnik Vorlesungsübung 1 Musterlösung 3.1 Kohlekraftwerk Aufgabe 1 Gesucht: Aufgrund der Vernachlässigung des Temperaturunterschiedes des Luft-, Rauchgas- und Brennstoffstromes
Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet
 Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet Unterrichtsmaterial - schriftliche Informationen zu Gasen für Studierende - Folien Fach Schultyp: Vorkenntnisse: Bearbeitungsdauer Thermodynamik
Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet Unterrichtsmaterial - schriftliche Informationen zu Gasen für Studierende - Folien Fach Schultyp: Vorkenntnisse: Bearbeitungsdauer Thermodynamik
ST Der Stirling-Motor als Wärmekraftmaschine
 ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
Übungen zur Thermodynamik (PBT) WS 2004/05
 1. Übungsblatt 1. Berechnen Sie ausgehend von der allgemeinen Gasgleichung pv = nrt das totale Differential dv. Welche Änderung ergibt sich hieraus in erster Näherung für das Volumen von einem Mol eines
1. Übungsblatt 1. Berechnen Sie ausgehend von der allgemeinen Gasgleichung pv = nrt das totale Differential dv. Welche Änderung ergibt sich hieraus in erster Näherung für das Volumen von einem Mol eines
Physikalisches Praktikum
 Physikalisches Praktikum Versuch 26: Stirling-Motor UNIVERSITÄT DER BUNDESWEHR MÜNCHEN Fakultät für Elektrotechnik und Informationstechnik Institut für Physik Oktober 2015 2 Versuch 26 Stirling-Motor Der
Physikalisches Praktikum Versuch 26: Stirling-Motor UNIVERSITÄT DER BUNDESWEHR MÜNCHEN Fakultät für Elektrotechnik und Informationstechnik Institut für Physik Oktober 2015 2 Versuch 26 Stirling-Motor Der
Klausur Strömungsmechanik 1 WS 2009/2010
 Klausur Strömungsmechanik 1 WS 2009/2010 03. März 2010, Beginn 15:00 Uhr Prüfungszeit: 90 Minuten Zugelassene Hilfsmittel sind: Taschenrechner (nicht programmierbar) TFD-Formelsammlung (ohne handschriftliche
Klausur Strömungsmechanik 1 WS 2009/2010 03. März 2010, Beginn 15:00 Uhr Prüfungszeit: 90 Minuten Zugelassene Hilfsmittel sind: Taschenrechner (nicht programmierbar) TFD-Formelsammlung (ohne handschriftliche
kg K dp p = R LuftT 1 ln p 2a =T 2a Q 12a = ṁq 12a = 45, 68 kw = 288, 15 K 12 0,4 Q 12b =0. Technische Arbeit nach dem Ersten Hauptsatz:
 Übung 9 Aufgabe 5.12: Kompression von Luft Durch einen Kolbenkompressor sollen ṁ = 800 kg Druckluft von p h 2 =12bar zur Verfügung gestellt werden. Der Zustand der angesaugten Außenluft beträgt p 1 =1,
Übung 9 Aufgabe 5.12: Kompression von Luft Durch einen Kolbenkompressor sollen ṁ = 800 kg Druckluft von p h 2 =12bar zur Verfügung gestellt werden. Der Zustand der angesaugten Außenluft beträgt p 1 =1,
Kleine Formelsammlung Technische Thermodynamik
 Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN-10: 3-446-22882-9 ISBN-13: 978-3-446-22882-5 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-22882-5
Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN-10: 3-446-22882-9 ISBN-13: 978-3-446-22882-5 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-22882-5
Inhaltsverzeichnis Allgemeine Grundlagen Fluide Phasen
 1. Allgemeine Grundlagen... 1 1.1 Energie-undStoffumwandlungen... 1 1.1.1 Energieumwandlungen... 2 1.1.2 Stoffumwandlungen... 6 1.1.3 Energie- und Stoffumwandlungen in technischen Prozessen... 9 1.1.4
1. Allgemeine Grundlagen... 1 1.1 Energie-undStoffumwandlungen... 1 1.1.1 Energieumwandlungen... 2 1.1.2 Stoffumwandlungen... 6 1.1.3 Energie- und Stoffumwandlungen in technischen Prozessen... 9 1.1.4
Orientierungshilfen für die Zugangsprüfung Physik
 Orientierungshilfen für die Zugangsprüfung Physik Anliegen der Prüfung Die Zugangsprüfung dient dem Herausstellen der Fähigkeiten des Prüflings, physikalische Zusammenhänge zu erkennen. Das physikalische
Orientierungshilfen für die Zugangsprüfung Physik Anliegen der Prüfung Die Zugangsprüfung dient dem Herausstellen der Fähigkeiten des Prüflings, physikalische Zusammenhänge zu erkennen. Das physikalische
Technische Thermodynamik. FB Maschinenwesen. Übungsaufgaben. Technische Thermodynamik. Wärmeübertragung. University of Applied Sciences
 University of Applied Sciences Übungsaufgaben Technische Thermodynamik Wärmeübertragung Prof. Dr.-Ing. habil. H.-J. Kretzschmar FB Maschinenwesen Technische Thermodynamik HOCHSCHULE ZITTAU/GÖRLITZ (FH)
University of Applied Sciences Übungsaufgaben Technische Thermodynamik Wärmeübertragung Prof. Dr.-Ing. habil. H.-J. Kretzschmar FB Maschinenwesen Technische Thermodynamik HOCHSCHULE ZITTAU/GÖRLITZ (FH)
Thermodynamik Formelsammlung
 RH-öln Thermoynamik ormelsammlung 2006 Thermoynamik ormelsammlung - I 1 Grunlagen Boltzmannkonstante: 1.3 Größen un Einheitensysteme Umrechnung ahrenheit nach Celsius: Umrechnung Celsius nach elvin: abgeschlossenes
RH-öln Thermoynamik ormelsammlung 2006 Thermoynamik ormelsammlung - I 1 Grunlagen Boltzmannkonstante: 1.3 Größen un Einheitensysteme Umrechnung ahrenheit nach Celsius: Umrechnung Celsius nach elvin: abgeschlossenes
Vorlesung #7. M.Büscher, Physik für Mediziner
 Vorlesung #7 Zustandsänderungen Ideale Gase Luftfeuchtigkeit Reale Gase Phasenumwandlungen Schmelzwärme Verdampfungswärme Dampfdruck van-der-waals Gleichung Zustandsdiagramme realer Gase Allgem. Gasgleichung
Vorlesung #7 Zustandsänderungen Ideale Gase Luftfeuchtigkeit Reale Gase Phasenumwandlungen Schmelzwärme Verdampfungswärme Dampfdruck van-der-waals Gleichung Zustandsdiagramme realer Gase Allgem. Gasgleichung
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Allgemeine Chemie. SS 2014 Thomas Loerting. Thomas Loerting Allgemeine Chemie
 Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Klausur Physikalische Chemie für TUHH (Chemie III)
 07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
Übungen Physik I. Wärmelehre Aufgabe 1.1.
 Übungen Physik I. Wärmelehre Aufgabe 1.1. Wie groß ist die Masse eines a) Kohlendioxidmoleküls (CO 2 ), b) H 2 CO 3 -, c) K 2 SO 4 -, d) HNO 3 - Moleküls in kg? Aufgabe 1.2. Welche 4 wichtigen periodischen
Übungen Physik I. Wärmelehre Aufgabe 1.1. Wie groß ist die Masse eines a) Kohlendioxidmoleküls (CO 2 ), b) H 2 CO 3 -, c) K 2 SO 4 -, d) HNO 3 - Moleküls in kg? Aufgabe 1.2. Welche 4 wichtigen periodischen
Stellen Sie für die folgenden Reaktionen die Gleichgewichtskonstante K p auf: 1/2O 2 + 1/2H 2 OH H 2 + 1/2O 2 H 2 O
 Klausur H2004 (Grundlagen der motorischen Verbrennung) 2 Aufgabe 1.) Stellen Sie für die folgenden Reaktionen die Gleichgewichtskonstante K p auf: 1/2O 2 + 1/2H 2 OH H 2 + 1/2O 2 H 2 O Wie wirkt sich eine
Klausur H2004 (Grundlagen der motorischen Verbrennung) 2 Aufgabe 1.) Stellen Sie für die folgenden Reaktionen die Gleichgewichtskonstante K p auf: 1/2O 2 + 1/2H 2 OH H 2 + 1/2O 2 H 2 O Wie wirkt sich eine
Manuel Kühner und Veit Hammerstingl. SS 2008 Stand: 24.05.2009
 Private Formelsammlung für Thermodynamik 1 TU München und Veit Hammerstingl SS 2008 Stand: 24.05.2009 Internetseite: www.bipede.de 1 cm3 10 6 m3 1 Hektoliter 1 hl 100 l 100 dm3 0, 1 m3 Druck in Pascal
Private Formelsammlung für Thermodynamik 1 TU München und Veit Hammerstingl SS 2008 Stand: 24.05.2009 Internetseite: www.bipede.de 1 cm3 10 6 m3 1 Hektoliter 1 hl 100 l 100 dm3 0, 1 m3 Druck in Pascal
Übungssunterlagen. Energiesysteme I. Prof. Dr.-Ing. Bernd Epple
 Übungssunterlagen Energiesysteme I Prof. Dr.-Ing. Bernd Epple 1 1. Allgemeine Informationen Zum Bearbeiten der Übungen können die Formelsammlungen aus den Fächern Technische Thermodynamik 1, Technische
Übungssunterlagen Energiesysteme I Prof. Dr.-Ing. Bernd Epple 1 1. Allgemeine Informationen Zum Bearbeiten der Übungen können die Formelsammlungen aus den Fächern Technische Thermodynamik 1, Technische
Technische Thermodynamik
 Technische Thermodynamik Einführung und Anwendung von Prof. Dr.-Ing.em. Erich Hahne 5., völlig überarbeitete Auflage Oldenbourg Verlag München Inhaltsverzeichnis Vorwort Formelzeichen Indizes V IX XIII
Technische Thermodynamik Einführung und Anwendung von Prof. Dr.-Ing.em. Erich Hahne 5., völlig überarbeitete Auflage Oldenbourg Verlag München Inhaltsverzeichnis Vorwort Formelzeichen Indizes V IX XIII
- potentiell E pot. Gesamtenergie: E = U + E kin + E pot. 3 Energiebilanz. 3.1 Energie. 3.1.1 Formen der Energie
 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie Innere Energie: U - thermisch - latent Äußere Energien: E a - kinetisch E kin - potentiell E pot Gesamtenergie: E = U + E kin + E pot 3.1-1 3.1.2 Die
3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie Innere Energie: U - thermisch - latent Äußere Energien: E a - kinetisch E kin - potentiell E pot Gesamtenergie: E = U + E kin + E pot 3.1-1 3.1.2 Die
Klausur im Fach Thermodynamik I, SS 2012 am 06.08.2012
 e r e n e g y e n g i n e e r i n g..t c o n o m i c s. e n v i e n r o n m Technische Universität Berlin INSTITUT FÜR ENERGIETECHNIK Prof. Dr.-Ing. G. Tsatsaronis. Klausur im Fach Thermodynamik I, SS
e r e n e g y e n g i n e e r i n g..t c o n o m i c s. e n v i e n r o n m Technische Universität Berlin INSTITUT FÜR ENERGIETECHNIK Prof. Dr.-Ing. G. Tsatsaronis. Klausur im Fach Thermodynamik I, SS
U. Nickel Irreversible Volumenarbeit 91
 U. Nickel Irreversible Volumenarbeit 91 geben, wird die bei unterschiedlichem Innen- und Außendruck auftretende Arbeit als irreversible Volumenarbeit irr bezeichnet. Die nachfolgend angegebene Festlegung
U. Nickel Irreversible Volumenarbeit 91 geben, wird die bei unterschiedlichem Innen- und Außendruck auftretende Arbeit als irreversible Volumenarbeit irr bezeichnet. Die nachfolgend angegebene Festlegung
Thermodynamische Berechnung des Modells eines Stirling-Motors Typ b
 ösung : Projekt Stirling-Motor nach dem Kartonmodell Seite von 7 hermodynamische Berechnung des Modells eines Stirling-Motors y b Zu.) Übertragen Sie das gegebene --Diagramm in ein entsrechendes -s-diagramm
ösung : Projekt Stirling-Motor nach dem Kartonmodell Seite von 7 hermodynamische Berechnung des Modells eines Stirling-Motors y b Zu.) Übertragen Sie das gegebene --Diagramm in ein entsrechendes -s-diagramm
2.3.4 Bereiche für Zustandsberechnung im h,s-diagramm...23. 2.3.3 Bereiche für Zustandsberechnung im T,s-Diagramm...22
 Inhaltsverzeichnis 1 Thermodynamische Größen...11 1.1 Größenarten...11 1.2 Größen und Einheiten...12 1.3 Umrechnung von Einheiten...14 2 Zustandsverhalten reiner Stoffe...15 2.1 Einphasengebiete und Phasenübergänge...15
Inhaltsverzeichnis 1 Thermodynamische Größen...11 1.1 Größenarten...11 1.2 Größen und Einheiten...12 1.3 Umrechnung von Einheiten...14 2 Zustandsverhalten reiner Stoffe...15 2.1 Einphasengebiete und Phasenübergänge...15
Was ist überhaupt Thermodynamik? Das Wort Thermodynamik kommt aus dem Griechischen von therme (Wärme) und dynamis (Kraft).
 Struktur Was ist Thermodynamik Geschichte Einstieg Thermodynamik Thermische Zustandsgrößen Thermische Zustandsgleichungen Thermodynamische Systeme Zustand und Prozess Hauptsätze Was ist überhaupt Thermodynamik?
Struktur Was ist Thermodynamik Geschichte Einstieg Thermodynamik Thermische Zustandsgrößen Thermische Zustandsgleichungen Thermodynamische Systeme Zustand und Prozess Hauptsätze Was ist überhaupt Thermodynamik?
Vordiplomsklausur Physik
 Institut für Physik und Physikalische Technologien der TU-Clausthal; Prof. Dr. W. Schade Vordiplomsklausur Physik 14.Februar 2006, 9:00-11:00 Uhr für den Studiengang: Maschinenbau intensiv (bitte deutlich
Institut für Physik und Physikalische Technologien der TU-Clausthal; Prof. Dr. W. Schade Vordiplomsklausur Physik 14.Februar 2006, 9:00-11:00 Uhr für den Studiengang: Maschinenbau intensiv (bitte deutlich
Verbundstudium TBW Teil 1 Wärmelehre 1 3. Semester
 Verbundstudium TBW Teil 1 Wärmelehre 1 3. Semester 1. Temperaturmessung Definition der Temperaturskala durch ein reproduzierbares thermodynam. Phänomen, dem Thermometer Tripelpunkt: Eis Wasser - Dampf
Verbundstudium TBW Teil 1 Wärmelehre 1 3. Semester 1. Temperaturmessung Definition der Temperaturskala durch ein reproduzierbares thermodynam. Phänomen, dem Thermometer Tripelpunkt: Eis Wasser - Dampf
Thermodynamik 2. Peter Junglas 27. 6. 2013
 Thermodynamik 2 Irreversible Prozesse Kreisprozesse des idealen Gases in der Anwendung Thermodynamisches Verhalten realer Stoffe Dampfkraftanlagen Aufgaben Anhang Peter Junglas 27. 6. 2013 1 Inhaltsverzeichnis
Thermodynamik 2 Irreversible Prozesse Kreisprozesse des idealen Gases in der Anwendung Thermodynamisches Verhalten realer Stoffe Dampfkraftanlagen Aufgaben Anhang Peter Junglas 27. 6. 2013 1 Inhaltsverzeichnis
11. Ideale Gasgleichung
 . Ideale Gasgleichung.Ideale Gasgleichung Definition eines idealen Gases: Gasmoleküle sind harte punktförmige eilchen, die nur elastische Stöße ausführen und kein Eigenvolumen besitzen. iele Gase zeigen
. Ideale Gasgleichung.Ideale Gasgleichung Definition eines idealen Gases: Gasmoleküle sind harte punktförmige eilchen, die nur elastische Stöße ausführen und kein Eigenvolumen besitzen. iele Gase zeigen
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Technische Thermodynamik. FB Maschinenwesen. SolvayEXL Version für Studierende
 Programmbibliothek für thermophysikalische Stoffdaten von SOLKANE Kältemitteln SolvayEXL Version für Studierende Prof. Dr.-Ing. habil. H.-J. Kretzschmar Dr.-Ing. I. Stöcker Dipl.-Inf. I. Jähne Dipl.-Ing.
Programmbibliothek für thermophysikalische Stoffdaten von SOLKANE Kältemitteln SolvayEXL Version für Studierende Prof. Dr.-Ing. habil. H.-J. Kretzschmar Dr.-Ing. I. Stöcker Dipl.-Inf. I. Jähne Dipl.-Ing.
Technische Thermodynamik
 Günter Cerbe Gernot Wilhelms 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Technische Thermodynamik Theoretische
Günter Cerbe Gernot Wilhelms 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Technische Thermodynamik Theoretische
Technische Thermodynamik / Energielehre. 3. Band eines Kompendiums zur Lehrveranstaltung. Formelsammlung
 Fakultät Maschinenwesen Institut für Energietechnik Technische Thermodynamik / Energielehre 3. Band eines Kompendiums zur Lehrveranstaltung Formelsammlung für das Grundstudium Maschinenbau, Verfahrenstechnik
Fakultät Maschinenwesen Institut für Energietechnik Technische Thermodynamik / Energielehre 3. Band eines Kompendiums zur Lehrveranstaltung Formelsammlung für das Grundstudium Maschinenbau, Verfahrenstechnik
Themengebiet: Thermodynamik. mol K. mol. ] eines Stoffes bestehend aus n Mol mit der Masse m gilt. M = m n. (2)
![Themengebiet: Thermodynamik. mol K. mol. ] eines Stoffes bestehend aus n Mol mit der Masse m gilt. M = m n. (2) Themengebiet: Thermodynamik. mol K. mol. ] eines Stoffes bestehend aus n Mol mit der Masse m gilt. M = m n. (2)](/thumbs/39/18548726.jpg) Seite 1 Themengebiet: Thermodynamik 1 Literatur D. Meschede, Gerthsen Physik, Springer F. Kohlrausch, Praktische Physik, Band 2, Teubner R.P. Feynman, R.B. Leighton und M. Sands, Feynman-Vorlesungen über
Seite 1 Themengebiet: Thermodynamik 1 Literatur D. Meschede, Gerthsen Physik, Springer F. Kohlrausch, Praktische Physik, Band 2, Teubner R.P. Feynman, R.B. Leighton und M. Sands, Feynman-Vorlesungen über
Übungsblatt 3 (10.06.2011)
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
x Enthalpie H x Freie Enthalpie
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Was ist Physikalische Chemie? Die klassischen Teilgebiete der Physikalischen Chemie sind:
 Was ist Physikalische Chemie? Die klassischen eilgebiete der Physikalischen Chemie sind: 1) hermodynamik (z. B. Energetik chemischer Reaktionen, Lage von Gleichgewichten). 2) Kinetik chemischer Reaktionen
Was ist Physikalische Chemie? Die klassischen eilgebiete der Physikalischen Chemie sind: 1) hermodynamik (z. B. Energetik chemischer Reaktionen, Lage von Gleichgewichten). 2) Kinetik chemischer Reaktionen
Grundlagen der Technischen Thermodynamik
 Grundlagen der Technischen Thermodynamik Lehrbuch für Studierende der Ingenieurwissenschaften Bearbeitet von Ernst Doering, Herbert Schedwill, Martin Dehli 1. Auflage 2012. Taschenbuch. xii, 494 S. Paperback
Grundlagen der Technischen Thermodynamik Lehrbuch für Studierende der Ingenieurwissenschaften Bearbeitet von Ernst Doering, Herbert Schedwill, Martin Dehli 1. Auflage 2012. Taschenbuch. xii, 494 S. Paperback
Ide egy rajz hiányzik (egy vonal, a végein két telegömb, a baloldali felett Q 1 és a másik felett Q 2 )
 1. Es gibt drei gleiche Glühlampen. An eine Batterie wird eine Glühlampe angeschlossen. An eine andere Batterie werden zwei Glühlampen in der Reihe angeschlossen. Bei welcher Anordnung gibt es mehr Licht?
1. Es gibt drei gleiche Glühlampen. An eine Batterie wird eine Glühlampe angeschlossen. An eine andere Batterie werden zwei Glühlampen in der Reihe angeschlossen. Bei welcher Anordnung gibt es mehr Licht?
Allgemeine Vorgehensweise
 Allgemeine Vorgehensweise 1. Skizze zeichnen und Systemgrenze ziehen 2. Art des Systems festlegen (offen, geschlossen, abgeschlossen) und Eigenschaften charakterisieren (z.b. adiabat, stationär, ruhend...)
Allgemeine Vorgehensweise 1. Skizze zeichnen und Systemgrenze ziehen 2. Art des Systems festlegen (offen, geschlossen, abgeschlossen) und Eigenschaften charakterisieren (z.b. adiabat, stationär, ruhend...)
Einführung in die Verbrennungskraftmaschine
 Institut für erbrennungskraftmaschinen Einführung in die erbrennungskraftmaschine,.05.0 Institut für erbrennungskraftmaschinen Ed-Übung Übersicht Grundlagen der hermodynamik Prozess und thermischer Wirkungsgrad
Institut für erbrennungskraftmaschinen Einführung in die erbrennungskraftmaschine,.05.0 Institut für erbrennungskraftmaschinen Ed-Übung Übersicht Grundlagen der hermodynamik Prozess und thermischer Wirkungsgrad
Nachtrag zu 11: 11.6.Statistische Physik: Entropie, Boltzmann-Verteilung
 Nachtrag zu 11: 11.6.Statistische Physik: Entropie, Boltzmann-Verteilung Ludwig Boltzmann 1860: Maxwellsche Geschwindigkeitsverteilung 1865: Clausius, thermodynamische Entropie, 2. Hauptsatz: Entropie
Nachtrag zu 11: 11.6.Statistische Physik: Entropie, Boltzmann-Verteilung Ludwig Boltzmann 1860: Maxwellsche Geschwindigkeitsverteilung 1865: Clausius, thermodynamische Entropie, 2. Hauptsatz: Entropie
Thermodynamik I SS 2010
 1 Thermodynamik I SS 2010 Prof. Dr.-Ing. G. Wilhelms Größen/Größengleichungen (GR) GR 1 - Größen, Größengleichungen Basisgrößen (BGR) BGR 1 - Masse, Stoffmenge BGR 2 - Länge, Längenausdehnung BGR 3 - Temperatur
1 Thermodynamik I SS 2010 Prof. Dr.-Ing. G. Wilhelms Größen/Größengleichungen (GR) GR 1 - Größen, Größengleichungen Basisgrößen (BGR) BGR 1 - Masse, Stoffmenge BGR 2 - Länge, Längenausdehnung BGR 3 - Temperatur
Energietechnik SS 2005
 Energietechnik SS 2005 Prof. Dr.-Ing. G. Wilhelms Das ideale Gas in Maschinen und Anlagen (I) Das ideale Gas in Gasturbinen (IG) IG 1 - Joule-Prozess IG 2 - Ericcson-Prozess IG 3 - andere Vergleichsprozesse
Energietechnik SS 2005 Prof. Dr.-Ing. G. Wilhelms Das ideale Gas in Maschinen und Anlagen (I) Das ideale Gas in Gasturbinen (IG) IG 1 - Joule-Prozess IG 2 - Ericcson-Prozess IG 3 - andere Vergleichsprozesse
