Spinodale Entmischung
|
|
|
- Ina Schulze
- vor 7 Jahren
- Abrufe
Transkript
1 Benjamin Andrae Spinodale Entmischung Seminarvortrag im Hauptseminar zur statistischen Mechanik bei Prof. Dr. Erwin Frey
2 Inhalt: Vorbemerkung zur Methode Qualitatives Quantitatives Weiterführendes: Van-der-Waals Gas Ergänzungen Literatur
3 Ziel: Vorbemerkung zur Methode Quantitative und Qualitative Beschreibung von Entmischungen Zugrundeliegende Theorie: Thermodynamik der Gleichgewichte, Beschreibung der Dynamik als Wechselwirkung von vielen Gleichgewichten Ergebnis: zumindest qualitativ richtige Beschreibung der beobachteten Entmischung
4 Entmischungsvorgänge Prozesse bei denen sich eine Phase in verschiedene Phasen teilt. Im Folgenden : Zwei Phasen einer binären Mischung (z.b. Metall-Legierung)
5 Stabilität von Legierungen Fig. 1 Mischung in Fig. 1 ist stabil Eine homogene binäre Mischung wird durch eine Konzentration vollständig charakterisiert (insgesamt konstante Teilchenzahl) Das örtliche chemische Potential µ=v * df/dc. (konstantes örtliches Volumen, konstante Temperatur) Koexistenz nur für µ 1 = µ 2, also für Doppeltangente in F/c Diagramm.
6 Eine Form der freien Energie, die Koexistenz zweier Konzentrationen ermöglicht Koexistenz in Fig. 2 möglich. Fig. 2 Abhängigkeit der Form der freien Energie von der Temperatur in Fig. 3. Für weitere Überlegungen: Form der freien Energie fest, also ideales quenching. Fig. 3
7 Fig. 4 Fig. 5 Fig. 6 Metastabil stabil instabil Binodal und Spinodal Stabile Konzentrationen gegen Temperatur angetragen ergeben Koexistenzkurve, genannt Binodal Für beide Konzentrationen c 0 und c 0 in Fig. 5 Entmischung in Gebiete mit c 1 und c 2. Ziel: Verringerung der freien Energie. Örtlich dµ/dc>0 Bewegung zu niedrigen Konzentrationen. Örtlich dµ/dc<0 Bewegung zu höheren Konzentrationen Wendepunkte in Fig. 5 definieren eine Spinodal.
8 Nukleation (Berg-ab-Diffusion) Meta-stabiler Bereich: Ausgleich kleiner Fluktuationen. Trotzdem Koexistenz: große Fluktuation Örtliches Einstellen der günstigen Konzentrationen normale Diffusion führt zur Entmischung. Die Zeitskala solcher großen zufälligen Fluktuationen ist Unterkühlung verlängerbar um Entmischung zu verhindern. Fig. 7
9 Spinodale Entmischung (Berg-auf-Diffusion) Unterhalb des Spinodals Verstärkung jeder Fluktuation. Entmischung geschieht eine Wellenlänge wird maximal verstärkt. Langwellige Fluktuationen langsam wegen Teilchentransport. Sehr kurzwellige Fluktuationen schaffen zuviel energetisch ungünstige Oberfläche wachsen garnicht. Bisher: Freie Energie der Entmischung als Summe der freien Energien der Gebiete. Nun: Oberflächenterm. Fig. 8
10 Fig. 9 Vergröberung ( coarse-graining ) Vergröberung des Systems schon implizit verwendet (örtliches chem. Potential). kleinen Volumenelemente, in denen schnell ein Gleichgewicht entsteht. Annahme: Wellenlängen innerhalb der Volumenelemente energetisch ungünstig Betrachte nur Fluktuationen, die die Konzentration innerhalb eines Volumenelementes weitgehend konstant lassen.
11 Das Funktional der freien Energie Jetzt: Ausdruck für freie Energie der Entmischung mit Oberflächenterm. Wahl: κ( ρ) 2 (einfache, stets positive Abhängigkeit von Gradienten der Dichte) F = f(ρ(r)) + κ( ρ(r)) 2 dv Dabei ist κ eine von beiden Materialien abhängige Konstante. Geometrischer Einfluss durch verschieden große Teilchen vernachlässigt.
12 Kontinuitätsgleichung und Flussdichte Erhaltung der Teilchenzahl Kontinuitätsgleichung dρ/dt = - j(r,t) Die gewöhnliche Definition der Flussdichte (mit D = konst.) j = - D ρ ist nicht ausreichend, weil so nur Berg-ab-Diffusion stattfindet. Fluss in Richtung der Gebiete mit geringerem chem. Potential: j = - M µ(r,t) M ist Mobilitätskonstante µ wird abhängen von F, also von ρ.
13 Das Chemische Potential als Funktionalableitung δf = µδn. Änderung von F bei Änderung von N (und somit von c) gibt einen neuen Ausdruck für das chemische Potential, der den Einfluss des Gradiententerms beinhaltet. µ( r, t ) = δ F[ρ( r, t )] / δ ρ( r, t ) Es ergibt sich nach Funktionalableitung: µ( r, t ) = d f(ρ( r, t )) / d ρ( r, t ) - 2κ 2 ρ( r, t ) Erster Term: Abhängigkeit des chem. Potentials eines Volumenelements von der Änderung der örtlichen freien Energie mit der örtlichen Konzentration (ohne Formulierung der Form der freien Energie nicht näher zu bestimmen). Zweiter Term: Einfluss der Oberflächen.
14 Die Herleitung der Cahn-Hilliard Gleichung Einsetzen in die Definition der Flussdichte: j( r, t ) = -M [δ 2 f / δ ρ 2 ρ - 2κ 3 ρ ] Einsetzen in Kontinuitätsgleichung ergibt Differentialgleichung: Cahn-Hilliard Gleichung. dρ/dt = M [δ 2 f / δ ρ 2 2 ρ - 2κ 4 ρ ] Bei dem zweiten Schritt wurde die Annahme gemacht, dass δ 2 f / δ ρ 2 unabhängig von ρ und damit von r ist. Das gilt offensichtlich nicht allgemein, sondern nur für den Anfang der Entmischung, wo wegen der kleinen Konzentrationsabweichungen vom Anfangszustand Fig. 2 durch ein Polynom 2ter Ordnung angenähert werden kann.
15 Die Lösung der Cahn-Hilliard Gleichung Zur Lösung: Fourier-transformation. (-ik) dρ/dt = -M ρ( k, t) [δ 2 f / δ ρ 2 k 2 + 2κk 4 ] Lösung dieser Gleichung ist offensichtlich: ρ( k, t) = ρ( k, 0) exp[-mk 2 (δ 2 f / δ ρ 2 + 2κk 2 )t] Es wachsen also solche Wellenlängen λ = 2π/κ exponential an, für die (δ 2 f / δ ρ 2 + 2κk 2 ) < 0 gilt. ρ( k, 0) ist anfängliche Dichte-Fluktuation.
16 Fig. 10 Fig. 11 Interpretation Ableiten von M k 2 (δ 2 f / δ ρ 2 + 2κk 2 ) ergibt den am schnellsten wachsende Wellenvektor als: k max = [-(δ 2 f / δ ρ 2 ) / 4κ] Nullsetzen von M k 2 (δ 2 f / δ ρ 2 + 2κk 2 ) ergibt den Kritische Wellenvektor k c = [-(δ 2 f / δ ρ 2 ) / 2κ] Fig. 11: Durch spinodale Entmischung einer Polystyrene- Polybutadiene-Toluene Mischung entstandenes Muster. Links oben in Fig.11: Fouriertransformierte zeigt die Existenz einer typischen Wellenlänge.
17 Fig. 12 Fig. 13 Van-der-Waals Gas Analogien zu einem Phasenübergang beim Van-der- Waals Gas. Grenzen des Koexistenzbereichs in Fig. 12 sind gleichzeitig die Punkte mit Doppeltangente in Fig. 13. Wegen P = - ( F/ V) stimmen die Wendepunkte in Fig. 13 mit den Extrempunkten der Van-der- Waals Isotermen überein Beim Van-der-Waals Gas durch Unterkühlung eine Phasentrennung verhinderbar, bis das System in den Bereich innerhalb der so definierten Spinodalen kommt.
18 Funktionalableitung Um die erste Funktionalableitung eines Funktionals nach einer bestimmten Funktion zu bestimmen, betrachet man, wie sich das Funtional bei einer kleinen Änderung der Funktion verändert: (1) δf[ρ(r)] = dr [ (ρ(r ) + δρ(r ))] 2 = (2) = dr 2[ (ρ(r )] [ δρ(r )] = (3) = - dr 2[ 2ρ(r )] δρ(r ). Bei Funktionalen der Form F[g(r)] = dr G(g(r )) ist die Funktionalableitung erster Ordnung definiert über δf[ρ(r)] = dr (δf[g]/ δρ(r )) δρ(r ) wobei (δf[g]/ δρ(r )) die Funktionalableitung darstellt. In unserem Fall ergibt sich also (δf[ρ]/ δ ρ(r )) = -2[ 2ρ(r )] Von (1) nach (2) wurde verwendet, dass, um die Änderung zu erhalten, noch der unveränderte Term abgezogen werden muss. Von (2) nach (3) wurde partiell integriert, wobei der Randterm nach dem Satz von Gauss, bei an den Rändern verschwindender Funktion, wegfällt.
19 Mit Hilfe der Funktionalableitung kann auch formal klar gemacht werden, warum µ(r,t) = δ F[ρ] / δ ρ(r,t) gilt. Es ist nämlich V = dr und eine Veränderung der freien Energie δ F liegt an Veränderungen δ dn(r ) der Teilchenzahl in so einem Volumen, die wiederum eine Änderung der Dichte δ ρ (r ) = δ dn(r ) / dr. Damit lässt sich δ F schreiben als µ(r ) δ dn(r ) = = dr µ(r ) δ ρ (r ). Hier ist nun gemäß der Definition der Funktionalableitung gezeigt, dass µ(r) = δ F[ρ] / δ ρ(r) gilt
20 Für die hier verwendeten Funktionen gilt: Fourierentwicklung f ~ (k) = (1/2π) - f(x) e ikx dx und mit g(x) = f(x) also auch g ~ (k) = (1/2π) - e ikx f(x) dx und mittels partieller Integration dann g ~ (k) = (-ik) (1/2π) - e ikx f(x) dx = = (-ik)f(x). Man kann also beim Übergang in der Fourierraum Gradienten durch (-ik) ersetzen.
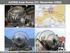
21 Literatur 1. Hellmig, Ralph Jörg: Phasenumwandlungen, Technische Universität Clausthal, Ws 2005/2006 (Fig. 7 und Fig. 8) 2. Bhadeshia, H.K.D.H.: Thermodynamics of Diffusion 3. Dhont, Jan K.G.: An Introduction to Dynamics of colloids, Elsevier Science B.V., Amsterdam, 1996 (Fig. 9) 4. Saidov, A.A. & Khabibullaev: Phase Seperation in Soft Matter Physics, Springer Verlag, Berlin-Heidelberg, Liquid-liquid unmixing-kinetics of phase seperation (Fig. 10 und Fig. 11) 6. Schwabl, Franz: Statistische Mechanik, Springer Verlag, Berlin-Heidelberg, (Fig. 12 und Fig. 13) 7. (Titelanimation) Bei Fragen wegen der Unvollständigkeit des Literaturverzeichnisses bitte an: benjamin.andrae@web.de
Vorlesung Statistische Mechanik: Ising-Modell
 Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
E 3. Ergänzungen zu Kapitel 3
 E 3. Ergänzungen zu Kapitel 3 1 E 3.1 Kritisches Verhalten des van der Waals Gases 2 E 3.2 Kritisches Verhalten des Ising Spin-1/2 Modells 3 E 3.3 Theorie von Lee und Yang 4 E 3.4 Skalenhypothese nach
E 3. Ergänzungen zu Kapitel 3 1 E 3.1 Kritisches Verhalten des van der Waals Gases 2 E 3.2 Kritisches Verhalten des Ising Spin-1/2 Modells 3 E 3.3 Theorie von Lee und Yang 4 E 3.4 Skalenhypothese nach
Karlsruher Institut für Technologie Festkörperphysik. Übungen zur Theoretischen Physik F SS 10
 Karlsruher Institut für Technologie Institut für Theoretische Festkörperphysik Übungen zur Theoretischen Physik F SS 10 Prof. Dr. G. Schön Lösungsvorschlag zu Blatt 2 Dr. J. Cole 30.04.2010 1. Van-der-Waals
Karlsruher Institut für Technologie Institut für Theoretische Festkörperphysik Übungen zur Theoretischen Physik F SS 10 Prof. Dr. G. Schön Lösungsvorschlag zu Blatt 2 Dr. J. Cole 30.04.2010 1. Van-der-Waals
Thermodynamik und Statistische Mechanik WS2014/2015
 Thermodynamik und Statistische Mechanik WS2014/2015 Martin E. Garcia Theoretische Physik, FB 10, Universität Kassel Email: garcia@physik.uni-kassel.de Vorlesungsübersicht 1) Einführung: -Makroskopische
Thermodynamik und Statistische Mechanik WS2014/2015 Martin E. Garcia Theoretische Physik, FB 10, Universität Kassel Email: garcia@physik.uni-kassel.de Vorlesungsübersicht 1) Einführung: -Makroskopische
Erreichte Punktzahlen: Die Bearbeitungszeit beträgt 3 Stunden.
 Fakultät für Physik der LMU München Prof. Ilka Brunner Vorlesung T4p, WS08/09 Klausur am 11. Februar 2009 Name: Matrikelnummer: Erreichte Punktzahlen: 1.1 1.2 1.3 2.1 2.2 2.3 2.4 Hinweise Die Bearbeitungszeit
Fakultät für Physik der LMU München Prof. Ilka Brunner Vorlesung T4p, WS08/09 Klausur am 11. Februar 2009 Name: Matrikelnummer: Erreichte Punktzahlen: 1.1 1.2 1.3 2.1 2.2 2.3 2.4 Hinweise Die Bearbeitungszeit
3. Diffusion und Brechungsindex
 3. Diffusion und Brechungsinde Die Diffusion in und aus einer Schicht ist die Grundlage vieler Sensoreffekte, wobei sich die einzelnen Sensoren dann nur noch in der Art der Übersetzung in ein meßbares
3. Diffusion und Brechungsinde Die Diffusion in und aus einer Schicht ist die Grundlage vieler Sensoreffekte, wobei sich die einzelnen Sensoren dann nur noch in der Art der Übersetzung in ein meßbares
Analysis III Gewöhnliche Differentialgleichungen 3. Übungsblatt (mit Lösungshinweisen)
 Analysis III Gewöhnliche Differentialgleichungen 3. Übungsblatt (mit Lösungshinweisen) Fachbereich Mathematik Wintersemester 0/0 Prof. Dr. Burkhard Kümmerer./3. November 0 Andreas Gärtner Walter Reußwig
Analysis III Gewöhnliche Differentialgleichungen 3. Übungsblatt (mit Lösungshinweisen) Fachbereich Mathematik Wintersemester 0/0 Prof. Dr. Burkhard Kümmerer./3. November 0 Andreas Gärtner Walter Reußwig
Werner Langbein. Thermodynamik. Gleichgewicht, Irreversible Prozesse, Schwankungen. Verlag Harri Deutsch
 Werner Langbein Thermodynamik Gleichgewicht, Irreversible Prozesse, Schwankungen Verlag Harri Deutsch Einleitung 1 1 Gleichgewichtsthermodynaimiik 3 1 Thermodynamische Systeme 5 1.1 Geometrie und Inventar
Werner Langbein Thermodynamik Gleichgewicht, Irreversible Prozesse, Schwankungen Verlag Harri Deutsch Einleitung 1 1 Gleichgewichtsthermodynaimiik 3 1 Thermodynamische Systeme 5 1.1 Geometrie und Inventar
6. Boltzmann Gleichung
 6. Boltzmann Gleichung 1 6.1 Herleitung der Boltzmann Gleichung 2 6.2 H-Theorem 3 6.3 Transportphänomene G. Kahl (Institut für Theoretische Physik) Statistische Physik II Kapitel 6 3. Juni 2013 1 / 23
6. Boltzmann Gleichung 1 6.1 Herleitung der Boltzmann Gleichung 2 6.2 H-Theorem 3 6.3 Transportphänomene G. Kahl (Institut für Theoretische Physik) Statistische Physik II Kapitel 6 3. Juni 2013 1 / 23
Statistische Thermodynamik I Lösungen zur Serie 11
 Statistische Thermodynamik I Lösungen zur Serie Verschiedenes 20 Mai 206 Barometrische Höhenformel: Betrachte die rdatmosphäre im homogenen Gravitationspotential M gz der rde Unter der Annahme, dass sich
Statistische Thermodynamik I Lösungen zur Serie Verschiedenes 20 Mai 206 Barometrische Höhenformel: Betrachte die rdatmosphäre im homogenen Gravitationspotential M gz der rde Unter der Annahme, dass sich
Exkurs: Method of multiple scales (Mehrskalen Methode)
 Exkurs: Method of multiple scales (Mehrskalen Methode) dr. karin mora* Im folgenden betrachten wir nichtlineare dynamische Systeme (NDS) mit sogenannten kleinen nichtlinearen Termen. Viele mathematische
Exkurs: Method of multiple scales (Mehrskalen Methode) dr. karin mora* Im folgenden betrachten wir nichtlineare dynamische Systeme (NDS) mit sogenannten kleinen nichtlinearen Termen. Viele mathematische
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt
BASISPRÜFUNG MATHEMATIK I UND II
 ETH Zürich Sommer 015 Dr. Ana Cannas BASISPRÜFUNG MATHEMATIK I UND II für die Studiengänge Agrar-, Erd-, Lebensmittelund Umweltnaturwissenschaften 1. Sei a) Ist das System lösbar? b) Lösen Sie das System
ETH Zürich Sommer 015 Dr. Ana Cannas BASISPRÜFUNG MATHEMATIK I UND II für die Studiengänge Agrar-, Erd-, Lebensmittelund Umweltnaturwissenschaften 1. Sei a) Ist das System lösbar? b) Lösen Sie das System
= n + + Thermodynamik von Elektrolytlösungen. Wdhlg: Chemisches Potential einer Teilchenart: Für Elektrolytlösungen gilt: wobei : und
 Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmetrie und physikalische Eigenschaften, Neumannsches Prinzip
 PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmeie und physikalische Eigenschaften, Neumannsches Prinzip 2. Thermodynamik fester Körper Phänomenologische Thermodynamik (Potentiale,
PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmeie und physikalische Eigenschaften, Neumannsches Prinzip 2. Thermodynamik fester Körper Phänomenologische Thermodynamik (Potentiale,
Thermodynamik. Christian Britz
 Hauptsätze der Klassische nanoskaliger Systeme 04.02.2013 Inhalt Einleitung Hauptsätze der Klassische nanoskaliger Systeme 1 Einleitung 2 Hauptsätze der 3 4 Klassische 5 6 7 nanoskaliger Systeme 8 Hauptsätze
Hauptsätze der Klassische nanoskaliger Systeme 04.02.2013 Inhalt Einleitung Hauptsätze der Klassische nanoskaliger Systeme 1 Einleitung 2 Hauptsätze der 3 4 Klassische 5 6 7 nanoskaliger Systeme 8 Hauptsätze
PROBEPRÜFUNG MATHEMATIK I UND II
 PROBEPRÜFUNG MATHEMATIK I UND II für die Studiengänge Agrar-, Erd-, Lebensmittelund Umweltnaturwissenschaften Für diese Probeprüfung sind ca 4 Stunden vorgesehen. Die eigentliche Prüfung wird signifikant
PROBEPRÜFUNG MATHEMATIK I UND II für die Studiengänge Agrar-, Erd-, Lebensmittelund Umweltnaturwissenschaften Für diese Probeprüfung sind ca 4 Stunden vorgesehen. Die eigentliche Prüfung wird signifikant
Differentialgleichungen
 Kapitel Differentialgleichungen Josef Leydold Mathematik für VW WS 05/6 Differentialgleichungen / Ein einfaches Modell (Domar) Im Domar Wachstumsmodell treffen wir die folgenden Annahmen: () Erhöhung der
Kapitel Differentialgleichungen Josef Leydold Mathematik für VW WS 05/6 Differentialgleichungen / Ein einfaches Modell (Domar) Im Domar Wachstumsmodell treffen wir die folgenden Annahmen: () Erhöhung der
Die innere Energie and die Entropie
 Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Virialentwicklung. Janek Landsberg Fakultät für Physik, LMU München. Janek Landsberg. Die Virialentwicklung. Verschiedene Potentiale
 Die Warum Fakultät für Physik, LMU München 14.06.2006 Die Warum 1 Die Der zweite Virialkoeffizient 2 Hard-Sphere-Potential Lennard-Jones-Potential 3 Warum 4 Bsp. Hard-Sphere-Potential Asakura-Oosawa-Potential
Die Warum Fakultät für Physik, LMU München 14.06.2006 Die Warum 1 Die Der zweite Virialkoeffizient 2 Hard-Sphere-Potential Lennard-Jones-Potential 3 Warum 4 Bsp. Hard-Sphere-Potential Asakura-Oosawa-Potential
5. Die Thermodynamischen Potentiale
 5. Die hermodynamischen Potentiale 5.1. Einführung der Potentiale Gibbs'sche Fundamentalgleichung. d = du + d, du + d δ Q d = = Ist die Entroie als Funktion von U und bekannt, = ( U, ) dann lassen sich
5. Die hermodynamischen Potentiale 5.1. Einführung der Potentiale Gibbs'sche Fundamentalgleichung. d = du + d, du + d δ Q d = = Ist die Entroie als Funktion von U und bekannt, = ( U, ) dann lassen sich
Probeklausur STATISTISCHE PHYSIK PLUS
 DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
Auswahl von Prüfungsfragen für die Prüfungen im September 2011
 Auswahl von Prüfungsfragen für die Prüfungen im September 2011 Was ist / sind / bedeutet / verstehen Sie unter... Wie nennt man / lautet / Wann spricht man von / Definieren Sie... Die anschließenden Fragen
Auswahl von Prüfungsfragen für die Prüfungen im September 2011 Was ist / sind / bedeutet / verstehen Sie unter... Wie nennt man / lautet / Wann spricht man von / Definieren Sie... Die anschließenden Fragen
Schwartz-Raum (Teil 1)
 Schwartz-Raum (Teil 1) Federico Remonda, Robin Krom 10. Januar 2008 Zusammenfassung Der Schwartz-Raum ist ein Funktionenraum, der besondere Regularitätseigenschaften besitzt, die uns bei der Fouriertransformation
Schwartz-Raum (Teil 1) Federico Remonda, Robin Krom 10. Januar 2008 Zusammenfassung Der Schwartz-Raum ist ein Funktionenraum, der besondere Regularitätseigenschaften besitzt, die uns bei der Fouriertransformation
Informationen. Anmeldung erforderlich: ab :00 bis spätestens :00
 10 Informationen Anmeldung erforderlich: ab 1.3. 16:00 bis spätestens 8. 3. 09:00 online im TISS (i (tiss.tuwien.ac.at) i Tutorium: Fr. 10:00 11:00, 11:00, Beginn: 15.3.2013 Gruppeneinteilung wird auf
10 Informationen Anmeldung erforderlich: ab 1.3. 16:00 bis spätestens 8. 3. 09:00 online im TISS (i (tiss.tuwien.ac.at) i Tutorium: Fr. 10:00 11:00, 11:00, Beginn: 15.3.2013 Gruppeneinteilung wird auf
Modelle zur Beschreibung von Gasen und deren Eigenschaften
 Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
6.2 Zweiter HS der Thermodynamik
 Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Thermodynamik und Statistische Mechanik
 Theoretische Physik Band 9 Walter Greiner Ludwig Neise Horst Stöcker Thermodynamik und Statistische Mechanik Ein Lehr- und Übungsbuch Mit zahlreichen Abbildungen, Beispielen und Aufgaben mit ausführlichen
Theoretische Physik Band 9 Walter Greiner Ludwig Neise Horst Stöcker Thermodynamik und Statistische Mechanik Ein Lehr- und Übungsbuch Mit zahlreichen Abbildungen, Beispielen und Aufgaben mit ausführlichen
Proseminar: Theoretische Physik. und Astroteilchenphysik. Fermi- und Bose Gase. Thermodynamisches Gleichgewicht
 Proseminar: Theoretische Physik und Astroteilchenphysik Thermodynamisches Gleichgewicht Fermi- und Bose Gase Inhalt 1. Entropie 2. 2ter Hauptsatz der Thermodynamik 3. Verteilungsfunktion 1. Bosonen und
Proseminar: Theoretische Physik und Astroteilchenphysik Thermodynamisches Gleichgewicht Fermi- und Bose Gase Inhalt 1. Entropie 2. 2ter Hauptsatz der Thermodynamik 3. Verteilungsfunktion 1. Bosonen und
Einführung in einige Teilbereiche der Wirtschaftsmathematik für Studierende des Wirtschaftsingenieurwesens
 in einige Teilbereiche der für Studierende des Wirtschaftsingenieurwesens Sommersemester 2013 Hochschule Augsburg : Gliederung 1 Finanzmathematik 2 Lineare Programme 3 Differentialgleichungen 4 Statistik:
in einige Teilbereiche der für Studierende des Wirtschaftsingenieurwesens Sommersemester 2013 Hochschule Augsburg : Gliederung 1 Finanzmathematik 2 Lineare Programme 3 Differentialgleichungen 4 Statistik:
Thermodynamik un Statistische Mechanik
 Theoretische Physik Band 9 Walter Greiner Ludwig Neise Horst Stöcker Thermodynamik un Statistische Mechanik Ein Lehr- und Übungsbuch Mit zahlreichen Abbildungen, Beispiele n und Aufgaben mit ausführlichen
Theoretische Physik Band 9 Walter Greiner Ludwig Neise Horst Stöcker Thermodynamik un Statistische Mechanik Ein Lehr- und Übungsbuch Mit zahlreichen Abbildungen, Beispiele n und Aufgaben mit ausführlichen
Differentialgleichungen
 Differentialgleichungen Eine einfache Differentialgleichung löst man bereits beim Integrieren in der Oberstufe. Sie hat die Form y (x) = f(x) und y wird gesucht. Beispiel: y (x) = 6x² - 4x + 1 fl y(x)
Differentialgleichungen Eine einfache Differentialgleichung löst man bereits beim Integrieren in der Oberstufe. Sie hat die Form y (x) = f(x) und y wird gesucht. Beispiel: y (x) = 6x² - 4x + 1 fl y(x)
8.3 Ausgleichsprozesse in abgeschlossenen und nichtabgeschlossenen Systemen - thermodynamisches Gleichgewicht und thermodynamische Potentiale
 8.3 Ausgleichsprozesse in abgeschlossenen und nichtabgeschlossenen Systemen - thermodynamisches Gleichgewicht und thermodynamische Potentiale Rückschau: Mechanisches Gleichgewicht und Stabilität Ein Körper
8.3 Ausgleichsprozesse in abgeschlossenen und nichtabgeschlossenen Systemen - thermodynamisches Gleichgewicht und thermodynamische Potentiale Rückschau: Mechanisches Gleichgewicht und Stabilität Ein Körper
Prüfungsvorbereitungskurs Höhere Mathematik 3
 Prüfungsvorbereitungskurs Höhere Mathematik 3 Gewöhnliche Differentialgleichungen Marco Boßle Jörg Hörner Mathematik Online Frühjahr 2011 PV-Kurs HM 3 Gew. DGl 1-1 Zusammenfassung y (x) = F (x, y) Allgemeine
Prüfungsvorbereitungskurs Höhere Mathematik 3 Gewöhnliche Differentialgleichungen Marco Boßle Jörg Hörner Mathematik Online Frühjahr 2011 PV-Kurs HM 3 Gew. DGl 1-1 Zusammenfassung y (x) = F (x, y) Allgemeine
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt 6
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Moderne Theoretische Physik III (Theorie F Statistische Mechanik SS 7 Prof. Dr. Alexander Mirlin Musterlösung: Blatt 6
Tunneleekt und Tunnelhamiltonian. Lukas Ogrodowski. Institut für Physik Albert-Ludwigs-Universität Freiburg. Quantendynamik in mesoskopischen Systemen
 Tunneleekt und Tunnelhamiltonian Lukas Ogrodowski Institut für Physik Albert-Ludwigs-Universität Freiburg Quantendynamik in mesoskopischen Systemen Gliederung 1 Motivation 2 Tunneleekt 3 Tunnelhamiltonian
Tunneleekt und Tunnelhamiltonian Lukas Ogrodowski Institut für Physik Albert-Ludwigs-Universität Freiburg Quantendynamik in mesoskopischen Systemen Gliederung 1 Motivation 2 Tunneleekt 3 Tunnelhamiltonian
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
1 Massenwirkungsgesetz
 1 Massenwirkungsgesetz Zeige: Bei konstantem Druck und konstanter emperatur gilt für chemische Reaktionen der Art a 1 A 1 + a A + : : : a L A L b 1 B 1 + b B + : : : b R B R : K c (A i ) ai c (B j ) bj
1 Massenwirkungsgesetz Zeige: Bei konstantem Druck und konstanter emperatur gilt für chemische Reaktionen der Art a 1 A 1 + a A + : : : a L A L b 1 B 1 + b B + : : : b R B R : K c (A i ) ai c (B j ) bj
16 Vektorfelder und 1-Formen
 45 16 Vektorfelder und 1-Formen 16.1 Vektorfelder Ein Vektorfeld v auf D R n ist eine Abbildung v : D R n, x v(x). Beispiele. Elektrisches und Magnetisches Feld E(x), B(x), Geschwindigkeitsfeld einer Strömung
45 16 Vektorfelder und 1-Formen 16.1 Vektorfelder Ein Vektorfeld v auf D R n ist eine Abbildung v : D R n, x v(x). Beispiele. Elektrisches und Magnetisches Feld E(x), B(x), Geschwindigkeitsfeld einer Strömung
3 Der 1. Hauptsatz der Thermodynamik
 3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
9. Phasengleichgewichte und Zustandsänderungen 9.1 Einkompentige Systeme
 9. Phasengleichgewichte und Zustandsänderungen 9.1 Einkompentige Systeme Temperaturabhängigkeit der freien Enthalpie dg = d( H TS ) = dh T ds S dt = C P dt TC P T H Da S > 0, nimmt G mit zunehmender Temperatur
9. Phasengleichgewichte und Zustandsänderungen 9.1 Einkompentige Systeme Temperaturabhängigkeit der freien Enthalpie dg = d( H TS ) = dh T ds S dt = C P dt TC P T H Da S > 0, nimmt G mit zunehmender Temperatur
Quantenmechanik I Sommersemester QM Web Page teaching/ss13/qm1.d.html
 Quantenmechanik I Sommersemester 2013 QM Web Page http://einrichtungen.physik.tu-muenchen.de/t30e/ teaching/ss13/qm1.d.html Hinweise Zusätzliche Übung: Aufgrund des großen Andrangs bieten wir eine zusätzliche
Quantenmechanik I Sommersemester 2013 QM Web Page http://einrichtungen.physik.tu-muenchen.de/t30e/ teaching/ss13/qm1.d.html Hinweise Zusätzliche Übung: Aufgrund des großen Andrangs bieten wir eine zusätzliche
Stabilität des isotropen Kristallwachstums nach TILLER sowie nach MULLINS und SEKERKA
 tabilität des isotropen Kristallwachstums nach TIER sowie nach MUIN und EKERKA liederung 1. Definition von Wachstumsstabilität 2. Konstitutionelle Unterkühlung das TIER-Kriterium 3. Dynamische törungstheorie
tabilität des isotropen Kristallwachstums nach TIER sowie nach MUIN und EKERKA liederung 1. Definition von Wachstumsstabilität 2. Konstitutionelle Unterkühlung das TIER-Kriterium 3. Dynamische törungstheorie
5 Interpolation und Approximation
 5 Interpolation und Approximation Problemstellung: Es soll eine Funktion f(x) approximiert werden, von der die Funktionswerte nur an diskreten Stellen bekannt sind. 5. Das Interpolationspolynom y y = P(x)
5 Interpolation und Approximation Problemstellung: Es soll eine Funktion f(x) approximiert werden, von der die Funktionswerte nur an diskreten Stellen bekannt sind. 5. Das Interpolationspolynom y y = P(x)
Relativistische Quantenmechanik und die Klein-Gordon Gleichung
 Relativistische Quantenmechanik und die Klein-Gordon Gleichung Oliver Smith o smit01 wwu.de) 17. Februar 2015 Wir wollen die Klein-Gordon Gleichung untersuchen und Formalismen einführen, um Parallelen
Relativistische Quantenmechanik und die Klein-Gordon Gleichung Oliver Smith o smit01 wwu.de) 17. Februar 2015 Wir wollen die Klein-Gordon Gleichung untersuchen und Formalismen einführen, um Parallelen
5 Harmonische Funktionen
 5 Harmonische Funktionen Generell kann man die allgemeine Lösung des elektrostatischen andwertproblems auch als Summe einer speziellen Lösung der Poisson-Gleichung und einer Lösung der Laplace-Gleichung
5 Harmonische Funktionen Generell kann man die allgemeine Lösung des elektrostatischen andwertproblems auch als Summe einer speziellen Lösung der Poisson-Gleichung und einer Lösung der Laplace-Gleichung
4 Gewöhnliche Differentialgleichungen
 4 Gewöhnliche Differentialgleichungen 4.1 Einleitung Definition 4.1 Gewöhnliche Differentialgleichung n-ter Ordnung Eine Gleichung, in der Ableitungen einer unbekannten Funktion y = y(x) bis zur n-ten
4 Gewöhnliche Differentialgleichungen 4.1 Einleitung Definition 4.1 Gewöhnliche Differentialgleichung n-ter Ordnung Eine Gleichung, in der Ableitungen einer unbekannten Funktion y = y(x) bis zur n-ten
Transport Einführung
 Transport Einführung home/lehre/vl-mhs-1/inhalt/folien/vorlesung/8_transport/deckblatt.tex Seite 1 von 24. p.1/24 1. Einführung 2. Transportgleichung 3. Analytische Lösung Inhaltsverzeichnis 4. Diskretisierung
Transport Einführung home/lehre/vl-mhs-1/inhalt/folien/vorlesung/8_transport/deckblatt.tex Seite 1 von 24. p.1/24 1. Einführung 2. Transportgleichung 3. Analytische Lösung Inhaltsverzeichnis 4. Diskretisierung
Topologie und Differentialrechnung mehrerer Veränderlicher, SS 2009 Modulprüfung/Abschlussklausur. Aufgabe Punkte
 Universität München 22. Juli 29 Topologie und Differentialrechnung mehrerer Veränderlicher, SS 29 Modulprüfung/Abschlussklausur Name: Aufgabe 2 3 4 Punkte Gesamtpunktzahl: Gesamturteil: Schreiben Sie unbedingt
Universität München 22. Juli 29 Topologie und Differentialrechnung mehrerer Veränderlicher, SS 29 Modulprüfung/Abschlussklausur Name: Aufgabe 2 3 4 Punkte Gesamtpunktzahl: Gesamturteil: Schreiben Sie unbedingt
Probestudium der Physik 2011/12
 Probestudium der Physik 2011/12 Karsten Kruse 2. Mechanische Schwingungen und Wellen - Theoretische Betrachtungen 2.1 Der harmonische Oszillator Wir betrachten eine lineare Feder mit der Ruhelänge l 0.
Probestudium der Physik 2011/12 Karsten Kruse 2. Mechanische Schwingungen und Wellen - Theoretische Betrachtungen 2.1 Der harmonische Oszillator Wir betrachten eine lineare Feder mit der Ruhelänge l 0.
d) Das ideale Gas makroskopisch
 d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
P = P(T, v) = k BT v b a v 2 (37.1)
 37 Van der Waals-Gas Das van der Waals-Gas wird als ein Modell für den Phasenübergang gasförmig flüssig vorgestellt und untersucht Van der Waals hat dieses Modell 1873 in seiner Doktorarbeit eingeführt
37 Van der Waals-Gas Das van der Waals-Gas wird als ein Modell für den Phasenübergang gasförmig flüssig vorgestellt und untersucht Van der Waals hat dieses Modell 1873 in seiner Doktorarbeit eingeführt
16 Elektromagnetische Wellen
 16 Elektromagnetische Wellen In den folgenden Kapiteln werden wir uns verschiedenen zeitabhängigen Phänomenen zuwenden. Zunächst werden wir uns mit elektromagnetischen Wellen beschäftigen und sehen, dass
16 Elektromagnetische Wellen In den folgenden Kapiteln werden wir uns verschiedenen zeitabhängigen Phänomenen zuwenden. Zunächst werden wir uns mit elektromagnetischen Wellen beschäftigen und sehen, dass
Ruprecht-Karls-Universität Heidelberg Vorbereitung zur Diplomprüfung Theoretische Physik
 Ruprecht-Karls-Universität Heidelberg Vorbereitung zur Diplomprüfung Theoretische Physik begleitend zur Vorlesung Statistische Mechanik und Thermodynamik WS 2006/2007 Prof. Dr. Dieter W. Heermann erstellt
Ruprecht-Karls-Universität Heidelberg Vorbereitung zur Diplomprüfung Theoretische Physik begleitend zur Vorlesung Statistische Mechanik und Thermodynamik WS 2006/2007 Prof. Dr. Dieter W. Heermann erstellt
Vorlesungsfolien Mathematik 3 WS 2010/11 UMIT. Einleitung
 Vorlesungsfolien Mathematik 3 WS 2010/11 Dr. Leonhard Wieser UMIT Einleitung Begriff Vektoranalysis: Kombination aus Linearer Algebra/Vektorrechnung mit Differential- und Integralrechnung Inhaltsangabe:
Vorlesungsfolien Mathematik 3 WS 2010/11 Dr. Leonhard Wieser UMIT Einleitung Begriff Vektoranalysis: Kombination aus Linearer Algebra/Vektorrechnung mit Differential- und Integralrechnung Inhaltsangabe:
Mehrdimensionale Integralrechnung 2
 Mehrdimensionale Integralrechnung Quiz Wir wollen die Dynamik zweier Teilchen beschreiben, die über ein hoch elastisches Seil verbunden sind und sich wild im Raum bewegen! Ein Kollege schlägt dazu vor
Mehrdimensionale Integralrechnung Quiz Wir wollen die Dynamik zweier Teilchen beschreiben, die über ein hoch elastisches Seil verbunden sind und sich wild im Raum bewegen! Ein Kollege schlägt dazu vor
Seminar zur Theorie der Teilchen und Felder. Kritische Phänomene. Florian König WS 2009/2010
 Seminar zur Theorie der Teilchen und Felder Kritische Phänomene Florian König WS 2009/2010 1 Phasendiagramme Thermodynamische Systeme treten oft in mehreren unterschiedlichen Phasen in Erscheinung. In
Seminar zur Theorie der Teilchen und Felder Kritische Phänomene Florian König WS 2009/2010 1 Phasendiagramme Thermodynamische Systeme treten oft in mehreren unterschiedlichen Phasen in Erscheinung. In
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 05. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 05. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 05. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 05. 07. 2007 Klausur Die Klausur
Grundlagen der Physik 2 Schwingungen und Wärmelehre
 Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik 14. 06. 2007 Othmar Marti (Universität Ulm) Schwingungen und Wärmelehre 14. 06.
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik 14. 06. 2007 Othmar Marti (Universität Ulm) Schwingungen und Wärmelehre 14. 06.
Schweredruck von Flüssigkeiten
 Schweredruck von Flüssigkeiten Flüssigkeiten sind nahezu inkompressibel. Kompressibilität κ: Typische Werte: Wasser: 4.6 10-5 1/bar @ 0ºC Quecksilber: 4 10-6 1/bar @ 0ºC Pentan: 4. 10-6 1/bar @ 0ºC Dichte
Schweredruck von Flüssigkeiten Flüssigkeiten sind nahezu inkompressibel. Kompressibilität κ: Typische Werte: Wasser: 4.6 10-5 1/bar @ 0ºC Quecksilber: 4 10-6 1/bar @ 0ºC Pentan: 4. 10-6 1/bar @ 0ºC Dichte
8.3 Ausgleichsprozesse in abgeschlossenen Systemen, thermodynamisches Gleichgewicht und thermodynamische Potentiale
 8.3 Ausgleichsprozesse in abgeschlossenen Systemen, thermodynamisches Gleichgewicht und thermodynamische Potentiale Rückschau: Mechanisches Gleichgewicht und Stabilität Ein Körper ist im Gleichgewicht,
8.3 Ausgleichsprozesse in abgeschlossenen Systemen, thermodynamisches Gleichgewicht und thermodynamische Potentiale Rückschau: Mechanisches Gleichgewicht und Stabilität Ein Körper ist im Gleichgewicht,
1. Die Wellengleichung
 1. Die Wellengleichung Die Wellengleichung ist eine partielle Differenzialgleichung für das Schallfeld. Sie lässt sich durch Linearisierung aus der Massenbilanz, der Impulsbilanz und der Energiebilanz
1. Die Wellengleichung Die Wellengleichung ist eine partielle Differenzialgleichung für das Schallfeld. Sie lässt sich durch Linearisierung aus der Massenbilanz, der Impulsbilanz und der Energiebilanz
6.1 Gleichgewichts- und Stabilitätsbedingungen
 4. Woche 6.1 Gleichgewichts- und Stabilitätsbedingungen 6.1.1 Extremaleigenschaften der Potentiale Die Hauptsätze der Thermodynamik lauten du δq pdv (das Erste) und (das Zweite). Da (für dn 0) δq TdS gilt
4. Woche 6.1 Gleichgewichts- und Stabilitätsbedingungen 6.1.1 Extremaleigenschaften der Potentiale Die Hauptsätze der Thermodynamik lauten du δq pdv (das Erste) und (das Zweite). Da (für dn 0) δq TdS gilt
u v w v = 1 w u w u v schon in der Mathematik gesehen?
 Die Kettenregel für die Thermodynamik Ziel ist die in der Thermodynamik benutzten Differentiationsregeln die auf den ersten Blick nicht denen aus der Mathematik ähneln doch als dieselben zu beschreiben
Die Kettenregel für die Thermodynamik Ziel ist die in der Thermodynamik benutzten Differentiationsregeln die auf den ersten Blick nicht denen aus der Mathematik ähneln doch als dieselben zu beschreiben
I el U el. P el W V 23+W F23. Musterlösung SS Aufgabe (34 Punkte) a) Energiebilanz für die Kammer A im Zeitintervall t 12 :
 Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Fokker-Planck Gleichung
 Fokker-Planck Gleichung Max Haardt WWU Münster 21. November 2008 Inhalt 1 Einleitung Langevin Gleichung Fokker-Planck Gleichung 2 Herleitung Mastergleichung Kramers-Moyal Entwicklung Fokker-Planck Gleichung
Fokker-Planck Gleichung Max Haardt WWU Münster 21. November 2008 Inhalt 1 Einleitung Langevin Gleichung Fokker-Planck Gleichung 2 Herleitung Mastergleichung Kramers-Moyal Entwicklung Fokker-Planck Gleichung
X.4 Elektromagnetische Wellen im Vakuum
 X.4 Elektromagnetische Wellen im Vakuum 173 X.4 Elektromagnetische Wellen im Vakuum In Abwesenheit von Quellen, ρ el. = 0 j el. = 0, nehmen die Bewegungsgleichungen (X.9) (X.11) für die elektromagnetischen
X.4 Elektromagnetische Wellen im Vakuum 173 X.4 Elektromagnetische Wellen im Vakuum In Abwesenheit von Quellen, ρ el. = 0 j el. = 0, nehmen die Bewegungsgleichungen (X.9) (X.11) für die elektromagnetischen
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test
 PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
2.2 4-Stromdichte [Griffiths , Jackson 11.9]
![2.2 4-Stromdichte [Griffiths , Jackson 11.9] 2.2 4-Stromdichte [Griffiths , Jackson 11.9]](/thumbs/52/29912127.jpg) Um zu verstehen, wie sich die elektromagnetischen Felder transformieren, gehen wir von den Maxwellgleichungen aus. Dazu brauchen wir zunächst die. 4-Stromdichte [Griffiths 1.3.4, Jackson 11.9] Die Ladungsdichte
Um zu verstehen, wie sich die elektromagnetischen Felder transformieren, gehen wir von den Maxwellgleichungen aus. Dazu brauchen wir zunächst die. 4-Stromdichte [Griffiths 1.3.4, Jackson 11.9] Die Ladungsdichte
Diskrete Populationsmodelle für Einzelspezies
 Diskrete Populationsmodelle für Einzelspezies Lisa Zang 30.10.2012 Quelle: J. D. Murray: Mathematical Biology: I. An Introduction, Third Edition, Springer Inhaltsverzeichnis 1. Einführung Einfache Modelle
Diskrete Populationsmodelle für Einzelspezies Lisa Zang 30.10.2012 Quelle: J. D. Murray: Mathematical Biology: I. An Introduction, Third Edition, Springer Inhaltsverzeichnis 1. Einführung Einfache Modelle
Verallgemeinerte Funktionen
 Verallgemeinerte Funktionen. Der Raum der Grundfunktionen Für den Vektorraum R n, n N, über R betrachten wir die Euklidische Norm kk W R n! R; v x 7! p ux x > x WD t n und bezeichnen eine Menge A R n als
Verallgemeinerte Funktionen. Der Raum der Grundfunktionen Für den Vektorraum R n, n N, über R betrachten wir die Euklidische Norm kk W R n! R; v x 7! p ux x > x WD t n und bezeichnen eine Menge A R n als
Seminar Level Set Methoden
 Seminar Level Set Methoden Geometric Flows and Variational Methods Michael Möller Institut für Numerische und Angewandte Mathematik Fachbereich Mathematik und Informatik WWU Münster SS 2007 1. Einführung
Seminar Level Set Methoden Geometric Flows and Variational Methods Michael Möller Institut für Numerische und Angewandte Mathematik Fachbereich Mathematik und Informatik WWU Münster SS 2007 1. Einführung
Moleküldynamik. Modell: Klassische Mechanik Newtonsche Bewegungsgleichungen. = m a i
 Mikroskopische Simulation der Molekülbewegungen Moleküldynamik Statistische Mechanik Modell: Klassische Mechanik Newtonsche Bewegungsgleichungen Makroskopische igenschaften des Systems (nergie, Temp, Druck,
Mikroskopische Simulation der Molekülbewegungen Moleküldynamik Statistische Mechanik Modell: Klassische Mechanik Newtonsche Bewegungsgleichungen Makroskopische igenschaften des Systems (nergie, Temp, Druck,
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Inhalt der Vorlesung. 1. Eigenschaften der Gase. 0. Einführung
 Inhalt der Vorlesung 0. Einführung 0.1 Themen der Physikal. Chemie 0.2 Grundbegriffe/ Zentrale Größe: Energie 0.3 Molekulare Deutung der inneren Energie U Molekülstruktur, Energieniveaus und elektromagn.
Inhalt der Vorlesung 0. Einführung 0.1 Themen der Physikal. Chemie 0.2 Grundbegriffe/ Zentrale Größe: Energie 0.3 Molekulare Deutung der inneren Energie U Molekülstruktur, Energieniveaus und elektromagn.
Höhere Mathematik II für die Fachrichtung Physik. Modulprüfung
 Institut für Analysis SS7 PD Dr. Peer Christian Kunstmann 8.9.7 Höhere Mathematik II für die Fachrichtung Physik Modulprüfung Aufgabe [5+5= Punkte] (a) Zeigen Sie, dass die Matrix α A α =, α. genau dann
Institut für Analysis SS7 PD Dr. Peer Christian Kunstmann 8.9.7 Höhere Mathematik II für die Fachrichtung Physik Modulprüfung Aufgabe [5+5= Punkte] (a) Zeigen Sie, dass die Matrix α A α =, α. genau dann
TP2: Elektrodynamik WS Arbeitsblatt 10 21/ Dipole und Multipole in stationären Feldern
 TP2: Elektrodynamik WS 2017-2018 Arbeitsblatt 10 21/22.12. 2017 Dipole und Multipole in stationären Feldern Die Multipolentwicklung ist eine hilfreiche Näherung zur Lösung der Poisson Gleichung, wenn eine
TP2: Elektrodynamik WS 2017-2018 Arbeitsblatt 10 21/22.12. 2017 Dipole und Multipole in stationären Feldern Die Multipolentwicklung ist eine hilfreiche Näherung zur Lösung der Poisson Gleichung, wenn eine
Systeme von Differentialgleichungen. Beispiel 1: Chemische Reaktionssysteme. Beispiel 2. System aus n Differentialgleichungen 1. Ordnung: y 1.
 Systeme von Differentialgleichungen Beispiel : Chemische Reaktionssysteme System aus n Differentialgleichungen Ordnung: y (x = f (x, y (x,, y n (x Kurzschreibweise: y y 2 (x = f 2(x, y (x,, y n (x y n(x
Systeme von Differentialgleichungen Beispiel : Chemische Reaktionssysteme System aus n Differentialgleichungen Ordnung: y (x = f (x, y (x,, y n (x Kurzschreibweise: y y 2 (x = f 2(x, y (x,, y n (x y n(x
Lösung zu den Testaufgaben zur Mathematik für Chemiker II (Analysis)
 Universität D U I S B U R G E S S E N Campus Essen, Mathematik PD Dr. L. Strüngmann Informationen zur Veranstaltung unter: http://www.uni-due.de/algebra-logic/struengmann.shtml SS 7 Lösung zu den Testaufgaben
Universität D U I S B U R G E S S E N Campus Essen, Mathematik PD Dr. L. Strüngmann Informationen zur Veranstaltung unter: http://www.uni-due.de/algebra-logic/struengmann.shtml SS 7 Lösung zu den Testaufgaben
Landau-Theorie der Phasenumwandlung von Membranen
 Landau-Theorie der Phasenumwandlung von Membranen Vorbemerkung Vorbemerkung: Um Einblick in die thermodynamischen aber auch strukturellen Eigenschaften von Lipidschichten zu erhalten, ist die klassische
Landau-Theorie der Phasenumwandlung von Membranen Vorbemerkung Vorbemerkung: Um Einblick in die thermodynamischen aber auch strukturellen Eigenschaften von Lipidschichten zu erhalten, ist die klassische
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Basisprüfung, Gruppe A Analysis I/II
 Offene Aufgaben. Jeder der folgenden sieben offenen Aufgaben ist eine einzelne thematisch verwandte Single Choice-Aufgabe vorangestellt. Beantworten Sie die Single Choice Aufgabe auf dem Antwortzettel.
Offene Aufgaben. Jeder der folgenden sieben offenen Aufgaben ist eine einzelne thematisch verwandte Single Choice-Aufgabe vorangestellt. Beantworten Sie die Single Choice Aufgabe auf dem Antwortzettel.
Vorlesung Physikalische Chemie IV Statistische Thermodynamik realer chemischer Systeme"
 Vorlesung Physikalische Chemie IV Statistische Thermodynamik realer chemischer Systeme" Dietmar Paschek SS 016 Gittermodell für Mischungen Grenzen der Bragg-Williams Näherung Das Ising Modell Quasi-Chemische
Vorlesung Physikalische Chemie IV Statistische Thermodynamik realer chemischer Systeme" Dietmar Paschek SS 016 Gittermodell für Mischungen Grenzen der Bragg-Williams Näherung Das Ising Modell Quasi-Chemische
System von n gewöhnlichen DG 1. Ordnung hat die allgemeine Form:
 C7.5 Differentialgleichungen 1. Ordnung - Allgemeine Aussagen System von n gewöhnlichen DG 1. Ordnung hat die allgemeine Form: Kompaktnotation: Anfangsbedingung: Gesuchte Lösung: Gleichungen dieser Art
C7.5 Differentialgleichungen 1. Ordnung - Allgemeine Aussagen System von n gewöhnlichen DG 1. Ordnung hat die allgemeine Form: Kompaktnotation: Anfangsbedingung: Gesuchte Lösung: Gleichungen dieser Art
Einführung in die Physikalische Chemie Teil 2: Makroskopische Phänomene und Thermodynamik
 Einführung in die Phsikalische Chemie Teil 2: Makroskopische Phänomene und Thermodnamik Kapitel 7: Boltzmann-Verteilung Kapitel 8: Statistische Beschreibung makroskopischer Grössen Kapitel 9: Thermodnamik:
Einführung in die Phsikalische Chemie Teil 2: Makroskopische Phänomene und Thermodnamik Kapitel 7: Boltzmann-Verteilung Kapitel 8: Statistische Beschreibung makroskopischer Grössen Kapitel 9: Thermodnamik:
Klausur zur Statistischen Physik SS 2013
 Klausur zur Statistischen Physik SS 2013 Prof. Dr. M. Rohlfing Die folgenden Angaben bitte deutlich in Blockschrift ausfüllen: Name, Vorname: geb. am: in: Matrikel-Nr.: Übungsgruppenleiter: Aufgabe maximale
Klausur zur Statistischen Physik SS 2013 Prof. Dr. M. Rohlfing Die folgenden Angaben bitte deutlich in Blockschrift ausfüllen: Name, Vorname: geb. am: in: Matrikel-Nr.: Übungsgruppenleiter: Aufgabe maximale
Vorlesung Statistische Mechanik: N-Teilchensystem
 Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Kinetische Theorie. Übersicht: Voraussetzungen: Verteilungsfunktionen Grundgleichungen: Kollissionen
 Kinetische Theorie Übersicht: Verteilungsfunktionen Grundgleichungen: Boltzmann Vlasov Fokker-Planck Kollissionen neutral trifft neutral neutral trifft geladen geladen trifft geladen Voraussetzungen: keine
Kinetische Theorie Übersicht: Verteilungsfunktionen Grundgleichungen: Boltzmann Vlasov Fokker-Planck Kollissionen neutral trifft neutral neutral trifft geladen geladen trifft geladen Voraussetzungen: keine
Spline-Interpolation
 Spline-Interpolation Tim Schmölzer 20 November 2009 Tim Schmölzer Spline-Interpolation 20 November 2009 1 / 38 Übersicht 1 Vorbemerkungen 2 Lösbarkeit des Interpolationsproblems 3 Stabilität der Interpolation
Spline-Interpolation Tim Schmölzer 20 November 2009 Tim Schmölzer Spline-Interpolation 20 November 2009 1 / 38 Übersicht 1 Vorbemerkungen 2 Lösbarkeit des Interpolationsproblems 3 Stabilität der Interpolation
Theorie der Wärme Musterlösung 11.
 Theorie der Wärme Musterlösung. FS 05 Prof. Thomas Gehrmann Übung. Edelgas im Schwerefeld Berechne den Erwartungswert der Energie eines monoatomaren idealen Gases z. B. eines Edelgases in einem zylindrischen
Theorie der Wärme Musterlösung. FS 05 Prof. Thomas Gehrmann Übung. Edelgas im Schwerefeld Berechne den Erwartungswert der Energie eines monoatomaren idealen Gases z. B. eines Edelgases in einem zylindrischen
Kurze Einführung zu Stabilität bei Differentialgleichungen und Einschrittverfahren
 Kurze Einführung zu Stabilität bei Differentialgleichungen und Einschrittverfahren Was sind typische qualitative Aussagen bei gewöhnlichen Differentialgleichungen der Form x (t) = f(t, x)? (1) 1. Andere
Kurze Einführung zu Stabilität bei Differentialgleichungen und Einschrittverfahren Was sind typische qualitative Aussagen bei gewöhnlichen Differentialgleichungen der Form x (t) = f(t, x)? (1) 1. Andere
Zusammenfassung 118 tet, konnte den Verlauf der experimentellen Daten wiedergeben. Das Wachstum der festen Phase aus der unterkühlten Schmelze wurde m
 Zusammenfassung In dieser Arbeit wurde die elektrostatische Levitation aufbauend auf der Arbeit von Meister [93] und Lohöfer weiterentwickelt und erfolgreich zum Einsatz gebracht. Die elektrostatische
Zusammenfassung In dieser Arbeit wurde die elektrostatische Levitation aufbauend auf der Arbeit von Meister [93] und Lohöfer weiterentwickelt und erfolgreich zum Einsatz gebracht. Die elektrostatische
Zusammenfassung: Flächenintegrale
 Zusammenfassung: Flächenintegrale Gerichtetes Flächenelement: "Fluss" durch Flächenelement: "Fläche über G": "Fluss" durch die Fläche : Für orthogonale Koordinaten: Betrag des Flächenelements: Richtung:
Zusammenfassung: Flächenintegrale Gerichtetes Flächenelement: "Fluss" durch Flächenelement: "Fläche über G": "Fluss" durch die Fläche : Für orthogonale Koordinaten: Betrag des Flächenelements: Richtung:
2 Grundgrößen und -gesetze der Elektrodynamik
 Grundgrößen und -gesetze der Elektrodynamik. Grundgrößen der Elektrodynamik.. Ladung und die dreidimensionale δ-distribution Ladung Q, q Ladungen treten in zwei Variationen auf: positiv und negativ Einheit:
Grundgrößen und -gesetze der Elektrodynamik. Grundgrößen der Elektrodynamik.. Ladung und die dreidimensionale δ-distribution Ladung Q, q Ladungen treten in zwei Variationen auf: positiv und negativ Einheit:
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan
 Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Magnetohydrodynamik. Ivan Kostyuk Universität Heidelberg
 Magnetohydrodynamik Ivan Kostyuk Universität Heidelberg 22.05.2015 Inhalt 1. Ladungen in Elektromagnetischen Feldern 1.1 E B Drift 1.2 Ladungen in inhomogenen magnetischen Feldern 1.3 Magnetische Flasche
Magnetohydrodynamik Ivan Kostyuk Universität Heidelberg 22.05.2015 Inhalt 1. Ladungen in Elektromagnetischen Feldern 1.1 E B Drift 1.2 Ladungen in inhomogenen magnetischen Feldern 1.3 Magnetische Flasche
2.3 Stoffmodelle für Reinstoffe Die Dampftabelle ... MPa C m 3 /kg m 3 /kg ... 0, ,23 0, ,
 2.3 Stoffmodelle für Reinstoffe 2. 3. 1 Die Dampftabelle Beispiel Wasser: 60 kg Nassdampf bei p = 2 bar = 0,2 MPa und V= 3 m 3, v = 0,05 m 3 /kg Drucktafel (Tab. A1.2)... MPa C m 3 /kg m 3 /kg...............
2.3 Stoffmodelle für Reinstoffe 2. 3. 1 Die Dampftabelle Beispiel Wasser: 60 kg Nassdampf bei p = 2 bar = 0,2 MPa und V= 3 m 3, v = 0,05 m 3 /kg Drucktafel (Tab. A1.2)... MPa C m 3 /kg m 3 /kg...............
Lehrbuch der Thermodynamik
 Ulrich Nickel Lehrbuch der Thermodynamik Eine verständliche Einführung Ж HANSER Carl Hanser Verlag München Wien VII Inhaltsverzeichnis 1 GRUNDBEGRIFFE DER THERMODYNAMIK 1 Einführung 1 Systeme 3 offene
Ulrich Nickel Lehrbuch der Thermodynamik Eine verständliche Einführung Ж HANSER Carl Hanser Verlag München Wien VII Inhaltsverzeichnis 1 GRUNDBEGRIFFE DER THERMODYNAMIK 1 Einführung 1 Systeme 3 offene
8. Mehrkomponentensysteme. 8.1 Partielle molare Größen. Experiment 1 unter Umgebungsdruck p:
 8. Mehrkomponentensysteme 8.1 Partielle molare Größen Experiment 1 unter Umgebungsdruck p: Fügen wir einer Menge Wasser n mit Volumen V (molares Volumen v m =V/n) bei einer bestimmten Temperatur T eine
8. Mehrkomponentensysteme 8.1 Partielle molare Größen Experiment 1 unter Umgebungsdruck p: Fügen wir einer Menge Wasser n mit Volumen V (molares Volumen v m =V/n) bei einer bestimmten Temperatur T eine
11. Der Phasenübergang
 11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
