Statistische Thermodynamik
|
|
|
- Lukas Ursler
- vor 7 Jahren
- Abrufe
Transkript
1 Statstsche Thermodynamk Prof. Dr. W.S. Veeman Inhalt Theore I. A. Enletung B. Molekular-Dynamk Berechnungen II. III. IV. De Energenveaus der Moleküle Moleküle ohne Wechselwrkung A. Vertelungen B. De wahrschenlchste Vertelung; das Boltzmann sche esetz Moleküle mt Wechselwrkung; A. De kanonsche esamthet B. De kanonsche ustandssumme für unabhänggen Telchen V. De statstsche Entrope A. Das Telchen n enem Kasten B. De Entrope Anwendungen VI. Informatonstheore VII. De Maxmum-Entrope-Methode VIII. En deales, enatomges as IX. De Clausus-Clapeyron sche lechung X. En deales mehratomges as A. Translaton B. Rotaton C. Schwngungen XI. Der lechvertelungssatz XII. De thermodynamschen röße XIII. De ustandsglechung enes dealen ases XIV. De lechgewchtskonstante XV. Der deale Krstall A. Ensten sche Modell B. Debye sche Modell XVI. Flüssgketen A. ellentheore B. Radale Vertelungsfunkton Lteratur P.W. Atkns, Physkalsche Cheme.B.Ott und. Boero-oates, Chemcal Thermodynamcs: Prncples and Applcatons, Kap. 0 u den Kapteln XV und XVI: B.. McLelland, Statctcal Thermodynamcs, Moore-Hummel: Physkalsche Cheme, Kap. und Kap.. und.
2 I. Enletung Theore I. Enletung Das Hauptproblem der Physkalschen Cheme besteht n der Berechnung von makroskopschen Egenschaften enes Systems aus den Egenschaften der Atome und Moleküle, aus welchen das System zusammengesetzt st. De makroskopschen Egenschaften von Systemen beschreben wr mt thermodynamschen Varablen. Bsher st be deser thermodynamschen Beschrebung ncht unsere Kenntns von den enzelnen Molekülen benützt worden, z.b. daß man m Prnzp mt quantenmechanschen Methoden de Struktur und Egenschaften enes Moleküls und de Wechselwrkungen zwschen Molekülen ausrechnen kann. De Statstsche Mechank beschrebt und erklärt das Verhalten makroskopscher Systeme auf rund der Egenschaften der Mkrotelchen (Atome, Moleküle, Ionen, usw.), aus denen de Systeme zusammengesetzt snd und auf rund der zwschen den Telchen wrkenden Kräfte. Es st gebräuchlch, zwschen der Statstschen Mechank des lechgewchtzustandes und des chtglechgewchtzustandes zu unterscheden. Erstere wrd gewöhnlch Statstsche Thermodynamk genannt und befaßt sch mt Systemen m thermodynamschen lechgewcht. Wr werden uns nur mt der Statstscher Thermodynamk beschäftgen. De Statstsche Thermodynamk versucht also ene Verknüpfung herzustellen zwschen mkroskopschen Molekülegenschaften (Quantenmechank) und makroskopschen thermodynamschen Egenschaften (Thermodynamk). Das Problem st natürlch, daß jedes makroskopsche System ene sehr große Anzahl von Telchen, Atomen oder Molekülen enthält. En ramm Sauerstoff besteht aus,88 x 0 Sauerstoff Molekülen. Scherlch kann man heutzutage de unterschedenen Energezustände enes Moleküls Sauerstoff ausrechnen und auch de Wechselwrkungen zwschen zwe oder dre Molekülen. Wahrschenlch kann man eben für 000 Moleküle mt zur et t0 gegebene Ortskoordnaten x, y, z, Massen m und Impulse p x, p y, p z dese Koordnaten für ene spätere et t ausrechnen (deses Wssenschaftstelgebet wrd Molekulare Dynamk genannt). Aber für 0 Telchen st ene solche Berechnung bsher, auch angenähert, ncht möglch. ede Theore, de versucht das Verhalten makroskopscher Systeme durch de Egenschaften von Molekülen zu deuten, muß sch auf statstschen Methoden stützen. In der Thermodynamk geht es um gemttelte Egenschaften. Unter dem Druck enes ases verstehen wr z.b. das zetlche Mttel der Kraft pro Flächenenhet, de de astelchen be hre Stößen an de Wand ausüben. Dabe st es ncht so wchtg zu wssen welche Telchen n enem bestmmten Augenblck an de Wand stoßen.
3 I. Enletung Molekular-Dynamk Berechnungen, ene Enführung We n der Enführung gesagt, st es für ene beschränkte ahl von Molekülen möglch bestmmte makroskopschen Egenschaften zu berechnen. Obwohl de Molekular-Dynamk Berechnungen ncht zu dem ebet der Statstschen Thermodynamk gehören, zegen wr her mt enem enfachen Bespel doch we das m Prnzp geht. Lass uns als Bespel versuchen zu berechnen, we groß der Druck enes ases st. Ausgegangen wrd von enem System mt dentschen Molekülen. Wr nehmen an, dass am etpunkt tt 0 de Raumkoordnaten x, y, z und de eschwndgketen v x, v y, v z von allen Telchen gegeben snd. Ene logsche Annahme für de Raumkoordnaten am tt 0 wäre, dass de Telchen enhetlch n enem Volumen vertelt snd (homogene Dchte). De eschwndgket st ene Vektorgröße mt Rchtung und röße. Für de rößen der Vektoren am tt 0 st ene vernünftge Annahme, dass se das Maxwell sche esetz entsprechen, sehe Abb. I.. Anzahl nedrge Temperatur hohe Temperatur eschwndgket Abb. I. De Maxwell sche eschwndgketsvertelung Für de Rchtungen der eschwndgketvektoren nehmen wr an, dass se weder enhetlch über allen Rchtungen vertelt snd (Abb. I.). Abb. I.
4 I. Enletung Mt desen Annahmen snd für alle Telchen am tt 0 de dre Raumkoordnaten x (t 0 ), y (t 0 ), z (t 0 ) und de eschwndgketen v x (t 0 ), v y (t 0 ), v z (t 0 ) gegeben. Wr können jetzt de Koordnaten und eschwndgketen für spätere eten berechnen, z.b. für tt 0 + t. Her muss t klener sen als de et zwschen den möglchen Stößen zwschen Telchen, z.b. t0-5 s. Dann: x y z ( t ) x ( t 0 ) + v x ( t 0 ) ( t ) y ( t 0 ) + v y ( t 0 ) ( t ) z ( t ) + v ( t ) t 0 z 0 t t Für jeden nächsten etntervall muss für alle Telchen berechnet werden, ob zwe Telchen n desem Intervall stößen werden oder ncht. Mt der gegebenen Durchmesser der Telchen und den Postonen und eschwndgketen der Telchen st es en enfaches geometrsches Problem zu berechnen ob de Telchen und j m etntervall t k+ -t k stößen oder ncht. Bem Stößen ändern sch de Rchtungen der eschwndgketsvektoren der beden betelgten Telchen und müssen dese bede Vektoren neu berechnet werden. Dafür gbt es mehrere Möglchketen. Man kann z.b. annehmen, dass de Telchen sch als harte Kugel verhalten (Bllardballe), oder man brngt de Abstandsabhänggket der Wechselwrkung n Rechnung mt z.b. dem Lennard-ones Modell (Abb. I.). Energe R Abb.I. De Wechselwrkungsenerge zweer Molekülen als Funkton hrer Entfernung R. Wenn de Rechnung fortgesetzt wrd und man betrachtet für jedes Intervall de möglchen Stöße und de Folgen für de eschwndgketsänderungen, dann st der Druck des ases, bestehend aus Moleküle, auf dem Wand zu berechnen. 4
5 I. Enletung Unter der Annahme, dass de Telchen elastsch mt der Wand stößen, st de Kraft auf der Wand glech an der Summe der Änderungen der Impulse pro etenhet (Impuls mv, wobe m de Masse der Telchen st). We das geht, kann man verenfacht m folgenden Bespel sehen. De Verenfachung besteht darn, dass wr annehmen, alle Telchen haben de gleche v x. De Abb. I.4 zegt, dass für allen Telchen n dem Volumen Ov x t, wofür v x nach rechts gerchtet st, n der et t de Wand errechen ( t wurde so kurz gewählt, dass n t kene Stöße, de v x ändern können, auftreten!). V FlächeO v x t Abb. I.4 ur de Moleküle nnerhalb enem ylnder mt dem Volumen Ov x t haben de Möglchket mt der Wand zu stößen Wenn m Volumen V sch n Mol Moleküle befnden, dann befnden sch m Volumen Ov x t: n V A Ov x t Telchen ( A Avogadro sche ahl), wovon de Hälfte sch nach rechts bewegt. De ahl der Moleküle, de mt der Wand stößen, st deshalb: n V A Ov x t Für elastschen Stößen glt, dass be enem Stoß de eschwndgketskomponente v x von Vorzechen ändert, so dass de Änderung der Impuls glech mv x st. Für allen Molekülen, de n t mt der Wand stoßen st de Änderung des Impulses an der Wand pro et t deshalb: n V A Ovx mvx naovx V m 5
6 I. Enletung Damt st der Druck auf der Wand: Kraft nmv x Druck I. Fläche V wenn Mm A, de molare Masse. Im obgen Bespel wurde angenommen, dass alle eschwndgketen glech snd, n der Molekular-Dynamk Berechnung muß für jeden etntervall berechnet werden, we vel Telchen mt der Wand stößen und we groß de Impulsänderung st. Der Druck st dann der Mttelwert für allen Telchen und vele etntervalle. Mt we vel Telchen man solche Rechnungen durchführen kann, hängt von der eschwndgket und Specherkapaztät des Rechners ab. In der Praxs können m Augenblck solche Berechnungen durchgeführt werden für ca Telchen und bs Schrtten. Beobachte, dass unsere enfache Betrachtung, de zu der l. I. geführt hat, schon für deale ase rchtg st, falls wr n l. I. de mttlere quadratsche eschwndgket v ensetzen: x nm v x p (vergleche mt Atkns I.) V 6
7 II. De Energenveaus der Moleküle II. De Energenveaus der Moleküle Der ustand enes Moleküls wrd so vollständg we möglch beschreben durch de Wellenfunkton Ψ, deren Änderung mt der et gegeben st durch de zetabhängge Schrödnger lechung: Ψ h ĤΨ (II.) t wobe Ĥ der Hamltonoperator st (sehe Theoretsche Cheme). Ĥ st enen Dfferentaloperator, der auf der Raumkoordnaten der Telchen operert. De Wellenfunkton Ψ kann geschreben werden als Produkt ψ(q)φ(t), wo ψ abhängg st von den Koordnaten q und φ von der et t. Für den Fall, daß der Hamlton Operator Ĥ ncht von der et abhängt, gbt ensetzen n (II.): Oder: dϕ Ĥψ(q)φ(t) φ(t)ĥψ(q) hψ(q) (II.) dt dφ Ĥψ(q) h (II.) ψ(q) φ(t) dt In deser lechung stehen lnks nur Terme, de von der Varablen q abhängen, auf der rechten Sete erschent ledglch de Varable t. lechung (II.) kann für belebge und unabhängge Werte von q und t nur erfüllt sen, wenn bede Seten glech ener Konstanten snd. Dese Konstante nennen wr E und erhalten zwe neue lechungen: Oder: dφ Ĥψ(q) E und h E (II.4) ψ(q) φ(t) dt Ĥψ Eψ und φ(t) Cexp Et h (II.5) De Lösung der zetunabhängge Schrödnger lechung Ĥ ψ Eψ (II.6) gbt für en solertes Molekül de Egenfunktonen (molekulare Wellenfunktonen) ψ0, ψ,... und Egenwerte (molekulare Energewerte) ε0, ε,...deses Moleküls. Es kann auch sen, daß g ustände gleche Energe ε haben, man sagt dann, daß das Energenveau ε g -fach entartet st. 7
8 III. Moleküle ohne Wechselwrkungen III. En System von Molekülen ohne Wechselwrkung (das Boltzmann sche esetz) A. Vertelungen Wr betrachten en System mt dentschen Telchen und jedes Telchen (Molekül, Atom,..) hat de Energenveaus ε 0, ε,..., ε.... De Telchen haben kene Wechselwrkung, aber können trotzdem durch Stöße Energe austauschen. De esamtenerge des Systems st enfach de Summe der Energen ε der ndvduellen Telchen, aber wr wssen noch ncht we de esamtenerge über de Moleküle vertelt st. Für de Anzahl der Telchen, de m ustand mt der Energe ε snd, schreben wr n, n st de Besetzungszahl des ustandes mt Energe ε. De Vertelung der Telchen über de ustände charaktersert das System mt Telchen und wrd de Konfguraton genannt. Es gbt vele Konfguratonen, nehmen wr z.b. 4 unterschedbare Moleküle a, b, c und d und jedes Molekül hat 6 Energezustände. De ver möglchen Vertelungen mt der esamtenerge E ε0 + ε snd: ε ε ε Abb. III. ε d c b a ε ε0 -a--b--c-- --a--b--d a--c--d b--c--d--- ede Vertelung n Abb. III. hat de glechen Besetzungszahlen n 0, n 0, n, n 0, n4 0 und n5 0 oder schematsch {, 0,, 0, 0, 0}. De Konfguraton {4, 0, 0, 0, 0, 0} kann man nur auf ene Wese errechen: ε ε ε Abb. III. ε ε ε 0 -a--b--c--d-- De Anzahl der Möglchketen ener Konfguraton {n0, n,...}, mt n0 + n +... zu errechen, nennen wr hr ewcht W. Für W kann man ableten (Intermezzo ): W! n0! n! n!... (III.) 8
9 III. Moleküle ohne Wechselwrkungen Intermezzo : Permutatonen und Kombnatonen In wevel unterschedbaren Rehefolgen kann man dre Buchstaben a, b, c schreben? a, b, c a, c, b b, a, c b, c, a c, a, b c, b, a Dese 6 Möglchketen werden de Permutatonen deser ruppe von dre Elementen genannt. Im algemenen Fall mt Elementen kann man de ahl von Permutatonen ausrechnen durch das folgende Verfahren: Für de erste Stelle n der Rehefolge kann man aus Elementen wählen, für de zwete Stelle nur aus - Elemente, wel en Element schon zugewesen st, usw. Das ahl von möglchen Rehefolgen st darum: (-)(-)(-)...! ( Fakultät). Für Elementen fndet man dann 6!.. 6 Möglchketen. etzt möchten wr wssen wevel Möglchketen es gbt, um ver Moleküle a, b, c, d glechmäßg zu vertelen über zwe Energenveaus ε und ε. Erstens geben wr de 4 (4!) Permutatonen von a, b, c, d an: abcd abdc acbd acdb adbc adcb bacd badc bcad bcda bdac bdca cabd cadb cbad cbda cdab cdba dabc dacb dbac dbca dcab dcba Wenn wr voraussetzen daß de ersten zwe Moleküle n jeder Rehe n ε snd (also a und b für "abcd") und Moleküle und 4 n ε, dann bleben nur 6 unterschedlche Vertelungen über, wel z.b. abcd, bacd, abdc und badc alle korresponderen mt Molekül a und b n ε und c und d n ε. Im allgemenen Fall wll man Moleküle vertelen über k Energenveaus, so daß de Besetzung von ε0 n0 st, von ε n, usw.; n0 + n + n +... De ahl der Permutatonen st weder!, aber es gbt wenger Möglchketen um de erwünschte Vertelung zu errechen wel n0 Moleküle auf n0! unterschedene Wese geordnet werden können, n auf n! Wesen, usw. De Anzahl der Kombnatonen st darum: W! n0! n! n!... (III.) Beachten Se, dass 0! st! Für das oben besprochene Bespel der Konfguraton {,0,,0,0,0} st das ewcht: 4! W 0000!!!!!! 4 (III.) 9
10 III. Moleküle ohne Wechselwrkungen und für de Konfguraton {4,0,0,0,0,0}: W 4! 4!0!0!0!0!0! (III.) Mt desem Bespel haben wr festgestellt, dass unterschedlche Konfguratonen unterschedlche ewchte haben können, auch Konfguratonen mt der gleche esamtenerge: E n ε. etzt setzen wr voraus, daß jede Vertelung, de de gleche esamtenerge entsprcht, de gleche Wahrschenlchket hat. De Wahrschenlchket ene bestmmte Konfguraton an zu treffen st dann proportonal zu dem ewcht deser Konfguraton. Man kann sch dann auch vorstellen, daß es ene Konfguraton gbt, de wahrschenlcher st als alle anderen Konfguratonen. Wenn es ene solche domnante Konfguraton oder Vertelung gbt, kann man erwarten, daß das System de meste et dese Konfguraton hat. B. De wahrschenlchste Vertelung, de Boltzmann sche Vertelung Wenn wr de wahrschenlchste Konfguraton bestmmen wollen, müssen wr nach denjengen Werten von n suchen, de zu enem Maxmum von W führen. Wel W ene Funkton von allen n st, könnte man denken daß man das Maxmum von W fnden kann durch W nach n zu dfferenzeren (we mmer be der Bestmmung des Maxmums ener Funkton): und W dw dn n 0 (III.4) W 0 n (III.5) Dass es so ncht geht, kommt wel de n ncht unabhängg snd. Erstens st de esamtenerge E des Systems gegeben, und deshalb glt: n ε E oder ε dn 0 (III.6) Ene zwete Beschränkung wrd gegeben durch das Krterum, daß n oder dn 0 (III.7) lechungen (III.6) und (III.7) zegen daß n der lechung (III.4) zwar µ Varablen dn snd, aber nur µ- snd unabhängg, wenn µ de ahl der Energenveaus st (µ kann unendlch groß sen). 0
11 III. Moleküle ohne Wechselwrkungen Um deses Problem zu lösen, st es erstens enfacher um ncht das Maxmum von W zu suchen, sondern das Maxmum von ln W: d ( lnw) lnw n dn 0 (III.8) Mt der Methode der unbestmmten Multplkatoren von Lagrange können wr ene lechung mt nur µ- Varablen herstellen. Intermezzo : Methode der unbestmmten Multplkatoren von Lagrange, (sehe auch achmann, Mathematk für Chemker, S. 5) Bespel: Für dre Varablen x,y,z st gefunden worden, dass de Änderungen x, y, z de folgenden Bedngungen erfüllen: a x + b y + c z 0 ( vergleche mt der ebenbedngung x + y + z 0 ( lnw ) n dn 0) Ene drekte Lösungsmethode st: x y z y + c z 0 z 0 jetzt snd y and z b a und c a a( y z) + b ( b a) y + ( c a) Ene andere Lösungsmethode st: völlg unabhängg, deshalb, wenn a x + b y + c z + δ ( x + y + z) ( a + δ ) x + ( b + δ ) y + ( c + δ ) z 0; 0, wo Wel δ ene belebge Konstante st, darf man δ-a setzen, dann: mt der Lösung: abc. ( b a) y + ( c a) z 0 y und z 0, δ ene belebge Konstante st; Ene lechung mt ebenbedngungen kann man also lösen, wenn man de mt ener belebgen Konstante multplzerten ebenbedngungen zur Hauptglechung addert. Durch ene geschckte
12 III. Moleküle ohne Wechselwrkungen Wahl der Konstanten kann man genau so vel Varablen elmneren we es ebenbedngungen gbt. Das st de Methode der unbestmmten Lagrangeschen Multplkatoren. ach deser Methode adderen wr de lechungen (III.6), (III.7) und (III.8), wobe (III.6) und (III.7) multplzert werden mt den Konstanten γ und -β: d ( lnw) lnw βε + γ dn 0 (III.9) n Es st klar, daß unabhängg der Werte von γ und β, (III.9) mmer rchtg sen muß, aber (III.9) hat noch mmer µ Varablen dn, wovon µ- unabhängg. Wr können aber γ und β so bestmmen daß de Koeffzenten von dnk und dnl n (III.9) glech 0 werden: ln W ln W βεk + γ 0 und βεl + γ 0 (III.0) nk nl etzt hat (III.9) nur noch µ- unabhängge Varablen und d(lnw) 0 für jede Änderung dn wenn: ln W βε + γ 0 k, l (III.) n Kombnaton von (III.0) und (III.) gbt: ln W βε + γ 0 für alle (III.) n Um dese lechungen lösen zu können, müssen wr lnw ausrechnen mt (III.): W! n! n!... (III.)
13
14 III. Moleküle ohne Wechselwrkungen x lnx! xlnx-x 0 5,,0 0 4, 9, ,5 45,6 00 6,7 60, ,0 60,6 In den Fällen worüber wr sprechen st x 0! Mt der Strlngschen Formel fndet man: lnw ln! ln n0! ln n!... ln! ln n! ( ) ln n ln n n ln n ln n (III.5) Dfferentaton nach n lefert ( st konstant und n j unabhängg von n ): ( njln nj) lnw n ln n ln n n ln n (III.6) n n n n j Das gefundene Extremum st wrklch en Maxmum, wel wetere Dfferentaton gbt: ln W n n De Werte von n wobe lnw maxmal st, nennen wr n *. Kombneren von (III.) und (III.6) gbt: ln n * + α βε 0 (III.7) wobe α γ- st. Mt gegebener esamtenerge E st dann de wahrschenlchste Besetzung des ustandes mt der Energe ε : n e α βε (III.8) * α βε Aus n e e α β ε e e α folgt: e βε e (III.9) 4
15 III. Moleküle ohne Wechselwrkungen Kombnaton von (III.8) und (III.9) führt zu der Boltzmann-Vertelung, wobe de wahrschenlchste Besetzung n* des ustandes ε gegeben st durch: n e βε * βε e Später werden wr noch β bestmmen! (III.0) etzt behaupten wr, daß alle Vertelungen, de abwechen von der wahrschenlchsten Vertelung, so unwahrschenlch snd, daß man dese Vertelungen völlg vernachlässgen kann. Als stark verenfachtes Bespel betrachten wr m Intermezzo 4 zwe Vertelungen. Intermezzo Elemente werden n.0 4 ruppen aufgetelt. Man verglecht nun de ahl der möglchen Anordnungen für den Fall, daß a. n jeder ruppe 000 Elemente snd, b. sch n ener Hälfte der ruppen 00 Elemente und n der anderen Hälfte 999 Elemente befnden. De ahl der möglche Anordnungen m Falle a. st: und m Falle b.: W b 7 0.! W a 0! 0!... ( ) 7 0.! ! ( 999!) 7 0.! ( 0!) 0000 Das Verhältns der Wahrschenlchketen beder Vertelungen st W W a b 00! 999! 000! 000! ! 999! ! 999! 000 De Vertelung a st 000 -mal wahrschenlcher als de sehr ähnlche Vertelung b. Sehr ähnlche Vertelungen können stark unterschedlche ewchte haben! Dabe beträgt de ahl der Elemente nur.0 7 ; de ahl der ruppen st.0 4. In Systemen, mt denen sch de Statstsche Mechank befaßt, st de ahl der Elemente (Moleküle) und ruppen (Energen) wesentlch größer (00 und mehr). Deshalb st de Methode, das System mt der wahrschenlchsten Vertelung zu beschreben, gerechtfertgt. C. De molekulare ustandssumme 5
16 III. Moleküle ohne Wechselwrkungen De Summe m enner der lechung (III.0) heßt de ustandssumme oder molekulare ustandssumme (engl. molecular partton functon) wenn man über Moleküle redet: e βε (III.) Dese Summe kann man auch etwas anders formuleren. In (III.) wrd über ustände summert, aber es kann sen, daß es g ustände mt der glechen Energe ε gbt (Entartung). Wr können (III.) dann auch schreben: Energe g e βε (III.) wobe nur über de Energewerte der veaus summert wrd. Dese zwe Beschrebungen snd völlg äquvalent: ustände Energe βε e βε g e (III.) Man seht auch warum de ustandssumme genannt wrd. De ustandssumme st wchtg, wel se alle thermodynamschen Informatonen über en System aus unabhänggen Telchen m thermschen lechgewcht enthält. Wenn wr de Besetzungszahlen der Energenveaus kennen, st es zum Bespel möglch, de esamtenerge des Systems E n ε anzugeben, ndem wr anstelle aller Vertelungen enfach de wahrschenlchste Vertelung ensetzen: E n * e βε ε ε (III.4) Man kann de Summe (I.8) so umformen, daß se nur noch enthält. Mt ergbt sch: βε e β βε εe E βε e β β (III.5) Wenn wr defntonsgemäß ε 0 0 wählen, st E de thermodynamsche nnere Energe U relatv zu hrem Wert be T0; deshalb: 6
17 III. Moleküle ohne Wechselwrkungen U U ( T 0) + E U ( 0) U( 0) (ln ) β β (III.6) ur Berechnung der nneren Energe U-U(0) braucht man nur de ustandssumme. Später werden wr sehen, daß man, wenn man de ustandssumme kennt, alle thermodynamschen Funktonen berechnen kann. Später werden wr auch bewesen daß: β kt (III.7) wobe k ene Konstante, de Boltzmann-Konstante, st und T de Temperatur n Kelvn. Mt (III.8) kann man de Temperaturabhänggket der ustandssumme betrachten: ε e kt (III.8) Für T 0 st /kt unendlch groß, und alle Terme n (III.) verschwnden bs auf enen, wenn man ε 0 0 wählt. Für den Fall, daß deser rundzustand ε 0 g 0 -fach entartet st, glt: g0 für T 0 (III.9) Für T wrd de Summe glech der Anzahl der ustände des Moleküls: für T De ustandssumme gbt also an, wevele ustände be ener gegebenen Temperatur für en Molekül thermsch zugänglch snd. Be T0 st nur der rundzustand besetzt, be sehr hohen Temperaturen snd praktsch alle ustände errechbar. Bespel De Schwngungsenergenveaus enes zweatomgen Moleküls (harmonscher Oszllator) snd gegeben durch: k εν ( ν+ ) hω mt ω, wobe (III.0) µ k Kraftkonstante und µ reduzerte Masse mm/(m+m) und ν de Schwngungsquantenzahl mt den Werten ν0,,,...; ε ħω. Dann: β ε e ν ν ν 0 e β ε ( ν + ) e βε β ε β ε β ε β ε e ( + e + e + e +...) β ε e (III.) 7
18 III. Moleküle ohne Wechselwrkungen Für r< und de unendlch velen Terme ener geometrsche Rehe glt: a + ar + a ar + ar +... r De Besetzungszahl des Energenveaus ε m st deshalb: n * m e β ε m β ε ( ) e e β mε (III.) Für I glt ε und dann fndet man be 00 K (β ): n 4 * 0,00 - ε 4 n* 0, ε n* 0, ε n * 0, ε n 0 * 0, ε > n* 8
19 IV. Moleküle mt Wechselwrkungen IV. Moleküle mt Wechselwrkungen A. De kanonsche esamthet etzt wollen wr de n Kap. III hergeleteten Ergebnsse so verallgemenern, daß se auch für Systeme gelten, deren Telchen unterenander n Wechselwrkung stehen. Dazu führen wr den Begrff esamthet (Eng. ensemble) en. Wr haben zuerst en geschlossenes System mt Telchen (Molekülen), dessen Volumen V und Temperatur T gegeben snd. etzt stellen wr uns ene esamthet vor, de besteht aus deser Systeme, wobe durch thermschen Kontakt alle Systeme de gleche Temperatur haben. Deshalb können de Systemen unterenander Energe austauschen aber de esamtenerge E soll konstant sen. Dese esamthet wrd de kanonsche esamthet genannt. kanonsche esamthet: esamtenerge E ahl der Telsysteme edes Telsystem hat Telchen, Volumen V und Temperatur T Ene esamthet st ncht en physkalsch exsterendes System, es st nur en Produkt unserer Vorstellung und wr können, wenn wr wollen, unendlch groß wählen. Der Begrff esamthet wrd aus dem folgenden rund engeführt. Alle thermodynamsche rößen enes Systems snd zetlche Mttelwerte. etlche Mttelwerte lassen sch schwer berechnen und darum formulert de statstsche Mechank das Postulat: Das etmttel ener dynamschen Egenschaft enes wrklchen Systems st glech dem esamthetsmttel ( ) deser Egenschaft n enem bestmmten Augenblck De esamtenerge E der esamthet st über alle leder der esamthet vertelt und der durchschnttlche Energewert enes ledes st dann E /. Dese röße können wr mt der nneren Energe dentfzeren, wenn, und darum auch E, gegen unendlch geht. wschen allen ledern besteht en thermscher Kontakt, so daß se unterenander Energe austauschen können. De Anzahl der leder ener esamthet mt Energe E bezechnen wr mt, und wr können dann, n vollständger Analoge zur Beschrebung enes Systems, von der esamthet sprechen mt den Begrffen ener Konfguraton und ener Vertelung mt dem ewcht W. Wr können weder voraussetzen, daß es Konfguratonen gbt, de sehr vel wahrschenlcher snd als andere. Es st z.b. absolut unwahrschenlch daß sch de ganze Energe E n enem System (enem led der esamthet) anhäufen wrd. Es gbt also weder ene domnerenden Konfguraton der esamthet mt der usammensetzung 0*, *, *,... und ewcht W*, womt wr de thermodynamschen Egenschaften des Systems ausrechend genau berechnen können, ndem wr enfach de Mttelwerte der betreffenden rößen über de wahrschenlchste Konfguraton berechnen. W!! 0!!... 9
20 IV. Moleküle mt Wechselwrkungen enau so we n IIb, mt ebenbedngungen fndet man: E E und * j e β e E j β E β E j e Q wobe E Q e de kanonsche ustandssumme st. (IV.) j * st ene exponentell abnehmende Funkton der Energe E j. Aber, je größer E j, desto mehr gbt es Möglchketen aus den Energen der Moleküle Ej zusammenzustellen. um Bespel für 4 Moleküle mt Energen ε0, ε, ε,... gbt es nur ene Möglchket E 4ε0 zu machen (Konfguraton {4,0,0,...} und ewcht 4! / (4! 0! 0!...) ), aber für de Energe: E ε0 + ε + ε + ε gbt es schon 4! / (!!!! 0!...) 4 Möglchketen. Deshalb nmmt de ustandsdchte, de ahl der ustände pro Energeenhet, schnell zu mt E j. Besetzung Energevertelung ustandsdchte Energe Abbldung Abb. zegt de Energeabhänggket des * und der ustandsdchte. Das Produkt j*. ustandsdchte gbt de Energevertelung der leder des esamthet. Es st nur ene schmale Bande mt enem scharfen Maxmum be der mttlere Energe. Fast alle leder der esamthet haben gerade dese Energe. We de molekulare ustandssumme, enthält auch de kanonsche ustandssumme alle für de Thermodynamk bedeutsame Informatonen über en System, aber se st ene allgemenere röße, als se ncht mehr de Unabhänggket der enzelnen Telchen voraussetzt. De nnere Energe für de kanonsche esamthet wrd zu: E * U U ( 0) E für (IV.) βe Ee Q Q und U U ln ( 0) (IV.) Q Q β β 0
21 IV. Moleküle mt Wechselwrkungen B. De kanonsche ustandssumme für unabhänggen, ncht-wechselwrkenden Telchen. De kanonsche ustandssumme st allgemener als de molekulare ustandssumme: kanonsche ustandssumme molekulare ustandssumme E Q e β e βε für Telchen mt Wechselwrkung mttlere Systemenerge E Σ n ε für unabhängge Telchen E Σ n ε etzt versuchen wr für unabhängge Telchen de kanonsche ustandssumme zu berechnen. Dann kann man schreben für de Energe: E j p j0ε0 + p jε+... p jε+... (IV.4) wobe pj de ahl der Moleküle mt Energe ε st m System mt Energe Ej. Deses System hat de Konfguraton: {p j0, p j, p j,..., p j,... } und: p j. Es gbt! Möglchketen um de Energe Ej zusammenzustellen. pj0! pj!... pj! Bespel: System mt Molekülen mt möglchen Energen ε 0, ε, ε : Systemenerge Konfguraton ewcht Anzahl E ε 0 + ε 0 {,0,0} E ε 0 + ε {,,0} E ε 0 + ε {,0,} E4 ε + ε {0,,0} E5 ε + ε {0,,} E 6 ε + ε {0,0,} Deshalb: Q e p! e! p!... ustä nde Energe βe j β j ε + jε+ j j j0 j ( p p...) (IV.5) Man kann bewesen (Intermezzo 4):
22 IV. Moleküle mt Wechselwrkungen Energe! Q ( pj pj e ) j β 0ε0+... ε +... βε e p! p!... j j0 j j für unterschedbaren Telchen (IV.6) /! für ununterschedbaren Telchen (IV.7) Für dentsche Atome oder Moleküle n enem as müssen wr (4) berückschtgen, für Atome oder Moleküle n enem Krstallgtter, mmer (4) wel de Telchen durch hre tterplatz unterschedbar snd Intermezzo 4 Um l. (IV.6) und (IV.7) m allgemenen Fall zu bewesen st ncht so lecht, wr prüfen l. (IV.7) darum nur für en enfaches Bespel. Für das oben dskuterten Bespel ( Moleküle und Energewerte) gbt l. (IV.5): E j Q e β βε ( e 0 ε0) βε ( + e ε) βε ( ε βε ε βε ε βε ε + e ) ( ) ( ) ( ) + e 0 + e 0 + e j βε e 0 βε + e βε + e (IV.8) Es st wchtg enzusehen, daß wr de Termen mt der Energe ε0+ε, ε0+ε und ε+ε zwemal gezählt haben, wel wr angenommen haben, daß de Stuaton mt Molekül n ε 0 und Molekül n ε unterscheden werden kann von Molekül n ε und Molekül n ε 0. Wenn, aber, Moleküle und ununterschedbar snd, gbt es ken untersched zwschen desen beden ustände. In desem Fälle haben wr n (44) alle Kreuzterme zwemal (!) zuvel gezählt. Für Moleküle st dese Faktor glech!. Leder gbt es n (44) auch Terme, wobe bede Telchen m glechen ustand snd ("Dagonalterme"). Man kann deswegen für nur zwe ununterschedbare Moleküle und ustände ncht enfach sagen: Q! Für Moleküle und 000 Molekülzustände, aber, gbt es 0 6 Möglchketen de beden Telchen zu vertelen, mt nur 000 Dagonalterme. Be gewöhnlchen Temperaturen stehen Moleküle so vele ustände zu Verfügung, daß man n guten Annäherung für ununterschedbaren Telchen schreben kann: Q! V. De statstsche Entrope
23 V. De statstsche Entrope V. A. Das Telchen n enem Kasten En Telchen mt der Masse m bewegt sch endmensonal entlang x. De Energe des Telchens kann geschreben werden als de Summe der knetschen und potentellen Energe: p E mv + V + V (V.) m Her st V de potentelle Energe und p der Impuls des Telchens pmv; p r st enen Vektor mt den Komponenten (p x,0,0). De Wellenfunkton Ψ des Telchens wrd durch de Schrödnger lechung gegeben: Ĥ Ψ EΨ (V.) Her st Ĥ der Hamltonoperator, der aus den klassschen Ausdruck für de Energe gefunden dx h wrd mt der Substtuton p x m. dt x Also: Hˆ h Ψ + V Ψ EΨ (V.) m x Das Telchen bewegt jetzt fre (d.h. V0) zwschen zwe Wänden be x0 und xl, Abb. 4. x x0 xl Abb. 4 Endmensonale Bewegung zwschen x0 und xl h m Ψ EΨ x (V.4) Als Randbedngungen gelten Ψ0 für x 0 und x L, wel das Telchen ncht ausserhalb der Wände gefunden wrd. De allgemene Lösung der l. (V.4) st: Ψ Asn kx + B cos kx (V.5)
24 V. De statstsche Entrope Mt der Randbedngung Ψ0 für x0 fnden wr sofort B0 und mt der zweten Randbedngung: A sn kl 0, oder: klnπ, n0,,,,4,. Ensetzen der Lösung (V.5) n der l. (V.4): h Ψ m x h m ( Ak sn kx) EAsn kx lefert: h k E mt m nπ k, n0,,,.. L Oder: n h E n (V.6) 8mL De l. (V.6) zegt daß de Energe des Telchens gequantelt st, Ursachen der Quantelung snd de Randbedngungen. Für L cm legen de Energenveaus sehr dcht zuenander, z. B. für en Xe Atom mt m.0-5 kg: h 8 h 4 0,5x0, aber für L nm 0,5x0 8mL 8mL Für ene endmensonale Bewegung st E n abhängg von (L) -, für ene dredmensonale Bewegung n enem Kasten mt Längen L,L, L st E n abhängg von (L L L ) - (Volumen) - : E (V.7) V V. B. De statstsche Entrope Bsher haben wr uns mt dem usammenhang zwschen der ustandssumme und der Energe beschäftgt (erster Hauptsatz der Thermodynamk). etzt möchten wr den usammenhang der ustandssumme und de Entrope dskuteren. und: E * U U ( 0) E für (V.8) * du de + Ed * (V.9) 4
25 V. De statstsche Entrope l. (V.9) zegt, daß ene Änderung du entstehen kann durch ene Änderung der Energenveaus E oder durch ene Änderung der Besetzungszahlen *. De Kombnaton der ersten und zweten Hauptsatz der Thermodynamk führt zu der Fundamentalglechung: du TdS - pdv (V.0) Be Erwärmen enes Systems be konstantem Volumen ändern sch nur de Besetzungen *, wel sch be der Änderung des Volumens enes ases be konstanter Temperatur de Energenveaus ändern müssen (l. V.7). Deshalb kann man stellen: oder: * TdS Ed (V.) * ds Ed T (V.) Wr defneren jetzt: k * S lnw (V.) wobe k ene Konstante st und W* st das ewcht der wahrschenlchsten Konfguraton, und bewesen jetzt, dass dese Defnton zu der l. (V. ) führt. Im Allgemen st W ene Funkton der Besetzungszahlen : W F,,,...) (V.4) ( ach Dfferenzerung der l. (V.) bekommt man: ds k ( lnw ) k d( ln W ) d (V.5) Be der Abletung der Boltzmann lechung haben wr gefunden (l. III.): ln W βε + γ 0 n für alle Ebenso kann man für de esamthet ableten: lnw β E + γ 0 für alle 5
26 V. De statstsche Entrope k Also: ds ( E γ ) Wel d 0 glt: kβ kγ β d (V.6) d Ed ds kβ E d (V.7) De lechungen (V.) und (V.7) stmmen überen wenn ß / kt st, und damt st de l. (V.) ene snnvolle Defnton der Entrope: k * S lnw (V.) De l. (V.) zegt dass für de wahrschenlchste Konfguraton de Entrope maxmal st. De Formel für de Entrope (V.) läßt sch umwandeln, da se als Funkton der ustandssumme auftrtt: k * k! k * S lnw ln ln! ln! * * 0!!... k * * * k ln ln + ln k * * * * * ln ln k ln ln * * ln * k * * ln (V.8) * Mt P, wobe P der Bruchtel der leder der esamthet st, de de Energe E haben, dann wrd (V.8): S k P ln P (V.9) etzt versuchen wr S n Q aus zu drücken: βe e βe * e und P und ln P β E ln Q Q Q 6
27 V. De statstsche Entrope S k ( E + ln Q) P β kβ P E + k ln Q P (V.0) Auch wssen wr: E * U U ( 0) E P E (V.8) De Kombnaton der l. (V.0) und (V.8) brngt: S U U (0) + k ln Q T QT Q + k ln Q β (V.) 7
28 VI. Informatonstheore VI. Informatonstheore Es gbt ene Bezehung zwschen der Entrope und dem Begrff Informatonsnhalt n der Informatonstheore. ach Shannon wrd der Informatonsnhalt I ener Kode defnert als: I ν log λ (Enhetbt) (VI.) wobe ν de ahl der Plätze n der Kode st und λ de Anzahl der Möglchketen pro Platz. Bespel: Würfel werfen (enmal): ν und λ6; I log 6, 58 bt. De Wahrschenlchket ene ahl zu werfen st /6 P 6 und: S k P ln P k ln + ln + ln + ln + ln + ln k ln 6 S und I snd proportonal! ( a b log x log x ) b log a Bespel. Der Informatonsnhalt enes Wurfes mt dem Würfel st,58 bt und das bedeutet, dass man gemttelt,58 Fragen stellen muss um zu raten was geworfen wurde:. Frage? Antwort: ja nen. Frage? 5? Antwort: a nen ja nen! 6!. Frage? 4? Antwort: ja nen ja nen!! 4! 5! Bespel. Bnäre ahlen Dezmale ahl Bnäre ahl
29 VI. Informatonstheore Der Informatonsnhalt der obenstehenden bnären ahl I log bt; ch brauche Fragen zur raten ener -bt bnären ahl:. Frage 0? a nen 000,00,00,0 00,0,0,. Frage 00? 0? a nen ja nen 000,00 00,0 00,0 0,. Frage 000? 00? 00? 0? a nen ja nen ja nen ja men 000! 00! 00! 0! 00! 0! 0!! Bespel : DS besteht aus ene Rehefolge von 4 Basen: Adenne (A), Uracl (U), Cytosne (C) und uanne (). Es gbt 0 Amnosäure und ene Rehefoge von dre Basen kodert für ene Amnosäure. De Rehefoge von 0 Amnosäuren entsprcht ene Informatonsnhalt I log 0 4, bt; ene Rehefolge von zwe Basen würde enen Informatonsnnhalt von nur I log 4 4 bt haben, dass st zu weng! Deshalb koderen dre Basen für ene Amnosäure. 9
30 VII. De Maxmum Entrope Methode VII. De Maxmum Entrope Methode An Hand des folgenden Bespels wrd de Methode demonstrert, se kann natürlch auch für andere ähnlche Probleme angewandt werden. In Polymermateralen snd de Polymerketten oft n ener bestmmten Rchtung mehr oder weng orentert, z.b. n Fasern durch das Verstrecken be der Produkton oder n Bautele, wo man sch n ener Rchtung bessere mechanschen Egenschaften wünscht. De Orenterung der Ketten kann mttels ener Orenterungvertelungsfunkton P(θ) festgelegt werden (Abb. VII..): P(θ) 0 o θ 90 o Abb. VII. Ene möglche Orenterungvertelungsfunkton Es st m Allgemenen ncht möglch P(θ) für vele Werte von θ zu messen. Relatv enfach st es mt IR, MR oder Doppelbrechungsmethoden de folgende röße zu bestmmen: P P( )(cos θ ) P (cos θ ) θ für dskrete Werte θ, (VII.) wobe P de Wahrschenlchket st, dass ene Molekülkette de Rchtung θ hat: P (VII.) Mt den lechungen (VII.) und (VII.) verfügen wr über zwe lechungen für unbekannte Werte P, es fehlen - lechungen. Wr suchen jetzt de Werte P, für de de l. (VII.) und (VII.) erfüllt werden und wofür: S k P ln P (VII.) maxmal st, oder: 0
31 VII. De Maxmum Entrope Methode ( ) + dp P k dp P S ds 0 ln (VII.4) Mathematsch gesehen st deses Problem dentsch zum Problem be der Abletung des Boltzmann schen esetz. De l. (VII.) und (VII.) erfüllen her de Rolle der ebenbedngungen. De Addton der l. (VII.), (VII.) und (VII.4) mt den Lagrange schen Konstanten λ und µ erbrngt: ( ) ( ) 0 sn cos ln dp P P P k θ θ θ µ λ (VII.5) Wenn wr für P P P θ θ θ + + n der l. (VII.5) ensetzen, haben wr + gekoppelten lechungen mt + unbekannten (P, λ und µ) und snd de P zu bestmmen. Das würde bedeuten, dass wr mt nur enem Messwert de wahrschenlchste Orenterungsvertelungsfunkton bestmmen können!
32 VIII. De Entrope enes enatomgen dealen ases, de ustandssumme der Translaton VIII. De Entrope enes enatomgen ases, de ustandssumme der Translaton Für en deales, enatomges as kann man de Entrope berechnen. In solch enem as snd de Atome unabhängg und ununterschedbar, deshalb: und: U U (0) S + k ln Q T (VII.) Q und ln Q ln ln! ln ln +! (VII.) Mt n A ( A Avogadrosche Konstante, n de Substanzmenge n Mol) und R k A, wrd l. (VII.): U U (0) S + nr T Für de nnere Energe gbt l.(iv.): ( ln ln + ) Q! U U ( 0) Q β Q! β! β β Wr können jetzt S ausdrücken n : S + nr T β ( ln ln + ) (VII.) Um S zu berechnen müssen wr jetzt de molekulare ustandssumme für en perfektes as n enem Behälter mt Volumen V bestmmen. Dafür brauchen wr de Energen deses ases: e βε Im allgemenen wrd de esamtenerge enes atomaren Systems gegeben durch de Translatonsenerge, de Rotatonsenerge, de Schwngungsenerge und de elektronsche Energe. Für Atome be Raumtemperatur kann man voraussetzen daß nur der elektronsche rundzustand besetzt st und dafür der Betrag der Elektronenenerge zu der esamtenerge glech null st. Weterhn können Telchen de bestehen aus en Atom kene Rotatonen und Schwngungen haben. De (atomaren ) Energen ε enes enatomgen as werden deshalb nur durch de Translatonbewegungen der Atome bestmmt. Wenn das Volumen en Parallelepped mt Längen X,Y, st kann man de Translatonsenerge schreben we en Summe der Translatonsenergen n der dre Rchtungen: ε ε + ε + ε ε ( x) + ε ( y) + ε ( z) x y z j k l
33 VIII. De Entrope enes enatomgen dealen ases, de ustandssumme der Translaton Herbe repräsenteren j, k und l de möglche Energewerte für de Bewegung entlang x, y oder z; dese Bewegungen snd unabhängg von enander und de Kombnaton j, k und l bestmmt. [ ] { } [ ] [ ] [ ] [ ] z y x l l k k j j l j k l k j z Exp y Exp x Exp z y x Exp Exp + + ) ( ) ( ) ( ) ( ) ( ) (,, βε βε βε ε ε ε β βε Unter Benützung der Ergebnsse des Telchen n enem Kasten fnden wr für de Energenveaus enes Telchens der Masse m n enem Behälter mt der Länge X: 8 ) ( ; 8 ) ( ; 8 ) ( m h l z my h k y mx h j x l k j ε ε ε und dann gbt es für x : h m X dj mx h j Exp mx h j Exp j x β π β β und : 4 8 β π β π π β m h V h m V h m XY z y x Λ Λ (VII.4) etzt benützen wr de l.(vii.4) um de Entrope enes dealen ases, lechung (VII.), weter zu berechnen: lechung Tetrode Sackur n V e nr n ev nr nr V nr k V nr V TV S A A Λ Λ + + Λ + + Λ + Λ Λ 5 ln ln ln ln ln ln β (VII.5) Mt desem Sackur-Tetrode-lechung können wr ene Verbndung mt dem klassschen Thermodynamk herstellen.
34 VIII. De Entrope enes enatomgen dealen ases, de ustandssumme der Translaton De Fundamentalglechung der klassschen Thermodynamk besagt: dutds-pdv (nur Volumenarbet). Be der Expanson enes dealen ases st du0, oder TdSpdV und: V e e e pdv nrtdv dv V S nr nr ln T TV V V V V V a V a V a ach der Sackur-Tetrode lechung ändert sch be der sothermschen Expanson enes deales as von Va nach Ve, de Entrope um: 5 5 e Ve e Va V S nr ln ln nr ln n AΛ n AΛ V we de l.(vii.5) n der klassschen Thermodynamk e a e a ; 4
35 IX. De Clausus-Clapeyron lechung IX. De Clausus-Clapeyron lechung De renzlne zwschen zwe Phasen wrd durch de Clausus-Clapeyron sche lechung gegeben: dp S HÜbergang dt V T V Übergang Für den Übergang flüssg-dampf glt: krtschen Punkt). V VDampf und dp dt H Verdampfung (wet weg vom T V S Dampf Wr betrachten zwe gleche Volumna Dampf und Flüssgket mt D Dampfmolekülen und F flüssge Molekülen. In ener ganz enfachen Beschrebung nehmen wr an, dass alle D Dampfmoleküle das Energenveau mt der Energe ε D besetzen und de Moleküle n der flüssge Phase das veau mt der Energe ε F. Für den Dampf haben wr gesehen, falls es en deales as st, dass de Energe pro Molekül: U U ( 0) kt Deshalb glt: ε kt und wr setzen ε E ; wr bewesen später, dass E>>kT st. D F ε D kt D ε F -E F Das Boltzmann sche esetz besagt: D F Exp ( ε ε ) D kt F Exp E kt wel ε D -ε F E Der Dampf st deal: n D RT D RT RT E RT E p F Exp nf Exp V V V kt V kt dp dt A A n F R E E n + F R E E Exp Exp V kt kt V kt kt wel E>>kT 5
36 IX. De Clausus-Clapeyron lechung dp dt nd R V E kt D E VT Für Mol Dampf glt: D A und V VDampf : dp dt V A Dampf E T H TV Verdampfung Dampf Ist E wrklch vel größer dann kt? Für Wasser be 98 K: HVerdampfung AE 4406, dann: und 4406 E 7,x0 6,0x0 kt be 98 K 4x0-0 E kt 7 4 6
37 X. De ustandssumme enes mehratomgen ases X De ustandssumme enes mehratomgen ases etzt versuchen wr mt der kanonschen ustandssumme de thermodynamschen Funktonen enes ases von mehratomgen Molekülen zu berechnen. Unter der Voraussetzung, daß de Moleküle dentsch und ununterschedbar snd, glt weder: Q! und wr brauchen nur de molekulare ustandssumme zu bestmmen. Der erste Schrtt st festzustellen daß de Energe enes Moleküls sch vertelen läßt n de knetsche Translatonsenerge ε T (Translatonen des Massenschwerpunkts) und de Energe der nneren Frehetsgrade des Moleküls, we Rotatonen, Schwngungen und Elektronenübergänge. De Energe nnerer ustände läßt sch mt guter äherung als Summe der Energeantele der als unabhängg betrachteten Rotatonen, Schwngungen und Elektronenübergänge darstellen: ε + T R S E ε + ε + ε ε (X.) Dese Energen kann man versuchen theoretsch zu berechnen (Quantenmechank) oder spektroskopsch zu bestmmen (Mkrowellen Spektroskope, Infrarot Spektroskope, UV und schtbares Lcht Spektroskope) und damt de ustandssumme erhalten: T R S E [ ] Exp[ β ( ε + ε + ε ε m )] j k l Exp βε + (X.) j, k, l, m In guter Annäherung snd dese Energen unabhängg vonenander, nur de Trennung der Rotatons- und Schwngungsenerge st problematsch, es gbt z.b. molekulare Übergänge wobe sch glechzetg der Rotatons- und Schwngungszustand enes Moleküls ändert (Atkns 8.d)). De Trennung der Kernbewegungen (Translaton, Rotaton und Schwngung) und Elektronenbewegungen wrd de Born-Oppenhemer-äherung genannt. Wenn wr trotzdem de ver Beträge der Energe als unabhängg betrachten, können wr schreben: j Exp Exp (a) Translatonsantel T T R S E [ βε ] Exp[ β ( ε j + ε k + ε l + ε m )] j, k, l, m T R S E T R S E [ βε j ] Exp[ βε k ] Exp[ βε l ] Exp[ βε m ] k l Für de molekulare ustandssumme enes Telchens mt der Masse m n enem Behälter mt Volumen V haben wr schon gefunden: m 7
38 X. De ustandssumme enes mehratomgen ases T V Λ, wobe (b) Rotatonsantel R β Λ h, πm β und m jetzt de esamtmasse des Moleküls st. kt Klasssch wrd de Energe enes roterenden Körpers gegeben durch: ε R (X.) Iαω wobe ω de Drehungsgeschwndgket st (n Radalen/s) und I α das Träghetssmoment des Körpers st für ene Rotaton um de Achse α (Abb. X.): I m R α α R m Abb. X. Das Träghetsmoment Mt der Defnton des Drehmpulses Iω ( und I snd Vektoren!) wrd de l. (X. ): R ε (X.4) I Um den quantenmechansche Ausdruck von (X.4) zu fnden, wrd ersetzt durch ( + ) h : R ( + ) h ε B ( + ) (X.5) I wobe de Rotatonsquantenzahl de Werte 0,,,. annehmen kann. De Quantenmechank zegt auch, dass der Rotatonszustand mt der Quantenzahl +-fach entartet st. ur der rundzustand 0 st ncht entartet. 8
39 X. De ustandssumme enes mehratomgen ases Rotatons- und Schwngungsenergen werden oft n cm - ( Wellenzahlen ) ausgedruckt, für de Umrechnung oule cm - kann man de folgenden Bezehungen verwenden: hc E hν oder λ E hc λ E Falls de Wellenlänge λ n cm ausgedruckt wrd, st n cm - : hc wobe R ε ( n cm R ε ( n oule) ) B' ( + ) hc B B ' hc En Körper hat unendlch vele und unterschedlche Träghetsmomente, wel es unendlch vele möglche Drehachsen gbt. Alle möglche Träghetsmomente können als ene Funkton von nur dre Hauptträghetsmomenten I A, I B und I C geschreben werden. Dese Hauptträghetsmomente gehören zu dre senkrechten Hauptachsen A, B und C. Im Allgemenen, falls das Molekül ene gewsse Symmetre hat, snd de Hauptachsen parallel zu den Symmetreachsen Man sprcht von enem sphärschen Kresel wenn IA IB IC st (z.b. CH4 und SF6), von enem symmetrschen Kresel wenn IA IB I, IC I // st (z.b. H) und von enem lnearen Kresel wenn I A I B I I und I C I // 0 snd (z.b. OCS). Für de Berechnung enes Träghetsmomentes wählen wr das Molekül 6OCS (Abb.X.). O C S x Den Ursprung enes Koordnatensystems legen wr zunächst ns entrum des S-Atoms (x S 0) und de x-achse durch das C (xx C ) und O (xx O ) Atom. En Träghetsmoment wrd mmer defnert n Bezug auf das Massenzentrum. Dese Massenzentrum des OCS Moleküls legt rgendwo auf de OCS Achse, be der Koordnate xx M. Wr fnden x M aus der Bedngung für den Massenschwerpunkt: ( x x ) m + ( x x ) m + ( x x ) m 0 O M O C M C S M S 9
40 X. De ustandssumme enes mehratomgen ases Für das Träghetsmoment I des OCS glt: I m O ( xo xm ) + mc ( xc xm ) + ms ( xs xm ) Mt r CO x O -x C 0,65 nm, r CS x C -x S 0,559 nm und de atomare Massenenhet, kg fnden wr x M 0,08 nm, IOCS, kg m und B 0,8 cm -. Für enen sphärschen (Träghetsmoment I) oder lnearen Kresel (Träghetsmoment II ) glt also: R ( + ) h ε B ( + ) (X.5) I wobe das veau (+)-fach entartet st. Für enen symmetrschen Kresel hat man: ε R, K B + ) + ( A B) ( K wobe 0,,,, und K0, ±, ±,,± und A h h, B 8π ci // 8π ci Das veau enes symmetrschen Kresels hat ene (+)-fache Entartung für K0 und ene (+)-fache Entartung für K 0. Für homonukleare, zwe-atomge Moleküle wrd en zusätzlches Problem gegeben durch de Symmetre des Moleküls. Für das Molekül Wasserstoff H zum Bespel, snd de zwe Protonen Fermonen mt ener Kernspnquantenzahl I/. Se unterlegen deshalb das Paul-Prnzp, was sagt daß de esamtwellenfunkton hr Vorzechen ändern muß, wenn man de bede Kerne vertauscht be ene Drehung um 80o. etzt st de Orenterung der Kernspns wchtg, es gbt Wasserstoff mt paralllelen Ausrchtung der Kernspns (Ortho-Wasserstoff) und Wasserstoff mt antparallelen Ausrchtung (Para-Wasserstoff). Durch Drehung um 80 o werden de beden Wasserstoffkerne vertauscht. Für Ortho-Wasserstoff muß dann de Rotatonswellenfunkton sen Vorzechen ändern, d.h. dass nur ungerade Werte von erlaubt snd. Für Para-Wasserstoff ändert sch be Drehung um 80 o de Kernspnwellenfunkton und blebt das Vorzechen der Rotatonswellenfunkton glech, d.h. nur gerade -Werte snd erlaubt. 40
41 X. De ustandssumme enes mehratomgen ases Für sphärsche und lneare Kresel können wr jetzt enen enfachen Ausdruck für den Rotatonsantel der molekularen ustandssumme fnden: R ustände j Exp Energewerte R R [ βε j ] ( + ) Exp[ βε ] ( + ) Exp[ βb ( + ) ] Für T hoch snd vele Energezustände besetzt und: R [ βb ( + ) ] ( + ) Exp[ β ( + ) ] ( + ) Exp 0 d βb kt B (X.6) (c) Schwngungsantel S Für en zweatomges Molekül kann man n erster äherung de Schwngung als enen harmonschen Oszllator beschreben. ach der Quantenmechank snd auch de Schwngungsenergen gequantelt: S ε ( ) n n + hω mt Schwngungsquantenzahl n0,,,.. Oft werden wr de Energe des Schwngungsgrundzustand (n0) glech null setzen, d.h. wr zehen von jeder Energe hω ab: S ε n nhω (X.7) Mt der l. (X. 7) fnden wr für de ustandssumme de unendlche geometrsche Rehe: S Exp n [ βnhω] ( Exp[ βhω] ) + ( Exp[ βhω] ) + ( Exp[ βhω] ) Exp n 0 [ βhω] n (X.8) Mehratomge (mehr als zwe) Moleküle haben mehrere Schwngungen. Ähnlch zu den Träghetsmomenten kann man auch für Schwngungen Hauptschwngungen (ormalschwngungen genannt) defneren. Ene belebge Schwngung kann als ene lneare Kombnaton von ormalschwngungen geschreben werden. En -atomges Molekül verfügt über Postonskoordnaten, Koordnaten snd für de Festlegung des ganzen Moleküls,, bzw. für de Festlegung der Rotaton des ganzen Moleküls. Also resulteren: 4
42 X. De ustandssumme enes mehratomgen ases -5 ormalschwngungen für lneare Moleküle -6 ormalschwngungen für ncht-lneare Moleküle Bespel: Wasserdampf hat dre ormalschwngungen: h ω 656 cm- h ω 594 cm- h ω 755 cm - De molekulare ustandssumme für Schwngungen st jetzt: S Exp [ βhω ] Exp[ βhω ] Exp[ βhω ] (X.9) Be Raumtemperatur st kt08 cm - und für Wasserdampf: S ( +,.0 )( + 4,7.0 )( +,4.0 ) d.h. nur der rundzustand st besetzt. (d) Elektronenantel E E In der Regel st kt << ε, z.b. für en Molekül mt ener UV-Absorpton be 50 nm st E ε cm -. Des bedeutet: E E [ ] Exp[ βε ] Exp βε (X.0) falls wr ε 0 setzen. Es könnte natürlch so sen, dass der rundzustand entartet st mt dem Entartungsgrad g, dann E g. usammenfassend haben wr jetzt de ustandssumme enes mehratomgen Moleküls: T R S E V kt g Λ B Exp[ ω (X.) βh ] Der Ausdruck (X.) st rchtg für Temperaturen hoch genug, so dass vele Rotatons- und Schwngungsnveaus besetzt snd, aber nur den elektronschen rundzustand st besetzt. Wenn auch nur den Schwngungsgrundzustand besetzt st, verschwndet das Produkt Π n (X.). 4
43 XI. Der lechvertelungssatz XI. Der lechvertelungssatz Wr versuchen jetzt abzuleten, we m lechgewcht de esamtenerge enes Moleküls über de Frehetsgraden Translaton, Rotaton und Schwngungen vertelt st. Dazu fangen wr mt dem Ausdruck für de esamtenerge U-U(0) an: Q ln Q U U ( 0) mt Q β β Q oder! Q. Unabhängg davon ob man unterschedbare oder ncht-unterschedbare Telchen hat, glt Dann: ln Q ln β β ln U U (0) β T T β R T R S E β β R S E S E β β β T R S E ( ) T R S E [ ε + ε + ε + ε ] wobe <ε> de mttleren Energen pro Molekül darstellen: Translaton T T ε T Λ V h.. kt T T T 4 β β Λ β Λ πm (XI.) Rotaton R ε R R β βb kt (XI.) Bβ β Schwngung S ε S S ( Exp β [ βhω] ) β Exp [ βhω] hωexp Exp [ βhω] [ βhω] Herfür kann man schreben, falls kt>>ħω: S ε [ βhω] [ β ω] hωexp Exp h kt β (XI.) De Translatonsenerge stellt sch nach der klassschen Physk aus dre Beträge zusammen: mv x + mv y + mvz. Pro quadratsche Term n dem klassschen Energeausdruck für de knetsche Energe gbt es m Mttel ene Energe kt. enauso für de Rotaton, pro 4
44 XI. Der lechvertelungssatz Rotatonsachse gbt es ene mttlere Energe pro Molekül von kt. De Schwngungsenerge besteht aus knetsche und potentelle Energe, jeder brngt m Mttel ene Energe kt. De esamtenerge vertelt sch also glechmäßg über de zur Verfügung stehenden Bewegungsmoden oder Frehetsgraden. 44
45 XII. De thermodynamschen röße XII De thermodynamschen röße Wr haben n den vorgehenden Kapteln gesehen, dass wr de Innere Energe U und de Entrope S n Q ausdrucken können: ( ln Q) Q U U ( 0) (XII.) Q β β S U U (0) + k ln Q (XII.) T Mt den l. (XII.) und (XII.) können wr auch den anderen theromodynamschen röße n Q ausdrucken: De Free Energe: F U U (0) U TS F ( 0) U (0) F F( 0) U U (0) T + k ln Q kt ln Q (XII.) T Der Druck p: df du TdS SdT TdS pdv TdS SdT pdv SdT F Q F F ln p kt df dv dt + V T V T V T T V (XII.4) F(0) Be der Herletung der l. (XII.4) haben wr angenommen, dass: 0, was nur rchtg V T st für deale ase. Deshalb zegt de l. (XII.4), dass für T0 auch p0 sen muss. De Enthalpe: H U + pv H ( 0) U (0) (nur deale ase) H H (0) U U (0) + pv Q ln Q + ktv Q β V T (XII.5) De free Enthalpe: H TS ( 0) H (0) (0) H H (0) TS ln Q ktv V T kt ln Q H H (0) U + U (0) kt ln Q pv kt ln Q (XII.6) 45
Die kanonische Zustandssumme (System) und ihr Zusammenhang mit der molekularen Zustandssumme (Einzelmolekül) unterscheidbare Teilchen:
 De molekulare Zustandssumme βε = e mt β = De kanonsche Zustandssumme (System) und hr Zusammenhang mt der molekularen Zustandssumme (Enzelmolekül) unterschedbare elchen: Q = ununterschedbareelchen Q : =!
De molekulare Zustandssumme βε = e mt β = De kanonsche Zustandssumme (System) und hr Zusammenhang mt der molekularen Zustandssumme (Enzelmolekül) unterschedbare elchen: Q = ununterschedbareelchen Q : =!
Abbildung 3.1: Besetzungszahlen eines Fermigases im Grundzustand (a)) und für eine angeregte Konfiguration (b)).
 44 n n F F a) b) Abbldung 3.: Besetzungszahlen enes Fermgases m Grundzustand (a)) und für ene angeregte Konfguraton (b)). 3.3 Ferm Drac Statstk In desem Abschntt wollen wr de thermodynamschen Egenschaften
44 n n F F a) b) Abbldung 3.: Besetzungszahlen enes Fermgases m Grundzustand (a)) und für ene angeregte Konfguraton (b)). 3.3 Ferm Drac Statstk In desem Abschntt wollen wr de thermodynamschen Egenschaften
10 Einführung in die Statistische Physik
 10 Enführung n de Statstsche Physk More s dfferent! P.W. Anderson, Nobelpres 1977 10.1 Prolegomena Technsch gesehen st de Rolle der Statstschen Mechank der Glechgewchtssysteme, ausgehend von unseren Kenntnsse
10 Enführung n de Statstsche Physk More s dfferent! P.W. Anderson, Nobelpres 1977 10.1 Prolegomena Technsch gesehen st de Rolle der Statstschen Mechank der Glechgewchtssysteme, ausgehend von unseren Kenntnsse
18. Vorlesung Sommersemester
 8. Vorlesung Sommersemester Der Drehmpuls des starren Körpers Der Drehmpuls des starren Körpers st etwas komplzerter. Wenn weder de Wnkelgeschwndgket um de feste Rotatonsachse st, so wrd mt Hlfe des doppelten
8. Vorlesung Sommersemester Der Drehmpuls des starren Körpers Der Drehmpuls des starren Körpers st etwas komplzerter. Wenn weder de Wnkelgeschwndgket um de feste Rotatonsachse st, so wrd mt Hlfe des doppelten
Rotation (2. Versuch)
 Rotaton 2. Versuch Bekannt snd berets Vektorfelder be denen das Lnenntegral über ene geschlossene Kurve Null wrd Stchworte: konservatve Kraft Potentalfelder Gradentenfeld. Es gbt auch Vektorfelder be denen
Rotaton 2. Versuch Bekannt snd berets Vektorfelder be denen das Lnenntegral über ene geschlossene Kurve Null wrd Stchworte: konservatve Kraft Potentalfelder Gradentenfeld. Es gbt auch Vektorfelder be denen
Die Hamilton-Jacobi-Theorie
 Kaptel 7 De Hamlton-Jacob-Theore Ausgearbetet von Rolf Horn und Bernhard Schmtz 7.1 Enletung Um de Hamlton schen Bewegungsglechungen H(q, p q k = p k H(p, q ṗ k = q k zu verenfachen, führten wr de kanonschen
Kaptel 7 De Hamlton-Jacob-Theore Ausgearbetet von Rolf Horn und Bernhard Schmtz 7.1 Enletung Um de Hamlton schen Bewegungsglechungen H(q, p q k = p k H(p, q ṗ k = q k zu verenfachen, führten wr de kanonschen
Werkstoffmechanik SS11 Baither/Schmitz. 5. Vorlesung
 Werkstoffmechank SS11 Bather/Schmtz 5. Vorlesung 0.05.011 4. Mkroskopsche Ursachen der Elastztät 4.1 Energeelastztät wrd bestmmt durch de Wechselwrkungspotentale zwschen den Atomen, oft schon auf der Bass
Werkstoffmechank SS11 Bather/Schmtz 5. Vorlesung 0.05.011 4. Mkroskopsche Ursachen der Elastztät 4.1 Energeelastztät wrd bestmmt durch de Wechselwrkungspotentale zwschen den Atomen, oft schon auf der Bass
16. Vorlesung Sommersemester
 16. Vorlesung Sommersemester 1 Das Egenwertproblem In allgemener Form hat das Egenwertproblem de Form A x = λ x, (1) wobe A ene n n-matrx, x en n-dmensonaler Vektor und λ der Egenwert st (n Englsch: egenvector,
16. Vorlesung Sommersemester 1 Das Egenwertproblem In allgemener Form hat das Egenwertproblem de Form A x = λ x, (1) wobe A ene n n-matrx, x en n-dmensonaler Vektor und λ der Egenwert st (n Englsch: egenvector,
3. Lineare Algebra (Teil 2)
 Mathematk I und II für Ingeneure (FB 8) Verson /704004 Lneare Algebra (Tel ) Parameterdarstellung ener Geraden Im folgenden betrachten wr Geraden m eukldschen Raum n, wobe uns hauptsächlch de Fälle n bzw
Mathematk I und II für Ingeneure (FB 8) Verson /704004 Lneare Algebra (Tel ) Parameterdarstellung ener Geraden Im folgenden betrachten wr Geraden m eukldschen Raum n, wobe uns hauptsächlch de Fälle n bzw
14 Exakte Statistik nichtwechselwirkender Teilchen
 Woche 4 Exakte Statstk nchtwechselwrkender Telchen 4 Bose-Ensten Statstk Engeführt von Satyendra ath Bose 924) für Photonen von A Ensten für massve Telchen 925) Voraussetzung: Bosonen Telchen mt ganzzahlgen
Woche 4 Exakte Statstk nchtwechselwrkender Telchen 4 Bose-Ensten Statstk Engeführt von Satyendra ath Bose 924) für Photonen von A Ensten für massve Telchen 925) Voraussetzung: Bosonen Telchen mt ganzzahlgen
Kreisel. koerperfestes KS. z y. raumfestes KS. Starrer Körper: System von Massepunkten m i, deren Abstände r i r j untereinander konstant sind.
 Kresel z y koerperfestes KS z y x raumfestes KS x Starrer Körper: System von Massepunkten m, deren Abstände r r j unterenander konstant snd. Der Zustand läßt sch beschreben durch: Poston des Schwerpunktes,
Kresel z y koerperfestes KS z y x raumfestes KS x Starrer Körper: System von Massepunkten m, deren Abstände r r j unterenander konstant snd. Der Zustand läßt sch beschreben durch: Poston des Schwerpunktes,
Einführung in die theoretische Physik 1
 Enführung n de theoretsche hysk 1 rof. Dr. L. Mathey Denstag 15:45 16:45 und Donnerstag 10:45 12:00 Begnn: 23.10.12 Jungus 9, Hörs 2 Mathey Enführung n de theor. hysk 1 1 Grundhypothese der Thermostatk
Enführung n de theoretsche hysk 1 rof. Dr. L. Mathey Denstag 15:45 16:45 und Donnerstag 10:45 12:00 Begnn: 23.10.12 Jungus 9, Hörs 2 Mathey Enführung n de theor. hysk 1 1 Grundhypothese der Thermostatk
Course Dec 15, Statistische Mechanik plus. Course Hartmut Ruhl, LMU, Munich. People involved. Rationale
 Dec 15, 2016 ASC, room A 238, phone 089-21804210, emal hartmut.ruhl@lmu.de Patrc Böhl, ASC, room A205, phone 089-21804640, emal patrc.boehl@phys.un-muenchen.de. Dsusson der Besetzungszahldarstellungen
Dec 15, 2016 ASC, room A 238, phone 089-21804210, emal hartmut.ruhl@lmu.de Patrc Böhl, ASC, room A205, phone 089-21804640, emal patrc.boehl@phys.un-muenchen.de. Dsusson der Besetzungszahldarstellungen
Für jeden reinen, ideal kristallisierten Stoff ist die Entropie am absoluten Nullpunkt gleich
 Drtter Hauptsatz der Thermodynamk Rückblck auf vorherge Vorlesung Methoden zur Erzeugung tefer Temperaturen: - umgekehrt laufende WKM (Wärmepumpe) - Joule-Thomson Effekt bs 4 K - Verdampfen von flüssgem
Drtter Hauptsatz der Thermodynamk Rückblck auf vorherge Vorlesung Methoden zur Erzeugung tefer Temperaturen: - umgekehrt laufende WKM (Wärmepumpe) - Joule-Thomson Effekt bs 4 K - Verdampfen von flüssgem
22. Vorlesung Sommersemester
 22 Vorlesung Sommersemester 1 Bespel 2: Würfel mt festgehaltener Ecke In desem Fall wählt man den Koordnatenursprung n der Ecke und der Würfel st durch den Berech x = 0 a, y = 0 a und z = 0 a bestmmt De
22 Vorlesung Sommersemester 1 Bespel 2: Würfel mt festgehaltener Ecke In desem Fall wählt man den Koordnatenursprung n der Ecke und der Würfel st durch den Berech x = 0 a, y = 0 a und z = 0 a bestmmt De
Grundlagen der Mathematik I Lösungsvorschlag zum 12. Tutoriumsblatt
 Mathematsches Insttut der Unverstät München Wntersemester 3/4 Danel Rost Lukas-Faban Moser Grundlagen der Mathematk I Lösungsvorschlag zum. Tutorumsblatt Aufgabe. a De Formel besagt, daß de Summe der umrahmten
Mathematsches Insttut der Unverstät München Wntersemester 3/4 Danel Rost Lukas-Faban Moser Grundlagen der Mathematk I Lösungsvorschlag zum. Tutorumsblatt Aufgabe. a De Formel besagt, daß de Summe der umrahmten
Dynamik starrer Körper
 Dynamk starrer Körper Bewegungen starrer Körper können n Translaton und Rotaton zerlegt werden. De Rotaton stellt enen nneren Frehetsgrad des Körpers dar, der be Punktmassen ncht exstert. Der Schwerpunkt
Dynamk starrer Körper Bewegungen starrer Körper können n Translaton und Rotaton zerlegt werden. De Rotaton stellt enen nneren Frehetsgrad des Körpers dar, der be Punktmassen ncht exstert. Der Schwerpunkt
19. Vorlesung Sommersemester
 19. Vorlesung Sommersemester 1 Allgemene Bewegung des starren Körpers Bsher wurde nur der Fall behandelt, dass de Drehachse festgehalten wrd. Im allgemenen Fall kommen als Probleme hnzu, dass 1. de Drehachse
19. Vorlesung Sommersemester 1 Allgemene Bewegung des starren Körpers Bsher wurde nur der Fall behandelt, dass de Drehachse festgehalten wrd. Im allgemenen Fall kommen als Probleme hnzu, dass 1. de Drehachse
Theoretische Physik: Mechanik
 Ferenkurs Theoretsche Physk: Mechank Sommer 018 Vorlesung 4 (mt freundlcher Genehmgung von Gramos Qerm, Jakob Unfred und Verena Walbrecht) Technsche Unverstät München 1 Fakultät für Physk Inhaltsverzechns
Ferenkurs Theoretsche Physk: Mechank Sommer 018 Vorlesung 4 (mt freundlcher Genehmgung von Gramos Qerm, Jakob Unfred und Verena Walbrecht) Technsche Unverstät München 1 Fakultät für Physk Inhaltsverzechns
Definition des linearen Korrelationskoeffizienten
 Defnton des lnearen Korrelatonskoeffzenten r xy x y y r x xy y 1 x x y y x Der Korrelatonskoeffzent st en Indkator dafür, we gut de Punkte (X,Y) zu ener Geraden passen. Sen Wert legt zwschen -1 und +1.
Defnton des lnearen Korrelatonskoeffzenten r xy x y y r x xy y 1 x x y y x Der Korrelatonskoeffzent st en Indkator dafür, we gut de Punkte (X,Y) zu ener Geraden passen. Sen Wert legt zwschen -1 und +1.
29 zweite Ableitungen der thermodynamischen Potentiale spezifische Wärme (thermischer response) E = = = T V N V N V N = = κ T.
 hermodynamsche resonse -unktonen: 9 zwete Abletungen der thermodynamschen Potentale sezfsche Wärme (thermscher resonse) E C S be konstantem olumen (sochor):,,, be konstantem Druck (sobar): C S Komressbltät
hermodynamsche resonse -unktonen: 9 zwete Abletungen der thermodynamschen Potentale sezfsche Wärme (thermscher resonse) E C S be konstantem olumen (sochor):,,, be konstantem Druck (sobar): C S Komressbltät
Der starre Körper. 1 Grundlagen. Dominik Fauser. 1.1 Denition. 1.2 Freiheitsgrade
 Der starre Körper Domnk Fauser 1 Grundlagen 1.1 Denton Als enen starren Körper bezechnet man en System von Massepunkten m, deren Abstände zuenander konstant snd: r j = r r j. Mest betrachtet man ene sehr
Der starre Körper Domnk Fauser 1 Grundlagen 1.1 Denton Als enen starren Körper bezechnet man en System von Massepunkten m, deren Abstände zuenander konstant snd: r j = r r j. Mest betrachtet man ene sehr
Sei T( x ) die Tangente an den Graphen der Funktion f(x) im Punkt ( x 0, f(x 0 ) ) : T( x ) = f(x 0 ) + f (x 0 ) ( x - x 0 ).
 Taylorentwcklung (Approxmaton durch Polynome). Problemstellung Se T( x ) de Tangente an den Graphen der Funkton f(x) m Punkt ( x 0, f(x 0 ) ) : T( x ) = f(x 0 ) + f (x 0 ) ( x - x 0 ). Dann kann man de
Taylorentwcklung (Approxmaton durch Polynome). Problemstellung Se T( x ) de Tangente an den Graphen der Funkton f(x) m Punkt ( x 0, f(x 0 ) ) : T( x ) = f(x 0 ) + f (x 0 ) ( x - x 0 ). Dann kann man de
2 Zufallsvariable und Verteilungen
 Zufallsvarable und Vertelungen 7 Zufallsvarable und Vertelungen Wr wollen uns jetzt mt Zufallsexpermenten beschäftgen, deren Ausgänge durch (reelle) Zahlen beschreben werden können, oder be denen man jedem
Zufallsvarable und Vertelungen 7 Zufallsvarable und Vertelungen Wr wollen uns jetzt mt Zufallsexpermenten beschäftgen, deren Ausgänge durch (reelle) Zahlen beschreben werden können, oder be denen man jedem
Elektron Loch Symmetrie und Grundzustand beim Fraktionellen Quanten Halleffekt (FQHE)
 Hauptsemnar Theoretsche Physk (Sommersemester 003) Elektron Loch Symmetre und Grundzustand bem Fraktonellen Quanten Halleffekt (FQHE) Srko Plz 04.06.003 Velen Dank an den Betreuer T. Sommer für sene Unterstützung
Hauptsemnar Theoretsche Physk (Sommersemester 003) Elektron Loch Symmetre und Grundzustand bem Fraktonellen Quanten Halleffekt (FQHE) Srko Plz 04.06.003 Velen Dank an den Betreuer T. Sommer für sene Unterstützung
Konkave und Konvexe Funktionen
 Konkave und Konvexe Funktonen Auch wenn es n der Wrtschaftstheore mest ncht möglch st, de Form enes funktonalen Zusammenhangs explzt anzugeben, so kann man doch n velen Stuatonen de Klasse der n Frage
Konkave und Konvexe Funktonen Auch wenn es n der Wrtschaftstheore mest ncht möglch st, de Form enes funktonalen Zusammenhangs explzt anzugeben, so kann man doch n velen Stuatonen de Klasse der n Frage
Modellierung von Molekülen
 Karl-Franzens-Unverstät Graz Modellerung von Molekülen Treffpunkt: Henrchstraße 28, 6. OG Betreuer: Dr. Oleksandr LOBODA Robn Guttmann, BSc Karl-Franzens-Unverstät Graz WS 2015/16 Zel des Versuches In
Karl-Franzens-Unverstät Graz Modellerung von Molekülen Treffpunkt: Henrchstraße 28, 6. OG Betreuer: Dr. Oleksandr LOBODA Robn Guttmann, BSc Karl-Franzens-Unverstät Graz WS 2015/16 Zel des Versuches In
7 Schrödingergleichung
 36 7 Schrödngerglechung 7 Schrödngerglechung De Schrödngerglechung spelt n der Quantenmechank ene zentrale Rolle. Mt hr wrd de Wellenfunkton des Systems berechnet. Der erste Bestandtel der Schrödngerglechung
36 7 Schrödngerglechung 7 Schrödngerglechung De Schrödngerglechung spelt n der Quantenmechank ene zentrale Rolle. Mt hr wrd de Wellenfunkton des Systems berechnet. Der erste Bestandtel der Schrödngerglechung
Theoretische Physik 2 (Theoretische Mechanik)
 Theoretsche Physk 2 (Theoretsche Mechank Prof. Dr. Th. Feldmann 28. Oktober 2013 Kurzzusammenfassung Vorlesung 4 vom 25.10.2013 1.6 Dynamk mehrerer Massenpunkte Dynamk für = 1... N Massenpunkte mt.a. komplzerter
Theoretsche Physk 2 (Theoretsche Mechank Prof. Dr. Th. Feldmann 28. Oktober 2013 Kurzzusammenfassung Vorlesung 4 vom 25.10.2013 1.6 Dynamk mehrerer Massenpunkte Dynamk für = 1... N Massenpunkte mt.a. komplzerter
Multilineare Algebra und ihre Anwendungen. Nr. 6: Normalformen. Verfasser: Yee Song Ko Adrian Jenni Rebecca Huber Damian Hodel
 ultlneare Algebra und hre Anwendungen Nr. : Normalformen Verfasser: Yee Song Ko Adran Jenn Rebecca Huber Daman Hodel 9.5.7 - - ultlneare Algebra und hre Anwendungen Jordan sche Normalform Allgemene heore
ultlneare Algebra und hre Anwendungen Nr. : Normalformen Verfasser: Yee Song Ko Adran Jenn Rebecca Huber Daman Hodel 9.5.7 - - ultlneare Algebra und hre Anwendungen Jordan sche Normalform Allgemene heore
Die Annäherung der Binomialverteilung durch die Normalverteilung am Beispiel eines Modells der Schadenversicherung
 am Bespel enes Modells der chadenverscherung Für das Modell ener chadenverscherung se gegeben: s w s. n 4 chaden enes Verscherungsnehmers, wenn der chadenfall entrtt Wahrschenlchket dafür, dass der chadenfall
am Bespel enes Modells der chadenverscherung Für das Modell ener chadenverscherung se gegeben: s w s. n 4 chaden enes Verscherungsnehmers, wenn der chadenfall entrtt Wahrschenlchket dafür, dass der chadenfall
Grundgedanke der Regressionsanalyse
 Grundgedanke der Regressonsanalse Bsher wurden durch Koeffzenten de Stärke von Zusammenhängen beschreben Mt der Regressonsrechnung können für ntervallskalerte Varablen darüber hnaus Modelle geschätzt werden
Grundgedanke der Regressonsanalse Bsher wurden durch Koeffzenten de Stärke von Zusammenhängen beschreben Mt der Regressonsrechnung können für ntervallskalerte Varablen darüber hnaus Modelle geschätzt werden
Regressionsgerade. x x 1 x 2 x 3... x n y y 1 y 2 y 3... y n
 Regressonsgerade x x x x 3... x n y y y y 3... y n Bem Auswerten von Messrehen wrd häufg ene durch theoretsche Überlegungen nahegelegte lneare Bezehung zwschen den x- und y- Werten gesucht, d.h. ene Gerade
Regressonsgerade x x x x 3... x n y y y y 3... y n Bem Auswerten von Messrehen wrd häufg ene durch theoretsche Überlegungen nahegelegte lneare Bezehung zwschen den x- und y- Werten gesucht, d.h. ene Gerade
PC4 Statistische Thermodynamik
 PC4 Statstsche Thermodynamk 1. Enletung 1.1 Enordnung n de Physkalsche Cheme 1.2 Konzept der Ensembles (Gesamtheten) 1.3 Postulate der Statstschen Thermodynamk 1.4 Hstorsche Entwcklung 2. Grundlagen der
PC4 Statstsche Thermodynamk 1. Enletung 1.1 Enordnung n de Physkalsche Cheme 1.2 Konzept der Ensembles (Gesamtheten) 1.3 Postulate der Statstschen Thermodynamk 1.4 Hstorsche Entwcklung 2. Grundlagen der
PC Der vollständige Laufzettel ist im Sekretariat einzureichen.
 2014-04-08 Physkalsche Cheme für Fortgeschrttene Praktkumsenführung Dr. Manuela Rechelt 0 Organsaton 0.1 Vorlesung De Klausur fndet etzt am 29.07.2014 (ncht 22.07.2014!) um 10:15 n Hörsaal 4 statt (Termn
2014-04-08 Physkalsche Cheme für Fortgeschrttene Praktkumsenführung Dr. Manuela Rechelt 0 Organsaton 0.1 Vorlesung De Klausur fndet etzt am 29.07.2014 (ncht 22.07.2014!) um 10:15 n Hörsaal 4 statt (Termn
Eine kurze Einführung in die Dichtefunktionaltheorie (DFT)
 Ene kurze Enführung n de Dchtefunktonaltheore (DFT) Mchael Martns Lteratur: W. Koch, M.C. Holthausen A Chemst s Gude to Densty Functonal Theory Wley-VCH 2001 Dchtefunktonaltheore p.1 Enletung Im Falle
Ene kurze Enführung n de Dchtefunktonaltheore (DFT) Mchael Martns Lteratur: W. Koch, M.C. Holthausen A Chemst s Gude to Densty Functonal Theory Wley-VCH 2001 Dchtefunktonaltheore p.1 Enletung Im Falle
Protokoll zu Versuch C1-Mischungsvolumina
 Protokoll zu Prnz: De sezfschen Mschungsvolumna ener Lösung werden durch auswegen fester Flüssgketsvolumna bekannter Lösungszusammensetzungen mt Hlfe von Pyknometern bestmmt. Theoretsche Grundlagen: Um
Protokoll zu Prnz: De sezfschen Mschungsvolumna ener Lösung werden durch auswegen fester Flüssgketsvolumna bekannter Lösungszusammensetzungen mt Hlfe von Pyknometern bestmmt. Theoretsche Grundlagen: Um
Temperaturabhängigkeit der Beweglichkeit
 Temperaturabhänggket der Beweglchket De Beweglchket nmmt mt zunehmender Temperatur ab! Streuung mt dem Gtter! Feldabhänggket der Beweglchket Für sehr hohe Feldstärken nmmt de Beweglchket n GaAs ab! Feldabhänggket
Temperaturabhänggket der Beweglchket De Beweglchket nmmt mt zunehmender Temperatur ab! Streuung mt dem Gtter! Feldabhänggket der Beweglchket Für sehr hohe Feldstärken nmmt de Beweglchket n GaAs ab! Feldabhänggket
Übungsklausur zur Vorlesung Wahrscheinlichkeit und Regression Lösungen. Übungsklausur Wahrscheinlichkeit und Regression Die Lösungen
 Übungsklausur Wahrschenlchket und Regresson De Lösungen. Welche der folgenden Aussagen treffen auf en Zufallsexperment zu? a) En Zufallsexperment st en emprsches Phänomen, das n stochastschen Modellen
Übungsklausur Wahrschenlchket und Regresson De Lösungen. Welche der folgenden Aussagen treffen auf en Zufallsexperment zu? a) En Zufallsexperment st en emprsches Phänomen, das n stochastschen Modellen
9 Komplexe Zahlen ( ) ( ) 9.1 Ziele. 9.2 Warum braucht man komplexe Zahlen? 9.3 Darstellung von komplexen Zahlen. r 2. j 2. j 1.
 Mathematk I / Komplexe Zahlen 9 Komplexe Zahlen 9. Zele Am Ende deses Kaptels hast Du ene Grundvorstellung was komplexe Zahlen snd. Du kannst se grafsch darstellen und enfache Berechnungen durchführen.
Mathematk I / Komplexe Zahlen 9 Komplexe Zahlen 9. Zele Am Ende deses Kaptels hast Du ene Grundvorstellung was komplexe Zahlen snd. Du kannst se grafsch darstellen und enfache Berechnungen durchführen.
Arbeitsgruppe Radiochemie Radiochemisches Praktikum P 06. Einführung in die Statistik. 1. Zählung von radioaktiven Zerfällen und Statistik 2
 ETH Arbetsgruppe Radocheme Radochemsches Praktkum P 06 Enführung n de Statstk INHALTSVERZEICHNIS Sete 1. Zählung von radoaktven Zerfällen und Statstk 2 2. Mttelwert und Varanz 2 3. Momente ener Vertelung
ETH Arbetsgruppe Radocheme Radochemsches Praktkum P 06 Enführung n de Statstk INHALTSVERZEICHNIS Sete 1. Zählung von radoaktven Zerfällen und Statstk 2 2. Mttelwert und Varanz 2 3. Momente ener Vertelung
Physik A VL11 ( )
 Physk A VL11 (0.11.01) Dynamk der Rotatonsbewegung I Kresbewegung und Kräfte Drehmoment und räghetsmoment Kresbewegung und Kräfte en Massepunkt (Schwerpunkt) führt nur ene ranslatonsbewegung aus ausgedehnte
Physk A VL11 (0.11.01) Dynamk der Rotatonsbewegung I Kresbewegung und Kräfte Drehmoment und räghetsmoment Kresbewegung und Kräfte en Massepunkt (Schwerpunkt) führt nur ene ranslatonsbewegung aus ausgedehnte
3.6 Molekulare Dynamik
 3.6 Molekulare Dynamk In den letzten 5 Jahrzehnten wurden drekte numersche Smulatonen zur statstschen Auswertung von Veltelchensystemen mmer wchtger. So lassen sch Phasenübergänge, aber auch makroskopsche
3.6 Molekulare Dynamk In den letzten 5 Jahrzehnten wurden drekte numersche Smulatonen zur statstschen Auswertung von Veltelchensystemen mmer wchtger. So lassen sch Phasenübergänge, aber auch makroskopsche
Daten sind in Tabellenform gegeben durch die Eingabe von FORMELN können mit diesen Daten automatisierte Berechnungen durchgeführt werden.
 Ene kurze Enführung n EXCEL Daten snd n Tabellenform gegeben durch de Engabe von FORMELN können mt desen Daten automatserte Berechnungen durchgeführt werden. Menüleste Symbolleste Bearbetungszele aktve
Ene kurze Enführung n EXCEL Daten snd n Tabellenform gegeben durch de Engabe von FORMELN können mt desen Daten automatserte Berechnungen durchgeführt werden. Menüleste Symbolleste Bearbetungszele aktve
Vorlesung 3 Differentialgeometrie in der Physik 13
 Vorlesung 3 Dfferentalgeometre n der Physk 13 Bemerkung. Ist M Manngfaltgket, p M und φ : U R n Karte mt p U, so nennt man U auch Koordnatenumgebung und φ auch Koordnatensystem n p. Bespel 2.4 Seen R >
Vorlesung 3 Dfferentalgeometre n der Physk 13 Bemerkung. Ist M Manngfaltgket, p M und φ : U R n Karte mt p U, so nennt man U auch Koordnatenumgebung und φ auch Koordnatensystem n p. Bespel 2.4 Seen R >
Bedingte Entropie. Bedingte Entropie. Bedingte Entropie. Kapitel 4: Bedingte Entropie I(X;Y) H(X Y) H(Y) H(X) H(XY)
 Bedngte Entrope Kaptel : Bedngte Entrope Das vorherge Theorem kann durch mehrfache Anwendung drekt verallgemenert werden H (... H ( = Ebenso kann de bedngt Entrope defnert werden Defnton: De bedngte Entrope
Bedngte Entrope Kaptel : Bedngte Entrope Das vorherge Theorem kann durch mehrfache Anwendung drekt verallgemenert werden H (... H ( = Ebenso kann de bedngt Entrope defnert werden Defnton: De bedngte Entrope
I)1. Kinematik. EP WS 2009/10 Dünnweber/Faessler
 I)1. Knematk I) Mechank 1.Knematk (Bewegung) 2. Dynamk on Massenpunkten (Enfluss on Kräften) 3. Starre Körper 4.Deformerbare Meden 5. Schwngungen, Wellen, Akustk I)1. Knematk Bewegungslehre (Zel: Quanttate
I)1. Knematk I) Mechank 1.Knematk (Bewegung) 2. Dynamk on Massenpunkten (Enfluss on Kräften) 3. Starre Körper 4.Deformerbare Meden 5. Schwngungen, Wellen, Akustk I)1. Knematk Bewegungslehre (Zel: Quanttate
( ) γ. (t 1 ) (t 2 ) = Arg γ 2(t 2 )
 Funktonentheore, Woche 10 Bholomorphe Abbldungen 10.1 Konform und bholomorph Ene konforme Abbldung erhält Wnkel und Orenterung. Damt st folgendes gement: Wenn sch zwe Kurven schneden, dann schneden sch
Funktonentheore, Woche 10 Bholomorphe Abbldungen 10.1 Konform und bholomorph Ene konforme Abbldung erhält Wnkel und Orenterung. Damt st folgendes gement: Wenn sch zwe Kurven schneden, dann schneden sch
wird auch Spannweite bzw. Variationsbreite genannt ist definiert als die Differenz zwischen dem größten und kleinsten Messwert einer Verteilung:
 Streuungswerte: 1) Range (R) ab metrschem Messnveau ) Quartlabstand (QA) und mttlere Quartlabstand (MQA) ab metrschem Messnveau 3) Durchschnttlche Abwechung (AD) ab metrschem Messnveau 4) Varanz (s ) ab
Streuungswerte: 1) Range (R) ab metrschem Messnveau ) Quartlabstand (QA) und mttlere Quartlabstand (MQA) ab metrschem Messnveau 3) Durchschnttlche Abwechung (AD) ab metrschem Messnveau 4) Varanz (s ) ab
9 Komplexe Zahlen ( ) ( ) 9.1 Ziele. 9.2 Warum braucht man komplexe Zahlen? 9.3 Darstellung von komplexen Zahlen. r 2. j 2. j 1.
 Mathematk I / Komplexe Zahlen 9 Komplexe Zahlen 9. Zele Am Ende deses Kaptels hast Du ene Grundvorstellung was komplexe Zahlen snd. Du kannst se grafsch darstellen und enfache Berechnungen durchführen.
Mathematk I / Komplexe Zahlen 9 Komplexe Zahlen 9. Zele Am Ende deses Kaptels hast Du ene Grundvorstellung was komplexe Zahlen snd. Du kannst se grafsch darstellen und enfache Berechnungen durchführen.
Stochastische Prozesse
 INSTITUT FÜR STOCHASTIK SS 009 UNIVERSITÄT KARLSRUHE Blatt 4 Prv.-Doz. Dr. D. Kadelka Dpl.-Math. W. Lao Übungen zur Vorlesung Stochastsche Prozesse Musterlösungen Aufgabe 16: (Success Run, Fortsetzung)
INSTITUT FÜR STOCHASTIK SS 009 UNIVERSITÄT KARLSRUHE Blatt 4 Prv.-Doz. Dr. D. Kadelka Dpl.-Math. W. Lao Übungen zur Vorlesung Stochastsche Prozesse Musterlösungen Aufgabe 16: (Success Run, Fortsetzung)
3 Elastizitätstheorie
 3 Elastztätstheore Für en elastsches Medum nmmt man enen spannungsfreen Referenzzustand an, der n Eulerkoordnaten durch x = Ax, t) gegeben st. Abwechungen werden beschreben durch de Verschebung ux, t)
3 Elastztätstheore Für en elastsches Medum nmmt man enen spannungsfreen Referenzzustand an, der n Eulerkoordnaten durch x = Ax, t) gegeben st. Abwechungen werden beschreben durch de Verschebung ux, t)
Statistik Exponentialfunktion
 ! " Statstk " Eponentalfunkton # $ % & ' $ ( )&* +, - +. / $ 00, 1 +, + ) Ensemble von radoaktven Atomkernen Zerfallskonstante λ [1/s] Lebensdauer τ 1/λ [s] Anzahl der pro Zetenhet zerfallenden Kerne:
! " Statstk " Eponentalfunkton # $ % & ' $ ( )&* +, - +. / $ 00, 1 +, + ) Ensemble von radoaktven Atomkernen Zerfallskonstante λ [1/s] Lebensdauer τ 1/λ [s] Anzahl der pro Zetenhet zerfallenden Kerne:
Experimentalphysik II (Kip SS 2007)
 permentalphsk II (Kp SS 007) Zusatvorlesungen: Z-1 n- und mehrdmensonale Integraton Z- Gradent, Dvergen und Rotaton Z-3 Gaußscher und Stokesscher Integralsat Z-4 Kontnutätsglechung Z-5 lektromagnetsche
permentalphsk II (Kp SS 007) Zusatvorlesungen: Z-1 n- und mehrdmensonale Integraton Z- Gradent, Dvergen und Rotaton Z-3 Gaußscher und Stokesscher Integralsat Z-4 Kontnutätsglechung Z-5 lektromagnetsche
Facility Location Games
 Faclty Locaton Games Semnar über Algorthmen SS 2006 Klaas Joeppen 1 Abstract Wr haben berets sehr häufg von Nash-Glechgewchten und vor allem von deren Exstenz gesprochen. Das Faclty Locaton Game betet
Faclty Locaton Games Semnar über Algorthmen SS 2006 Klaas Joeppen 1 Abstract Wr haben berets sehr häufg von Nash-Glechgewchten und vor allem von deren Exstenz gesprochen. Das Faclty Locaton Game betet
Modellierung von Molekülen
 Karl-Franzens-Unverstät Graz Modellerung von Molekülen Treffpunkt: Henrchstraße 28, 6. OG, Raum 613 Betreuer: Oleksandr Loboda, Raum 417A (4. OG), Tel: 380 5447, e-mal: oleksandr.loboda@un-graz.at Robn
Karl-Franzens-Unverstät Graz Modellerung von Molekülen Treffpunkt: Henrchstraße 28, 6. OG, Raum 613 Betreuer: Oleksandr Loboda, Raum 417A (4. OG), Tel: 380 5447, e-mal: oleksandr.loboda@un-graz.at Robn
I) Mechanik 1.Kinematik (Bewegung)
 I)1. Knematk I) Mechank 1.Knematk (Bewegung) 2. Dynamk on Massenpunkten (Enfluss on Kräften) 3. Starre Körper 4.Deformerbare Meden 5. Schwngungen, Wellen, Akustk I)1. Knematk Bewegungslehre (Zel: Quanttate
I)1. Knematk I) Mechank 1.Knematk (Bewegung) 2. Dynamk on Massenpunkten (Enfluss on Kräften) 3. Starre Körper 4.Deformerbare Meden 5. Schwngungen, Wellen, Akustk I)1. Knematk Bewegungslehre (Zel: Quanttate
Die mathematischen Grundlagen der Wellenmechanik
 De mathematschen Grundlagen der Wellenmechank Zustände und deren Darstellung En physkalsches System wrd durch enen Zustand u charaktersert, ndem es durch ene bestmmte expermentelle Präparaton gebracht
De mathematschen Grundlagen der Wellenmechank Zustände und deren Darstellung En physkalsches System wrd durch enen Zustand u charaktersert, ndem es durch ene bestmmte expermentelle Präparaton gebracht
6.4 Auswahlregeln für Schwingungsspektroskopie 6 AUSWAHLREGELN 72
 6 AUSWAHLREGELN 72 En Spezalfall, be dem sch de Berechnung der drekten Produkte noch weter verenfachen lässt, st der Gerade-Ungerade-Formalsmus Als Aussage ergbt sch: In Übergangsmetallkomplexen mt Inversonszentrum
6 AUSWAHLREGELN 72 En Spezalfall, be dem sch de Berechnung der drekten Produkte noch weter verenfachen lässt, st der Gerade-Ungerade-Formalsmus Als Aussage ergbt sch: In Übergangsmetallkomplexen mt Inversonszentrum
Statistik und Wahrscheinlichkeitsrechnung
 Statstk und Wahrschenlchketsrechnung Statstk und Wahrschenlchketsrechnung 5. Vorlesung Dr. Jochen Köhler.03.0 Statstk und Wahrschenlchketsrechnung Wchtg!!! Vorlesung Do 4.03.0 HCI G3 Übung 5 D 9.03.0 Fnk
Statstk und Wahrschenlchketsrechnung Statstk und Wahrschenlchketsrechnung 5. Vorlesung Dr. Jochen Köhler.03.0 Statstk und Wahrschenlchketsrechnung Wchtg!!! Vorlesung Do 4.03.0 HCI G3 Übung 5 D 9.03.0 Fnk
4.6 Das Pumping-Lemma für reguläre Sprachen:
 Theoretsche Informatk 1 Vorlesungsskrpt vom Fretag, 30 Jun 000 Index: Erstellt von: (Matrkelnummer: 70899) Sete : 46 Das Pumpng-Lemma für reguläre Sprachen 1 Satz W 1 Zugrundelegende Idee des Pumpng-Lemma
Theoretsche Informatk 1 Vorlesungsskrpt vom Fretag, 30 Jun 000 Index: Erstellt von: (Matrkelnummer: 70899) Sete : 46 Das Pumpng-Lemma für reguläre Sprachen 1 Satz W 1 Zugrundelegende Idee des Pumpng-Lemma
Fallstudie 1 Diskrete Verteilungen Abgabe: Aufgabentext und Lösungen schriftlich bis zum
 Abgabe: Aufgabentext und Lösungen schrftlch bs zum 15. 6. 2012 I. Thema: Zehen mt und ohne Zurücklegen Lesen Se sch zunächst folgenden Text durch! Wr haben bsher Stchprobenzehungen aus Grundgesamtheten
Abgabe: Aufgabentext und Lösungen schrftlch bs zum 15. 6. 2012 I. Thema: Zehen mt und ohne Zurücklegen Lesen Se sch zunächst folgenden Text durch! Wr haben bsher Stchprobenzehungen aus Grundgesamtheten
1 Mehrdimensionale Analysis
 1 Mehrdmensonale Analyss Bespel: De Gesamtmasse der Erde st ene Funton der Erddchte ρ Erde und des Erdradus r Erde De Gesamtmasse der Erde st dann m Erde = V Erde ρ Erde Das Volumen ener Kugel mt Radus
1 Mehrdmensonale Analyss Bespel: De Gesamtmasse der Erde st ene Funton der Erddchte ρ Erde und des Erdradus r Erde De Gesamtmasse der Erde st dann m Erde = V Erde ρ Erde Das Volumen ener Kugel mt Radus
1 Finanzmathematik. 1.1 Das Modell. Sei Xt
 1.1 Das Modell Se Xt der Pres enes Assets zur Zet t und X = X ) 1 d der Rd +-dmensonale Presprozess. Das Geld kann auch zu dem rskolosen Znssatz r be ener Bank angelegt werden. Der Wert deser Anlage wrd
1.1 Das Modell Se Xt der Pres enes Assets zur Zet t und X = X ) 1 d der Rd +-dmensonale Presprozess. Das Geld kann auch zu dem rskolosen Znssatz r be ener Bank angelegt werden. Der Wert deser Anlage wrd
-70- Anhang: -Lineare Regression-
 -70- Anhang: -Lneare Regressn- Für ene Messgröße y f(x) gelte flgender mathematsche Zusammenhang: y a+ b x () In der Regel läßt sch durch enen Satz vn Messwerten (x, y ) aber kene Gerade zechnen, da de
-70- Anhang: -Lneare Regressn- Für ene Messgröße y f(x) gelte flgender mathematsche Zusammenhang: y a+ b x () In der Regel läßt sch durch enen Satz vn Messwerten (x, y ) aber kene Gerade zechnen, da de
Weitere NP-vollständige Probleme
 Wetere NP-vollständge Probleme Prosemnar Theoretsche Informatk Marten Tlgner December 10, 2014 Wr haben letzte Woche gesehen, dass 3SAT NP-vollständg st. Heute werden wr für enge wetere Probleme n NP zegen,
Wetere NP-vollständge Probleme Prosemnar Theoretsche Informatk Marten Tlgner December 10, 2014 Wr haben letzte Woche gesehen, dass 3SAT NP-vollständg st. Heute werden wr für enge wetere Probleme n NP zegen,
Analysis I. Vorlesung 17. Logarithmen. R R, x exp x,
 Prof. Dr. H. Brenner Osnabrück WS 2013/2014 Analyss I Vorlesung 17 Logarthmen Satz 17.1. De reelle Exponentalfunkton R R, x exp x, st stetg und stftet ene Bjekton zwschen R und R +. Bewes. De Stetgket
Prof. Dr. H. Brenner Osnabrück WS 2013/2014 Analyss I Vorlesung 17 Logarthmen Satz 17.1. De reelle Exponentalfunkton R R, x exp x, st stetg und stftet ene Bjekton zwschen R und R +. Bewes. De Stetgket
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stchwörter von der letzten Vorlesung können Se sch noch ernnern? Gasgesetz ür deale Gase pv = nr Gelestete Arbet be sotherme Ausdehnung adabatsche Ausdehnung 2 n Reale Gase p + a 2 ( V nb) =
An welche Stchwörter von der letzten Vorlesung können Se sch noch ernnern? Gasgesetz ür deale Gase pv = nr Gelestete Arbet be sotherme Ausdehnung adabatsche Ausdehnung 2 n Reale Gase p + a 2 ( V nb) =
Modellierung von Molekülen
 Karl-Franzens-Unverstät Graz Modellerung von Molekülen Praktkumsversuch für Lehramtskanddaten Treffpunkt: Henrchstraße 28, 6. OG, Raum 613 Betreuer: Grygory Dolgonos, Raum 20 (1. OG), Tel: 380 5421, e-mal:
Karl-Franzens-Unverstät Graz Modellerung von Molekülen Praktkumsversuch für Lehramtskanddaten Treffpunkt: Henrchstraße 28, 6. OG, Raum 613 Betreuer: Grygory Dolgonos, Raum 20 (1. OG), Tel: 380 5421, e-mal:
Noethertheorem. 30. Januar 2012
 Noethertheorem 30. Januar 2012 1 Inhaltsverzechns 1 Symmetre 3 1.1 Symmetre n der Geometre................... 3 1.2 Symmetre n der Mathematk.................. 3 1.3 Symmetre n der Physk.....................
Noethertheorem 30. Januar 2012 1 Inhaltsverzechns 1 Symmetre 3 1.1 Symmetre n der Geometre................... 3 1.2 Symmetre n der Mathematk.................. 3 1.3 Symmetre n der Physk.....................
3. Vorlesung Sommersemester
 3. Vorlesung Sommersemester 1 Bespele (Fortsetzung) 1. Der starre Körper: Formulerung der Zwangsbedngungen später. Anschaulch snd schon de Frehetsgrade: dre der Translaton (z. B. Schwerpuntsoordnaten)
3. Vorlesung Sommersemester 1 Bespele (Fortsetzung) 1. Der starre Körper: Formulerung der Zwangsbedngungen später. Anschaulch snd schon de Frehetsgrade: dre der Translaton (z. B. Schwerpuntsoordnaten)
Modellieru g vo Moleküle
 La orü u ge aus Physkals her Che e Karl-Fra ze s-u verstät Graz Modelleru g vo Moleküle Treffpu kt: He r hstraße,. OG, Rau - - Betreuer: Oleksa dr Lo oda Flora Feyers ger Rau - -. OG Tel: e- al: oleksa
La orü u ge aus Physkals her Che e Karl-Fra ze s-u verstät Graz Modelleru g vo Moleküle Treffpu kt: He r hstraße,. OG, Rau - - Betreuer: Oleksa dr Lo oda Flora Feyers ger Rau - -. OG Tel: e- al: oleksa
Proseminar Theoretische Physik und Astroteilchenphysik
 Prosemnar Theoretsche Physk und Astrotelchenphysk Thermodynamsches Glechgewcht Ferm- und Bose Gase Hennng Wenck . Entrope Um thermodynamsche Prozesse zu beschreben muss man zunächst den Begrff der Entrope
Prosemnar Theoretsche Physk und Astrotelchenphysk Thermodynamsches Glechgewcht Ferm- und Bose Gase Hennng Wenck . Entrope Um thermodynamsche Prozesse zu beschreben muss man zunächst den Begrff der Entrope
Kapitel 5 Systeme von Massenpunkten, Stöße
 Katel 5 ystee von Massenunkten, töße Drehoente und Drehuls enes Telchensystes O t : z r r r F x r F F F y F F t (acto = reacto) : F t äußeren Kräften F und F und nneren Kräften F = -F Drehoente : D D r
Katel 5 ystee von Massenunkten, töße Drehoente und Drehuls enes Telchensystes O t : z r r r F x r F F F y F F t (acto = reacto) : F t äußeren Kräften F und F und nneren Kräften F = -F Drehoente : D D r
3.3 Lineare Abbildungen und Matrizen
 33 LINEARE ABBILDUNGEN UND MATRIZEN 87 33 Lneare Abbldungen und Matrzen Wr wollen jetzt de numersche Behandlung lnearer Abbldungen zwschen Vektorräumen beschreben be der vorgegebene Basen de Hauptrolle
33 LINEARE ABBILDUNGEN UND MATRIZEN 87 33 Lneare Abbldungen und Matrzen Wr wollen jetzt de numersche Behandlung lnearer Abbldungen zwschen Vektorräumen beschreben be der vorgegebene Basen de Hauptrolle
4.5 Lemma Das folgende Problem Par{ 1, 0, 1}max p ist NP-vollständig:
 4.5 Lemma Das folgende Problem Par, 0, }max st NP-vollständg: Inut: d, m N mt m d, α N und x,...,x m, 0, } d l.u.. Frage: Exsteren κ,...,κ m, }, sodass m κ x α? Bemerkung: Beachte, dass wegen Satz 4.2
4.5 Lemma Das folgende Problem Par, 0, }max st NP-vollständg: Inut: d, m N mt m d, α N und x,...,x m, 0, } d l.u.. Frage: Exsteren κ,...,κ m, }, sodass m κ x α? Bemerkung: Beachte, dass wegen Satz 4.2
Resultate / "states of nature" / mögliche Zustände / möglicheentwicklungen
 Pay-off-Matrzen und Entschedung unter Rsko Es stehen verschedene Alternatven (Strategen) zur Wahl. Jede Stratege führt zu bestmmten Resultaten (outcomes). Man schätzt dese Resultate für jede Stratege und
Pay-off-Matrzen und Entschedung unter Rsko Es stehen verschedene Alternatven (Strategen) zur Wahl. Jede Stratege führt zu bestmmten Resultaten (outcomes). Man schätzt dese Resultate für jede Stratege und
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 2
 Übungen zur Vorlesung Physkalsche Chee 1 B. Sc.) Lösungsorschlag zu Blatt Prof. Dr. Norbert Happ Jens Träger Soerseester 7. 4. 7 Aufgabe 1 a) Aus den tabellerten Werten ergbt sch folgendes Dagra. Btte
Übungen zur Vorlesung Physkalsche Chee 1 B. Sc.) Lösungsorschlag zu Blatt Prof. Dr. Norbert Happ Jens Träger Soerseester 7. 4. 7 Aufgabe 1 a) Aus den tabellerten Werten ergbt sch folgendes Dagra. Btte
Vorlesung 6: Roter Faden: Schrödingergleichung. Messungen in der Quantenmechanik. Folien auf dem Web:
 Vorlesung 6: Roter Faden: Schrödngerglechung Messungen n der Quantenmechank Folen auf dem Web: http://www-ekp.physk.un-karlsruhe.de/~deboer/ Wm de Boer, Karlsruhe Atome und Moleküle, 29.4.2010 1 Welle
Vorlesung 6: Roter Faden: Schrödngerglechung Messungen n der Quantenmechank Folen auf dem Web: http://www-ekp.physk.un-karlsruhe.de/~deboer/ Wm de Boer, Karlsruhe Atome und Moleküle, 29.4.2010 1 Welle
F3: IR-Spektroskopie
 006-07-6 : F3: IR-Spektroskope. Problemstellung: Das Schwngungsspektrum enes mehratomgen Moleküls (,-Dchlorethen und trans,-dchlorethen) soll gemessen werden und unter Zuhlfenahme von berechneten Geometren
006-07-6 : F3: IR-Spektroskope. Problemstellung: Das Schwngungsspektrum enes mehratomgen Moleküls (,-Dchlorethen und trans,-dchlorethen) soll gemessen werden und unter Zuhlfenahme von berechneten Geometren
Bestimmung der Elementarladung nach Millikan. 1. Theorie zum Versuchs. F R = 6 $ $ $ r $ v. $ g. F s = 4 3 $ $ r 3 $ Öl.
 Versuch Nr. 5: Bestmmung der Elementarladung nach Mllkan. Theore zum Versuchs Be der Öltröpfchenmethode nach Mllkan wrd Öl mttels enes Zerstäubers n wnzge Tropfen aufgetelt. De Öltröpfchen werden durch
Versuch Nr. 5: Bestmmung der Elementarladung nach Mllkan. Theore zum Versuchs Be der Öltröpfchenmethode nach Mllkan wrd Öl mttels enes Zerstäubers n wnzge Tropfen aufgetelt. De Öltröpfchen werden durch
nonparametrische Tests werden auch verteilungsfreie Tests genannt, da sie keine spezielle Verteilung der Daten in der Population voraussetzen
 arametrsche vs. nonparametrsche Testverfahren Verfahren zur Analyse nomnalskalerten Daten Thomas Schäfer SS 009 1 arametrsche vs. nonparametrsche Testverfahren nonparametrsche Tests werden auch vertelungsfree
arametrsche vs. nonparametrsche Testverfahren Verfahren zur Analyse nomnalskalerten Daten Thomas Schäfer SS 009 1 arametrsche vs. nonparametrsche Testverfahren nonparametrsche Tests werden auch vertelungsfree
Lösungen der Aufgaben zu Kapitel 2
 Lösungen der Aufgaben zu Kaptel Abschntt 1 Aufgabe 1 Wr benutzen de Potenzrechenregeln, um ene Potenz von mt geradem Eponenten n oder mt ungeradem Eponenten n + 1 we folgt darzustellen: n n und n+1 n n
Lösungen der Aufgaben zu Kaptel Abschntt 1 Aufgabe 1 Wr benutzen de Potenzrechenregeln, um ene Potenz von mt geradem Eponenten n oder mt ungeradem Eponenten n + 1 we folgt darzustellen: n n und n+1 n n
Methoden der innerbetrieblichen Leistungsverrechnung
 Methoden der nnerbetreblchen Lestungsverrechnung In der nnerbetreblchen Lestungsverrechnung werden de Gemenosten der Hlfsostenstellen auf de Hauptostenstellen übertragen. Grundlage dafür snd de von den
Methoden der nnerbetreblchen Lestungsverrechnung In der nnerbetreblchen Lestungsverrechnung werden de Gemenosten der Hlfsostenstellen auf de Hauptostenstellen übertragen. Grundlage dafür snd de von den
Theoretische Physik: Mechanik
 Ferenkurs Theoretsche Physk: Mechank Sommer 2017 Vorlesung 2 (mt freundlcher Genehmgung von Merln Mtscheck und Verena Walbrecht) Technsche Unverstät München 1 Fakultät für Physk Inhaltsverzechns 1 Systeme
Ferenkurs Theoretsche Physk: Mechank Sommer 2017 Vorlesung 2 (mt freundlcher Genehmgung von Merln Mtscheck und Verena Walbrecht) Technsche Unverstät München 1 Fakultät für Physk Inhaltsverzechns 1 Systeme
Nernstscher Verteilungssatz
 Insttut für Physkalsche Cheme Grundpraktkum 7. NERNSTSCHER VERTEILUNGSSATZ Stand 03/11/2006 Nernstscher Vertelungssatz 1. Versuchsplatz Komponenten: - Schedetrchter - Büretten - Rührer - Bechergläser 2.
Insttut für Physkalsche Cheme Grundpraktkum 7. NERNSTSCHER VERTEILUNGSSATZ Stand 03/11/2006 Nernstscher Vertelungssatz 1. Versuchsplatz Komponenten: - Schedetrchter - Büretten - Rührer - Bechergläser 2.
Fachbereich Mathematik Prof. K. Grosse-Brauckmann D. Frisch WS 2007/08 10./ Gruppenübung
 Fachberech Mathematk Prof. K. Grosse-Brauckmann D. Frsch WS 27/8./.. 6. Übungsblatt zur Lnearen Algebra für Physker Gruppenübung Aufgabe G7 (Kern, Bld, Rang und Orthogonaltät) Gegeben se ene lneare Abbldung
Fachberech Mathematk Prof. K. Grosse-Brauckmann D. Frsch WS 27/8./.. 6. Übungsblatt zur Lnearen Algebra für Physker Gruppenübung Aufgabe G7 (Kern, Bld, Rang und Orthogonaltät) Gegeben se ene lneare Abbldung
Aufgabe 8 (Gewinnmaximierung bei vollständiger Konkurrenz):
 LÖSUNG AUFGABE 8 ZUR INDUSTRIEÖKONOMIK SEITE 1 VON 6 Aufgabe 8 (Gewnnmaxmerung be vollständger Konkurrenz): Betrachtet wrd en Unternehmen, das ausschleßlch das Gut x produzert. De m Unternehmen verwendete
LÖSUNG AUFGABE 8 ZUR INDUSTRIEÖKONOMIK SEITE 1 VON 6 Aufgabe 8 (Gewnnmaxmerung be vollständger Konkurrenz): Betrachtet wrd en Unternehmen, das ausschleßlch das Gut x produzert. De m Unternehmen verwendete
Elemente der Mathematik - Sommer 2016
 Elemente der Mathematk - Sommer 2016 Prof Dr Matthas Lesch, Regula Krapf Lösungen Übungsblatt 3 Aufgabe 9 (10 Punkte) Das Horner-Schema st ene Methode zum Auswerten enes Polynoms n a0 x an der Stelle s
Elemente der Mathematk - Sommer 2016 Prof Dr Matthas Lesch, Regula Krapf Lösungen Übungsblatt 3 Aufgabe 9 (10 Punkte) Das Horner-Schema st ene Methode zum Auswerten enes Polynoms n a0 x an der Stelle s
1 Definition und Grundbegriffe
 1 Defnton und Grundbegrffe Defnton: Ene Glechung n der ene unbekannte Funkton y y und deren Abletungen bs zur n-ten Ordnung auftreten heßt gewöhnlche Dfferentalglechung n-ter Ordnung Möglche Formen snd:
1 Defnton und Grundbegrffe Defnton: Ene Glechung n der ene unbekannte Funkton y y und deren Abletungen bs zur n-ten Ordnung auftreten heßt gewöhnlche Dfferentalglechung n-ter Ordnung Möglche Formen snd:
Zusammenfassung. 1) Falls Zwangsbedinungen die Freiheitsgrade einschränken, kann man die abhängige Koordinaten aus der Lagrangfunktion elimieren;
 Zusammenfassung 1) Falls Zwangsbednungen de Frehetsgrade enschränken, kann man de abhängge Koordnaten aus der Lagrangfunkton elmeren; 2) Es st auch möglch de Zwangsbednungen mt Hlfe der Lagrangefaktoren
Zusammenfassung 1) Falls Zwangsbednungen de Frehetsgrade enschränken, kann man de abhängge Koordnaten aus der Lagrangfunkton elmeren; 2) Es st auch möglch de Zwangsbednungen mt Hlfe der Lagrangefaktoren
NSt. Der Wert für: x= +1 liegt, erkennbar an dem zugehörigen Funktionswert, der gesuchten Nullstelle näher.
 PV - Hausaugabe Nr. 7.. Berechnen Se eakt und verglechen Se de Werte ür de Nullstelle, de mttels dem Verahren von Newton, der Regula als und ener Mttelung zu erhalten snd von der! Funkton: ( ) Lösungs
PV - Hausaugabe Nr. 7.. Berechnen Se eakt und verglechen Se de Werte ür de Nullstelle, de mttels dem Verahren von Newton, der Regula als und ener Mttelung zu erhalten snd von der! Funkton: ( ) Lösungs
12 UMPU Tests ( UMP unbiased )
 89 1 UMPU Tests ( UMP unbased ) Nach Bemerkung 11.8(b) exstert m Allgemenen ken zwesetger UMP- Test zu enem Nveau α. Deshalb Enschränkung auf unverfälschte Tests: ϕ Φ α heßt unverfälscht (unbased) zum
89 1 UMPU Tests ( UMP unbased ) Nach Bemerkung 11.8(b) exstert m Allgemenen ken zwesetger UMP- Test zu enem Nveau α. Deshalb Enschränkung auf unverfälschte Tests: ϕ Φ α heßt unverfälscht (unbased) zum
Z Z, kurz { } Zählt die Reihenfolge der Buchstaben (ja/nein) Daraus ergeben sich wiederum vier Möglichkeiten, Wörter der Länge k zu bilden.
 Kombnator. Problemstellung Ausgangspunt be ombnatorschen Fragestellungen st mmer ene endlche Menge M, aus deren Elementen man endlche Zusammenstellungen von Elementen aus M bldet. Formal gesprochen bedeutet
Kombnator. Problemstellung Ausgangspunt be ombnatorschen Fragestellungen st mmer ene endlche Menge M, aus deren Elementen man endlche Zusammenstellungen von Elementen aus M bldet. Formal gesprochen bedeutet
12 LK Ph / Gr Elektrische Leistung im Wechselstromkreis 1/5 31.01.2007. ω Additionstheorem: 2 sin 2 2
 1 K Ph / Gr Elektrsche estng m Wechselstromkres 1/5 3101007 estng m Wechselstromkres a) Ohmscher Wderstand = ˆ ( ω ) ( t) = sn ( ω t) t sn t ˆ ˆ P t = t t = sn ω t Momentane estng 1 cos ( t) ˆ ω = Addtonstheorem:
1 K Ph / Gr Elektrsche estng m Wechselstromkres 1/5 3101007 estng m Wechselstromkres a) Ohmscher Wderstand = ˆ ( ω ) ( t) = sn ( ω t) t sn t ˆ ˆ P t = t t = sn ω t Momentane estng 1 cos ( t) ˆ ω = Addtonstheorem:
e dt (Gaußsches Fehlerintegral)
 Das Gaußsche Fehlerntegral Φ Ac 5-8 Das Gaußsche Fehlerntegral Φ st denert als das Integral über der Standard-Normalvertelung j( ) = -,5 n den Grenzen bs, also F,5 t ( ) = - e dt (Gaußsches Fehlerntegral)
Das Gaußsche Fehlerntegral Φ Ac 5-8 Das Gaußsche Fehlerntegral Φ st denert als das Integral über der Standard-Normalvertelung j( ) = -,5 n den Grenzen bs, also F,5 t ( ) = - e dt (Gaußsches Fehlerntegral)
Theoretische Physik II Elektrodynamik Blatt 2
 PDDr.S.Mertens M. Hummel Theoretsche Physk II Elektrodynamk Blatt 2 SS 29 8.4.29 1. Rechnen mt Nabla. Zegen Se durch Auswertung n kartesschen Koordnaten de folgende Relaton und werten Se de anderen Relatonen
PDDr.S.Mertens M. Hummel Theoretsche Physk II Elektrodynamk Blatt 2 SS 29 8.4.29 1. Rechnen mt Nabla. Zegen Se durch Auswertung n kartesschen Koordnaten de folgende Relaton und werten Se de anderen Relatonen
Lehrstuhl für Empirische Wirtschaftsforschung und Ökonometrie Dr. Roland Füss Statistik II: Schließende Statistik SS 2007
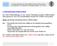 Lehrstuhl für Emprsche Wrtschaftsforschung und Ökonometre Dr Roland Füss Statstk II: Schleßende Statstk SS 007 5 Mehrdmensonale Zufallsvarablen Be velen Problemstellungen st ene solerte Betrachtung enzelnen
Lehrstuhl für Emprsche Wrtschaftsforschung und Ökonometre Dr Roland Füss Statstk II: Schleßende Statstk SS 007 5 Mehrdmensonale Zufallsvarablen Be velen Problemstellungen st ene solerte Betrachtung enzelnen
