Alkohole. Ableitung. R - H R - OH Funktionelle Gruppe: -OH. Einteilung. - einwertig. 1-Propanol. - zweiwertig. 1,2-Propandiol
|
|
|
- Lorenz Kuntz
- vor 8 Jahren
- Abrufe
Transkript
1 Alkohole (Alkanole)
2 Alkohole Ableitung R - H R - Funktionelle Gruppe: - Alkan Alkohol Hydroxyl-Gruppe Einteilung - einwertig Propanol - zweiwertig CH 1,2-Propandiol - dreiwertig CH 1,2,3-Propantriol (Glycerin) 2
3 Alkohole - primär 1-Propanol - sekundär CH 2-Propanol (Isopropylalkohol) - terciär C H 3 C 2-Methyl-2-propanol (terc.butylalkohol) 3
4 Nomenklatur der Alkohole IUPAC: Alkan + ol + Trivialnamen Alken + ol Alkin + ol CH CH H 3 C C sek. Butylalkohol 2-Butanol Isobutylalkohol 2-Methyl-1-propanol terc.butylalkohol 2-Methyl-2-propanol CH HC C 2-Propen-1-ol (Allylalkohol) 2-Propin-1-ol (Propargylalkohol) 4
5 Nomenklatur, Vorkommen Gruppen R- R-- -- C 2 H 5 -- Alkoxy-Gruppen Methoxy-Gruppe Ethoxy-Gruppe Vorkommen Methanol, Holzgeist, Ethanol, Weingeist, C 2 H 5 Glycerin Sorbit usw. in freier oder gebundener Form in der Natur 5
6 Physikalische Eigenschaften, Darstellung Aggregatzustand: Flüssigkeiten oder Feststoffe Siedepunkt: H-Bindungen hohe Siedepunkte Löslichkeit: niedere Vertreter (C 1 -C 3 ) sind mit wasser mischbar Dichte: kleiner, als die des Wassers δ δ+.. C n H 2n+1 R.. H Darstellung - R X R R C R' H 2 H + R C + R' R CH H 2 C H 3 CH 6
7 Darstellung R C Reduktion 4H R Katalysator: CuCr 2 4 R C R' LiAlH 4 R + R' Ethanol: durch alkoholische Gärung unter Wirkung des Enzyms Zymase aus landwirtschaftlichen Produkten (Stärke, zuckerhaltige Früchte, Traube, usw.) C 6 H C 2 H 5 + 2C 2 7
8 Chemische Eigenschaften 1. Säure-Basen-Eigenschaften H +.. R.. H Base δ δ+ Säure H + + H + äußerst schwache Säuren! C 2 H 5 i.pr t.bu pk a
9 Chemische Eigenschaften R NaNH 2 (NaH) R Na + (Na) Natriumalkoxid :H - :NH 2 - starke Basen H R + HBr R + H + Br (sehr starke Säuren, pk A 2 4) ~ 9
10 Chemische Eigenschaften 2. Bildung der Alkoxide, bzw. Ether Na Na Natriumethoxid I 3. Bildung der Ester Ethyl-methylether -H 2 R + R' C R C R' Ester (Anstelle R-C kann auch R-C-Cl eingesetzt werden!) 10
11 Chemische Eigenschaften 4. Dehydratation (Wasserabspaltung) β α R -H 2 R CH Alken 5. Bildung von Alkylhalogeniden R R X 11
12 Chemische Eigenschaften 6. xidation R xidation Cr 3 R CH Aldehyd KMn 4 R C Carbonsäure R R' CH Cr 3 R R' C Keton 12
13 Chemische Eigenschaften Einige wichtige Vertreter der Alkohole Methanol,, Sdp. 65 o C, Lösungsmittel, Ausgangsstoff, toxisch Ethanol, C 2 H 5, Sdp. 78,4 o C, Lösungsmittel, Ausgangsstoff, 95,6% Ethanol - 4,4% Wasser: azeotropes Gemisch, Sdp. 78,1 o C 1-Propanol, 2-Propanol, C 3 H 7 Butanol: C 4 H 9, 4 Konstitutionsisomere Amyl-alkohol: C 5 1-ctanol: C 8 H 17 Fettalkohole C 10 C 18 13
14 Zwei- und mehrwertige Alkohole Zweiwertige Alkohole: -Diol -Glykol R C R' H C C C C n C Geminale Diole (Glykole) geminale vicinale disjunkt Diole - hydratisierte Derivate der Aldehyde und Ketone, - existieren nur in wässrigen Lösungen R CH -H 2 R CH Aldehyd R C R' H -H 2 R C R' Keton 14
15 Vicinale Diole (Glykole) CH Ethylenglykol Sdp. 198 C 1,2-Propandiol Glycerin Pentaerythrit CH H C Sdp. 290 C Schmp C 15
16 Aromatische Hydroxyverbindungen Klassifizierung: Phenole Die Gruppe ist direkt mit dem aromatischen Ring verbunden. aromatische Alkohole Ein H-Atom in der Seitenkette ist durch die Gruppe ersetzt. (sp 3 -C- Bindung!) Verbindung von Phenol-Typ Toluol Verbindung von aromatischem Alkohol-Typ 16
17 Phenole Vorkommen: - Steinkohlenteer - Pflanzen (als Etherderivate) Na Herstellung: Ar-S 2 Na Ar-Na + Na 2 S C Ar-X Na H 2 Ar- + NaX Physikalische Eigenschaften: - hauptsächlich Feststoffe - hohe Siedepunkte - unangenehmer ( phenolartiger ) Geruch - geringe Löslichlichkeit in Wasser 17
18 Chemische Eigenschaften - schwach saure Eigenschaft :.. δ : - Na + δ δ + Na + H2 δ pk A = 9,95 Natriumphenoxid (Natriumphenolat) mesomeriestabilisiertes Phenoxid-Anion 2 N N 2 N 2 2,4,6-Trinitrophenol (Pikrinsäure) pk A = 0,95 starke Säure o-krezol pk A = 10,28 18
19 Chemische Eigenschaften - Electrophile Substitution: die Gruppe aktiviert die o- und p-ständige C-Atome im Benzolkern sehr stark (+ M Effekt) - Bromierung Br2/H2 Br Br - Nitrierung: mit verd.salpetersäure - Sulfonierung mit cc. H 2 S 4 Br 2,4,6-Tribromphenol + N 2 + S 2 N 2 p-nitrophenol o-nitrophenol S 2 19 p- und o-phenolsulfonsäure
20 Phenol Herstellung von Farbstoffen Synthese von Aspirin, Herbizide Nerven-/Zellgift Desinfektionsmittel Synthese von Kunstharzen Konservierung von Holz Hautaufhellung Peeling (Schälkur) - xidation empfindliche Verbindungen gegen xidationsmittel färben sich rötlich an der Luft -FeCl 3 (Fe 3+ -Ionen): charateristische Farbereaktion Phenol: violett Brenzcatechin: grün 20
21 Phenole Klassifizierung: nach der Anzahl der Gruppen Zweiwertige Phenole Brenzcatechin Resorcin Hydrochinon Ausgangsstoff Antiseptikum Reduktionsmittel, in der Pharmaindustrie Photographie Dreiwertige Phenole Pyrogallol Hydroxyhydrochinon Phloroglucin seine alkalische Nachweis von Lignin 21 Lösung absorbiert 2
22 Phenole CH Phenol o-kresol m-kresol p-kresol Thymol Desinfektionsmittel Naphthol 2-Naphthol α-naphthol ß-Naphthol α β Br Br Cl Br N 2 2,4,6-Tribromphenol 5-Chlor-2-nitro- phenol
23 Phenole H H Resveratrol Traubensaft: 1,10 mg/l antioxidative Rotwein: Eigenschaften mg/l Arteriosklerose, Herzkrankheiten, Arthritis, Autoimmunkrankheiten neuroprotektive Wirkung beim Glaukom, antikanzerogene wirkung Nahrungsergänzungsmittel H 5 C 2 C 2 H 5 Stilböstrol östrogene Wirkung Synthetische, nichtsteroidale, selektive Estrogen-Rezeptor-Modulatore (DES, 1938) Teratogen, Krebserregend Behandlung der Inkontinenz bei Hunden Wachstumsfaktor 23
24 Tannin 24
25 Phenole Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Pentachlorphenol fungizide Wirkung Hexachlorophen antiseptische Wirkung N 2 N 2 N 2 N 2 N 2 N 2 Pikrinsäure starke Säure pk A = 0,95 N 2 Trinitro-m-kresol Ammoniumsalz: Ekrasit N 2 Naphthalingelb (Martiusgelb) 25
26 Aromatische Alkohole β α CH CH Benzylalkohol Ester in ätherischen Ölen Jazminblütenöl β-phenylethanol Hauptbestandteil des Rosenöls Zimtalkohol hyazinthenartiger Geruch Chemische Eigenschaften: wie bei den aliphatischen Alkoholen 26
27 Phenolalkohol CH3 Salicylalkohol in Weidenarten CH CH Coniferylalkohol CH CH Sinapinalkohol Bausteine des Lignins Stoffe, die in die pflanzliche Zellwandeingelagert werden und dadurch die Verholzung der Zelle bewirken (Lignifizierung). Etwa 20 % bis 30 % der Trockenmasse verholzter Pflanzen bestehen aus Ligninen 27
28 28
29 Chinone oxid. red. 1,4-Benzochinon Hydrochinon ungesättigte, cyclische, aber nicht aromatische Verbindung oxid. red. 1,2-Benzochinon Brenzcatechin 29
30 Chemische Eigenschaften - starke xidationsmittel H N NH2 - Reaktionen der Carbonylgruppe und der C=C Doppelbindung (z.b. Br 2 -addition) ximbildung xidation N - oxidative Spaltung der C=C Bindung: Synthese der Maleinsäure CH-C CH-C 30
31 Chemische Eigenschaften - xidation von Hydrochinon oxid. red. - Komplexbildung mit Hydrochinon: Chinhydron Schmp C tiefgrüne, schillernde Kristalle Charge-transfer Komplex 31
32 Ubichinone H 3 C H 3 C ( -CH=CH- ) n -H Hilfssubstrat für den Wasserstoffaustausch und Elektronentransport in der Atmungskette in den Zellen des Pflanzen- und Tierreichs 32
33 Polycyclische Chinone 1,4-Naphthochinon Juglon Anthrachinon In Walnussschalen Antibakterielle, fungitoxische W. Blutungsstillend Allelopathie H Alizarin (Farbstoff) 33
34 Polycyclische Chinone CH C CH CH 2 Vitamin K 1 (Phyllochinon) (unentbehrlich für den Vorgang der Blutgerinnung) 34
35 Aliphatische Ether charakteristische Bindung C C Einteilung - einfache Ether - gemischte Ether Diethylether R R R R' CH Methylvinylether 35
36 Aliphatische Ether - offenkettige Ether Ethylmethylether - cyclische Ether H 2 C C H 2 Tetrahydrofuran Darstellung - aus Akoholen 2R cc. H 2 S 4 -H 2 R R einfache Ether - Williamson-Synthese R Na + R' I R R' (+ NaI) R' X (+ NaX) gemischte Ether 36
37 Physikalische Eigenschaften - Siedepunkt: rel. niedrig, z.b. Diethylether Sdp. 34,6 o C - Löslichkeit: in Wasser gering - leichtbewegliche flüchtige Flüssigkeiten, von großer Brennbarkeit Chemische Eigenschaften: - stabile, wenig polare Moleküle, geringe Reaktivität Nu: C δ+ δ R resistent gegen nucleophile Reagenzien; R - schwache Abgangsgruppe! 37
38 Säure-Basen-Eigenschaften Alkohol.. R.. H Acidität Ether.. R.. R Basicität Bildung von xoniumsalzen - mit cc. Schwefelsäure + C 2 H 5 C 2 H H 2 S 4 H HS 4 _ Diethyloxonium-hydrogensulfat C 2 H 5 C 2 H 5 - mit cc. Salzsäure R R.... H + Cl rel. labiles Addukt 38
39 Säure-Basen-Eigenschaften Lewissche Säure-Basen-Komplexe C 2 H 5 C 2 H BF 3 stabiler destillierbarer Komplex Sdp. 126 C 39
40 Ether Diethylether - Lösungsmittel, Sdp. 34,6 o C - Bildung von Peroxiden: bei längerem Aufbewahren an der Luft und im Licht H C Hydroperoxid-diethylether * CH * n polymeres Ethylidenperoxid explosionsfähige Substanz!! Nachweis: KI H + I 2 Entfernung: FeS 4 ox. Fe 2 (S 4 ) 3 40
41 Cyclische Ether C C Epoxy-Ring Ethylenoxid Sdp. 11,7 C H H H 2 C C H 2 Sdp. 101,4 C Schmp C Dioxan 41
42 Synthesen aus Ethylenoxid Ethylenglykol H 2 HCl Cl - -HCl R RNH 2 R Halbether von Ethylenglykol HX NH R 1,2-Aminoalkohol X Halogenhydrin 42
43 Synthesen aus Ethylenoxid Cellosolve = Halbether von Ethylenglykol Methylcellosolv Ethylenoxid C 2 H 5 Ethylcellosolv C 2 H 5 43
44 Macrocyclische Polyether (Kronenether) - macrocyclische Struktur (z.b. 18-Ringe) - variierbare Ringgröße - ungewöhnliche komplexbildende Eigenschaft - große Giftigkeit [18]-Krone-6 oder [18]- 6 44
45 Phenolether Flüssigkeiten mit angenehmem Geruch (Bestandteile von pflanzlichen Ölen und Aromastoffen) Anisol Guaiacol Veratrol CH CH CH CH Anethol Eugenol Nerolin 45
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Physikalische Eigenschaften der Alkohole
 Physikalische Eigenschaften der Alkohole Die Struktur von Alkoholen ist ähnlich der von Wasser 96pm 110pm 143pm 96pm Methanol 109 104.5 108.9 I_folie228 Wasserstoffbrückenbindungen: BDE = 21KJ/mol 207pm
Physikalische Eigenschaften der Alkohole Die Struktur von Alkoholen ist ähnlich der von Wasser 96pm 110pm 143pm 96pm Methanol 109 104.5 108.9 I_folie228 Wasserstoffbrückenbindungen: BDE = 21KJ/mol 207pm
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen
 KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
Organische Chemie Bausatz mit 109 Atomen Best.- Nr. MT00206
 Organische Chemie Bausatz mit 109 Atomen Best.- Nr. MT00206 1. Beschreibung Der Bausatz gestattet die Darstellung von Basismolekülen der modernen Chemie sowohl in einer Kompaktform als auch in einer Form,
Organische Chemie Bausatz mit 109 Atomen Best.- Nr. MT00206 1. Beschreibung Der Bausatz gestattet die Darstellung von Basismolekülen der modernen Chemie sowohl in einer Kompaktform als auch in einer Form,
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
4. Schwefelhaltige Verbindungen
 Ri 206 4. chwefelhaltige Verbindungen Äbersicht toffklasse Formel Z toffklasse Formel Z Thiole ulfide Disulfide ulfoxide ulfone R H -II ulfonsäuren H ulfonylhalogenide X R R -II R R ulfonsäureester -I
Ri 206 4. chwefelhaltige Verbindungen Äbersicht toffklasse Formel Z toffklasse Formel Z Thiole ulfide Disulfide ulfoxide ulfone R H -II ulfonsäuren H ulfonylhalogenide X R R -II R R ulfonsäureester -I
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
Übersicht, Nomenklatur Bisher hauptsächlich Kohlenwasserstoffe, jetzt immer mehr funktionalsierte Verbindungen:
 132 Alkohole und Phenole Übersicht, Nomenklatur Bisher hauptsächlich Kohlenwasserstoffe, jetzt immer mehr funktionalsierte Verbindungen: ydroxylgruppe, aber - Nomenklatur C Methan C Methanol oder ydroxymethan
132 Alkohole und Phenole Übersicht, Nomenklatur Bisher hauptsächlich Kohlenwasserstoffe, jetzt immer mehr funktionalsierte Verbindungen: ydroxylgruppe, aber - Nomenklatur C Methan C Methanol oder ydroxymethan
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Hydrierung von Kohlenmonoxid zu Methanol Kataly?sche Umsetzung von Ethen mit Wasser zu Ethanol
 Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Beispiele zur Multiple-Choice Prüfung in OC
 1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
Halogenalkane. Radikalische Halogenierung von Alkanen. Addition von Halogenwasserstoffen an Alkene. H 3 C + HBr H C C C H.
 alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
Abituraufgaben Alkohole 1978/IV 1982/II/1 1984/II/1 1984/III/1 1984/IV/4.3
 Abituraufgaben Alkohole 1978/IV 1.1 Erstellen Sie die Formel des einfachsten dreiwertigen Alkanols (Triol), das zugleich primärer, sekundärer und tertiärer Alkohol ist. Benennen Sie die Verbindung eindeutig.
Abituraufgaben Alkohole 1978/IV 1.1 Erstellen Sie die Formel des einfachsten dreiwertigen Alkanols (Triol), das zugleich primärer, sekundärer und tertiärer Alkohol ist. Benennen Sie die Verbindung eindeutig.
Phenole sind aromatische Verbindungen, bei denen mindestens eine OH-Gruppe direkt mit dem Stammsystem verbunden. 2-Methylphenol o-kresol
 Ri 97 2.2. Phenole Phenole sind aromatische Verbindungen, bei denen mindestens eine -Gruppe direkt mit dem Stammsystem verbunden ist. Nomenklatur Die wichtigsten Phenole tragen weit verbreitete Trivialnamen.
Ri 97 2.2. Phenole Phenole sind aromatische Verbindungen, bei denen mindestens eine -Gruppe direkt mit dem Stammsystem verbunden ist. Nomenklatur Die wichtigsten Phenole tragen weit verbreitete Trivialnamen.
Hydroxylderivate. Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit. Bruch der C-H- und der C-OBindungen. Prof. Dr. Ivo C.
 Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
2. Sauerstoffhaltige Verbindungen
 Ri 81 2. Sauerstoffhaltige Verbindungen In einem organischen MolekÄl besitzen im Allgemeinen die verschiedenartig gebundenen C- Atome verschiedene xidationszahlen. Die xidationszahl eines C-Atoms wird
Ri 81 2. Sauerstoffhaltige Verbindungen In einem organischen MolekÄl besitzen im Allgemeinen die verschiedenartig gebundenen C- Atome verschiedene xidationszahlen. Die xidationszahl eines C-Atoms wird
VO-5. Organische Chemie 2. Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria.
 VO-5 Organische Chemie 2 Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria. wolfgang.schoefberger@jku.at 89 Mesomerer Effekt verringert die
VO-5 Organische Chemie 2 Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria. wolfgang.schoefberger@jku.at 89 Mesomerer Effekt verringert die
ORGANISCHE CHEMIE TEIL 2 ORGANISCHE SAUERSTOFFVERBINDUNGEN FMS
 KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN FMS Skript rganische Chemie 2 (FMS) V1.0 10/13 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole...
KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN FMS Skript rganische Chemie 2 (FMS) V1.0 10/13 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole...
9. Alkohole, Ether und Phenole
 Inhalt Index 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und Darstellung und 2) Alkohole und Phenole als Säuren und Basen.
Inhalt Index 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und Darstellung und 2) Alkohole und Phenole als Säuren und Basen.
Ether sind kettenfärmige Verbindungen vom Typ R-O-R' oder Heterocyclen mit mindestens einem O-Atom im Ring.
 Ri 104 2.3. Ether Ether sind kettenfärmige Verbindungen vom Typ R--R' oder Heterocyclen mit mindestens einem -Atom im Ring. Sie kännen formal auch als Disubstitutionsprodukte von Wasser betrachtet werden.
Ri 104 2.3. Ether Ether sind kettenfärmige Verbindungen vom Typ R--R' oder Heterocyclen mit mindestens einem -Atom im Ring. Sie kännen formal auch als Disubstitutionsprodukte von Wasser betrachtet werden.
Organische Chemie I Chemie am 16.11.2012. Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2
 Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
O H H 3 C. Methanol. Molekulargewicht Siedepunkt Löslichkeit in Wasser H 3 C-OH. unbegrenzt H 3 C-Cl. 7.4 g/l H 3 C-CH 3 -24/C -88/C
 Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
1. Derivatisierung und anschließende Schmelzpunktbestimmung. Umsetzung von Alkoholen mit Säurechloriden unter Basenkatalyse.
 Alkohole 1. Derivatisierung und anschließende Schmelzpunktbestimmung Veresterung nach Schotten-Baumann bzw. Einhorn (Pyridin) Umsetzung von Alkoholen mit Säurechloriden unter Basenkatalyse. R 2-OH Carbamate
Alkohole 1. Derivatisierung und anschließende Schmelzpunktbestimmung Veresterung nach Schotten-Baumann bzw. Einhorn (Pyridin) Umsetzung von Alkoholen mit Säurechloriden unter Basenkatalyse. R 2-OH Carbamate
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Organische Moleküle. Verschiedene Ansichten des Methans
 Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
9. Alkohole. Alkohole können als Derivate des Wassers betrachtet werden, bei denen ein Wasserstoff durch einen Alkylrest ausgetauscht wurde:
 9. Alkohole Als ALKOHOLE (Alkanole) bezeichnet man organische Verbindungen, die mindestens eine Hydroxygruppe (-OH) (als Gruppe höchster Priorität) besitzen. Bei den Resten R handelt es sich um ALKYLGRUPPEN!
9. Alkohole Als ALKOHOLE (Alkanole) bezeichnet man organische Verbindungen, die mindestens eine Hydroxygruppe (-OH) (als Gruppe höchster Priorität) besitzen. Bei den Resten R handelt es sich um ALKYLGRUPPEN!
Organische Chemie I. OC I Lehramt F. H. Schacher 1
 Organische Chemie I OC I Lehramt F. H. Schacher 1 8. Ether 8.1. Allgemeines 8.2. Nomenklatur + wichtige Vertreter 8.3. Synthesen 8.4. Reaktionen 8.5. Kronenether 8.6. Ether als Schutzgruppen 8.7. Ether
Organische Chemie I OC I Lehramt F. H. Schacher 1 8. Ether 8.1. Allgemeines 8.2. Nomenklatur + wichtige Vertreter 8.3. Synthesen 8.4. Reaktionen 8.5. Kronenether 8.6. Ether als Schutzgruppen 8.7. Ether
Zur Benennung organischer Moleküle
 Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Ketone gehären zu den Carbonylverbindungen. Sie tragen als funktionelle Gruppe eine nicht endståndige Carbonylgruppe. R 1 R 2
 rganische Chemie Ri 12 2.5. Ketone Ketone gehären zu den Carbonylverbindungen. Sie tragen als funktionelle Gruppe eine nicht endståndige Carbonylgruppe. R 1 C R 2 R 1 C R 2 R 1 C R 2 Strukturformel Elektronenstrichformel
rganische Chemie Ri 12 2.5. Ketone Ketone gehären zu den Carbonylverbindungen. Sie tragen als funktionelle Gruppe eine nicht endståndige Carbonylgruppe. R 1 C R 2 R 1 C R 2 R 1 C R 2 Strukturformel Elektronenstrichformel
P1 Säuren und Laugen aus Erde, Feuer, Luft und Wasser (ca. 25 Stunden)
 SLZB Fachbereich Naturwissenschaften Schulinternes Curriculum für das Fach Chemie Klasse 9 P1 Säuren und Laugen aus Erde, Feuer, Luft und Wasser (ca. 25 ) Sicherheitsbelehrung Wdh. PSE Atombau Säuren und
SLZB Fachbereich Naturwissenschaften Schulinternes Curriculum für das Fach Chemie Klasse 9 P1 Säuren und Laugen aus Erde, Feuer, Luft und Wasser (ca. 25 ) Sicherheitsbelehrung Wdh. PSE Atombau Säuren und
Erftgymnasium der Stadt Bergheim. Schulinternes Curriculum für das Fach Chemie in der Sekundarstufe II
 Erftgymnasium der Stadt Bergheim Schulinternes Curriculum für das Fach Chemie in der Sekundarstufe II Als Fortführung des Unterrichts in der Sekundarstufe I wird Schülerinnen und Schülern ein anwendungs-
Erftgymnasium der Stadt Bergheim Schulinternes Curriculum für das Fach Chemie in der Sekundarstufe II Als Fortführung des Unterrichts in der Sekundarstufe I wird Schülerinnen und Schülern ein anwendungs-
IR-Spektroskopie organischer Moleküle
 Die Infrarot-Spektroskopie dient in der Organischen Chemie der Ermittlung von Strukturelementen, funktionellen Gruppen und ggf. von Isomeren und Konformeren. Ein Schwingungsspektrum eines organischen Moleküls
Die Infrarot-Spektroskopie dient in der Organischen Chemie der Ermittlung von Strukturelementen, funktionellen Gruppen und ggf. von Isomeren und Konformeren. Ein Schwingungsspektrum eines organischen Moleküls
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2015
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2015 Nachtrag Aromatische Substitution Sicherheitsbelehrung: Regeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2015 Nachtrag Aromatische Substitution Sicherheitsbelehrung: Regeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse September
Bereich der 1 H-chemischen Verschiebung (Abb. nach: Friebolin)
 Bereich der 1 -chemischen Verschiebung (Abb. nach: Friebolin) 1 -NM-Spektroskopie 1 Der esonanzbereich der Protonen in organischen Molekülen ist ca. 10 ppm breit. Nur saure Protonen (z.b. COO oder SO 3
Bereich der 1 -chemischen Verschiebung (Abb. nach: Friebolin) 1 -NM-Spektroskopie 1 Der esonanzbereich der Protonen in organischen Molekülen ist ca. 10 ppm breit. Nur saure Protonen (z.b. COO oder SO 3
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1)
CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1)
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Hegel-Gymnasium Stuttgart-Vaihingen. Klasse 8
 24.September 2011 Hegel-Gymnasium Stuttgart-Vaihingen Curriculum Chemie Klasse 8 bis 10 Klasse 8 Kern- und Teilkompetenzen Kerncurriculum / Bildungsstandards / Teil der zentralen Jahrgangsarbeiten (ca.
24.September 2011 Hegel-Gymnasium Stuttgart-Vaihingen Curriculum Chemie Klasse 8 bis 10 Klasse 8 Kern- und Teilkompetenzen Kerncurriculum / Bildungsstandards / Teil der zentralen Jahrgangsarbeiten (ca.
P9 Kunststoffe Moleküle ohne Ende
 SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
Grundwissen Chemie. 8. Jahrgangsstufe, Gruppe I
 Grundwissen Chemie 8. Jahrgangsstufe, Gruppe I Stoffe, Experimente - Stoffe und Stoffgemische unterscheiden Stoffeigenschaften, Reinstoffe, Gemische, Trennverfahren - Teilchenmodell: Atome und Moleküle
Grundwissen Chemie 8. Jahrgangsstufe, Gruppe I Stoffe, Experimente - Stoffe und Stoffgemische unterscheiden Stoffeigenschaften, Reinstoffe, Gemische, Trennverfahren - Teilchenmodell: Atome und Moleküle
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
Katalysatoren - Chemische Partnervermittlung im virtuellen Labor
 Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
R O R, R O Ar, Ar O Ar
 omenklatur Ether: C 3 C 2 C 2 C 3 Diethylether "Ether" R R, R Ar, Ar Ar Diphenylether C 3 C 3 C C 3 C 3 tert.-butylmethylether (MTBE) Folie256 Bezeichnung der R als Alkoxy-Gruppe C 3 C 2 C 2 p-ethoxybenzoesäure
omenklatur Ether: C 3 C 2 C 2 C 3 Diethylether "Ether" R R, R Ar, Ar Ar Diphenylether C 3 C 3 C C 3 C 3 tert.-butylmethylether (MTBE) Folie256 Bezeichnung der R als Alkoxy-Gruppe C 3 C 2 C 2 p-ethoxybenzoesäure
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Homologe Reihe der unverzweigten primären Alkohole C n H
 8.01 omologe eihe der unverzweigten primären Alkohole C n (2n+2) systematischer Name Konstitution iedepunkt chmelzpunkt Methanol 65 98 Ethanol 78 117 1-Propanol 97 126 1-Butanol ( ) 2 118 89 1-Pentanol
8.01 omologe eihe der unverzweigten primären Alkohole C n (2n+2) systematischer Name Konstitution iedepunkt chmelzpunkt Methanol 65 98 Ethanol 78 117 1-Propanol 97 126 1-Butanol ( ) 2 118 89 1-Pentanol
Chemische Reaktionen ergeben neue Stoffe mit neuen Eigenschaften
 1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
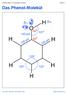 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
9. Alkohole, Ether und Phenole
 Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 9. Alkohole, Ether und Phenole Bis jetzt haben wir fast bei jedem Kapitel eine neue funktionelle Gruppe und auch eine wichtige neue
Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 9. Alkohole, Ether und Phenole Bis jetzt haben wir fast bei jedem Kapitel eine neue funktionelle Gruppe und auch eine wichtige neue
CHE 172.1: Organische Chemie für die Life Sciences
 1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
Nomenklatur. 2. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen. 3,3,4,4-Tetramethylheptan
 Nomenklatur Alkane. Ermittle die längte Kohlenstoffkette Stammname 8 8 8 -Methyloctan -Ethyloctan -Propyloctan. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen
Nomenklatur Alkane. Ermittle die längte Kohlenstoffkette Stammname 8 8 8 -Methyloctan -Ethyloctan -Propyloctan. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen
Estersynthese. Weiterbildung für fachfremd unterrichtende Lehrkräfte
 Estersynthese Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchenversuch
Estersynthese Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchenversuch
Redoxreaktionen. Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden
 Nach Lavoisier: : Redoxreaktionen Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden Aufnahme von Sauerstoff zb.: Verbrennen von Magnesium : Abgabe von Sauerstoff
Nach Lavoisier: : Redoxreaktionen Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden Aufnahme von Sauerstoff zb.: Verbrennen von Magnesium : Abgabe von Sauerstoff
Inhaltsverzeichnis. 3 Gesättigte Kohlenwasserstoffe (Alkane) 3.1 Offenkettige Alkane 3.2 Cyclische Alkane
 Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Carbonyl- und Enolatchemie
 Carbonyl- und Enolatchemie 1 Addition von rganometall-eagenzien an Carbonylverbindungen eformatzky-eaktion: Zn-eagenz weniger reaktiv als Grignard, greift keine Ester an! Br 2 Zn ZnBr 2 Br Zn 2 1 2 Barbier-eaktion:
Carbonyl- und Enolatchemie 1 Addition von rganometall-eagenzien an Carbonylverbindungen eformatzky-eaktion: Zn-eagenz weniger reaktiv als Grignard, greift keine Ester an! Br 2 Zn ZnBr 2 Br Zn 2 1 2 Barbier-eaktion:
Aldehyde und Ketone Carbonylverbindungen
 Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
FARBREAKTIONEN. 1. Farbgebende Strukturen 2. Gruppenreaktionen 3. Weitere Nachweisreaktionen
 FABEAKTIE 1. Farbgebende trukturen 2. Gruppenreaktionen 3. Weitere achweisreaktionen 1 1. Farbgebende trukturen adikale achweis f. Phenothiazine (Licht, 2 ) ' ' e e. ' tiefrot '. '. Disproportionierung
FABEAKTIE 1. Farbgebende trukturen 2. Gruppenreaktionen 3. Weitere achweisreaktionen 1 1. Farbgebende trukturen adikale achweis f. Phenothiazine (Licht, 2 ) ' ' e e. ' tiefrot '. '. Disproportionierung
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Produkte der POLYGON CHEMIE AG. Inkrustationsinhibitoren + Dispergatoren
 HYDRODIS ADW 3814/N Threshold-aktives, nicht Ca-sensibles Sequestrier- und Dispergiermittel mit ausgeprägtem Schmutztragevermögen. Zeichnet sich aus durch die sehr gute Kombination von Sequestrier- und
HYDRODIS ADW 3814/N Threshold-aktives, nicht Ca-sensibles Sequestrier- und Dispergiermittel mit ausgeprägtem Schmutztragevermögen. Zeichnet sich aus durch die sehr gute Kombination von Sequestrier- und
9. Alkohole. Alkohole können als Derivate des Wassers betrachtet werden, bei denen ein Wasserstoff durch einen Alkylrest ausgetauscht wurde: IOMC
 9. Alkohole Als ALKOHOLE (Alkanole) bezeichnet man organische Verbindungen, die mindestens eine Hydroxygruppe (-OH) (als Gruppe höchster Priorität) besitzen. Bei den Resten R handelt es sich um ALKYLGRUPPEN!
9. Alkohole Als ALKOHOLE (Alkanole) bezeichnet man organische Verbindungen, die mindestens eine Hydroxygruppe (-OH) (als Gruppe höchster Priorität) besitzen. Bei den Resten R handelt es sich um ALKYLGRUPPEN!
Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015
 Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015 Name: Vorname: Matrikel-Nr.: geborenam: in: Wiederholer dieser Klausur:
Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015 Name: Vorname: Matrikel-Nr.: geborenam: in: Wiederholer dieser Klausur:
Referat: Katalytische Hydrierungen
 Referat: Katalytische Hydrierungen Inhalt 1.1 Allgemein über Hydrierungen (Anlagerung von Wasserstoff) Seite 3 Die chemische Reaktion, katalytische Hydrierung 1.2 Die Beeinflussung der Hydrierdauer Seite
Referat: Katalytische Hydrierungen Inhalt 1.1 Allgemein über Hydrierungen (Anlagerung von Wasserstoff) Seite 3 Die chemische Reaktion, katalytische Hydrierung 1.2 Die Beeinflussung der Hydrierdauer Seite
Einführung. KLASSE: 9TE NAME: Vorname: Datum: LTAM Naturwissenschaften 9e Chemische Gleichungen 1 -
 Einführung Ein Gärtner bestellt beim Großhändler Blumen. Dort werden Tulpen in Dreier-Sträußen und Vergissmeinnichtchen in Zweier-Sträußen angeboten. Für Valentinstag, möchte der Gärtner ein Sonderangebot
Einführung Ein Gärtner bestellt beim Großhändler Blumen. Dort werden Tulpen in Dreier-Sträußen und Vergissmeinnichtchen in Zweier-Sträußen angeboten. Für Valentinstag, möchte der Gärtner ein Sonderangebot
chulportfolio 3. Schulkonzept 3.7 Kern- und Schulcurricula G9 (Klasse 5 11) Chemie Chemie Klasse 11
 Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
b) Synthese - der Nucleoside nach Vorbrüggen (am Beispiel eines RNA-Bausteins)
 b) Synthese - der ucleoside nach Vorbrüggen (am Beispiel eines RA-Bausteins) Ac TMSTf Me 3 Si - Tf Ac Ac Ac Ac achbargruppeneffekt Ac - Tf TMS TMSCl TMS- freies Elektronenpaar am Stickstoffatom jetzt nucleophil
b) Synthese - der ucleoside nach Vorbrüggen (am Beispiel eines RA-Bausteins) Ac TMSTf Me 3 Si - Tf Ac Ac Ac Ac achbargruppeneffekt Ac - Tf TMS TMSCl TMS- freies Elektronenpaar am Stickstoffatom jetzt nucleophil
Datum: Name: Klasse: Kenntnis der wichtigsten physikalischen und chemischen Eigenschaften der Stoffklassen der Alkohole und Phenole.
 Alkohole 1. Theorie Unter einem Alkohol versteht man einen Kohlenwasserstoff, welcher mindestens eine ydroxyl- Gruppe trägt. Alkohole können also durch die Formel R- symbolisiert werden. Dabei bedeutet
Alkohole 1. Theorie Unter einem Alkohol versteht man einen Kohlenwasserstoff, welcher mindestens eine ydroxyl- Gruppe trägt. Alkohole können also durch die Formel R- symbolisiert werden. Dabei bedeutet
Wird vom Korrektor ausgefüllt: Aufgabe 1 2 3 4 5 6 7 8 9 10 11 12 Punkte
 Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Organische Chemie. 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8. Lehrstuhl für Organische Chemie
 Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Aufgabe S. 2/a (2 Punkte) Wodurch können Sie 2-Hexen von 2-Methylpentan unterscheiden?
 16-2 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
16-2 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
Moderne Aldol-Reaktionen
 Moderne Aldol-Reaktionen Katrina Brendle Institut für Organische Chemie Seminar zum Fortgeschrittenenpraktium KIT Universität des Landes Baden-Württemberg und nationales Großforschungszentrum in der Helmholtz-Gemeinschaft
Moderne Aldol-Reaktionen Katrina Brendle Institut für Organische Chemie Seminar zum Fortgeschrittenenpraktium KIT Universität des Landes Baden-Württemberg und nationales Großforschungszentrum in der Helmholtz-Gemeinschaft
Emulgatoren. Definition Aufbau Einsatz Vertiefung I-5 I-5
 I-5 I-5 Emulgatoren sind Substanzen, mit denen sich die Grenzflächenspannung zwischen zwei nicht mischbaren Phasen (Flüssigkeiten, Gase) verringern lässt. Die nicht mischbaren Flüssigkeiten, z.b. Fett
I-5 I-5 Emulgatoren sind Substanzen, mit denen sich die Grenzflächenspannung zwischen zwei nicht mischbaren Phasen (Flüssigkeiten, Gase) verringern lässt. Die nicht mischbaren Flüssigkeiten, z.b. Fett
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Dünnschichtchromatographie. - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie
 Dünnschichtchromatographie - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie Dünnschichtchromatographie (DC) Trennmethode mit vielen Vorteilen gegenüber klassischen Verfahren (Destillation,
Dünnschichtchromatographie - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie Dünnschichtchromatographie (DC) Trennmethode mit vielen Vorteilen gegenüber klassischen Verfahren (Destillation,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer. Brennstoffe. Wir Unterscheiden grundsätzlich Brennstoffe in:
 Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Kennsilbe. -an. -en -in. -yl. -ol. -al (VI) -on. (VII) -säure (VIII)
 Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Homologe Reihe der Alkane. Benennung der Alkane. Konstitutionsisomerie. Isomerie. Was versteht man unter der Homologen Reihe der Alkane?
 Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
Chemie. Grundkurs. Beispielaufgabe A 4. Auswahlverfahren: Hessisches Kultusministerium. Landesabitur 2007 Beispielaufgaben
 Hessisches Kultusministerium Landesabitur 2007 Beispielaufgaben Chemie Grundkurs Beispielaufgabe A 4 Auswahlverfahren: Von vier Teilaufgaben (A1 A4) müssen drei Teilaufgaben bearbeitet werden. Einlese-
Hessisches Kultusministerium Landesabitur 2007 Beispielaufgaben Chemie Grundkurs Beispielaufgabe A 4 Auswahlverfahren: Von vier Teilaufgaben (A1 A4) müssen drei Teilaufgaben bearbeitet werden. Einlese-
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Organisch-Chemisches Grundpraktikum. trans-1,2-cyclohexandiol
 rganischhemisches Grundpraktikum Präparat 06: trans1,2yclohexandiol Gliederung: I. Literatur... 1 II. Präparateigenschaften... 1 III. Stöchiometrische Reaktionsgleichung... 1 IV. Reaktionsmechanismus...
rganischhemisches Grundpraktikum Präparat 06: trans1,2yclohexandiol Gliederung: I. Literatur... 1 II. Präparateigenschaften... 1 III. Stöchiometrische Reaktionsgleichung... 1 IV. Reaktionsmechanismus...
Chemische Reaktionen
 Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
Als Grundlage für die Revision wird die Monographie gemäß HELV. mit folgendem Änderungsvorschlag herangezogen:
 !!! NEE ÖAB-MONOGAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
!!! NEE ÖAB-MONOGAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
ORGANISCHE CHEMIE TEIL 2 ORGANISCHE SAUERSTOFFVERBINDUNGEN
 KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN Skript rganische Chemie 2 (GF) V2.0 02/14 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole... 02 1.1
KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN Skript rganische Chemie 2 (GF) V2.0 02/14 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole... 02 1.1
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution
 14.01 Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution Substitutenten Geschwindigkeit (Reaktivität) Richtung (Regioselektivität) Interpretation 1. 2,,
14.01 Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution Substitutenten Geschwindigkeit (Reaktivität) Richtung (Regioselektivität) Interpretation 1. 2,,
Klausur - Lösungsbogen
 Prof. Dr. J. Daub Februar 2005 Klausur - Lösungsbogen zur Vorlesung "rganische Chemie II (Reaktionen, Reaktionsmechanismen) für Studierende der Chemie und der Biochemie 3. Semester" WS 2004/2005 14. Februar
Prof. Dr. J. Daub Februar 2005 Klausur - Lösungsbogen zur Vorlesung "rganische Chemie II (Reaktionen, Reaktionsmechanismen) für Studierende der Chemie und der Biochemie 3. Semester" WS 2004/2005 14. Februar
Lernaufgabe: Richtigstellen von Reaktionsgleichungen
 Lernaufgabe: Richtigstellen von Reaktionsgleichungen Hilfreiche Angaben: Unterrichtsfach: Chemie Schultyp: Maturitätsschulen Jahrgangsstufe, Kurs: Grundlagenfach Bearbeitungsdauer: 20 Minuten Bearbeitung,
Lernaufgabe: Richtigstellen von Reaktionsgleichungen Hilfreiche Angaben: Unterrichtsfach: Chemie Schultyp: Maturitätsschulen Jahrgangsstufe, Kurs: Grundlagenfach Bearbeitungsdauer: 20 Minuten Bearbeitung,
SUPERABSORBER. Eine Präsentation von Johannes Schlüter und Thomas Luckert
 SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
