Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil X. Peter Schmieder AG NMR
|
|
|
- Til Schneider
- vor 6 Jahren
- Abrufe
Transkript
1 Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil X
2 Das Programm 2/03 Beim letztes Mal Das dynamic range Problem Proteine SQC 3D- und 4D-NMR 5 N-editierte Spektren Kopplungskonstanten mit dem SQC Screening mit NMR
3 Das Programm 3/03 eute 3 C, 5 N-Tripelresonanzspektren Sequenzspezifische Zuordnung in Proteinen (3) Deuterierung von Proteinen TROSY Strukturbestimmung von Proteinen
4 4/03 Tripelresonanztechniken
5 5/03 Wir haben gesehen, dass die homonuklearen Spektren NOESY und TOCSY mit ilfe der heteronuklearen Techniken auf 3D-Spektren erweitert werden können um die Überlagerung zu reduzieren. Die Strategie der sequentiellen Zuordnung hat sich dadurch aber nicht grundlegend geändert. Es werden weiter NOESY und TOCSY verwendet, die bessere Auflösung in den 3D-Spektren ermöglicht die Zuordnung größerer Proteine.
6 6/03 Wenn aber das TOCSY bzw. ein Transfer via Protonen- Kopplungen nicht mehr funktioniert oder sehr ineffizient wird, wie das bei größeren Proteinen der Fall ist, dann versagt die Strategie. Die sequentielle und Seitenkettenzuordnung muss dann mit Techniken bewerkstelligt werden, die nicht mehr auf Protonen-Kopplungen basieren sondern auf den Kopplungen zwischen den eterokernen.
7 7/03 eteronukleare 3D-NOESY-Spektren werden nur noch für das Bestimmen von Abständen im Molekül verwendet. Der Transfer von Magnetisierung über heteronukelare Kopplungen ist auch bei größeren Proteinen noch effektiv. Man verwendet dabei Protein die sowohl an 5 N als auch an 3 C markiert sind und die Kopplungen zwischen diesen Kernen. Da nun, 3 C und 5 N verwendet werden spricht man von Tripelresonanztechniken
8 8/03 J-Kopplungen zwischen eterokernen in Proteinen R 2 J N,CO < z!! C 35 z 90 z C 7 z N z N 55 z C 5 z C O C O C 40 z R
9 9/03 Wegen der Unterschiede zwischen den aliphatischen und den Carbonyl-Kohlenstoffen betrachet man die beiden getrennt:. Chemische Verschiebung δ CO ~ ppm δ Cα/β ~ 0-70 ppm 2. Kohlenstoff-Kohlenstoffkopplung J(CO,Cα) ~ 55 z J(C,C) ~35 z 3. Carbonyle haben keine Protonen gebunden Die Carbonyle sind die vierte Kernsorte
10 0/03 Will man Carbonyle als vierte Kernsorte betrachten, dann muss man auch Pulse haben, die entweder die Carbonyle oder die aliphatischen Kerne treffen, aber nicht beide. Das kann durch selektiven Pulse mit ausgefeilten Pulsformen geschehen. Oder mit einem simplen Trick, der darauf basiert, dass das Magnetfeld, das der Puls ausübt, durch off-resonance -Effekte größer wird
11 /03 B eff = (B ) 2 + (B 0 ω/γ) 2 B eff = ( B B γ 2 2 ) + ( 0 ω/ ) γb eff = (γb ) 2 + Ω 2 B tan θ tan = (B 0 θ = ω/γ) Ω = ( B ω / γ ) γb B 0 θ B eff > B B eff B Zudem ist der Weg der Magnetisierung zurück zur z- Achse kürzer
12 2/03 Wir suchen also nun den Abstand vom Sender, an dem der Puls, der eine Drehung von 90 an der Stelle des Senders bewirkt, eine Drehung von 360 bewirkt, dann hat der Puls keinen Effekt gehabt. γb eff * τ p = τ p = /4 * γb γb eff = (γb ) 2 + Ω 2 (γb ) 2 + Ω 2 * /γb = 4 + Ω2 /(γb ) 2 = 4 Ω 2 /(γb ) 2 = 5 Ω = 5 * γb
13 3/03 Der Abstand zwischen den Carbonylen und den Cα Kohlenstoffen beträgt ca. 20 ppm. Auf einem 600 Mz-Gerät (ca. 50 Mz für 3 C) sind das 8000 z Ω = 5 * γb also γb = 4647 z und damit ist τ p = 54 μsec Damit haben wir einen sehr robusten selektiven Puls
14 4/03 Sequentielle Zuordnung Wir müssen mit den Tripelresonanzexperimenten das gleiche erreichen, was mit NOESY/TOCSY bewerkstelligt worden ist. Im TOCSY gab es nur eine Korrelation vom N zum α, beim NOESY gab es zwei, einmal die gleiche wie im TOCSY, dazu den über das Carbonyl hinweg
15 Sequenzspezifische Zuordnung 5/03 So sieht der sequential walk mit homonuklearen Spektren aus d αn 2 d Nα (i,i) 2 d αn 3 d Nα (i,i) 3 d αn 4 d Nα (i,i) 4
16 Sequenzspezifische Zuordnung 6/03 Wir machen mit den heteronuklearen Kopplungen auch eine sequential walk J NCα 2 J NCα 2 2 J NCα 3 J NCα 3 2 J NCα 4 J NCα 4
17 7/03 Die Unterscheidung der beiden Signale vom N zum C α gelingt uns durch ein Spektrum das eine ähnliche Korrelation ergibt, aber unter Nutzung des Carbonyl. Die beiden Experimente heißen NCA und N(CO)CA, wobei der Name schon den Weg der Magnetisierung verrät. NCA: N(CO)CA: J NN J NCα/ 2 J NCα N N C α J NN J NCΟ J C αcο N N CO C α ier gibt es keine 2 J NCΟ
18 8/03 NCA R C C 2 J NC = 7 z N J N = 90 z O C N C J NC = z C O C R
19 9/03 N(CO)CA R C C J NC = 5 z N J N = 90 z O C N C C J CC = 55 z O C R
20 20/03 Protonendetektion ist wie gehabt immer am empfindlichsten, in beiden Fällen geht man nach dem Weg von N zum Cα auch wieder zurück zum N und detektiert dort: out and back Dabei muss immer wieder Magnetisierung von einem Kern zu einem einer anderen Kernsorte transferiert werden, das geht am besten mit dem INEPT-Schritt
21 2/03 Der INEPT-Schritt kann dabei ganz allgemein zum Transfer zwischen zwei beliebigen Kernsorten dienen, die Wartezeiten müssen nur an die Kopplungskonstanten angepasst werden n X m Y 90 y Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 90 y 2z X 80 y x Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 90 x πj X Δ πj X Δ 2
22 22/03 Bei Protonen haben wir schon gesehen das man bei mehr als einem Kopplungspartner die Wartezeiten nicht auf /2J setzen darf sondern kürzer halten muss 90 y Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 Entkopplung 2z X y x x πj X Δ 2 n X z 90 x πj X Δ
23 23/03 X: X x sin πj X Δ 2 X 2 : X x sin πj X Δ 2 cos πj 2X Δ 2 X 3 : X x sin πj X Δ 2 cos πj 2X Δ 2 cos πj 3X Δ 2 90 y Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 Entkopplung 2z X y x x πj X Δ 2 n X z 90 x πj X Δ
24 24/03 Dann bauen wir uns unsere Pulssequenz 90 y Δ /2 Δ /2 5 N z 90 x πj X Δ Δ 2 /2 Δ 2 /2 Entkopplung πj X Δ 2 2z X y Δ 2 kann hier für den Fall N eingestellt werden, also genau /2J (5.5 msec). 2 N wird dann unterdrückt (Seitenketten von Asn und Gln). Damit sind wir vom Proton zum Stickstoff gekommen, nun weiter zum Kohlenstoff
25 25/03 90 y Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 J = z Δ 3 = /4J = 22 msec 3 C α keine N-C-Kopplung Wir hängen ein weiteres INEPT an, dabei ist zu bedenken, dass der Stickstoff 2 Kopplungen zu C α hat, Δ 3 ist also nicht /2J sondern /4J
26 26/03 90 y Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 3 C Man stellt aber fest, dass die 80 Pulse überhand nehmen, man muss bedenken wofür man die braucht...
27 27/03 n X m Y 90 y Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 90 y 2z X 80 y x Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 90 x πj X Δ πj X Δ 2 Während Δ 2 soll die J XY aktiv sein. Es soll aber keine chemische Verschiebung auf Y entstehen, deshalb der 80 Puls. Der alleine würde die Kopplung aber refocussieren, also brauchen wir noch den zweiten 80 Puls. Wäre uns die chemische Verschiebung egal, bräuchten wir keinen Puls.
28 28/03 90 y Δ /2 Δ /2 Δ 2 /2 Δ 2 /2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 3 C Die Situation haben hier zweimal. Was wir eigentlich aber wollen ist Kopplung während Δ 2 und Δ 3 und keine chemische Verschiebung auf 5 N
29 29/03 90 y Δ /2 Δ /2 Δ 2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 Δ 3 /2 > Δ 2 3 C α Dann kann man sehr viele streichen. Δ 2 und Δ 3 kann man zusammenfassen, ein 80 Puls muss in der Mitte der 5N-Evolution sitzen, ein zweiter 80 Puls ist nötig
30 30/03 90 y Δ /2 Δ /2 Δ 2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 3 C α keine N-CO-Kopplung 3 CO Kopplung zwischen N und CO wird refocussiert, denn unsere Pulse sind ja selektiv für C α oder CO und ohne Puls auf CO kann sich Kopplung während Δ3 nicht entwickeln
31 3/03 90 y Δ /2 Δ /2 Δ 2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 t /2 t /2 3 C α Nach dem zweiten INEPT-Transfer wird nicht refocussiert sondern wie beim SQC nur die chemische Verschiebung des zweiten Kerns detektiert
32 32/03 90 y 90 y Δ /2 Δ /2 Δ 2 Entkopplung Δ 2 Δ /2 Δ /2 5 N Δ 3 /2 Δ 3 /2 t /2 t /2 Entk. Δ 3 /2 Δ 3 /2 3 C α Dann geht s wieder zurück zum Stickstoff und dann zum Proton und dann wird mit 5 N-Entkopplung detektiert
33 33/03 90 y 90 y Δ /2 Δ /2 Δ 2 Entkopplung Δ 2 Δ /2 Δ /2 5 N Δ 3 /2 Δ 3 /2 t /2 t /2 Entk. Δ 3 /2 Δ 3 /2 3 C α In der Mitte der Pulssequenz haben wir ein 5 N, 3 C α -SQC durchgeführt
34 34/03 Damit haben wir das NCA gebaut, es wird normalerweise als 3D-Spektrum aufgenommen, mit den chemischen Verschiebungen von C α, N und N auf den 3 Achsen. Die chemische Verschiebung der 5 N-Kerne wird in einem constant-time Experiment detektiert 90 y Entkopplung Δ 2 Δ /2 Δ /2 t /2 t /2 (Δ 3 -t 2 )/2 (Δ 3 +t 2 )/2 Entk.
35 35/03 Dann müssen wir aber wegen der Kopplung von N zu CO etwas unternehmen und einen Entkopplungspuls einbauen, den brauchen 90 y Entkopplung Δ 2 Δ /2 Δ /2 t /2 t /2 (Δ 3 -t 2 )/2 (Δ 3 +t 2 )/2 Entk. t 2 /2 wir auch in t
36 36/03 Die Wasserunterdrückung machen wir mit WATERGATE 90 y Entkopplung Δ 2 Δ /2 90 2O 90 2O Δ /2 t /2 t /2 (Δ 3 -t 2 )/2 (Δ 3 +t 2 )/2 Entkopp. t 2 /2
37 37/03 Da der Stickstoffkern mit zwei C α koppelt bekommen wir auch jeweils zwei Korrelationen, die für eine sequentielle Zuordnung reichen, wenn wir sie denn unterscheiden können. Diese Unterscheidung kann durch das N(CO)CA bewerkstelligt werden, in dem der Transfer zum Carbonyl noch dazu kommnt
38 38/03 90 y Δ /2 Δ /2 Δ 2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 J = 5 z Δ 3 = /2J = 33 msec 3 CO Der Anfang vom N(CO)CA ist genau wie beim NCA, nur gehen wir nicht zum C α sondern zum CO, hier gibt es nur eine Kopplung, also /2J für Δ3
39 39/03 90 y Δ /2 Δ /2 Δ 2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 3 CO Δ 4 /2 Δ 4 /2 J = 55 z Δ 4 = /2J = 9 msec 3 C α Dann kommt der INEPT-Schritt zum C α
40 40/03 90 y Δ /2 Δ /2 Δ 2 Entkopplung 5 N Δ 3 /2 Δ 3 /2 3 CO Δ 4 /2 Δ 4 /2 3 C α Evolutionszeit um die chemische Verschiebung auf dem C α zu bekommen t /2 t /2
41 4/03 Der Rest ist wie beim NCA, Wasserunterdrückung mit WATERGATE, Evolutionszeit für 5 N als constant time Experiment und das Experiment wird als dreidimensionales Spektrum aufgenommen mit, 5 N und 3 C α chemischen Verschiebungen.
42 42/03 N(CO)CA Entkopplung 5 N Entk. 3 CO 3 C α G z
43 43/03 N(CO)CA Entkopplung 5 N Entk. 3 CO 3 C α G z 5 N, 3 CO-SQC
44 44/03 N(CO)CA Entkopplung 5 N Entk. 3 CO 3 C α G z 3 CO, 3 C α -SQC
45 45/03 Die 5 N-Verschiebung dient dabei der Beseitigung von Überlagerung durch die dritte Dimension, die sequentielle Zuordnung erfolgt über die -C-planes der 3D-Spektren
46 46/03 3D-NMR
47 47/03 NCA N(CO)CA δ C3 δ C3 = sequentielle Signale δ C2 δ C2 δ C4 δ C4 δ C δ C δ δ 2 δ 3 δ δ 2 δ 3
48 48/ δ C3 δ C2 Damit sind wir bereit für den sequential walk im NCA δ C4 δ C δ 2 δ 3 δ 4
49 49/03 Man kann analog zu NCA/N(CO)CA auch Experimente machen die die chemische Verschiebung des CO detektieren, auch da ist ein Paar von Experimente möglich: das NCO und das N(CA)CO. Zusammen ergeben sich wieder eine bzw. zwei Korrelationen so dass eine sequentielle Zuordnung möglich ist. Noch besser ist es aber, wenn das C β als weitere chemische Verschiebung hinzukommt.
50 50/03 Um nach dem Transfer vom N zum C α auch noch den Schritt zum C β zu machen, benötigt man einen COSY-artigen Transfer. Die Kopplungen zwischen C α und C β sind in Proteinen recht uniform, der Transfer wird sich also gut steuern lassen. Allerdings wollen wir ja C α und C β detektieren, der Transfer sollte also so angelegt sein, daß beide Signale ungefähr gleich groß sind
51 5/03 Die folgende Sequenz wird verwendet: 90 y 90 y 3 C Δ/2 Δ/2 t Δ/2 Δ/2 C αz 90 C x -C αy πj CC Δ -C αy cos πj CC Δ + 2C αx C βz sin πj CC Δ 90 C y -C αy cos πj CC Δ -2C αz C βx sin πj CC Δ
52 52/03 90 y 90 y 3 C Δ/2 Δ/2 t Δ/2 Δ/2 -C αy cos πj CC Δ -2C αz C βx sin πj CC Δ πωt -C αy cos πj CC Δ cos πω α t -2C αz C βx sin πj CC Δ cos πω β t 90 C y πj CC Δ -C αy cos πj CC Δ cos πω α t + 2C αx C βz sin πj CC Δ cos πω β t -C αy cos 2 πj CC Δ cos πω α t + C αy sin 2 πj CC Δ cos πω β t
53 53/03 90 y 90 y 3 C Δ/2 Δ/2 t Δ/2 Δ/2 -C αy cos 2 πj CC Δ cos πω α t + C αy sin 2 πj CC Δ cos πω β t Konstante! Konstante! Wir haben also am Ende vom C α zwei Signale mit gleicher Phase aber unterschiedlichem Vorzeichen, die die chemischen Verschiebungen von C α und C β tragen. Und mit Δ = /4J CC ergibt sich für beide Terme der Faktor ½.
54 54/03 NCACB R J CC = 35 z C C 2 J NC = 7 z N J N = 90 z O C N C J NC = z C O C J CC = 35 z R
55 55/03 N(CO)CACB R J CC = 35 z C C J NC = 5 z N J N = 90 z O C N C C J CC = 55 z O C R
56 56/03 Die Namen der Experimente ergeben sich aus der bisherigen Logik der Namensgebung. Allerdings kann man die gleichen Spektren mit einem kompakteren Paar an Pulssequenzen erhalten, die mit den C-gebundenen Protonen starten. Das sind das CBCA(CO)NN und das CBCANN. Wie die beiden arbeiten wollen wir uns jetzt schematisch anschauen
57 57/03 CBCA(CO)NN Entkopplung 5 N Entkopplung 3 C α/β 3 CO Beginn und Detektion auf dem Proton: Empfindlichkeit!
58 58/03 CBCA(CO)NN Δ /2 Δ /2 Δ 2 Entkopplung 5 N Entkopplung 3 C α/β 3 CO INEPT von Protonen zu Kohlenstoffen
59 59/03 CBCA(CO)NN Entkopplung 5 N Entkopplung 3 C α/β 3 CO COSY von Kohlenstoff zu Kohlenstoff
60 60/03 CBCA(CO)NN Entkopplung 5 N Entkopplung 3 C α/β 3 CO INEPT von aliphatischem C zu Carbonyl-C
61 6/03 CBCA(CO)NN Entkopplung 5 N Entkopplung 3 C α/β 3 CO INEPT von Carbonyl-C zu Stickstoff
62 62/03 CBCA(CO)NN Entkopplung 5 N Entkopplung 3 C α/β 3 C INEPT von Stickstoff zu Aminoproton
63 63/03 CBCA(CO)NN Entkopplung 5 N Entkopplung 3 C α/β 3 CO.Evolution: chemische Verschiebung von aliphatischen C, als constant time Experiment
64 64/03 CBCA(CO)NN Entkopplung 5 N Entkopplung 3 C α/β 3 CO 2.Evolution: chemische Verschiebung von Stickstoff, als constant time Experiment
65 65/03 CBCANN Entkopplung 5 N Entkopplung 3 C α/β ier wird wieder die Kopplung zwischen C α und N genutzt, also sind wieder zwei Wege für den Magnetisierungstransfer vorhanden und es sollten 4 Signale werden
66 66/03 Sequentielle Zuordnung
67 67/03 Sequentielle Zuordnung
68 68/03 Sequentielle Zuordnung
69 69/03 Sequentielle Zuordnung
70 70/03 Mit den beiden Experimenten sind wieder sequentielle Nachbarschaften etabliert worden. Um eine eindeutige Zuordnung zu machen muss man die Reihe der Aminosäuren mir der Sequenz abgleichen, d.h. man braucht Information über den Aminosäuretyp Die bekommt man entweder aus den Spinsystemen der Seitenketten (siehe unten) oder aus den chemischen Verschiebungen von Cα und Cβ.
71 7/03 Aminosäuretyp-Bestimmung
72 72/03 backbone -Zuordnung 5 N [ppm] N-SQC ohne Zuordnung [ppm] 35
73 73/03 backbone -Zuordnung G5 5 N [ppm] W4 ε M25 N47 L3 V53 G5 V58 V9 Y3 D48 A56 R2 V23 T4 D40 N35 G28 T37 S9 T32 Y57 K59 D4 F52 E45 Q50 T24 Y5 R49 K6 K8 E3 K39 I30 V44 E22 K27 N38 D29 W4 L0 E7 K46 D2 E7 L8 D62 K26 K60 V46 L6 L34 Q6 A L2 A55 L33 W42 ε S36 W42 N47 N 2 N38 N 2 N35 N 2 Q50 N 2 Q6 N N-SQC mit Zuordnung R49 ε [ppm] R2 ε 35
74 74/03 Diese backbone -Zuordnung beinhaltet die Zuordnung der Aminoprotonen, der Stickstoffkerne und der beiden Kohlenstoffe Cα und Cβ. Sie kann mit weiteren Tripelresonanzexperimenten auf die Seitenketten erweitert werden BA(CO)NN α und β (CCO)NN-TOCSY Protonen der Seitenkette ()C(CO)NN-TOCSY Kohlenstoffe der Seitenkette Man führt aber auch noch eine andere Zuordnung durch
75 75/03 Seitenkettenzuordnung
76 76/03 CC-COSY 3 C α/β Entkopplung Beginn und Detektion auf dem Proton: Empfindlichkeit!
77 77/03 CC-COSY 3 C α/β Entkopplung INEPT von Protonen zu Kohlenstoffen
78 78/03 CC-COSY 3 C α/β Entkopplung COSY von Kohlenstoff zu Kohlenstoff
79 79/03 CC-COSY 3 C α/β Entkopplung INEPT von Kohlenstoffen zu Protonen
80 80/03 CC-COSY 3 C α/β Entkopplung.Evolution: chemische Verschiebung von Protonen 2.Evolution: chemische Verschiebung von Kohlenstoffen
81 8/03 CC-TOCSY 3 C α/β TOCSY-Mix. Entkopplung So wie im Protonen-Fall das COSY durch das TOCSY ergänzt werden kann um das ganze Spinsystem abzuklopfen geht das auch im Kohlenstoff-Fall. Ansonsten ist das Experiment wie das CC-COSY
82 82/03 CC-COSY CC-COSY CC-TOCSY CC-TOCSY
83 83/03
84 84/03 NMR an großen Proteinen
85 NMR an großen Proteinen 85/03 Wenn die Größe der Proteine weiter zunimmt, wird es aber auch mit den bislang gezeigten Tripelresonanzexperimente immer schwieriger. Zum einen wird die Zahl der Signale immer größer ohne das die Dispersion der Signale sich ändert. Zum anderen wird die Relaxation der involvierten Kerne immer effizienter, dadurch wird die Linienbreite immer größer und der Transfer von Magnetisierung wird immer schwächer bei gleichbleibender Länge der Wartezeiten (da sich die Kopplungen nicht ändern)
86 NMR an großen Proteinen 86/03 Die Zahl der Signale nimmt zu Ubiquitin (76 aa) Cph-Δ2 (54 aa) ppm ppm ppm
87 NMR an großen Proteinen 87/03 Die Linien werden breiter, das sorgt für mehr Überlagerung und für ineffizienteren Magnetisierungstransfer z 0 z 50 z ppm ppm ppm
88 NMR an großen Proteinen 88/03 Während man gegen die zunehmende Zahl der Signale nur wenig tun kann, kann man sich überlegen wie man die zunehmende Relaxation zurückdrängt. Dazu gibt es zwei Vorgehensweisen, die man sowohl unabhängig als auch gemeinsam nutzen kann: Deuterierung TROSY
89 NMR an großen Proteinen 89/03 Die auptquelle der Relaxation ist für die involvierten Kerne unterschiedlich Protonen ( ) Kohlenstoff ( 3 C) Stickstoff ( 5 N) andere Protonen das direkt gebunden Proton das direkt gebunden Proton Wobei der Unterschied zwischen Stickstoff und Kohlenstoff gebundenen Protonen die Austauschbarkeit mit dem Wasser ist
90 NMR an großen Proteinen 90/03 Wir haben gesehen das viele der Experimente die wir bislang gesehen haben mit dem N beginnen und es auch detektieren. Das macht man sich zu nutze: Die Proteine werden deuteriert (in D 2 O) hergestellt und erst am Ende in 2 O überführt wo nur die austauschbaren Protonen (hauptsächlich die N ) zurücktauschen. Damit sind um die N -Protonen nur noch wenige andere Protonen und der auptrelaxationspartner der Kohlenstoffe ist weg
91 NMR an großen Proteinen 9/03 Deuterierung normales Protein deuteriertes Protein = - C = -N
92 NMR an großen Proteinen 92/03 Deuterierung Protonenspins werden verdünnt, die C-- Wechselwirkung entfernt N D D N N C D D N D D C D D γ D /γ ~ /6.5 C C D= D=0,02
93 NMR an großen Proteinen 93/03 Jetzt bleiben noch die Stickstoffkerne, die ihren auptrelaxationspartner noch haben. Beim TROSY (Transverse Relaxation Optimized SpectroscopY) werden nun unterschiedliche Relaxationseffekte genutzt um die Linien von Stickstoff und N zu verbessern
94 NMR an großen Proteinen 94/03 Zwei der wichtigsten Relaxationsmechanismen haben wir zu Beginn kennen gelernt, die Dipol-Dipol-Wechselwirkung (DD) und die chemical-shift-anisotropie (CSA). Beide Mechanismen können sich gegenseitig beeinflussen. DD CSA
95 NMR an großen Proteinen 95/03 Bei kleinen Molekülen ist diese Beeinflussung nicht leicht zu erkennen 5 N-SQC 5 N-SQC no decoupling
96 NMR an großen Proteinen 96/03 Wir erinnern uns aber, dass den vier Komponenten des Multipletts die beiden unterschiedlichen Spinzustände (α und β) zuzuordnen sind. Es stellt sich heraus, dass die Beeinflussung von CSA und DD bei jeder anders ist. αα βα αβ ββ N R α ~ (D N + CSA ) R β ~ (D N -CSA ) R αn ~ (D N + CSA N ) R βn ~ (D N -CSA N )
97 NMR an großen Proteinen 97/03 Und bei großen Molekülen ist das dann in der Tat zu sehen, jeweils eine Linie von und 5 N ist schmal, eine der vier Peaks des Multipletts also besonders scharf 5 N-SQC 5 N-SQC no decoupling 5 δ N(ppm) δ (ppm) δ (ppm)
98 NMR an großen Proteinen 98/03 Man kann nun berechnen wann der Effekt am größten ist D N =(/2 2) γ γ N μ(h/2π(r N ) 3 ) CSA =(/2 2) γ B 0 Δσ CSA N =(/2 2) γ N B 0 Δσ N γ = 2.6 *0 8 (Ts) - γ N = *0 7 (Ts) - Δσ = - 6 ppm Δσ N = - 60 ppm Δσ / Δσ N = γ N / γ (D N CSA N ) = (D N CSA ) = 0 for the same B 0 B 0 = 25.6 T ~. Gz
99 NMR an großen Proteinen 99/03 Mit realistischen Annahmen liegt das Maximum nah bei 950 Mz 900 Mz 900 Mz
100 NMR an großen Proteinen 00/03 Um nur den einen Peak zu erhalten benutzt man diese Pulssequenz, das ganze kann aber auch in jedes Tripelresonanzexperiment eingebaut werden y Δ/2 Δ/2 Δ/2 Δ/ n X t /2 t /2
101 NMR an großen Proteinen 0/03 Am Ende erhält man dann im TROSY scharfe Linien auch für größere Moleküle 5 δ N(ppm) δ (ppm)
102 02/03 Grundlagen der NMR-Spektroskopie Techniken für organische Moleküle Techniken für Peptide Techniken für Proteine
103 03/03 That s it Fragen: schmieder@fmp-berlin.de Scripte:
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil IX. Peter Schmieder AG NMR
 Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil IX Das Programm 2/104 Beim letztes Mal Methoden zur Bestimmung von skalaren Kopplungskonstanten Das
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil IX Das Programm 2/104 Beim letztes Mal Methoden zur Bestimmung von skalaren Kopplungskonstanten Das
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III. Peter Schmieder AG NMR
 Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III Programm 2/92 Was haben wir uns letztes Mal angeschaut: Wie beschreibt man Experimente mit Produktoperatoren Wie funktioniert
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III Programm 2/92 Was haben wir uns letztes Mal angeschaut: Wie beschreibt man Experimente mit Produktoperatoren Wie funktioniert
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil V. Peter Schmieder AG NMR
 Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil V Das Programm 2/96 Beim letzten Mal Mehrdimensionale NMR-Spektroskopie COSY, DQF-COSY und Phasencyclen
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil V Das Programm 2/96 Beim letzten Mal Mehrdimensionale NMR-Spektroskopie COSY, DQF-COSY und Phasencyclen
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil IV. Peter Schmieder AG NMR
 Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil IV Das Programm 2/91 Beim letzten Mal Produktoperatoren INEPT DEPT Das Programm 3/91 Heute Mehrdimensionale
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil IV Das Programm 2/91 Beim letzten Mal Produktoperatoren INEPT DEPT Das Programm 3/91 Heute Mehrdimensionale
Teil 3 2D-NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil VIII. Peter Schmieder AG NMR
 Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil VIII Das Programm 2/100 Beim letztes Mal Heteronukleare NMR an Peptiden Das Programm /100 Heute Methoden
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil VIII Das Programm 2/100 Beim letztes Mal Heteronukleare NMR an Peptiden Das Programm /100 Heute Methoden
4.57 ppm 1.45 ppm = 3.12 ppm 3.12 ppm * MHz = Hz Hz = rad/sec
 (1) Zwei Signale liegen im Protonenspektrum bei 1.45 und 4.57 ppm, das Spektrometer hat eine Frequenz von 400.13 MHz. Wieweit liegen die Signale in Hz bzw. in rad/sec auseinander? 4.57 ppm 1.45 ppm = 3.12
(1) Zwei Signale liegen im Protonenspektrum bei 1.45 und 4.57 ppm, das Spektrometer hat eine Frequenz von 400.13 MHz. Wieweit liegen die Signale in Hz bzw. in rad/sec auseinander? 4.57 ppm 1.45 ppm = 3.12
INADEQUATE 13 C, 13 C-COSY
 INADEQUATE 13 C, 13 C-COSY Die bisher diskutierten Korrelationsmethoden beruhen auf Protonen. Da das eigentliche Skelett eines organischen Moleküls das Kohlenstoffgerüst ist, wäre es in einigen Fällen
INADEQUATE 13 C, 13 C-COSY Die bisher diskutierten Korrelationsmethoden beruhen auf Protonen. Da das eigentliche Skelett eines organischen Moleküls das Kohlenstoffgerüst ist, wäre es in einigen Fällen
Multipuls-NMR in der Organischen Chemie. 1 H, 1 H, 1 H Relayed-COSY und TOCSY
 1 H, 1 H, 1 H Relayed-COSY und TOCSY Das 1 H, 1 H, 1 H-Relay-COSY-Experiment gehört historisch zu den älteren und wurde später durch das weit überlegene TOCSY-Experiment ersetzt. Dennoch sei es hier kurz
1 H, 1 H, 1 H Relayed-COSY und TOCSY Das 1 H, 1 H, 1 H-Relay-COSY-Experiment gehört historisch zu den älteren und wurde später durch das weit überlegene TOCSY-Experiment ersetzt. Dennoch sei es hier kurz
Molekulare Biophysik. NMR-Spektroskopie (Teil 3)
 Molekulare Biophysik NMR-Spektroskopie (Teil 3) Das NMR-Spektrometer Das NMR-Spektrometer 3/102 Probenwechsler Magnet Hardware-Schrank Probenkopf Das NMR-Spektrometer 4/102 Magnet B 0 [Tesla] 0 [MHz] 1.4
Molekulare Biophysik NMR-Spektroskopie (Teil 3) Das NMR-Spektrometer Das NMR-Spektrometer 3/102 Probenwechsler Magnet Hardware-Schrank Probenkopf Das NMR-Spektrometer 4/102 Magnet B 0 [Tesla] 0 [MHz] 1.4
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil VI. Peter Schmieder AG NMR
 Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil VI Das Programm 2/105 Beim letztes Mal Heteronukleare NMR Ein Beispiel Das Programm 3/105 Heute Peptide
Vorlesung Mehrdimensionale NMR-Spektroskopie- Grundlagen und Anwendungen in der Strukturaufklärung Teil VI Das Programm 2/105 Beim letztes Mal Heteronukleare NMR Ein Beispiel Das Programm 3/105 Heute Peptide
Homonukleare Korrelationsspektroskopie (COSY)
 Homonukleare Korrelationsspektroskopie (COSY) Hier wird ähnlich wie bei HETCOR in beiden Dimensionen die chemische Verschiebung abgebildet. Im homonuklearen Fall ( 1 H, 1 H COSY) jedoch, ist es in beiden
Homonukleare Korrelationsspektroskopie (COSY) Hier wird ähnlich wie bei HETCOR in beiden Dimensionen die chemische Verschiebung abgebildet. Im homonuklearen Fall ( 1 H, 1 H COSY) jedoch, ist es in beiden
Molekulare Biophysik. NMR-Spektroskopie (Teil 2)
 Molekulare Biophysik NMR-Spektroskopie (Teil 2) NMR-Parameter NMR-Parameter 3/88 Folgenden NMR-Parameter sind von Interesse chemische Verschiebung skalare Kopplung Relaxation / NOE-Effekt NMR-Parameter
Molekulare Biophysik NMR-Spektroskopie (Teil 2) NMR-Parameter NMR-Parameter 3/88 Folgenden NMR-Parameter sind von Interesse chemische Verschiebung skalare Kopplung Relaxation / NOE-Effekt NMR-Parameter
Polarisationstransfer
 Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil II. Peter Schmieder AG NMR
 Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil II Programm 2/114 Was haben wir uns letztes Mal angeschaut: Wie kommt es zum Effekt der kernmagnetischen Resonanz Was ist das
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil II Programm 2/114 Was haben wir uns letztes Mal angeschaut: Wie kommt es zum Effekt der kernmagnetischen Resonanz Was ist das
3D NMR Experimente. Pulssequenz des 3D 15N-NOESY-HSQC
 3D NMR Experimente Pulssequenz des 3D 15N-NOESY-SQC 1) Zum Beispiel sinnvoll, wenn sich viele Signale in einem 2D Spektrum, z.b. einem 1-1 NOESY oder TOCSY überlagern. 2) Kombination mit einem anderen
3D NMR Experimente Pulssequenz des 3D 15N-NOESY-SQC 1) Zum Beispiel sinnvoll, wenn sich viele Signale in einem 2D Spektrum, z.b. einem 1-1 NOESY oder TOCSY überlagern. 2) Kombination mit einem anderen
Bestimmung der Struktur einer (un)bekannten Verbindung
 Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
Chemische und Magnetische Äquivalenz
 Chemische und Magnetische Äquivalenz Das Aussehen von NMR-Signalen in Mehr-Spinsystemen wird ganz wesentlich davon beeinflusst, ob es äquivalente Kerne gibt oder nicht. ierbei sind zwei wichtige Arten
Chemische und Magnetische Äquivalenz Das Aussehen von NMR-Signalen in Mehr-Spinsystemen wird ganz wesentlich davon beeinflusst, ob es äquivalente Kerne gibt oder nicht. ierbei sind zwei wichtige Arten
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil I. Peter Schmieder AG NMR
 Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil I Die Vorlesung 2/116 1. Grundlagen der NMR-Spektroskopie NMR-Prinzip, FT-NMR, Signaldetektion 2. Mehrdimensionale NMR (2D) Vektormodell,
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil I Die Vorlesung 2/116 1. Grundlagen der NMR-Spektroskopie NMR-Prinzip, FT-NMR, Signaldetektion 2. Mehrdimensionale NMR (2D) Vektormodell,
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Spinsysteme. AX 3 -Spinsystem
 Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Spektroskopische Methoden in der Organischen Chemie (OC IV) C NMR Spektroskopie
 6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
Spektroskopie-Seminar SS NMR-Spektroskopie. C-NMR-Spektroskopie und 2D-Spektroskopie
 13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
Zentralabstand b, Spaltbreite a. Dreifachspalt Zentralabstand b, Spaltbreite a. Beugungsgitter (N Spalte, N<10 4, Abstand a)
 Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
3.7 Gekoppelte Spinsysteme
 - 47-3.7 Gekoppelte Spinsysteme 3.7. Matrixdarstellung von Operatoren in Systemen mit mehreren Spins Um Rechnungen für Systeme aus mehr als einem Spin durchführen zu können, müssen wir die Matrixdarstellungen
- 47-3.7 Gekoppelte Spinsysteme 3.7. Matrixdarstellung von Operatoren in Systemen mit mehreren Spins Um Rechnungen für Systeme aus mehr als einem Spin durchführen zu können, müssen wir die Matrixdarstellungen
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
4.6 Strukturbestimmung in Proteinen
 - 54-4.6 Strukturbestimmung in Proteinen 4.6.1 Aminosäuren und Proteine Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen: sie spielen nicht nur für die Struktur eine wichtige
- 54-4.6 Strukturbestimmung in Proteinen 4.6.1 Aminosäuren und Proteine Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen: sie spielen nicht nur für die Struktur eine wichtige
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
Aufgabe 1: (18 Punkte)
 Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
Multipuls-NMR in der Organischen Chemie. Puls und FID
 Puls und FID Obwohl der Puls eine bestimmte, am NMR-Spektrometer vorab eingestellte Sendefrequenz ν 1 hat, ist er in der Lage, über einen relativ weiten Frequenzbereich von mehreren khz, den gesamten Resonanzbereich
Puls und FID Obwohl der Puls eine bestimmte, am NMR-Spektrometer vorab eingestellte Sendefrequenz ν 1 hat, ist er in der Lage, über einen relativ weiten Frequenzbereich von mehreren khz, den gesamten Resonanzbereich
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Methodische Ansätze zur Strukturaufklärung: Rnt. - Kernmagnetische Resonanzspektroskopie (NMR)
 ? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
Einführung in die NMR-Spektroskopie. NMR-Spektroskopie. Teil 1: Einführung und Grundlagen der 1 H NMR. Das NMR Spektrometer
 NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
Vorlesung "Grundlagen der Strukturaufklärung"
 Vorlesung "Grundlagen der trukturaufklärung" für tudenten des tudiengangs "Bachelor Chemie" ommersemester 2003 Zeit: Montag, 9:00 bis 12:00 und Dienstag, 12:00 bis 14:00 Ort: MG 088 (Montags) und MC 351
Vorlesung "Grundlagen der trukturaufklärung" für tudenten des tudiengangs "Bachelor Chemie" ommersemester 2003 Zeit: Montag, 9:00 bis 12:00 und Dienstag, 12:00 bis 14:00 Ort: MG 088 (Montags) und MC 351
Kurs "Spektroskopische Methoden in der Anorganischen und Organischen Chemie" Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt 1)
 Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Molekulare Biophysik. NMR-Spektroskopie (Teil 1)
 Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/93 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/93 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Chemisches Grundpraktikum II (270002) Kernresonanzspektroskopie. NMR-Spektroskopie
 hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
Hochauflösende NMR in Festkörpern
 Hochauflösende NMR in Festkörpern Strukturaufklärung in Phosphatgläsern Anne Wiemhöfer Agnes Wrobel Gliederung Auftretende Wechselwirkungen in der Festkörper NMR Flüssig- vs. Festkörper-NMR NMR Techniken
Hochauflösende NMR in Festkörpern Strukturaufklärung in Phosphatgläsern Anne Wiemhöfer Agnes Wrobel Gliederung Auftretende Wechselwirkungen in der Festkörper NMR Flüssig- vs. Festkörper-NMR NMR Techniken
NMR-Spektroskopie. Magnet. Steuerung. Probenrohr Spinner. Shimspulen. B -Spulen. Gradient 2. Vorverstärker
 NMR-Spektroskopie Magnet Steuerung He He CPU Frequenz Pulsform Pulsleistung Zeitkontrolle Temperierung Gradienten Shim/Lock/Gas Vorverstärker N N Probenrohr Spinner Shimspulen B -Spulen Gradient 2 H K
NMR-Spektroskopie Magnet Steuerung He He CPU Frequenz Pulsform Pulsleistung Zeitkontrolle Temperierung Gradienten Shim/Lock/Gas Vorverstärker N N Probenrohr Spinner Shimspulen B -Spulen Gradient 2 H K
Das NMR-Experiment in der Vektordarstellung
 Das NMR-Experiment in der Vektordarstellung Kerne mit einer Spinquantenzahl I = ½ ( 1 H, 13 C) können in einem äußeren statischen homogenen Magnetfeld B 0 (Vektorfeld) zwei Energiezustände einnehmen: +½
Das NMR-Experiment in der Vektordarstellung Kerne mit einer Spinquantenzahl I = ½ ( 1 H, 13 C) können in einem äußeren statischen homogenen Magnetfeld B 0 (Vektorfeld) zwei Energiezustände einnehmen: +½
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
NMR-Lösungsmittel. 1 H-NMR. Bei der Verwendung der normalen, nichtdeuterierten Lösungsmittel. Spektroskopie in der Organischen Chemie
 NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ
 Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Digitalisierung und ihre Konsequenzen
 Digitalisierung und ihre Konsequenzen Bisher haben wir im Zusammenhang mit dem FID und den daraus resultierenden frequenzabhängigen Spektren immer nur von stetigen Funktionen gesprochen. In Wirklichkeit
Digitalisierung und ihre Konsequenzen Bisher haben wir im Zusammenhang mit dem FID und den daraus resultierenden frequenzabhängigen Spektren immer nur von stetigen Funktionen gesprochen. In Wirklichkeit
13 C, 1 H-Kopplungskonstanten. 13 C, 1 H-Kopplungen hier leichter erkannt werden können. Spektroskopie in der Organischen Chemie
 Spektroskopie in der Organischen hemie 13, 1 -Kopplungskonstanten NMR-Signalaufspaltungen aufgrund von skalaren Kopplungen treten grundsätzlich bei beiden Kopplungspartnern auf. Entsprechend kann man 13,
Spektroskopie in der Organischen hemie 13, 1 -Kopplungskonstanten NMR-Signalaufspaltungen aufgrund von skalaren Kopplungen treten grundsätzlich bei beiden Kopplungspartnern auf. Entsprechend kann man 13,
D-(+)-Biotin (Vitamin H)
 D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
Hochauflösende Probenköpfe für 19. F NMR Anwendungen. Aitor Moreno Vierzigste Bruker NMR Benutzertagung 2016, Karlsruhe 09.
 Hochauflösende Probenköpfe für F NMR Anwendungen Aitor Moreno Vierzigste Bruker NMR Benutzertagung 206, Karlsruhe 09. November 206 Fluorit (CaF 2 ), lat. fluores Innovation with Integrity Wieso F NMR?
Hochauflösende Probenköpfe für F NMR Anwendungen Aitor Moreno Vierzigste Bruker NMR Benutzertagung 206, Karlsruhe 09. November 206 Fluorit (CaF 2 ), lat. fluores Innovation with Integrity Wieso F NMR?
Analytische Chemie III: Strukturaufklärung
 Analytische Chemie III: Strukturaufklärung Verbindung Struktur Sinnesorgan der Chemiker 1 Analytische Chemie III: Strukturaufklärung Inhalt - Strategien zur Stoffisolierungen / Probenvorbereitung - 13
Analytische Chemie III: Strukturaufklärung Verbindung Struktur Sinnesorgan der Chemiker 1 Analytische Chemie III: Strukturaufklärung Inhalt - Strategien zur Stoffisolierungen / Probenvorbereitung - 13
Spektroskopie in der Organischen Chemie. 1 H, 1 H-Kopplungskonstanten. Geminale Kopplungen
 Spektroskopie in der rganischen hemie Geminale Kopplungen 1, 1 -Kopplungskonstanten Wenn sich die beiden Kopplungspartner (wie Zwillinge; lat.: gemini) am gleichen Kohlenstoffatom befinden, also nur zwei
Spektroskopie in der rganischen hemie Geminale Kopplungen 1, 1 -Kopplungskonstanten Wenn sich die beiden Kopplungspartner (wie Zwillinge; lat.: gemini) am gleichen Kohlenstoffatom befinden, also nur zwei
1 NMR von Proteinen. 1.1 Proteine Strukturbestimmung Motivation und Grundlagen
 1.1 Proteine 1.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
1.1 Proteine 1.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
gleicher Magnetfeldstärke die Resonanzfrequenz entsprechend kleiner; z.b: 400 MHz 1 H, aber MHz 13 C.
 Der 13 C-Kern ist in seinen wichtigsten Kerneigenschaften dem 1 H ähnlich. Er ist ebenso ein Spin-½-Kern, weist also im äußeren Magnetfeld B 0 nur zwei praktisch gleich populierte Energiezustande auf.
Der 13 C-Kern ist in seinen wichtigsten Kerneigenschaften dem 1 H ähnlich. Er ist ebenso ein Spin-½-Kern, weist also im äußeren Magnetfeld B 0 nur zwei praktisch gleich populierte Energiezustande auf.
NMR Spektroskopie. 1nm Frequenz X-ray UV/VIS Infrared Microwave Radio
 NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
Protein-NMR. Vertiefungsfach Analytische Chemie (WS2015/16) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC
 Protein-NMR Vertiefungsfach Analytische Chemie (WS2015/16) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Themenübersicht Termin 1 am 30.11.15: Biochemie von Proteinen (Aufbau,
Protein-NMR Vertiefungsfach Analytische Chemie (WS2015/16) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Themenübersicht Termin 1 am 30.11.15: Biochemie von Proteinen (Aufbau,
AQ -1 = 1.2 Hz digitale Auflösung pro 1.2 Hz ein Datenpunkt
 6. Datenaufnahme mit dem FT-Spektrometer: Digitalisierung Anregung Detektion Auswertung RF-Pulse/ Delays Digitalisierung des im AD-Wandler Fouriertransformation, Fensterfunktion, Apodisierung... Der Analog-Digital-onverter
6. Datenaufnahme mit dem FT-Spektrometer: Digitalisierung Anregung Detektion Auswertung RF-Pulse/ Delays Digitalisierung des im AD-Wandler Fouriertransformation, Fensterfunktion, Apodisierung... Der Analog-Digital-onverter
INEPT und HSQC. Ein INEPT Transfer wird durch die folgende Pulssequenz erreicht: Ausgehend von der Gleichgewichtsmagnetisierung I z erhält man somit:
 NEPT und HQC n dieem Kapitel werden heteronukleare NMR-Korrelatioeperimente und deren Anwendung am Beipiel de NEPT Tranfer und de HQC Eperimente eingeführt. NEPT Beim NEPT (nenitive Nuclei Enhanced b Polariation
NEPT und HQC n dieem Kapitel werden heteronukleare NMR-Korrelatioeperimente und deren Anwendung am Beipiel de NEPT Tranfer und de HQC Eperimente eingeführt. NEPT Beim NEPT (nenitive Nuclei Enhanced b Polariation
Der Kern-Overhauser-Effekt (Nuclear Overhauser Effect, NOE)
 Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
6 NMR von Proteinen. 6.1 Proteine Strukturbestimmung Motivation und Grundlagen
 6.1 Proteine 6.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
6.1 Proteine 6.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
Einführung in die Bearbeitung und Auswertung von 2D-NMR-Spektren
 Einführung in die Bearbeitung und Auswertung von 2D-NMR-Spektren Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie I Einführungskurs 2D-NMR-Spektren 1 Theorie Bei mehrdimensionalen Spektren ist
Einführung in die Bearbeitung und Auswertung von 2D-NMR-Spektren Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie I Einführungskurs 2D-NMR-Spektren 1 Theorie Bei mehrdimensionalen Spektren ist
NMR Spektroskopie I = 0 : C, 16 O (sogenannte gg-kerne haben immer I=0!) I = 1/2: 1 H, 13 C, 15 N, 19 F, 31 P,... I = 1: 2. H=D, 6 Li, 14 N I = 3/2: 7
 NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
Übungen zur Ingenieur-Mathematik III WS 2011/12 Blatt Aufgabe 25: Berechnen Sie den kritischen Punkt der Funktion
 Übungen zur Ingenieur-Mathematik III WS 11/1 Blatt 8 3.11.11 Aufgabe 5: Berechnen Sie den kritischen Punkt der Funktion fx, y 3x 5xy y + 3 und entscheiden Sie, ob ein Maximum, Minimum oder Sattelpunkt
Übungen zur Ingenieur-Mathematik III WS 11/1 Blatt 8 3.11.11 Aufgabe 5: Berechnen Sie den kritischen Punkt der Funktion fx, y 3x 5xy y + 3 und entscheiden Sie, ob ein Maximum, Minimum oder Sattelpunkt
NMR (Kernmagnetische Resonanz, Nuclear Magnetic Resonance) Horst Friebolin: Wiley, VCH, ISBN-10: , 49,90 Euro
 NMR (Kernmagnetische Resonanz, Nuclear Magnetic Resonance) Horst Friebolin: Wiley, VCH, ISBN-10: 3527315713, 49,90 Euro 1 NMR historisch Isidor Isaac Rabi Nobelpreis 1944 Weist in Molekularstrahlexperiment
NMR (Kernmagnetische Resonanz, Nuclear Magnetic Resonance) Horst Friebolin: Wiley, VCH, ISBN-10: 3527315713, 49,90 Euro 1 NMR historisch Isidor Isaac Rabi Nobelpreis 1944 Weist in Molekularstrahlexperiment
6 NMR von Proteinen. 6.1 Proteine Strukturbestimmung Motivation und Grundlagen
 6.1 Proteine 6.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
6.1 Proteine 6.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
Magnetresonanztomographie (MRT) * =
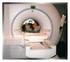 γ * γ π Beispiel: - Protonen ( H) Messung - konstantes B-Feld (T) in -Richtung - Gradientenfeld (3mT/m) in -Richtung - bei 0: f 00 4,6 MH Wie stark ist Frequenveränderung Df der Spins bei 0 mm? f (0mm)
γ * γ π Beispiel: - Protonen ( H) Messung - konstantes B-Feld (T) in -Richtung - Gradientenfeld (3mT/m) in -Richtung - bei 0: f 00 4,6 MH Wie stark ist Frequenveränderung Df der Spins bei 0 mm? f (0mm)
2.3.4 Drehungen in drei Dimensionen
 2.3.4 Drehungen in drei Dimensionen Wir verallgemeinern die bisherigen Betrachtungen nun auf den dreidimensionalen Fall. Für Drehungen des Koordinatensystems um die Koordinatenachsen ergibt sich 1 x 1
2.3.4 Drehungen in drei Dimensionen Wir verallgemeinern die bisherigen Betrachtungen nun auf den dreidimensionalen Fall. Für Drehungen des Koordinatensystems um die Koordinatenachsen ergibt sich 1 x 1
Der Kern-Overhauser-Effekt (Nuclear Overhauser Effect, NOE)
 Der Kern-Overhauser-Effekt (Nuclear Overhauser Effect, NOE) B 2 S I Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten H-Kerns
Der Kern-Overhauser-Effekt (Nuclear Overhauser Effect, NOE) B 2 S I Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten H-Kerns
Aufgabe 1. Die Determinante ist eine lineare Abbildung von C n n nach C? Nein (außer für n = 1). Es gilt det(λa) = (λ) n det(a).
 Aufgabe Die Determinante ist eine lineare Abbildung von C n n nach C? Nein (außer für n = Es gilt det(λa = (λ n det(a det I n = n? Nein (außer für n = Es gilt deti n = det(ab = det A det B? Ja det(a =
Aufgabe Die Determinante ist eine lineare Abbildung von C n n nach C? Nein (außer für n = Es gilt det(λa = (λ n det(a det I n = n? Nein (außer für n = Es gilt deti n = det(ab = det A det B? Ja det(a =
6 NMR von Proteinen. 6.1 Proteine Strukturbestimmung Motivation und Grundlagen
 6.1 Proteine 6.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
6.1 Proteine 6.1.1 Motivation und Grundlagen Proteine gehören zu den wichtigsten Bestandteilen aller lebenden Organismen. Sie stellen den mengenmäßig größten Anteil der Biomoleküle und spielen eine wichtige
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
Studying Invisible Excited Protein States in Slow Exchange with a Major State Conformation
 Studying Invisible Excited Protein States in Slow Exchange with a Major State Conformation JACS 2012 Pramodh Vallurupalli, Guillaume Bouvignies, and Lewis E. Kay MR-Seminar Nina Kubatova 1 13.10.2014 Inhaltverzeichnis
Studying Invisible Excited Protein States in Slow Exchange with a Major State Conformation JACS 2012 Pramodh Vallurupalli, Guillaume Bouvignies, and Lewis E. Kay MR-Seminar Nina Kubatova 1 13.10.2014 Inhaltverzeichnis
Kombinierte Übungen zur Spektroskopie Beispiele für die Bearbeitung
 Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Kernmagnetismus und Magnetfelder
 Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Vorbereitung. µ z = mγ h (1) γ = gq 2m wobei q die Ladung und m die Masse des Teilchens beschreiben.
 Physikalisches Fortgeschrittenenpraktikum NMR-Spektroskopie Vorbereitung Armin Burgmeier Robert Schittny 1. Theoretische Grundlagen 1.1. Kerndrehimpuls und magnetisches Moment Nach der Quantentheorie besitzt
Physikalisches Fortgeschrittenenpraktikum NMR-Spektroskopie Vorbereitung Armin Burgmeier Robert Schittny 1. Theoretische Grundlagen 1.1. Kerndrehimpuls und magnetisches Moment Nach der Quantentheorie besitzt
Inhalt. a) Typische Wechselwirkungen im Festkörper. b) Spektrenform für Einkristalle und Pulver. c) Messung und Interpretation einfacher Systeme
 Inhalt. Grundlagen der FK-NMR-Spektroskopie a) Typische Wechselwirkungen im Festkörper b) Spektrenform für Einkristalle und Pulver c) Messung und Interpretation einfacher Systeme. Wichtige Techniken und
Inhalt. Grundlagen der FK-NMR-Spektroskopie a) Typische Wechselwirkungen im Festkörper b) Spektrenform für Einkristalle und Pulver c) Messung und Interpretation einfacher Systeme. Wichtige Techniken und
Übungsaufgaben NMR-Spektroskopie (1)
 Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Bestimmung der Struktur einer (un)bekannten Verbindung
 Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektroskopie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie neue Produktlinie,
Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektroskopie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie neue Produktlinie,
Anwendung neuerer spektroskopischer Techniken in der pharmazeutischen Chemie
 Anwendung neuerer spektroskopischer Techniken in der pharmazeutischen Chemie (ausgewählte spektroskopische Methoden MR) Wolfgang Holzer Department für Arzneistoffsynthese Fakultät für Lebenswissenschaften,
Anwendung neuerer spektroskopischer Techniken in der pharmazeutischen Chemie (ausgewählte spektroskopische Methoden MR) Wolfgang Holzer Department für Arzneistoffsynthese Fakultät für Lebenswissenschaften,
Die chemische Verschiebung - 1
 Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
Einführung in die NMR-Spektroskopie im Rahmen des Praktikums OC-II
 Einführung in die NMR-Spektroskopie im Rahmen des Praktikums O-II Till Opatz Kerne im statischen Magnetfeld Zeeman-Aufspaltung -1-3/2 Energie -1/2 +1/2 0 +1-1/2 +1/2-3/2 I = 1/2 I = 1 I = 3/2 Insgesamt
Einführung in die NMR-Spektroskopie im Rahmen des Praktikums O-II Till Opatz Kerne im statischen Magnetfeld Zeeman-Aufspaltung -1-3/2 Energie -1/2 +1/2 0 +1-1/2 +1/2-3/2 I = 1/2 I = 1 I = 3/2 Insgesamt
Physikalische Grundlagen der Magnetresonanz-Tomographie MRT
 Physikalische Grundlagen der Magnetresonanz-Tomographie MRT http://www.praxis-nuramed.de/images/mrt_3_tesla.png Seminarvortrag am 30.05.2016 von Nanette Range MRT Bilder Nanette Range 30.05.2016 2 Motivation
Physikalische Grundlagen der Magnetresonanz-Tomographie MRT http://www.praxis-nuramed.de/images/mrt_3_tesla.png Seminarvortrag am 30.05.2016 von Nanette Range MRT Bilder Nanette Range 30.05.2016 2 Motivation
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
4. Verzerrungen. Der Abstand von zwei Punkten ändert sich. Der Winkel zwischen drei Punkten ändert sich
 4. Verzerrungen Wird ein Körper belastet, so ändert sich seine Geometrie. Die Punkte des Körpers ändern ihre Lage. Sie erfahren eine Verschiebung. Ist die Verschiebung für benachbarte Punkte unterschiedlich,
4. Verzerrungen Wird ein Körper belastet, so ändert sich seine Geometrie. Die Punkte des Körpers ändern ihre Lage. Sie erfahren eine Verschiebung. Ist die Verschiebung für benachbarte Punkte unterschiedlich,
Edelgas-polarisierte. NMR- Spektroskopie. Jonas Möllmann Jan Mehlich. SoSe 2005
 Edelgas-polarisierte NMR- Spektroskopie Jonas Möllmann Jan Mehlich SoSe 2005 NMR Prinzip Aufspaltung der Kernspins in verschiedene Niveaus durch angelegtes Magnetfeld Messung des Besetzungs- unterschiedes
Edelgas-polarisierte NMR- Spektroskopie Jonas Möllmann Jan Mehlich SoSe 2005 NMR Prinzip Aufspaltung der Kernspins in verschiedene Niveaus durch angelegtes Magnetfeld Messung des Besetzungs- unterschiedes
Übersicht 13 C-NMR-Spektroskopie
 Üersicht 13 C-NMR-Spektroskopie Intensität / Integrl Chemische Verschieung Kopplung / Multipliität nlog 1 -NMR, er weniger empfindlich wichtige Experimente off-resonn-entkopplung Breitndentkopplung Polristionstrnsfer
Üersicht 13 C-NMR-Spektroskopie Intensität / Integrl Chemische Verschieung Kopplung / Multipliität nlog 1 -NMR, er weniger empfindlich wichtige Experimente off-resonn-entkopplung Breitndentkopplung Polristionstrnsfer
Das Welcome-Kit soll neuen Institutsangehörigen helfen, vom NMR-Service am Institut besser zu profitieren.
 NMR-Laboratorium des Instituts für Chemie Universität Zürich Irchel, Winterthurerstrasse 190, 8057 Zürich Welcome-Kit Das Welcome-Kit soll neuen Institutsangehörigen helfen, vom NMR-Service am Institut
NMR-Laboratorium des Instituts für Chemie Universität Zürich Irchel, Winterthurerstrasse 190, 8057 Zürich Welcome-Kit Das Welcome-Kit soll neuen Institutsangehörigen helfen, vom NMR-Service am Institut
Anwendung von künstlichen neuronalen Netzen in der Analyse zweidimensionaler NMR-Spektren
 Anwendung von künstlichen neuronalen Netzen in der Analyse zweidimensionaler NMR-Spektren Dissertation zur Erlangung des Doktorgrades des Fachbereichs Chemie der Universität Hamburg von Christian Seeberger
Anwendung von künstlichen neuronalen Netzen in der Analyse zweidimensionaler NMR-Spektren Dissertation zur Erlangung des Doktorgrades des Fachbereichs Chemie der Universität Hamburg von Christian Seeberger
Zusammenfassung des Seminarsvortrags Nuclear magnetic resonance
 Zusammenfassung des Seminarsvortrags Nuclear magnetic resonance Andreas Bünning 9. Januar 2012 Betreuer: Dr. Andreas Thomas Seite 1 3 PHYSIKALISCHE GRUNDLAGEN 1 Motivation Die nuclear magnetic resonance,
Zusammenfassung des Seminarsvortrags Nuclear magnetic resonance Andreas Bünning 9. Januar 2012 Betreuer: Dr. Andreas Thomas Seite 1 3 PHYSIKALISCHE GRUNDLAGEN 1 Motivation Die nuclear magnetic resonance,
1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie
 Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
Pharmazeutische Chemie
 Pharmazeutische Chemie PROTEINSTRUKTUREN UND NMR SPEKTROSKOPIE Reto Bader Mirjam Lerch Dr.Oliver Zerbe Department Angewandte Biowissenschaften Institut für Pharmazeutische Wissenschaften Sommersemester
Pharmazeutische Chemie PROTEINSTRUKTUREN UND NMR SPEKTROSKOPIE Reto Bader Mirjam Lerch Dr.Oliver Zerbe Department Angewandte Biowissenschaften Institut für Pharmazeutische Wissenschaften Sommersemester
2D-NMR- Spektroskopie
 2. 2D-NMR-Spektroskopie 2D-NMR- Spektroskopie Organische Chemie Dr. I. Kempter - 28 - 2. 2D-NMR-Spektroskopie Überblick Der Einsatz von zweidimensionalen ermöglicht es die Nachteile eines eindimensionalen
2. 2D-NMR-Spektroskopie 2D-NMR- Spektroskopie Organische Chemie Dr. I. Kempter - 28 - 2. 2D-NMR-Spektroskopie Überblick Der Einsatz von zweidimensionalen ermöglicht es die Nachteile eines eindimensionalen
Mathematische Probleme, SS 2015 Montag $Id: quadratisch.tex,v /06/22 12:08:41 hk Exp $
 Mathematische Probleme, SS 15 Montag 6 $Id: quadratischtex,v 111 15/06/ 1:08:41 hk Exp $ 4 Kegelschnitte 41 Quadratische Gleichungen In der letzten Sitzung hatten wir die Normalform (1 ɛ )x + y pɛx p =
Mathematische Probleme, SS 15 Montag 6 $Id: quadratischtex,v 111 15/06/ 1:08:41 hk Exp $ 4 Kegelschnitte 41 Quadratische Gleichungen In der letzten Sitzung hatten wir die Normalform (1 ɛ )x + y pɛx p =
Research Collection. Pharmazeutische Chemie Sommersemester Educational Material. ETH Library
 Research Collection Educational Material Pharmazeutische Chemie Sommersemester 2001 Author(s): Bader, Reto; Lerch, Mirjam; Zerbe, Oliver Publication Date: 2001 Permanent Link: https://doi.org/10.3929/ethz-a-004337686
Research Collection Educational Material Pharmazeutische Chemie Sommersemester 2001 Author(s): Bader, Reto; Lerch, Mirjam; Zerbe, Oliver Publication Date: 2001 Permanent Link: https://doi.org/10.3929/ethz-a-004337686
NMR-Methoden zur chiralen Erkennung
 Spektroskopie in der rganischen hemie NMR-Methoden zur chiralen Erkennung Mit Ausnahme der D-Spektroskopie (D = irculardichroismus) sind alle spektroskopischen Methoden auch die NMR achiral, d.h. sie können
Spektroskopie in der rganischen hemie NMR-Methoden zur chiralen Erkennung Mit Ausnahme der D-Spektroskopie (D = irculardichroismus) sind alle spektroskopischen Methoden auch die NMR achiral, d.h. sie können
4.9.7 Konstruktion der Suffixbäume
 .9.7 Konstruktion der Suffixbäume Beipiel: xabxa (siehe Abbildung.27) Man beginnt mit der Konstruktion eines Suffixbaumes für gesamten String und schreibt eine 1 am Blatt, weil der Suffix xabxa an der
.9.7 Konstruktion der Suffixbäume Beipiel: xabxa (siehe Abbildung.27) Man beginnt mit der Konstruktion eines Suffixbaumes für gesamten String und schreibt eine 1 am Blatt, weil der Suffix xabxa an der
Spinsysteme und skalare Kopplung
 Spinsysteme und skalare Kopplung Ein Spin-1/2-Kern X ( 1 oder 13 C) kann zwei Energieniveaus mit einem gegebenen Energieunterschied ΔE besetzen (Grundzustand 1/2 bzw. α und angeregter Zustand +1/2 bzw.
Spinsysteme und skalare Kopplung Ein Spin-1/2-Kern X ( 1 oder 13 C) kann zwei Energieniveaus mit einem gegebenen Energieunterschied ΔE besetzen (Grundzustand 1/2 bzw. α und angeregter Zustand +1/2 bzw.
Übungsblatt 1: Lösungswege und Lösungen
 Übungsblatt : Lösungswege und Lösungen 5..6 ) Hier geht es weniger um mathematisch-strenge Beweise als darum, mit abstrakten Vektoren ohne Komponenten) zu hantieren und damit die Behauptungen plausibel
Übungsblatt : Lösungswege und Lösungen 5..6 ) Hier geht es weniger um mathematisch-strenge Beweise als darum, mit abstrakten Vektoren ohne Komponenten) zu hantieren und damit die Behauptungen plausibel
Transformation von Gauß-Krüger(GK)- Koordinaten des Systems MGI in Universal Transversal Mercator(UTM)- Koordinaten des Systems ETRS89
 Transformation von Gauß-Krüger(GK)- Koordinaten des Systems MGI in Universal Transversal Mercator(UTM)- Koordinaten des Systems ETRS89 1. Inhaltsverzeichnis 1. Inhaltsverzeichnis...2 2. Leitfaden...3 3.
Transformation von Gauß-Krüger(GK)- Koordinaten des Systems MGI in Universal Transversal Mercator(UTM)- Koordinaten des Systems ETRS89 1. Inhaltsverzeichnis 1. Inhaltsverzeichnis...2 2. Leitfaden...3 3.
