Molekularbiologisches Praktikum Versuch in vitro Mutagenese
|
|
|
- Lorenz Graf
- vor 6 Jahren
- Abrufe
Transkript
1 Molekularbiologisches Praktikum Versuch in vitro Mutagenese Der Versuch startet am ersten Versuchstag um 9:00 mit einem schriftlichen Antestat im Raum NC5/174
2 In vitro Mutagenese Prof. Dr. B. Hovemann Antestat Unmittelbar vor Beginn des Versuches muss von jeder Teilnehmerin und jedem Teilnehmer ein Antestat abgelegt werden. Dafür wird vorausgesetzt, dass die theoretischen Hintergründe beherrscht werden und der prinzipielle, praktische Ablauf des Versuches bekannt ist. Bei groben Wissenslücken müssen die Teilnehmerin oder der Teilnehmer vom Versuchstag ausgeschlossen werden. Es sei hier explizit darauf hingewiesen, dass diese Versuchsbeschreibung keine vollständige Darstellung aller zugrunde liegenden biochemischen und molekularbiologischen Hintergründe leisten soll. Neben dieser Versuchsbeschreibung wird deshalb die Kenntnis des Skriptes zur Vorlesung Molekulargenetische Methoden in der Biochemie -- SS 2013 (VL-Nr ) von Prof. Dr. Hovemann, sowie des Skriptes GFP Fluoreszierende Proteine vorausgesetzt. Im Antestat werden Kenntnisse zu den Themen Eigenschaften von DNA Chromophorbildung bei fluoreszierenden Proteinen Mutageneseverfahren, speziell QuikChange-Verfahren Native PAGE vs. SDS-PAGE, Polymerisation von Gelen Proteinexpression in Bakterienkulturen Proteinisolierung durch Affinitätschromatographie Gefahrstoffe in diesem Versuch und der Umgang mit ihnen erwartet. gez. B. Hovemann, die Praktikumsbetreuer
3 in vitro Mutagenese Molekularbiologisches Praktikum 5. Semester AG Hovemann 1. Versuchstag in vitro Mutagenese Proteinexpression dsred-expressoder K83M- Vektor Mutagenese durch PCR Agarose-Gel herstellen dsred-his oder dsred-his K83M Klone Einzelkolonie Transformationskontrolle DpnI-Verdau der Ausgangs- DNA Aliquot 50 ml LBamp 200 -Kulturen Aliquot Agarose-Gelelektrophorese Bis OD 600=0,6 wachsen lassen Kompetente NovaBlue Zellen herstellen Transformation Induktion mit IPTG LB-amp IPTG-Platten herstellen Bakterienwachstum über Nacht Proteinexpression über Nacht 2. Versuchstag Auswertung Bestimmung der Transformationsrate aus dem Kontrollansatz Kontrolle der Mutagenese Proteinisolierung Ni-Säule äquilibrieren Bakterienlyse Lysat 5 ml Flüssigkulturen direkt mit IPTG induzieren UV-Lampe Ni-Säulen- Affinitätschromatographie Acrylamid-Gel herstellen Native Acrylamid-Gelelektrophorese Durchlauf, Wasch- und Elutionsfraktionen über Nacht wachsen lassen 3. Versuchstag Gel direkt einscannen Fraktionen einscannen Kulturen fotographieren Blot einscannen Panceau S - Färbung Western- Blot
4 Die in vitro Mutagenese gehört zu den wichtigen Methoden der Molekularbiologie, da sie das gezielte Modifizieren von Gensequenzen ermöglicht. Damit ist man nicht mehr auf ungerichtete Mutations-Ereignisse angewiesen ist, wie dies bei in vivo Mutagenese Methoden (Röntgenstrahlung, chemische Reagenzien) der Fall ist. Eingesetzt wird die in vitro Mutagenese häufig für die Untersuchung essentieller Proteinregionen, z. B. katalytischer Domänen und Co-Faktor- Bindestellen. Ziel ist es dabei, einzelne Aminosäuren dieser Regionen aus zu tauschen und die Auswirkung auf die Proteinaktivität zu bestimmen. Die im Versuch eingesetzte Methode ist das QuikChange-Verfahren. Bei diesem Verfahren wird eine Punktmutation durch eine PCR-ähnliche Methode (PCR-Zyklus Bedingungen, jedoch ohne exponentiellen Produktanstieg Warum?) direkt in das klonierte Gen eingeführt. Der Einfachheit halber wird diese im weiteren Verlauf des Skriptes trotzdem als PCR bezeichnet. Das Gen befindet sich in einem Plasmid, das aus dam + E. coli präpariert worden ist. Anschließend wird die DNA des unveränderten Ausgangsplasmids durch die methylierungsabhängige Restriktion mit DpnI zerstört. Das neusynthetisierte, nicht methylierte Plasmid mit der veränderten Gensequenz bleibt erhalten und wird in einen geeigneten Bakterienstamm transformiert (siehe Abbildung).
5 Im Praktikumsversuch wird eine in vitro Mutagenese des rot fluoreszierenden dsred-express- Proteins durchgeführt (siehe auch: GFP - Fluoreszierende Proteine). Durch den Austausch des Lysins an Position 83 gegen Methionin (K83M Mutante) wird der Rotanteil des Emissionsspektrums des Proteins verändert, so dass das Protein anschließend lila fluoresziert. Ebenso kann durch die Rückmutation (M83K) das wildtypische Emissionsspektrum wieder hergestellt werden. Die Farbveränderung ist in Bakterienkolonien nach Ausbildung des Chromophors sichtbar. Dieser Prozess dauert einige Stunden. Das Ergebnis des Experiments lässt sich so nach einigen Stunden direkt auf der Agarplatte beurteilen. Versuchstag 1 1. Herstellung kompetenter NovaBlue Bakterien a) Reagenzien: TB(transformation buffer), ph 6,7 Für 250 ml 15 mm 250 mm 10 mm ph-wert von 55 mm CaCl 2 2 H 2 O KCl PIPES 6,7 mit 5 N KOH MnCl 2 4 H 2 O 0,756 g 0,55 g 4,66 g einstellen 2,72 g auf 250 ml LB(lysogeny broth)-medium Tetracyclin-Stocklösung 5 g Hefeextrakt 12,5 mg/ml Tetracyclin 2 g MgCl 2 2 H 2 O in EtOH (abs.) 5 g NaCl 10 g Pepton in 1 l b) Durchführung: Kompetente NovaBlue Bakterien 50 ml frisches LB-tet 25 -Medium werden mit 1,5 ml einer vorbereiteten über Nacht Kultur angeimpft und bei 37 C und 240 rpm im Schüttler bis zu einer OD 600 von 0,5 bis 0,6 wachsen gelassen (viertelstündlich kontrollieren!). Jede Gruppe nimmt sich 10 ml Kultur in ein 15 ml Röhrchen ab und kühlt die Zellen für 10 Minuten im
6 Eis/Wasser-Bad. (Um eine möglichst hohe Kompetenz der Zellen zu erhalten, müssen die Zellen ab diesem Zeitpunkt möglichst auf Eis gehalten werden und die Zeiten dazwischen, z. B. beim Zentrifugieren, müssen minimiert werden!) Die Bakteriensuspension wird bei 4 C in einer Tischzentrifuge 1 Minute bei rpm (1.700 g) pelletiert. Nach der Zentrifugation, werden die Bakterien in 2,4 ml eiskaltem TB-Puffer resuspendiert und die Suspension 10 Minuten auf Eis inkubiert. Es wird wiederum 1 Minute bei 4 C und rpm zentrifugiert, das Pellet in 340 µl TB-Puffer resuspendiert und die Suspension dann auf zwei Reaktionsgefäße aufgeteilt. Nun werden je 11,9 µl DMSO zugegeben, gemischt und die Zellen bis zur Verwendung im Eis/Wasser-Bad gelagert (mindestens 10 min). 2. Animpfen der Expressionskulturen a) Reagenzien: LB-Medium 1 M IPTG-Stocklösung 40 mg/ml Carbenecillin-Stocklösung b) Durchführung: 50 ml LB-carb 40 -Medium werden mit einer vorbereiteten über Nacht Kultur auf eine OD 600 von etwa 0,1 angeimpft und bei 37 C und 240 rpm bis zu einer OD 600 von 0,5 bis 0,6 wachsen gelassen. Anschließend wird mit 50 µl 1 M IPTG (1 mm Endkonzentration) die Proteinexpression über Nacht bei 37 C im Schüttler induziert. 3. in vitro Mutagenese a) Reagenzien: 10 Pfu Polymerase-Puffer 50 ng/µl Plasmid-Lösung (pdsred-express oder pdsred-express K83M) dntp-mix (je 10 mm pro Nukleotid) 2,5 U/µl Pfu DNA-Polymerase 10 U/µl FastDigest DpnI
7 TBE(TRIS-Borat-EDTA)-Puffer, ph 8,0 1 l Stocklösung (50 ) 1 mm 40 mm EDTA TRIS/Acetat 100 ml 0,5 M EDTA 242 g TRIS 57,1 ml Eisessig auf 1 l mit >> ph 8,0 SOB(super optimal broth)-medium SOC(SOB with catabolite repression)-medium 5 g 2,5 mm 10 mm 8,6 mm 20 g in Hefe-Extrakt KCl MgCl 2 NaCl Pepton 1 l 20 mm Glukose in SOB-Medium Ethidiumbromid-Stocklösung 10 mg/ml in Ethidiumbromid b) Verwendete Primer: Wildtyp zu Mutante (K83M): K83M forward: K83M reverse: 5 -CGACATCCCCGACTACATGAAGCTGTCCTTCCCCGA-3 5 -TCGGGGAAGGACAGCTTCATGTAGTCGGGGATGTCG-3 Mutante zu Wildtyp (M83K, entspricht pdsred-express): M83K forward: M83K reverse: 5 -CGACATCCCCGACTACAAGAAGCTGTCCTTCCCCGAGG-3 5 -CCTCGGGGAAGGACAGCTTCTTGTAGTCGGGGATGTCG-3
8 c) Durchführung: Der PCR-Ansatz wird nach folgendem Schema pipettiert: PCR-Ansatz: 40 µl 5 µl 1 µl 1 µl 1 µl 1 µl dann 1 µl 10 Pfu Polymerase-Puffer mit MgSO 4 Plasmid-Lösung (entspricht 50 ng) 50 µm Primer forward 50 µm Primer reverse dntp-mix Pfu DNA Polymerase Anschließend erfolgt die PCR nach folgendem Programm: PCR-Programm: Vorbehandlung 2 Minuten bei 95 C 12 Zyklen mit 30 Sekunden bei 95 C 1 Minute bei 55 C 7 Minuten bei 72 C Denaturierung Annealing Elongation (2 min/kb) Nachbehandlung 10 Minuten bei 72 C LB-amp IPTG-Platten Agarose-Gel Während die PCR läuft, werden drei zur Selektion transformierter Bakterien benötigte LB-carb 40 -IPTG-Platten hergestellt. Dazu werden in der Mikrowelle 1,5 % (w/v) Agar-Agar in 100 ml LB-Medium geschmolzen (nicht überkochen lassen), nach Abkühlen auf ca. 60 C mit 200 µl Carbenicillin-Stocklösung und 100 µl IPTG-Stocklösung versetzt und in Schalen gegossen. Nach dem Erstarren werden die Platten markiert und zum Trocknen in den 37 C Brutschrank gegeben. Da sowohl PCR als auch DpnI-Verdau auf einem Agarose-Gel analysiert werden sollen, wird auch dieses während die PCR läuft hergestellt. Dazu wird 1 % (w/v) Agarose in TBE-Puffer geschmolzen (nicht überkochen lassen!), Ethidiumbromid- Stocklösung mit einer Verdünnung von 1: zugegeben und in die mit einem Kamm versehene Form gegossen.
9 Gefahrenhinweis: Ethidiumbromid ist sehr giftig, mutagen, umweltgefährdend und somit gefährlich für den Laboranten. Deshalb müssen alle Arbeiten mit Ethidiumbromid unter dem Abzug durchgeführt werden. Da die im Laborgebrauch üblichen Latex-Handschuhe von Ethidiumbromid durchdrungen werden können, müssen bei allen Arbeiten Nitril-Handschuhe getragen werden. Mit Ethidiumbromid in Kontakt gekommene Gegenstände und Pufferlösungen müssen in den besonders gekennzeichneten Abfallbehältern entsorgt werden. Zum Überprüfen der PCR wird ein 15 µl Aliquot abgenommen und auf Eis gelagert. Zum restlichen PCR-Ansatz wird 1 µl FastDigest DpnI gegeben und fünf Minuten bei 37 C inkubiert. Vom DpnI-Verdau werden anschließend ebenfalls 15 µl abgenommen und zusammen mit dem PCR-Aliquot durch Gelelektrophorese analysiert. Der Rest (20 µl) wird verwendet, um die hergestellten, kompetenten NovaBlue Bakterien über Hitze-Schock zu transformieren. Als Kontrolle der Transformationseffizienz wird 1 µl des Ausgangsplasmids der PCR (5 ng/µl) in einem getrennten Ansatz transformiert. Für die Transformation werden DNA und Bakterien kurz gemischt und 30 Minuten im Eis/Wasser-Bad inkubiert, bevor der Hitze-Schock durch 30 Sekunden Erwärmen auf 42 C (Wasserbad!) erfolgt. Nach Zugabe von 800 µl eiskaltem SOC- Medium werden die Bakterien für 30 Minuten bei 37 C unter Schütteln wachsen gelassen, bevor sie bei rpm kurz pelletiert werden. Für die in vitro Mutagenese Ansätze wird der Überstand bis auf 200 µl entfernt, das Pellet darin resuspendiert und der gesamte Ansatz auf einer LB-carb 40 -IPTG-Platte ausgestrichen. Für die Kontrollen mit dem geschlossenen Plasmid wird 1/10 des gesamten Ansatzes auf eine Platte ausgestrichen und der Rest bei rpm kurz pelletiert. Der Überstand wird bis auf 200 µl entfernt, das Pellet darin resuspendiert und der gesamte Ansatz auf einer weiteren LB-carb 40 -IPTG-Platte ausgestrichen. Anschließend werden die Platten über Nacht bei 37 C im Brutschrank inkubiert.
10 Versuchstag 2 1. Auswertung der Transformation Zur Bestimmung der Transformationseffizienz der kompetenten Zellen wird die Transformationsrate (Kolonien pro µg DNA) aus den Kontrollansätzen mit pdsred- Express bzw. pdsred-express K83M bestimmt. Dazu werden die Kolonien auf der Platte gezählt und aus der eingesetzten DNA-Menge die Transformationsrate berechnet. Zusätzlich wird aus der nach linearer Amplifikation und vollständigem Verdau des Ausgangsplasmids berechneten DNA-Menge die Transformationsrate der Mutagenese Ansätze bestimmt. Über den Anteil der für die Mutation positiven Klone kann daraus der Mutationserfolg ermittelt werden. 2. Kontrolle der Mutagenese Zum Nachweis der Mutagenese werden die Platten unter UV Licht ausgewertet. Eine Einzelkolonie wird in 5 ml LB-carb 40 -IPTG-Medium resuspendiert und über Nacht bei 37 C unter Schütteln wachsen gelassen.
11 3. Protein-Präparation über Affinitätschromatographie a) Geräte: Microfluidizer b) Reagenzien: Protino Ni-TED 150 Säulen 8 LEW(lysis-equilibration-wash)-Puffer 4 Elutionspuffer c) Durchführung: Die am Vortag angeimpften Expressionskulturen werden in einer Kühlzentrifuge pelletiert (4.500 g, 10 min und 4 C), in 20 ml 1 LEW-Puffer resuspendiert und auf
12 Eis aufbewahrt. Mittels eines Microfluiziders werden die Bakterienzellen aufgeschlossen. Anschließend erfolgt eine Zentrifugation bei rpm (SS34-Rotor) und 4 C für 20 Minuten, um die Bakterienreste zu pelletieren. Der Überstand wird in ein 50 ml Falkon überführt und auf Eis aufbewahrt. Während die Zellreste pelletiert werden, wird die Protino Säule mit 1 LEW-Puffer äquilibriert. Dazu wird 320µl 1 LEW-Puffer auf die Säulen gegeben und der Durchlauf verworfen. Nachdem die Säule äquilibriert wurde, wird das geklärte Lysat auf die Säule gegeben. Der Durchlauf wird in einem 50 ml Röhrchen aufgefangen! Nachdem das Lysat durchgelaufen ist, wird die Säule zwei Mal mit je 320µl 1 LEW-Puffer gewaschen und diese beiden Waschfraktionen separat aufgefangen. Anschließend wird mit drei Mal je 240µl 1 Elutionspuffer eluiert. Dabei werden jeweils 1 ml Fraktionen für die Elektrophorese in Reaktionsgefäßen aufgefangen und für die Auswertung zusammen mit dem Durchlauf und den Waschfraktionen eingescannt. 4. Native Polyacrylamid-Gelelektrophorese a) Reagenzien: Wassergesättigtes Butanol 10 % (v/v) Essigsäure Upper-TRIS (nativ) Lower TRIS (nativ) 0,5 M TRIS/HCl, ph 6,8 1,5 M TRIS/HCl, ph 8,8 in in Sammelgel (4 %) Trenngel (10 %) 10,5 ml 15 ml 2 ml Rotiphorese Gel 30 5 ml Lower-TRIS 2,5 ml Upper-TRIS 10 ml Rotiphorese Gel µl 10 % (w/v) APS-Lösung 300 µl 10 % (w/v) APS-Lösung 15 µl TEMED 30 µl TEMED
13 Stopfgel Probenpuffer (5 ) 1 % (w/v) Agarose 0,1 % (w/v) Bromphenolblau 16,7 % (v/v) Lower-TRIS (nativ) 25 % (v/v) Glycerin in 60 mm TRIS/HCl, ph 6,8 in Laufpuffer (nativ) PanceauS - Lösung 192 mm Glycin 0,2 %(v/v) PanceauS 25 mm TRIS/HCl, ph 8,8 5 % (v/v) Essigsäure in in Gefahrenhinweise: Unpolymerisiertes Acrylamid ist krebserregend und ein starkes Nervengift. Gefährlich sind vor allem das Verschlucken und die Berührung mit der Haut, daher müssen alle Arbeiten mit Acrylamid (auch den polymerisierten Gelen) mit Handschuhen durchgeführt werden. b) Durchführung: Polyacrylamid-Gel Es werden native diskontinuierliche Gele mit einem 4 %igen Sammelgel und einem 10 %igen Trenngel verwendet. Zum Gießen wird zunächst das Trenngel vorbereitet (APS und TEMED jedoch erst unmittelbar vor dem Gießen zugeben!) und luftblasenfrei in die mit Stopfgel abgedichtete Kammer gefüllt, wobei zum unteren Ende des Kamms mindestens 0,5 cm freibleiben müssen. Während der Polymerisation wird das Trenngel mit 200 µl wassergesättigtem Butanol überschichtet, da diese durch Luftsauerstoff gestört wird. Nach dem Polymerisieren des Trenngels (durch vorsichtiges Kippen der Kammer testen), wird das Butanol abgegossen und das Sammelgel gegossen. Dieses kann schon während der Polymerisation des Trenngels vorbereitet werden (APS und TEMED jedoch erst unmittelbar vor dem Gießen zugeben!). Um ein vollständiges Polymerisieren des Sammelgels zu gewährleisten, ist es wichtig, dass der Kamm so in die Kammer eingeführt wird, dass keine Luftblasen eingeschlossen werden. Dies gelingt am besten, wenn man den Kamm leicht schräg hält. Wenn die Polymerisation des Sammelgels abgeschlossen ist, wird die Kammer mit Laufpuffer gefüllt und erst dann der Kamm entfernt.
14 Versuchstag 3 Jeweils 20 µl der Proben aus den Fraktionen der Proteinisolierung werden vor dem Auftragen mit 5 Probenpuffer versetzt und dann aufgetragen. Während sich die Proben im Sammelgel befinden, wird eine Spannung von 8 V/cm angelegt. Die Spannung wird bei Eintritt der Proben in das Trenngel auf 12 V/cm erhöht. Nach Abschluss der Elektrophorese (Bromphenolblaubande am unteren Ende des Gels) wird das Trenngel vom Sammel- und Stopfgel getrennt und eingescannt (fotographiert). Anschließend wird die Proteintrennung mit einem Semi-Dry Western Blot Verfahren auf Nitrocellulose übertragen und mit PanceauS-Färbung angefärbt. Diese Färbung wird dokumentiert (Einscannen). Der dritte Versuchstag dient der Auswertung der Experimente vom Vortag. Dazu werden 1,5 ml der 5 ml Expressionskulturen aus der in vitro Mutagenese in Reaktionsgefäße überführt, die Zellen sedimentiert (1 min, rpm) und eingescannt.
15
16
17
18
19
20 Formblatt Z AUFZEICHNUNGEN ÜBER GENTECHNISCHE ARBEITEN NACH GENTAUFZV (V. 1.1) Aufzeichnungen sollen den Weg eines GVO von der Erzeugung über die Verwendung, Vermehrung, Lagerung bis zur Vernichtung transparent dokumentieren und ermöglichen, dass die gentechnischen Arbeiten auch nach Abschluss der Arbeiten nachvollzogen werden können. Bei einem vollständig ausgefüllten Formblatt werden die Laborbücher nicht mehr als Aufzeichnungsbestandteil benötigt. Die Aufzeichnungen sind jeweils zeitnah zur Erzeugung der GVO zu erstellen. Die Aufzeichnungen dürfen weder durch Streichungen noch auf andere Weise unleserlich gemacht werden. Es dürfen keine Veränderungen vorgenommen werden, die nicht erkennen lassen, ob sie bei der ursprünglichen Eintragung oder erst später vorgenommen worden sind. Aufzeichnungen können auch auf elektronischem Weg geführt werden, doch dann ist ein regelmäßiger Ausdruck erforderlich. (Hinweis: Bei gentechnische Arbeiten im Produktionsbereich sowie bei S3- u. S4-Arbeiten und Freisetzungen sind zusätzliche Aufzeichnungen nach 2 Abs. 3-5 GenTAufzV erforderlich.) 1. Name und Anschrift des Betreibers: 2. Lage der gentechnischen Anlage: 3. Namen der Projektleiter: 4. Namen der Beauftragten für die Biologische Sicherheit: 5. Ab Sicherheitsstufe 2: Bei Umgang mit humanpathogenen Organismen Nennung der Personen, die in der gentechnischen Anlage tätig sind: 6. Thema der Arbeit Die Arbeiten wurden bereits in dem Zulassungsverfahren Az.: beschrieben. Die dabei ausgefüllten Formblätter und die Sicherheitseinstufung der Genehmigungsbehörde (siehe Zulassungsbescheid) sind als Bestandteil der Aufzeichnungen beigefügt. Es handelt sich um weitere Arbeiten der Sicherheitsstufe 1, die nicht in einem Zulassungsverfahren beschrieben wurden. Eine Projektbeschreibung und Risikobewertung folgt unter Ziffer Sicherheitsstufe der Arbeit: Anlagen (für alle GVO der Tabelle unter Ziffer 12 erforderlich): Karten der Vektoren Ausführliche Darstellung und Charakterisierungen des Inserts/Konstrukts/GVOs Durch das Ankreuzen wird bestätigt, dass diese Unterlagen vorliegen und Bestandteil der Aufzeichnungen sind. 9. Zeitpunkt des Beginns und Abschlusses der gentechnischen Arbeit: Beginn: Abschluss (nach vollständiger Entsorgung der GVO): 10. Aufbewahrungsfristen (gemäß 4 GenTAufzV): S1 bis zum (10 Jahre nach vollständiger Entsorgung der GVO): (Datum) S2, S3, S4 bis zum (30 Jahre nach vollständiger Entsorgung der GVO): (Datum) Aktenzeichen des Bescheides / Nr. der gentechnischen Anlage:
21 - 2 - Formblatt Z 11.a Beschreibung des Projektes, der Zielsetzung und der dazugehörigen Arbeitsschritte 11.b Risikobewertung Hierbei handelt es sich um eine konkrete Bewertung der verwendeten Organismen und übertragenen Gene eines Projektes, durchzuführen vor Aufnahme der Arbeit und in regelmäßigen Abständen. [weitere Hilfestellung/Kriterien siehe Anhang I zur GenTSV] Verwendete Spenderorganismen und deren Risikogruppen: Gefährdungspotentiale der übertragenen Nukleinsäuren: Verwendete Vektoren: Verwendete Empfängerorganismen und deren Risikogruppen: Erzeugte GVO und deren Risikogruppen: Datum und Unterschrift der Projektleiterin bzw. des Projektleiters Aktenzeichen des Bescheides / Nr. der gentechnischen Anlage:
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS
 Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Gentechnologie: Isolierung und Charakterisierung von DNA
 Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
SDS Polyacrylamidgelelektrophorese (SDS-PAGE) Mini-Gelträger nach Anleitung zusammenbauen. Saubere Handschuhe tragen!!!
 aktualisiert, 08.03.2011, Wera Roth1 SDS Polyacrylamidgelelektrophorese (SDS-PAGE) Anleitung für Minigele Mini-Gelträger nach Anleitung zusammenbauen. Saubere Handschuhe tragen!!! Glasscheiben ordentlich
aktualisiert, 08.03.2011, Wera Roth1 SDS Polyacrylamidgelelektrophorese (SDS-PAGE) Anleitung für Minigele Mini-Gelträger nach Anleitung zusammenbauen. Saubere Handschuhe tragen!!! Glasscheiben ordentlich
Molekulare Klonierung Praktikum
 Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014
 Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014 Tag 1 PCR Die Polymerase-Kettenreaktion (engl. polymerase chain reaction) ermöglicht die selektive
Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014 Tag 1 PCR Die Polymerase-Kettenreaktion (engl. polymerase chain reaction) ermöglicht die selektive
GEBRAUCHSANLEITUNG. Glutatione Agarose Resin
 GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers (4) Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Proteinreinigung Techniken & Methoden der Proteinreinigung
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers (4) Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Proteinreinigung Techniken & Methoden der Proteinreinigung
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
3 GFP green fluorescent protein
 SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
Plasmidpräparation aus Bakterien Inhalt
 Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
SCRIPTUM HIGH PRECISE
 Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
Gentechnologie: Klonierung und Transformation von DNA
 Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila
 Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
F-I Molekulare Zoologie: Teil I: Expressionsanalysen. Expressionsanalyse mittels RT-PCR
 F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
6.3 Arbeiten mit Proteinen
 6 Methoden 47 6.3 Arbeiten mit Proteinen 6.3.1 Außenmembranproteinpräparation Um die Lokalisierung der Autotransporterproteine zu überprüfen, müssen die einzelnen Kompartimente der Bakterienzelle voneinander
6 Methoden 47 6.3 Arbeiten mit Proteinen 6.3.1 Außenmembranproteinpräparation Um die Lokalisierung der Autotransporterproteine zu überprüfen, müssen die einzelnen Kompartimente der Bakterienzelle voneinander
Heterologe Expression und Aufreinigung von SEPALLATA3 aus Escherichia coli
 1 Heterologe Expression und Aufreinigung von SEPALLATA3 aus Escherichia coli Organisatorisches: Termine: 24.10.2014; 7.11.2014, 14.11.2014 Beginn: 8.15 Uhr im Seminarraum 124, Philosophenweg 12 Am Beginn
1 Heterologe Expression und Aufreinigung von SEPALLATA3 aus Escherichia coli Organisatorisches: Termine: 24.10.2014; 7.11.2014, 14.11.2014 Beginn: 8.15 Uhr im Seminarraum 124, Philosophenweg 12 Am Beginn
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
F-I Molekulare Zoologie: Teil II: Expressionsanalysen. Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse
 F-I Molekulare Zoologie: Teil II: Expressionsanalysen Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse Inhalt: Seite I. Allgemeines 1 II. Durchführung der Elektrophorese
F-I Molekulare Zoologie: Teil II: Expressionsanalysen Proteinexpressionsanalyse mittels SDS-Polyacrylamidgelelektrophorese und Western Blot Analyse Inhalt: Seite I. Allgemeines 1 II. Durchführung der Elektrophorese
Protokoll Praktikum für Humanbiologie Studenten
 Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Kapillarelektrophorese DNA-Sequenzierung
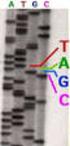
 Kapillarelektrophorese DNA-Sequenzierung DNA Kettenanalyse oder DNA-Sequenzierung wird bei der Anordnung der Primärstruktur und Bestimmung der Nukleotid-Basensequenz verwendet. Die Analyse basiert auf
Kapillarelektrophorese DNA-Sequenzierung DNA Kettenanalyse oder DNA-Sequenzierung wird bei der Anordnung der Primärstruktur und Bestimmung der Nukleotid-Basensequenz verwendet. Die Analyse basiert auf
3 METHODEN. 3.1 DNA-Techniken
 3 METHODEN 3.1 DNA-Techniken 3.1.1 Isolierung von DNA Die Isolierung von Plasmid-DNA im analytischen Maßstab erfolgte nach der Methode von Holmes & Quigley (1981). Der QIAprep Spin Miniprep Kit (Kap. 2.7)
3 METHODEN 3.1 DNA-Techniken 3.1.1 Isolierung von DNA Die Isolierung von Plasmid-DNA im analytischen Maßstab erfolgte nach der Methode von Holmes & Quigley (1981). Der QIAprep Spin Miniprep Kit (Kap. 2.7)
Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele
 Versuch 1: Restriktionsenzyme als molekulare Werkzeuge Versuchsinhalt Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele Zwei
Versuch 1: Restriktionsenzyme als molekulare Werkzeuge Versuchsinhalt Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele Zwei
Modul 4 SS 2015. Western Blot. Tag 1: Proteinbestimmung, SDS-PAGE-Gel-Herstellung S. 3. Tag 2: Gelelektrophorese, Western Blot, Blockierung S.
 Modul 4 SS 2015 Western Blot Tag 1: Proteinbestimmung, SDS-PAGE-Gel-Herstellung S. 3 Tag 2: Gelelektrophorese, Western Blot, Blockierung S. 6 Tag 3: Detektion der Proteine auf der Membran S. 10 1 Über
Modul 4 SS 2015 Western Blot Tag 1: Proteinbestimmung, SDS-PAGE-Gel-Herstellung S. 3 Tag 2: Gelelektrophorese, Western Blot, Blockierung S. 6 Tag 3: Detektion der Proteine auf der Membran S. 10 1 Über
Genisolierung in 2 Stunden : Die Polymerase-Ketten-Reaktion (PCR)
 PCR Genisolierung in 2 Stunden : Die Polymerase-Ketten-Reaktion (PCR) von Kary B. Mullis entwickelt (1985) eigentlich im Mai 1983 bei einer nächtlichen Autofahrt erstes erfolgreiches Experiment am 16.12.1983
PCR Genisolierung in 2 Stunden : Die Polymerase-Ketten-Reaktion (PCR) von Kary B. Mullis entwickelt (1985) eigentlich im Mai 1983 bei einer nächtlichen Autofahrt erstes erfolgreiches Experiment am 16.12.1983
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
Plasmid DNA purification
 Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
9 Praxis: Proteinbestimmung und proteolytischer Verdau von Bacteriorhodopsin
 9 Praxis: Prteinbestimmung und prtelytischer Verdau vn Bacterirhdpsin 9.1 Quantitative Prteinbestimmung Meistens erflgen die Prteinbestimmungen in Küvetten. Generell gilt hierbei, dass die Küvette im Referenzstrahlengang
9 Praxis: Prteinbestimmung und prtelytischer Verdau vn Bacterirhdpsin 9.1 Quantitative Prteinbestimmung Meistens erflgen die Prteinbestimmungen in Küvetten. Generell gilt hierbei, dass die Küvette im Referenzstrahlengang
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein (1) Plasmidpräparation
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein (1) Plasmidpräparation
Vom Ei zum Proteinkristall. Reinigung und Kristallisation von Lysozym
 Vom Ei zum Proteinkristall Reinigung und Kristallisation von Lysozym Isolierung von Lysozym aus Hühnereiweiß (Protokoll adaptiert von www.biochemie.uni-jena.de/files/praktikum/lysozym.pdf) Einführung in
Vom Ei zum Proteinkristall Reinigung und Kristallisation von Lysozym Isolierung von Lysozym aus Hühnereiweiß (Protokoll adaptiert von www.biochemie.uni-jena.de/files/praktikum/lysozym.pdf) Einführung in
Überproduktion der Taq DNA Polymerase mit rekombinanten E. coli Zellen
 Überproduktion der Taq DNA Polymerase mit rekombinanten E. coli Zellen Versuchsleiter: Bernhard Eikmanns Protokollführung: Karl Varadi Gruppe: 11 Durchführung: 11.11 15.11.2002 Protokoll testiert: WS02
Überproduktion der Taq DNA Polymerase mit rekombinanten E. coli Zellen Versuchsleiter: Bernhard Eikmanns Protokollführung: Karl Varadi Gruppe: 11 Durchführung: 11.11 15.11.2002 Protokoll testiert: WS02
Inhaltsverzeichnis. Polymerase Chain Reaction Theoretischer Hintergrund - 2 -
 Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013
 Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013 Projekt: Zellbiologie: Expression und Reinigung der onkogenen Kinase Abl an der Ecole Polytechnique Fédérale de Lausanne, EPFL
Schlussbericht zur Studienwoche Biologie und Medizin vom 17. 23. März 2013 Projekt: Zellbiologie: Expression und Reinigung der onkogenen Kinase Abl an der Ecole Polytechnique Fédérale de Lausanne, EPFL
1. Proteinnachweis mit Bradford-Farbreagenz
 1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
1. Proteinnachweis mit Bradford-Farbreagenz 96-well-Platte Pipetten (10, 20 und 200 µl) Pipettenspitzen Proteinvorratslösung (1 mg/ml Albumin in destillierten Wasser) Destilliertes Wasser Bradford Farbreagenz
Das grün fluoreszierende Protein (GFP)
 Datum Arbeitsplan 17.10.11 S1 Belehrung, kompetente E. coli Zellen herstellen, PCR GFP 24.10.11 Gelelektrophorese GFP, Vortrag, Gel-Aufreinigung, Konzentrationsbestimmung 31.10.11 Reformationstag 07.11.11
Datum Arbeitsplan 17.10.11 S1 Belehrung, kompetente E. coli Zellen herstellen, PCR GFP 24.10.11 Gelelektrophorese GFP, Vortrag, Gel-Aufreinigung, Konzentrationsbestimmung 31.10.11 Reformationstag 07.11.11
1. PCR Polymerase-Kettenreaktion
 entechnische Verfahren 1. PCR Polymerase-Kettenreaktion Die PCR (engl. Polymerase Chain Reaction) ist eine Methode, um die DNA zu vervielfältigen, ohne einen lebenden Organismus, wie z.b. Escherichia coli
entechnische Verfahren 1. PCR Polymerase-Kettenreaktion Die PCR (engl. Polymerase Chain Reaction) ist eine Methode, um die DNA zu vervielfältigen, ohne einen lebenden Organismus, wie z.b. Escherichia coli
Biochemisches Praktikum SS07, Versuch II: Reinigung eines rekombinanten Proteins
 VERSUCH II: REINIGUNG EINES REKOMBINANTEN PROTEINS AUS ESCHERICHIA COLI Literatur: Einschlägige Biochemie und Genetik Lehrbücher. Sambrook and Russel: Molecular Cloning, 3rd Edition (2001) Prinzip: In
VERSUCH II: REINIGUNG EINES REKOMBINANTEN PROTEINS AUS ESCHERICHIA COLI Literatur: Einschlägige Biochemie und Genetik Lehrbücher. Sambrook and Russel: Molecular Cloning, 3rd Edition (2001) Prinzip: In
Plasmidisolierung. Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern.
 Plasmidisolierung Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern. Was können Sie lernen? Sie lernen eine ringförmige DNA, ein Plasmid, zu isolieren. Mit diesem
Plasmidisolierung Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern. Was können Sie lernen? Sie lernen eine ringförmige DNA, ein Plasmid, zu isolieren. Mit diesem
Praktikumsanleitung: Proteine III Sodium-Dodecyl-Sulfate Polyacrylamid-Gel- Elektrophorese
 Praktikumsanleitung: Proteine III Sodium-Dodecyl-Sulfate Polyacrylamid-Gel- Elektrophorese Lerninhalt: Proteinanalytische Methoden: Elektrophorese, Färbung und Molekulargewichtsbestimmung, Primär-, Sekundär-,
Praktikumsanleitung: Proteine III Sodium-Dodecyl-Sulfate Polyacrylamid-Gel- Elektrophorese Lerninhalt: Proteinanalytische Methoden: Elektrophorese, Färbung und Molekulargewichtsbestimmung, Primär-, Sekundär-,
Praktikum Biochemie Einführung in die Molekularbiologie. Bettina Siebers
 Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Praktikum Biochemie Einführung in die Molekularbiologie Bettina Siebers Rekombinante Expression einer Esterase aus Pseudomonas aeruginosa in E. coli Polyacrylamide Gelelektrophorese (PAGE) Denaturierende
Zur Bedeutung der Aminosäure Histidin für den Verlauf der Intoxikation des Cytotoxins aus Pseudomonas aeruginosa, insbesondere der Oligomerisation
 Zur Bedeutung der Aminosäure Histidin für den Verlauf der Intoxikation des Cytotoxins aus Pseudomonas aeruginosa, insbesondere der Oligomerisation Marita Elisabeth Langewische INHALTSVERZEICHNIS Seite
Zur Bedeutung der Aminosäure Histidin für den Verlauf der Intoxikation des Cytotoxins aus Pseudomonas aeruginosa, insbesondere der Oligomerisation Marita Elisabeth Langewische INHALTSVERZEICHNIS Seite
Fortbildung für Biologen an der Oranienschule
 Fortbildung für Biologen an der Oranienschule Am 28.01.08 fand die erste ganztägige schulinterne Lehrerfortbildung für Biologen an der Oranienschule unter der Leitung von Frau Dr. Wismar und Herrn Bender
Fortbildung für Biologen an der Oranienschule Am 28.01.08 fand die erste ganztägige schulinterne Lehrerfortbildung für Biologen an der Oranienschule unter der Leitung von Frau Dr. Wismar und Herrn Bender
Versuchsanleitung: RFLP als Modell für einen DNA-Fingerprint
 RFLP als Modell für einen DNA-Fingerprint Teil 1: Restriktionsverdau 1.1: Thermoblock / Wasserbad auf 37 C vorheizen 1.2: Puffer Y+/Tango auftauen und auf Eis stellen 1.3: 4 Proben, RSA I und H 2 O demin.
RFLP als Modell für einen DNA-Fingerprint Teil 1: Restriktionsverdau 1.1: Thermoblock / Wasserbad auf 37 C vorheizen 1.2: Puffer Y+/Tango auftauen und auf Eis stellen 1.3: 4 Proben, RSA I und H 2 O demin.
aktualisiert, 10.03.2011, Wera Roth, DE1 WESTERN BLOT
 1 aktualisiert, 10.03.2011, Wera Roth, DE1 WESTERN BLOT 1. Hinweise zu Membranen a. Nitrocellulose b. PVDF (alternativ) 2. Aufbau des Transfers a. Naßblot b. Semi-dry (alternativ) 3. Färben und Dokumentation
1 aktualisiert, 10.03.2011, Wera Roth, DE1 WESTERN BLOT 1. Hinweise zu Membranen a. Nitrocellulose b. PVDF (alternativ) 2. Aufbau des Transfers a. Naßblot b. Semi-dry (alternativ) 3. Färben und Dokumentation
Western Blot. Zuerst wird ein Proteingemisch mit Hilfe einer Gel-Elektrophorese aufgetrennt.
 Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR
 Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR Vorbereitung Lehrer Für jede Arbeitsgruppe werden 550 µl InstaGene-Matrix aliquotiert! Das Tube wird mit IG beschriftet!
Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR Vorbereitung Lehrer Für jede Arbeitsgruppe werden 550 µl InstaGene-Matrix aliquotiert! Das Tube wird mit IG beschriftet!
Warum man nicht schon in der SDS- Page eine Immunfärbung machen kann. Warum bei A-Tailingzyklus die A s nich immer mehr werden
 Molbi Nachklausur 2009 Hier mal so die Fragen die mir noch so einfallen. Also es war gefragt: Warum man nicht schon in der SDS- Page eine Immunfärbung machen kann. Warum bei A-Tailingzyklus die A s nich
Molbi Nachklausur 2009 Hier mal so die Fragen die mir noch so einfallen. Also es war gefragt: Warum man nicht schon in der SDS- Page eine Immunfärbung machen kann. Warum bei A-Tailingzyklus die A s nich
SingleQuant Assay Kit
 GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II
 Arbeitsblatt 1 Analyse von DNA 1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II Bevor Sie anfangen: Alle Reagenzien müssen vor Gebrauch vollständig aufgetaut sein und durchmischt
Arbeitsblatt 1 Analyse von DNA 1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II Bevor Sie anfangen: Alle Reagenzien müssen vor Gebrauch vollständig aufgetaut sein und durchmischt
5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp)
 8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
4. Material und Methoden
 4. Material und Methoden 4.1. Analytik von Proteinen 4.1.1. Proteinbestimmung nach Bradford Die Proben sollten je 2 bis 20 µg Protein enthalten und möglichst frei von Detergentien sein. Sie wurden mit
4. Material und Methoden 4.1. Analytik von Proteinen 4.1.1. Proteinbestimmung nach Bradford Die Proben sollten je 2 bis 20 µg Protein enthalten und möglichst frei von Detergentien sein. Sie wurden mit
Entwicklungsbiologie der Pflanzen biol 117
 Entwicklungsbiologie der Pflanzen biol 117 WS 2015/2016 Prof. Dr. Margret Sauter und Mitarbeiter Inhaltsverzeichnis Versuchsplan der einzelnen Kurstage 3 Seite Versuch 1 Auftrennung von Proteinen über
Entwicklungsbiologie der Pflanzen biol 117 WS 2015/2016 Prof. Dr. Margret Sauter und Mitarbeiter Inhaltsverzeichnis Versuchsplan der einzelnen Kurstage 3 Seite Versuch 1 Auftrennung von Proteinen über
Borrelia burgdorferi s.l.
 BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Kursinhalte der Weiterbildung Molekulare Biotechnologie (MNr.: 237 / 0411 / 2010)
 Kursinhalte der Weiterbildung Molekulare Biotechnologie (MNr.: 237 / 0411 / 2010) Schwerpunkte im Bereich BIOANALYTIK Polyacrylamidelektrophorese von Nukleinsäuren im Vertikalsystem Agarosegelelektrophorese
Kursinhalte der Weiterbildung Molekulare Biotechnologie (MNr.: 237 / 0411 / 2010) Schwerpunkte im Bereich BIOANALYTIK Polyacrylamidelektrophorese von Nukleinsäuren im Vertikalsystem Agarosegelelektrophorese
Produktinformation Saturn-2D REDOX Labeling Kit
 Saturn-2D REDOX Labeling Kit Produktinformation Saturn-2D REDOX Labeling Kit Produkt-Nr. PR34, PR35 NH DyeAGNOSTICS GmbH Weinbergweg 23 D-06120 Halle Deutschland Technischer Support Fon: +49 (0) 345-2799
Saturn-2D REDOX Labeling Kit Produktinformation Saturn-2D REDOX Labeling Kit Produkt-Nr. PR34, PR35 NH DyeAGNOSTICS GmbH Weinbergweg 23 D-06120 Halle Deutschland Technischer Support Fon: +49 (0) 345-2799
6 Anhang Verzeichnis häufig gebrauchter Lösungen und Puffer
 6 Anhang 85 6 Anhang 6.1 Verzeichnis häufig gebrauchter Lösungen und Puffer Alkoholreihe (30%, 70%, 90%, 100% Ethanol) Zur Vereinfachung wurde das käufliche 98,8%- Ethanol als 100%-ig gesetzt. Die entsprechenden
6 Anhang 85 6 Anhang 6.1 Verzeichnis häufig gebrauchter Lösungen und Puffer Alkoholreihe (30%, 70%, 90%, 100% Ethanol) Zur Vereinfachung wurde das käufliche 98,8%- Ethanol als 100%-ig gesetzt. Die entsprechenden
SDS-PAGE - ELEKTROPHORESE
 Arbeitsunterlagen zum Beispiel SDS-PAGE - ELEKTROPHORESE Stand: Oktober 2006 SDS-PAGE 1 Inhaltsverzeichnis Einige wichtige Sicherheitsregeln...3 Grundlagen...4 Isoelektrische Fokussierung (IEF)...4 SDS-PAGE:
Arbeitsunterlagen zum Beispiel SDS-PAGE - ELEKTROPHORESE Stand: Oktober 2006 SDS-PAGE 1 Inhaltsverzeichnis Einige wichtige Sicherheitsregeln...3 Grundlagen...4 Isoelektrische Fokussierung (IEF)...4 SDS-PAGE:
Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres (Marmota monax)
 Aus der Abteilung Innere Medizin II der Medizinischen Universitätsklinik der Albert-Ludwigs-Universität Freiburg im Breisgau Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres
Aus der Abteilung Innere Medizin II der Medizinischen Universitätsklinik der Albert-Ludwigs-Universität Freiburg im Breisgau Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres
Arbeitsblatt 1 Teil 1
 Arbeitsblatt 1 Teil 1 Klonierung Schneiden und Religieren der DNA Bevor Sie anfangen, prüfen Sie ob alle Materialen vorhanden, bzw. eingeschaltet oder beschriftet sind: - Isolierende Styroporkiste mit
Arbeitsblatt 1 Teil 1 Klonierung Schneiden und Religieren der DNA Bevor Sie anfangen, prüfen Sie ob alle Materialen vorhanden, bzw. eingeschaltet oder beschriftet sind: - Isolierende Styroporkiste mit
Mycoplasma gallisepticum
 BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Molekulargenetische Experimente IV: Plasmidpräparation
 Molekulargenetische Experimente IV: Plasmidpräparation Plasmide sind kleine, ringförmige DNA-Moleküle in Bakterien, die in der Lage sind, sich selbst mit Hilfe von Enzymen zu replizieren. Gene, die auf
Molekulargenetische Experimente IV: Plasmidpräparation Plasmide sind kleine, ringförmige DNA-Moleküle in Bakterien, die in der Lage sind, sich selbst mit Hilfe von Enzymen zu replizieren. Gene, die auf
Protokoll zur Übung PCR
 Protokoll zur Übung PCR im Rahmen des Praktikums Labor an der TU Wien Durchgeführt bei Ao.Univ.Prof. Mag. Dr.rer.nat. Robert Mach Verfasser des Protokolls: Gwendolin Korinek 0625083 & Daniel Bomze 0726183
Protokoll zur Übung PCR im Rahmen des Praktikums Labor an der TU Wien Durchgeführt bei Ao.Univ.Prof. Mag. Dr.rer.nat. Robert Mach Verfasser des Protokolls: Gwendolin Korinek 0625083 & Daniel Bomze 0726183
Chlamydia sp. BACTOTYPE PCR Amplification Kit. Gebrauchsanweisung. Labor Diagnostik Leipzig
 BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
A) Arbeiten mit gentechnisch veränderten Mikroorganismen (GVM)
 Anlage 1 zum Gentechnikgesetz Anmelde- bzw. Antragsunterlagen für Arbeiten mit GVO gemäß 19 und 20: A) Arbeiten mit gentechnisch veränderten Mikroorganismen (GVM) B) Arbeiten mit gentechnisch veränderten
Anlage 1 zum Gentechnikgesetz Anmelde- bzw. Antragsunterlagen für Arbeiten mit GVO gemäß 19 und 20: A) Arbeiten mit gentechnisch veränderten Mikroorganismen (GVM) B) Arbeiten mit gentechnisch veränderten
KULTIVIERUNG VON MIKROORGANISMEN
 KULTIVIERUNG VON MIKROORGANISMEN KULTIVIERUNG VON MIKROORGANISMEN Verfahren, das Bakterien außerhalb des natürlichen Standortes zur Vermehrung bringt (unbelebte Substrate oder Zellkulturen) 1 Voraussetzungen
KULTIVIERUNG VON MIKROORGANISMEN KULTIVIERUNG VON MIKROORGANISMEN Verfahren, das Bakterien außerhalb des natürlichen Standortes zur Vermehrung bringt (unbelebte Substrate oder Zellkulturen) 1 Voraussetzungen
Drosophila melanogaster
 Modul biol113 Zellbiologie Drosophila melanogaster Komponenten der angeborenen Immunabwehr Experimente 1) RT (Reverse Transkriptase)-PCR zum Nachweis einer AMP- Expression nach Infektion 1.1 PCR-Reaktion
Modul biol113 Zellbiologie Drosophila melanogaster Komponenten der angeborenen Immunabwehr Experimente 1) RT (Reverse Transkriptase)-PCR zum Nachweis einer AMP- Expression nach Infektion 1.1 PCR-Reaktion
Klassifizierung: noch nicht abgeschlossen, Verwandtschaftsverhältnis zur Familie: Desulvovibrionaceae - Vertreter Desulvovibrio desulfuricans
 AVID X / 1998 Lawsonia intracellularis Seite -1- Klassifizierung: noch nicht abgeschlossen, Verwandtschaftsverhältnis zur Familie: Desulvovibrionaceae - Vertreter Desulvovibrio desulfuricans 1. ALLGEMEINES
AVID X / 1998 Lawsonia intracellularis Seite -1- Klassifizierung: noch nicht abgeschlossen, Verwandtschaftsverhältnis zur Familie: Desulvovibrionaceae - Vertreter Desulvovibrio desulfuricans 1. ALLGEMEINES
DNA Isolierung. Praktikum Dr. László Kredics
 Isolierung Praktikum Dr. László Kredics Aufgabe: Isolierung von Plasmid aus Bakterienzellen Plasmid : pbluescript Vektor, Gröβe: 2960 Bps 1. 1,5 ml Bakterienkultur in Eppendorf-Röhrchen pipettieren, 2
Isolierung Praktikum Dr. László Kredics Aufgabe: Isolierung von Plasmid aus Bakterienzellen Plasmid : pbluescript Vektor, Gröβe: 2960 Bps 1. 1,5 ml Bakterienkultur in Eppendorf-Röhrchen pipettieren, 2
Squish PCR: Zeitsparende Methode zur Genotypisierung von Drosophila Stämmen
 Squish PCR: Zeitsparende Methode zur Genotypisierung von Drosophila Stämmen Einleitung: Drosophila melanogaster hat sich als Modellorganismus in der Entwicklungsbiologie und der Genetik bewährt, und findet
Squish PCR: Zeitsparende Methode zur Genotypisierung von Drosophila Stämmen Einleitung: Drosophila melanogaster hat sich als Modellorganismus in der Entwicklungsbiologie und der Genetik bewährt, und findet
Western-Blot Master-Anweisung, letzte Bearb. Feb 2014
 Western-Blot Master-Anweisung, letzte Bearb. Feb 2014 Proteintransfer (Handschuhe anziehen!) Behandlung der fertigen Gele: - Befülle 2 Schalen mit Transferpuffer (1 für die Gele, 1 für die Membranen) -
Western-Blot Master-Anweisung, letzte Bearb. Feb 2014 Proteintransfer (Handschuhe anziehen!) Behandlung der fertigen Gele: - Befülle 2 Schalen mit Transferpuffer (1 für die Gele, 1 für die Membranen) -
Anlagen. Chemikalien. Ethidiumbromid/Acridinorange - Färbelösung:
 92 Anlagen Chemikalien Ethidiumbromid/Acridinorange - Färbelösung: 1.1 Stammlösung: 50 mg Ethidiumbromid (No. 11615, Merck, Darmstadt), 15 mg Acridinorange (No. 15931, Merck, Darmstadt), 49 ml 10% EDTA-Lösung
92 Anlagen Chemikalien Ethidiumbromid/Acridinorange - Färbelösung: 1.1 Stammlösung: 50 mg Ethidiumbromid (No. 11615, Merck, Darmstadt), 15 mg Acridinorange (No. 15931, Merck, Darmstadt), 49 ml 10% EDTA-Lösung
Methoden 17. 5% Triton X-100 50 mm EDTA 50 mm Tris-HCl ph 8,0
 Methoden 17 3. Methoden 3.1 DNA-Präparationen 3.1.1 Isolierung von Plasmid-DNA nach der Rapid-Boiling-Methode (nach Evans and Wahl, 1987) Zur schnellen Isolation von Plasmid-DNA für Restriktions- und PCR-Analysen
Methoden 17 3. Methoden 3.1 DNA-Präparationen 3.1.1 Isolierung von Plasmid-DNA nach der Rapid-Boiling-Methode (nach Evans and Wahl, 1987) Zur schnellen Isolation von Plasmid-DNA für Restriktions- und PCR-Analysen
Reagenzien Isolierung von Nukleinsäuren
 Aufbewahrung bei Raumtemperatur Anwendung Isolierung ultrareiner Plasmid-DNA aus Bakterienkulturen von 1 ml bis 800 ml. Die Plasmid-DNA eignet sich für Manuelle und automatisierte Sequenzierung mit Fluoreszenzfarbstoffen
Aufbewahrung bei Raumtemperatur Anwendung Isolierung ultrareiner Plasmid-DNA aus Bakterienkulturen von 1 ml bis 800 ml. Die Plasmid-DNA eignet sich für Manuelle und automatisierte Sequenzierung mit Fluoreszenzfarbstoffen
Probe und Probenmenge Wassermenge Auftragspuffermenge 5 µl Kaninchenmuskelextrakt 50 µl 100 µl
 Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
SDS-PAGE und Western Blotting
 1 Enzymaktivierung und Pathogenabwehr Praktikumsabschnitt zum Modul Molekularbiologie und Biochemie der Pflanzen WS 09/19 SDS-PAGE und Western Blotting Polyacrylamid-Gel-Elektrophorese in der Gegenwart
1 Enzymaktivierung und Pathogenabwehr Praktikumsabschnitt zum Modul Molekularbiologie und Biochemie der Pflanzen WS 09/19 SDS-PAGE und Western Blotting Polyacrylamid-Gel-Elektrophorese in der Gegenwart
Zellbiologie: BSc Arbeiten 15/16
 Zellbiologie: BSc Arbeiten 15/16 Lehrstuhl Zellbiologie: Arbeitsgruppen Prof. Benedikt Kost Prof. Georg Kreimer PD Michael Lebert Slot Zeitraum Anzahl Plätze Semester 1 24.08.15 09.10.15 4 Ferien 2 09.11.15
Zellbiologie: BSc Arbeiten 15/16 Lehrstuhl Zellbiologie: Arbeitsgruppen Prof. Benedikt Kost Prof. Georg Kreimer PD Michael Lebert Slot Zeitraum Anzahl Plätze Semester 1 24.08.15 09.10.15 4 Ferien 2 09.11.15
1 µl BamHI H 2 O 21 µl H 2 O 30 µl Volumen 18 µl H 2 O 30 µl Inkubation 2h @ 37 C 2h @ 37 C
 F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen. Methanol-Fixierung
 Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Methanol-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen.
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Methanol-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen.
Regulation der Genexpression und Aufreinigung von Proteinkomplexen
 DEPARTMENT BIOCHEMIE LABORATORIUM FÜR MOLEKULARE BIOLOGIE GENZENTRUM DER LUDWIG-MAXIMILIANS-UNIVERSITÄT MÜNCHEN Biochemisches Praktikum 2 (Fortgeschrittenenpraktikum) Februar 2014 Regulation der Genexpression
DEPARTMENT BIOCHEMIE LABORATORIUM FÜR MOLEKULARE BIOLOGIE GENZENTRUM DER LUDWIG-MAXIMILIANS-UNIVERSITÄT MÜNCHEN Biochemisches Praktikum 2 (Fortgeschrittenenpraktikum) Februar 2014 Regulation der Genexpression
2 Material und Methoden
 Material und Methoden 24 2 Material und Methoden 2.1 Material 2.1.1 Laborgeräte Kühl- und Tiefkühlschrank (-20 C) Zentrifugen: Tischzentrifuge 5415C Avanti J20 Avanti J25 Sigma 4K15C Elektroporator (Gene
Material und Methoden 24 2 Material und Methoden 2.1 Material 2.1.1 Laborgeräte Kühl- und Tiefkühlschrank (-20 C) Zentrifugen: Tischzentrifuge 5415C Avanti J20 Avanti J25 Sigma 4K15C Elektroporator (Gene
Elektrophorese. Zentrum für Mikro- und Nanotechnologien http://www.tu-ilmenau.de/nano
 Elektrophorese Die SDS- Polyacrylamidgelelektrophorese ist eine schnelle und empfindliche Methode, die zudem eine hohe Auflösung erlaubt. Schon 1 μg (2 pmol) eines Proteins ergeben eine erkennbare Bande.
Elektrophorese Die SDS- Polyacrylamidgelelektrophorese ist eine schnelle und empfindliche Methode, die zudem eine hohe Auflösung erlaubt. Schon 1 μg (2 pmol) eines Proteins ergeben eine erkennbare Bande.
SERVAGel N Native Gel Precast Vertical Gels for native Electrophoresis
 GEBRAUCHSANLEITUNG SERVAGel N Native Gel Precast Vertical Gels for native Electrophoresis (Kat.-Nr. 43250, 43251, 43252, 43253) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg Phone +49-6221-138400,
GEBRAUCHSANLEITUNG SERVAGel N Native Gel Precast Vertical Gels for native Electrophoresis (Kat.-Nr. 43250, 43251, 43252, 43253) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg Phone +49-6221-138400,
Produktkatalog 2010. Molekularbiologische Reagenzien
 Produktion, Vertrieb und Serviceleistung im Bereich der Molekularbiologie und Medizin Produktkatalog 2010 Molekularbiologische Reagenzien Molegene GmbH Bienenweg 28 35764 Sinn Tel. 02772-570952 Fax 02772-570945
Produktion, Vertrieb und Serviceleistung im Bereich der Molekularbiologie und Medizin Produktkatalog 2010 Molekularbiologische Reagenzien Molegene GmbH Bienenweg 28 35764 Sinn Tel. 02772-570952 Fax 02772-570945
PCR-Nachweis der pssuara / bar - Genkassette in transgenen Kulturpflanzen
 Methodensammlung des LAG PCR-Nachweis der pssuara / bar - Genkassette in transgenen Kulturpflanzen erstellt vom Unterausschuß Methodenentwicklung des LAG Status: verabschiedet 1. Zweck und Anwendungsbereich
Methodensammlung des LAG PCR-Nachweis der pssuara / bar - Genkassette in transgenen Kulturpflanzen erstellt vom Unterausschuß Methodenentwicklung des LAG Status: verabschiedet 1. Zweck und Anwendungsbereich
Identifizierung positiver Klone aus einer λ-phagenbibliothek
 Identifizierung positiver Klone aus einer λ-phagenbibliothek Betreuer: Elke Muth-Köhne und Nora Cavara Beginn des Versuchs: 9.00 Uhr im Praktikumssaal NBCF 04 Nord 1. Theoretischer Hintergrund 1.1 Screening
Identifizierung positiver Klone aus einer λ-phagenbibliothek Betreuer: Elke Muth-Köhne und Nora Cavara Beginn des Versuchs: 9.00 Uhr im Praktikumssaal NBCF 04 Nord 1. Theoretischer Hintergrund 1.1 Screening
Genetik Praktikumsklausur SS2005
 Genetik Praktikumsklausur SS2005 1. Aufgabe: Der Genotyp AbaB wird geselbstet, dabei werden 256 Nachkommen gebildet. Davon erhalten 16 Pflanzen den Genotyp ABAB a) gekoppelt b) nicht gekoppelt c) teilweise
Genetik Praktikumsklausur SS2005 1. Aufgabe: Der Genotyp AbaB wird geselbstet, dabei werden 256 Nachkommen gebildet. Davon erhalten 16 Pflanzen den Genotyp ABAB a) gekoppelt b) nicht gekoppelt c) teilweise
Etablierung einer. Homemade - PCR
 Etablierung einer Homemade - PCR Anja Schöpflin Institut für Pathologie Universitätsklinikum Freiburg Überblick: Anwendungsgebiete der PCR Anforderungen an Primer Auswahl geeigneter Primer / Primerdesign
Etablierung einer Homemade - PCR Anja Schöpflin Institut für Pathologie Universitätsklinikum Freiburg Überblick: Anwendungsgebiete der PCR Anforderungen an Primer Auswahl geeigneter Primer / Primerdesign
Mycobacterium paratuberculosis
 BACTOTYPE PCR Amplification Kit Mycobacterium paratuberculosis Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Mycobacterium paratuberculosis Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
GENSPIRALE- PRAKTIKUM 1
 GENSPIRALE- PRAKTIKUM 1 FRAGE- UND PROBLEMSTELLUNG In diesem Praktikum, das am Anfang von dreien Genspirale-Praktika steht, soll zuerst das gentechnische und sterile Arbeiten gelernt werden. Anschliessend
GENSPIRALE- PRAKTIKUM 1 FRAGE- UND PROBLEMSTELLUNG In diesem Praktikum, das am Anfang von dreien Genspirale-Praktika steht, soll zuerst das gentechnische und sterile Arbeiten gelernt werden. Anschliessend
D-(+)-Biotin (Vitamin H)
 D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
Molekulare Verfahren im Kontext mit klinischer Praxis und Bestandsbetreuung beim Schwein
 Molekulare Verfahren im Kontext mit klinischer Praxis und Bestandsbetreuung beim Schwein DNA-Extraktion Photometrie Polymerase-Kettenreaktion (PCR) Restriktionsanalyse Agarose-Gelelektrophorese Polyacrylamid-Gelelektrophorese
Molekulare Verfahren im Kontext mit klinischer Praxis und Bestandsbetreuung beim Schwein DNA-Extraktion Photometrie Polymerase-Kettenreaktion (PCR) Restriktionsanalyse Agarose-Gelelektrophorese Polyacrylamid-Gelelektrophorese
4. Methoden. 4.1 Molekularbiologische Methoden
 4. Methoden 4.1 Molekularbiologische Methoden Extraktion und Ethanolfällung von DNA oder RNA Die zu extrahierende DNA oder RNA wurde mit einem Volumen Phenol/Chloroform/Isoamylalkohol versetzt, stark gevortext
4. Methoden 4.1 Molekularbiologische Methoden Extraktion und Ethanolfällung von DNA oder RNA Die zu extrahierende DNA oder RNA wurde mit einem Volumen Phenol/Chloroform/Isoamylalkohol versetzt, stark gevortext
Proteinanalyse mittels SDS-PAGE (SDS Polyacrylamid Gel-Elektrophorese)
 Praktikum IV, SS 07 Biologieversuch 2-23.05.2007 Proteinanalyse mittels SDS-PAGE (SDS Polyacrylamid Gel-Elektrophorese) Zahner Michele (zahnerm@student.ethz.ch) Büchi Luca (lbuechi@student.ethz.ch) Reibisch
Praktikum IV, SS 07 Biologieversuch 2-23.05.2007 Proteinanalyse mittels SDS-PAGE (SDS Polyacrylamid Gel-Elektrophorese) Zahner Michele (zahnerm@student.ethz.ch) Büchi Luca (lbuechi@student.ethz.ch) Reibisch
3 Material und Methoden
 Material und Methoden 24 3 Material und Methoden 3.1 Geräte und Verbrauchsmaterialien 3.1.1 Laborgeräte Agarosegel Elektrophorese Kammern Brutschrank Calculator Gene Quant II Fluoreszenz-Imager FLA 3000
Material und Methoden 24 3 Material und Methoden 3.1 Geräte und Verbrauchsmaterialien 3.1.1 Laborgeräte Agarosegel Elektrophorese Kammern Brutschrank Calculator Gene Quant II Fluoreszenz-Imager FLA 3000
Praktikumsteil Charakterisierung und Genotypisierung floraler homöotischer Mutanten
 Praktikumsteil Charakterisierung und Genotypisierung floraler homöotischer Mutanten Im diesem Praktikumsteil sollen homöotische Mutanten von Arabidopsis untersucht werden. Abb 1, Aufbau einer Blüte einer
Praktikumsteil Charakterisierung und Genotypisierung floraler homöotischer Mutanten Im diesem Praktikumsteil sollen homöotische Mutanten von Arabidopsis untersucht werden. Abb 1, Aufbau einer Blüte einer
Molekularbiologie I. PCR Klonierung Transformation Southern Blot Hybridisierung BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN V 2.
 V 2.6 Molekularbiologie I BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN PCR Klonierung Transformation Southern Blot Hybridisierung Abteilung für Biochemie und Molekularbiologie, Fachbereich
V 2.6 Molekularbiologie I BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN PCR Klonierung Transformation Southern Blot Hybridisierung Abteilung für Biochemie und Molekularbiologie, Fachbereich
Qualitätskontrolle von Lebensmitteln: Was esse ich wirklich?
 Qualitätskontrolle von Lebensmitteln: Was esse ich wirklich? Im Unterricht habt ihr bereits einige Methoden und Vorgehensweisen der Molekularbiologie kennengelernt. Aber wo finden diese Methoden im täglichen
Qualitätskontrolle von Lebensmitteln: Was esse ich wirklich? Im Unterricht habt ihr bereits einige Methoden und Vorgehensweisen der Molekularbiologie kennengelernt. Aber wo finden diese Methoden im täglichen
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen Vorbereitung auf diesen Praktikumsteil: Organisation 2. Praktikumstag: - Für den Bioinformatik-Teil benötigen Sie am 2. Tag dieses
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen Vorbereitung auf diesen Praktikumsteil: Organisation 2. Praktikumstag: - Für den Bioinformatik-Teil benötigen Sie am 2. Tag dieses
Molekularbiologie II. Rekombinante PCR Zielgerichtete Mutagenese Heterologe Expression His-Tag Aufreinigung BIOCHEMISCHES ANFÄNGERPRAKTIKUM
 V 1.8 Molekularbiologie II BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN Rekombinante PCR Zielgerichtete Mutagenese Heterologe Expression His-Tag Aufreinigung Abteilung für Biochemie und Molekularbiologie,
V 1.8 Molekularbiologie II BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN Rekombinante PCR Zielgerichtete Mutagenese Heterologe Expression His-Tag Aufreinigung Abteilung für Biochemie und Molekularbiologie,
peqgold TriFast FL Methode für die gleichzeitige Extraktion von RNA, DNA und Proteinen aus flüssigen Proben.
 peqgold TriFast FL Methode für die gleichzeitige Extraktion von RNA, DNA und Proteinen aus flüssigen Proben. Best.-Nr. 30-2110 100 ml 30-2120 200 ml 30-2130 500 ml Lagerung: Lichtgeschützt bei 4 C für
peqgold TriFast FL Methode für die gleichzeitige Extraktion von RNA, DNA und Proteinen aus flüssigen Proben. Best.-Nr. 30-2110 100 ml 30-2120 200 ml 30-2130 500 ml Lagerung: Lichtgeschützt bei 4 C für
