PC I Thermodynamik J. Stohner / M. Quack SoSe 2006
|
|
|
- Markus Beckenbauer
- vor 7 Jahren
- Abrufe
Transkript
1 PC I Thermodynamik J. Stohner / M. Quack SoSe 2006 Musterlösung zu Übung Druckfehler: In der Spalte 2 der Tabelle 4.1 (Seite 73) muss es T K /K statt T K heissen. 9.2 Bild 4.3a stellt das Phasendiagramm von Wasser bei niedrigen Drücken dar: der Tripelpunkt (fest-flüssig-gasförmig) von Wasser liegt bei p = Pa und T = K (0.01 o C). Bild 4.3b stellt dasselbe Phasendiagramm bei höheren Drücken dar. Dabei sieht man, dass in diesem Hochdruckbereich mehrere Eisphasen, mit I bis VI gekennzeichnet, existieren. Eis IV ist eine metastabile Phase und kommt daher im Gleichgewichtsdiagramm nicht vor. Der Phasenübergang I-flüssig entspricht der Grenzkurve fest-flüssig in Bild 4.3a. Es gibt auch andere Tripelpunkte, wie z.b. bei Koexistenz von Eis I, II und III (bei p 2 kbar, T 30 o C). Bild 4.3c stellt ein Phasendiagramm von Kohlendioxid dar: der Tripelpunkt (fest-flüssiggasförmig) liegt bei p = 5.1 bar und T = 57 o C, der kritische Punkt für die fluide Phase liegt bei T = 31 o C und p = 74 bar. Bild 4.3d stellt das Phasendiagramm von Kohlenstoff bei hohen Drücken dar. Beim festen Kohlenstoff unterscheidet man zwischen Graphit, Diamant und eventuell metallischem Kohlenstoff (Met im Diagramm). Es sind zwei Tripelpunkte (Graphit-Diamant-flüssige Phase, und Diamant-metallischer Kohlenstoff- flüssige Phase) ersichtlich. Nach neueren Unterlagen (F. P. Bundy et al., Carbon Vol 34, pp , 1996) gilt die metallische Phase von C als gut etabliert. Bild 4.4a stellt ein Phasendiagramm von 4 He dar. Man erkennt den kritischen Punkt, zwei flüssige Phasen (flüssig He II und flüssig He I) und eine feste Phase mit einem Tripelpunkt zwischen fest, flüssig I und flüssig II. Bild 4.4b zeigt ein Phasendiagramm von Schwefel. Man erkennt die Existenz zwischen zwei festen Phasen (rhombisch und monoklin), drei Tripelpunkte (rhombisch-monoklingasförmig, monoklin-flüssig-gasförmig, rhombisch-monoklin-flüssig). Der kritische Punkt für die fluide Phase liegt ausserhalb des dargestellten Bereichs. 9.3 Im Gleichgewicht nein, da P +F = K +2 gilt, mit K = 1 (reiner Schwefel), also P +F = 3. Wäre es möglich, Schwefel gasförmig, flüssig, in rhombischer und in monokliner fester Form gleichzeitig zu finden (P = 4), so müsste F = 3 4 = 1 sein, was ein Widerspruch ist, da F 0 sein muss. Unter Nichtgleichgewichtsbedingungen wäre die gleichzeitige Existenz von vier Phasen des Schwefels allerdings möglich. 1
2 9.4 Für das 2-Phasensystem Flüssigkeit/Gas zwischen 400 und 800 C gilt: Zahl der Stoffe in der Gasphase = 4, nämlich S 2 (g), S 4 (g), S 6 (g), S 8 (g). Zahl der unabhängigen Gleichgewichtsreaktionen = 3, mögliche Wahl: 2 S 2 (g) = S 4 (g) 3 S 2 (g) = S 6 (g) 4 S 2 (g) = S 8 (g) Es können auch andere unabhängige Linearkombinationen dieser stöchiometrischen Gleichungen betrachtet werden. Somit ergibt sich K = 1 (Zahl der Stoffe oder Molekülsorten abzüglich der Zahl der linear unabhängigen Gleichgewichtsreaktionen). Damit folgt für die Zahl der Freiheitsgrade F = K + 2 P = 1. Für das Gleichgewicht oberhalb 800 C gilt: Zahl der Stoffe in der Gasphase = 1 (S 2 (g)). Somit K = 1 und F = 1. Die Anzahl der Freiheitsgrade hängt nicht von der Anzahl der Oligomere im Gleichgewichtssystem ab, weil die Zahl der unabhängigen Gleichgewichtsreaktionen in gleichem Ausmass ansteigt wie die Anzahl der Oligomere. 9.5 Unter der Annahme einer idealen Gasphase und unter Vernachlässigung des Volumens der Flüssigkeit (V fl << V g ) kann die Clausius-Clapeyron Gleichung für das Flüssigkeit/Gas Gleichgewicht umgeformt werden zu d ln(p/p ) d (1/T ) = vh R Unter Vernachlässigung der Temperaturabhängigkeit von v H ergibt die Integration der Clausius-Clapeyron-Gleichung zwischen den Grenzen (p 1, T 1 ) und(p 2, T 2 ) ln p 2 = ( vh 1 1 ) p 1 R T 2 T 1 Bei p 1 = p = 1 bar liegt die Siedetemperatur von Schwefel bei T 1 = 717 K (444 C). Ausgehend von diesem Zustand ergibt sich gemäss obiger Gleichung mit v H = 106 kj/mol für T 2 = 1073 K ein Druck von p 2 = 365 bar. Die Troutonsche Regel besagt, dass die Verdampfungsentropie, und damit der Quotient aus Verdampfungswärme v H und Siedetemperatur T v, bei 1 atm Druck für viele Stoffe etwa v S = vh (85 ± 10) J K 1 mol 1 T v beträgt. Für T v = 717 K (444 C) liefert diese Regel den Schätzwert v H 61 kj/mol, und damit ergibt sich für T = 1073 K ein Druck von p = 30 bar. Die beiden Methoden ergeben stark verschiedene Werte. Die Troutonsche Regel gilt nur für Stoffe, die weder in der flüssigen noch in der Dampfphase assoziiert sind, was für das betrachtete System nicht zutrifft. Dies als mögliche Erklärung. 2
3 Fortsetzung von Bild 4.4b mit Siedepunkt bei 1 bar und obigen Schätzwerten für 800 C v H = 106 kj/mol Druck/atm R M fl 1 bar v H = 61 kj/mol (Troutonsche Regel) g R: rhombisch, M: monoklin T v = 444 C Temperatur / C 3
4 9.6 Für Teilaufgaben a) und b) verwenden wir Gl. (4.18a-c) aus dem Skript: a = 27R2 T 2 K 64p K b = RT K V K = 3RT K = 3b Wir benutzen für die Gaskonstante im folgenden R = dm 3 bar mol 1 K 1 und finden damit für a, b und V K (in der Tabelle V vdw k V K ): c) Man erhält für das van-der-waals Gas: RT K V K p K = 8 3 = ) Partielles Ableiten von Gl. (4.17c) aus dem Skript und Substitution (V m = V K, p = p K, T = T K ) ergeben: [ ] [ [ p RT = V m T K V m V m b a ]] Vm 2 = RT K T K (V K b) a VK 3 [ 2 ] [ [ p Vm 2 = RT T K V m (V m b) 2 + 2a ]] RT K Vm 3 = 2 T K (V K b) 3 3 2a VK 4 = 2RT K (V K b) 3 6a VK 4 p K = RT K V K b a V 2 K 4
5 4.1.3) Auflösen von Gl. (4.17a) nach a Einsetzen in Gl. (4.17b) a = RT KV 3 K 2(V K b) 2 (1) Einsetzen von (4) in (1) 0 = 0 = b = V K 3 a = sowie (4) und (5) in Gl. (1.95c) p K = 2RT K (V K b) 3 3RT K (V K b) 2 V K (2) 2 V K b 3 V K (3) RT K VK 3 2(V K V K /3) 2 = 9RT KV K 8 RT K V K V K /3 9RT K 8V K Einsetzen von (7) in (4) und (5) liefert schliesslich (4) (5) = 3RT K 8V K (6) V K = 3RT K (7) b = RT K (8) a = 27R2 T 2 K 64p K (9) 9.8 Man betrachte das Gleichungssystem ( aus ) der Clausius-Gleichung ( p = p(v m, T ) selbst und dp d 2 ) p den beiden Sattelpunktskriterien = 0 und dv m T dvm 2 = 0. Dieses ist genau am T kritischen Punkt (p = p K, V m = V K, T = T K ) erfüllt und man kann es nach den Konstanten a, b, c auflösen (z.b. durch Variablensubstitution oder mit einem Algebra-Programm wie Maple). p K = RT K V K a c T K (V K + b) 2 (10) ( ) dp = 0 = RT K dv m T K (V K a) 2 + 2c T K (V K + b) 3 (11) ( d 2 ) p 2RT K dvm 2 = 0 = T K (V K a) 3 6c T K (V K + b) 4 (12) Daraus ergeben sich die Zusammenhänge zwischen den kritischen Grössen V K, p K, T K und den Parametern a, b, c a = V K RT K 4p K (13) b = 3 RT K V K 8 p K (14) c = 27 TK 3R2 64 p K (15) 5
6 und umgekehrt V K = 2b + 3a (16) TK 2 = 8 c (17) 27 (a + b)r p 2 cr K = 27 8(a + b) 3 (18) Mit den Tabellenwerten T K = K, p K = bar und V K = dm 3 mol 1 (aus Aufgabe 9.6) für CO 2 ergeben sich a = dm 3 mol 1, b = dm 3 mol 1 und c = 1112 dm 6 mol 2 bar K. Mit dem gerundeten Tabellenwert V K = 0.09 dm 3 mol 1 erhält man a = dm 3 mol 1, b = dm 3 mol 1 und c = 1112 dm 6 mol 2 bar K. Geht man für die van-der-waals Gleichung analog vor (dies ist in Aufgabe 9.7 im Detail gezeigt), so ergeben sich für die van der Waals Parameter (für T K und p K werden die exp. Werte eingesetzt) und V K mit V K = 3RT K (19) a = R 2 T 2 K p K (20) b = RT K (21) die folgenden Werte: a = 3.66 bar dm 6 mol 2, b = dm 3 mol 1 und V K = dm 3 mol 1. Bild 1 und 2 zeigen Isothermen in der Nähe des kritischen Punktes für CO 2. Dabei ist zu beachten, dass die 3-Parametergleichung von Clausius den Sattelpunkt der kritischen Isothermen (T = K) definitionsgemäss genau im kritischen Punkt (0.092 dm 3 mol 1, bar) hat, während der Sattelpunkt der kritischen van-der-waals-isotherme durch den dazu signifikant verschiedenen Punkt (3RT K /( ), p K ) = ( dm 3 mol 1, bar) festgelegt ist ( d.h. der kritische Punkt der van-der-waals Gleichung fällt nicht notwendigerweise genau mit dem wirklichen kritischen Punkt des realen Gases zusammen). 6
7 Bild 1: Clausius-Isothermen (CO 2 ) für T = ( n) K, n = 2, 1, 0, 1, 2 (von unten nach oben). Bild 2: van-der-waals Isothermen (CO 2, a = 3.66 bar dm 6 mol 2, b = dm 3 mol 1 ) für T = ( n) K, n = 2, 1, 0, 1, 2 (von unten nach oben). 7
8 9.9 p id = mrt MV n = m M = Pa = 49.6 mol p vdw = RT (V/n) b a (V/n) 2 = J mol 1 K K 0.1 m 3 /(49.6 mol) m 3 mol Pa m6 mol 2 (0.1 m 3 /(49.6 mol)) 2 = Pa Damit ergibt sich ein Fehler von: f 100% p id p vdw p vdw = 0.8% 9.10 Wenn man für T K und V K die experimentellen Werte verwendet, um die van-der-waals Parameter zu berechnen, ergeben sich diese mit p K = 3RT K 8V K (22) a = 9 8 RT KV K (23) b = V K 3 (24) zu a = 2.61 bar dm 6 mol 2 und b = dm 3 mol 1. Damit berechnet man p K = bar, was zu vergleichen ist mit dem exp. Wert p K = bar. Verwendet man für p K und V K die experimentellen Werte, um die van-der-waals Parameter zu berechnen, ergeben sich diese mit T K = 8V Kp K (25) 3R a = 3p K VK 2 (26) b = V K 3 zu a = 1.87 bar dm 6 mol 2 und b = dm 3 mol 1. Damit bestimmt man T K = K, was zu vergleichen ist mit dem exp. Wert von T K = K. In Bild 3 und 4 sind die mit den verschiedenen Sätzen von van-der-waals Parametern berechneten Isothermen aus den Aufgaben 9.8 und 9.10 für T = K, K und K (bzw. für T = K, K und K für den van der Waals Parameter Satz berechnet mit den experimentellen Werten für p K und V K ) dargestellt und zusätzlich die entsprechenden Isothermen, die mit der Clausius Gleichung berechnet bzw. experimentell bestimmt wurden. Wie schon in 9.8 diskutiert ist die Übereinstimmung zwischen der mit der Clausius Gleichung berechneten Isothermen und den experimentell bestimmten hervorragend. Dagegen beschreiben alle drei Sätze von van der Waals Parametern das Gebiet in der Nähe des kritischen Punktes gleich gut, obwohl dies auf den ersten Blick in Bild 3 und 4 nicht unmittelbar erkennbar ist. Die Abweichung der jeweils zu berechnenden kritischen Grösse (gemäss Gl. (19), (22) oder (25)) beträgt in jedem Fall etwa 30% (dies ist einsichtig, da nach van-der-waals RT K /(p K V K ) = 8/3 = 2.67 ist aber mit den experimentellen Werten für CO 2 sich RT K /(p K V K ) = berechnet, so dass X K = X K,exp 3.724/2.67 für X = p, V bzw. T K = T K,exp 2.67/3.724). (27) 8
9 Bild 3: Clausius-Isothermen (CO 2 ) für T= K, K und K und die entsprechenden experimentell bestimmten Isothermen. Bild 4: van-der-waals-isothermen berechnet mit den drei verschiedenen Sätzen von Parametern (siehe Text) und die entsprechenden experimentell bestimmten Isothermen für T = K, K und K. 9
10 Bild 5: van-der-waals Isothermen für CO 2 berechnet mit den drei verschiedenen Sätzen von Parametern (siehe Text). Beachten Sie die verschiedenen Skalierungen innerhalb der y-achsen. Für jeweils eine Isotherme ist die Koexistenzlinie berechnet worden (wie im Skript auf S beschrieben). Anmerkung: Die van-der-waals Isotherme für T=303.6 K, die in Bild 4.7 (Skript S. 69) gezeigt ist, ist nur qualitativ richtig, das Minimum und Maximum ist dort der Anschauung halber übertrieben dargestellt. 10
11 Anwendung von CO 2 als kritisches Lösungsmittel: Wegen seiner relativ kleinen kritischen Werte (p K =73.8 bar, V K = dm 3 bzw. T K = K) hat Kohlendioxid zur Zeit mit Abstand die grösste technische Bedeutung als hyperkritisches Lösungsmittel. So wird mit ihm Coffein aus den grünen Kaffeebohnen extrahiert. Bei Experimenten der landwirtschaftlichen Abteilung des Northern Regional Research Center in Peoria (Illinois) erwies es sich als ein sehr nützliches, nicht polares Lösemittel, um Fett von Fleisch zu lösen. Bei Temperaturen über 304 K und unter Drücken von mehreren Hundert Bar vermag Kohlendioxid das gesamte Fett von Fleischproben aufzulösen. Bei solch einem Auflösevorgang wird aber auch jegliches im Fleisch enthaltene Pestizid oder Arzneimittelrest ebenfalls mitgelöst. Nach Entspannung der hyperkritischen Lösung auf Normaldruck verdampft es unmittelbar, während die ursprünglich gelösten Fette, Arzneimittel und Pestizide als Feststoffe abregnen und untersucht werden können. Weitere Beispiele von überkritschen Lösungsmitteln mit leicht zugänglichen Druck- und Temperaturbedingungen sind z.b. Ethylen, C 2 H 6, SO 2 und Propylen. Diese würden sich als Lösungsmittel für unpolare Substanzen eignen. Des Weiteren könnte man CHClF 2 und HCl als polare hyperkritische Lösungsmittel verwenden (wobei überkritisches HCl vermutlich ein sehr aggressives Lösungsmittel ist). 11
Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H 2 O von
 Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Vorlesung Statistische Mechanik: Ising-Modell
 Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Physikalisches Anfaengerpraktikum. Zustandsgleichung idealer Gase und kritischer Punkt
 Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 2- Siedediagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Siedediagramm wird dieses Vorgespräch durch einen Multiple-Choice
PCG-Grundpraktikum Versuch 2- Siedediagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Siedediagramm wird dieses Vorgespräch durch einen Multiple-Choice
Die 4 Phasen des Carnot-Prozesses
 Die 4 Phasen des Carnot-Prozesses isotherme Expansion: A B V V T k N Q ln 1 1 isotherme Kompression: adiabatische Kompression: adiabatische Expansion: 0 Q Q 0 C D V V T k N Q ln 2 2 S Q 1 1 /T1 T 1 T 2
Die 4 Phasen des Carnot-Prozesses isotherme Expansion: A B V V T k N Q ln 1 1 isotherme Kompression: adiabatische Kompression: adiabatische Expansion: 0 Q Q 0 C D V V T k N Q ln 2 2 S Q 1 1 /T1 T 1 T 2
Phasengleichgewicht und Phasenübergänge. Gasförmig
 Phasengleichgewicht und Phasenübergänge Siedetemperatur Flüssig Gasförmig Sublimationstemperatur Schmelztemperatur Fest Aus unserer Erfahrung mit Wasser wissen wir, dass Substanzen ihre Eigenschaften bei
Phasengleichgewicht und Phasenübergänge Siedetemperatur Flüssig Gasförmig Sublimationstemperatur Schmelztemperatur Fest Aus unserer Erfahrung mit Wasser wissen wir, dass Substanzen ihre Eigenschaften bei
A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Versuch Beschreiben Sie die Vorgänge, die in der Nähe des kritischen Punktes zu beobachten sind.
 1 Versuch 220 Reale Gase 1. Aufgaben 1.1 Nehmen Sie ein Isothermennetz für Schwefelhexafluorid (SF 6 ) auf. Bestimmen Sie daraus die kritischen Daten, und berechnen Sie die Konstanten der Van-der-Waals-Gleichung.
1 Versuch 220 Reale Gase 1. Aufgaben 1.1 Nehmen Sie ein Isothermennetz für Schwefelhexafluorid (SF 6 ) auf. Bestimmen Sie daraus die kritischen Daten, und berechnen Sie die Konstanten der Van-der-Waals-Gleichung.
11. Der Phasenübergang
 11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
Mischphasenthermodynamik Prüfung
 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Mischphasenthermodynamik Prüfung 06. 03. 2017 Teil 1 : Fragenteil Gesamte Bearbeitungszeit
Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Mischphasenthermodynamik Prüfung 06. 03. 2017 Teil 1 : Fragenteil Gesamte Bearbeitungszeit
4. Freie Energie/Enthalpie & Gibbs Gleichungen
 4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
PC-Übung Nr.3 vom
 PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
Verflüssigung von Gasen / Joule-Thomson-Effekt
 Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Prof. Dr. Peter Vogl, Thomas Eissfeller, Peter Greck. Übung in Thermodynamik und Statistik 4B Blatt 8 (Abgabe Di 3. Juli 2012)
 U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Physikalisches Praktikum I
 Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Ideale und Reale Gase. Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig)
 Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
1 Massenwirkungsgesetz
 1 Massenwirkungsgesetz Zeige: Bei konstantem Druck und konstanter emperatur gilt für chemische Reaktionen der Art a 1 A 1 + a A + : : : a L A L b 1 B 1 + b B + : : : b R B R : K c (A i ) ai c (B j ) bj
1 Massenwirkungsgesetz Zeige: Bei konstantem Druck und konstanter emperatur gilt für chemische Reaktionen der Art a 1 A 1 + a A + : : : a L A L b 1 B 1 + b B + : : : b R B R : K c (A i ) ai c (B j ) bj
2.1 Bestimmung einiger Isothermen von Schwefelhexafluorid SF 6
 Atom- und Kernphysi-Versuch 31 AKP-31-1 Zustandsgrößen realer Gase 1 Vorbereitung Koexistenz von Flüssigeiten und Dampf, Dampfdruc, Verdampfungswärme, Koexistenz von Festörper und Flüssigeit, Koexistenz
Atom- und Kernphysi-Versuch 31 AKP-31-1 Zustandsgrößen realer Gase 1 Vorbereitung Koexistenz von Flüssigeiten und Dampf, Dampfdruc, Verdampfungswärme, Koexistenz von Festörper und Flüssigeit, Koexistenz
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti Ulf Wiedwald 16. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 16. 07. 2007
Grundlagen der Physik II Othmar Marti Ulf Wiedwald 16. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 16. 07. 2007
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14,
 ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
Carnotscher Kreisprozess
 Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
Versuch 8 Dampfdruck von Wasser
 Grundpraktikum der Fakultät für Physik Georg August Universität Göttingen Versuch 8 Dampfdruck von Wasser Praktikant: Joscha Knolle Ole Schumann E-Mail: joscha@htilde.de Durchgeführt am: 23.04.2012 Abgabe:
Grundpraktikum der Fakultät für Physik Georg August Universität Göttingen Versuch 8 Dampfdruck von Wasser Praktikant: Joscha Knolle Ole Schumann E-Mail: joscha@htilde.de Durchgeführt am: 23.04.2012 Abgabe:
d) Das ideale Gas makroskopisch
 d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
Die Zustandsgleichung realer Gase
 Die Zustandsgleichung realer Gase Grolik Benno, Kopp Joachim 2. Januar 2003 1 Grundlagen des Versuchs Der Zustand eines idealen Gases wird durch die drei elementaren Zustandsgrößen Druck p, Temperatur
Die Zustandsgleichung realer Gase Grolik Benno, Kopp Joachim 2. Januar 2003 1 Grundlagen des Versuchs Der Zustand eines idealen Gases wird durch die drei elementaren Zustandsgrößen Druck p, Temperatur
Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet
 Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet Unterrichtsmaterial - schriftliche Informationen zu Gasen für Studierende - Folien Fach Schultyp: Vorkenntnisse: Bearbeitungsdauer Thermodynamik
Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet Unterrichtsmaterial - schriftliche Informationen zu Gasen für Studierende - Folien Fach Schultyp: Vorkenntnisse: Bearbeitungsdauer Thermodynamik
PC-Übung Nr.1 vom
 PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
P = P(T, v) = k BT v b a v 2 (37.1)
 37 Van der Waals-Gas Das van der Waals-Gas wird als ein Modell für den Phasenübergang gasförmig flüssig vorgestellt und untersucht Van der Waals hat dieses Modell 1873 in seiner Doktorarbeit eingeführt
37 Van der Waals-Gas Das van der Waals-Gas wird als ein Modell für den Phasenübergang gasförmig flüssig vorgestellt und untersucht Van der Waals hat dieses Modell 1873 in seiner Doktorarbeit eingeführt
Physikalische Umwandlungen reiner Stoffe
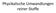 Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagrame Phasenübergänge, die D Gleichgewichtkriterium Die Abhängigkeit der
Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagrame Phasenübergänge, die D Gleichgewichtkriterium Die Abhängigkeit der
Lösungen 10 (Kinetik)
 Chemie I WS 2003/2004 Lösungen 10 (Kinetik) Aufgabe 1 Verschiedenes 1.1 Als Reaktionsgeschwindigkeit v c wird die Ableitung der Konzentration eines Reaktanden A nach der Zeit t, dividiert durch dessen
Chemie I WS 2003/2004 Lösungen 10 (Kinetik) Aufgabe 1 Verschiedenes 1.1 Als Reaktionsgeschwindigkeit v c wird die Ableitung der Konzentration eines Reaktanden A nach der Zeit t, dividiert durch dessen
Reale Gase - kritischer Pumkt
 1 Reale Gase - kritischer Pumkt In diesem Versuch werden Isothermen eines realen Gases (Ethan oder Schwefelhexafluorid) im Temperaturbereich zwischen 10 C und 50 C vermessen und mit den Isothermen des
1 Reale Gase - kritischer Pumkt In diesem Versuch werden Isothermen eines realen Gases (Ethan oder Schwefelhexafluorid) im Temperaturbereich zwischen 10 C und 50 C vermessen und mit den Isothermen des
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler
 U München Reinhard Scholz Physik Department, 33 homas Eissfeller, Peter Greck, illmann Kubis, Christoph Schindler http://www.wsi.tum.de/33/eaching/teaching.htm Übung in heoretischer Physik 5B (hermodynamik)
U München Reinhard Scholz Physik Department, 33 homas Eissfeller, Peter Greck, illmann Kubis, Christoph Schindler http://www.wsi.tum.de/33/eaching/teaching.htm Übung in heoretischer Physik 5B (hermodynamik)
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
Lösungen zur Übungsklausur Thermodynamik WS 2003/04
 Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
Reale Gase. Versuch: RG. Inhaltsverzeichnis. Fachrichtung Physik. Erstellt: E. Beyer Aktualisiert: am Physikalisches Grundpraktikum
 Versuch: RG Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: E. Beyer Aktualisiert: am 01. 10. 2010 Bearbeitet: J. Kelling F. Lemke S. Majewsky M. Justus Reale Gase Inhaltsverzeichnis 1 Aufgabenstellung
Versuch: RG Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: E. Beyer Aktualisiert: am 01. 10. 2010 Bearbeitet: J. Kelling F. Lemke S. Majewsky M. Justus Reale Gase Inhaltsverzeichnis 1 Aufgabenstellung
! #!! % & ( )! ! +, +,# # !.. +, ) + + /) # %
 ! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
Probeklausur STATISTISCHE PHYSIK PLUS
 DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
Die innere Energie and die Entropie
 Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Thermodynamik I Formeln
 Thermodynamik I Formeln Tobi 4. September 2006 Inhaltsverzeichnis Thermodynamische Systeme 3. Auftriebskraft........................................ 3 2 Erster Hauptsatz der Thermodynamik 3 2. Systemenergie........................................
Thermodynamik I Formeln Tobi 4. September 2006 Inhaltsverzeichnis Thermodynamische Systeme 3. Auftriebskraft........................................ 3 2 Erster Hauptsatz der Thermodynamik 3 2. Systemenergie........................................
Versuch Nr. 7. = q + p dv
 Hochschule Augsburg Versuch Nr. 7 Physikalisches Aufbauten 7 a bzw. 27 a Praktikum Spezifische Verdampfungsenthalpie - Dampfdruckkurve 1. Grundlagen_und_Versuchsidee 1.1 Definition der Verdampfungsenthalpie:E
Hochschule Augsburg Versuch Nr. 7 Physikalisches Aufbauten 7 a bzw. 27 a Praktikum Spezifische Verdampfungsenthalpie - Dampfdruckkurve 1. Grundlagen_und_Versuchsidee 1.1 Definition der Verdampfungsenthalpie:E
Praktikum Physikalische Chemie I. Versuch 4. p, V, T - Verhalten realer Gase am Beispiel von SF 6
 Praktikum Physikalische Chemie I ersuch 4 p,, T - erhalten realer Gase am Beispiel von SF 6 1. Grundlagen Komprimiert man ein Gas isotherm, so steigt dessen Druck näherungsweise gemäß dem idealen Gasgesetz
Praktikum Physikalische Chemie I ersuch 4 p,, T - erhalten realer Gase am Beispiel von SF 6 1. Grundlagen Komprimiert man ein Gas isotherm, so steigt dessen Druck näherungsweise gemäß dem idealen Gasgesetz
Antrieb und Wärmebilanz bei Phasenübergängen. Speyer, März 2007
 Antrieb und Wärmebilanz bei Phasenübergängen Speyer, 19-20. März 2007 Michael Pohlig, WHG-Durmersheim michael@pohlig.de Literatur: Physik in der Oberstufe; Duden-PAETEC Schmelzwärme wird auch als Schmelzenergie
Antrieb und Wärmebilanz bei Phasenübergängen Speyer, 19-20. März 2007 Michael Pohlig, WHG-Durmersheim michael@pohlig.de Literatur: Physik in der Oberstufe; Duden-PAETEC Schmelzwärme wird auch als Schmelzenergie
A 2.6 Wie ist die Zusammensetzung der Flüssigkeit und des Dampfes eines Stickstoff-Sauerstoff-Gemischs
 A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Der Dampfdruck von Wasser
 Physikalisches Grundpraktikum Versuch 8 Der Dampfdruck von Wasser Praktikant: Tobias Wegener Alexander Osterkorn E-Mail: tobias.wegener@stud.uni-goettingen.de a.osterkorn@stud.uni-goettingen.de Tutor:
Physikalisches Grundpraktikum Versuch 8 Der Dampfdruck von Wasser Praktikant: Tobias Wegener Alexander Osterkorn E-Mail: tobias.wegener@stud.uni-goettingen.de a.osterkorn@stud.uni-goettingen.de Tutor:
Versuch 8: Der Dampfdruck von Wasser
 Versuch 8: Der Dampfdruck von Wasser Inhaltsverzeichnis 1 Einführung 3 2 Theorie 3 2.1 Reale Gase.................................... 3 2.2 Dampfdruck................................... 3 2.3 Arrhenius-Plot.................................
Versuch 8: Der Dampfdruck von Wasser Inhaltsverzeichnis 1 Einführung 3 2 Theorie 3 2.1 Reale Gase.................................... 3 2.2 Dampfdruck................................... 3 2.3 Arrhenius-Plot.................................
Physikalische Umwandlungen reiner Stoffe
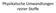 Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der
Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der
Phasenumwandlungsenthalpie
 Universität Potsdam Institut für Physik und Astronomie Grundpraktikum 7 Phasenumwandlungsenthalpie Die Enthalpieänderung beim Übergang eines Systems in einen anderen Aggregatzustand kann unter der Voraussetzung,
Universität Potsdam Institut für Physik und Astronomie Grundpraktikum 7 Phasenumwandlungsenthalpie Die Enthalpieänderung beim Übergang eines Systems in einen anderen Aggregatzustand kann unter der Voraussetzung,
PhysikalischeUmwandlungen
 PhysikalischeUmwandlungen reinerstoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der Stabilität
PhysikalischeUmwandlungen reinerstoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der Stabilität
Prof. Dr. Elmar Grosse-Klönne Institut für Mathematik
 Prof. Dr. Elmar Grosse-Klönne Institut für Mathematik Lineare Algebra Analytische Geometrie I* Übungsaufgaben, Blatt Musterlösungen Aufgabe. Es seien A, B, C Teilmengen einer Menge X. Zeige: i A B C =
Prof. Dr. Elmar Grosse-Klönne Institut für Mathematik Lineare Algebra Analytische Geometrie I* Übungsaufgaben, Blatt Musterlösungen Aufgabe. Es seien A, B, C Teilmengen einer Menge X. Zeige: i A B C =
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases. f=5 Translation + Rotation. f=7 Translation + Rotation +Vibration. Wiederholung
 1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung
 Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Physik III - Anfängerpraktikum- Versuch 203
 Physik III - Anfängerpraktikum- Versuch 203 Sebastian Rollke (103095) und Daniel Brenner (105292) 1. Februar 2005 Inhaltsverzeichnis 1 Vorbetrachtung 2 2 Theorie 2 2.1 Die mikroskopischen Vorgänge bei
Physik III - Anfängerpraktikum- Versuch 203 Sebastian Rollke (103095) und Daniel Brenner (105292) 1. Februar 2005 Inhaltsverzeichnis 1 Vorbetrachtung 2 2 Theorie 2 2.1 Die mikroskopischen Vorgänge bei
PC I Thermodynamik und Transportprozesse
 20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
Phasengleichgewicht. 1. Experimentelle Bestimmung des Dampfdrucks von Methanol als Funktion der Temperatur. A fl. A g
 Physikalisch-Chemische Praktika Phasengleichgewicht Versuch T-2 Aufgaben 1. Experimentelle Bestimmung des Dampfdrucks von Methanol als Funktion der Temperatur. 2. Ermittlung der Phasenumwandlungsenthalpie
Physikalisch-Chemische Praktika Phasengleichgewicht Versuch T-2 Aufgaben 1. Experimentelle Bestimmung des Dampfdrucks von Methanol als Funktion der Temperatur. 2. Ermittlung der Phasenumwandlungsenthalpie
4.6.5 Dritter Hauptsatz der Thermodynamik
 4.6 Hauptsätze der Thermodynamik Entropie S: ds = dq rev T (4.97) Zustandsgröße, die den Grad der Irreversibilität eines Vorgangs angibt. Sie ist ein Maß für die Unordnung eines Systems. Vorgänge finden
4.6 Hauptsätze der Thermodynamik Entropie S: ds = dq rev T (4.97) Zustandsgröße, die den Grad der Irreversibilität eines Vorgangs angibt. Sie ist ein Maß für die Unordnung eines Systems. Vorgänge finden
Die Innere Energie U
 Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
6.2 Zweiter HS der Thermodynamik
 Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
212 - Siedepunktserhöhung
 1 - Siedeunktserhöhung 1. Aufgabe Es ist für verschiedene in Wasser lösliche Stoffe die Siedeunktserhöhung ihrer Lösung zu messen und daraus die molare Masse zu bestimmen.. Grundlagen Stichworte: Damfdruck,
1 - Siedeunktserhöhung 1. Aufgabe Es ist für verschiedene in Wasser lösliche Stoffe die Siedeunktserhöhung ihrer Lösung zu messen und daraus die molare Masse zu bestimmen.. Grundlagen Stichworte: Damfdruck,
Themengebiet: Thermodynamik. mol K. mol. ] eines Stoffes bestehend aus n Mol mit der Masse m gilt. M = m n. (2)
![Themengebiet: Thermodynamik. mol K. mol. ] eines Stoffes bestehend aus n Mol mit der Masse m gilt. M = m n. (2) Themengebiet: Thermodynamik. mol K. mol. ] eines Stoffes bestehend aus n Mol mit der Masse m gilt. M = m n. (2)](/thumbs/39/18548726.jpg) Seite 1 Themengebiet: Thermodynamik 1 Literatur D. Meschede, Gerthsen Physik, Springer F. Kohlrausch, Praktische Physik, Band 2, Teubner R.P. Feynman, R.B. Leighton und M. Sands, Feynman-Vorlesungen über
Seite 1 Themengebiet: Thermodynamik 1 Literatur D. Meschede, Gerthsen Physik, Springer F. Kohlrausch, Praktische Physik, Band 2, Teubner R.P. Feynman, R.B. Leighton und M. Sands, Feynman-Vorlesungen über
Vorlesung #7. M.Büscher, Physik für Mediziner
 Vorlesung #7 Zustandsänderungen Ideale Gase Luftfeuchtigkeit Reale Gase Phasenumwandlungen Schmelzwärme Verdampfungswärme Dampfdruck van-der-waals Gleichung Zustandsdiagramme realer Gase Allgem. Gasgleichung
Vorlesung #7 Zustandsänderungen Ideale Gase Luftfeuchtigkeit Reale Gase Phasenumwandlungen Schmelzwärme Verdampfungswärme Dampfdruck van-der-waals Gleichung Zustandsdiagramme realer Gase Allgem. Gasgleichung
Die kinetische Gastheorie beruht auf den folgenden drei Annahmen:
 Physikalische Chemie Modul II Versuch: Reales Gas 20. Juli 2010 1 Einleitung Die kinetische Gastheorie beruht auf den folgenden drei Annahmen: 1. Das Gas besteht aus Molekülen der Masse m und dem Durchmesser
Physikalische Chemie Modul II Versuch: Reales Gas 20. Juli 2010 1 Einleitung Die kinetische Gastheorie beruht auf den folgenden drei Annahmen: 1. Das Gas besteht aus Molekülen der Masse m und dem Durchmesser
Bernhard Härder. Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik W/ WESTAR.P WISSENSCHAFTEN. Skripte, Lehrbücher Band 2
 Bernhard Härder Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik Skripte, Lehrbücher Band 2 W/ WESTAR.P WISSENSCHAFTEN Inhaltsverzeichnis Vorwort zur ersten Auflage Vorwort zur
Bernhard Härder Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik Skripte, Lehrbücher Band 2 W/ WESTAR.P WISSENSCHAFTEN Inhaltsverzeichnis Vorwort zur ersten Auflage Vorwort zur
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Grundlagen der Physik 3 Lösung zu Übungsblatt 2
 Grundlagen der Physik 3 Lösung zu Übungsblatt 2 Daniel Weiss 17. Oktober 2010 Inhaltsverzeichnis Aufgabe 1 - Zustandsfunktion eines Van-der-Waals-Gases 1 a) Zustandsfunktion.................................
Grundlagen der Physik 3 Lösung zu Übungsblatt 2 Daniel Weiss 17. Oktober 2010 Inhaltsverzeichnis Aufgabe 1 - Zustandsfunktion eines Van-der-Waals-Gases 1 a) Zustandsfunktion.................................
PC I Thermodynamik J. Stohner/M. Quack Sommer Übung 12
 PC I Thermodynamik J. Stohner/M. Quack Sommer 2006 Übung 12 Ausgabe: Dienstag, 20. 6. 2006 Rückgabe: Dienstag, 27. 6. 2006 (vor Vorlesungsbeginn) Besprechung: Freitag, 30.6./Montag, 3.7.2006 (in der Übungsstunde)
PC I Thermodynamik J. Stohner/M. Quack Sommer 2006 Übung 12 Ausgabe: Dienstag, 20. 6. 2006 Rückgabe: Dienstag, 27. 6. 2006 (vor Vorlesungsbeginn) Besprechung: Freitag, 30.6./Montag, 3.7.2006 (in der Übungsstunde)
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd
 A1-1 1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd Bereiten Sie folgende Themengebiete vor Zustandsdiagramme von Einkomponentensystemen
A1-1 1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd Bereiten Sie folgende Themengebiete vor Zustandsdiagramme von Einkomponentensystemen
Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt
 1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Allgemeine Chemie. SS 2014 Thomas Loerting. Thomas Loerting Allgemeine Chemie
 Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan
 Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Dampfdruckmessungen an 1-Butanol und Ethanol
 Dampfdruckmessungen an 1-Butanol und Ethanol Jorge Ferreiro, D-CHAB, 1. Semester, fjorge@student.ethz.ch Lisa Kamber, D-CHAB, 1. Semester, kamberl@student.ethz.ch Assistentin: Maria Grazia Santangelo Abstract:
Dampfdruckmessungen an 1-Butanol und Ethanol Jorge Ferreiro, D-CHAB, 1. Semester, fjorge@student.ethz.ch Lisa Kamber, D-CHAB, 1. Semester, kamberl@student.ethz.ch Assistentin: Maria Grazia Santangelo Abstract:
Verdampfungswärme und Dampfdruck-Kurve
 Versuch 203 Verdampfungswärme und Dampfdruck-Kurve Thorben Linneweber Marcel C. Strzys 26.05.2009 Technische Universität Dortmund Zusammenfassung Protokoll zur Bestimmung der Dampfdruckkurve von Wasser,
Versuch 203 Verdampfungswärme und Dampfdruck-Kurve Thorben Linneweber Marcel C. Strzys 26.05.2009 Technische Universität Dortmund Zusammenfassung Protokoll zur Bestimmung der Dampfdruckkurve von Wasser,
Bekannter Stoff aus dem 1. Semester:
 Bekannter Stoff aus dem 1. Semester: Atombau! Arten der Teilchen! Elemente/Isotope! Kernchemie! Elektronenhülle/Quantenzahlen Chemische Bindung! Zustände der Materie! Ionenbindung! Atombindung! Metallbindung
Bekannter Stoff aus dem 1. Semester: Atombau! Arten der Teilchen! Elemente/Isotope! Kernchemie! Elektronenhülle/Quantenzahlen Chemische Bindung! Zustände der Materie! Ionenbindung! Atombindung! Metallbindung
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
-aus theoretischen Ansätzen - Approximationen
 2.3 Bestimmung von Zustandsgrößen Zustand wird bestimmt durch zwei unabhängige, intensive Zustandsgrößen Bestimmung anderer Zustandsgrößen aus Stoffmodellen Zustandsgleichungen Stoffmodelle aus - Experimenten
2.3 Bestimmung von Zustandsgrößen Zustand wird bestimmt durch zwei unabhängige, intensive Zustandsgrößen Bestimmung anderer Zustandsgrößen aus Stoffmodellen Zustandsgleichungen Stoffmodelle aus - Experimenten
Lernziele: Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme,
 Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Spezialfälle. BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz. bei V, n = konstant: p = const.
 Spezialfälle BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz p V = n R T bei V, n = konstant: p = const. T Druck Druck V = const. Volumen T 2 T 1 Temperatur
Spezialfälle BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz p V = n R T bei V, n = konstant: p = const. T Druck Druck V = const. Volumen T 2 T 1 Temperatur
Protokoll Dampfdruck. Punkte: /10
 Protokoll Dampfdruck Gruppe Biologie Assistent: Olivier Evelyn Jähne, Eva Eickmeier, Claudia Keller Kontakt: claudiakeller@teleport.ch Sommersemester 2006 6. Juni 2006 Punkte: /0 . Einleitung Wenn eine
Protokoll Dampfdruck Gruppe Biologie Assistent: Olivier Evelyn Jähne, Eva Eickmeier, Claudia Keller Kontakt: claudiakeller@teleport.ch Sommersemester 2006 6. Juni 2006 Punkte: /0 . Einleitung Wenn eine
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11
 Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
