Wichtig: Unterschied zwischen Konstitution, Konformation und Konfiguration
|
|
|
- Bettina Reuter
- vor 7 Jahren
- Abrufe
Transkript
1 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 3. Alkene 3.1 Nomenklatur, Konfiguration Nomenklatur 1-exen 3-exen 1,3-exadien 1,2-exadien C 3 1-Chlor-4-ethyl- 7-methyl-2-octen 1-thylcyclopropen 5-Chlor-1,3-cyclohexadien Trivialnamen: thenyl "Vinyl" "Vinylchlorid" 2-Propenyl "Allyl" "Allylbromid" Konfiguration Isomere Unterschiedliche Verbindungen mit gleicher Summenformel Konstitutions-Isomere eihenfolge der Verknüpfung der Atome ist verschieden Stereoisomere Gleiche Konstitution, aber unterschiedliche Anordnung der Atome im aum Stereoformel, Stereochemie Konformations-Isomere Durch Drehung um infachbindung ineinander überführbar Gleichgewicht bei aumtemperatur Konfigurations-Isomere Nicht ineinander überführbar ohne Bindungsbruch (kein Gleichgewicht) nantiomere Wie Bild und Spiegelbild (vgl. Kapitel 5.2) Diastereomere Nicht wie Bild und Spiegelbild (vgl. Kapitel 5.2) Wichtig: Unterschied zwischen Konstitution, Konformation und Konfiguration 23
2 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Beispiel: Butan im Vergleich mit 2-Buten Konformations-Isomere Konfigurations-Isomere 14 kj/mol 150 kj/mol anti syn (anti) "trans" (syn) "cis" besser: Z -Z-Nomenklatur: Prioritätsregeln richten sich nach der rdnungszahl. t > t > Z D 2-Chlorethyl > thyl D > 3.2 Darstellung Petrochemie vergleiche Kapitel und (Crack-Verfahren, SP etc.) ydrierung von Alkinen Kat. A 1 2 Z-Alken Kat. B 1 -Alken "Stereoselektive eaktion" von zwei Konfigurationsisomeren wird nur eines (= selektiv) gebildet 24
3 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Dehydratisierung von Alkoholen liminierung 1. rdnung (1-eaktion) 170 C 3 C C 2 2 C C 2 95% 2 S 4 thanol 2 3 C C C C 3 C C C % 2 S 4 2-Propanol C 3 3 C C C 3 85 C 20% 2 S 4 3 C C C 2 3 C 2 2-thyl-2-propanol "tert-butanol" chanismus: önstedt-säurekatalyse : eaktionsgeschwindigkeit G ~ c(alkohol) eaktivität: tert.-alkohol > sek.-alkohol > prim.-alkohol Grund: Stabilisierung der Zwischenstufe, ein Carbeniumion, durch yperkonjugation. 25
4 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler M-Theorie: σ C p z C p z leer C σ C sp 2 -ybrid VB-Theorie: C C C C somerie, "no bond resonance" elative eaktionsgeschwindigkeit Aktivierungsenergie C 2 G 1 C 2 G 3 G 2 C 3 1 -Alk. 2 -Alk. 3 -Alk. Alkylreste stabilisieren Carbeniumionen durch yperkonjugation 26
5 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Die egiochemie der 1-liminierung: 2 auptprodukte Nebenprodukt Saytzeff-egel: Bei liminierungen (Dehydratisierung, 1; Dehydrohalogenierung, 2) wird das stabilste Alken, d. h. mit den meisten Alkylresten an der Doppelbindung, als auptprodukt gebildet Dehydrohalogenierung liminierung 2. rdnung (2-eaktion) trocken erh. K ( K 2 ) K in t N Pyridin (schwächere Base als K) 27
6 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler chanismus: Baseninduktion C C anti C C Übergangszustand C C 2 C C lektronenpaare klappen um; Übergangszustand; eaktionsgeschwindigkeit G ~ c( ) c(-x) liminierung zweiter rdnung Vergleich des eaktionsprofils einer 2- gegenüber einer 1-eaktion: 2 ÜZ ÜZ 1 ÜZ ZS C 3 dukt dukt Produkt Produkt eaktionskoordinate in Übergangszustand (ÜZ) ist ein Maximum im eaktionsprofil, eine entsprechende Spezies existiert nicht. ine Zwischenstufe (ZS) ist ein Minimum im eaktionsprofil, eine entsprechende Spezies existiert und kann durch geeignete xperimente nachgewiesen werden. Bei der 1-eaktion ist die ZS ein Carbeniumion. 28
7 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Die egiochemie der 2-liminierung: s gilt ebenfalls die Saytzeff-egel K Stereochemie: anti-liminierung t t t t Z D t D D t t D t Z mit D ohne D s handelt sich um eine stereospezifische eaktion: Bei gegebener Stereochemie (Konfiguration) des duktes wird nicht jede beliebige, sondern eine bestimmte Konfiguration des Produktes gebildet Dehalogenierung von 1,2-Dihalogenverbindungen C C Zn ' C C' Zn 2 29
8 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 3.3 eaktionen von Alkenen Katalytische ydrierung Siehe Kapitel alogenierung 2 oder 2 bei aumtemperatur, spontan, ohne Initiator lektrophile Addition A : lektrophil lektronenmangelverbindung chanismus: δ δ π-komplex Produkt omonium-ion Carbenium-Ion eaktionsprofil: π dukt CΙ BΙ Produkt eaktionskoordinate 30
9 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Stereochemie: anti-addition wichtig bei cyclischen Systemen: 2 oder? cis trans anti- Addition oben unten Im ing keine freie Drehbarkeit um jede C-C-infachbindung cis/trans-isomerie (auch eine Konfigurationsisomerie) 31
10 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler ydrohalogenierung (ionisch) chanismus: A Zwischenstufe: Carbeniumion egiochemie: oder? Prinzip: stabileres Carbeniumion wird gebildet, vgl. Kapitel oder 2 -Carbeniumion 1 -Carbeniumion auptprodukt Markownikoff-egel: "Wer schon hat, dem wird gegeben" Lukas 3:21-22 "Bei einer elektrophilen Addition von X an Alkene addiert der Wasserstoff an den Kohlenstoff, der bereits die meisten Wasserstoffe trägt." 32
11 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler ydrohalogenierung (radikalisch) chanismus: Kettenreaktion adikalstarter S Start: S S Fortpflanzung: Im Vergleich zur ionischen ydrohalogenierung ist die egiochemie bei der radikalischen eaktion scheinbar umgekehrt, d. h. es bildet sich das Anti-Markownikoff-Produkt. Das zugrunde liegende Prinzip ist aber auch hier die Bildung des stabilsten adikals als Zwischenstufe. Die Umkehrung der egiochemie erfolgt daher nur scheinbar: während es sich bei der ionischen eaktion beim lektrophil um ein handelt, ist bei der radikalischen Variante ein -adikal das lektrophil ydratisierung 2 kat. chanismus: säurekatalysierte A 2-2 egiochemie: es gilt die Markownikoff-egel, lektrophil ist 33
12 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler ydroborierung 1) B 2 6 2) Na, 2 2 egiochemie: Anti-Markownikoff-Alkohol wird gebildet lektrophil ist B 3, wird im zweiten Schritt in umgewandelt, B 3 als Äquivalent für chanismus: B 2 6 B 3 B 3 Na, Dihydroxylierung 2 2 s 4 - () 2 s 2 1,2-Diol B 2 B 2 chanismus: cyclische Zwischenstufe, cis-dihydroxylierung s s 2 2 () 2 s 2 Stereochemie: syn, cis-addition s cis-cyclohexan- 1,2-diol 34
13 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler poxidierung PhC 2 "Persäure" poxid Stereochemie: cis-addition Bedeutung: Umwandlung in trans-diole durch ingöffnung 2 kat. trans-diol Angriff von unten, anti 35
14 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler zonolyse 1) 3 2) Zn/ C 2 Formal: ' '' ''' 2 "" ' '' ''' chanismus: 1,3-Dipol Primärozonid Zn zonid Bedeutung: Abbau von Alkenen zu Carbonylverbindungen 1) 3 2) Zn/ ' 1) 3 1' 2) Zn/ ' ' 1 C 2 36
15 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 3.4 Polymere I: Polyaddition Definition Poly-Addition 2 2 C C 2 Dimer Trimer Polymer: n > 10 3 ligomer: n < 10 2 C C n t n Polymerisationsmechanismen adikalische Polymerisation Kettenreaktion Start: durch Initiatorradikal S, vgl. Kap S S S 1 -adikal 2 -adikal stabilisiert adikal durch Konjugation ( = Phenyl) oder durch yperkonjugation ( = Alkyl) S S S S Konjugation somerie esonanz 37
16 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Kettenfortpflanzung: S S S S n S Abbruch: analog S Kationische Polymerisation Initiierung durch lektrophil: Kation oder Lewis-Säure n Abbruch - n F 3 B F 3 B F 3 B Abbruch F 3 B n egiochemie: Markownikoff-egel 38
17 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Übergangsmetallkatalyse z.b. Ti t 2 Al Ziegler, Natta Ti t 2 Al 2 freie Koordinationsstelle, lektrophil, wie Kap Bedeutung: oft hochselektive Polymerisationen möglich Stereoselektivität Taktizität z.b. Polypropen isotaktisch Fp. 175 C syndiotaktisch Fp. 125 C ataktisch Fp. <24 C Anionische Polymerisation Nu CN Nu CN Nu CN CN CN n Nu CN CN CN n CN stabilisiert negative Ladung Michael-eaktion, vgl. Kap
18 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Beispiele Polyethylen ("thylen" then) ÜM-Kat. n 2 C C 2 n aus Crackprozeß LDP d < 0.95 g cm 3 DP d > 0.95 g cm 3 ÜM = Übergangsmetall P Formteile, Folien, ohre, Schläuche Polypropylen ("Propylen" Propen) aus Crackprozeß ÜM-Kat. n PP wichtig: Taktizität (vgl. Kap ) Polystyrol ("Styrol" Phenylethen Vinylbenzol) Ph n Ph Ph Ph Ph PS wichtig: Taktizität (vgl. Kap ) Verpackungen, Formteile, Isoliermaterial Sehr geringe Dichte: Styropor: PS aufgeschäumt Polyvinylchlorid ("Vinylchlorid" Chlorethen) n PVC Behälter, Folien, Beschichtungen, ohre, Schläuche, Bodenbeläge Probleme: Monomer carzinogen; Polymer: ntsorgung 40
19 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Synthese Monomer (VC) 2 - (VC) PVC ist sehr hart, in der egel ist der insatz von Weichmachern, z. B. DP, erforderlich. Di(2-ethylhexyl)phthalat "Teflon" (Polytetrafluorethen) F F F F F F F F F F F F F F F F F F F F PTF sehr hart, sehr inert, sehr thermostabil Polyacrylnitril ("Acrylnitril" Cyanoethen) CN Formteile, Fasern Polymethylmethacrylat C 2 Plexiglas, glasartig n CN CN CN CN "Dralon" = C 2 PAN PMMA 41
20 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Quervernetzung Bei der Quervernetzung entstehen dreidimensionale Netzwerke, die sich durch sehr große Molmassen sowie Unlöslichkeit auszeichnen. Quervernetzung lässt sich durch Copolymerisation (Ionenaustauscher-arze, Trägerharze, unlöslich, aber quellfähig) oder Vulkanisation (Gummi) erzielen Copolymerisation PSDVB Vulkanisation 99% 1% Styrol DVB "Isopren" Natur nzym n Z-1,4-Polyisopren "Naturkautschuk", S 8 (S) n Vulkanisation von Gummi (Goodyear 1838) (S) n (S) n ligosulfid-ücken künstliche Dien-Polymere: n S 8 Quervernetzung Butadien Polybutadien Naturkautschuk-rsatz "Chloropren" n Neopren inert gegen Lösungsmittel etc. 42
21 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Polybutadien: 1,2- vs. 1,4-Addition Konjugation X X X X 1,2-Addition 1,4-Addition n Anhang DIN 6120 "ecyclingsymbole" 02 PD PT P-D PVC P-LD PP PS? PT (Polyester): vgl. Kap "other" 43
Inhaltsverzeichnis zu Kapitel 3. Alkene
 Inhaltsverzeichnis zu Kapitel 3. Alkene 3. Alkene 3.1 Nomenklatur, Konfiguration 37 3.1.1 Nomenklatur 37 3.1.2 Konfiguration 37 3.2 Darstellung 38 3.2.1 Petrochemie 38 3.2.2 ydrierung von Alkinen 38 3.2.3
Inhaltsverzeichnis zu Kapitel 3. Alkene 3. Alkene 3.1 Nomenklatur, Konfiguration 37 3.1.1 Nomenklatur 37 3.1.2 Konfiguration 37 3.2 Darstellung 38 3.2.1 Petrochemie 38 3.2.2 ydrierung von Alkinen 38 3.2.3
Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. Dr. J. Christoffers Institut für Organische Chemie Universität Stuttgart 29.04.2003 Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. Einführung 2.
Prof. Dr. J. Christoffers Institut für Organische Chemie Universität Stuttgart 29.04.2003 Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. Einführung 2.
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Vinyl-Polymerisation (Vollhardt, 3. Aufl., S , 4. Aufl. S ; Hart, S , S )
 Vorlesung 23. Polyolefine Vinyl-Polymerisation (Vollhardt, 3. Aufl., S. 532-538, 4. Aufl. S. 599-605; art, S. 116-118, S. 497-507) Thermodynamik: Die π-bindung der Alkene ist um etwa 80 kj mol 1 schwächer
Vorlesung 23. Polyolefine Vinyl-Polymerisation (Vollhardt, 3. Aufl., S. 532-538, 4. Aufl. S. 599-605; art, S. 116-118, S. 497-507) Thermodynamik: Die π-bindung der Alkene ist um etwa 80 kj mol 1 schwächer
Kapitel 5: Additionen an C-C- Mehrfachbindungen
 Kapitel 5: Additionen an C-C- hrfachbindungen» Theorie, Konzepte, chanismus - MO Theorie: elektrophile Addition (Brom/Olefin) und [2+4]- Cycloaddition (Diels-Alder-Reaktion) - Bromierung der Doppelbindung:
Kapitel 5: Additionen an C-C- hrfachbindungen» Theorie, Konzepte, chanismus - MO Theorie: elektrophile Addition (Brom/Olefin) und [2+4]- Cycloaddition (Diels-Alder-Reaktion) - Bromierung der Doppelbindung:
2.1 Homologe Reihe, Nomenklatur, Konstitution, Konformation CH 2
 Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
REAKTIONEN DER ORGANISCHEN CHEMIE
 REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
Eliminierungsreaktionen: E1- und E2- Mechanismen; Olefine
 Eliminierungsreaktionen: E1 und E2 chanismen; lefine Allgemeine Gleichung der Eliminierung: Base X X Die Bindung wird am Atom gebrochen. Für die Qualität der Abgangsgruppe X gelten die selben egeln wie
Eliminierungsreaktionen: E1 und E2 chanismen; lefine Allgemeine Gleichung der Eliminierung: Base X X Die Bindung wird am Atom gebrochen. Für die Qualität der Abgangsgruppe X gelten die selben egeln wie
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Inhaltsübersicht zur Vorlesung Experimentalchemie Organische Chemie
 1. Allgemeines Funktionelle Gruppen und Substanzklassen. Methoden zur Strukturaufklärung, Projektionen (Keil-Strich, Sägebock, Fischer, Newman) 2. Bindungstheorie Hybridisierung, MO-Schema, Mesomerie,
1. Allgemeines Funktionelle Gruppen und Substanzklassen. Methoden zur Strukturaufklärung, Projektionen (Keil-Strich, Sägebock, Fischer, Newman) 2. Bindungstheorie Hybridisierung, MO-Schema, Mesomerie,
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Vorlesung 20/21. Alkine sind Kohlenwasserstoffe mit einer CC-Dreifachbindung
 Vorlesung 0/1. Alkine sind Kohlenwasserstoffe mit einer -Dreifachbindung Nomenklatur (Vollhardt, 3. Aufl., S. 563-564, 4. Aufl. S. 631-63; art, S. 85-89; Buddrus, S. 87-88) Die längste Kette mit möglichst
Vorlesung 0/1. Alkine sind Kohlenwasserstoffe mit einer -Dreifachbindung Nomenklatur (Vollhardt, 3. Aufl., S. 563-564, 4. Aufl. S. 631-63; art, S. 85-89; Buddrus, S. 87-88) Die längste Kette mit möglichst
Aufgaben zu ungesättigten Kohlenwasserstoffen und ihren Reaktionen
 Aufgaben zu ungesättigten Kohlenwasserstoffen und ihren eaktionen wichtige Fachbegriffe: positive und negative induktive Effekte, elektrophile Addition, egel von Markovnikov, Eliminierung, cis-trans-isomerie
Aufgaben zu ungesättigten Kohlenwasserstoffen und ihren eaktionen wichtige Fachbegriffe: positive und negative induktive Effekte, elektrophile Addition, egel von Markovnikov, Eliminierung, cis-trans-isomerie
Organische Chemie Chemielaboranten 1-12
 Organische Chemie Chemielaboranten 1-12 1.2 Alkene Alkene- und Cycloalkene sind aliphatische respektive cycloaliphatische, ungesättigte Kohlenwasserstoffe mit einer oder mehreren Doppelbindungen. Die Endung
Organische Chemie Chemielaboranten 1-12 1.2 Alkene Alkene- und Cycloalkene sind aliphatische respektive cycloaliphatische, ungesättigte Kohlenwasserstoffe mit einer oder mehreren Doppelbindungen. Die Endung
Kunststoffe- Plastics
 Kunststoffe - Plastics Polymerisation / Polykondensation Polyaddition Kunststoffe - Allgemeines Begriffssammlung im Kunststoff-Umfeld: Polyaddition, PE, PET, Polystyrol, Polymere, Styropor, Poly-, Elastan,
Kunststoffe - Plastics Polymerisation / Polykondensation Polyaddition Kunststoffe - Allgemeines Begriffssammlung im Kunststoff-Umfeld: Polyaddition, PE, PET, Polystyrol, Polymere, Styropor, Poly-, Elastan,
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. hristoffers, Vorlesung Organische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. inführung 1.1 Atomorbitale Die Atome im Molekülverband werden durch lektronen
Prof. hristoffers, Vorlesung Organische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. inführung 1.1 Atomorbitale Die Atome im Molekülverband werden durch lektronen
[4+2] Cycloaddition Diels Alder
![[4+2] Cycloaddition Diels Alder [4+2] Cycloaddition Diels Alder](/thumbs/53/32900999.jpg) [4+2] Cycloaddition Diels Alder Additionsreaktion zwischen einem 1,3 Dien und einem Alken (Dienophil). Methode zur Synthese von einfach ungesättigten 6 Ringen. 3 Bindungen werden zu 2 Bindungen und einer
[4+2] Cycloaddition Diels Alder Additionsreaktion zwischen einem 1,3 Dien und einem Alken (Dienophil). Methode zur Synthese von einfach ungesättigten 6 Ringen. 3 Bindungen werden zu 2 Bindungen und einer
CCl 3. 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan
 V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
Unterrichtsstunde zum Thema Kunststoffe. von Stefan Döge
 Unterrichtsstunde zum Thema Kunststoffe von Stefan Döge Inhalt 1. Begriff Kunststoff und Einteilung 2. Kunststoffarten 3. Reaktionsarten 4. Taktizität, Copolymere 5. Verarbeitung 6. Wiederverwertung 7.
Unterrichtsstunde zum Thema Kunststoffe von Stefan Döge Inhalt 1. Begriff Kunststoff und Einteilung 2. Kunststoffarten 3. Reaktionsarten 4. Taktizität, Copolymere 5. Verarbeitung 6. Wiederverwertung 7.
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Ziegler Natta Katalysatoren. Dennis Weber
 en Dennis Weber Inhalt Polymerisation Am Beispiel Ethen Ziegler Natta Polymerisation Taktizität Ziegler Natta Katalysator Metallocenkatalysatoren Polymerisation Hochdruckpolymerisation von Ethen seit 1935
en Dennis Weber Inhalt Polymerisation Am Beispiel Ethen Ziegler Natta Polymerisation Taktizität Ziegler Natta Katalysator Metallocenkatalysatoren Polymerisation Hochdruckpolymerisation von Ethen seit 1935
Makromoleküle sind keine Erfindung des Menschen. Die Natur produziert jährlich mehr als Tonnen Polysaccharide und Lignin.
 Vorlesung 22 Polymere Allgemein istoriker teilen die Menschheitsgeschichte nach den vorwiegend verwendeten Werkstoffen ein: Steinzeit, Bronzezeit, Eisenzeit 1980 hat der Wert der Weltkunststoff-Produktion
Vorlesung 22 Polymere Allgemein istoriker teilen die Menschheitsgeschichte nach den vorwiegend verwendeten Werkstoffen ein: Steinzeit, Bronzezeit, Eisenzeit 1980 hat der Wert der Weltkunststoff-Produktion
H 3 C 1. 1-Brom-4-methyl-1-penten (nicht: 5-Methyl-3-hexen)
 Alkene und Alkine Merkmal von Salatöl: enthält --Doppelbindungen. Oft werden Alkene durch Eliminierung dargestellt. Umgekehrt kann eine Doppelbindung durch Addition wieder in eine Einfachbindung umgewandelt
Alkene und Alkine Merkmal von Salatöl: enthält --Doppelbindungen. Oft werden Alkene durch Eliminierung dargestellt. Umgekehrt kann eine Doppelbindung durch Addition wieder in eine Einfachbindung umgewandelt
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Physikalische Eigenschaften der Alkohole
 Physikalische Eigenschaften der Alkohole Die Struktur von Alkoholen ist ähnlich der von Wasser 96pm 110pm 143pm 96pm Methanol 109 104.5 108.9 I_folie228 Wasserstoffbrückenbindungen: BDE = 21KJ/mol 207pm
Physikalische Eigenschaften der Alkohole Die Struktur von Alkoholen ist ähnlich der von Wasser 96pm 110pm 143pm 96pm Methanol 109 104.5 108.9 I_folie228 Wasserstoffbrückenbindungen: BDE = 21KJ/mol 207pm
Std. Stoffklassen Konzepte & Methoden Reaktionen 2 Struktur und Bindung 2 Alkane Radikale Radikal-Reaktionen 2 Cycloalkane Konfiguration &
 Materialien (Version: 26.06.2001) Diese Materialien dienen zur Überprüfung des Wissens und sind keine detailierten Lernunterlagen. Vorschlag: fragen Sie sich gegenseitig entsprechend dieser Listen ab.
Materialien (Version: 26.06.2001) Diese Materialien dienen zur Überprüfung des Wissens und sind keine detailierten Lernunterlagen. Vorschlag: fragen Sie sich gegenseitig entsprechend dieser Listen ab.
1. Klausur zur Vorlesung. Einführung in die organische Chemie WS 03/04 11.12.2003
 1. Klausur zur Vorlesung Einführung in die organische Chemie WS 03/04 11.12.2003 Vorname (bitte deutlich schreiben): Nachname (bitte deutlich schreiben): Matrikelnummer: Studiengang: o Chemie (Diplom)
1. Klausur zur Vorlesung Einführung in die organische Chemie WS 03/04 11.12.2003 Vorname (bitte deutlich schreiben): Nachname (bitte deutlich schreiben): Matrikelnummer: Studiengang: o Chemie (Diplom)
1. Übungsblatt Radikale
 Prof. Dr. liver Reiser Institut für rganische Chemie Universität Regensburg 1. Übungsblatt Radikale Aufgabe 1: Mittels radikalischer Chlorierung oder omierung können Alkylhalogenie aus Alkanen effektiv
Prof. Dr. liver Reiser Institut für rganische Chemie Universität Regensburg 1. Übungsblatt Radikale Aufgabe 1: Mittels radikalischer Chlorierung oder omierung können Alkylhalogenie aus Alkanen effektiv
Alkane als Kraftstoffe
 Alkane als Kraftstoffe Du hast bereits gelernt, dass bei der fraktionierten Destillation Alkane erhalten werden können, die geeignet sind als Kraftstoffe eingesetzt zu werden. Unterschiedliche Motoren
Alkane als Kraftstoffe Du hast bereits gelernt, dass bei der fraktionierten Destillation Alkane erhalten werden können, die geeignet sind als Kraftstoffe eingesetzt zu werden. Unterschiedliche Motoren
Substituenten-Effekt auf die Orientierung der Zweitsubstituenten Orientierung bei der Toluolsubstitution
 Substituenten-Effekt auf die rientierung der Zweitsubstituenten rientierung bei der Toluolsubstitution I_folie215 3 3 3 3 meta para 58 % Nitrierung 4 % 38 % = N 2 N 3 / 2 S 4 Sulfonierung 32 % 6 % 62 %
Substituenten-Effekt auf die rientierung der Zweitsubstituenten rientierung bei der Toluolsubstitution I_folie215 3 3 3 3 meta para 58 % Nitrierung 4 % 38 % = N 2 N 3 / 2 S 4 Sulfonierung 32 % 6 % 62 %
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Inhaltsverzeichnis zu Kapitel 2. Alkane
 Inhaltsverzeichnis zu Kapitel 2. Alkane 2. Alkane 2.1. Valenzstrichformel, omologe Reihe, Nomenklatur, Konstitution, 22 Konformation 2.1.1. Valenzstrichformel 22 2.1.2. omologe Reihe 23 2.1.3. Konstitutionsisomere
Inhaltsverzeichnis zu Kapitel 2. Alkane 2. Alkane 2.1. Valenzstrichformel, omologe Reihe, Nomenklatur, Konstitution, 22 Konformation 2.1.1. Valenzstrichformel 22 2.1.2. omologe Reihe 23 2.1.3. Konstitutionsisomere
Organische Chemie I. OC I Lehramt F. H. Schacher 1
 Organische Chemie I OC I Lehramt F. H. Schacher 1 8. Ether 8.1. Allgemeines 8.2. Nomenklatur + wichtige Vertreter 8.3. Synthesen 8.4. Reaktionen 8.5. Kronenether 8.6. Ether als Schutzgruppen 8.7. Ether
Organische Chemie I OC I Lehramt F. H. Schacher 1 8. Ether 8.1. Allgemeines 8.2. Nomenklatur + wichtige Vertreter 8.3. Synthesen 8.4. Reaktionen 8.5. Kronenether 8.6. Ether als Schutzgruppen 8.7. Ether
CHE 172.1: Organische Chemie für die Life Sciences
 1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
Kohlenstoffverbindungen
 Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Carbonyl- und Enolatchemie
 Carbonyl- und Enolatchemie 1 Addition von rganometall-eagenzien an Carbonylverbindungen eformatzky-eaktion: Zn-eagenz weniger reaktiv als Grignard, greift keine Ester an! Br 2 Zn ZnBr 2 Br Zn 2 1 2 Barbier-eaktion:
Carbonyl- und Enolatchemie 1 Addition von rganometall-eagenzien an Carbonylverbindungen eformatzky-eaktion: Zn-eagenz weniger reaktiv als Grignard, greift keine Ester an! Br 2 Zn ZnBr 2 Br Zn 2 1 2 Barbier-eaktion:
M U S T E R L Ö S U N G
 Universität egensburg Institut für rganische Chemie Prof. Dr.. eiser 3. Klausur zum rganisch-chemischen Praktikum I für Studierende der Chemie und der Biochemie im SS 999 am Freitag, dem 3. Juli 999 M
Universität egensburg Institut für rganische Chemie Prof. Dr.. eiser 3. Klausur zum rganisch-chemischen Praktikum I für Studierende der Chemie und der Biochemie im SS 999 am Freitag, dem 3. Juli 999 M
Wiederholungs-Klausur zur Vorlesung OC1 "Organischen Chemie 1" SS 2013 am
 Wiederholungs-Klausur zur Vorlesung OC1 "Organischen Chemie 1" SS 2013 am 11.10.2013 A Name...MUSTERLÖSUNG... Vorname... Matrikel-Nr... Studiengang... Viel Erfolg! Bitte schreiben Sie Ihren Namen in BLOCKSCHRIFT
Wiederholungs-Klausur zur Vorlesung OC1 "Organischen Chemie 1" SS 2013 am 11.10.2013 A Name...MUSTERLÖSUNG... Vorname... Matrikel-Nr... Studiengang... Viel Erfolg! Bitte schreiben Sie Ihren Namen in BLOCKSCHRIFT
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe
 1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2016
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Nachtrag Aromatische Substitution Sicherheitsbelehrung: Regeln für das Arbeiten im Labor Prof. r. Rasmus Linser September 2016
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Nachtrag Aromatische Substitution Sicherheitsbelehrung: Regeln für das Arbeiten im Labor Prof. r. Rasmus Linser September 2016
Hydroxylderivate. Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit. Bruch der C-H- und der C-OBindungen. Prof. Dr. Ivo C.
 Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Moleküle mit mehr als einem Chiralitätselement
 Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Geänderter Termin zur Nachholklausur: 11.April, Uhr, H46. Klausur zur Vorlesung OCII Reaktionsmechanismen WS 2007/2008.
 liver eiser, Institut für rganische Chemie der Universität egensburg Geänderter Termin zur Nachholklausur: 11.April, 10-12 Uhr, 46 Klausur zur Vorlesung CII eaktionsmechanismen W 2007/2008 Lösungsblatt
liver eiser, Institut für rganische Chemie der Universität egensburg Geänderter Termin zur Nachholklausur: 11.April, 10-12 Uhr, 46 Klausur zur Vorlesung CII eaktionsmechanismen W 2007/2008 Lösungsblatt
4 Additionen an CC-Mehrfachbindungen
 4 Additionen n -Mehrfchindungen Thermodynmische Aspekte der Additionsrektionen n Ethylen Mittlere Bindungsenergien (hängig von der Art der Alkylreste): : 345 kj mol 1 =: 610 kj mol 1 : 837 kj mol 1 610
4 Additionen n -Mehrfchindungen Thermodynmische Aspekte der Additionsrektionen n Ethylen Mittlere Bindungsenergien (hängig von der Art der Alkylreste): : 345 kj mol 1 =: 610 kj mol 1 : 837 kj mol 1 610
Katalyse. Martin Babilon 14/07/2011. Katalyse. Martin Babilon Universität Paderborn. 14 Juli Montag, 18. Juli 2011
 Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
O H H 3 C. Methanol. Molekulargewicht Siedepunkt Löslichkeit in Wasser H 3 C-OH. unbegrenzt H 3 C-Cl. 7.4 g/l H 3 C-CH 3 -24/C -88/C
 Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen
 KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
Prof. Dr. Andreas Speicher
 BSc Plus MINT: Ringvorlesung Forschung in Natur- und Ingenieurwissenschaften Die Chemie der Kunststoffe Prof. Dr. Andreas Speicher Universität des Saarlandes Organische Chemie Universität des Saarlandes
BSc Plus MINT: Ringvorlesung Forschung in Natur- und Ingenieurwissenschaften Die Chemie der Kunststoffe Prof. Dr. Andreas Speicher Universität des Saarlandes Organische Chemie Universität des Saarlandes
Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig
 26 sisomerie (Stereoisomerie I) Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig Isomerie II: sisomere: sisomere (bzw. Konformere) sind Isomere, die sich durch
26 sisomerie (Stereoisomerie I) Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig Isomerie II: sisomere: sisomere (bzw. Konformere) sind Isomere, die sich durch
Übungsblatt 04 - OC I - SoSe 2014 (Prof. Bunz)
 Übungsblatt 04 - C I - SoSe 2014 (Prof. Bunz) 1. Setzen Sie die folgenden Verbindungen jeweils mit 2 und KMn 4 um (gefolgt von einer wässrigen Aufarbeitung) und zeichnen Sie die daraus resultierenden Reaktionsprodukte.
Übungsblatt 04 - C I - SoSe 2014 (Prof. Bunz) 1. Setzen Sie die folgenden Verbindungen jeweils mit 2 und KMn 4 um (gefolgt von einer wässrigen Aufarbeitung) und zeichnen Sie die daraus resultierenden Reaktionsprodukte.
Kunststoffe. Martina Gerardi, Maxym Hrytsay. Baustoffe 1. Zfi 2a
 Kunststoffe Martina Gerardi, Maxym Hrytsay Baustoffe 1 Zfi 2a Inhaltsverzeichnis Thermoplast... 2 Polyethylen PE... 2 Polypropylen PP... 2 Polystyrol PS... 2 Polyvinylchlorid PVC... 2 Polymethylmethacrylat
Kunststoffe Martina Gerardi, Maxym Hrytsay Baustoffe 1 Zfi 2a Inhaltsverzeichnis Thermoplast... 2 Polyethylen PE... 2 Polypropylen PP... 2 Polystyrol PS... 2 Polyvinylchlorid PVC... 2 Polymethylmethacrylat
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Inhaltsverzeichnis. 3 Gesättigte Kohlenwasserstoffe (Alkane) 3.1 Offenkettige Alkane 3.2 Cyclische Alkane
 Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik
 Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 34 Geben Sie die systematischen Namen jeder der folgenden Verbindungen an: Welche der Verbindungen aus Übung besitzen E- und
Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 34 Geben Sie die systematischen Namen jeder der folgenden Verbindungen an: Welche der Verbindungen aus Übung besitzen E- und
Aufgaben zur Chemie der Alkohole und Ether (incl. deren Herstellung)
 Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) C2CL Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer
Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) C2CL Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer
Kapitel 2: Eliminierungen unter Bildung von Alkenen + H 2
 Vorlesung C-II für Nebenfächler Kapitel : Eliminierungen unter Bildung von Alkenen Alkene sind wichtige technische Grundchemikalien für die organische Synthese und für die industrielle Produktion. Die
Vorlesung C-II für Nebenfächler Kapitel : Eliminierungen unter Bildung von Alkenen Alkene sind wichtige technische Grundchemikalien für die organische Synthese und für die industrielle Produktion. Die
Zusammenfassung 2. Teil
 Zusammenfassung 2. Teil Aromaten Wichtigste Vertreter: C 3 Vorkommen und Isolation: rdöl Verwendung: Lösungsmittel, Ausgangsmaterial für Synthesen Benzol (krebserregend) Toluol Bestandteil im Benzin, Benzolfreie
Zusammenfassung 2. Teil Aromaten Wichtigste Vertreter: C 3 Vorkommen und Isolation: rdöl Verwendung: Lösungsmittel, Ausgangsmaterial für Synthesen Benzol (krebserregend) Toluol Bestandteil im Benzin, Benzolfreie
Ein Alkan, dem ein H-Atom fehlt, wird Alkyl-Rest genannt. Der Name ergibt sich aus dem Alkan, jedoch mit der Endung yl:
 Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Homologe Reihe der Alkane. Benennung der Alkane. Konstitutionsisomerie. Isomerie. Was versteht man unter der Homologen Reihe der Alkane?
 Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Grundwissenkarten Hans-Carossa- Gymnasium
 Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Butan, Hexan, 3-Methyl-Pentan,...,Di-Chlor Ethan, 1,2-Di-Chlorethen, 1-Chlor-Butan, 2- Chlor Butan,...
 Butan, exan, 3-Methyl-Pentan,...,Di-Chlor Ethan, 1,2-Di-Chlorethen, 1-Chlor-Butan, 2- Chlor Butan,... Diese Oxidationsreaktion ist eine Radikalische ( bezogen auf auf das AGENS!) Substitution ( bezogen
Butan, exan, 3-Methyl-Pentan,...,Di-Chlor Ethan, 1,2-Di-Chlorethen, 1-Chlor-Butan, 2- Chlor Butan,... Diese Oxidationsreaktion ist eine Radikalische ( bezogen auf auf das AGENS!) Substitution ( bezogen
Kennsilbe. -an. -en -in. -yl. -ol. -al (VI) -on. (VII) -säure (VIII)
 Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Organische Chemie für MST 3. Lienkamp / Prucker / Rühe
 Organische Chemie für MST 3 Lienkamp / Prucker / Rühe Inhalt 3 Ether Nomenklatur, Herstellung, Reaktionen, Etherperoxide, Epoxide, SU 8 Alkohole Nomenklatur, Eigenschaften, Herstellung, Reaktionen, Oxidations
Organische Chemie für MST 3 Lienkamp / Prucker / Rühe Inhalt 3 Ether Nomenklatur, Herstellung, Reaktionen, Etherperoxide, Epoxide, SU 8 Alkohole Nomenklatur, Eigenschaften, Herstellung, Reaktionen, Oxidations
Prof. Dr. P. Rademacher Organische Chemie IV
 Prof Dr P ademacher rganische hemie IV arbene und itrene 1 Einleitung arbene sind Verbindungen mit zweibindigem Kohlenstoff, der ein Elektronensextett besitzt Einfachstes arben : 2 = thylen Substituierte
Prof Dr P ademacher rganische hemie IV arbene und itrene 1 Einleitung arbene sind Verbindungen mit zweibindigem Kohlenstoff, der ein Elektronensextett besitzt Einfachstes arben : 2 = thylen Substituierte
Kapitel 1: Alkene ihre Eigenschaften und Reaktionen
 Vorlesung C-II für Nebenfächler Kapitel 1: Alkene ihre Eigenschaften und eaktionen 1.1. Einführung Folie S.6: rbitalschema, typische Energiewerte Alkene sind direkt aus Erdölfraktionen durch Cracken usw.
Vorlesung C-II für Nebenfächler Kapitel 1: Alkene ihre Eigenschaften und eaktionen 1.1. Einführung Folie S.6: rbitalschema, typische Energiewerte Alkene sind direkt aus Erdölfraktionen durch Cracken usw.
Teil 3. Additionsreaktionen
 Teil 3 Additionsreaktionen 69 3.1 lektrophile Additionen (A ) 3.1.1 inleitung und Grundbegriffe Triebkraft von Additionsreaktionen. Die Grundlage der eaktivität von lefinen in Additionsreaktionen ist die
Teil 3 Additionsreaktionen 69 3.1 lektrophile Additionen (A ) 3.1.1 inleitung und Grundbegriffe Triebkraft von Additionsreaktionen. Die Grundlage der eaktivität von lefinen in Additionsreaktionen ist die
Übersicht: Organische Experimentalchemie für Mediziner und Zahnmediziner (122101) WS 2010/11. 7.Aufl., Kap. 11)
 Übersicht: Organische Experimentalchemie für Mediziner und Zahnmediziner (122101) Prof. Dr. Ernst-Ulrich Würthwein,, Organisch-Chemisches Institut, WWU Münster WS 2010/11 10/11,, Mo.-Fr. 8-98 Uhr A. Einführung:
Übersicht: Organische Experimentalchemie für Mediziner und Zahnmediziner (122101) Prof. Dr. Ernst-Ulrich Würthwein,, Organisch-Chemisches Institut, WWU Münster WS 2010/11 10/11,, Mo.-Fr. 8-98 Uhr A. Einführung:
Schulinterner Lehrplan für das Fach Chemie in Qualifikationsphase 1
 Schulinterner Lehrplan für das Fach Chemie in Qualifikationsphase 1 Grundkurs 1. Säuren, Basen und analytische Verfahren (Inhaltsfeld 2) (Kontext: Säuren und Basen in Alltagsprodukten) 6 Std. Säuren und
Schulinterner Lehrplan für das Fach Chemie in Qualifikationsphase 1 Grundkurs 1. Säuren, Basen und analytische Verfahren (Inhaltsfeld 2) (Kontext: Säuren und Basen in Alltagsprodukten) 6 Std. Säuren und
Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen
 2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene
Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene
Hoch effiziente asymmetrische Katalyse durch doppelte Aktivierung von Nucleophil und Elektrophil Jun-An Ma und Dominique Cahard Angew. Chem.
 och effiziente asymmetrische Katalyse durch doppelte Aktivierung von ucleophil und Elektrophil Jun-An Ma und Dominique Cahard Angew. Chem. 2004, 116, 4666-4683 1. Einleitung ymmetrische Katalysereaktionen
och effiziente asymmetrische Katalyse durch doppelte Aktivierung von ucleophil und Elektrophil Jun-An Ma und Dominique Cahard Angew. Chem. 2004, 116, 4666-4683 1. Einleitung ymmetrische Katalysereaktionen
Kunststoffe. Eigenschaften und Darstellungen
 Kunststoffe Eigenschaften und Darstellungen Philipps Universität Marburg Fachbereich 15: Chemie Experimentalvortrag Dozenten: Dr. Philipp Reiß Prof. Dr. Bernhard Neumüller Referent: Martin Stolze Was sind
Kunststoffe Eigenschaften und Darstellungen Philipps Universität Marburg Fachbereich 15: Chemie Experimentalvortrag Dozenten: Dr. Philipp Reiß Prof. Dr. Bernhard Neumüller Referent: Martin Stolze Was sind
7 Reaktionen von Carbonylverbindungen
 Übung zur Vorlesung rganische Chemie II eaktivität (Dr. St. Kirsch, Dr. A. Bauer) 7 eaktionen von Carbonylverbindungen 7.1 Ketone/Aldehyde und eteroatomnucleophile 7.1-70 Vervollständigen Sie die folgenden
Übung zur Vorlesung rganische Chemie II eaktivität (Dr. St. Kirsch, Dr. A. Bauer) 7 eaktionen von Carbonylverbindungen 7.1 Ketone/Aldehyde und eteroatomnucleophile 7.1-70 Vervollständigen Sie die folgenden
Kapitel 4: Eliminierung - Übersicht
 » Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
» Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 kript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 email: michael.mueller@rwthaachen.de eaktionsmechanismen und Namensreaktionen
kript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 email: michael.mueller@rwthaachen.de eaktionsmechanismen und Namensreaktionen
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
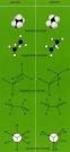 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Übergangsmetall-Verbindungen in der Organischen Synthese Prof. Dr. Günter Helmchen
 Übergangsmetall-Verbindungen in der Organischen Synthese Prof. Dr. Günter Helmchen Teil I 1. Einleitung, Übersicht, Literatur 2. -Komplexe 2.1 Einleitung, Übersicht 2.2 -Eliminierung (Mechanismus) 2.3
Übergangsmetall-Verbindungen in der Organischen Synthese Prof. Dr. Günter Helmchen Teil I 1. Einleitung, Übersicht, Literatur 2. -Komplexe 2.1 Einleitung, Übersicht 2.2 -Eliminierung (Mechanismus) 2.3
Grundlagen der organischen Chemie
 H. Kaufmann А. Hädener Grundlagen der organischen Chemie 10., vollständig neu überarbeitete und erweiterte Auflage Birkhäuser Verlag Basel Boston Berlin г 1.1 Definition der organischen Chemie 1 1.2 Unterschiede
H. Kaufmann А. Hädener Grundlagen der organischen Chemie 10., vollständig neu überarbeitete und erweiterte Auflage Birkhäuser Verlag Basel Boston Berlin г 1.1 Definition der organischen Chemie 1 1.2 Unterschiede
Grundlagen der Organischen Chemie
 Hendrik Zipse Grundlagen der Organischen Chemie 3. korrigierte Auflage Shaker Verlag Aachen 2014 Hendrik Zipse Grundlagen der Organischen Chemie 3. korrigierte Auflage Shaker Verlag Aachen 2014 Bibliografische
Hendrik Zipse Grundlagen der Organischen Chemie 3. korrigierte Auflage Shaker Verlag Aachen 2014 Hendrik Zipse Grundlagen der Organischen Chemie 3. korrigierte Auflage Shaker Verlag Aachen 2014 Bibliografische
Isomerie organischer Verbindungen
 15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1
 Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
3.2.2 Beschreiben Sie für jedes der beiden Moleküle die räumliche Anordnung der
 Abituraufgaben Alkene 1979/II/2 2.1 Chlorwasserstoff reagiert mit Buten -(1). Formulieren und begründen Sie den Ablauf der Reaktion. 2.2 Chlorwasserstoff reagiert mit Butadien -(1,3). Formulieren Sie die
Abituraufgaben Alkene 1979/II/2 2.1 Chlorwasserstoff reagiert mit Buten -(1). Formulieren und begründen Sie den Ablauf der Reaktion. 2.2 Chlorwasserstoff reagiert mit Butadien -(1,3). Formulieren Sie die
GRUNDLAGEN DER ORGANISCHEN CHEMIE
 Grundlagen der rganischen hemie Prof. Martens Vorlesung zu den GUDLAGE DE GAISE EMIE Wintersemester 2003 / 2004 Universität ldenburg 3 3 3 l 3 3 Mitschrift verfasst von Mika ashan Letzter Stand: 03. Juli
Grundlagen der rganischen hemie Prof. Martens Vorlesung zu den GUDLAGE DE GAISE EMIE Wintersemester 2003 / 2004 Universität ldenburg 3 3 3 l 3 3 Mitschrift verfasst von Mika ashan Letzter Stand: 03. Juli
Kunststoffe. Charakterisierung nach Eigenschaften. Wichtige Kunststofftypen
 Kunststoffe Kunststoff, oft auch Plastik (aus: engl. plastics) genannt, sind synthetisch hergestellte Stoffe, die man begrifflich von den Naturstoffen, wie zum Beispiel Holz, Leder, Horn, Gestein und Metallen
Kunststoffe Kunststoff, oft auch Plastik (aus: engl. plastics) genannt, sind synthetisch hergestellte Stoffe, die man begrifflich von den Naturstoffen, wie zum Beispiel Holz, Leder, Horn, Gestein und Metallen
