Kapitel 3: Nucleophile Substitution am gesättigten (sp 3 ) C-Atom
|
|
|
- Julian Dittmar
- vor 6 Jahren
- Abrufe
Transkript
1 Kapitel 3: ucleophile Substitution am gesättigten (sp 3 ) -Atom 3.1. Allgemeines Reaktionsschema und Grundlagen δ δ Solvens X YI Y Substrat ucleophil Substitutionsprodukt XI nucleofuge Abgangsgruppe (engl. leaving group) Reaktionstyp: Austausch eines Substituenten am gesättigten -Atom durch einen anderen. ucleophil und Abgangsgruppe entsprechen sich. Das angreifende ucleophil bringt sein freies Elektronenpaar zur Bindung ein, das ucleophil nimmt seine Bindungselektronen mit. Fragen: Welche Abgangsgruppen X kennt man, bzw. sind üblich? Welche ucleophile kommen in Frage, welche Produkte kann man herstellen. Wie ist der detaillierte Reaktionsmechanismus? Einflüsse darauf haben die Substratstruktur, die Abgangsgruppe, das ucleophil und nicht zuletzt das Solvens. Als Abgangsgruppen dienen meist die schon bei der Eliminierung bekannten alogensubstituenten I > Br > (Fluor nicht, ist inert) und die Tosylgruppe. e S z.b. 3 R S Me S F 3 Tosyl- Methylsulfat- Trifluorsulfonat- Triflat Faustregel: Eine Abgangsgruppe ist desto besser, je stärker die korrespondierende Säure ist. - ist eine erbärmliche Abgangsgruppe, - 2 ist eine gute Abgangsgruppe (vgl. Dehydratisierung von Alkoholen)! 1
2 Wie steht s mit den ucleophilen? ucleophile leben von der Qualität ihres freien Elektronenpaars. Faustregeln: In protischen Solventien (z.b. Ethanol) 1. Die ucleophilie ist desto besser je schwächer die korrespondierende Säure ist. z.b. - ist ein um Größenordnungen besseres ucleophil als Wasser. 2. ucleophile der höheren Perioden des PSE sind im Vergleich erheblich stärkere ucleophile In dipolar-aprotischen Lösungsmitteln (Aceton, Acetonitril Dimethylformamid etc.) gilt die obige Regel r. 2 nicht. Alle ucleophile werden reaktiver. Woran liegt das? In protischen Lösungsmitteln sind die kleinen Anionen der zweiten Periode sehr stark solvatisiert. Die großen Anionen der höheren Perioden haben wegen der größeren Kugeloberfläche eine geringere Ladungsdichte und sind deshalb weniger solvatisiert. ucleophilie einiger typischer ucleophile für die Reaktion mit Bromethan in Ethanol als Solvens Ph-Se - > Ph-Se - > PhP 3 > I - sehr gute > - > - > - > R 3 I gute > Br- > I 3 > Ph- - > -S- mittlere - > 3- - > > 2 > R- schwache Folie: Produktpalette, ucleophile Man kann die typischen ucleophile auch nach dem nucleophilen Atom sortieren: -ucleophile, -ucleophile, Se-ucleophile usw. Die X-ucleophile bringen ja das charakteristische Element mit in die neue Verbindung. 2
3 3.2. Ethersynthesen Einfache Ether aus primären Alkoholen: Primäre n 2n1 - werden mit katalytischer Menge konz. 2 S 4 erhitzt. 2 S 4 - Dibutylether Abgangsgruppe: 2, ucleophil: der Alkohol, hier Butanol. Ist mechanistisch eine S 2-Reaktion Funktioniert nur für symmetrische Ether Mit sekundären/tert. Alkoholen geht das nicht. Warum? Alkenbildung! Dehydratiserung! Williamsonsche Ethersynthese: Unsymmetrisches Beispiel: Ethylpentylether 1. Erzeugung von a-ethanolat a-metall a 1/ zugeben: 1-Butylchlorid Erhitzen a (Das Ethanol sollte wasserfrei sein) a allgemein: R- - a R X R--R a X - Eine typische S 2-Reaktion. Geht am besten mit primären Alkylhalogeniden und primären Alkoholaten. Bei Verzweigung Verluste durch Eliminierung. Phenolether sind leichter herzustellen, man braucht nur atronlauge zu: pks von Phenol ca. 10 besonders mit ilfe der Phasentransferkatalyse! 3
4 Analog zu den Ethern kann man auch Thioether herstellen. Dazu muss ein Alkylhalogenid oder tosylat mit einem Alkylsulfid oder Arylsulfid umgesetzt werden. Auch hier geht viel leichter als bei den -Ethern. Warum? Weil wiederum der pks-wert in der gleichen Größenordnung wie die Phenole. Beipiele: Ph- 2 -Br as Ph- 2 -S ein Thiol Butyl Br ½ 2 S Bu-S-Bu PhS a Ph-S - a in Et Ph-S - a Br( 2 ) 7 Ph-S-( 2 ) 7 abr 3.3. Phasentransferkatalyse Phasentransferkatalyse Ph- - a n- 4 9 Br keine Reaktion Ph--a n- 4 9 Br "Adogen-'' Ph n-h 4 9 -Ph BuBr Br-Ph ADG Br - ADG Ph- rganische Phase Wasser 3 polarer BuBr abr Ph- - a weniger polar 4
5 3.4. Stickstoffnucleophile sind etwas anders zu handhaben, wegen ihrer Basizität. Modellreaktion: 1-hlorbutan 3 z.b. Einleiten in eine Lösung in Methanol Tetrabutylammonium-hlorid ein Quartäres Ammoniumsalz Unter industriellen Bedingungen vermeidet man die Bildung des Quartärsalz und trennt die primären, sekundären und tertiären Amine durch Destillation, nachdem man mit a oder a 3 alle Ammoniumsalze freigesetzt hat. Durch das alogenalkan wird das Produktverhältnis bestimmt oder beeinflußt. Die Quartärsalze erhält man durch Umsetzung des tertiären Amins mit dem Alkylierungsmittel. (ADGE!!!, siehe Phasentransferkatalyse) 5
6 Spezialfälle: Synthese von Glycin, einfachsten Aminosäure: hloressigsäure 3 /( 4 ) Im Isoelektrischen Punkt fällt die zwitterionische Form aus. Synthese primärer Amine nach GABRIEL K Et K R-X - K X - X K/ 2 R- 2 Vermeidung der mehrfachen Alkylierung. Insbesondere auch zur Einführung der Aminogruppe bei manchen Aminosäuresynthesen. yanid als Kohlenstoffnucleophil: 2 I I a 2 I a ebenprodukt (erbärmlich stinkend): I [Ein Isocyanid, Phänomen des ambidenten Anions (zweizähnig)]die yanogruppe kann zum Benzylamin hydriert werden oder durch ydrolyse zur 6
7 arbonsäure verseift werden! Weitere -ucleophile in Kapitel V! 3.5. Zum Mechanismus von S 2-Reaktion: Alle bisher behandelte Substitutionsreaktionen sind S2-Reaktionen. Bekannt ist der "Regenschirm-Mechanismus" auf molekularer Ebene (in der Vorstellung, die man sich von Molekülen macht): YI δ δ X solvens δ δ Y XI RG = d[ry/dt = k 2 [RX][Y-] Übergangszustand: ÜZ Y X G RX YI - RY XI - G Reaktion Relative Reaktionsgeschwindigkeit der S2-Reaktion an Alkylhalogeniden -X 1 2 -X 3 x X 1 x X- 8 x 10-4 ( ) 2-2 -X 9 x 10-4 ( ) 3 -X <
8 Stereoelektronische Visualisierung u : X lineare Anordnung Substrat u : X u sekundär Alkylgruppe u : no chance X Konsequenz des "Umklappens": Inversion des Tetraeders. Man sieht s aber nur wenn man mit geeigneten substituierten ycloalkan oder mit einem chiralen, nichtracemischen Edukt arbeitet. Definition für eine chirale Substanz: EE = Enantiomerenüberschuß (in Prozent) EE = () ( ) () (-) x 100 EE = 100: enantiomerenrein; 100 > EE > 0: nichtracemisch; EE = 0: racemisch Analoge Definitionen gelernt für Diastereomere (DE = Diastereomerenüberschuß usw.) 8
9 Überführung eines Enantiomeren in spiegelbildliche Enantiomer durch eine S 2- Prozedur. Man nennt diese peration WALDE-yclus. Walden hat 1896 als Erster einen solchen yclus nachgewiesen, ohne den genauen Reaktionsmechanismus zu kennen. Statt dem riginalexperiment ein besser überschaubares Beispiel: 3 S Ph 2 20 [α] = D 33 = Tos S 2 in Pyridin 3 Ph 2 - a Et S Tos Inversion R Ph 2 20 [α] = - 32,2 D a Et/ 2 R Ac Ph 2 achweis der Inversion an einem achiralen Beispiel Et, Erh. 3 Tos a ISe-Ph - 3 Se-Ph SePh Die S 2-Reaktion ist wertvoll, weil die stereochemische Information erhalten bleibt. Aber die Reaktion versagt, wenn durch sterische inderung die Annäherung des angreifenden ucleophils verhindert wird. Ist dies der Fall beobachtet man stattdessen die Eliminierung zum Alken. Sofern die Basizität ausreicht werden ein Proton und die Abgangsgruppe abgespalten (E 2 ). 9
10 z.b. 3 Br a Et E 2 S Solvolyse / S 1-Reaktion Gute Abgangsgruppen: Alkylhalogenide, Tosylate und noch bessere, z.b. F 3 -S-R Verzweigung am Reaktionszentrum Weitere elektronenziehende Substituenten Sehr polares Lösungsmittel: z.b. Methanol, Ethanol Wasser/Ethanol, Wasser/Ameisensäure (Zusatz von 2 erhöht die Polarität) Beispiele: 3 Br Solv. Et 3 3 Et Et S E 1 3 Br Et (80) 2 (20) 25 Et 29% 58% 13% E 1 E1 S 1 10
11 ÜZ I gemeinsame Zwischenstufe ÜZ II 13% 29% verschiedene Produkte R-X, Solvens 58% Die Bildung des arbeniumions erfolgt mit mit einer unimolekularen Kinetik (S 1), welche die gemessene Kinetik ist. Von der Zwischenstufe arbeniumion ausgehend können mehrere Produkte gebildet werden. 3.7 Bildung von alogenverbindungen a) durch Addition von X an Alkene b) durch Addition von alogenen an Alkene c) durch Substitution alogene sind in Form der Anionen nicht nur Abgangsgruppen, sie sind auch ucleophile, wenn Substrtate mit geeigneten Abgangsgruppen zur Verfpgun stehen. 1. Reaktion von Alkoholen mit alogenwasserstoffen an primären Alkylhalogeniden -( 2 ) konz. Br/konz. 2 S 4 -( 2 ) 6-2 -Br 2 eigentliches Substrat ist der protonierte Alkohol: Wasser ist eine gute Abgangsgruppe, - - nur eine schlechte. 2. Reaktionen von tertiären Alkoholen mit alogenwasserstoffen -X X 2 oft in Minuten im Scheidetrichter unter Bildung des Alkylhalogenids als organische Phase. 11
12 3. Aus Alkoholen mit mineralischen Säurehalogeniden S 2, P 3, PBr 3, P(rot) Iod = PI3 in situ. z.b.: S2 - S S 2 ist eine S 2 -Reaktion mit einer guten Abgangsgruppe 4. Substitution an Tosylaten ier bedarf es eines besonderen Typs von Lösungsmitteln Apolare Solventien Protische Solventien - 2 Dipolar-aprotische Solventien δ δ δ δ 3 δ δ 3 Aceton Acetonitril Dimethylformamid 12
13 Die positive Ladung ist am eteroatom konzentriert, die negative Ladung ist über mehrere Atome verteilt. Dipolar-aprotische LM solvatisieren bevorzugt Kation, deshalb steigt die ucleophilie der Anionen. Die alogenidionen zeigen jetzt die Reihenfolge: (F ) > > Br > I Anwendungsbeispiel (für primäre und sekundäre Substrate): Tos Pyridin Tos Li DMF 13
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
CCl 3. 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan
 V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
Halogenalkane. Radikalische Halogenierung von Alkanen. Addition von Halogenwasserstoffen an Alkene. H 3 C + HBr H C C C H.
 alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
Übungsblatt 6 - Lösung
 Übungen rganische hemie für Studierende der Lehrämter und der Biologie (Diplom), WS 2003/04 Dr.. abrele Übungsblatt 6 - Lösung 1. n-butylbromid, sec-butylbromid und tert-butylbromid werden jeweils mit
Übungen rganische hemie für Studierende der Lehrämter und der Biologie (Diplom), WS 2003/04 Dr.. abrele Übungsblatt 6 - Lösung 1. n-butylbromid, sec-butylbromid und tert-butylbromid werden jeweils mit
N H H. Carbanionen Lewis-Basen Olefine (Alkane) Die Stärke der Nucleophilie wird von versch. Faktoren beeinflußt z.b.
 Organische hemie Nucleophil = kernliebend Nucleophil = Teilchen oder Gruppe, die Lewis-basische Eigenschaften aufweist (also mind. ein freies Elektronenpaar besitzt), es gibt neutrale Nucleophile sowie
Organische hemie Nucleophil = kernliebend Nucleophil = Teilchen oder Gruppe, die Lewis-basische Eigenschaften aufweist (also mind. ein freies Elektronenpaar besitzt), es gibt neutrale Nucleophile sowie
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Nucleophile Substitution
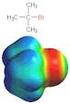 3. Nucleophile Substitution 3.1 Nucleophile Substitution Vom alogenalkan zum Alkohol Erhitzt man eine heterogene Mischung aus Bromethan und Kalilauge, so wird das Gemisch homogen. Es entsteht das wasserlösliche
3. Nucleophile Substitution 3.1 Nucleophile Substitution Vom alogenalkan zum Alkohol Erhitzt man eine heterogene Mischung aus Bromethan und Kalilauge, so wird das Gemisch homogen. Es entsteht das wasserlösliche
3 Eliminierungen. 3.1 Begriffe und mechanistische Einteilung. Abspaltung zweier Atome bzw. Atomgruppen aus einem Molekül
 3 Eliminierungen 3.1 Begriffe und mechanistische Einteilung Abspaltung zweier Atome bzw. Atomgruppen aus einem Molekül Einteilung nach den Positionen der abgespaltenen Gruppen 1,1-Eliminierung (α-eliminierung)
3 Eliminierungen 3.1 Begriffe und mechanistische Einteilung Abspaltung zweier Atome bzw. Atomgruppen aus einem Molekül Einteilung nach den Positionen der abgespaltenen Gruppen 1,1-Eliminierung (α-eliminierung)
Kapitel 2: Eliminierungen unter Bildung von Alkenen + H 2
 Vorlesung C-II für Nebenfächler Kapitel : Eliminierungen unter Bildung von Alkenen Alkene sind wichtige technische Grundchemikalien für die organische Synthese und für die industrielle Produktion. Die
Vorlesung C-II für Nebenfächler Kapitel : Eliminierungen unter Bildung von Alkenen Alkene sind wichtige technische Grundchemikalien für die organische Synthese und für die industrielle Produktion. Die
Kapitel 4: Eliminierung - Übersicht
 » Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
» Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
1. Klausur zum Praktikum Organische Chemie I für Studierende der Chemie und der Biochemie im SS 2000
 Prof. Dr. B. König Prof. Dr. Th. Troll 1. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Dienstag, dem 30. Mai 2000 Name: Mustermann...Vorname: Max...
Prof. Dr. B. König Prof. Dr. Th. Troll 1. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Dienstag, dem 30. Mai 2000 Name: Mustermann...Vorname: Max...
Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff
 Vorlesung 16 Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff Bimolekulare nucleophile Substitutionen (S N 2-Reaktionen) In Vorlesung 11 hatten wir bereits die nucleophile Substitution
Vorlesung 16 Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff Bimolekulare nucleophile Substitutionen (S N 2-Reaktionen) In Vorlesung 11 hatten wir bereits die nucleophile Substitution
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Organische Chemie für Bioinformatiker. Dozentin: Dr. Stefanie Kellner 3. Stock BioSysM: Raum 03.
 Organische Chemie für Bioinformatiker Dozentin: Dr. Stefanie Kellner Email: stefanie.kellner@cup.lmu.de 3. Stock BioSysM: Raum 03.037F 1 BioSysM 2 Vorlesungsplan Reaktionen in der organischen Chemie Elektrophile
Organische Chemie für Bioinformatiker Dozentin: Dr. Stefanie Kellner Email: stefanie.kellner@cup.lmu.de 3. Stock BioSysM: Raum 03.037F 1 BioSysM 2 Vorlesungsplan Reaktionen in der organischen Chemie Elektrophile
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Aufgaben zur Chemie der Alkohole und Ether (incl. deren Herstellung)
 Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Nucleophile Katalyse am Beispiel von 4-(Dimethylamino)pyridin
 Nucleophile Katalyse am Beispiel von 4-(Dimethylamino)pyridin Matthias Kellermeier Einordnung der nucleophilen Katalyse und Beispiele nucleophiler Katalysatoren Nucleophile Katalyse bislang wenig erforscht;
Nucleophile Katalyse am Beispiel von 4-(Dimethylamino)pyridin Matthias Kellermeier Einordnung der nucleophilen Katalyse und Beispiele nucleophiler Katalysatoren Nucleophile Katalyse bislang wenig erforscht;
Die verschiedenen Mechanismen der Nucleophilen Substitution
 Die verschiedenen Mechanismen der Nucleophilen Substitution Dinah Shafry 21. Juni 2010 Inhalt Vom Alkan zum Alkohol...2 Struktur der Alkane...2 Die Lösung des Problems...2 Die nucleophile Substitution...2
Die verschiedenen Mechanismen der Nucleophilen Substitution Dinah Shafry 21. Juni 2010 Inhalt Vom Alkan zum Alkohol...2 Struktur der Alkane...2 Die Lösung des Problems...2 Die nucleophile Substitution...2
Halogenderivate der Alkane
 Halogenderivate der Alkane Einteilung - gesättigte und ungesättigte Halogenverb. - nach der Anzahl der -Atome, = 1,2,3, - Dihalogenide: n geminale vicinale disjunkt H 2 H 2 H H 2 primäre, sekundäre, terciäre
Halogenderivate der Alkane Einteilung - gesättigte und ungesättigte Halogenverb. - nach der Anzahl der -Atome, = 1,2,3, - Dihalogenide: n geminale vicinale disjunkt H 2 H 2 H H 2 primäre, sekundäre, terciäre
Physikalische Eigenschaften der Alkohole
 Physikalische Eigenschaften der Alkohole Die Struktur von Alkoholen ist ähnlich der von Wasser 96pm 110pm 143pm 96pm Methanol 109 104.5 108.9 I_folie228 Wasserstoffbrückenbindungen: BDE = 21KJ/mol 207pm
Physikalische Eigenschaften der Alkohole Die Struktur von Alkoholen ist ähnlich der von Wasser 96pm 110pm 143pm 96pm Methanol 109 104.5 108.9 I_folie228 Wasserstoffbrückenbindungen: BDE = 21KJ/mol 207pm
O H H 3 C. Methanol. Molekulargewicht Siedepunkt Löslichkeit in Wasser H 3 C-OH. unbegrenzt H 3 C-Cl. 7.4 g/l H 3 C-CH 3 -24/C -88/C
 Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Aufgaben zur Chemie der Alkohole und Ether (incl. deren Herstellung)
 Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) C2CL Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer
Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) C2CL Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer
Übung Nr. 13. Vorlesung Allgemeine Chemie II Teil Organische Chemie Frühjahrssemester Mi bzw. Fr
 Übung Nr. 13 Mi. 30.05.2012 bzw. Fr. 01.06.2012 1. Eliminierungen I Geben Sie für die untenstehenden Reaktionen die jeweiligen Produkte an! Um welche Namensreaktion handelt es sich? Welcher Typ Eliminierung
Übung Nr. 13 Mi. 30.05.2012 bzw. Fr. 01.06.2012 1. Eliminierungen I Geben Sie für die untenstehenden Reaktionen die jeweiligen Produkte an! Um welche Namensreaktion handelt es sich? Welcher Typ Eliminierung
Synthese von Alkylhalogeniden: R X (X = F, Cl, Br, I)
 Synthese von Alkylhalogeniden: R X (X = F, l,, I) I_folie107 1) Radikalische Substitution: R + X 2 T oder hν R X + X (X = F, l, ) 2) Elektrophile Addition an Alkene: + X R 2 R 2 (X = l,, I) R 2 R 2 X Alken
Synthese von Alkylhalogeniden: R X (X = F, l,, I) I_folie107 1) Radikalische Substitution: R + X 2 T oder hν R X + X (X = F, l, ) 2) Elektrophile Addition an Alkene: + X R 2 R 2 (X = l,, I) R 2 R 2 X Alken
Nucleophile Substitutionsreaktionen am gesättigten C-Atom
 ucleophile Substitutionsreaktionen am gesättigten C-Atom 2 2.1 ucleophile und Elektrophile; Abgangsgruppen Etwas überspitzt ausgedrückt, ist rganische Chemie deshalb verhältnismäßig einfach erlernbar,
ucleophile Substitutionsreaktionen am gesättigten C-Atom 2 2.1 ucleophile und Elektrophile; Abgangsgruppen Etwas überspitzt ausgedrückt, ist rganische Chemie deshalb verhältnismäßig einfach erlernbar,
b) Zeichnen Sie die beiden möglichen Isomere der Aldol-Kondensation und bezeichnen Sie die Stereochemie der Produkte.
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
Organische Chemie I Molekül der Woche - Azulen
 I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
2.3 Die S N 2-Reaktion (Bimolekulare nucleophile Substitution)
 23 Die 2-eaktion (Bimolekulare nucleophile ubstitution) Y: + X Y X Y + X: Übergangszustand E eaktanten X + Y Produkte Y+ X eaktionskoordinate Kinetisches Kriterium: eaktion 2 rdnung d[x] dt = k 2 [X] [Y
23 Die 2-eaktion (Bimolekulare nucleophile ubstitution) Y: + X Y X Y + X: Übergangszustand E eaktanten X + Y Produkte Y+ X eaktionskoordinate Kinetisches Kriterium: eaktion 2 rdnung d[x] dt = k 2 [X] [Y
LÖSUNGEN DER AUFGABEN ZUM 5. PRAKTIKUM
 LÖUNGEN DER AUFGABEN ZUM 5. PRAKTIKUM 1. Elektrophile und nukleophile Teilchen Elektrophile Teilchen: Es handelt sich um Elektronenpaarakzeptoren, also LEWI-äuren. Beispiele sind: +, Br +, I +, BF3, All3,
LÖUNGEN DER AUFGABEN ZUM 5. PRAKTIKUM 1. Elektrophile und nukleophile Teilchen Elektrophile Teilchen: Es handelt sich um Elektronenpaarakzeptoren, also LEWI-äuren. Beispiele sind: +, Br +, I +, BF3, All3,
Teil 2. Substitutionsreaktionen an Aliphaten
 Teil 2 Substitutionsreaktionen an Aliphaten 27 2.1 cleophile Substitutionen (S N ) 2.1.1 Einleitung und Grundbegriffe Bei Substitutionsreaktionen wird ein Molekülteil durch einen anderen verdrängt. Bei
Teil 2 Substitutionsreaktionen an Aliphaten 27 2.1 cleophile Substitutionen (S N ) 2.1.1 Einleitung und Grundbegriffe Bei Substitutionsreaktionen wird ein Molekülteil durch einen anderen verdrängt. Bei
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1
 Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
a) Vervollständigen Sie das Freie-Enthalpie-Diagramm der Reaktion, indem Sie den zutreffenden Buchstaben A D in die leeren Kreise setzen:
 1. Aufgabe Für die Reaktion R-X + u R-u + X findet man folgendes Reaktionsdiagramm: a) Vervollständigen Sie das Freie-Enthalpie-Diagramm der Reaktion, indem Sie den zutreffenden Buchstaben A D in die leeren
1. Aufgabe Für die Reaktion R-X + u R-u + X findet man folgendes Reaktionsdiagramm: a) Vervollständigen Sie das Freie-Enthalpie-Diagramm der Reaktion, indem Sie den zutreffenden Buchstaben A D in die leeren
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 kript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 email: michael.mueller@rwthaachen.de eaktionsmechanismen und Namensreaktionen
kript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 email: michael.mueller@rwthaachen.de eaktionsmechanismen und Namensreaktionen
R OH R SH HO HS Alkanol Alkanthiol Hydroxy-Gruppe Mercapto-Gruppe
 Vorlesung 32 Thioalkohole (= Thiole, Mercaptane) und Thioether (Vollhardt, 3. Aufl.,. 363-366, 4. Aufl.,. 415-419 Mitte; art,. 272-273; Buddrus,. 279-284) sind die chwefelanaloga der Alkohole und Ether.
Vorlesung 32 Thioalkohole (= Thiole, Mercaptane) und Thioether (Vollhardt, 3. Aufl.,. 363-366, 4. Aufl.,. 415-419 Mitte; art,. 272-273; Buddrus,. 279-284) sind die chwefelanaloga der Alkohole und Ether.
Geänderter Termin zur Nachholklausur: 11.April, Uhr, H46. Klausur zur Vorlesung OCII Reaktionsmechanismen WS 2007/2008.
 liver eiser, Institut für rganische Chemie der Universität egensburg Geänderter Termin zur Nachholklausur: 11.April, 10-12 Uhr, 46 Klausur zur Vorlesung CII eaktionsmechanismen W 2007/2008 Lösungsblatt
liver eiser, Institut für rganische Chemie der Universität egensburg Geänderter Termin zur Nachholklausur: 11.April, 10-12 Uhr, 46 Klausur zur Vorlesung CII eaktionsmechanismen W 2007/2008 Lösungsblatt
Selbsteinschätzungstest zum Vorkurs Organische Chemie
 WS 15/16 1/16 Selbsteinschätzungstest zum Vorkurs rganische hemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NIT die späteren Studieninhalte. Die Inhalte des Vorkurses
WS 15/16 1/16 Selbsteinschätzungstest zum Vorkurs rganische hemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NIT die späteren Studieninhalte. Die Inhalte des Vorkurses
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
Die Übungsfragen sind online Besprechung: Mittwoch, 28. September 2016
 Die Übungsfragen sind online http://www.cup.lmu.de/oc/linser/oc-for-biologists/ esprechung: Mittwoch, 28. eptember 2016 Link zur Klausuranmeldung: http://www.cup.lmu.de/anmeld/ocbioklausur/ Wiederholungsklausur:
Die Übungsfragen sind online http://www.cup.lmu.de/oc/linser/oc-for-biologists/ esprechung: Mittwoch, 28. eptember 2016 Link zur Klausuranmeldung: http://www.cup.lmu.de/anmeld/ocbioklausur/ Wiederholungsklausur:
Lösungen zu Übungsaufgaben Mechanismen 1 LK 12/1 Chemie
 1. Die radikalische Substitution 2-Methylbutan soll mit Brom im Sinne einer radikalischen Substitution reagieren. Betrachtet sei zunächst nur die Monobromierung. a) Formulieren Sie die Summengleichung
1. Die radikalische Substitution 2-Methylbutan soll mit Brom im Sinne einer radikalischen Substitution reagieren. Betrachtet sei zunächst nur die Monobromierung. a) Formulieren Sie die Summengleichung
7 Reaktionen von Carbonylverbindungen
 Übung zur Vorlesung rganische Chemie II eaktivität (Dr. St. Kirsch, Dr. A. Bauer) 7 eaktionen von Carbonylverbindungen 7.1 Ketone/Aldehyde und eteroatomnucleophile 7.1-70 Vervollständigen Sie die folgenden
Übung zur Vorlesung rganische Chemie II eaktivität (Dr. St. Kirsch, Dr. A. Bauer) 7 eaktionen von Carbonylverbindungen 7.1 Ketone/Aldehyde und eteroatomnucleophile 7.1-70 Vervollständigen Sie die folgenden
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester am
 Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
NMR-Methoden zur chiralen Erkennung
 Spektroskopie in der rganischen hemie NMR-Methoden zur chiralen Erkennung Mit Ausnahme der D-Spektroskopie (D = irculardichroismus) sind alle spektroskopischen Methoden auch die NMR achiral, d.h. sie können
Spektroskopie in der rganischen hemie NMR-Methoden zur chiralen Erkennung Mit Ausnahme der D-Spektroskopie (D = irculardichroismus) sind alle spektroskopischen Methoden auch die NMR achiral, d.h. sie können
weiteres Beispiel für Stereoisomere: Enantiomere Spiegelebene
 Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
kj/mol kj/mol 500 I Halogenmethan
 250 200 150 100 50 0 Vorlesung 11. alogenalkane CalogenBindungsstärke nimmt mit zunehmender Größe des alogens ab CalogenBindungslänge nimmt in derselben Richtung zu (Vollhardt,. Aufl., S. 206, Tab. 61,
250 200 150 100 50 0 Vorlesung 11. alogenalkane CalogenBindungsstärke nimmt mit zunehmender Größe des alogens ab CalogenBindungslänge nimmt in derselben Richtung zu (Vollhardt,. Aufl., S. 206, Tab. 61,
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
9. Alkohole, Ether und Phenole
 Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 9. Alkohole, Ether und Phenole Bis jetzt haben wir fast bei jedem Kapitel eine neue funktionelle Gruppe und auch eine wichtige neue
Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 9. Alkohole, Ether und Phenole Bis jetzt haben wir fast bei jedem Kapitel eine neue funktionelle Gruppe und auch eine wichtige neue
Aromatische Diazoniumionen
 Aromatische Diazoniumionen Wichtige Reaktive Zwischenstufe Aromatische Diazoniumionen Aromatische Diazoniumionen Azofarbstoffe Organische Chemie für MST 7 Lienkamp/ Prucker/ Rühe 7 Inhalt Amine Nomenklatur,
Aromatische Diazoniumionen Wichtige Reaktive Zwischenstufe Aromatische Diazoniumionen Aromatische Diazoniumionen Azofarbstoffe Organische Chemie für MST 7 Lienkamp/ Prucker/ Rühe 7 Inhalt Amine Nomenklatur,
M U S T E R L Ö S U N G
 Universität Regensburg Institut für rganische Chemie Prof. r.. Reiser. Klausur zum rganisch-chemischen Praktikum I für Studierende der Chemie und der iochemie im SS 999 am Mittwoch, dem. Juni 999 M U S
Universität Regensburg Institut für rganische Chemie Prof. r.. Reiser. Klausur zum rganisch-chemischen Praktikum I für Studierende der Chemie und der iochemie im SS 999 am Mittwoch, dem. Juni 999 M U S
FARBREAKTIONEN. 1. Farbgebende Strukturen 2. Gruppenreaktionen 3. Weitere Nachweisreaktionen
 FABEAKTIE 1. Farbgebende trukturen 2. Gruppenreaktionen 3. Weitere achweisreaktionen 1 1. Farbgebende trukturen adikale achweis f. Phenothiazine (Licht, 2 ) ' ' e e. ' tiefrot '. '. Disproportionierung
FABEAKTIE 1. Farbgebende trukturen 2. Gruppenreaktionen 3. Weitere achweisreaktionen 1 1. Farbgebende trukturen adikale achweis f. Phenothiazine (Licht, 2 ) ' ' e e. ' tiefrot '. '. Disproportionierung
Nucleophile Substitution am gesättigten C-Atom S N -Mechanismus
 ucleophile ubstitution am gesättigten Atom chanismus Prinzip der nucleophilen ubstitution am sp 3 hybridisierten Atom: u : u : ucleophil Elektrophil Abgangsgruppe Dabei treffen wir noch keine Aussage über
ucleophile ubstitution am gesättigten Atom chanismus Prinzip der nucleophilen ubstitution am sp 3 hybridisierten Atom: u : u : ucleophil Elektrophil Abgangsgruppe Dabei treffen wir noch keine Aussage über
CHE 172.1: Organische Chemie für die Life Sciences
 1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
Butan, Hexan, 3-Methyl-Pentan,...,Di-Chlor Ethan, 1,2-Di-Chlorethen, 1-Chlor-Butan, 2- Chlor Butan,...
 Butan, exan, 3-Methyl-Pentan,...,Di-Chlor Ethan, 1,2-Di-Chlorethen, 1-Chlor-Butan, 2- Chlor Butan,... Diese Oxidationsreaktion ist eine Radikalische ( bezogen auf auf das AGENS!) Substitution ( bezogen
Butan, exan, 3-Methyl-Pentan,...,Di-Chlor Ethan, 1,2-Di-Chlorethen, 1-Chlor-Butan, 2- Chlor Butan,... Diese Oxidationsreaktion ist eine Radikalische ( bezogen auf auf das AGENS!) Substitution ( bezogen
Organisch-Chemisches Institut Fakultät für Chemie und Geowissenschaften Universität Heidelberg 4. September 2015
 Organisch-Chemisches Institut Fakultät für Chemie und Geowissenschaften Universität Heidelberg 4. September 2015 Musterlösung Zwischennachklausur II zur Experimentalvorlesung Organische Chemie von Prof.
Organisch-Chemisches Institut Fakultät für Chemie und Geowissenschaften Universität Heidelberg 4. September 2015 Musterlösung Zwischennachklausur II zur Experimentalvorlesung Organische Chemie von Prof.
1.) Organometallverbindungen sind wichtige Reagenzien für C C-Bindungsbildungen. Der am Metall gebundene Kohlenstoff ist nukleophil (10 Punkte).
 Lösung zur Übung 7 1.) rganometallverbindungen sind wichtige Reagenzien für C C-Bindungsbildungen. Der am Metall gebundene Kohlenstoff ist nukleophil (10 Punkte). a) para-bromtoluol A wird mit n-butyllithium
Lösung zur Übung 7 1.) rganometallverbindungen sind wichtige Reagenzien für C C-Bindungsbildungen. Der am Metall gebundene Kohlenstoff ist nukleophil (10 Punkte). a) para-bromtoluol A wird mit n-butyllithium
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
Eliminierungsreaktionen: E1- und E2- Mechanismen; Olefine
 Eliminierungsreaktionen: E1 und E2 chanismen; lefine Allgemeine Gleichung der Eliminierung: Base X X Die Bindung wird am Atom gebrochen. Für die Qualität der Abgangsgruppe X gelten die selben egeln wie
Eliminierungsreaktionen: E1 und E2 chanismen; lefine Allgemeine Gleichung der Eliminierung: Base X X Die Bindung wird am Atom gebrochen. Für die Qualität der Abgangsgruppe X gelten die selben egeln wie
Hydroxylderivate. Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit. Bruch der C-H- und der C-OBindungen. Prof. Dr. Ivo C.
 Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
Hydroxylderivate Alkohole und Phenole. Säure-BaseEigenschaften. Reaktionen mit Bruch der C-H- und der C-OBindungen. 1 Alkohole: Grundlagen, Nomenklatur Alkohole: R-OH; funktionelle Gruppe: Hydroxy-Gruppe
Vorlesung 47. Aminosäuren, Peptide und Proteine
 Vorlesung 47. Aminosäuren, Peptide und Proteine Bedeutung der Proteine in der atur: Vollhardt, 3. Aufl., S. 1285/1286, 4. Aufl., S. 1371; art S. 608-609; Buddrus, S. 753. Etwa 18% des menschlichen Körpers
Vorlesung 47. Aminosäuren, Peptide und Proteine Bedeutung der Proteine in der atur: Vollhardt, 3. Aufl., S. 1285/1286, 4. Aufl., S. 1371; art S. 608-609; Buddrus, S. 753. Etwa 18% des menschlichen Körpers
Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether)
 Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Übung zur Vorlesung Organische Chemie II Reaktivität (Dr. St. Kirsch, Dr. A. Bauer) Wintersemester 2008/09 O 2 N
 Übung zur Vorlesung rganische Chemie II eaktivität (Dr. St. Kirsch, Dr. A. Bauer) zu 7.1-70: C [pts] (PhMe) 110 C Entfernung mit ilfe eines Wasserabscheiders Zusatzfrage: i) Was bedeutet die Abkürzung
Übung zur Vorlesung rganische Chemie II eaktivität (Dr. St. Kirsch, Dr. A. Bauer) zu 7.1-70: C [pts] (PhMe) 110 C Entfernung mit ilfe eines Wasserabscheiders Zusatzfrage: i) Was bedeutet die Abkürzung
Organische Chemie I/II. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Klausur - Lösungsbogen
 Prof. Dr. J. Daub Februar 2005 Klausur - Lösungsbogen zur Vorlesung "rganische Chemie II (Reaktionen, Reaktionsmechanismen) für Studierende der Chemie und der Biochemie 3. Semester" WS 2004/2005 14. Februar
Prof. Dr. J. Daub Februar 2005 Klausur - Lösungsbogen zur Vorlesung "rganische Chemie II (Reaktionen, Reaktionsmechanismen) für Studierende der Chemie und der Biochemie 3. Semester" WS 2004/2005 14. Februar
Inhaltsverzeichnis. 3 Gesättigte Kohlenwasserstoffe (Alkane) 3.1 Offenkettige Alkane 3.2 Cyclische Alkane
 Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
1. Übungsblatt Radikale
 Prof. Dr. liver Reiser Institut für rganische Chemie Universität Regensburg 1. Übungsblatt Radikale Aufgabe 1: Mittels radikalischer Chlorierung oder omierung können Alkylhalogenie aus Alkanen effektiv
Prof. Dr. liver Reiser Institut für rganische Chemie Universität Regensburg 1. Übungsblatt Radikale Aufgabe 1: Mittels radikalischer Chlorierung oder omierung können Alkylhalogenie aus Alkanen effektiv
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
Vorlesung 41. Mechanismus der Säure-katalysierten Veresterung Schritt 1: Protonierung der Carboxylgruppe. Schritt 2: H + Schritt 3: O R'
 Vorlesung 41 arbonsäureester Die Entstehung von arbonsäureestern bei der Umsetzung von arbonsäurechloriden oder anhydriden mit Alkoholen wurde bereits besprochen. arbonsäureester lassen sich auch direkt
Vorlesung 41 arbonsäureester Die Entstehung von arbonsäureestern bei der Umsetzung von arbonsäurechloriden oder anhydriden mit Alkoholen wurde bereits besprochen. arbonsäureester lassen sich auch direkt
Stickstoffhaltige Verbindungen
 Stickstoffhaltige Verbindungen Nitroderivate, Amine, Diazound Azoverbindungen. Prof. Ivo C. Ivanov 1 Nitroderivate der KW CH-Acidität von Nitroverbindungen: Nitro-aci-Nitro- Tautomerie: oder: aci-form
Stickstoffhaltige Verbindungen Nitroderivate, Amine, Diazound Azoverbindungen. Prof. Ivo C. Ivanov 1 Nitroderivate der KW CH-Acidität von Nitroverbindungen: Nitro-aci-Nitro- Tautomerie: oder: aci-form
Stoffklasse Alkane Alkene/Alkine Aromaten
 Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
1. Gruppe: Nucleophile Substitution
 1. Gruppe: ucleophile ubstitution 1 1. ubstitutionstypen: C Y C Y Klassifizierung der ubstitution je nach atur von Y: - Y kann ein ukleophil sein: (ersetzt das ukleophil => Lewis - Base): δ δ a, 3, BuMg
1. Gruppe: ucleophile ubstitution 1 1. ubstitutionstypen: C Y C Y Klassifizierung der ubstitution je nach atur von Y: - Y kann ein ukleophil sein: (ersetzt das ukleophil => Lewis - Base): δ δ a, 3, BuMg
Std. Stoffklassen Konzepte & Methoden Reaktionen 2 Struktur und Bindung 2 Alkane Radikale Radikal-Reaktionen 2 Cycloalkane Konfiguration &
 Materialien (Version: 26.06.2001) Diese Materialien dienen zur Überprüfung des Wissens und sind keine detailierten Lernunterlagen. Vorschlag: fragen Sie sich gegenseitig entsprechend dieser Listen ab.
Materialien (Version: 26.06.2001) Diese Materialien dienen zur Überprüfung des Wissens und sind keine detailierten Lernunterlagen. Vorschlag: fragen Sie sich gegenseitig entsprechend dieser Listen ab.
9. Alkohole, Ether und Phenole
 Inhalt Index 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und Darstellung und 2) Alkohole und Phenole als Säuren und Basen.
Inhalt Index 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und Darstellung und 2) Alkohole und Phenole als Säuren und Basen.
8. Halogenalkane : Nucleophile Substitutions- und Eliminerungsreaktionen
 Inhalt Index 8. Halogenalkane : Nucleophile Substitutions- und Eliminerungsreaktionen Halogenalkane sind in der organischen Synthese sehr wichtig, und werden auch in der Industrie als Lösungsmittel, im
Inhalt Index 8. Halogenalkane : Nucleophile Substitutions- und Eliminerungsreaktionen Halogenalkane sind in der organischen Synthese sehr wichtig, und werden auch in der Industrie als Lösungsmittel, im
Vergleichende Reaktionsmechanismen
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Vergleichende Reaktionsmechanismen 1. rdnen Sie die angegebenen Reaktionen einem Reaktionstyp zu und formulieren Sie den Reaktionsmechanismus. Radikalische
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Vergleichende Reaktionsmechanismen 1. rdnen Sie die angegebenen Reaktionen einem Reaktionstyp zu und formulieren Sie den Reaktionsmechanismus. Radikalische
Alkene / Additions-, Eliminierungsreaktionen
 2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
Klausur zur Vorlesung OCII Reaktionsmechanismen WS 2008/2009
 liver Reiser, Institut für rganische Chemie der Universität Regensburg Klausur zur Vorlesung CII Reaktionsmechanismen WS 008/009 ame Matr.r. 3 4 5 6 a+b 6c 6d 7 8 Σ ote xxoooxxx 0 0 0 0 0 + 3 5 0 0 00+
liver Reiser, Institut für rganische Chemie der Universität Regensburg Klausur zur Vorlesung CII Reaktionsmechanismen WS 008/009 ame Matr.r. 3 4 5 6 a+b 6c 6d 7 8 Σ ote xxoooxxx 0 0 0 0 0 + 3 5 0 0 00+
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren Brombutanen
 1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen
 KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Kapitel 5. Aromatische Substitutionsreaktionen. 5.1 Elektrophile Substitutionen
 Kapitel 5 Aromatische Substitutionsreaktionen In der organischen Chemie ist der Reaktionstyp der Substitutionsreaktionen sehr zahlreich und weitverbreitet. Dabei ist bekannt, daß die Wahl des Lösungsmittels
Kapitel 5 Aromatische Substitutionsreaktionen In der organischen Chemie ist der Reaktionstyp der Substitutionsreaktionen sehr zahlreich und weitverbreitet. Dabei ist bekannt, daß die Wahl des Lösungsmittels
13.1. Struktur der Carbonyl-Gruppe, Prinzipielle Reaktivität
 13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
VO-5. Organische Chemie 2. Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria.
 VO-5 Organische Chemie 2 Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria. wolfgang.schoefberger@jku.at 89 Mesomerer Effekt verringert die
VO-5 Organische Chemie 2 Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria. wolfgang.schoefberger@jku.at 89 Mesomerer Effekt verringert die
Suzuki-Reaktion. - Kupplung einer Aryl- oder Vinylboronsäure mit einem Aryloder Vinylhalogenid - verläuft Palladiumkatalysiert
 Suzuki-Reaktion - Kupplung einer Aryl- oder Vinylboronsäure mit einem Aryloder Vinylhalogenid - verläuft Palladiumkatalysiert Allgemein: R-X + R -B-R R-R + X-B-R R-X + R -B-() 2 R-R + X-B-() 2 R, R = Aryl-
Suzuki-Reaktion - Kupplung einer Aryl- oder Vinylboronsäure mit einem Aryloder Vinylhalogenid - verläuft Palladiumkatalysiert Allgemein: R-X + R -B-R R-R + X-B-R R-X + R -B-() 2 R-R + X-B-() 2 R, R = Aryl-
Klausur zum OC-Praktikum für Studierende der Lehrämter gleichzeitig Wiederholungsklausuren für Biologen 3. Sem., im WS 2002/03 M U S T E R L Ö S U N G
 Klausur zum -Praktikum für Studierende der Lehrämter gleichzeitig Wiederholungsklausuren für Biologen 3. Sem., im WS 2002/03 am Samstag, den 8. Februar 2003, 9 13 Uhr in den örsä1en 43/44 M U S T E R L
Klausur zum -Praktikum für Studierende der Lehrämter gleichzeitig Wiederholungsklausuren für Biologen 3. Sem., im WS 2002/03 am Samstag, den 8. Februar 2003, 9 13 Uhr in den örsä1en 43/44 M U S T E R L
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2016
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Nachtrag Aromatische Substitution Sicherheitsbelehrung: Regeln für das Arbeiten im Labor Prof. r. Rasmus Linser September 2016
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Nachtrag Aromatische Substitution Sicherheitsbelehrung: Regeln für das Arbeiten im Labor Prof. r. Rasmus Linser September 2016
