3. Material und Methoden
|
|
|
- Kora Krüger
- vor 6 Jahren
- Abrufe
Transkript
1 36 3. Material und Methoden 3.1 Probanden und Materialien Probanden Das Vorhaben zur Generierung und Charakterisierung von CMV-spezifischen T-Zellen wurde durch die Ethikkommission der Charité Universitätsmedizin Berlin genehmigt. In der Studie wurden 5 gesunde und 10 nierentransplantierte Spender untersucht, die schriftlich informiert wurden und sich freiwillig für die Teilnahme bereit erklärten. Es wurden nur Spender für die Studie zugelassen, die zu Beginn eine positive CMV-Serologie aufwiesen. Tabelle 3: Probanden Spender Geschlecht Alter Art der Immunsuppression Monate nach Transplantation H-1 f 56 keine --- H-2 m 27 keine --- H-3 m 36 keine --- H-4 f 48 keine --- H-5 m 37 keine --- Mittelwert TX-1 m 56 Dreifachtherapie #, Rappamycin TX-2 m 24 Dreifachtherapie # 24 TX-3 f 62 Dreifachtherapie # 35 TX-4 f 60 Dreifachtherapie # 41 TX-5 m 46 Steroide, CNI 7 TX-6 m 23 Dreifachtherapie # 12 TX-7 m 39 Dreifachtherapie # 16 TX-8 m 64 Dreifachtherapie # 85 TX-9 f 69 Steroide, CNI 35 TX-10 f 60 Dreifachtherapie # 79 Mittelwert CNI, Calcineurininhibitor; MMF, Mycophenolatmofetil; m, männlich; f, weiblich # Die Dreifachtherapie besteht aus Steroiden, MMF und CNI 11
2 37 Tabelle 4: Geräte Art des Gerätes Zentrifuge Sterilbank Inkubator Mikroskop Autoklav Kühlschrank Wasserbad Stickstofftank -80 C Gefriertruhe Feinwaage ph-meter Gamma-Cell 40 (Bestrahlung) Pipetten 1ml/ 200µl/ 10µl Pipetierhilfe ELISA/ Fluoreszenzmessgerät CliniMACS Plus MiniMACS Separator Rotationseinrichtung Steril Tube Fuser Heizblock Thermocycler Cycler Gene Amp 9700 Durchflusszytometer Calibur Neubauer Zählkammer Einfrierbox Glaswaren Hersteller Heraeus Heraeus Heraeus Leica Gössner Liebherr GFL Taylor-Wharton Heraeus Satorius Wiss.-techn. Werkstätte Atomic Energy Greiner Matrix Technologies Tecan Miltenyi Biotech Miltenyi Biotech Miltenyi Biotech Applied Critical Fluids Kleinfeld Labortechnik Perkin Elmer Applied Biosystems Becton& Dickinson Fein-Optik Nalgene Schott
3 38 Tabelle 5: Einwegartikel Artikel Hersteller Anwendung Pipettenspitzen 1ml/ 200µl/ 10µl Eppendorf allgemein Transferpipetten 1,2,5,10,25 ml Becton& Dickinson allgemein Eppendorftubes 0,5, 1,5 ml Eppendorf allgemein Falcon-Röhrchen 15, 50ml Becton& Dickinson allgemein Pasteurpipetten Sarstedt Zellkultur 96-Lochplatten Rundboden Corning Zellkultur 24, 96-Lochplatten Flachboden Corning Zellkultur Zellkulturflaschen 25, 75 cm 2 Corning Zellkultur Zellsieb 40µm Greiner Zellkultur Sterilfilter 0,2µm Fisher Scientific Zellkultur Einwegspritzen 2, 5, 10, ml Braun allgemein 14ml-Röhrchen Greiner Ficollgradient Zitrat-/ Heparinröhrchen Sarstedt Blutentnahme MiniMACS-Säule Miltenyi Biotech T-Zell Isolierung Transferbeutel 600ml Miltenyi Biotech GMP T-Zell Isolierung CliniMACS-Schlauch Set Miltenyi Biotech GMP T-Zell Isolierung PreSystem Filter Miltenyi Biotech GMP T-Zell Isolierung Luer/Spike Interconnector Miltenyi Biotech GMP T-Zell Isolierung 96-Lochplatten unbeschichtet Nunc ELISA Kryoröhrchen 1,8, 5 ml Nunc Zelleinfrierung Micronicröhrchen 0,5, 5 ml Becton&Dickinson Durchflusszytometrie Tabelle 6: Reagenzien Reagenz Hersteller Anwendung PBS Biochrom allgemein RPMI-Medium Biochrom Zellkultur Fötales Kälberserum Biochrom Zellkultur Penizillin/ Streptomyzin Biochrom Zellkultur Proleukin 2 (IL-2) Chiron T-Zellkultur Aciclovir Ratiopharm LCL-Zellkultur Cyclosporin A Novatis LCL-Zellkultur B 95-8 Viruslysat Quelle Rooney LCL-Zellkultur Ficoll Plaque Amersham PBMC-Isolierung Tryphanblau Sigma Zellzählung Dimethylsulfoxid Sigma Kryokonservierung
4 39 pp65-peptidpool JPT Peptide Technologies T-Zellstimulation IE-1-Peptidpool JPT Peptide Technologies T-Zellstimulation IFN-γ-Secretion Assay Miltenyi Biotech T-Zellisolierung EDTA Sigma MACS-Puffer CliniMACS Cytokine Capture System Miltenyi Biotech T-Zellisolierung GMP Humanes AB Serum Sigma T-Zellkultur GMP Calcein AM Mobitech Zytotoxizitätstest Triton X 100 Sigma Zytotoxizitätstest Human IFN-γ-ELISA Set Becton& Dickinson ELISA ELISA Substrat Becton& Dickinson ELISA Tween 20 Sigma ELISA Natriumhydrogencarbonat Sigma ELISA Dinatriumcarbonat Sigma ELISA Schwefelsäure Sigma ELISA Natriumazid Sigma für FACS-Puffer Paraformaldehyd Sigma Zellfixierung Brefeldin A Becton& Dickinson Durchflusszytometrie Perm 2 Lösung Becton& Dickinson Durchflusszytometrie Anti-CD3-FITC/ PE/ PerCp/ APC Becton& Dickinson Durchflusszytometrie Anti-CD8-FITC/ PE/ PerCp/ APC Becton& Dickinson Durchflusszytometrie Anti-CD4-FITC/ PE/ PerCp/ APC Becton& Dickinson Durchflusszytometrie Anti-CD16-FITC/ PE Becton& Dickinson Durchflusszytometrie Anti-CD19-PE Becton& Dickinson Durchflusszytometrie Anti-IFN-γ-FITC Becton& Dickinson Durchflusszytometrie Anti-CD27-PE Becton& Dickinson Durchflusszytometrie Anti-CD28-FITC Becton& Dickinson Durchflusszytometrie Anti-CD62L-PerCp Becton& Dickinson Durchflusszytometrie Anti-CCR7-FITC Becton& Dickinson Durchflusszytometrie β-mercaptoethanol Sigma Für Lysispuffer RNeasy Mini Kit Qiagen RNA Isolierung First Strand Buffer Gibco cdns-synthese Dithiothreitol Gibco cdns Synthese Reverse Transkriptase Gibco cdns Synthese RNAse Inhibitor Promega cdns Synthese Oligo dt Primer Pharmacia cdns Synthese Desoxynukleosidtriphsphate Pharmacia cdns Synthese DNAse Ambion cdns Synthese TaqMan Universal Master Mix Applied Biosystems TRBV-Analyse TRBV Primer und Sonden Institut für Kardiologie TRBV-Analyse Mycoplasma Detection Kit Roche Reinheitsprüfung GMP
5 40 Medien und Puffer Zellkulturmedium: 500ml RPMI-Medium 2mM L-Glutamin 50 ml fötales Kälberserum 5 ml Penizillin/ Streptomyzin T- Zellkulturmedium: 500ml RPMI-Medium 2mM L-Glutamin 50 ml fötales Kälberserum 5 ml Penizillin/ Streptomycin U IL-2 (100 U/ml) GMP-Zellkulturmedium 500ml RPMI-Medium 2mM L-Glutamin 50 ml humanes AB Serum FACS-Puffer 500 ml PBS 5ml fötales Kälberserum 0,01% Natriumazid Fixierungslösung 100 ml PBS 2g Paraformaldehyd ELISA-Coatingpuffer 500 ml destilliertes H 2 O 1,78g Dinatriumcarbonat 4,2g Natriumhydrogencarbonat EILSA-Waschpuffer 500 ml PBS 250 µl Tween 20 Einfriermedium 45ml fötales Kälberserum 5ml Dimethylsulfoxid
6 41 MACS-Puffer 500 ml PBS 25ml fötales Kälberserum 2mM EDTA 3.2 Methoden PBMC-Isolierung PBMCs wurden mit Hilfe eines Dichtegradienten aus peripherem Blut der Probanden isoliert. Dazu wurde das Blut 1:1 mit PBS verdünnt. 14 ml Röhrchen wurden mit jeweils 3ml Ficoll Plaque bestückt und vorsichtig mit 7 ml Blut überschichtet. Die Röhrchen wurden bei Raumtemperatur (RT) für 40 Minuten bei 400xg mit ausgeschalteter Bremse zentrifugiert. Anschließend wurde die Interphase, welche die PBMCs enthält, mit einer Pasteurpipette vorsichtig abgezogen. Die Zellen wurden in 50 ml PBS überführt und 2-mal gewaschen Zellzählung und Vitalitätsbestimmung Zellsuspensionen wurden mit Tryphanblau im Verhältnis 1:1 gemischt und auf eine Neubauer-Zählkammer aufgebracht. Es wurden die lebenden ungefärbten Zellen in allen 4 Quadraten ausgezählt und der Mittelwert pro Quadrat errechnet. Dieser wurde mit 2 multipliziert um die Verdünnung zu berücksichtigen. Der entstehende Wert ergab die Zellkonzentration x10 4 pro ml Zellsuspension Einfrieren und Auftauen von Zellen PBMCs, LCLs, oder T-Zelllinien wurden eingefroren, soweit sie für eine spätere Verwendung vorgesehen waren. Dazu wurden die Zellen gezählt und 2-mal in Zellkulturmedium bei 4 C gewaschen. Das Pellet wurde gebrochen und 20 min auf Eis gekühlt. Danach wurden die Zellen in 4 C kaltem Einfriermedium in einer Konzentration von 5 bis 10x10 6 /ml resuspendiert und zügig in beschriftete Kryoröhrchen überführt. Die Kryoröhrchen wurden mit Hilfe einer Einfrierbox auf -70 C abgekühlt und anschließend in flüssigen Stickstoff gelagert.
7 42 Zum Auftauen wurden die Kryoröhrchen in einem 37 C warmen Wasserbad bis knapp über den Schmelzpunkt erwärmt. Die Suspension wurde anschließend zügig in 50 ml eiskaltes Zellkulturmedium überführt und 2-mal gewaschen LCL-Generierung und -Kultivierung 5 x 10 6 PBMCs wurden in 200 μl B95-8 Viruslysat resuspendiert und anschließend mit 1,8 ml Zellkulturmedium aufgefüllt, dem 1µg/ml Cyclosporin A zur Inhibition der T-Zellfunktion zugesetzt war. 1 ml dieser Suspension wurde in 5 Vertiefungen einer 96-Lochplatte mit Flachboden gleichmäßig verteilt. Die restliche Suspension wurde im Verhältnis 1:1 mit Zellkulturmedium und Cyclosporin A verdünnt und in weitere 10 Vertiefungen der 96- Lochplatte aufgebracht. Die Zellen wurden in einem Inkubator bei 37 C und 5% CO 2 kultiviert. 100 µl des Überstandes wurden jede Woche durch frisches Zellkulturmedium ersetzt. Nach 2-3 Wochen zeigten die LCLs starkes Wachstum und konnten Schrittweise in eine 24-Lochplatte, eine 25 cm 2 Kulturflasche und letztendlich in eine 75 cm 2 Kulturflasche expandiert werden. Ab diesem Zeitpunkt galt die LCL-Linie als etabliert, und dem Medium wurde ab diesem Zeitpunkt 25µg/ml Aciclovir zur Hemmung der EBV-Replikation zugesetzt. Bei etablierten LCL-Linien wurde 2-mal wöchentlich das Medium gewechselt, wobei die Hälfte der Suspension durch frisches Zellkulturmedium ersetzt wurde T-Zell-Generierung und -Kultivierung Die Generierung der T-Zelllinien fand durch spezifische Stimulation, Isolierung der IFN-γsezernierenden Zellen und deren Expansion statt. Zur Stimulation wurden die PBMCs der Spender in Zellkulturmedium mit einer Konzentration von 2x 10 7 /ml resuspendiert. Jeweils 0,5 ml der Zellsuspension wurde in eine Vertiefung einer 24-Lochplatte gegeben, mit 1µg/ml pp65- oder IE-1-Peptidpool versetzt und für 6h im Inkubator kultiviert. Für die Isolation mittels IFN-γ-Secretion Assay wurden die Zellen unter Zugabe von 2ml kaltem PBS mit einer Pasteurpipette in ein 50ml Falcon Tube überführt. Die Zellen wurden bei 4 C mit 400xg für 10 Minuten zentrifugiert und das Pellet gebrochen. Danach wurden 100µl kaltes Zellkulturmedium und 25µl Catch Antikörper pro 2x10 7 PBMCs hinzugefügt und für 10 Minuten auf Eis inkubiert. Die Zellen wurden mit kaltem Zellkulturmedium 2-mal gewaschen. Für die IFN-γ-Sezernierung wurden die Zellen
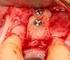
8 43 mit warmem Medium auf eine Konzentration von 1x10 6 /ml eingestellt und auf mehre Falcon Röhrchen verteilt, sodass maximal 25ml in jedem Röhrchen waren. Die Röhrchen wurden anschließend für 50 Minuten in einer Rotationseinrichtung bei 37 C und 5% CO 2 mit langsamer Rotation belassen. Der Stopp der IFN-γ-Sezernierung erfolgte durch die Zugabe von 25 ml kaltem Zellkulturmedium und der Inkubation für 10 Minuten auf Eis. Die Zellen wurden gewaschen und mit 100µl Medium und 25 µl Detection Antikörper pro 2x10 7 Zellen für 10 Minuten auf Eis fluorometrisch gefärbt. Nach einem Waschschritt konnten einige Zellen für die Bestimmung der spezifischen Vorfrequenz entnommen werden. Dazu wurde deren Oberfläche mit anti-cd3/ -CD4 und -CD8 Antikörpern gefärbt. Der Großteil der Zellen wurde mit Hilfe der anti-pe-microbeads magnetisch markiert. Dazu wurden Konzentrationen wie bei den anderen Markierungsschritten verwendet und die Zellen für 20 Minuten bei 4 C inkubiert. Nach dem Waschen wurden die IFN-γ-sezernierenden Zellen im MiniMACS- Separator unter Verwendung von 2 MiniMACS-Säulen isoliert. Die radioaktive Bestrahlung der Negativfraktion erfolgte mit 30 Gray (Gy). Diese wurde anschließend gewaschen und in 1ml T-Zellkulturmedium resuspendiert und in eine Vertiefung einer 24-Lochplatte aufgebracht. Die isolierten IFN-γ-sezernierenden Zellen wurden ebenfalls in 1 ml T- Zellkulturmedium resuspendiert und den Feederzellen zugesetzt. Die Platte wurde im Inkubator für Tage inkubiert, wobei bei Farbumschlag des Indikators die Hälfte des Mediums durch frisches ersetzt wurde. Zusätzlich wurde die Kultur täglich im Lichtmikroskop untersucht. Bei der Ausbildung einer konfluenten Zellschicht wurde der Inhalt jeder Vertiefung auf zwei neue Vertiefungen verteilt und mit T-Zellkulturmedium aufgefüllt T-Zell-Generierung und -Kultivierung unter GMP-Bedingungen Alle Arbeiten fanden in einem Labor mit A- und B-Reinraumklasse unter Verwendung zugelassener Schutzkleidung statt. Um mögliche Kontaminationen auszuschließen, wurden bis auf die Expansion der T-Zellen alle Arbeiten in geschlossenen Systemen durchgeführt. Dazu wurden Beutel- und Schlauchsysteme verwendet, die sich mit Hilfe eines Plastikschweißgerätes (steril tube fuser) beliebig miteinander verbinden oder trennen ließen. Die Isolierung der IFN-γ-sezernierenden Zellen wurde automatisch mit Hilfe eines CliniMACS Plus durchgeführt (Abbildung 5). 1x10 9 PBMCs des haemapoetischen Stammzellspenders wurden dazu in einen Transferbeutel unter Verwendung einer 50 ml Einwegspritze vorgelegt. Anschließend erfolgten zwei Waschschritte, bei denen jeweils
9 44 500ml kaltes GMP-Zellkulturmedium in den Beutel gefüllt und dieser für 10 Minuten bei 4 C und 400xg zentrifugiert wurde. Der Überstand wurde in einen weiteren Transferbeutel überführt, nachdem dieser mittels Tubing Heat Sealer an die Schläuche des ersten angeschweißt wurde. Nach den Waschschritten wurden die Zellen in 100ml GMP- Zellkulturmedium aufgenommen und durch Verwendung einer 2ml Einwegspritze mit 1µg/ml pp65- und IE-1-Peptidpool versetzt. Die Stimulation der Zellen erfolgte für 6h in einem Inkubator. Anschließend wurden die Zellen mittels CliniMACS-Cytokin-Capture-System markiert. Dazu wurden die Zellen 1-mal gewaschen und in 10ml kaltem GMP- Zellkulturmedium resuspendiert. Die Suspension wurde mit 7,5ml Catchmatrix Reagenz durch eine 10ml Einwegspritze versetzt und 5 Minuten auf Eis inkubiert. Nach Ablauf der Zeit wurde zu den Zellen 500ml warmes GMP-Zellkulturmedium gegeben. Der Inhalt wurde gleichmäßig auf 4 Beutel verteilt, und diese wurden bis zu einem Volumen von 250ml mit warmem GMP-Zellkulturmedium befüllt. Zur IFN-γ-Sezernierung wurden die 4 Beutel für 45 Minuten im Inkubator unter langsamer Rotation kultiviert. Die Unterbrechung der Sezernierung erfolgte durch Zugabe von 250 ml kaltem GMP-Zellkulturmedium. Nach einer Inkubation von 10 Minuten auf Eis wurden die Beutel zentrifugiert und der Überstand entfernt. Die Zellen wurden in einem Beutel vereinigt und in 10ml kaltem Medium aufgenommen. Anschließend wurden die Zellen mit 7,5ml IFN-γ-Enrichment Reagenz versetzt und für 15 Minuten auf Eis inkubiert. Die Zellen wurden 1-mal gewaschen und in 100 ml resuspendiert. Der Transferbeutel wurde mit Hilfe des Luer/Spike Interconnectors mit den CliniMACS-Schlauchsystem und dem PreSystem Filter verbunden. Das System wurde in den CliniMACS Plus eingespannt (Abbildung 5). Dieser wurde mit dem Programm ENRICHMENT 3.1 gestartet und führte automatisch die Selektion der magnetisch markierten IFN- γ-sezernierenden Zellen durch.
10 45 Abb. 5. Aufbau eines CliniMACS Plus Die Abbildung stellt einen CliniMACS Plus mit eingespanntem Beutel-/ Schlauchsystem zur magnetischen Isolierung von Zellen dar. Die einzelnen Elemente sind durch Pfeile gekennzeichnet. Die Abbildung ist einem technischen Datenblatt der Firma Miltenyi Biotech GmbH entnommen. Die Zellzahl der selektionierten Positivfraktion wurde mit einer Neubauer Zählkammer bestimmt und 5x10 5 der Zellen wurden pro Vertiefung in einer 24-Lochplatte ausgesät. Jeder Vertiefung wurden 2x10 7 mit 30 Gy bestrahlte Zellen der Negativfraktion als Feeder zugesetzt. Jede Vertiefung enthielt 2ml GMP-Zellkulturmedium, das anstelle von humanem AB-Serum autologes Serum des Stammzellspenders enthielt und mit 100 U/ml IL-2 versetzt war. Die Zellen wurden für 14 Tage kultiviert, wobei das Wachstum der Zellen jeden Tag unter dem Lichtmikroskop kontrolliert wurde. Beim Umschlag des Farbindikators wurde 1ml des Mediums durch frisches ersetzt. Beim Erreichen einer konfluenten Zellschicht wurde der Inhalt jeder Vertiefung auf zwei neue verteilt und mit GMP-Zellkulturmedium, dem 100 U/ml IL-2 zugesetzt war, aufgefüllt Durchflusszytometrie Oberflächenfärbung 5x10 5-1x10 6 Zellen wurden in 0,5 ml Micronic Röhrchen überführt, mit FACS-Puffer aufgefüllt und 10 Minuten bei RT mit 400xg zentrifugiert. Der Überstand wurde abgesaugt,
11 46 das Pellet gebrochen und der Waschschritt wiederholt. Anschließend wurden die Zellen in 50µl FACS-Puffer resuspendiert und mit den vom Hersteller empfohlenen Konzentrationen der Antikörper für 10 min bei 4 C gefärbt. Nach dem Färben wurden die Zellen 2-mal gewaschen und für die Analyse in 100 µl FACS-Puffer aufgenommen. Intrazellulärfärbung 1x10 6 Zellen wurden in 0,5 ml Micronic Röhrchen überführt und 2-mal gewaschen. Das Pellet wurde in 100µl Fixierlösung aufgenommen und für 20 Minuten bei 4 C inkubiert. Die Zellen wurden 2-mal gewaschen und anschließend permeabilisiert. Dazu wurde Perm2- Lösung 1:10 mit destilliertem Wasser verdünnt und auf 4 C gekühlt. Anschließend wurden 100 µl dieser Verdünnung auf die pelletierten Zellen gegeben. Diese wurden 20 Minuten bei 4 C inkubiert und anschließend 2-mal gewaschen. Die Zellen wurden in 50µl FACS-Puffer aufgenommen und nach Herstellerangaben mit den jeweiligen Antikörpern für 30 Minuten bei 4 C gefärbt. Nach 2-maligen Waschen wurde das Pellet für die Analyse in 100µl FACS- Puffer aufgenommen. Analyse und Auswertung Die gefärbten Zellen wurden mit einem Durchflusszytometer der Marke Calibur mittels CellQuest-Software gemessen und anschließend unter Verwendung der Cytomation Summit Software ausgewertet Zytotoxizitätstestung Zur Bestimmung des lytischen Potenzials wurde ein fluorometrischer Zytotoxizitätstest durchgeführt. Dazu wurden 1x10 6 Zielzellen mit 500µl einer 20mM Calceinlösung für 30 Minuten im Inkubator gefärbt. Die Färbung wurde anschließend durch die Zugabe von 10ml Zellkulturmedium abgestoppt. Die Zielzellen wurden 2-mal mit Zellkulturmedium gewaschen und bei einer Konzentration von 4x10 4 Zellen/ml resuspendiert. Es wurden jeweils 100µl dieser Suspension in 24 Vertiefungen einer 96-Lochplatte mit Flachboden pipettiert. Jeweils 4 dieser Vertiefungen sind anschließend mit 100µl Zellkulturmedium (Spontanlyse), einer 0,9% Triton-X100-Lösung (Maximallyse), 1,6x10 5 T-Zellen (40:1), 8x10 4 T-Zellen (20:1) 4x10 4 T- Zellen (10:1) und 2x10 4 T-Zellen (5:1) befüllt worden. Nach einer Inkubation von 4h bei
12 47 37 C und 5% CO 2 wurden 100 µl Überstand aus jeder Vertiefung in eine neue 96-Lochplatte überführt. Die Überstände wurden in einem Fluoreszenzmessgerät analysiert und die Menge des freigesetzten Calceins bestimmt. Für die Bestimmung der spezifischen Lyse wurden Mittelwerte aus den Vierfachwerten gebildet, wobei Ausreißer zuvor durch einen Test nach Nalimov identifiziert und ausgeschlossen wurden (139). Die spezifische Lyse wurde wie folgt berechnet: Lyse in %= (mittlere Fluoreszenz der Probe mittlere Spontanlyse) / (mittlere Maximallyse mittlere Spontanlyse) Die Ausreißer wurden nach Nalimov folgendermaßen identifiziert: mit r* = Sensitivität, x* = möglicher Ausreißer, x = Mittelwert, s = Standardabweichung, und n = Anzahl der Experimente Für die Sensitivität wurde der Wert 1,645 eingesetzt. Damit bestand bei einem Formelergebnis von >1,645 eine hohe Wahrscheinlichkeit (95%), dass x* ein Ausreißer ist Epitopmapping und IFN-γ-ELISA Zur Bestimmung der Epitopspezifitäten wurden die T-Zelllinien mit pp65- oder IE-1- Mappingpools stimuliert (Abbildung 13). Dazu wurden jeweils 1x10 6 autologe LCLs mit 1µg/ml eines Mappingpools für 2h im Inkubator beladen. Die Zellen wurden 2-mal mit Zellkulturmedium gewaschen und bei einer Konzentration von 5x10 5 Zellen/ml resuspendiert. 100µl dieser Suspension wurde in die Vertiefungen einer 96-Lochplatte mit Rundboden gegeben. Anschließend wurden 100µl T-Zellsuspension mit gleicher Konzentration dazugegeben. Die Platte wurde für 6h bei 37 C und 5% CO 2 inkubiert. 100µl Überstand wurde in eine neue Platte übertragen und bei -20 C eingefroren. Die Überstände wurden am nächsten Tag unter Verwendung des humanen IFN-γ-ELISA-Sets auf ihren Gehalt an IFN-γ untersucht. Die Vertiefungen einer unbeschichteten 96-Lochplatte mit Flachboden wurden über Nacht mit 50µl einer in Coating-Puffer 1:400 verdünnten Capture-Antikörperlösung bei 4 C beladen. Am nächsten Tag wurde jede Vertiefung durch wiederholtes Auffüllen und Entfernen mit 300µl ELISA Waschpuffer 3-mal gewaschen. Anschließend wurden freie Bindungsstellen mit 200µl FACS-Puffer für 1h bei RT beblockt. Nach 3-maligem Waschen wurde 50µl Probenüberstand in die Vertiefung aufgebracht und für
13 48 2h bei RT inkubiert. Die Vertiefungen wurden 5-mal gewaschen und 50µl einer 1:400 verdünnten Mischung aus Detektionsantikörper und Enzymreagenz wurden aufgebracht und 1h bei RT inkubiert. Anschließend wurde 7-mal gewaschen und jede Vertiefung wird mit 50µl Substratlösung für 5 Minuten behandelt. Die enzymatische Färbereaktion wurde durch das Hinzupipettieren von 50µl 1M Schwefelsäure gestoppt. Die Platte wurde anschließend in einem ELISA-Messgerät analysiert Analyse der T-Zellrezeptor Beta variablen Gene (TRBV) RNA Isolierung Die Isolierung der RNA aus den T-Zellen erfolgte mit Hilfe des RNeasy Mini Kit nach Herstellerangaben. Zuvor wurde das Zellpellet in einem RNAse inaktivierenden guanidiniumisothiocyanathaltigen Puffer lysiert und mit β-mercaptoethanol in einem Verhältnis 1:143 versetzt. Die Fällung wurde mit -20 C kaltem 70%igem Ethanol durchgeführt, das in einem Verhältnis 1:2 eingesetzt wurde. Die Bindung an die Silikamembran der Säule erfolgte, indem das Gemisch aufgetragen und für 15 Sekunden bei 1000xg zentrifugiert wurde. Der Durchlauf wurde verworfen und die Säule mit den zu dem Kit zugehörigen Puffern gewaschen. Vor der Elution wurde die Säule getrocknet. Zur vollständigen Elution der an der Silikamembran gebundenen Gesamt-RNA, wurden die Säulen zweimal für 5 Minuten bei 37 C mit jeweils 22 μl RNase freiem Wasser inkubiert und im Anschluss für 1 Minute bei 1000xg zentrifugiert. cdna-synthese Für das Umschreiben der RNA in cdna wurde die Moloney Murine Leukemia Virus Reverse Transkriptase, eine RNA-abhängige DNA-Polymerase, verwendet. Zur Synthese der cdna wurden Oligo-Desoxythymidin- (OdT-) Primer eingesetzt, die sich an den 3 -Poly A- Schwanz der mrna anlagern. Es wurden maximal 2 μg RNA in einem Volumen von 18 μl eingesetzt und mit 2 μl OdT-Primer (0,1 mg/ml) gemischt. Um die Ausbildung von Sekundärstrukturen zu vermeiden, wurden die Ansätze für 10 Minuten bei 75 C inkubiert und anschließend 2 Minuten auf Eis abgekühlt. Folgender Mix wurde je Reaktionsansatz zugegeben:
14 49 8µl First Strand Puffer 4 µl Dithiothreitol 4µl Desoxynukleosidtriphosphat 2µl DNAse 0,5µl RNAse-Inhibitor Durch die Zugabe der DNAse und die anschließende 30-minütige Inkubation bei 37 C wurden DNA-Restkontaminationen eliminiert. Die DNAse wurde bei 75 C inaktiviert. Nach dem Abkühlen auf Eis wurde 1 μl Reverse Transkriptase und 1 μl RNAse-Inhibitor hinzugegeben. Die cdna-synthese erfolgte für 60 Minuten bei 42 C mit einem abschließenden Enzyminaktivierungsschritt bei 95 C für 5 Minuten. Die synthetisierte cdna wurde bis zur Real Time PCR bei -20 C aufbewahrt. Real Time PCR Die Real Time PCR ist eine Methode zur Amplifikation von spezifischen DNA-Abschnitten, die auf dem Prinzip der herkömmlichen PCR beruht und darüber hinaus eine quantitative Bestimmung geringster DNA-Mengen ermöglicht. Die Quantifizierung wird mit Hilfe von Fluoreszenzfarbstoffen am Ende eines PCR-Zyklus durchgeführt, da bei dieser Methode die Fluoreszenz proportional mit der Menge der gebildeten DNA zunimmt. Für die Quantifizierung muss ein Schwellenwert (Cycle of Threshold; C t ) überschritten werden, sodass die Fluoreszenz vom Hintergrund klar zu unterscheiden ist. Die für die Taqman PCR verwendeten Primer und Fluoreszenzsonden wurden durch das Institut für Kardiologie and Pneumonologie der Charité Universitätsmedizin zur Verfügung gestellt. Alle Proben wurden in Doppelansätzen analysiert. Diese setzten sich wie folgt zusammen: 2µl cdna 6,25µl TaqMan Universal Master Mix 0,25µl Sonde 2,5 µl Primer 1,5µl H 2 O
15 50 Die Analyse erfolgte in einem Gene Amp 9700 Cycler. Das Standardprogramm für die Real Time PCR bestand aus vier Schritten. Zunächst wurden kontaminierende RNA-Fragmente bei 50 C für 2 Minuten zerkleinert. Anschließend erfolgte die Denaturierung der cdna durch einen Heißstart bei 95 C für 10 Minuten. Danach wurden 40 Zyklen mit jeweils einem Denaturierungsschritt bei 95 C für 15 Sekunden und einem Annealing- und Extensionsschritt bei 60 C für 60 Sekunden durchgeführt. Um die Reproduzierbarkeit der Methode zu gewährleisten, wurden alle Proben in einer Doppelbestimmung analysiert. Dabei wurde bei einer Abweichung des C t -Wertes von mehr als 0,5 die Messung der Probe wiederholt. Für die Auswertung wurden die Proben auf das Gen hypoxanthine phosphoribosyl-transferase (HPRT) normalisiert, welches in allen Zelltypen gleichmäßig exprimiert wird. Dies erfolgte nach der Formel: 2 -ΔCt mit ΔC t = C t (Zielgen) - C t (HPRT) Mykoplasmenantigennachweis Der Zellkulturüberstand der unter GMP-Bedingungen hergestellten T-Zelllinien wurde mit Hilfe des Mycoplasma Detection Kit auf Mykoplasmenantigene untersucht. Mit Hilfe dieses Kits lassen sich Antigene der verbreitetsten Mykoplasmenarten (M. arginini; M. hyorhinis; M. orale; A. laidlawii) durch ELISA nachweisen. Für jede Probe und jede Mykoplasmenart wurden 4-fach Bestimmungen genau nach Herstellerangaben und unter der exklusiven Verwendung der Kitmaterialien durchgeführt. Ein Positivstandard und eine Negativkontrolle wurden zusätzlich mitgeführt. Der Test wurde in einem ELISA-Messgerät ausgewertet. Der Test galt nur dann als aussagekräftig, wenn der Positivstandard ein eindeutiges Signal auslöste und keines bei der Negativkontrolle detektiert werden konnte Aerobe-/anaerobe Bakterienkultur und LPS-Testung Zellsuspensionen der unter GMP-Bedingungen hergestellten T-Zelllinien wurden mittels ELISA auf LPS und mittels Aufbringung auf wachstumsfördernde Nährböden auf aerobe und anaerobe Bakterien untersucht. Diese Untersuchungen wurden im Routinelabor des Institutes für Mikrobiologie der Charité Universitätsmedizin durchgeführt.
16 HLA-Typisierung Zur Bestimmung allogener Kreuzkontaminationen des unter GMP-Bedingungen hergestellten T-Zellproduktes wurde eine HLA-Typisierung durchgeführt. Dieser wurde hochauflösend auf genetischer Ebene im Institut für Rechtsmedizin der Charité Berlin durchgeführt CMV-PCR Zum Zeitpunkt der Generierung der pp65- und IE-1-spezifischen T-Zelllinien wurde die Menge an CMV-DNA im peripheren Blut der Spender mittels PCR bestimmt. Diese Untersuchung wurde im Routinelabor des Institutes für Medizinische Immunologie der Charité Universitätsmedizin durchgeführt Statistische Analysen Die statistischen Analysen wurden mittels SPSS-Software durchgeführt. Es wurden pp65- und IE-1-spezifische T-Zelllinien eines Spenders paarweise miteinander verglichen. Dazu wurde der nichtparametrische Wilcoxontest angewendet. Ein Ergebnis wurde als signifikant betrachtet, wenn ein p-wert kleiner 0,05 erreicht wurde.
Protokoll Praktikum für Humanbiologie Studenten
 Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
SCRIPTUM HIGH PRECISE
 Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
Plasmidpräparation aus Bakterien Inhalt
 Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Institute for Immunology and Thymus Research Laboratory for Autologous Adult Stem Cell Research and Therapy
 Institute for Immunology and Thymus Research Laboratory for Autologous Adult Stem Cell Research and Therapy Rudolf-Huch-Str. 14 D- 38667 Bad Harzburg Tel: +49 (0)5322 96 05 14 Fax: +49 (0)5322 96 05 16
Institute for Immunology and Thymus Research Laboratory for Autologous Adult Stem Cell Research and Therapy Rudolf-Huch-Str. 14 D- 38667 Bad Harzburg Tel: +49 (0)5322 96 05 14 Fax: +49 (0)5322 96 05 16
en zum sicheren Einfrieren und Auftauen von Zellkulturen in TPP-Kryoröhrchen
 Empfehlung mpfehlungen en zum sicheren Einfrieren und Auftauen von Zellkulturen in TPP-Kryoröhrchen Information der Biochrom AG vom 23. Mai 2011 Zellkulturen können durch Kryokonservierung nahezu unbegrenzt
Empfehlung mpfehlungen en zum sicheren Einfrieren und Auftauen von Zellkulturen in TPP-Kryoröhrchen Information der Biochrom AG vom 23. Mai 2011 Zellkulturen können durch Kryokonservierung nahezu unbegrenzt
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS
 Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Kapillarelektrophorese DNA-Sequenzierung
 Kapillarelektrophorese DNA-Sequenzierung DNA Kettenanalyse oder DNA-Sequenzierung wird bei der Anordnung der Primärstruktur und Bestimmung der Nukleotid-Basensequenz verwendet. Die Analyse basiert auf
Kapillarelektrophorese DNA-Sequenzierung DNA Kettenanalyse oder DNA-Sequenzierung wird bei der Anordnung der Primärstruktur und Bestimmung der Nukleotid-Basensequenz verwendet. Die Analyse basiert auf
AdnaTest ColonCancerDetect
 AdnaTest ColonCancerDetect RT-PCR-Nachweis von Darmkrebs-assoziierter Genexpression in angereicherten Tumorzellen Zur In-vitro-Diagnostik Gebrauchsanweisung T-1-505 Inhaltsverzeichnis Bestellinformation...
AdnaTest ColonCancerDetect RT-PCR-Nachweis von Darmkrebs-assoziierter Genexpression in angereicherten Tumorzellen Zur In-vitro-Diagnostik Gebrauchsanweisung T-1-505 Inhaltsverzeichnis Bestellinformation...
AdnaTest ER/PR-Detect
 PCR-Expressionsanalyse der Östrogen- und Progesteron- Hormonrezeptoren in angereicherten Tumorzellen Zur In-vitro-Diagnostik Gebrauchsanweisung T-1-532 Inhaltsverzeichnis Bestellinformation... 3 Anwendungszweck...
PCR-Expressionsanalyse der Östrogen- und Progesteron- Hormonrezeptoren in angereicherten Tumorzellen Zur In-vitro-Diagnostik Gebrauchsanweisung T-1-532 Inhaltsverzeichnis Bestellinformation... 3 Anwendungszweck...
CryoPure Einfriersystem Beleben Sie Ihre Kryokonservierung. Effiziente und zuverlässige Kryokonservierung
 CryoPure Einfriersystem Beleben Sie Ihre Kryokonservierung Effiziente und zuverlässige Kryokonservierung CryoPure Einfriersystem CryoPure - Qualitätskonzept Um Zellmaterialien und deren Bestandteile bei
CryoPure Einfriersystem Beleben Sie Ihre Kryokonservierung Effiziente und zuverlässige Kryokonservierung CryoPure Einfriersystem CryoPure - Qualitätskonzept Um Zellmaterialien und deren Bestandteile bei
Insectomed SF express: Hinweise zur z. len. Information der Biochrom AG vom 05. Mai 2010
 Insectomed SF express: Hinweise zur z Adaption der Insektenzellen len Information der Biochrom AG vom 05. Mai 2010 Das neue serumfreie Insektenzellmedium Insectomed SF express der Biochrom AG eignet sich
Insectomed SF express: Hinweise zur z Adaption der Insektenzellen len Information der Biochrom AG vom 05. Mai 2010 Das neue serumfreie Insektenzellmedium Insectomed SF express der Biochrom AG eignet sich
GEBRAUCHSANLEITUNG. Glutatione Agarose Resin
 GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
GEBRAUCHSANLEITUNG Glutatione Agarose Resin Agarose zur Affinitätsreinigung von GST-Tag-Fusionsproteinen und anderen Glutathion-Bindungsproteinen (Kat.-Nr. 42172) SERVA Electrophoresis GmbH - Carl-Benz-Str.
4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd30-igg1-tnf- Fusionsproteins
 ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
AdnaTest EMT-2/StemCell Add-on ProstateDetect
 AdnaTest EMT-2/StemCell Add-on ProstateDetect RT-PCR-Nachweis von Prostatakrebs-assoziierter Genexpression in angereicherten Tumorzellen Nur für Forschungszwecke Gebrauchsanweisung T-1-537-PP Inhaltsverzeichnis
AdnaTest EMT-2/StemCell Add-on ProstateDetect RT-PCR-Nachweis von Prostatakrebs-assoziierter Genexpression in angereicherten Tumorzellen Nur für Forschungszwecke Gebrauchsanweisung T-1-537-PP Inhaltsverzeichnis
Plasmid DNA purification
 Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
Plasmid DNA purification Excerpt from user manual - Deutsch - NucleoBond Xtra NucleoBond Xtra NucleoBond Xtra Plus NucleoBond Xtra Plus January 2013 / Rev. 11 Plasmid DNA Purification Deutsch Einleitung
4 Methoden. 4.1 Enzymimmunoassay (EIA) 4.1.1 Bestimmung der Zytokine IFNγ, IL-4 und IL-6
 Methoden 35 4 Methoden 4.1 Enzymimmunoassay (EIA) 4.1.1 Bestimmung der Zytokine IFNγ, IL-4 und IL-6 Zur Bestimmung der Zytokine IFNγ, IL-4 und IL-6 wurden Tests der Firma Hölzel Diagnostica Handels GmbH,
Methoden 35 4 Methoden 4.1 Enzymimmunoassay (EIA) 4.1.1 Bestimmung der Zytokine IFNγ, IL-4 und IL-6 Zur Bestimmung der Zytokine IFNγ, IL-4 und IL-6 wurden Tests der Firma Hölzel Diagnostica Handels GmbH,
Das Reagenz speziell für die Transfektion von Säugerzellen mit sirna und mirna
 METAFECTENE SI + Das Reagenz speziell für die Transfektion von Säugerzellen mit sirna und mirna Bestellinformationen, MSDS, Publikationen und Anwendungsbeispiele unter www.biontex.com Produkt Katalognummer
METAFECTENE SI + Das Reagenz speziell für die Transfektion von Säugerzellen mit sirna und mirna Bestellinformationen, MSDS, Publikationen und Anwendungsbeispiele unter www.biontex.com Produkt Katalognummer
SICH AUF DIE PROLIFERATION UND APOPTOSE VON
 GELEE ROYALE (RJ) UND Human Interferon-AlphaN3 (HuIFN-ΑlphaN3) WIRKEN SICH AUF DIE PROLIFERATION UND APOPTOSE VON CaCo 2 ZELLEN AUS UND VERINGERN IHR TUMORIGENES POTENTIAL IN VITRO FILIPIČ B. 1), GRADIŠNIK
GELEE ROYALE (RJ) UND Human Interferon-AlphaN3 (HuIFN-ΑlphaN3) WIRKEN SICH AUF DIE PROLIFERATION UND APOPTOSE VON CaCo 2 ZELLEN AUS UND VERINGERN IHR TUMORIGENES POTENTIAL IN VITRO FILIPIČ B. 1), GRADIŠNIK
Reagenzien Isolierung von Nukleinsäuren
 Aufbewahrung bei Raumtemperatur Anwendung Isolierung ultrareiner Plasmid-DNA aus Bakterienkulturen von 1 ml bis 800 ml. Die Plasmid-DNA eignet sich für Manuelle und automatisierte Sequenzierung mit Fluoreszenzfarbstoffen
Aufbewahrung bei Raumtemperatur Anwendung Isolierung ultrareiner Plasmid-DNA aus Bakterienkulturen von 1 ml bis 800 ml. Die Plasmid-DNA eignet sich für Manuelle und automatisierte Sequenzierung mit Fluoreszenzfarbstoffen
F-I Molekulare Zoologie: Teil I: Expressionsanalysen. Expressionsanalyse mittels RT-PCR
 F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen. Methanol-Fixierung
 Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Methanol-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen.
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Methanol-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen.
Die Rolle des NLRP3- Inflammasom in der Pathogenese der idiopathischen pulmonalen Fibrose und Sarkoidose
 Aus der Medizinischen Universitätsklinik und Poliklinik Abteilung für Pneumologie der Albert-Ludwigs-Universität Freiburg im Breisgau Die Rolle des NLRP3- Inflammasom in der Pathogenese der idiopathischen
Aus der Medizinischen Universitätsklinik und Poliklinik Abteilung für Pneumologie der Albert-Ludwigs-Universität Freiburg im Breisgau Die Rolle des NLRP3- Inflammasom in der Pathogenese der idiopathischen
RealLine DNA Extraction 2
 RealLine Pathogen Diagnostic Kits Gebrauchsinformation RealLine DNA Extraction 2 KIT FÜR DIE EXTRAKTION VON DNA AUS KLINISCHEN PROBEN In-vitro Diagnostikum RealLine DNA-Extraction 2 VBC8897 96 Tests gültig
RealLine Pathogen Diagnostic Kits Gebrauchsinformation RealLine DNA Extraction 2 KIT FÜR DIE EXTRAKTION VON DNA AUS KLINISCHEN PROBEN In-vitro Diagnostikum RealLine DNA-Extraction 2 VBC8897 96 Tests gültig
UE Biochemie II: Flow Cytometry
 UE Biochemie II: Flow Cytometry Lerninhalt: Grundlagen der Durchflußzytometrie: Forward Scatter, Side Scatter, Fluoreszenzintensität; FACS; Lymphozytenpräparation über Ficoll; Hintergrund: Siehe Vorlesung
UE Biochemie II: Flow Cytometry Lerninhalt: Grundlagen der Durchflußzytometrie: Forward Scatter, Side Scatter, Fluoreszenzintensität; FACS; Lymphozytenpräparation über Ficoll; Hintergrund: Siehe Vorlesung
VERSUCH 4: BASOPHIL ACTIVATION TEST
 VERSUCH 4: BASOPHIL ACTIVATION TEST LERNZIELE: 1) IgE Status allergischer vs. naiver Mäuse mittels Basophil Activation TEST 2) Auswertung von FACS Daten mittels Cyflogic Software 3) Statistischer Vergleich
VERSUCH 4: BASOPHIL ACTIVATION TEST LERNZIELE: 1) IgE Status allergischer vs. naiver Mäuse mittels Basophil Activation TEST 2) Auswertung von FACS Daten mittels Cyflogic Software 3) Statistischer Vergleich
EliSpot in der Borreliose-Diagnostik
 EliSpot in der Borreliose-Diagnostik 27.02.2016 Update Lyme Disease for Practitioners BCA-clinic Augsburg Infektion - Infektionserkrankung Invasion und Vermehrung von Mikroorganismen im menschlichen Organismus
EliSpot in der Borreliose-Diagnostik 27.02.2016 Update Lyme Disease for Practitioners BCA-clinic Augsburg Infektion - Infektionserkrankung Invasion und Vermehrung von Mikroorganismen im menschlichen Organismus
Im Einsatz reduziert der C-Chip das Infektionsrisiko durch minimierte Exposition zu biologisch aktiven, infektiösen Materialien.
 Tipps zum Zählen von Zellen mit der neuen Einweg-Zählkammer C-Chip C Chip Biochrom AG Information Die Einweg-Zählkammer C-Chip aus Kunststoff sieht genauso aus wie die bekannte Neubauer improved -Zählkammer.
Tipps zum Zählen von Zellen mit der neuen Einweg-Zählkammer C-Chip C Chip Biochrom AG Information Die Einweg-Zählkammer C-Chip aus Kunststoff sieht genauso aus wie die bekannte Neubauer improved -Zählkammer.
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila
 Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
Funktionelle Organisation des Zellkerns: DNA-Methylierung in Drosophila 01.-04.03.04 Joachim Marhold, Regine Garcia Boy, Natascha Kunert, Cora Mund, Frank Lyko Programm 01.03.04: Präparation genomischer
Datasheet. TriFaster Maximo Aufreinigung von DNA, RNA und Protein aus einer Probe
 TriFaster Maximo Aufreinigung von DNA, RNA und Protein aus einer Probe Features: - Extraktion von RNA, DNA und Proteinen aus der gleichen Probe - Für kleine und große Mengen von Probe - Gleichzeitiges
TriFaster Maximo Aufreinigung von DNA, RNA und Protein aus einer Probe Features: - Extraktion von RNA, DNA und Proteinen aus der gleichen Probe - Für kleine und große Mengen von Probe - Gleichzeitiges
Genisolierung in 2 Stunden : Die Polymerase-Ketten-Reaktion (PCR)
 PCR Genisolierung in 2 Stunden : Die Polymerase-Ketten-Reaktion (PCR) von Kary B. Mullis entwickelt (1985) eigentlich im Mai 1983 bei einer nächtlichen Autofahrt erstes erfolgreiches Experiment am 16.12.1983
PCR Genisolierung in 2 Stunden : Die Polymerase-Ketten-Reaktion (PCR) von Kary B. Mullis entwickelt (1985) eigentlich im Mai 1983 bei einer nächtlichen Autofahrt erstes erfolgreiches Experiment am 16.12.1983
Durchflusszytometrie (Flow
 Durchflusszytometrie (Flow cytometry) Institut für Immunologie und Biotechnologie ie, Medizin inischeische Fakult ultät Universität Pécs Das Prinzip und Bedeutung der Durchflusszytometrie Flowcytometrie
Durchflusszytometrie (Flow cytometry) Institut für Immunologie und Biotechnologie ie, Medizin inischeische Fakult ultät Universität Pécs Das Prinzip und Bedeutung der Durchflusszytometrie Flowcytometrie
peqgold TriFast FL Methode für die gleichzeitige Extraktion von RNA, DNA und Proteinen aus flüssigen Proben.
 peqgold TriFast FL Methode für die gleichzeitige Extraktion von RNA, DNA und Proteinen aus flüssigen Proben. Best.-Nr. 30-2110 100 ml 30-2120 200 ml 30-2130 500 ml Lagerung: Lichtgeschützt bei 4 C für
peqgold TriFast FL Methode für die gleichzeitige Extraktion von RNA, DNA und Proteinen aus flüssigen Proben. Best.-Nr. 30-2110 100 ml 30-2120 200 ml 30-2130 500 ml Lagerung: Lichtgeschützt bei 4 C für
3. Material und Methodik
 3. Material und Methodik 3.1 Arbeitsmaterial und Chemikalien - FITC anti-human CD14-Antikörper, Pharmingen, Heidelberg - PE anti-human TNF-á Antikörper, Pharmingen, Heidelberg - PE anti-human IL-6 Antikörper,
3. Material und Methodik 3.1 Arbeitsmaterial und Chemikalien - FITC anti-human CD14-Antikörper, Pharmingen, Heidelberg - PE anti-human TNF-á Antikörper, Pharmingen, Heidelberg - PE anti-human IL-6 Antikörper,
3 Material und Methodik 3.1 Arbeitsmaterial und Chemikalien
 3 Material und Methodik 3.1 Arbeitsmaterial und Chemikalien FITC anti-human CD14-Antikörper, Pharmingen, Heidelberg PE anti-human TNF-α Antikörper, Pharmingen, Heidelberg PE anti-human IL-6 Antikörper,
3 Material und Methodik 3.1 Arbeitsmaterial und Chemikalien FITC anti-human CD14-Antikörper, Pharmingen, Heidelberg PE anti-human TNF-α Antikörper, Pharmingen, Heidelberg PE anti-human IL-6 Antikörper,
Entwicklung und Validierung der VIROTYPE BVDV real-time RT-PCR
 Entwicklung und Validierung der real-time RT-PCR Gaunitz C, Engemann C, Labitzke M, Schroeder C, Kühn TE, Gabert, J Labor Diagnostik GmbH Leipzig Gliederung Testprinzip Testprotokoll Testcharakteristik
Entwicklung und Validierung der real-time RT-PCR Gaunitz C, Engemann C, Labitzke M, Schroeder C, Kühn TE, Gabert, J Labor Diagnostik GmbH Leipzig Gliederung Testprinzip Testprotokoll Testcharakteristik
Die Isolierung von Cosmid-DNA erfolgte entsprechend den Protokollen von Sambrook et al. (1989).
 3 Methoden 3.1 Isolierung von Cosmid-DNA Die Isolierung von Cosmid-DNA erfolgte entsprechend den Protokollen von Sambrook et al. (1989). 3.2 Präparation von YAC-DNA aus Hefezellen Die Hefe-DNA wurde modifiziert
3 Methoden 3.1 Isolierung von Cosmid-DNA Die Isolierung von Cosmid-DNA erfolgte entsprechend den Protokollen von Sambrook et al. (1989). 3.2 Präparation von YAC-DNA aus Hefezellen Die Hefe-DNA wurde modifiziert
Nachweis von DNA im Wein
 Abschlussbericht über den Forschungsauftrag Nachweis von DNA im Wein Projektlaufzeit: 01.01.2001 bis 31.03.2003 Prof. Dr. Ralf Kaldenhoff Universität Würzburg Julius-von-Sachs-Institut für Biowissenschaften
Abschlussbericht über den Forschungsauftrag Nachweis von DNA im Wein Projektlaufzeit: 01.01.2001 bis 31.03.2003 Prof. Dr. Ralf Kaldenhoff Universität Würzburg Julius-von-Sachs-Institut für Biowissenschaften
SingleQuant Assay Kit
 GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
4.2 Kokulturen Epithelzellen und Makrophagen
 Ergebnisse 4.2 Kokulturen Epithelzellen und Makrophagen Nach der eingehenden Untersuchung der einzelnen Zelllinien wurden die Versuche auf Kokulturen aus den A549-Epithelzellen und den Makrophagenzelllinien
Ergebnisse 4.2 Kokulturen Epithelzellen und Makrophagen Nach der eingehenden Untersuchung der einzelnen Zelllinien wurden die Versuche auf Kokulturen aus den A549-Epithelzellen und den Makrophagenzelllinien
Plasmidisolierung. Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern.
 Plasmidisolierung Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern. Was können Sie lernen? Sie lernen eine ringförmige DNA, ein Plasmid, zu isolieren. Mit diesem
Plasmidisolierung Mit Plasmiden können Sie Gene in Organismen einschleusen und so deren Eigenschaften verändern. Was können Sie lernen? Sie lernen eine ringförmige DNA, ein Plasmid, zu isolieren. Mit diesem
Verzeichnis der Abkürzungen... 6. 1. Einleitung... 9
 Inhaltsverzeichnis Verzeichnis der Abkürzungen... 6 1. Einleitung... 9 1.1 Probiotika...9 1.1.1 Definition und Historisches...9 1.1.2 Klinische Bedeutung probiotisch wirksamer Bakterienstämme...9 1.1.3
Inhaltsverzeichnis Verzeichnis der Abkürzungen... 6 1. Einleitung... 9 1.1 Probiotika...9 1.1.1 Definition und Historisches...9 1.1.2 Klinische Bedeutung probiotisch wirksamer Bakterienstämme...9 1.1.3
Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR
 Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR Vorbereitung Lehrer Für jede Arbeitsgruppe werden 550 µl InstaGene-Matrix aliquotiert! Das Tube wird mit IG beschriftet!
Praktikum: Nachweis einer gentechnischen Veränderung in Lebensmitteln durch PCR Vorbereitung Lehrer Für jede Arbeitsgruppe werden 550 µl InstaGene-Matrix aliquotiert! Das Tube wird mit IG beschriftet!
Metabolische Veränderungen und Zelltod in neuralen Zellen. durch Advanced Glycation Endproducts -
 Metabolische Veränderungen und Zelltod in neuralen Zellen durch Advanced Glycation Endproducts - Implikationen für die Pathogenese der Alzheimer schen Demenz Dissertation zur Erlangung des naturwissenschaftlichen
Metabolische Veränderungen und Zelltod in neuralen Zellen durch Advanced Glycation Endproducts - Implikationen für die Pathogenese der Alzheimer schen Demenz Dissertation zur Erlangung des naturwissenschaftlichen
Produktinformation Saturn-2D REDOX Labeling Kit
 Saturn-2D REDOX Labeling Kit Produktinformation Saturn-2D REDOX Labeling Kit Produkt-Nr. PR34, PR35 NH DyeAGNOSTICS GmbH Weinbergweg 23 D-06120 Halle Deutschland Technischer Support Fon: +49 (0) 345-2799
Saturn-2D REDOX Labeling Kit Produktinformation Saturn-2D REDOX Labeling Kit Produkt-Nr. PR34, PR35 NH DyeAGNOSTICS GmbH Weinbergweg 23 D-06120 Halle Deutschland Technischer Support Fon: +49 (0) 345-2799
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen. Formaldehyd-Fixierung
 Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu
Immunofluoreszenz-Markierung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu
Immunologische Techniken. Gelpräzipitationsreaktionen 1. Immundiffusion 2. Immunelektrophorese
 Immunologische Techniken Gelpräzipitationsreaktionen 1. Immundiffusion 2. Immunelektrophorese Direkte und indirekte Hämagglutination Direkte Hämagglutination: wenig empfindlich Indirekte Hämagglutination:
Immunologische Techniken Gelpräzipitationsreaktionen 1. Immundiffusion 2. Immunelektrophorese Direkte und indirekte Hämagglutination Direkte Hämagglutination: wenig empfindlich Indirekte Hämagglutination:
EdU Click FC ROTI kit für Flow Cytometry
 Gebrauchsanweisung EdU Click FC ROTI kit für Flow Cytometry ROTI kit für Flow Cytometry Carl Roth GmbH + Co. KG EdU Click FC ROTI kit für Flow Cytometry Einleitung und Produktbeschreibung: Die Detektion
Gebrauchsanweisung EdU Click FC ROTI kit für Flow Cytometry ROTI kit für Flow Cytometry Carl Roth GmbH + Co. KG EdU Click FC ROTI kit für Flow Cytometry Einleitung und Produktbeschreibung: Die Detektion
BLOCK 9. Dengue Fieber/ ELISA. N.Brandl 2008
 BLOCK 9 Dengue Fieber/ ELISA N.Brandl 2008 Versuchsaufbau 1. 2. 3. 4. 5. 6. 7. 8. 1. Coaten und Blocken 2. Waschen (3x) 3. Patientenserum (30min) 4. Waschen (3x) 5. Detektionsantikörper (30min) 6. Waschen
BLOCK 9 Dengue Fieber/ ELISA N.Brandl 2008 Versuchsaufbau 1. 2. 3. 4. 5. 6. 7. 8. 1. Coaten und Blocken 2. Waschen (3x) 3. Patientenserum (30min) 4. Waschen (3x) 5. Detektionsantikörper (30min) 6. Waschen
KULTIVIERUNG VON MIKROORGANISMEN
 KULTIVIERUNG VON MIKROORGANISMEN KULTIVIERUNG VON MIKROORGANISMEN Verfahren, das Bakterien außerhalb des natürlichen Standortes zur Vermehrung bringt (unbelebte Substrate oder Zellkulturen) 1 Voraussetzungen
KULTIVIERUNG VON MIKROORGANISMEN KULTIVIERUNG VON MIKROORGANISMEN Verfahren, das Bakterien außerhalb des natürlichen Standortes zur Vermehrung bringt (unbelebte Substrate oder Zellkulturen) 1 Voraussetzungen
LD BioScreen. Low Density Biochip Schnelltest-Systeme. Offenes System für Sandwich-Immunoassays. LD BioScreen
 LD BioScreen Low Density Biochip Schnelltest-Systeme Offenes System für Sandwich-Immunoassays LD BioScreen Die Alternative zur Mikrotiterplatte Für Assays im Forschungslabor Sie sparen Material, Zeit und
LD BioScreen Low Density Biochip Schnelltest-Systeme Offenes System für Sandwich-Immunoassays LD BioScreen Die Alternative zur Mikrotiterplatte Für Assays im Forschungslabor Sie sparen Material, Zeit und
4. Material und Methoden
 16 4. Material und Methoden 4.1 Patienten: Wir untersuchten Leukozyten von Frühgeborenen, Reifgeborenen und von Erwachsenen. Die Einschlusskriterien für die Frühgeborenen waren 1. Gestationsalter 24 32
16 4. Material und Methoden 4.1 Patienten: Wir untersuchten Leukozyten von Frühgeborenen, Reifgeborenen und von Erwachsenen. Die Einschlusskriterien für die Frühgeborenen waren 1. Gestationsalter 24 32
3 GFP green fluorescent protein
 SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
Mycoplasma gallisepticum
 BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
3 Methoden. Methoden 24. 3.1 Zellkultur. Kultivieren von Zellen
 Methoden 24 3 Methoden 3.1 Zellkultur Kultivieren von Zellen Die Nierenkarzinomzelllinien A498, SN12 und ACHN (Referenzen für die verwendeten Zelllinien siehe unter 2.2) wurden nach Anleitung der American
Methoden 24 3 Methoden 3.1 Zellkultur Kultivieren von Zellen Die Nierenkarzinomzelllinien A498, SN12 und ACHN (Referenzen für die verwendeten Zelllinien siehe unter 2.2) wurden nach Anleitung der American
5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp)
 8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
Firmengründung 1992 GLP-Status seit 1993. 41468 Neuss Am Röttgen 126
 Firmengründung 1992 GLP-Status seit 1993 41468 Neuss Am Röttgen 126 Fragestellung: Quantifizierung von 5-Methyltetrahydrofolat in Humanplasma und -vollblut Begriffsbestimmung: Folsäure hitzelabiles, lichtempfindliches,
Firmengründung 1992 GLP-Status seit 1993 41468 Neuss Am Röttgen 126 Fragestellung: Quantifizierung von 5-Methyltetrahydrofolat in Humanplasma und -vollblut Begriffsbestimmung: Folsäure hitzelabiles, lichtempfindliches,
Mycobacterium paratuberculosis
 BACTOTYPE PCR Amplification Kit Mycobacterium paratuberculosis Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Mycobacterium paratuberculosis Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Wochenbericht vom 5.7.99 16.7.99, 03.01.00 04.02.00 Infektionsimmunologie
 Wochenbericht vom 5.7.99 16.7.99, 03.01.00 04.02.00 Infektionsimmunologie Nils Volkening Ziel der Untersuchung ist die quantitative Angabe der nachgewiesenen Antikörper gegen z.b. CMV, HSV, VZV, jeweils
Wochenbericht vom 5.7.99 16.7.99, 03.01.00 04.02.00 Infektionsimmunologie Nils Volkening Ziel der Untersuchung ist die quantitative Angabe der nachgewiesenen Antikörper gegen z.b. CMV, HSV, VZV, jeweils
RESOLUTION OIV/OENO 427/2010 KRITERIEN FÜR METHODEN ZUR QUANTIFIZIERUNG VON POTENTIELL ALLERGENEN RÜCKSTÄNDEN EIWEISSHALTIGER SCHÖNUNGSMITTEL IM WEIN
 RESOLUTION OIV/OENO 427/2010 KRITERIEN FÜR METHODEN ZUR QUANTIFIZIERUNG VON POTENTIELL ALLERGENEN RÜCKSTÄNDEN EIWEISSHALTIGER SCHÖNUNGSMITTEL IM WEIN Die GENERALVERSAMMLUNG, unter Berücksichtigung des
RESOLUTION OIV/OENO 427/2010 KRITERIEN FÜR METHODEN ZUR QUANTIFIZIERUNG VON POTENTIELL ALLERGENEN RÜCKSTÄNDEN EIWEISSHALTIGER SCHÖNUNGSMITTEL IM WEIN Die GENERALVERSAMMLUNG, unter Berücksichtigung des
2.1.4. Industriell gefertigte Testkits für den Nachweis von IgG- oder IgM- Antikörpern gegen A. phagocytophilum
 2. Material und Methoden 2.1. Materialverzeichnis 2.1.1. Technische Geräte Brutschrank (Heraeus, Hanau) Fluoreszenzmikroskop mit einer Wellenlänge von 390-420 nm (Zeiss, Jena) Vortex Mixer Reax 2000 (Heidolph,
2. Material und Methoden 2.1. Materialverzeichnis 2.1.1. Technische Geräte Brutschrank (Heraeus, Hanau) Fluoreszenzmikroskop mit einer Wellenlänge von 390-420 nm (Zeiss, Jena) Vortex Mixer Reax 2000 (Heidolph,
Gebrauchsanweisung. Microbial Transglutaminase (MTG) ELISA
 Gebrauchsanweisung Microbial Transglutaminase (MTG) ELISA Enzymimmunoassay zur quantitativen Bestimmung von Mikrobieller Transglutaminase (MTG) Art.-Nr. E021 Für Forschungs & Entwicklungszwecke Revision
Gebrauchsanweisung Microbial Transglutaminase (MTG) ELISA Enzymimmunoassay zur quantitativen Bestimmung von Mikrobieller Transglutaminase (MTG) Art.-Nr. E021 Für Forschungs & Entwicklungszwecke Revision
Applications Note 229 August 2010
 Applications Note 229 August 2010 Weiterverwendung von mehrfach in Eppendorf BioPhotometer plus TM und UVette gemessenen DNA- Proben für PCR- und real-time PCR Experimente Martin Armbrecht, Nils Gerke,
Applications Note 229 August 2010 Weiterverwendung von mehrfach in Eppendorf BioPhotometer plus TM und UVette gemessenen DNA- Proben für PCR- und real-time PCR Experimente Martin Armbrecht, Nils Gerke,
Charakterisierung von Tumor initiierenden Zellen mit randomisierten Phagenpeptidbanken
 Charakterisierung von Tumor initiierenden Zellen mit randomisierten Phagenpeptidbanken S. Adebahr 1, M. Henke 1, R. Mertelsmann 2, G. Niedermann 1, M. Trepel 2,3 1 Klinik für Strahlenheilkunde, Universitätsklinikum
Charakterisierung von Tumor initiierenden Zellen mit randomisierten Phagenpeptidbanken S. Adebahr 1, M. Henke 1, R. Mertelsmann 2, G. Niedermann 1, M. Trepel 2,3 1 Klinik für Strahlenheilkunde, Universitätsklinikum
Santa Cruz, Santa Cruz, USA. Bovines Serumalbumin, BSA, Fraktion V Serva, Heidelberg Miltenyi Biotec, Bergisch Gladbach. BD Biosciences, Heidelberg
 8 Materialien 8.1 Reagenzien 8.1.1 Reagenzien für die Blutentnahme, Isolierung von PBMC, Magnetische Zellseparation und Durchflusszytometrie anticd 14-PerCP, #345786 antiigg 2a -FITC, #349051 antiigg 2a
8 Materialien 8.1 Reagenzien 8.1.1 Reagenzien für die Blutentnahme, Isolierung von PBMC, Magnetische Zellseparation und Durchflusszytometrie anticd 14-PerCP, #345786 antiigg 2a -FITC, #349051 antiigg 2a
Borrelia burgdorferi s.l.
 BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
5x QPCR Mix (ROX) Datenblatt. Artikel-Nr. BS µl Artikel-Nr. BS µl. (Nur für Forschung und in vitro-anwendungen)
 Datenblatt Artikel-Nr. BS76.520.0200 200 µl Artikel-Nr. BS76.520.1000 1.000 µl Artikel-Nr. BS76.520.5000 5.000 µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS76.520.0200 200 µl Artikel-Nr. BS76.520.1000 1.000 µl Artikel-Nr. BS76.520.5000 5.000 µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
PFBV - ELISA. Enzyme Linked Immuno Sorbent Assay. zum Nachweis des. Pelargonium flower break virus (PFBV)
 Baumgartenstr. 5 D-79285 Ebringen (FRG) Tel.: +49 7664 600254 Fax: +49 7664 600255 Email: info@steffens-biotec.com PFBV - ELISA Enzyme Linked Immuno Sorbent Assay zum Nachweis des Pelargonium flower break
Baumgartenstr. 5 D-79285 Ebringen (FRG) Tel.: +49 7664 600254 Fax: +49 7664 600255 Email: info@steffens-biotec.com PFBV - ELISA Enzyme Linked Immuno Sorbent Assay zum Nachweis des Pelargonium flower break
Packungsbeilage. Trypsin ELISA IVD 01-10-200 MAIER. analytik. Löhergasse 1. 74889 Sinsheim. Germany
 MAIER analytik g m b h Packungsbeilage Trypsin ELISA IVD 01-10-200 MAIER analytik g m b h Löhergasse 1 74889 Sinsheim Germany Tel.: 07261/655053 Fax.: 07261/979912 e-mail: intelact@t-online.de http://www.maier-analytik.de
MAIER analytik g m b h Packungsbeilage Trypsin ELISA IVD 01-10-200 MAIER analytik g m b h Löhergasse 1 74889 Sinsheim Germany Tel.: 07261/655053 Fax.: 07261/979912 e-mail: intelact@t-online.de http://www.maier-analytik.de
SERVALight EosUltra Western Blot Chemilumineszenz HRP Substrat Kit
 GEBRAUCHSANLEITUNG SERVALight EosUltra Western Blot Chemilumineszenz HRP Substrat Kit (Kat.-Nr. 42586) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG SERVALight EosUltra Western Blot Chemilumineszenz HRP Substrat Kit (Kat.-Nr. 42586) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
Inauguraldissertation zur Erlangung der Doktorwürde der Medizinischen Fakultät der Christian-Albrechts-Universität zu Kiel.
 Aus der Medizinischen Klinik II, Hämatologie und Onkologie (Direktor: Prof. Dr. med. Dr. rer. nat. Michael Kneba) im Universitätsklinikum Schleswig-Holstein, Campus Kiel an der Christian-Albrechts-Universität
Aus der Medizinischen Klinik II, Hämatologie und Onkologie (Direktor: Prof. Dr. med. Dr. rer. nat. Michael Kneba) im Universitätsklinikum Schleswig-Holstein, Campus Kiel an der Christian-Albrechts-Universität
Gentechnologie: Isolierung und Charakterisierung von DNA
 Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Klassifizierung: noch nicht abgeschlossen, Verwandtschaftsverhältnis zur Familie: Desulvovibrionaceae - Vertreter Desulvovibrio desulfuricans
 AVID X / 1998 Lawsonia intracellularis Seite -1- Klassifizierung: noch nicht abgeschlossen, Verwandtschaftsverhältnis zur Familie: Desulvovibrionaceae - Vertreter Desulvovibrio desulfuricans 1. ALLGEMEINES
AVID X / 1998 Lawsonia intracellularis Seite -1- Klassifizierung: noch nicht abgeschlossen, Verwandtschaftsverhältnis zur Familie: Desulvovibrionaceae - Vertreter Desulvovibrio desulfuricans 1. ALLGEMEINES
Inhaltsverzeichnis. Polymerase Chain Reaction Theoretischer Hintergrund - 2 -
 Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Western Blot. Zuerst wird ein Proteingemisch mit Hilfe einer Gel-Elektrophorese aufgetrennt.
 Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
III. Material und Methode
 III. Material und Methode 1. Herkunft der Eier Die Untersuchungen wurden an Hühnerembryonen der Rasse Weißes Leghorn durchgeführt. Diese stammten aus dem Tierstall der Veterinärmedizin der FU Berlin. 2.
III. Material und Methode 1. Herkunft der Eier Die Untersuchungen wurden an Hühnerembryonen der Rasse Weißes Leghorn durchgeführt. Diese stammten aus dem Tierstall der Veterinärmedizin der FU Berlin. 2.
ELISA PeliClass human IgG subclass kit REF M1551
 Sanquin Reagents Plesmanlaan 5 0 CX Amsterdam The Netherlands Phone: +.0.5.599 Fax: +.0.5.570 Email: reagents@sanquin.nl Website: www.sanquinreagents.com M55/ November 007 ELISA PeliClass human IgG subclass
Sanquin Reagents Plesmanlaan 5 0 CX Amsterdam The Netherlands Phone: +.0.5.599 Fax: +.0.5.570 Email: reagents@sanquin.nl Website: www.sanquinreagents.com M55/ November 007 ELISA PeliClass human IgG subclass
Chlamydia sp. BACTOTYPE PCR Amplification Kit. Gebrauchsanweisung. Labor Diagnostik Leipzig
 BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
MutaREAL Cytomegalovirus real time PCR Kit
 MutaREAL Cytomegalovirus real time PCR Kit Screening Test für den Nachweis von humanen Cytomegaloviren (CMV) mittels real time PCR. KV2900324 KV2900396 Nur für Forschungszwecke Immundiagnostik AG, Stubenwald-Allee
MutaREAL Cytomegalovirus real time PCR Kit Screening Test für den Nachweis von humanen Cytomegaloviren (CMV) mittels real time PCR. KV2900324 KV2900396 Nur für Forschungszwecke Immundiagnostik AG, Stubenwald-Allee
Probe und Probenmenge Wassermenge Auftragspuffermenge 5 µl Kaninchenmuskelextrakt 50 µl 100 µl
 Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
1 µl BamHI H 2 O 21 µl H 2 O 30 µl Volumen 18 µl H 2 O 30 µl Inkubation 2h @ 37 C 2h @ 37 C
 F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
www.gbo.com/bioscience Gewebekultur 1 Zell- und Microplatten 2 HTS- 3 Immunologie/ HLA 4 Mikrobiologie/ Bakteriologie Mehrzweckgefäße 5 Röhrchen/
 13 Reaktions/ 2 HTS 1 Zell und Reaktionsgefäße für die PCR 7 I 2 PCR Tubes 7 I 2 PCR 8er Streifen 7 I 3 PCR 7 I 4 Polypropylen 7 I 4 384 Well Polypropylen 7 I 4 PCR Kompatibilitätstabelle 7 I 6 ThermoQuick
13 Reaktions/ 2 HTS 1 Zell und Reaktionsgefäße für die PCR 7 I 2 PCR Tubes 7 I 2 PCR 8er Streifen 7 I 3 PCR 7 I 4 Polypropylen 7 I 4 384 Well Polypropylen 7 I 4 PCR Kompatibilitätstabelle 7 I 6 ThermoQuick
Einfluss von Immunsuppressiva auf die antivirale T-Zellantwort ex vivo
 Aus der Universitätsklinik für Kinder- und Jugendmedizin Tübingen Abteilung Kinderheilkunde I mit Poliklinik Ärztlicher Direktor: Professor Dr. R. Handgretinger Einfluss von Immunsuppressiva auf die antivirale
Aus der Universitätsklinik für Kinder- und Jugendmedizin Tübingen Abteilung Kinderheilkunde I mit Poliklinik Ärztlicher Direktor: Professor Dr. R. Handgretinger Einfluss von Immunsuppressiva auf die antivirale
Inhaltsverzeichnis. Seite 1
 Inhaltsverzeichnis Inhaltsverzeichnis... 1 Abkürzungen... 2 1 Zusammenfassung... 3 2 Einleitung... 4 3 Material und Methoden... 5 3.1 Messung der Absorptionsspektren... 5 3.2.1 Kultivierung der Kartoffel...
Inhaltsverzeichnis Inhaltsverzeichnis... 1 Abkürzungen... 2 1 Zusammenfassung... 3 2 Einleitung... 4 3 Material und Methoden... 5 3.1 Messung der Absorptionsspektren... 5 3.2.1 Kultivierung der Kartoffel...
Etablierung einer. Homemade - PCR
 Etablierung einer Homemade - PCR Anja Schöpflin Institut für Pathologie Universitätsklinikum Freiburg Überblick: Anwendungsgebiete der PCR Anforderungen an Primer Auswahl geeigneter Primer / Primerdesign
Etablierung einer Homemade - PCR Anja Schöpflin Institut für Pathologie Universitätsklinikum Freiburg Überblick: Anwendungsgebiete der PCR Anforderungen an Primer Auswahl geeigneter Primer / Primerdesign
Bradford Reagent, 5x
 GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
o 16 µl als Backup für PCR s
 Metagenomsequenzierung von klinischen LiquorProben Standard Operating Protocol Dr. Meik Dilcher, Abteilung für Virologie, Universitätsmedizin Göttingen Email: mdilche1@gwdg.de Dieses Protokoll wurde im
Metagenomsequenzierung von klinischen LiquorProben Standard Operating Protocol Dr. Meik Dilcher, Abteilung für Virologie, Universitätsmedizin Göttingen Email: mdilche1@gwdg.de Dieses Protokoll wurde im
Vorbereitungen. 1 Vortage: - Mit LehrerIn Kontakt aufnehmen: Schüler sollen Geranienblätter mitbringen!! - sonst: Geranienblätter besorgen!!
 Vorbereitungen 1 Vortage: - Mit LehrerIn Kontakt aufnehmen: Schüler sollen Geranienblätter mitbringen!! - sonst: Geranienblätter besorgen!! 2 am Tag: - alle Reagenzien aus dem Kühlschrank holen: sie sollten
Vorbereitungen 1 Vortage: - Mit LehrerIn Kontakt aufnehmen: Schüler sollen Geranienblätter mitbringen!! - sonst: Geranienblätter besorgen!! 2 am Tag: - alle Reagenzien aus dem Kühlschrank holen: sie sollten
Lebend / Tot Differenzierung von bierschädlichen Bakterien mittels Real-Time PCR
 Lebend / Tot Differenzierung von bierschädlichen Bakterien mittels Real-Time PCR Autoren: Dipl.-Ing. Andreas Brandl, Dr.-Ing. Christoph Tenge, Prof. Dr.-Ing. Eberhard Geiger, Lehrstuhl für Technologie
Lebend / Tot Differenzierung von bierschädlichen Bakterien mittels Real-Time PCR Autoren: Dipl.-Ing. Andreas Brandl, Dr.-Ing. Christoph Tenge, Prof. Dr.-Ing. Eberhard Geiger, Lehrstuhl für Technologie
Identifizierung positiver Klone aus einer λ-phagenbibliothek
 Identifizierung positiver Klone aus einer λ-phagenbibliothek Betreuer: Elke Muth-Köhne und Nora Cavara Beginn des Versuchs: 9.00 Uhr im Praktikumssaal NBCF 04 Nord 1. Theoretischer Hintergrund 1.1 Screening
Identifizierung positiver Klone aus einer λ-phagenbibliothek Betreuer: Elke Muth-Köhne und Nora Cavara Beginn des Versuchs: 9.00 Uhr im Praktikumssaal NBCF 04 Nord 1. Theoretischer Hintergrund 1.1 Screening
WST-1 CTLL-2 Proliferations-Kit (ready-to-use)
 Immunservice WST-1 CTLL-2 Proliferations-Kit (ready-to-use) Optimiert für Anwendungen mit CTLL-2 Zellen GEBRAUCHSANWEISUNG Nur zu Forschungszwecken. Nicht zum Einsatz in diagnostischen oder therapeutischen
Immunservice WST-1 CTLL-2 Proliferations-Kit (ready-to-use) Optimiert für Anwendungen mit CTLL-2 Zellen GEBRAUCHSANWEISUNG Nur zu Forschungszwecken. Nicht zum Einsatz in diagnostischen oder therapeutischen
Praktikumsteil: Zellkultur und Fluoreszenzmikroskopie
 (Version: 2008 12 02) Praktikumsteil: Zellkultur und Fluoreszenzmikroskopie Darstellung und Untersuchung von Zellorganellen und Zytoskelettkomponenten Einleitung Der Lokalisation von Proteinen kommt in
(Version: 2008 12 02) Praktikumsteil: Zellkultur und Fluoreszenzmikroskopie Darstellung und Untersuchung von Zellorganellen und Zytoskelettkomponenten Einleitung Der Lokalisation von Proteinen kommt in
Versuchsanleitungen für das Praktikum des Mastermoduls Ernährung und Immunologie
 Arbeitsanleitungen für das Praktikum des Mastermoduls Ernährung und Immunologie 2011 1 Versuchsanleitungen für das Praktikum des Mastermoduls Ernährung und Immunologie Arbeitsanleitungen für das Praktikum
Arbeitsanleitungen für das Praktikum des Mastermoduls Ernährung und Immunologie 2011 1 Versuchsanleitungen für das Praktikum des Mastermoduls Ernährung und Immunologie Arbeitsanleitungen für das Praktikum
3. Hämoglobin-Screening bei Blutspendern Spezielle Fragestellung
 3. Hämoglobin-Screening bei Blutspendern 3.1. Spezielle Fragestellung Eine Messung der Hämoglobin-Konzentration ist als Tauglichkeitsuntersuchung vor jeder freiwilligen Blutspende vorgeschrieben. Bei Unterschreiten
3. Hämoglobin-Screening bei Blutspendern 3.1. Spezielle Fragestellung Eine Messung der Hämoglobin-Konzentration ist als Tauglichkeitsuntersuchung vor jeder freiwilligen Blutspende vorgeschrieben. Bei Unterschreiten
Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres (Marmota monax)
 Aus der Abteilung Innere Medizin II der Medizinischen Universitätsklinik der Albert-Ludwigs-Universität Freiburg im Breisgau Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres
Aus der Abteilung Innere Medizin II der Medizinischen Universitätsklinik der Albert-Ludwigs-Universität Freiburg im Breisgau Herstellung und Charakterisierung von zellpermeablem Interferon-α des Waldmurmeltieres
Der Einfluss von Vitamin D 3 auf endotheliale Reparaturprozesse im Zusammenhang mit der Präeklampsie
 Aus der Klinik für Frauenheilkunde und Geburtshilfe der Medizinischen Hochschule Hannover Der Einfluss von Vitamin D 3 auf endotheliale Reparaturprozesse im Zusammenhang mit der Präeklampsie Dissertation
Aus der Klinik für Frauenheilkunde und Geburtshilfe der Medizinischen Hochschule Hannover Der Einfluss von Vitamin D 3 auf endotheliale Reparaturprozesse im Zusammenhang mit der Präeklampsie Dissertation
Gebrauchsanleitung ChromoQuant QF-PCR Kit P/N 412.001-48
 Gebrauchsanleitung ChromoQuant QF-PCR Kit P/N 412.001-48 ChromoQuant Das ChromoQuant in vitro Diagnose-Set QF-PCR 1 zur Analyse von häufigen chromosomalen Erkrankungen der Chromosomen 13, 18 und 21 412.001-48u
Gebrauchsanleitung ChromoQuant QF-PCR Kit P/N 412.001-48 ChromoQuant Das ChromoQuant in vitro Diagnose-Set QF-PCR 1 zur Analyse von häufigen chromosomalen Erkrankungen der Chromosomen 13, 18 und 21 412.001-48u
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Testosteron ELISA, EIA
 Testosteron ELISA, EIA Enzymimmunoassay für Testosteron in porcinem Serum/Plasma Kurzbeschreibung der Assay-Durchführung 1. Testbestandteile und Lösungen auf Raumtemperatur bringen (Ausnahme: Tracer-Stammlösung
Testosteron ELISA, EIA Enzymimmunoassay für Testosteron in porcinem Serum/Plasma Kurzbeschreibung der Assay-Durchführung 1. Testbestandteile und Lösungen auf Raumtemperatur bringen (Ausnahme: Tracer-Stammlösung
Genetik im Unterricht WS 01/02
 Fachdidaktisches Praktikum B.Durst, H-G.Edelmann Stand 24. 2. 02 Seite 32 AB 1 für LehrerInnen Seite 1/5 Vorbereitungen 1 Vortage: - Mit LehrerIn Kontakt aufnehmen: Schüler sollen Geranienblätter mitbringen!!
Fachdidaktisches Praktikum B.Durst, H-G.Edelmann Stand 24. 2. 02 Seite 32 AB 1 für LehrerInnen Seite 1/5 Vorbereitungen 1 Vortage: - Mit LehrerIn Kontakt aufnehmen: Schüler sollen Geranienblätter mitbringen!!
Die antivirale Therapie der chronischen Hepatitis B: Identifikation neuer Resistenzmutationen und Optimierung der Verlaufskontrolle
 Angefertigt am Fachbereich 08 - Biologie und Chemie in Zusammenarbeit mit dem Institut für Medizinische Virologie am Fachbereich 11- Medizin der Justus-Liebig-Universität Gießen Die antivirale Therapie
Angefertigt am Fachbereich 08 - Biologie und Chemie in Zusammenarbeit mit dem Institut für Medizinische Virologie am Fachbereich 11- Medizin der Justus-Liebig-Universität Gießen Die antivirale Therapie
