Thermodynamik 2 Klausur 12. März Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen.
|
|
|
- Waldemar Adenauer
- vor 6 Jahren
- Abrufe
Transkript
1 Institut für Energie- und Verfahrenstechnik Thermodynamik und Energietechnik Prof. Dr.-Ing. habil. Jadran Vrabec ThEt Thermodynamik 2 Klausur 12. März 2010 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 5 nummerierte Seiten Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind als Hilfsmittel zugelassen. Geben Sie diese Aufgabenstellung bitte zusammen mit Ihren Lösungsblättern ab. Füllen Sie die Angaben zu Ihrer Person aus und versehen Sie jedes Lösungsblatt mit Ihrem Namen. Name: Vorname: Matrikelnummer: Unterschrift: Angaben zur Korrektur Aufgabe Maximale Punktzahl Erreichte Punkte Korrektor Zwischensumme Bonuspunkte Summe Bewertung - 1 -
2 Aufgabe 1 (14 Punkte) Ausgehend von einer zentralen Kälteanlage (ZKA) wird ṁ = 2,5 kg/s verflüssigtes Octafluorcyclobutan (C 4F 8) zu k = 10 hier als gleichartig angenommenen Verbrauchern transportiert, von denen jeder einen Massenstrom von ṁ / k erhält. Die folgenden Schritte eines Kompressionskälteprozesses finden in der ZKA statt. Das Kühlgut darf die Temperatur T 0 = 0 C nicht überschreiten. Bei der Kühlung ist eine Temperaturdifferenz ΔT 10 K zwischen Kühlgut und Kältemittel zu garantieren. 1 2 Kompression des Dampfs beginnt bei der Temperatur T 1 = 15 C mit einem isentropen Wirkungsgrad von η s = 75 %, wobei die Temperatur T 2 erreicht wird. 2 3 Vollständige Kondensation ohne Unterkühlung durch isobare Wärmeabgabe an die Umgebung bei einem Druck von p 2 = p s(30 C) Beim Transport von der ZKA zum Verbraucher ist eine Wärmeübertragung zwischen dem kondensierten Kältemittel bei p 3 und dem verdampften Kältemittel bei p 1 zu berücksichtigen. Es liegt mindestens eine Temperaturdifferenz von ΔT = 15 K vor. Die folgenden Schritte finden beim Verbraucher statt: 3 4 Drosselung des flüssigen, unterkühlten Kältemittels auf den Druck p Teilweise Verdampfung, wobei die Kälteleistung erbracht wird. (Punkt 5 liegt im ND) Beim Transport vom Verbraucher zur ZKA ist ebenfalls eine Zustandsänderung des Kältemittels zu berücksichtigen: 5 1 Isobare Wärmezufuhr aus der Umgebung. Der Transport stellt eine zusätzliche Wärmelast von 2 kw pro Verbraucher dar. Der Druckverlust beim Transport ist zu vernachlässigen. a) Skizzieren Sie den Kälteprozess qualitativ in einem log p, h - Diagramm. (4 P) b) Welche technische Leistung muss der Kompressor erbringen? Gehen Sie dabei zunächst vom isentropen Fall aus, und berücksichtigen Sie dann den Wirkungsgrad des Kompressors. (5 P) c) Welche Kälteleistung ergibt sich bei einem Verbraucher, und welcher Dampfgehalt x 5 wird beim Erbringen der Kälteleistung erreicht? (4 P) d) Welche Leistungszahl ergibt sich für den dargestellten Prozess? (1 P) Daten und Hinweise: Die molare Masse von Octafluorcyclobutan beträgt 200 g/mol, damit ist R = 0, J/(g*K). T ps ρ' ρ'' h' h'' s' s'' c p' c p'' C kpa kg/m³ kg/m³ kj/kg kj/kg J/(g*K) J/(g*K) J/(g*K) J/(g*K) , , ,6 307,8 0,9612 1,411 1,032 0, , ,14 210,7 320,7 1,038 1,429 1,077 0, , ,70 232,7 332,4 1,113 1,449 1,127 0, , ,29 255,8 347,7 1,186 1,470 1,186 0, ,1 280,2 359,7 1,259 1,490 1,273 1, ,7 306,6 369,6 1,332 1,505 1,457 1,2490 ' siedende Flüssigkeit Das Gas kann als ideales Gas betrachtet werden '' gesättigter Dampf
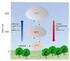
3 Aufgabe 2 (22 Punkte): Das Bild zeigt ein Verfahren der Meerwasserentsalzung mit indirekter Übertragung der Kondensationswärme. Da Verdunstungsbefeuchter und Kondensator keine Einheit mit direktem thermischem Kontakt darstellen, sind viele konstruktive Möglichkeiten zur Gestaltung der beiden Anlagenelemente möglich. Der Befeuchter wird z.b. mit Holzlamellen versehen, an denen die Sole herunter rieselt. Die Luft (L1) wird im Kondensator gekühlt, wobei der enthaltene Wasserdampf teilweise auskondensiert (W5). Dabei wird das Meerwasser (W1 W2) aufgeheizt. Im Solarkollektor wird das Meerwasser weiter erhitzt (W3) und dann im Verdunstungsbefeuchter über Dornbüsche versprüht. Während es herunter rinnt verdunstet ein Teil des Wassers, das übrige Wasser erwärmt die im Gegenstrom aufsteigende Luft(L3 L4). Um den Wasserstrom (W1 W3) zu verringern, wird ein Teil (75%) der Wärme durch zahlreiche Wärmerohre der feuchten Luft im Kondensator (rechts) entzogen und der trockenen Luft im Befeuchter (links) zugeführt. Zur erneuten Wasserdampfaufnahme muss die Luft (L3) erwärmt werden. Das geschieht durch die über die Wärmerohre zugeführte Wärme und das im Solarkollektor aufgeheizte Wasser
4 Annahmen für die Rechnung: Die Luft kann im Kondensator von t L1 = 80 C, ϕ L1 =0,95 auf t L2 = 35 C abgekühlt werden. Im Zustand L3 ist sie mit Wasserdampf gesättigt. Das auskondensierte Wasser (W5) verläßt den Kondensator mit t kond = 35 C. Das Meerwasser (W1) wird von t W1 = 25 C auf t W2 = 70 C aufgeheizt. Die Fragen a) bis e) sind mit dem h 1+x,x-Diagramm zu lösen, die Frage f) ohne Informationen aus dem Diagramm. a) Tragen Sie die Zustandspunkte der Luft in dem h 1+x,x-Diagramm ein. Berücksichtigen Sie die zahlreichen Zwischenaufheizungen durch die Wärmerohre. Im Effekt ist die Summe der zahlreichen Aufheizungen und Befeuchtungen eine Zustandsänderung nahe an der Sättigungslinie. (4 P) b) Bestimmen Sie die spezifischen Enthalpien h 1+x der Luftzustände L1 und L2. Beachten Sie die Übersättigung der Luft im Zustand L2. (3 P) c) Wie viel Meerwasser kann pro m 3 Luft (Zustand L3) aufgewärmt werden? Wie viel Kondensat fällt pro m 3 Luft aus? d) Stellen Sie die Massen- und Enthalpiebilanz für den Befeuchter auf, unter der Annahme, dass die Luft unten mit t L3 = 35 C eintritt und oben mit t L4 = 80 C, ϕ L4 =0,95 austritt und die Sole (W4) mit t S = 45 C unten abläuft. Beachten Sie, dass 75% der der Luft entnommenen Wärme über die Wärmerohre übertragen wird. Wie hoch muss die Eintrittstemperatur des Meerwassers sein? (4 P) e) Das Meerwasser steht im Solarkollektor unter einem Druck von 1,2 bar. Welche Wärmemenge ist erforderlich für die Aufheizung des Meerwassers im Solarkollektor? Wie viel ist das pro kg Destillat? (2 P) f) Berechnen Sie die spezifischen Enthalpien der Luftzustände L1 und L2 ohne Informationen aus dem Diagramm. (6 P) (3P) Stoffdaten: Luft und Wasserdampf können als ideale Gase betrachtet werden. Dampfdruck von Wasser: p 3970,148 K ln =11, p0 T - 40,052 K mit T < 390 K in K, p0 = 1 bar Der Gesamtdruck beträgt Pa. Die Verdampfungsenthalpie von Wasser bei 0 C beträgt h v0 = r 0 = 2500 kj/kg. Die Enthalpie ist 0 kj/kg für trockene Luft und flüssiges Wasser bei 0 C. Die spezifische isobare Wärmekapazität der trockenen Luft: c pl = 1,004 kj/(kg K) des Wasserdampfs: c p,h2o,g. = 1,860 kj/(kg K) des flüssigen Wassers: c p,h2o,fl. = 4,192 kj/(kg K) Molmassen: Luft: 28,96 g/mol Wasser: 18,015 g/mol R m = 8, J/(mol K) - 4 -
5 Aufgabe 3 (14 Punkte): In naher Zukunft wird Heizöl knapp und teuer werden. Erdgas wird dann ebenfalls teurer. Deshalb werden heute wieder nachwachsende Rohstoffe wie Holzpellets aus gepressten Holzabfällen als Heizmaterial genutzt. Holzpellets haben einen Energieinhalt = unterer Heizwert = 5 kwh/kg. Die Zusammensetzung des trockenen Holzes in Massenanteilen (kg/kg): ζ C = 0,50 kg/kg; ζ H2 = 0,06 kg/kg; ζ O2 = 0,42 kg/kg; ζ N2 = 0,01 kg/kg, ζ K = 0,01 kg/kg. Das 0,01 kg/kg sind verschiedene Mineralstoffe, die hier vereinfachend als Kalium angenommen werden sollen. a) Bestimmen Sie die molare Zusammensetzung des trockenen Holzes und den unteren Heizwert pro mol. (4 P) b) Bestimmen Sie in der Reaktionsgleichung die stöchiometrischen Faktoren und die zugeführte Sauerstoffmenge wenn Luft mit λ=1,2 zugeführt wird. ν CC CC + ν HH2 HH 2 + ν OO2 OO 2 + ν NN2 NN 2 + ν KK KK + ν OO2,LLLLLLLL OO 2 + ν NN2,LLLLLLLL NN 2 ν CCCC2 CCCC 2 + ν HH2OO HH 2 OO + ν PPPPPPPPPPPPPPhee KK 2 CCOO 3 + ν OO2,RRRRRRRR OO 2 + ν NN2,gggggg NN 2 Die Pottasche = Kaliumcarbonat (K 2CO 3) bleibt als Asche zurück. Beachten Sie den Bedarf an C und O in der Pottasche. (4 P) Wie ist die Zusammensetzung des Abgases? (2 P) c) Welche maximale Temperatur stellt sich in der Flamme ein, bevor Wärme an die Wände der Brennkammer abgegeben wird? Luft und Holz werden mit T = T θ = 25 C zugeführt. Vernachlässigen Sie die Enthalpie der Asche. (2 P) d) Welche Wärme lässt sich pro kg Holzpellets gewinnen, wenn die Abgase mit 110 C den Ofen verlassen? (2 P) λλ = ψψ OO2,EEEEEEEEEEEE ψψ OO2,SSSSöcchiiiiiiiiiiiiiiiiiih EEEEEEEEEEEE Stoffdaten: Stoff M g / mol B h Θ kj / mol C 12,000 0 H 2 2,007 0 T max c o p TΘ J / (mol K) C c o p TΘ J / (mol K) N 2 28, ,28 30,11 O 2 32, ,17 31,75 CO 2 44,00-393,51 54,44 45,85 H 2O (l) 18, ,83 H 2O (g) 18, ,83 43,97 36,15 K 39,098 0 Molare Zusammensetzung der trockenen Luft: ψ N2 = 0,79 mol/mol; ψ O2 = 0,21 mol/mol.
6 - 6 -
Thermodynamik 2 Klausur 17. Februar 2015
 Thermodynamik 2 Klausur 17. Februar 2015 Bearbeitungszeit: Umfang der Aufgabenstellung: 120 Minuten 5 nummerierte Seiten 2 Diagramme Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner
Thermodynamik 2 Klausur 17. Februar 2015 Bearbeitungszeit: Umfang der Aufgabenstellung: 120 Minuten 5 nummerierte Seiten 2 Diagramme Alle Unterlagen zu Vorlesung und Übung sowie Lehrbücher und Taschenrechner
Kraft- und Arbeitsmaschinen Klausur zur Diplom-Hauptprüfung, 26. Juli 2006
 Kraft- und Arbeitsmaschinen Klausur zur Diplom-Hauptprüfung, 26. Juli 2006 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten; Die Foliensammlung, Ihre Mitschrift der Vorlesung
Kraft- und Arbeitsmaschinen Klausur zur Diplom-Hauptprüfung, 26. Juli 2006 Bearbeitungszeit: 120 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten; Die Foliensammlung, Ihre Mitschrift der Vorlesung
HP 2003/04-3: Blockschaltbild eines Dampfkraftwerks:
 HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: Teilaufgaben: 1 Welche Energieformen werden den Bauteilen Dampferzeuger, Turbine, Generator und Verbraucher
HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: HP 003/04-3: Blockschaltbild eines Dampfkraftwerks: Teilaufgaben: 1 Welche Energieformen werden den Bauteilen Dampferzeuger, Turbine, Generator und Verbraucher
Energie- und Kältetechnik Klausur WS 2008/2009
 Aufgabenteil / 00 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
Aufgabenteil / 00 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
Klausur Thermische Kraftwerke (Energieanlagentechnik I)
 Klausur Thermische Kraftwerke (Energieanlagentechnik I) Datum: 09.03.2009 Dauer: 1,5 Std. Der Gebrauch von nicht-programmierbaren Taschenrechnern und schriftlichen Unterlagen ist erlaubt. Aufgabe 1 2 3
Klausur Thermische Kraftwerke (Energieanlagentechnik I) Datum: 09.03.2009 Dauer: 1,5 Std. Der Gebrauch von nicht-programmierbaren Taschenrechnern und schriftlichen Unterlagen ist erlaubt. Aufgabe 1 2 3
Übungssunterlagen. Energiesysteme I. Prof. Dr.-Ing. Bernd Epple
 Übungssunterlagen Energiesysteme I Prof. Dr.-Ing. Bernd Epple 1 1. Allgemeine Informationen Zum Bearbeiten der Übungen können die Formelsammlungen aus den Fächern Technische Thermodynamik 1, Technische
Übungssunterlagen Energiesysteme I Prof. Dr.-Ing. Bernd Epple 1 1. Allgemeine Informationen Zum Bearbeiten der Übungen können die Formelsammlungen aus den Fächern Technische Thermodynamik 1, Technische
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 3. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 3 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3 Bilanzgleichungen 3.3.1 Massebilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 3 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3 Bilanzgleichungen 3.3.1 Massebilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Projekt Aufgabensammlung Thermodynamik
 Projekt Aufgabensammlung Thermodynamik Nr. Quelle Lösungssicherheit Lösung durch abgetippt durch 1 Klausur 1 (1) OK Navid Matthes 2 Probekl. WS06 (1) / Kl.SS04 (1) 100% Prof. Seidel. (Nav.) Matthes (Nav)
Projekt Aufgabensammlung Thermodynamik Nr. Quelle Lösungssicherheit Lösung durch abgetippt durch 1 Klausur 1 (1) OK Navid Matthes 2 Probekl. WS06 (1) / Kl.SS04 (1) 100% Prof. Seidel. (Nav.) Matthes (Nav)
Übung 3. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) Verständnis des thermodynamischen Gleichgewichts
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ein Braunkohle-Kraftwerk arbeitet nach dem Clausius-Rankine-Prozess mit einfacher Zwischenüberhitzung
 Klausuraufgaben Thermodynamik (F 0 A) BRAUNKOHLE-KRAFTWERK Ein Braunkohle-Kraftwerk arbeitet nach dem Clausius-Rankine-Prozess mit einfacher Zwischenüberhitzung und Anzapf-Vorwärmung. Dabei wird der Wassermassenstrom
Klausuraufgaben Thermodynamik (F 0 A) BRAUNKOHLE-KRAFTWERK Ein Braunkohle-Kraftwerk arbeitet nach dem Clausius-Rankine-Prozess mit einfacher Zwischenüberhitzung und Anzapf-Vorwärmung. Dabei wird der Wassermassenstrom
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Professor Dr. Dr.-Ing. habil. H. Müller-Steinhagen. Praktikum
 UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Professor Dr. Dr.-Ing. habil. H. Müller-Steinhagen Praktikum Bestimmung der Leistungszahl einer elektrisch angetriebenen Wasser / Wasser-Wärmepumpe
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Professor Dr. Dr.-Ing. habil. H. Müller-Steinhagen Praktikum Bestimmung der Leistungszahl einer elektrisch angetriebenen Wasser / Wasser-Wärmepumpe
Stellen Sie für die folgenden Reaktionen die Gleichgewichtskonstante K p auf: 1/2O 2 + 1/2H 2 OH H 2 + 1/2O 2 H 2 O
 Klausur H2004 (Grundlagen der motorischen Verbrennung) 2 Aufgabe 1.) Stellen Sie für die folgenden Reaktionen die Gleichgewichtskonstante K p auf: 1/2O 2 + 1/2H 2 OH H 2 + 1/2O 2 H 2 O Wie wirkt sich eine
Klausur H2004 (Grundlagen der motorischen Verbrennung) 2 Aufgabe 1.) Stellen Sie für die folgenden Reaktionen die Gleichgewichtskonstante K p auf: 1/2O 2 + 1/2H 2 OH H 2 + 1/2O 2 H 2 O Wie wirkt sich eine
Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol
![Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol](/thumbs/50/26795947.jpg) 2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
Aufgabe 1 : (10 + 6 + 4 = 20 Punkte)
 Aufgabe 1 : (10 + 6 + 4 = 20 Punkte) Wirtschaftlichkeitsbetrachtung Als Jungingenieur arbeiten Sie in einer mittleren Firma an der Auslegung eines neuen Produktionsprozesses. Bei der Planung haben Sie
Aufgabe 1 : (10 + 6 + 4 = 20 Punkte) Wirtschaftlichkeitsbetrachtung Als Jungingenieur arbeiten Sie in einer mittleren Firma an der Auslegung eines neuen Produktionsprozesses. Bei der Planung haben Sie
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spindler
 UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spindler Prüfung "Technische Thermodynamik 1+2" 18. August 2014 Zeit: 180 min. zugelassen: für Aufgabe 1-4 Taschenrechner
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spindler Prüfung "Technische Thermodynamik 1+2" 18. August 2014 Zeit: 180 min. zugelassen: für Aufgabe 1-4 Taschenrechner
Übungsaufgaben zur Thermodynamik
 Übungsaufgaben zur Thermodynamik Übungsbeispiel 1 Ein ideales Gas hat bei einem Druck von 2,5 bar und ϑl = 27 C eine Dichte von ρ1 = 2,7 kg/m 3. Durch isobare Wärmezufuhr soll sich das Gasvolumen Vl verdoppeln
Übungsaufgaben zur Thermodynamik Übungsbeispiel 1 Ein ideales Gas hat bei einem Druck von 2,5 bar und ϑl = 27 C eine Dichte von ρ1 = 2,7 kg/m 3. Durch isobare Wärmezufuhr soll sich das Gasvolumen Vl verdoppeln
Klausur im Fach Thermodynamik I, SS 2012 am 06.08.2012
 e r e n e g y e n g i n e e r i n g..t c o n o m i c s. e n v i e n r o n m Technische Universität Berlin INSTITUT FÜR ENERGIETECHNIK Prof. Dr.-Ing. G. Tsatsaronis. Klausur im Fach Thermodynamik I, SS
e r e n e g y e n g i n e e r i n g..t c o n o m i c s. e n v i e n r o n m Technische Universität Berlin INSTITUT FÜR ENERGIETECHNIK Prof. Dr.-Ing. G. Tsatsaronis. Klausur im Fach Thermodynamik I, SS
Institut für Energiesysteme und Energietechnik. Vorlesungsübung 1. Musterlösung
 Institut für Energiesysteme und Energietechnik Vorlesungsübung 1 Musterlösung 3.1 Kohlekraftwerk Aufgabe 1 Gesucht: Aufgrund der Vernachlässigung des Temperaturunterschiedes des Luft-, Rauchgas- und Brennstoffstromes
Institut für Energiesysteme und Energietechnik Vorlesungsübung 1 Musterlösung 3.1 Kohlekraftwerk Aufgabe 1 Gesucht: Aufgrund der Vernachlässigung des Temperaturunterschiedes des Luft-, Rauchgas- und Brennstoffstromes
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
wegen Massenerhaltung
 3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
Technische Thermodynamik. FB Maschinenwesen. Übungsaufgaben Kälte- und Wärmepumpentechnik. University of Applied Sciences
 University of Applied Sciences Übungsaufgaben Kälte- und Wärmepumpentechnik Prof. Dr.-Ing. habil. H.-J. Kretzschmar FB Maschinenwesen Technische Thermodynamik 1 2 1 Kompressionskältemaschinen und -wärmepumpen
University of Applied Sciences Übungsaufgaben Kälte- und Wärmepumpentechnik Prof. Dr.-Ing. habil. H.-J. Kretzschmar FB Maschinenwesen Technische Thermodynamik 1 2 1 Kompressionskältemaschinen und -wärmepumpen
Verbrennungstechnik. 1. Brennstoffe. 1.Brennstoffe. 2.Heizwert. 2.1 Oberer Heizwert 2.2 Unterer Heizwert. 3.Verbrennungsvorgang
 Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
Stickstoff kann als ideales Gas betrachtet werden mit einer spezifischen Gaskonstante von R N2 = 0,297 kj
 Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Klausur zur Vorlesung. Thermodynamik
 Institut für Thermodynamik 25. August 2010 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Institut für Thermodynamik 25. August 2010 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw. Gedankengang muss stets
Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K
![Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K Fundamentalgleichung für die Entropie. spezifische Entropie: s = S/m molare Entropie: s m = S/n. Entropie S [S] = J/K](/thumbs/26/9282771.jpg) Fundamentalgleichung für die Entropie Entropie S [S] = J/K spezifische Entropie: s = S/m molare Entropie: s m = S/n Mit dem 1. Hauptsatz für einen reversiblen Prozess und der Definition für die Entropie
Fundamentalgleichung für die Entropie Entropie S [S] = J/K spezifische Entropie: s = S/m molare Entropie: s m = S/n Mit dem 1. Hauptsatz für einen reversiblen Prozess und der Definition für die Entropie
Fachrichtung Klima- und Kälteanlagenbauer
 Fachrichtung Klima- und Kälteanlagenbauer 1-7 Schüler Datum: 1. Titel der L.E. : 2. Fach / Klasse : Fachrechnen, 3. Ausbildungsjahr 3. Themen der Unterrichtsabschnitte : 1. Zustandsänderung 2. Schmelzen
Fachrichtung Klima- und Kälteanlagenbauer 1-7 Schüler Datum: 1. Titel der L.E. : 2. Fach / Klasse : Fachrechnen, 3. Ausbildungsjahr 3. Themen der Unterrichtsabschnitte : 1. Zustandsänderung 2. Schmelzen
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Thermodynamik. Eine Einführung in die Grundlagen. Von. Dr.-Ing. Hans Dieter Baehr. o. Professor an der Technischen Hochschule Braunschweig
 Thermodynamik Eine Einführung in die Grundlagen und ihre technischen Anwendungen Von Dr.-Ing. Hans Dieter Baehr o. Professor an der Technischen Hochschule Braunschweig Mit 325 Abbildungen und zahlreichen
Thermodynamik Eine Einführung in die Grundlagen und ihre technischen Anwendungen Von Dr.-Ing. Hans Dieter Baehr o. Professor an der Technischen Hochschule Braunschweig Mit 325 Abbildungen und zahlreichen
KLAUSUR HEIZTECHNIK II SS Name: Vorname: Gesamtpunktzahl: Aufgabe 25 Punkte
 Fachhochschule Gießen-Friedberg Prof. Dr.-Ing. Boris Kruppa KLAUSUR HEIZTECHNIK II SS 2010 Fachbereich MMEW Montag, 12. Juli 2010 Name: Vorname: Gesamtpunktzahl: 110 Matrikelnummer: Erreichte Punktzahl:
Fachhochschule Gießen-Friedberg Prof. Dr.-Ing. Boris Kruppa KLAUSUR HEIZTECHNIK II SS 2010 Fachbereich MMEW Montag, 12. Juli 2010 Name: Vorname: Gesamtpunktzahl: 110 Matrikelnummer: Erreichte Punktzahl:
NH3 Kälteanlage PFA/ Inhalt
 Anlagenkonzept PFA NH3 Kälteanlage PFA/ Inhalt - Walter Wettstein AG - Kältekreisläufe von Kunsteisbahnen - Abwärmenutzung von Kunsteisbahnen - Anlagenkonzept PFA - Meilensteine im Projekt - Erfahrungen
Anlagenkonzept PFA NH3 Kälteanlage PFA/ Inhalt - Walter Wettstein AG - Kältekreisläufe von Kunsteisbahnen - Abwärmenutzung von Kunsteisbahnen - Anlagenkonzept PFA - Meilensteine im Projekt - Erfahrungen
Übungen. Vorlesung. Energietechnik
 Fachhochschule Münster Fachbereich Maschinenbau Motoren- und Energietechnik-Labor Prof. Dr. R. Ullrich Übungen zur Vorlesung Energietechnik Version 1/99 - 2 - Übung 1 1.) Die wirtschaftlich gewinnbaren
Fachhochschule Münster Fachbereich Maschinenbau Motoren- und Energietechnik-Labor Prof. Dr. R. Ullrich Übungen zur Vorlesung Energietechnik Version 1/99 - 2 - Übung 1 1.) Die wirtschaftlich gewinnbaren
Lösungen zu den Zusatzübungen zur Physik für Ingenieure (Maschinenbau) (WS 13/14)
 Lösungen zu den Zusatzübungen zur hysik für Ingenieure (Maschinenbau) (WS 13/14) rof. W. Meyer Übungsgruppenleiter: A. Berlin & J. Herick (NB 2/28) Zusatzübung (Lösung) alle Angaben ohne Gewähr Zusatzaufgabe
Lösungen zu den Zusatzübungen zur hysik für Ingenieure (Maschinenbau) (WS 13/14) rof. W. Meyer Übungsgruppenleiter: A. Berlin & J. Herick (NB 2/28) Zusatzübung (Lösung) alle Angaben ohne Gewähr Zusatzaufgabe
Grundlagen der Wärmelehre
 Ausgabe 2007-09 Grundlagen der Wärmelehre (Erläuterungen) Die Wärmelehre ist das Teilgebiet der Physik, in dem Zustandsänderungen von Körpern infolge Zufuhr oder Abgabe von Wärmeenergie und in dem Energieumwandlungen,
Ausgabe 2007-09 Grundlagen der Wärmelehre (Erläuterungen) Die Wärmelehre ist das Teilgebiet der Physik, in dem Zustandsänderungen von Körpern infolge Zufuhr oder Abgabe von Wärmeenergie und in dem Energieumwandlungen,
7.2 Energiebilanz bei chemischen Stoffumwandlungen
 7.2 Energiebilanz bei chemischen Stoffumwandlungen Betrachtung eines Reaktionsgefäßes mit eintretenden Edukten und austretenden Produkten am Beispiel der Verbrennung eines Brennstoffes mit Luft (kinetische
7.2 Energiebilanz bei chemischen Stoffumwandlungen Betrachtung eines Reaktionsgefäßes mit eintretenden Edukten und austretenden Produkten am Beispiel der Verbrennung eines Brennstoffes mit Luft (kinetische
Klausur Strömungsmechanik 1 WS 2009/2010
 Klausur Strömungsmechanik 1 WS 2009/2010 03. März 2010, Beginn 15:00 Uhr Prüfungszeit: 90 Minuten Zugelassene Hilfsmittel sind: Taschenrechner (nicht programmierbar) TFD-Formelsammlung (ohne handschriftliche
Klausur Strömungsmechanik 1 WS 2009/2010 03. März 2010, Beginn 15:00 Uhr Prüfungszeit: 90 Minuten Zugelassene Hilfsmittel sind: Taschenrechner (nicht programmierbar) TFD-Formelsammlung (ohne handschriftliche
Klausur Wärmelehre E2/E2p, SoSe 2012 Braun. Formelsammlung Thermodynamik
 Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Dampfkraftprozess Dampfturbine
 Fachgebiet für Energiesysteme und Energietechnik Prof. Dr.-Ing. B. Epple Musterlösung Übung Energie und Klimaschutz Sommersemester 0 Dampfkraftprozess Dampfturbine Aufgabe : Stellen Sie den Dampfkraftprozess
Fachgebiet für Energiesysteme und Energietechnik Prof. Dr.-Ing. B. Epple Musterlösung Übung Energie und Klimaschutz Sommersemester 0 Dampfkraftprozess Dampfturbine Aufgabe : Stellen Sie den Dampfkraftprozess
Übungen zur Thermodynamik (PBT) WS 2004/05
 1. Übungsblatt 1. Berechnen Sie ausgehend von der allgemeinen Gasgleichung pv = nrt das totale Differential dv. Welche Änderung ergibt sich hieraus in erster Näherung für das Volumen von einem Mol eines
1. Übungsblatt 1. Berechnen Sie ausgehend von der allgemeinen Gasgleichung pv = nrt das totale Differential dv. Welche Änderung ergibt sich hieraus in erster Näherung für das Volumen von einem Mol eines
Schriftliche Prüfung aus VO Kraftwerke am Name/Vorname: / Matr.-Nr./Knz.: / V1 = 2,7 Liter
 Schriftliche Prüfung aus VO Kraftwerke am 10.11.2015 Name/Vorname: / Matr.-Nr./Knz.: / 1. Stirlingmotor (25 Punkte) Ein Stirlingmotor soll zur Stromerzeugung in einem 50 Hz Netz eingesetzt werden. Es wird
Schriftliche Prüfung aus VO Kraftwerke am 10.11.2015 Name/Vorname: / Matr.-Nr./Knz.: / 1. Stirlingmotor (25 Punkte) Ein Stirlingmotor soll zur Stromerzeugung in einem 50 Hz Netz eingesetzt werden. Es wird
4 Kältesysteme. Mehr Informationen zum Titel. 4.1 Direkte Kühlung
 Mehr Informationen zum Titel 4 Kältesysteme 4.1 Direkte Kühlung Unter direkter Kühlung bzw. direkter Verdampfung versteht man die Heranführung des Kältemittels an das zu kühlende Medium (Flüssigkeit, Gase,
Mehr Informationen zum Titel 4 Kältesysteme 4.1 Direkte Kühlung Unter direkter Kühlung bzw. direkter Verdampfung versteht man die Heranführung des Kältemittels an das zu kühlende Medium (Flüssigkeit, Gase,
FI 1 Messblende Gesamtluft FI 2 Messblende Abluft
 Trocknung Labor für Thermische Verfahrenstechnik bearbeitet von Prof. Dr.-Ing. habil. R. Geike 1. Beschreibung der Anlage und der Versuchsdurchführung Bei diesem Versuch handelt es sich um die Trocknung
Trocknung Labor für Thermische Verfahrenstechnik bearbeitet von Prof. Dr.-Ing. habil. R. Geike 1. Beschreibung der Anlage und der Versuchsdurchführung Bei diesem Versuch handelt es sich um die Trocknung
5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme
 5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme Für isotherme reversible Prozesse gilt und daher Dies
5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel-isotherme Arbeitsprozesse Energiebilanz für geschlossene Systeme Für isotherme reversible Prozesse gilt und daher Dies
Thermodynamik II. Themenbereich: Gemische idealer Gase
 Thermodynamik II Themenbereich: Gemische idealer Gase Übungsbeispiel l Ein Gasgemisch hat folgende Zusammensetzung in Raumanteilen (Volumenanteilen) bei einem Gesamtdruck p = 1010 mbar und 0 C: O 2 0,21
Thermodynamik II Themenbereich: Gemische idealer Gase Übungsbeispiel l Ein Gasgemisch hat folgende Zusammensetzung in Raumanteilen (Volumenanteilen) bei einem Gesamtdruck p = 1010 mbar und 0 C: O 2 0,21
Allgemeine Chemie. SS 2014 Thomas Loerting. Thomas Loerting Allgemeine Chemie
 Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Aufgaben zum Stirlingschen Kreisprozess Ein Stirling-Motor arbeite mit 50 g Luft ( M= 30g mol 1 )zwischen den Temperaturen = 350 C und T3
 Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Praktikum Physik. Protokoll zum Versuch 5: Spezifische Wärme. Durchgeführt am Gruppe X
 Praktikum Physik Protokoll zum Versuch 5: Spezifische Wärme Durchgeführt am 10.11.2011 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
Praktikum Physik Protokoll zum Versuch 5: Spezifische Wärme Durchgeführt am 10.11.2011 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
Kleine Formelsammlung Technische Thermodynamik
 Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
Mensch und Technik. Berechnungen und Beispiele
 1 Berechnungen und Beispiele Wärmekapazität Wird einem Stoff durch Erwärmen Energie zugeführt, so steigt deren Temperatur, dies ist stoffabhängig und der Temperaturanstieg ist proportional zur Wärmemenge:
1 Berechnungen und Beispiele Wärmekapazität Wird einem Stoff durch Erwärmen Energie zugeführt, so steigt deren Temperatur, dies ist stoffabhängig und der Temperaturanstieg ist proportional zur Wärmemenge:
Übungen zur Vorlesung. Energiesysteme
 Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
Willkommen. welcome. bienvenu. Raumlufttechnik hx-diagramm Energierückgewinnung und Energieeffizienztechnologien
 Willkommen bienvenu welcome Raumlufttechnik hx-diagramm Energierückgewinnung und Energieeffizienztechnologien in der Lüftungstechnik Dipl.-Ing. Christian Backes backes@howatherm.de Dr.-Ing. Christoph Kaup
Willkommen bienvenu welcome Raumlufttechnik hx-diagramm Energierückgewinnung und Energieeffizienztechnologien in der Lüftungstechnik Dipl.-Ing. Christian Backes backes@howatherm.de Dr.-Ing. Christoph Kaup
Hilfe. Wasserdampftafel und Prozesse Excel Makros. Version 1.19-10/2007. Josef BERTSCH Gesellschaft m.b.h & Co
 Wasserdampftafel und Prozesse Excel Makros Hilfe Version 1.19-10/2007 Josef BERTSCH Gesellschaft m.b.h & Co Kessel und Energietechnik Apparatebau Nahrungsmittelanlagen Zentrale: A-6700 Bludenz, Herrengasse
Wasserdampftafel und Prozesse Excel Makros Hilfe Version 1.19-10/2007 Josef BERTSCH Gesellschaft m.b.h & Co Kessel und Energietechnik Apparatebau Nahrungsmittelanlagen Zentrale: A-6700 Bludenz, Herrengasse
SORTEN VON DAMPF / DAMPF UND DRUCK / VAKUUM
 SORTEN VON DAMPF / DAMPF UND DRUCK / VAKUUM In diesem Kapitel werden kurz einige wichtige Begriffe definiert. Ebenso wird das Beheizen von Anlagen mit Dampf im Vakuumbereich beschrieben. Im Sprachgebrauch
SORTEN VON DAMPF / DAMPF UND DRUCK / VAKUUM In diesem Kapitel werden kurz einige wichtige Begriffe definiert. Ebenso wird das Beheizen von Anlagen mit Dampf im Vakuumbereich beschrieben. Im Sprachgebrauch
Thermodynamik I - Übung 1. Nicolas Lanzetti
 Thermodynamik I - Übung 1 Nicolas Lanzetti Nicolas Lanzetti 02.10.2015 1 Hinweise zu der Übung Name: Nicolas Lanzetti; 5. Semester Maschinenbau; Mail: Raum: CHN C14; Zeit: Freitag, 8:15-10:00; Alle Unterlagen:
Thermodynamik I - Übung 1 Nicolas Lanzetti Nicolas Lanzetti 02.10.2015 1 Hinweise zu der Übung Name: Nicolas Lanzetti; 5. Semester Maschinenbau; Mail: Raum: CHN C14; Zeit: Freitag, 8:15-10:00; Alle Unterlagen:
Literatur. [1] Cerbe, G. / Hoffmann, H.-J. Einführung in die Thermodynamik Carl Hanser Verlag 2002 Preis ca. 29,90
![Literatur. [1] Cerbe, G. / Hoffmann, H.-J. Einführung in die Thermodynamik Carl Hanser Verlag 2002 Preis ca. 29,90 Literatur. [1] Cerbe, G. / Hoffmann, H.-J. Einführung in die Thermodynamik Carl Hanser Verlag 2002 Preis ca. 29,90](/thumbs/39/18694191.jpg) Literatur [1] Cerbe, G. / Hoffmann, H.-J. Einführung in die Thermodynamik Carl Hanser Verlag 2002 Preis ca. 29,90 [2] Grigull, U. (Hrsg.) Wasserdampftafeln Springer Verlag 1990 [3] Merker, G.P. / Stiesch,
Literatur [1] Cerbe, G. / Hoffmann, H.-J. Einführung in die Thermodynamik Carl Hanser Verlag 2002 Preis ca. 29,90 [2] Grigull, U. (Hrsg.) Wasserdampftafeln Springer Verlag 1990 [3] Merker, G.P. / Stiesch,
Thermodynamik Formelsammlung
 RH-öln Thermoynamik ormelsammlung 2006 Thermoynamik ormelsammlung - I 1 Grunlagen Boltzmannkonstante: 1.3 Größen un Einheitensysteme Umrechnung ahrenheit nach Celsius: Umrechnung Celsius nach elvin: abgeschlossenes
RH-öln Thermoynamik ormelsammlung 2006 Thermoynamik ormelsammlung - I 1 Grunlagen Boltzmannkonstante: 1.3 Größen un Einheitensysteme Umrechnung ahrenheit nach Celsius: Umrechnung Celsius nach elvin: abgeschlossenes
J und κ =1, 4 behandelt werden. kg K. a) Berechnen Sie die fehlenden Temperaturen und Drücke!
 Übung 11 Aufgabe 7.6: Offene Gaturbine Eine Gaturbinenanlage untercheidet ich vom reveriblen oule-proze dadurch, da der Verdichter und die Turbine nicht ientrop arbeiten. E gilt vielmehr: η S,V =0, 85
Übung 11 Aufgabe 7.6: Offene Gaturbine Eine Gaturbinenanlage untercheidet ich vom reveriblen oule-proze dadurch, da der Verdichter und die Turbine nicht ientrop arbeiten. E gilt vielmehr: η S,V =0, 85
Energietechnik SS 2005
 Energietechnik SS 2005 Prof. Dr.-Ing. G. Wilhelms Das ideale Gas in Maschinen und Anlagen (I) Das ideale Gas in Gasturbinen (IG) IG 1 - Joule-Prozess IG 2 - Ericcson-Prozess IG 3 - andere Vergleichsprozesse
Energietechnik SS 2005 Prof. Dr.-Ing. G. Wilhelms Das ideale Gas in Maschinen und Anlagen (I) Das ideale Gas in Gasturbinen (IG) IG 1 - Joule-Prozess IG 2 - Ericcson-Prozess IG 3 - andere Vergleichsprozesse
( ) 3 = Grösse = Zahlenwert Einheit. Inhalte gemäss Rahmenlehrplan 2012 GESO. Geltende Ziffern
 GEWERBLICH-INDUSTRIELLE BERUFSSCHULE BERN BERUFSMATURITÄTSSCHULE BMS Gesundheit und Soziales GESO Formelsammlung Physik David Kamber, Ruben Mäder Stand 7.5.016 Inhalte gemäss Rahmenlehrplan 01 GESO Mechanik:
GEWERBLICH-INDUSTRIELLE BERUFSSCHULE BERN BERUFSMATURITÄTSSCHULE BMS Gesundheit und Soziales GESO Formelsammlung Physik David Kamber, Ruben Mäder Stand 7.5.016 Inhalte gemäss Rahmenlehrplan 01 GESO Mechanik:
kg K dp p = R LuftT 1 ln p 2a =T 2a Q 12a = ṁq 12a = 45, 68 kw = 288, 15 K 12 0,4 Q 12b =0. Technische Arbeit nach dem Ersten Hauptsatz:
 Übung 9 Aufgabe 5.12: Kompression von Luft Durch einen Kolbenkompressor sollen ṁ = 800 kg Druckluft von p h 2 =12bar zur Verfügung gestellt werden. Der Zustand der angesaugten Außenluft beträgt p 1 =1,
Übung 9 Aufgabe 5.12: Kompression von Luft Durch einen Kolbenkompressor sollen ṁ = 800 kg Druckluft von p h 2 =12bar zur Verfügung gestellt werden. Der Zustand der angesaugten Außenluft beträgt p 1 =1,
Moorburg und Fernwärme Klimaschutz mit Kohle?
 HINTERGRUNDPAPIER Landesverband Hamburg Landesarbeitsgemeinschaft Energie Jörg Behrschmidt (Sprecher) joerg.behrschmidt@hamburg.gruene.de Christoph Schreiber (Sprecher) christoph.schreiber@hamburg.gruene.de
HINTERGRUNDPAPIER Landesverband Hamburg Landesarbeitsgemeinschaft Energie Jörg Behrschmidt (Sprecher) joerg.behrschmidt@hamburg.gruene.de Christoph Schreiber (Sprecher) christoph.schreiber@hamburg.gruene.de
Klausur zur Vorlesung. Thermodynamik
 Institut für Thermodynamik 2. März 2009 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw Gedankengang muss erkennbar
Institut für Thermodynamik 2. März 2009 Technische Universität Braunschweig Prof. Dr. Jürgen Köhler Klausur zur Vorlesung Thermodynamik Für alle Aufgaben gilt: Der Rechen- bzw Gedankengang muss erkennbar
ENTLÜFTEN UND ENTGASEN
 ENTLÜFTEN UND ENTGASEN Luft ist ein sehr schlechter Wärmeleiter. Gerade bei Wärmetauschern müssen deshalb die Rohrleitungen an der höchsten Stelle der Anlage entlüftet werden. Bei sehr großen Dampfund
ENTLÜFTEN UND ENTGASEN Luft ist ein sehr schlechter Wärmeleiter. Gerade bei Wärmetauschern müssen deshalb die Rohrleitungen an der höchsten Stelle der Anlage entlüftet werden. Bei sehr großen Dampfund
Institut für Thermodynamik Prof. Dr. rer. nat. M. Pfitzner Thermodynamik I - Lösung 1. Einleitende Fragen
 Einleitende Fragen 1. Was versteht man unter Thermodynamik? Thermodynamik ist die Lehre von den Energieumwandlungen und den Zusammenhängen zwischen den Eigenschaften der Stoffe. 2. Erklären Sie folgende
Einleitende Fragen 1. Was versteht man unter Thermodynamik? Thermodynamik ist die Lehre von den Energieumwandlungen und den Zusammenhängen zwischen den Eigenschaften der Stoffe. 2. Erklären Sie folgende
Mitsubishi Electric Europe B.V. Air Conditioning Division Gothaer Str Ratingen. Art.-Nr /2007
 Mitsubishi Electric Europe B.V. Air Conditioning Division Gothaer Str. 8 40880 Ratingen Klima-Abc Art.-Nr. 207223-2 10/2007 in 7 Minuten KLIMAEXPERTE Kältemittel- Kreislauf COP/EER C 1 2 3 Ein wichtiges
Mitsubishi Electric Europe B.V. Air Conditioning Division Gothaer Str. 8 40880 Ratingen Klima-Abc Art.-Nr. 207223-2 10/2007 in 7 Minuten KLIMAEXPERTE Kältemittel- Kreislauf COP/EER C 1 2 3 Ein wichtiges
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seminar Thermische Abfallbehandlung - Veranstaltung 4 - Dampfkraftprozesse
 Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
KLAUSUR HEIZTECHNIK II SS Name: Vorname: Gesamtpunktzahl: Aufgabe 50 Punkte. 2 m. 5 m
 Fachhochschule Gießen-Friedberg Prof. Dr.-Ing. Boris Kruppa KLAUSUR HEIZTECHNIK II SS 2009 Fachbereich MMEW Mittwoch, 08. Juli 2009 Name: Vorname: Gesamtpunktzahl: 120 Matrikelnummer: Erreichte Punktzahl:
Fachhochschule Gießen-Friedberg Prof. Dr.-Ing. Boris Kruppa KLAUSUR HEIZTECHNIK II SS 2009 Fachbereich MMEW Mittwoch, 08. Juli 2009 Name: Vorname: Gesamtpunktzahl: 120 Matrikelnummer: Erreichte Punktzahl:
Inhaltsverzeichnis. Hans-Joachim Kretzschmar, Ingo Kraft. Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6
 Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
Berechnung von ORC-Prozessen mit Kältemitteln
 Hochschule für Angewandte Wissenschaften Hamburg Hamburg University of Applied Sciences Berechnung von ORC-Prozessen mit Kältemitteln Diplomarbeit Christoph Wiesner Matr.-Nr.: 1858108 1. Betreuer: Prof.
Hochschule für Angewandte Wissenschaften Hamburg Hamburg University of Applied Sciences Berechnung von ORC-Prozessen mit Kältemitteln Diplomarbeit Christoph Wiesner Matr.-Nr.: 1858108 1. Betreuer: Prof.
Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der Pkw- Klimatisierung
 Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der Pkw- Klimatisierung Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der
Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der Pkw- Klimatisierung Fehlermöglichkeiten bei der Auswertung thermodynamischer Messungen an Wärmeaustauschern der
Maßeinheiten der Wärmelehre
 Maßeinheiten der Wärmelehre Temperatur (thermodynamisch) Benennung der Einheit: Einheitenzeichen: T für Temp.-punkte, ΔT für Temp.-differenzen Kelvin K 1 K ist der 273,16te Teil der (thermodynamischen)
Maßeinheiten der Wärmelehre Temperatur (thermodynamisch) Benennung der Einheit: Einheitenzeichen: T für Temp.-punkte, ΔT für Temp.-differenzen Kelvin K 1 K ist der 273,16te Teil der (thermodynamischen)
Das h,x-diagramm Aufbau und Anwendung
 Das h,x-diagramm Aufbau und Anwendung Building Technologies s Inhaltsverzeichnis 1.Thermodynamische Grundlagen 2. Der Aufbau des h,x-diagramms 3. Die Anwendung des h,x-diagramms 4. Berechnungsgrundlagen
Das h,x-diagramm Aufbau und Anwendung Building Technologies s Inhaltsverzeichnis 1.Thermodynamische Grundlagen 2. Der Aufbau des h,x-diagramms 3. Die Anwendung des h,x-diagramms 4. Berechnungsgrundlagen
Bild 1: Siedeverhalten im beheizten Rohr (Nach VDI- Wärmeatlas, hier liegend gezeichnet)
 erdampfung Labor für Thermische erfahrenstechnik bearbeitet von Prof. r.-ing. habil. R. Geike. Grundlagen der erdampfung In der chemischen, pharmazeutischen und Lebensmittelindustrie sowie in weiteren
erdampfung Labor für Thermische erfahrenstechnik bearbeitet von Prof. r.-ing. habil. R. Geike. Grundlagen der erdampfung In der chemischen, pharmazeutischen und Lebensmittelindustrie sowie in weiteren
Technische Universität Kaiserslautern Lehrstuhl Entwurf Mikroelektronischer Systeme Prof. Dr.-Ing. N. Wehn. Probeklausur
 Technische Universität Kaiserslautern Lehrstuhl Entwurf Mikroelektronischer Systeme Prof. Dr.-Ing. N. Wehn 22.02.200 Probeklausur Elektrotechnik I für Maschinenbauer Name: Vorname: Matr.-Nr.: Fachrichtung:
Technische Universität Kaiserslautern Lehrstuhl Entwurf Mikroelektronischer Systeme Prof. Dr.-Ing. N. Wehn 22.02.200 Probeklausur Elektrotechnik I für Maschinenbauer Name: Vorname: Matr.-Nr.: Fachrichtung:
T1 Molare Masse nach Viktor Meyer Protokoll
 Christian Müller Jan Philipp Dietrich Inhalt: a) Versuchserläuterung b) Messwerte c) Berechnung der Molaren Masse d) Berechnung der Dampfdichte e) Fehlerberechnung T1 Molare Masse nach Viktor Meyer Protokoll
Christian Müller Jan Philipp Dietrich Inhalt: a) Versuchserläuterung b) Messwerte c) Berechnung der Molaren Masse d) Berechnung der Dampfdichte e) Fehlerberechnung T1 Molare Masse nach Viktor Meyer Protokoll
Im Mittel ist die Teilchenenergie im Dampf um die Verdampfungsenergie E V höher als in der Flüssigkeit. Auch hier gilt das BOLTZMANN-Theorem:!
 3. Aggregatzustände 3.1. Flüssigkeit und Dampf Wir betrachten Flüssigkeit + angrenzendes Volumen : Die Flüssigkeitsteilchen besitzen eine gewisse Verteilung der kinetischen Energie Es kommt vor, dass ein
3. Aggregatzustände 3.1. Flüssigkeit und Dampf Wir betrachten Flüssigkeit + angrenzendes Volumen : Die Flüssigkeitsteilchen besitzen eine gewisse Verteilung der kinetischen Energie Es kommt vor, dass ein
Wärmepumpe DT400-1P. NTL-Schriftenreihe Versuchsanleitung - Wärmepumpe
 Wärmepumpe DT400-1P NTL-Schriftenreihe Versuchsanleitung - Wärmepumpe Wärmepumpe Allgemein Eine Wärmepumpe ist eine Wärmekraftmaschine. Sie hebt Wärme von einem Körper tieferer Temperatur T 1 auf einen
Wärmepumpe DT400-1P NTL-Schriftenreihe Versuchsanleitung - Wärmepumpe Wärmepumpe Allgemein Eine Wärmepumpe ist eine Wärmekraftmaschine. Sie hebt Wärme von einem Körper tieferer Temperatur T 1 auf einen
T R O C K N U N G. Versuch 2.7. Trocknung
 Versuch 2.7. Trocknung 2.7. Trocknung von Feststoffen 2.7.0. Verzeichnis der verwendeten Symbole X X Y ϕ m i Gutfeuchte, Beladung des Gutes mittlere Gutfeuchte absolute Luftfeuchte, Beladung der Luft relative
Versuch 2.7. Trocknung 2.7. Trocknung von Feststoffen 2.7.0. Verzeichnis der verwendeten Symbole X X Y ϕ m i Gutfeuchte, Beladung des Gutes mittlere Gutfeuchte absolute Luftfeuchte, Beladung der Luft relative
4 Phasendiagramme. Für den kritischen Punkt von Kohlendioxid werden 304,14 K und 7,375 MPa angegeben, für den Tripelpunkt 216,58 K und 518 kpa.
 ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Biophysikalische Chemie Prof. Dr. Walter Langel 4 Phasendiagramme 1 Skizzieren
ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Biophysikalische Chemie Prof. Dr. Walter Langel 4 Phasendiagramme 1 Skizzieren
wegen adiabater Kompression, d.h. kein Wärmeaustausch mit der Umgebung, gilt:
 Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Wärmepumpe mit Erdsonde 10 kw:
 Wärme aus dem Erdreich: Die Sole/Wasser-Wärmepumpe entzieht dem Erdboden Wärme mit Hilfe von Erdkollektoren oder Erdsonden und kann ganzjährig den gesamten Heizbetrieb mit Warmwasser übernehmen. Vor allem
Wärme aus dem Erdreich: Die Sole/Wasser-Wärmepumpe entzieht dem Erdboden Wärme mit Hilfe von Erdkollektoren oder Erdsonden und kann ganzjährig den gesamten Heizbetrieb mit Warmwasser übernehmen. Vor allem
Thermodynamik I. Sommersemester 2012 Kapitel 5, Teil 1. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 5, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 5, Teil 1: Übersicht 5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel isotherme
Thermodynamik I Sommersemester 2012 Kapitel 5, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 5, Teil 1: Übersicht 5. Energieumwandlungen als reversible und nichtreversible Prozesse 5.1 Reversibel isotherme
Thermodynamik. Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen.
 Thermodynamik Was ist das? Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen. Gesetze der Thermodynamik Erlauben die Voraussage, ob eine bestimmte
Thermodynamik Was ist das? Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen. Gesetze der Thermodynamik Erlauben die Voraussage, ob eine bestimmte
Ergänzung im Web www.thermodynamik-formelsammlung.de
 Ergänzung im Web www.thermodynamik-formelsammlung.de Kapitel 13 Ideale Gasgemische Anhang B Zustandsdiagramme B5 B6 lg p,h-diagramm für Propan h 1+x,x w -Diagramm für feuchte Luft (farbig) AnhangC Stoffwert-Bibliotheken
Ergänzung im Web www.thermodynamik-formelsammlung.de Kapitel 13 Ideale Gasgemische Anhang B Zustandsdiagramme B5 B6 lg p,h-diagramm für Propan h 1+x,x w -Diagramm für feuchte Luft (farbig) AnhangC Stoffwert-Bibliotheken
Isotherme 3. 4 Adiabate 2 T 1. Adiabate Isotherme T 2. Arbeit nach außen = eingeschlossene Kurve
 Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
1. Aufgabe (18,5 Punkte)
 TECHNISCHE UNIVERSITÄT MÜNCHEN LEHRSTUHL FÜR THERMODYNAMIK Prof. Dr.-Ing. T. Sattelmayer Prof. W. Polifke, Ph.D. Diplomvorprüfung Thermodynamik I Wintersemester 2008/2009 5. März 2009 Teil II: Wärmetransportphänomene
TECHNISCHE UNIVERSITÄT MÜNCHEN LEHRSTUHL FÜR THERMODYNAMIK Prof. Dr.-Ing. T. Sattelmayer Prof. W. Polifke, Ph.D. Diplomvorprüfung Thermodynamik I Wintersemester 2008/2009 5. März 2009 Teil II: Wärmetransportphänomene
Physikalisches Grundpraktikum Taupunktmessung. Taupunktmessung
 Aufgabenstellung: 1. Bestimmen Sie den Taupunkt. Berechnen Sie daraus die absolute und relative Luftfeuchtigkeit. 2. Schätzen Sie die Messunsicherheit ab! Stichworte zur Vorbereitung: Temperaturmessung,
Aufgabenstellung: 1. Bestimmen Sie den Taupunkt. Berechnen Sie daraus die absolute und relative Luftfeuchtigkeit. 2. Schätzen Sie die Messunsicherheit ab! Stichworte zur Vorbereitung: Temperaturmessung,
Selz & Cie GmbH, Fabrikstr. 15, D Heidelberg Tel. (+49) 06221/ Fax
 Kleine Einführung in Raumklimatechnik Der Mensch kann sich den wechselnden äußeren Luftzuständen anpassen (akklimatisieren). Dennoch gibt es einen deutlichen Bereich, den Behaglichkeitsbereich, innerhalb
Kleine Einführung in Raumklimatechnik Der Mensch kann sich den wechselnden äußeren Luftzuständen anpassen (akklimatisieren). Dennoch gibt es einen deutlichen Bereich, den Behaglichkeitsbereich, innerhalb
Was haben wir gelernt?
 Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Die Heizungsanlage eines Hauses wird auf Ölfeuerung umgestellt. Gleichzeitig wird mit dieser Anlage Warmwasser aufbereitet.
 Übungsaufgaben zur Wärmelehre mit Lösungen 1) Die Heizungsanlage eines Hauses wird auf Ölfeuerung umgestellt. Gleichzeitig wird mit dieser Anlage Warmwasser aufbereitet. Berechnen Sie die Wärme, die erforderlich
Übungsaufgaben zur Wärmelehre mit Lösungen 1) Die Heizungsanlage eines Hauses wird auf Ölfeuerung umgestellt. Gleichzeitig wird mit dieser Anlage Warmwasser aufbereitet. Berechnen Sie die Wärme, die erforderlich
Thermodynamik I. Sommersemester 2012 Kapitel 4, Teil 2. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 4, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 4, Teil 2: Übersicht 4 Zweiter Hauptsatz der Thermodynamik 4.5 Entropiebilanz 4.5.1 Allgemeine Entropiebilanz 4.5.2
Thermodynamik I Sommersemester 2012 Kapitel 4, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 4, Teil 2: Übersicht 4 Zweiter Hauptsatz der Thermodynamik 4.5 Entropiebilanz 4.5.1 Allgemeine Entropiebilanz 4.5.2
Wärmepumpe. Mag. Dipl.-Ing. Katharina Danzberger
 Mag. Dipl.-Ing. Katharina Danzberger 1. Zielsetzung Im Rahmen der Übung sollen die Wärmebilanz und die Leistungszahl bzw. der COP (Coefficient Of Performance) der installierten n bestimmt und diskutiert
Mag. Dipl.-Ing. Katharina Danzberger 1. Zielsetzung Im Rahmen der Übung sollen die Wärmebilanz und die Leistungszahl bzw. der COP (Coefficient Of Performance) der installierten n bestimmt und diskutiert
Betriebsfeld und Energiebilanz eines Ottomotors
 Fachbereich Maschinenbau Fachgebiet Kraft- u. Arbeitsmaschinen Fachgebietsleiter Prof. Dr.-Ing. B. Spessert März 2013 Praktikum Kraft- und Arbeitsmaschinen Versuch 1 Betriebsfeld und Energiebilanz eines
Fachbereich Maschinenbau Fachgebiet Kraft- u. Arbeitsmaschinen Fachgebietsleiter Prof. Dr.-Ing. B. Spessert März 2013 Praktikum Kraft- und Arbeitsmaschinen Versuch 1 Betriebsfeld und Energiebilanz eines
ST Der Stirling-Motor als Wärmekraftmaschine
 ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
Technische Thermodynamik. FB Maschinenwesen. Übungsaufgaben. Technische Thermodynamik. Wärmeübertragung. University of Applied Sciences
 University of Applied Sciences Übungsaufgaben Technische Thermodynamik Wärmeübertragung Prof. Dr.-Ing. habil. H.-J. Kretzschmar FB Maschinenwesen Technische Thermodynamik HOCHSCHULE ZITTAU/GÖRLITZ (FH)
University of Applied Sciences Übungsaufgaben Technische Thermodynamik Wärmeübertragung Prof. Dr.-Ing. habil. H.-J. Kretzschmar FB Maschinenwesen Technische Thermodynamik HOCHSCHULE ZITTAU/GÖRLITZ (FH)
Die Anwendung des h-x-diagramms
 Die Anwendung des h-x-diagramms 1. Mischen zweier Luftmengen 2 2. Lufterwlrmung 3 3.12EHUIOlFHQNOXQJ 3.2.1DVVNOXQJ 4. Luftbefeuchtung 5 4.1.Befeuchtung mit Wasser 4.2.=XVWDQGVlQGHUXQJLP['LDJUDPP 4.3.Befeuchtung
Die Anwendung des h-x-diagramms 1. Mischen zweier Luftmengen 2 2. Lufterwlrmung 3 3.12EHUIOlFHQNOXQJ 3.2.1DVVNOXQJ 4. Luftbefeuchtung 5 4.1.Befeuchtung mit Wasser 4.2.=XVWDQGVlQGHUXQJLP['LDJUDPP 4.3.Befeuchtung
Fachprüfung Bauphysik Herbst 2015 SS 15
 Prüfungstag: 26.08.2015 Prüfungsdauer: 60 Minuten Fachprüfung Bauphysik Herbst 2015 SS 15 Aufgabenteil Name, Vorname Matrikelnummer Herr / Frau Studiengang: Bauingenieurwesen (Bachelor) UTRM (Bachelor)
Prüfungstag: 26.08.2015 Prüfungsdauer: 60 Minuten Fachprüfung Bauphysik Herbst 2015 SS 15 Aufgabenteil Name, Vorname Matrikelnummer Herr / Frau Studiengang: Bauingenieurwesen (Bachelor) UTRM (Bachelor)
