Inspektion der Aufbereitung
|
|
|
- Nadine Böhler
- vor 6 Jahren
- Abrufe
Transkript
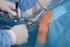
1 Medizinprodukte in Krankenhäusern Inspektion der Aufbereitung Ergebnisse der behördlichen Überprüfung von zentralen Sterilgutversorgungsabteilungen (ZSVA) Dr. Jürgen Barion, Arnsberg* Seit 2003 wird die Aufbereitung von Medizinprodukten in Nordrhein-Westfalen systematisch behördlich überprüft. Der Vergleich der Inspektionsergebnisse aus den Jahren 2004/2005 mit denen aus den Jahren 2008/2009 zeigt, dass sich die Bedingungen und Abläufe in den zentralen Sterilgutversorgungsabteilungen deutlich verbessert haben. die eine allgemeine übergeordnete Bedeutung haben. Folgende Punkte werden daher im Weiteren behandelt bzw. erörtert: Kritische Mängel Qualitätsmanagement Räumlichkeiten Qualifizierung/Validierung RDG* Personal * Reinigungs-/Desinfektions-Gerät In der Grafik sind die Ergebnisse prozentual dargestellt, da sich die Anzahl der ausgewerteten Inspektionsberichte bei den beiden Jahresgruppen unterscheidet (Abb. 1). Einleitung Die fünf Bezirksregierungen in Nordrhein-Westfalen sind die zuständigen Überwachungsbehörden nach 26 des Medizinproduktegesetzes (MPG). Hierbei werden Hersteller, Betreiber, Sonderanfertiger und Vertriebsunternehmen überprüft. Allein im Regierungsbezirk Arnsberg (ca. 3,8 Millionen Einwohner) handelt es sich dabei insgesamt um ca Institutionen und Einrichtungen. Im Rahmen der systematischen und risikoabgestuften Überwachung werden auch Einrichtungen inspiziert, die Medizinprodukte hygienisch aufbereiten. In den Fachkreisen ist seit Jahren bekannt, dass die Aufbereitung von Medizinprodukten in Deutschland teilweise nicht fachgerecht durchgeführt wird (1). Die Inspektion der Aufbereitung von Medizinprodukten hat im Regierungsbezirk Arnsberg in den vergangenen Jahren unter anderem dazu geführt, dass in einzelnen Einrichtungen die Aufbereitung von bestimmten Medizinprodukten untersagt wurde, dass Auflagen verfügt wurden z. B. im Zusammenhang mit der Qualifizierung der Gerätschaften, der Validierung von Verfahren, etc. oder dass die zentrale Sterilgutversorgungsabteilung geschlossen werden musste. Material und Methoden Ungefähr 65 Krankenhäuser im Regierungsbezirk Arnsberg haben eine ZSVA. Diese sind alle bis 2009 mindestens einmal überprüft worden. Die Anzahl der Mitarbeiter in den ZSVA lag zwischen 35 Personen und drei Mitarbeitern. Die Menge der aufbereiteten Medizinprodukte bewegte sich zwischen maximal StE bzw Siebchargen und mindestens 2000 StE bzw Siebchargen pro Jahr. Insgesamt sind 50 Inspektionsberichte ausgewertet worden, und zwar 30 aus den Jahren 2004/2005 und 20 aus den Jahren 2008/2009. Ziel der Auswertung war eine mögliche Trendermittlung und keine detaillierte statistische Analyse. Eine klare Einteilung aller Mängel in entsprechende Gruppen ist nicht eindeutig möglich. Z. B. kann die Ursache für eine nicht sachgerechte Vorreinigung in einer mangelhaften Ausbildung, nicht sachgerechter Dokumentation oder Archivierung von Herstellervorgaben, einer fehlenden oder fehlerhaften Verfahrensanweisung oder auch in einer fehlenden Qualifizierung von Gerätschaften etc. liegen. Deshalb basiert der Vergleich der Inspektionsergebnisse auf dem Themenkreis Kritische Mängel und Beanstandungen aus vier Bereichen, Kritische Mängel Basierend auf dem 28 des Medizinproduktegesetzes wurde bei Kritischen Mängeln das weitere Betreiben bzw. die weitere Aufbereitung von einzelnen Medizinprodukten oder Produktgruppen oder bestimmte Aufbereitungsschritte mit sofortiger Wirkung untersagt. 2004/2005 wurden in 16 (= 53 %) der 30 überprüften Einrichtungen Kritische Mängel festgestellt. Der häufigste Kritische Mangel war die nicht sachgerechte Aufbereitung von Kritisch-C-Produkten. Es handelt sich hierbei nach der RKI/BfArM- Empfehlung (2) um Produkte mit besonders hohen Anforderungen an die Aufbereitung. In neun Einrichtungen (= 30 %) wurde die Aufbereitung von Kritisch-C-Produkten untersagt. Eine Validierung der Verfahren lag nicht vor, ein entsprechendes QM- System war nicht implementiert und ein Zertifikat einer akkreditierten Institution war nicht vorhanden. Nach Auffassung des OVG Münster (3) wird die Vermutungswirkung der RKI/BfArM-Empfehlung bei der Aufbereitung von Kritisch-C- Produkten nur dann erfüllt, wenn die Zertifizierung des Qualitätsmanagementsystems durch eine von der zuständigen Behörde (hier: ZLG) akkreditierten Stelle erfolgte. Weitere Kritische Mängel waren z. B. die Sterilisation der Produkte ohne vorherige Reinigung und defekte Medizinprodukte Journal 18. Jahrgang Heft
2 Konnektoren an den Beladewagen bzw. Einschüben für minimalinvasive chirurgische Instrumente (MIC) 2008/2009 hatten sieben (= 35%) von 20 überprüften Einrichtungen einen Kritischen Mangel. Bei drei Institutionen (= 15%) war der Kritische Mangel die manuelle Reinigung und Desinfektion von Kritisch-B-Produkten. Diese Produkte mit einer hohen Anforderung an die Aufbereitung müssen entsprechend der RKI/BfArM-Empfehlung in jedem Fall einer maschinellen Reinigung/Desinfektion unterzogen werden. In keinem der untersagten Fälle konnte ausreichend begründet werden, unter Berücksichtigung der Patientensicherheit, warum nur eine manuelle Aufbereitung erfolgt. Eine höhere Anzahl von möglichen Anwendungen des Instruments durch die weniger aggressive manuelle Aufbereitung ist keine ausreichende Begründung, eine maschinelle Reinigung und Desinfektion nicht durchzuführen. Nach Beschluss des Verwaltungsgerichts Köln (4) müssen Produkte der Risikoklasse Kritisch B mit validierten Verfahren und grundsätzlich maschinell aufbereitet werden wurden in zwei Häusern die weitere Aufbereitung von Kritischen Medizinprodukten untersagt, da die verwendeten Reinigungs- und Desinfektions-Geräte (RDG) nicht qualifiziert waren und die Verfahren nicht validiert. Dies bedeutete in der praktischen Konsequenz eine Schließung der ZSVA. Aufgrund juristischer Aspekte wurden in diesen Fällen Bußgeldverfahren eingeleitet. Die Bezirksregierung Arnsberg hatte alle Krankenhäuser im Regierungsbezirk in den Jahren 2004 und 2005 auf die besonderen Anforderungen im Zusammenhang der Aufbereitung von Medizinprodukten hingewiesen. Das VG Arnsberg hat 2004 (5) die Notwendigkeit der Validierung von Aufbereitungsverfahren bestätigt hat das Bundesministerium für Gesundheit einen Erfahrungsbericht über die Aufbereitung veröffentlicht (6). Deshalb konnte 2009 kein Krankenhaus mehr beanspruchen, keine Kenntnisse über die Anforderungen bei der Aufbereitung von Medizinprodukten zu haben. Es wurde juristisch geprüft, inwieweit ein Vorsatz gegeben war, da über Jahre die Kosten für die Qualifizierung der Geräte und Validierung der Verfahren eingespart wurden und die Patientensicherheit dabei nicht berücksichtigt wurde. Die verhängten Bußgelder betrugen rund Euro. Lediglich in einem Fall wurde in den Jahren 2008/2009 die Aufbereitung von Kritisch-C-Produkten untersagt. Der deutliche Rückgang bei diesem Kritischen Mangel zwischen 2004/2005 (9 Fälle = 30 %) und 2008/2009 (ein Fall = 5 %) weist schon auf eine deutliche Verbesserung der Abläufe in den ZSVA hin. Qualitätsmanagement Die kontinuierliche Gewährleistung der Qualität der Aufbereitung muss durch ein Qualitätsmanagementsystem (QMS) sichergestellt werden (2). Bei 21 (= 70 %) von den 2004 und 2005 überprüften Krankenhäusern war ein QMS auch nicht in Ansätzen vorhanden. Die vorgelegten Verfahrens- oder Arbeitsanweisungen erfassten nur grob die existierenden Prozesse und wurden nicht systematisch gesteuert. Im Gegensatz dazu hatten die 2008 und 2009 überprüften Krankenhäuser grundsätzlich ein implementiertes Qualitätsmanagementsystem (2, 7, 8, 9). Die vorgefundenen Verfahrensoder Arbeitsanweisungen erfassten die wichtigsten Einzelschritte der Aufbereitung. Abhängig von dem Qualitätsbewusstsein der Geschäftsführung des Krankenhauses und der Leitung der ZSVA wurden in einigen Fällen gute und lebendige Qualitätsmanagementsysteme angetroffen. Räume Die Raumsituation der in 2004 und 2005 überprüften Krankenhäuser war häufig unbefriedigend. Die Trennung kontaminierter Materialien von dekontaminierten Materialien und die Abtrennung von sterilisierten Materialien war oft nicht vorhanden ( Einraumlösung ). Damit hat in diesen Häusern z. B. die Gefahr einer Verwechslung zwischen unreinen und reinen Instrumenten und die Gefahr einer Spritzwasserkontamination bestanden. In 16 Einrichtungen (= 53 %) ist die fehlende Raumtrennung beanstandet worden. Die 2008 und 2009 überprüften Krankenhäuser hatten häufig eine neu- oder umgebaute ZSVA (50 % = 10 ZSVA). Die bauliche Trennung in drei Bereiche war hier umgesetzt worden. Pläne über einen Um- oder Neubau der ZSVA wurden in sechs überprüften Einrichtungen vorgelegt (= 30 %) (10, 11, 12, 13). Qualifizierung/ Validierung RDG Definitionen der Qualifizierung und der Validierung befinden sich in den einschlägigen Normen (z. B. DIN EN ISO 15883). Verfahren können nur dann validiert werden, wenn qualifizierte Gerätschaften verwendet werden. Die Notwendigkeit einer Validierung der Aufbereitungsverfahren wurde 2004 von dem VG Arnsberg bestätigt (5). In den Jahren hatten 27 ZSVA (= 90 % der überprüften Abteilungen) keine qualifizierten Reinigungs- und Desinfektionsgeräte. Da eine Verfahrensvalidierung nur mit qualifizierten Geräten erfolgen kann, waren die Verfahren dementsprechend auch nicht validiert. Als Maßnahmen im Nachgang zu den Inspektionen wurden Nachrüstungsaktionen bei Altgeräten oder/und zusätzliche Sicherheitsmaßnahmen eingefordert. Eine Validierung der Verfahren musste erfolgen (14, 15, 16, 17). Im Zusammenhang mit der Qualifizierung und Validierung sind auch in den 2008/2009 überprüften ZSVA Mängel festgestellt worden. Grund- 2 Medizinprodukte Journal 18. Jahrgang Heft
3 sätzlich verfügten die Einrichtungen aber über qualifizierte Gerätschaften und validierte Verfahren (Ausnahmen s. Kritische Mängel ). Mängel waren zum Beispiel die fehlende Dokumentation über den Proteinnachweis und mangelhafte Angaben über die verwendeten betreibertypischen Beladungen bei der Validierung (18, 19, 20). Auch war in einigen Fällen kein dokumentiertes Verfahren installiert, welches bei Leihsieben bewertete, ob die Instrumente dieses Siebes von der Validierung erfasst werden. Personal 2004/2005 arbeiteten in den ZSVA häufig Personen, die über keine spezifische Qualifikation verfügten und auch nicht entsprechend geschult worden waren. Absolventen von Fachkundelehrgängen wurden kaum angetroffen. Auch schien oft die Motivation der Mitarbeiter in der ZSVA sehr gering zu sein. In 22 Einrichtungen (=73 %) hatte keine Person mit Leitungsfunktion einen Fachkunde (FK)-III- oder mindestens Fachkunde-II-Lehrgang absolviert (2, 21). Hier hat es einen deutlichen Wandel gegeben. Die Leitungen der ZSVA, die 2008 und 2009 überprüft wurden, waren meistens gut qualifiziert und auch hoch motiviert. Auch die Schulungssystematik und Schulungsdokumentation war nicht mehr vergleichbar mit der vorgefundenen Situation der Jahre 2004/2005. Nur bei fünf Einrichtungen (= 25 %) verfügte die Leitung der ZSVA nicht über einen FK-III-Lehrgang. Diskussion Der Vergleich der Inspektionsergebnisse aus den Jahren 2004/2005 mit denen aus den Jahren 2008/2009 zeigt eine deutliche Verbesserung der Bedingungen in den Zentralen Sterilgutversorgungseinheiten. Einerseits resultiert dies aus einer konsequenten Überwachung aller ZSVA. Die Schließung von Abteilungen oder die Untersagung der Aufbereitung von bestimmten Produkten ist innerhalb der regionalen Fachkreise sehr schnell kommuniziert worden. Andererseits hat auch ohne Zweifel die deutlich verbesserte Qualifikation der Mitarbeiter in den Sterilgutversorgungseinheiten, insbesondere die der Leitungen, zu erheblichen Verbesserungen der Abläufe in den Aufbereitungsabteilungen geführt. Schlussfolgerung Die Kombination der behördlichen Überwachung und der Verbesserung der Qualifikation der Mitarbeiter in den ZSVA hat zu einer Reduzierung der Kritischen Mängel, Mängel im Zusammenhang mit dem Qualitätsmanagement, der Personalqualifikation, der Qualifizierung und Validierung (RDGs) und der Raumsituation geführt. In letzter Konsequenz bedeutet dies eine Erhöhung der Patientensicherheit. Danksagung Für die freundliche Unterstützung möchte ich mich bedanken bei Frau Dr. Mosbacher-Vogel (Bezirksregierung Detmold), Herrn Dr. Terhechte (Bezirksregierung Münster) und Herrn Dr. Kaufmann (Bezirksregierung Arnsberg). Hinweis Erstveröffentlichung in ZentrSteril 2010; 18(5): *Anschrift des Verfassers: Dr. Jürgen Barion Bezirksregierung Arnsberg, Dezernat 24 Seibertzstr Arnsberg juergen.barion@ bezreg-arnsberg.nrw.de Literatur 1. Hygea (Hygiene in der Gastroenderologie Endoskop-Aufbereitung). Präsentation beim 4. Ulmer Syposium Krankenhausinfektionen 2001 (Abstrakt FV 14) 2. Bundesgesundheitsblatt 2001; 44: ; Springerverlag OVG Münster: Beschluss vom B 1192/07 4. Verwaltungsgericht Köln: Beschluss vom (7 L 63/09) 5. Verwaltungsgericht Arnsberg: Beschluss vom (3 L 1444/04) 6. Bundesministerium für Gesundheit, Erfahrungsbericht zur Aufbereitung von Medizinprodukten in Deutschland, Bonn, Berlin Empfehlung des AK Qualität (32): Aufbau von Qualitätsmanagement in der Praxis der ZSVA. Zentr Steril 2004; 12: Empfehlung des AK Qualität (37). Zentr Steril 2005; 13: Empfehlung des AK Qualität (44): Erstellung von Verfahrensanweisungen. Zentr Steril 2006; 14: Kramer, Heeg, Botzenhart, Krankenhausund Praxishygiene, 1. Aufl. München, Jena: Urban und Fischer, 2001Krankenhausund Praxishygiene, S h t t p : / / w w w. z l g. d e / d o w n l o a d / M P / Empfehlg_.pdf themen/m/medizinprodukte/merkblatt_ hyg_aufbereitung.pdf 13. Empfehlung des AK Qualität (52). Zentr Steril 2007; 15: Empfehlung des AK Qualität (29). Zentr Steril 2003; 11: DGKH; Leitlinienentwurf für die Validierung und Routineüberwachung von Prozessabläufen bei maschinellen Reinigungsverfahren mit thermischer Desinfektion für thermostabile Medizinprodukte. Hyg Med. 2003; 28 (6): Dr. Linner; Validierung bei Reinigungsund Desinfektionsgeräten aus Sicht des Anwenders; Aseptica 2005; 11 (2): Leitlinie von DGKH, DGSV und AKI für die Validierung und Routineüberwachung maschineller Reinigungs- und Desinfektionsprozesse für thermostabile Medizinprodukte und zu Grundsätzen der Geräteauswahl; Stand: Januar Hyg Med 2005; 30 (4): Empfehlung des AK Qualität (42). Zentr Steril 2006; 14: Empfehlung des AK Qualität (53). Zentr Steril 2008; 16: Leitlinie von DGKH, DGSV und AKI für die Validierung und Routine-überwachung maschineller Reinigungs- und thermischer Desinfektionsprozesse für Medizinprodukte und zu Grundsätzen der Geräteauswahl; Zentr Steril 2008; 16, Suppl Deutsche Gesellschaft für Sterilgutversorgung 21, Empfehlungen des AK Qualität (53). Zentr Steril 2008; 16: 61. Medizinprodukte Journal 18. Jahrgang Heft
4 4 Medizinprodukte Journal 18. Jahrgang Heft
5 Medizinprodukte Journal 18. Jahrgang Heft
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen. Referent: Dipl.-Ing. Burkhard Schulze
 Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen
 Behörde für betrieblichen Arbeits-, Umwelt- und Verbraucherschutz Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen AMAH 27.06.2015 Fragen, die der Vortrag beantworten soll Warum dürfen
Behörde für betrieblichen Arbeits-, Umwelt- und Verbraucherschutz Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen AMAH 27.06.2015 Fragen, die der Vortrag beantworten soll Warum dürfen
Verfahrensanweisung: Hygienische Aufbereitung von Medizinprodukten
 Seite 1 von 5 1 Zweck... 1 2 Geltungsbereich... 1 3 Abkürzungen... 2 4 Definitionen... 2 5 Beschreibung... 4 5.1 Allgemeines... 4 5.2 Zuständigkeiten und Verantwortlichkeiten... 4 5.3 Ablauf einer Überwachung
Seite 1 von 5 1 Zweck... 1 2 Geltungsbereich... 1 3 Abkürzungen... 2 4 Definitionen... 2 5 Beschreibung... 4 5.1 Allgemeines... 4 5.2 Zuständigkeiten und Verantwortlichkeiten... 4 5.3 Ablauf einer Überwachung
Bernd Vogler Fachauditor für hygienische Aufbereitung
 Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ)
 Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Skalpell, Spritze oder Koloskop. Mehrfach verwenden eine sichere Sache?!
 Infektionen im Krankenhaus Pro Jahr erleiden in Deutschland ca. 600.000 800.000 Patienten Infektionen, die sie sich im Krankenhaus zuziehen. Nosokomiale Infektionen Ca. 50.000 Patienten sterben an diesen
Infektionen im Krankenhaus Pro Jahr erleiden in Deutschland ca. 600.000 800.000 Patienten Infektionen, die sie sich im Krankenhaus zuziehen. Nosokomiale Infektionen Ca. 50.000 Patienten sterben an diesen
Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und Aufbereitungsverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen
 Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
Die Sicht des Gesetzgebers
 Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Anforderungen an die Aufbereitung von Medizinprodukten Gesundheitssystem Pflichten Reinigung Desinfektion Sterilisation Haftung
 Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN
 Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Erfahrungen aus der Zertifizierung
 DGSV-Kongress 2010 08.10.2010, Fulda Erfahrungen aus der Zertifizierung von Qualitätsmanagement-Systemen nach DIN EN ISO 13485 für die Aufbereitung von Medizinprodukten Dr. Thomas Kießling Sachverständiger
DGSV-Kongress 2010 08.10.2010, Fulda Erfahrungen aus der Zertifizierung von Qualitätsmanagement-Systemen nach DIN EN ISO 13485 für die Aufbereitung von Medizinprodukten Dr. Thomas Kießling Sachverständiger
Sichere Aufbereitung von Medizinprodukten in der Praxis und Klinik 3. Forum und Fortbildung am 14. Juni 2014 in Hannover
 Sichere Aufbereitung von Medizinprodukten in der Praxis und Klinik 3. Forum und Fortbildung am 14. Juni 2014 in Hannover Leitlinie von DGKH, DGSV und AKI in Kooperation mit dem VAH zur Validierung der
Sichere Aufbereitung von Medizinprodukten in der Praxis und Klinik 3. Forum und Fortbildung am 14. Juni 2014 in Hannover Leitlinie von DGKH, DGSV und AKI in Kooperation mit dem VAH zur Validierung der
ZSVA: Zertifizierung + Barcode Klinikum Heidenheim
 ZSVA: Zertifizierung + Barcode Klinikum Heidenheim Jürgen Bierlein Ltg. ZSVA Wir stellen uns Vor 11.1 VZ-Stellen auf 12 Mitarbeiter Ca. 45.000 StE im Jahr Betriebszeit von 6.00-21.00h Rufbereitschaft am
ZSVA: Zertifizierung + Barcode Klinikum Heidenheim Jürgen Bierlein Ltg. ZSVA Wir stellen uns Vor 11.1 VZ-Stellen auf 12 Mitarbeiter Ca. 45.000 StE im Jahr Betriebszeit von 6.00-21.00h Rufbereitschaft am
Vivantes Netzwerk für Gesundheit GmbH
 Vivantes Netzwerk für Gesundheit GmbH Vivantes Service GmbH, Prokuristin und Betriebsleiterin Marlis Schwericke Auguste-Viktoria- Klinikum Humboldt-Klinikum Klinikum Am Urban Klinikum Hellersdorf Klinikum
Vivantes Netzwerk für Gesundheit GmbH Vivantes Service GmbH, Prokuristin und Betriebsleiterin Marlis Schwericke Auguste-Viktoria- Klinikum Humboldt-Klinikum Klinikum Am Urban Klinikum Hellersdorf Klinikum
Aktuelle Ereignisse und Probleme im 17-ten Jahr nach der Einführung des MPG
 Aktuelle Ereignisse und Probleme im 17-ten Jahr nach der Einführung des MPG Sind in allen MP- Aufbereitungsabteilungen grundsätzliche Aspekte der Aufbereitung in Ordnung? Sind alle grundsätzlichen Probleme
Aktuelle Ereignisse und Probleme im 17-ten Jahr nach der Einführung des MPG Sind in allen MP- Aufbereitungsabteilungen grundsätzliche Aspekte der Aufbereitung in Ordnung? Sind alle grundsätzlichen Probleme
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung
 Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
Leitlinie für die Validierung maschineller Reinigungs- und Desinfektionsprozesse zur Aufbereitung flexibler Endoskope
 Bericht der Leitliniengruppe der DGKH, DGSV DEGEA, DGVS und AKI zur Erarbeitung der Leitlinie für die Validierung maschineller Reinigungs- und Desinfektionsprozesse zur Aufbereitung flexibler Endoskope
Bericht der Leitliniengruppe der DGKH, DGSV DEGEA, DGVS und AKI zur Erarbeitung der Leitlinie für die Validierung maschineller Reinigungs- und Desinfektionsprozesse zur Aufbereitung flexibler Endoskope
NA(R)KA 2016 Details der Sterilgutaufbereitung aus Sicht der Bezirksregierung. Freitag Dominique-André Busch
 NA(R)KA 2016 Details der Sterilgutaufbereitung aus Sicht der Bezirksregierung Freitag 23.09.2016 Dominique-André Busch Ablauf Kurzer Überblick über die Systematik des Medizinproduktegesetzes (MPG) Grundlagen
NA(R)KA 2016 Details der Sterilgutaufbereitung aus Sicht der Bezirksregierung Freitag 23.09.2016 Dominique-André Busch Ablauf Kurzer Überblick über die Systematik des Medizinproduktegesetzes (MPG) Grundlagen
Umgang mit unsteril angelieferten Implantaten
 Kreiskrankenhaus Erding mit Klinik Dorfen Akademisches Lehrkrankenhaus Technische Universität München Umgang mit unsteril angelieferten Implantaten Birgit Wagener 03. März 2011 Gliederung 1. Vorstellung
Kreiskrankenhaus Erding mit Klinik Dorfen Akademisches Lehrkrankenhaus Technische Universität München Umgang mit unsteril angelieferten Implantaten Birgit Wagener 03. März 2011 Gliederung 1. Vorstellung
Anlage zur Akkreditierungsurkunde D-PL nach DIN EN ISO/IEC 17025: und nach Richtlinie 93/42/EWG 2
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14004-01-05 nach DIN EN ISO/IEC 17025:2005 1 und nach Richtlinie 93/42/EWG 2 Gültigkeitsdauer: 11.06.2015 bis 10.06.2020 Ausstellungsdatum:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14004-01-05 nach DIN EN ISO/IEC 17025:2005 1 und nach Richtlinie 93/42/EWG 2 Gültigkeitsdauer: 11.06.2015 bis 10.06.2020 Ausstellungsdatum:
Medizinproduktegesetz
 Medizinproduktegesetz Anforderungen an maschinelle Reinigung und Desinfektion A. Prozesse Die Prozesse der Reinigung und Desinfektion von Medizinprodukten sind grundsätzlich zu validieren. Dazu sind qualifizierte
Medizinproduktegesetz Anforderungen an maschinelle Reinigung und Desinfektion A. Prozesse Die Prozesse der Reinigung und Desinfektion von Medizinprodukten sind grundsätzlich zu validieren. Dazu sind qualifizierte
Aufbereitung von MIC- und Hohlkörper-Instrumenten
 Arbeitskreis Medizinprodukte Aufbereitung Hannover 14. Juni 2014 Aufbereitung von MIC- und Hohlkörper-Instrumenten Jörn Krämer Vertrieb Webeco GmbH An der Trave 14 23923 Selmsdorf Tel.: 0451-2807212 Mobil
Arbeitskreis Medizinprodukte Aufbereitung Hannover 14. Juni 2014 Aufbereitung von MIC- und Hohlkörper-Instrumenten Jörn Krämer Vertrieb Webeco GmbH An der Trave 14 23923 Selmsdorf Tel.: 0451-2807212 Mobil
Erfahrungen der. DQS GmbH. bei der Zertifizierung von Medizinprodukteherstellern
 Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
MPG und VO zum 94. N. Buchrieser
 MPG und VO zum 94 N. Buchrieser Gesetze und Regelwerke EU-Direktive 93/42/EWG Medizinproduktegesetz Verordnung zum 94 MPG (ÖGSV-LL 11) RDG-Normen (ÖNORM EN ISO 15883 Teil 1-7) Sterilisatornormen (EN 285,
MPG und VO zum 94 N. Buchrieser Gesetze und Regelwerke EU-Direktive 93/42/EWG Medizinproduktegesetz Verordnung zum 94 MPG (ÖGSV-LL 11) RDG-Normen (ÖNORM EN ISO 15883 Teil 1-7) Sterilisatornormen (EN 285,
Fachausbildung in der ZSVA QUO vadis, wohin führt der Weg? Berufsbild für Mitarbeiter in der Medizinprodukteaufbereitung 9. ZSVA-Forum am 4.
 Fachausbildung in der ZSVA QUO vadis, wohin führt der Weg? Berufsbild für Mitarbeiter in der Medizinprodukteaufbereitung 9. ZSVA-Forum am 4. Juni 2015 Anke Carter - Vorstandsmitglied DGSV e.v. Von Anfang
Fachausbildung in der ZSVA QUO vadis, wohin führt der Weg? Berufsbild für Mitarbeiter in der Medizinprodukteaufbereitung 9. ZSVA-Forum am 4. Juni 2015 Anke Carter - Vorstandsmitglied DGSV e.v. Von Anfang
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis
 Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Medizinprodukteaufbereitung aus Sicht der Bezirksregierung
 Medizinprodukteaufbereitung aus Sicht der Bezirksregierung Dr. Arno Terhechte Dezernat 24 Pharmazeutische Angelegenheiten Themen: Warum werden Betreiber inspiziert? Welche Betreibertypen werden überwacht?
Medizinprodukteaufbereitung aus Sicht der Bezirksregierung Dr. Arno Terhechte Dezernat 24 Pharmazeutische Angelegenheiten Themen: Warum werden Betreiber inspiziert? Welche Betreibertypen werden überwacht?
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie
 Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels
 Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Bernd Vogler Fachauditor für hygienische Aufbereitung
 Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Aktuelles zur Entwicklung der regulativen Anforderungen an die Medizinprodukteaufbereitung aus Sicht der Überwachung
 Aktuelles zur Entwicklung der regulativen Anforderungen an die Medizinprodukteaufbereitung aus Sicht der Überwachung Dr. Andrea Johmann Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln
Aktuelles zur Entwicklung der regulativen Anforderungen an die Medizinprodukteaufbereitung aus Sicht der Überwachung Dr. Andrea Johmann Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln
Umsetzung der Hygienerichtlinien
 Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
NACHWEISBARE UND QUALITÄTSSICHERE AUFBEREITUNG VON MEDIZINPRODUKTEN
 NACHWEISBARE UND QUALITÄTSSICHERE AUFBEREITUNG VON MEDIZINPRODUKTEN Anke Carter, Münchener Medizin Mechanik GmbH, Planegg, Deutschland Anke.Carter@mmmgroup.com Zusammenfassung Der nachweisbaren und qualitätssicheren
NACHWEISBARE UND QUALITÄTSSICHERE AUFBEREITUNG VON MEDIZINPRODUKTEN Anke Carter, Münchener Medizin Mechanik GmbH, Planegg, Deutschland Anke.Carter@mmmgroup.com Zusammenfassung Der nachweisbaren und qualitätssicheren
Weiterbildung. Fachkundelehrgänge I, II und III G S V
 A-8045 Graz, Ursprungweg 160 Tel: 0316/69 47 11, Fax: DW 4 e-mail: office@oegsv.com, Internet: www.oegsv.com G S V Weiterbildung Fachkundelehrgänge I, II und III Stand: März 2016 Weiterbildungslehrgang
A-8045 Graz, Ursprungweg 160 Tel: 0316/69 47 11, Fax: DW 4 e-mail: office@oegsv.com, Internet: www.oegsv.com G S V Weiterbildung Fachkundelehrgänge I, II und III Stand: März 2016 Weiterbildungslehrgang
Die Neuerungen bei den Anforderungen nach dem DStV-Qualitätssiegel. Anforderungen nach dem DStV-Qualitätssiegel
 Die Neuerungen bei den Anforderungen nach dem DStV-Qualitätssiegel Anforderungen nach dem DStV-Qualitätssiegel Neuerungen bei den Anforderungen des DStV-Qualitätssiegels aufgrund der neuen DIN EN ISO 9001:2015
Die Neuerungen bei den Anforderungen nach dem DStV-Qualitätssiegel Anforderungen nach dem DStV-Qualitätssiegel Neuerungen bei den Anforderungen des DStV-Qualitätssiegels aufgrund der neuen DIN EN ISO 9001:2015
Medizinprodukte-Überwachung im Land Bremen
 Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
Einsatzort: Name LehrgangsteilnehmerIn: Name der Leitung Aufbereitungseinheit: Name MentorIn:
 Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (gültig ab 01.01.2013) Der Lehrgangsteilnehmer
Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (gültig ab 01.01.2013) Der Lehrgangsteilnehmer
Validierung von Reinigungs-/Desinfektionsprozessen
 GEWERBEAUFSICHTSAMT Aufbereitung von Medizinprodukten (MP) in Kliniken und Praxen Validierung von Reinigungs-/Desinfektionsprozessen Um einen validierten Aufbereitungsprozess für Medizinprodukte (MP) zu
GEWERBEAUFSICHTSAMT Aufbereitung von Medizinprodukten (MP) in Kliniken und Praxen Validierung von Reinigungs-/Desinfektionsprozessen Um einen validierten Aufbereitungsprozess für Medizinprodukte (MP) zu
Validierung, validiertes Verfahren
 MELAG informiert Validierung, validiertes Verfahren Validierung von Sterilisationsprozessen von Praxis-Autoklaven, EN 17665, Erst-Validierung, Re-Validierung Sehr geehrte Frau Doktor, Sehr geehrter Herr
MELAG informiert Validierung, validiertes Verfahren Validierung von Sterilisationsprozessen von Praxis-Autoklaven, EN 17665, Erst-Validierung, Re-Validierung Sehr geehrte Frau Doktor, Sehr geehrter Herr
Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW
 Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW Dr. med. univ. Sebastian Werner 1,2 1 HygCen Germany GmbH, Schwerin / Bochum 2 Abteilung für Hygiene, Sozial- und Umweltmedizin,
Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW Dr. med. univ. Sebastian Werner 1,2 1 HygCen Germany GmbH, Schwerin / Bochum 2 Abteilung für Hygiene, Sozial- und Umweltmedizin,
Hygienestraße. Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten
 Hygienestraße Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten Herausforderung Krankenhausinfektion Reinigung von Hilfsmitteln und Medizinprodukten Krankenhausinfektionen bedeuten
Hygienestraße Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten Herausforderung Krankenhausinfektion Reinigung von Hilfsmitteln und Medizinprodukten Krankenhausinfektionen bedeuten
Softwarevalidierung aus Anwendersicht. DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009
 Softwarevalidierung aus Anwendersicht DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009 Softwarevalidierung aus Anwendersicht Geräte mit automatischen Prozessabläufen zur Aufbereitung von Medizinprodukten
Softwarevalidierung aus Anwendersicht DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009 Softwarevalidierung aus Anwendersicht Geräte mit automatischen Prozessabläufen zur Aufbereitung von Medizinprodukten
Errichten. Sterilisation+Desinfektion+Reinigung von MP
 Medizinproduktegesetz (MPG) 1.1.1997 Klinische Bewertung + Prüfung Herstellung Funktionstüchtigkeit Inbetriebnahme Instandhaltung Errichten Betrieb Inverkehrbringen Leistungsfähigkeit Überwachung Sicherheit
Medizinproduktegesetz (MPG) 1.1.1997 Klinische Bewertung + Prüfung Herstellung Funktionstüchtigkeit Inbetriebnahme Instandhaltung Errichten Betrieb Inverkehrbringen Leistungsfähigkeit Überwachung Sicherheit
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten
 Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen fest an Zertifizierungsstellen
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen fest an Zertifizierungsstellen
Alles sauber oder was
 DGSV Kongress 2010 Alles sauber oder was Aufbereitung von Medizinprodukten in der Arztpraxis 12.10.2010 Kassenärztliche Vereinigung Baden-Württemberg Arztstruktur An der vertragsärztlichen Versorgung teilnehmende
DGSV Kongress 2010 Alles sauber oder was Aufbereitung von Medizinprodukten in der Arztpraxis 12.10.2010 Kassenärztliche Vereinigung Baden-Württemberg Arztstruktur An der vertragsärztlichen Versorgung teilnehmende
Einsatzort: Name Lehrgangsteilnehmer/in: Name der Leitung Aufbereitungseinheit: Name Mentor/in:
 Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (vorliegende Version 03 ist gültig ab
Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (vorliegende Version 03 ist gültig ab
Reinigungs- und Desinfektionsgeräte (RDG)
 Reinigungs- und Desinfektionsgeräte (RDG) Referent Beat Reber Maschineningenieur FH/STV Leiter Markt Schweiz Belimed Sauter AG, Sulgen 12.09.2011 BRE 1 Übersicht der Themen Definition der Reinigung- und
Reinigungs- und Desinfektionsgeräte (RDG) Referent Beat Reber Maschineningenieur FH/STV Leiter Markt Schweiz Belimed Sauter AG, Sulgen 12.09.2011 BRE 1 Übersicht der Themen Definition der Reinigung- und
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit?
 Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Partikelreinheit und Hygiene aus Sicht der Zentralsterilisation. Gabriela Egeli BODE AG
 Partikelreinheit und Hygiene aus Sicht der Zentralsterilisation Gabriela Egeli BODE AG Inhalt Aufbereitungskreislauf Hygienerelevante Punkte in der ZSVA Infrastruktur / Räumlichkeiten Personalmanagement
Partikelreinheit und Hygiene aus Sicht der Zentralsterilisation Gabriela Egeli BODE AG Inhalt Aufbereitungskreislauf Hygienerelevante Punkte in der ZSVA Infrastruktur / Räumlichkeiten Personalmanagement
Übersicht über ISO 9001:2000
 Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen
 Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen F. H. H. Brill Dr. Brill + Partner GmbH Institut für Hygiene und Mikrobiologie, Hamburg, www.brillhygiene.com
Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen F. H. H. Brill Dr. Brill + Partner GmbH Institut für Hygiene und Mikrobiologie, Hamburg, www.brillhygiene.com
Neuerscheinung Oktober Auflage -
 Leitlinie von DGKH, DGSV und AKI für die Validierung und Routineüberwachung maschineller Reinigungs- und thermischer Desinfektionsprozesse für Medizinprodukte Neuerscheinung Oktober 2014-4. Auflage - Robert
Leitlinie von DGKH, DGSV und AKI für die Validierung und Routineüberwachung maschineller Reinigungs- und thermischer Desinfektionsprozesse für Medizinprodukte Neuerscheinung Oktober 2014-4. Auflage - Robert
Sicherstellung einer sachgerechten Aufbereitung von Medizinprodukten im niedergelassenen, ärztlichen Bereich
 Sicherstellung einer sachgerechten Aufbereitung von Medizinprodukten im niedergelassenen, ärztlichen Bereich Abschlussarbeit zum Fachkundelehrgang III für Leiter/innen der zentralen Sterilgutversorgung
Sicherstellung einer sachgerechten Aufbereitung von Medizinprodukten im niedergelassenen, ärztlichen Bereich Abschlussarbeit zum Fachkundelehrgang III für Leiter/innen der zentralen Sterilgutversorgung
Qualitätsindikatoren in der Infektionsprävention- Was haben wir zu erwarten?
 Dr. Dr. Alexander Steiner Qualitätsindikatoren in der Infektionsprävention- Was haben wir zu erwarten? 1 Agenda 1 2 3 4 5 Novelle des SGB V durch das KHSG Beschluss des G-BA vom 17.12.2015 Das Verfahren
Dr. Dr. Alexander Steiner Qualitätsindikatoren in der Infektionsprävention- Was haben wir zu erwarten? 1 Agenda 1 2 3 4 5 Novelle des SGB V durch das KHSG Beschluss des G-BA vom 17.12.2015 Das Verfahren
ÜBERPRÜFUNG VON REINIGUNGS- UND DESINFEKTIONSGERÄTEN
 Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien 6 Stand: 29. Februar 2012 ÜBERPRÜFUNG VON REINIGUNGS- UND DESINFEKTIONSGERÄTEN
Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien 6 Stand: 29. Februar 2012 ÜBERPRÜFUNG VON REINIGUNGS- UND DESINFEKTIONSGERÄTEN
Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH
 Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH Olympus Deutschland Medical Systems Jesco Danylow, Produktmanagement Hannover, 11. Juni 2016 Inhalt 1. Einführung
Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH Olympus Deutschland Medical Systems Jesco Danylow, Produktmanagement Hannover, 11. Juni 2016 Inhalt 1. Einführung
8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis"
 8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis" Aufbereitung von Medizinprodukten in der Zahnarztpraxis Überwachung durch das Regierungspräsidiums Kassel Dipl. -Ing. (FH) Ilker Büyükok, MHBA
8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis" Aufbereitung von Medizinprodukten in der Zahnarztpraxis Überwachung durch das Regierungspräsidiums Kassel Dipl. -Ing. (FH) Ilker Büyükok, MHBA
Brush-Up Wissensauffrischung für die ZSVA
 Programm Brush-Up Wissensauffrischung für die ZSVA 2014 Tuttlingen Berlin Bochum Einleitung Brush-up (to brush up sth. - etw. aufpolieren) bereits vorhandener Kenntnisse und für alle, die ihre Sach- und
Programm Brush-Up Wissensauffrischung für die ZSVA 2014 Tuttlingen Berlin Bochum Einleitung Brush-up (to brush up sth. - etw. aufpolieren) bereits vorhandener Kenntnisse und für alle, die ihre Sach- und
EN ISO Ein Meilenstein?
 Ein Meilenstein? ÖGSV Kongress 2007 3.-5. Mai 2007 Baden / Österreich T. Miorini Institut für angewandte Hygiene, Graz, Austria EN ISO 15883 hat ihre Schatten voraus geworfen Hersteller: Anpassung der
Ein Meilenstein? ÖGSV Kongress 2007 3.-5. Mai 2007 Baden / Österreich T. Miorini Institut für angewandte Hygiene, Graz, Austria EN ISO 15883 hat ihre Schatten voraus geworfen Hersteller: Anpassung der
Umsetzung des Medizinprodukterechts
 Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Podiumsdiskussion. Dr. Früh Control GmbH DGSV-Kongress
 Podiumsdiskussion Dr. Früh Control GmbH DGSV-Kongress 10-09 1 Generelle Vorgaben für Medizinprodukte Medizinprodukte-Gesetz 14: Medizinprodukte dürfen nicht betrieben und angewendet werden, wenn sie Mängel
Podiumsdiskussion Dr. Früh Control GmbH DGSV-Kongress 10-09 1 Generelle Vorgaben für Medizinprodukte Medizinprodukte-Gesetz 14: Medizinprodukte dürfen nicht betrieben und angewendet werden, wenn sie Mängel
70 JAHRE WEBECO WEGWEISENDE STERILGUTAUF- BEREITUNG
 70 JAHRE WEBECO WEGWEISENDE STERILGUTAUF- BEREITUNG Der A 0 -Wert als Maßstab für die thermische Desinfektion Konzept und Anforderungen an unterschiedliche Medizinprodukte Thomas Kühne 5. Forum und Fortbildung
70 JAHRE WEBECO WEGWEISENDE STERILGUTAUF- BEREITUNG Der A 0 -Wert als Maßstab für die thermische Desinfektion Konzept und Anforderungen an unterschiedliche Medizinprodukte Thomas Kühne 5. Forum und Fortbildung
Wie bereite ich mich auf ein Audit der ZSVA vor? Dr. sc. nat. Nicola Franscini, Abteilung Medizinprodukte, Swissmedic
 Wie bereite ich mich auf ein Audit der ZSVA vor? Dr. sc. nat. Nicola Franscini, Abteilung Medizinprodukte, Swissmedic Swissmedic Schweizerisches Heilmittelinstitut Hallerstrasse 7 CH-3000 Bern 9 www.swissmedic.ch
Wie bereite ich mich auf ein Audit der ZSVA vor? Dr. sc. nat. Nicola Franscini, Abteilung Medizinprodukte, Swissmedic Swissmedic Schweizerisches Heilmittelinstitut Hallerstrasse 7 CH-3000 Bern 9 www.swissmedic.ch
Marktüberwachung in der Behördenpraxis
 REGIERUNG VON SCHWABEN Gewerbeaufsichtsamt Am Beispiel: Aufbereitung von Medizinprodukten Dipl.-Ing. (FH) M. Kremmel Augsburg, 12.10.2007 Vortragsthemen Aufgaben der Gewerbeaufsicht Aufbereitung von Medizinprodukten
REGIERUNG VON SCHWABEN Gewerbeaufsichtsamt Am Beispiel: Aufbereitung von Medizinprodukten Dipl.-Ing. (FH) M. Kremmel Augsburg, 12.10.2007 Vortragsthemen Aufgaben der Gewerbeaufsicht Aufbereitung von Medizinprodukten
Aufbereitung von Endoskopen durch die ZSVA
 Aufbereitung von Endoskopen durch die ZSVA 11. Erlanger Steritreff 13.05.2014 Universitätsklinikum Erlangen Gliederung A) Allgemeiner Teil B) Gesetzlich Bestimmungen, Normen und Empfehlungen C) Praktische
Aufbereitung von Endoskopen durch die ZSVA 11. Erlanger Steritreff 13.05.2014 Universitätsklinikum Erlangen Gliederung A) Allgemeiner Teil B) Gesetzlich Bestimmungen, Normen und Empfehlungen C) Praktische
Sachkenntnis-Lehrgang Hygienemanagement/Aufbereitung von Medizinprodukten
 Die erfolgreiche Teilnahme am Sachkenntnis-Lehrgang Hygienemanagement/Aufbereitung von Medizinprodukten gibt den Teilnehmern die notwendige Sicherheit, als Hygienebeauftragter und/oder Beauftragter für
Die erfolgreiche Teilnahme am Sachkenntnis-Lehrgang Hygienemanagement/Aufbereitung von Medizinprodukten gibt den Teilnehmern die notwendige Sicherheit, als Hygienebeauftragter und/oder Beauftragter für
DECKBLATT. Selbstauskunft von Einrichtungen für ambulantes Operieren
 DECKBLATT (diese Seite bitte nicht an HLPUG senden!) Selbstauskunft von Einrichtungen für ambulantes Operieren für die Erhebung der Qualität des Hygienemanagements auf Grundlage des Infektionsschutzgesetzes
DECKBLATT (diese Seite bitte nicht an HLPUG senden!) Selbstauskunft von Einrichtungen für ambulantes Operieren für die Erhebung der Qualität des Hygienemanagements auf Grundlage des Infektionsschutzgesetzes
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen
 Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT. Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung
 KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
Qualitätsmanagement nach DIN EN ISO 9000ff
 Qualitätsmanagement nach DIN EN ISO 9000ff Die Qualität von Produkten und Dienstleistungen ist ein wesentlicher Wettbewerbsfaktor. Soll dauerhaft Qualität geliefert werden, ist die Organisation von Arbeitsabläufen
Qualitätsmanagement nach DIN EN ISO 9000ff Die Qualität von Produkten und Dienstleistungen ist ein wesentlicher Wettbewerbsfaktor. Soll dauerhaft Qualität geliefert werden, ist die Organisation von Arbeitsabläufen
Wichtige Punkte der Qualitätssicherung in einer ärztlichen Privatapotheke
 Gesundheitsdirektion Wichtige Punkte der Qualitätssicherung in einer ärztlichen Privatapotheke Symposium Vereinigung Zürcher Internisten Universität Irchel 28. Januar 2016 Janine Arvedson, Heilmittelinspektorin
Gesundheitsdirektion Wichtige Punkte der Qualitätssicherung in einer ärztlichen Privatapotheke Symposium Vereinigung Zürcher Internisten Universität Irchel 28. Januar 2016 Janine Arvedson, Heilmittelinspektorin
Verantwortung t bei der Aufbereitung von Medizinprodukten
 5. Schweizerische Fachtage über die Sterilisation, 3. 4. Juni 2009 Verantwortung t bei der Aufbereitung von Medizinprodukten aus Sicht der Behörde Markus Weiss Inspektor Swissmedic, Abteilung Medizinprodukte
5. Schweizerische Fachtage über die Sterilisation, 3. 4. Juni 2009 Verantwortung t bei der Aufbereitung von Medizinprodukten aus Sicht der Behörde Markus Weiss Inspektor Swissmedic, Abteilung Medizinprodukte
Aufbereitung von Medizinprodukten: Was fordert die Hygiene?
 Aufbereitung von Medizinprodukten: Was fordert die Hygiene? BVMed-Hygieneforum 2015 Prävention von Krankenhausinfektionen Berlin, 2.12.2015 Chirurgie-Instrumenten-Arbeitsgruppe (CLEANICAL ) Berlin Dr.
Aufbereitung von Medizinprodukten: Was fordert die Hygiene? BVMed-Hygieneforum 2015 Prävention von Krankenhausinfektionen Berlin, 2.12.2015 Chirurgie-Instrumenten-Arbeitsgruppe (CLEANICAL ) Berlin Dr.
Konformitätsbewertung 3.9 A 10
 Antworten und Beschlüsse des EK-Med Konformitätsbewertung 3.9 A 10 Besondere Fragestellungen bei der Zertifizierung von Qualitätsmanagementsystemen nach DIN EN ISO 13485 in Unternehmen der Orthopädie-,
Antworten und Beschlüsse des EK-Med Konformitätsbewertung 3.9 A 10 Besondere Fragestellungen bei der Zertifizierung von Qualitätsmanagementsystemen nach DIN EN ISO 13485 in Unternehmen der Orthopädie-,
Die Aufbereitung zahnärztlicher Instrumente
 Die Aufbereitung zahnärztlicher Instrumente Autor: Dr. Gerd Leidig, QM-Berater und Auditor, Mailadresse: gerd.leidig@online.de Rechtliche Grundlagen Die Aufbereitung... ist unter Berücksichtigung der Angaben
Die Aufbereitung zahnärztlicher Instrumente Autor: Dr. Gerd Leidig, QM-Berater und Auditor, Mailadresse: gerd.leidig@online.de Rechtliche Grundlagen Die Aufbereitung... ist unter Berücksichtigung der Angaben
Aktualisierung der Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten (KRINKO/BfArM, 2001)
 Aktualisierung der Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten (KRINKO/BfArM, 2001) Hintergrund und Sachstand M. Mielke Robert Koch-Institut Sachgerechte Aufbereitung von Medizinprodukten
Aktualisierung der Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten (KRINKO/BfArM, 2001) Hintergrund und Sachstand M. Mielke Robert Koch-Institut Sachgerechte Aufbereitung von Medizinprodukten
Durchführung von internen Audits Seite 2 von 6
 Durchführung von internen Audits Seite 2 von 6 1 Zweck Diese Verfahrensanweisung regelt das Vorgehen bei der Planung, Durchführung und Dokumentation von internen Audits in Arzneimittel-Überwachungsbehörden
Durchführung von internen Audits Seite 2 von 6 1 Zweck Diese Verfahrensanweisung regelt das Vorgehen bei der Planung, Durchführung und Dokumentation von internen Audits in Arzneimittel-Überwachungsbehörden
MELA quick 12+ Kompakt. Schnell. Stark.
 MELA quick 12+ Kompakt. Schnell. Stark. Die Anforderung. Die Anforderungen an die Aufbereitung zahnärztlicher Instrumente werden vom Robert-Koch-Institut (RKI) definiert. Übertragungsinstrumente für den»semikritischen«einsatz
MELA quick 12+ Kompakt. Schnell. Stark. Die Anforderung. Die Anforderungen an die Aufbereitung zahnärztlicher Instrumente werden vom Robert-Koch-Institut (RKI) definiert. Übertragungsinstrumente für den»semikritischen«einsatz
Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) - Validierung und Typprüfung
 Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) - Validierung und Typprüfung M. Feltgen, S. Werner HygCen Germany GmbH, Schwerin / Bochum
Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) - Validierung und Typprüfung M. Feltgen, S. Werner HygCen Germany GmbH, Schwerin / Bochum
Ausstattung Praxis 1 : Bohrerbad, Tauchdesinfektion (= chem. Desinfektion), Autoklav mit Gravitationsverfahren
 Anlage 23 Beispiele für die Aufbereitung von Medizinprodukten Nachdem der Praxisinhaber den prinzipiellen Ablauf der Aufbereitung vorbereitet hat, muss er nun unter seinen individuellen Praxisbedingungen
Anlage 23 Beispiele für die Aufbereitung von Medizinprodukten Nachdem der Praxisinhaber den prinzipiellen Ablauf der Aufbereitung vorbereitet hat, muss er nun unter seinen individuellen Praxisbedingungen
Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung
 Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung Angestellten Forum des ZVK Stuttgart 04.03.2016 Birgit Reinecke ZentraleEinrichtungPhysiotherapieund
Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung Angestellten Forum des ZVK Stuttgart 04.03.2016 Birgit Reinecke ZentraleEinrichtungPhysiotherapieund
Empfehlungen zur Qualitätssicherung bei der maschinellen Aufbereitung und Sterilisation von Medizinprodukten
 Empfehlungen zur Qualitätssicherung bei der maschinellen Aufbereitung und Sterilisation von Medizinprodukten Die Verantwortlichkeiten und Inhalte bei der Prozessvalidierung Einleitung Die hiermit vorgelegten
Empfehlungen zur Qualitätssicherung bei der maschinellen Aufbereitung und Sterilisation von Medizinprodukten Die Verantwortlichkeiten und Inhalte bei der Prozessvalidierung Einleitung Die hiermit vorgelegten
 Leistungsspektrum in Arztpraxen und ambulanten OP Zentren Chirurgie / Orthopädie - Bandnähte an großen und kleinen Gelenken - Gelenksspiegelungen - Hämorrhoidenentfernung - Leistenbrüche - Spaltung von
Leistungsspektrum in Arztpraxen und ambulanten OP Zentren Chirurgie / Orthopädie - Bandnähte an großen und kleinen Gelenken - Gelenksspiegelungen - Hämorrhoidenentfernung - Leistenbrüche - Spaltung von
Endoskop-Aufbereitung durch die ZSVA
 Endoskop-Aufbereitung durch die ZSVA DGSV - Fulda - 2013 Gliederung A) Allgemeiner Teil B) Gesetzlich Bestimmungen, Normen und Empfehlungen C) Praktische Umsetzung D) Chancen und Risiken E) Informatives
Endoskop-Aufbereitung durch die ZSVA DGSV - Fulda - 2013 Gliederung A) Allgemeiner Teil B) Gesetzlich Bestimmungen, Normen und Empfehlungen C) Praktische Umsetzung D) Chancen und Risiken E) Informatives
Antrag auf Erteilung einer Konzession gemäß 30 Gewerbeordnung (GewO)
 An Kreis Mettmann Der Landrat Gesundheitsamt, 53-11 Düsseldorfer Str. 47 40822 Mettmann Antrag auf Erteilung einer Konzession gemäß 30 Gewerbeordnung (GewO) 1. Angaben zum Antragsteller Name, Vorname Anschrift
An Kreis Mettmann Der Landrat Gesundheitsamt, 53-11 Düsseldorfer Str. 47 40822 Mettmann Antrag auf Erteilung einer Konzession gemäß 30 Gewerbeordnung (GewO) 1. Angaben zum Antragsteller Name, Vorname Anschrift
Steffen Wolf Referat II 4 - Technischer Verbraucherschutz, Marktaufsicht
 Die einheitliche Überwachung in Deutschland 15. DGSV-Kongress vom 03.10. 05.10.2011 in Fulda Steffen Wolf Referat II 4 - Technischer Verbraucherschutz, Marktaufsicht 1 Gliederung Kompetenz von Bund und
Die einheitliche Überwachung in Deutschland 15. DGSV-Kongress vom 03.10. 05.10.2011 in Fulda Steffen Wolf Referat II 4 - Technischer Verbraucherschutz, Marktaufsicht 1 Gliederung Kompetenz von Bund und
RECONIC SICHER NACHHALTIG WIRTSCHAFTLICH. RECONIC ist eine eingetragene Marke der VANGUARD AG
 RECONIC SICHER NACHHALTIG WIRTSCHAFTLICH RECONIC ist eine eingetragene Marke der VANGUARD AG VANGUARD GRUPPE VANGUARD ist Ihr strategischer Partner für die qualitätsgesicherte, nachhaltige und wirtschaftliche
RECONIC SICHER NACHHALTIG WIRTSCHAFTLICH RECONIC ist eine eingetragene Marke der VANGUARD AG VANGUARD GRUPPE VANGUARD ist Ihr strategischer Partner für die qualitätsgesicherte, nachhaltige und wirtschaftliche
Überprüfung der Aufbereitung von Medizinprodukten in Krankenanstalten im Rahmen der sanitären Aufsicht
 Überprüfung der Aufbereitung von Medizinprodukten in Krankenanstalten im Rahmen der sanitären Aufsicht Prof. Dr. Elisabeth Presterl MBA Medizinische Universität Wien Klin. Inst. f. Krankenhaushygiene Indirekte
Überprüfung der Aufbereitung von Medizinprodukten in Krankenanstalten im Rahmen der sanitären Aufsicht Prof. Dr. Elisabeth Presterl MBA Medizinische Universität Wien Klin. Inst. f. Krankenhaushygiene Indirekte
kommender Medizinprodukte bezeichnet werden, die sich von der technischen Aufbereitung abgrenzt.
 Stand: 01.12.2013 Anforderungen an die hygienische 1 Aufbereitung von Medizinprodukten in Nordrhein- Westfalen Hier sind ausschließlich Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten
Stand: 01.12.2013 Anforderungen an die hygienische 1 Aufbereitung von Medizinprodukten in Nordrhein- Westfalen Hier sind ausschließlich Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten
Validierung manueller Aufbereitungsprozesse im niedergelassenen Bereich. Petra Labonte
 Validierung manueller Aufbereitungsprozesse im niedergelassenen Bereich Petra Labonte Geltungsbereich: Sowohl die Leitlinie zur Validierung der manuellen Aufbereitung als auch die Medizinproduktebetreiber-Verordnung
Validierung manueller Aufbereitungsprozesse im niedergelassenen Bereich Petra Labonte Geltungsbereich: Sowohl die Leitlinie zur Validierung der manuellen Aufbereitung als auch die Medizinproduktebetreiber-Verordnung
RKI-Empfehlung/Risikobewertung 11.1
 Anhang 1 Unkritische Medizinprodukte Medizinprodukte, die lediglich mit intakter Haut in Unkritische Medizinprodukte z.b. Instrumente für Maßnahmen ohne Schleimhautkontakt (z.b. extraorale Teile des Gesichtsbogens,
Anhang 1 Unkritische Medizinprodukte Medizinprodukte, die lediglich mit intakter Haut in Unkritische Medizinprodukte z.b. Instrumente für Maßnahmen ohne Schleimhautkontakt (z.b. extraorale Teile des Gesichtsbogens,
Sachkundelehrgang für Hygiene, Medizinprodukteaufbereitung und Qualitätsmanagement für Ärzte und erfahrenes Op-Personal
 Prof. Dr. Dr. Bernhard Lachenmayr Neuhauserstr. 23 80331 München Sachkundelehrgang für Hygiene, Medizinprodukteaufbereitung und Qualitätsmanagement für Ärzte und erfahrenes Op-Personal zum Erwerb der Sachkenntnis
Prof. Dr. Dr. Bernhard Lachenmayr Neuhauserstr. 23 80331 München Sachkundelehrgang für Hygiene, Medizinprodukteaufbereitung und Qualitätsmanagement für Ärzte und erfahrenes Op-Personal zum Erwerb der Sachkenntnis
Trinkwasserhygiene. Gefährdungsanalyse nach 16. Trinkwasserverordnung (TrinkwV) Jürgen Burg Landratsamt Ortenaukreis Trinkwasserüberwachung
 Trinkwasserhygiene Gefährdungsanalyse nach 16 Trinkwasserverordnung (TrinkwV) Jürgen Burg Landratsamt Ortenaukreis Trinkwasserüberwachung Arbeitskreis Krankenhausingenieure Baden - Württemberg 27.10.2016
Trinkwasserhygiene Gefährdungsanalyse nach 16 Trinkwasserverordnung (TrinkwV) Jürgen Burg Landratsamt Ortenaukreis Trinkwasserüberwachung Arbeitskreis Krankenhausingenieure Baden - Württemberg 27.10.2016
Einteilung der Medizinprodukte nach RKI (Risikobewertung und Einstufung von Medizinprodukten vor der Aufbereitung)
 ÖGSV Fachkundelehrgang I 11 Einteilung der Medizinprodukte nach RKI (Risikobewertung und Einstufung von Medizinprodukten vor der Aufbereitung) M.T. Enko 2015 Inhalt 1 Ziel des Unterrichtes:... 3 2 Änderungen
ÖGSV Fachkundelehrgang I 11 Einteilung der Medizinprodukte nach RKI (Risikobewertung und Einstufung von Medizinprodukten vor der Aufbereitung) M.T. Enko 2015 Inhalt 1 Ziel des Unterrichtes:... 3 2 Änderungen
6 Instrumentenhygiene/Aufbereitung von Medizinprodukten
 6 Instrumentenhygiene/Aufbereitung von Medizinprodukten Komplexe Instrumententechnik Gesetzliche Regelungen MPG 140 Die moderne Medizin ist ohne ihre technische Ausrüstung nicht mehr denkbar. Letztere
6 Instrumentenhygiene/Aufbereitung von Medizinprodukten Komplexe Instrumententechnik Gesetzliche Regelungen MPG 140 Die moderne Medizin ist ohne ihre technische Ausrüstung nicht mehr denkbar. Letztere
Unkritisch Semikritisch Kritisch: Grundlagen zur Aufbereitung und Klassifizierung von Instrumenten und Medizinprodukten
 Unkritisch Semikritisch Kritisch: Grundlagen zur Aufbereitung und Klassifizierung von Instrumenten und Medizinprodukten Workshop zum 3. Hygienetag der KVB Nürnberg Qualitätssicherung, Team Qualitätsmanagement/QZ/Hygiene
Unkritisch Semikritisch Kritisch: Grundlagen zur Aufbereitung und Klassifizierung von Instrumenten und Medizinprodukten Workshop zum 3. Hygienetag der KVB Nürnberg Qualitätssicherung, Team Qualitätsmanagement/QZ/Hygiene
In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm der DGSV zur Einstufung
 64 DGSV Zentralsterilisation 1/2013 Notwendige Korrektur des Flussdiagramms der DGSV 2012 im nuar 2013 In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm
64 DGSV Zentralsterilisation 1/2013 Notwendige Korrektur des Flussdiagramms der DGSV 2012 im nuar 2013 In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm
Aktuelles zum Management von Medizinprodukten Pflicht und Kür
 Aktuelles zum Management von Medizinprodukten Pflicht und Kür Dr. Wolfgang Rulf 2013 Gliederung der Arbeitssitzung Die Prüfungs-Ankündigung Notwendige Literatur Grundsätzliches Vorbereitung Begehung Fehler
Aktuelles zum Management von Medizinprodukten Pflicht und Kür Dr. Wolfgang Rulf 2013 Gliederung der Arbeitssitzung Die Prüfungs-Ankündigung Notwendige Literatur Grundsätzliches Vorbereitung Begehung Fehler
Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation
 Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation Präsentation von Markus Geissmann anlässlich der 7èmes Journées Nationales Suissessursur la Stérilisation
Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation Präsentation von Markus Geissmann anlässlich der 7èmes Journées Nationales Suissessursur la Stérilisation
ÖGSV Fachtagung 2013 Thea Enko
 ÖGSV Fachtagung 2013 Thea Enko Leitlinie zur Auswahl von aufbereitbaren Medizinprodukten Ziel: Beschaffung optimieren Fehlkäufe vermeiden Hilfestellung bei der Beschaffung von aufbereitbaren Medizinprodukten
ÖGSV Fachtagung 2013 Thea Enko Leitlinie zur Auswahl von aufbereitbaren Medizinprodukten Ziel: Beschaffung optimieren Fehlkäufe vermeiden Hilfestellung bei der Beschaffung von aufbereitbaren Medizinprodukten
