5.4 Der 1. Hauptsatz der Thermodynamik Innere Energie
|
|
|
- Julius Färber
- vor 7 Jahren
- Abrufe
Transkript
1 5.4 Der. Hautsatz der Therodynaik In Ka. 5.3 haben wir (hoentlich) gelernt, dass die Teeratur ein Maß ür die Energie ist, die in der ungeordneten Wärebewegung der Teilchen steckt. Wir wissen auch, wie diese Energie von der Molekülor (Anzahl der Freiheitsgrade) abhängt. I Kaitel 5.4 wenden wir den aus der Mechanik bekannten Energieerhaltungssatz au therodynaische Systee an. Die innere Energie eines therodynaischen Systes kann au verschiedene Weise verändert werden, z.b. durch Zu- oder Abuhr von Wäre oder echanischer Arbeit. Wir ragen insbesondere nach der Wäreenge, die nötig ist, u die Teeratur eines Syste u ein bestites Maß zu erhöhen, d.h. nach der Wärekaazität. Sie werden außerde den Unterschied zwischen Wärekaazität bei konstante Voluen und Wärekaazität bei konstante Druck eines Gases sowie die Zustandsgröße Enthalie kennen lernen Innere Energie Die gesate in der ungeordneten Bewegung der Teilchen geseicherte Energie bezeichnen wir als innere Energie U. Die innere Energie ist dait eine Zustandsgröße. Die Teeratur ist ein Maß ür die Energie der Teilchen (sieh Ka. 5.3). Die innere Energie U hängt dait natürlich von der Teeratur und der Anzahl der Teilchen (bzw. von Stoenge oder der Masse) i Syste ab. Teeratur (kinetische) Energie der ungeordneten Bewegung der Teilchen T ~ E kin E kin = kt Gesate Therische Energie i Syste bei N Teilchen U = N kt U = nn A kt ( N Ak = R ) U = n RT Innere Energie eines idealen Gases: [Gl ] Die Innere Energie U ist eine Zustandsgröße Die Innere Energie U eines idealen Gas hängt nur von Teeratur ab, U = U ( T ) U T Zustände it gleicher Teeratur haben die gleiche innere Energie U U ist roortional zur Teeratur: U ~ T U hängt nicht vo Druck oder vo Voluen V ab! Die innere Energie ändert sich durch jede Art von Energiezuuhr ins Syste oder Energieabgabe des Systes, z.b. bei einer Zustandsänderung : Δ U = U U I Allgeeinen interessieren uns nur solche Veränderungen der inneren Energie, nicht jedoch die absolute Größe der inneren Energie. So sielt z.b. die cheische Energie des Systes keine Rolle, solange keine cheischen Reaktionen ablauen. Ebenso ist die (sehr große!) in den Atokernen (bzw. der Masse) geseicherte Energie nur dann von Bedeutung, wenn Kernreaktionen ablauen. hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. /5
2 Veränderung der inneren Energie U eines Systes z.b. durch Wärezuuhr / Wäreabgabe Q Voluenänderungsarbeit W (Bs.: Kolben wird it Krat F u Weg s verschoben) ech. Arbeitszuuhr ohne Vol.- Veränderung (z.b. Welle, Rührer, ) Wellenarb. elektr. Energ. Syste Q W s F Elektrische Energie etc Wäre und (Voluenänderungs-) Arbeit Die wichtigsten Energieoren, die die innere Energie eines Systes verändern können sind Wäre Q und (Voluenänderungs-) Arbeit W. Wäre Q ist die Energie, die au Grund einer Teeraturdierenz zwischen zwei Systeen übertragen wird. Die Richtung des Energielusses ist dabei ier: hohe Teeratur niedrige Teeratur! Voluenänderungsarbeit W ist die Energie, die bei Koression oder Exansion eines Fluids übertragen wird Eine Voluenänderung ist wegen der Druckkräte ier it einer Übertragung von echanischer Arbeit verbunden (Mechanik: Arbeit = Krat * Weg ) Koression: Voluen wird kleiner, de Syste wird Arbeit zugeührt Exansion: Voluen wird größer, das Syste gibt Arbeit ab Anangs- und Endzustand des Systes haben bestite Werte der inneren Energie U unabhängig davon, ob Energie in For von Wäre Q und/oder Arbeit W ausgetauscht wurde Die Innere Energie U ist eine Zustandsgröße! (beschreibt Lage des Systes) Zustand U Zustand U Wäre Arbeit Wäre und Voluen-Änderungsarbeit sind Prozessgrößen (werden bei Prozess ausgetauscht, sind vo Weg i Zustandsdiagra abhängig) hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. /5
3 Wir verwenden die olgende Vorzeichenkonvention ür alle Energien, die de Syste zugeührt werden bzw. vo Syste abgegeben werden: Syste wird Energie zugeührt W > 0 bzw. Q > Syste gibt Energie ab W < 0 bzw. Q < 0 W + Syste (innere Energie U) Q + W - Q - Arbeit Wäre WARNUNG: Diese Konvention ist wird zwar so in den eisten Büchern verwendet aber leider nicht in allen! Es gab schon Studenten, die in der Klausur Foreln aus verschiedenen Büchern it verschiedenen Konventionen kobinierten (und dait natürlich nur unsinnige Resultate erhielten!) Bs.: Ein Motor ( Syste ) gibt insgesat (Sue über alle Prozessschritte) Arbeit ab, dait ist W ges < 0. Wenn wir den Nutzen gerne als ositive Größe hätten, dann deinieren wir die Nutzarbeit als W = W, dait ist W > 0. Wäre Q Nutz ges Wenn zwei Körer it verschiedenen Teeraturen in Kontakt koen, dann ströt Wäre vo heißen zu kalten Körer. In den eisten Fällen erhöht sich dadurch die Teeratur des zuvor kalten Körers. Die Wäreenge Δ Q, die ür eine Teeraturerhöhung u Δ T benötigt wird, ist roortional zu Δ T : Δ Q ~ ΔT Δ Q = C ΔT (C : Wärekaazität, [ C ] = J ) K [Gl ] Δ Q ist außerde roortional zur Stoenge n bzw. der Masse des betrachteten Systes: Δ Q ~ n ΔT Δ Q = nc ΔT (C : Molare Wärekaazität, [ C ] J = ) [Gl ] ol K Δ Q ~ ΔT Δ Q = c ΔT (c : seziische Wärekaazität, [ c ] J ) [Gl ] k K Voluenänderungsarbeit W Wir betrachten einen Kolben, der in eine Zylinder u die Strecke ds verschoben wird. Die Arbeits-Zuuhr bei Verschieben des Kolbens ist dann dw = F d s it F = A dw = Ad s Wir haben hier so gerechnet, als sei i Außenrau der Druck =0! Wenn außen der norale Lutdruck herrscht, dann wird ein Teil der Krat und ein Teil der Arbeit durch den Lutdruck augebracht. Für die Energiebilanz (z.b. bei eine koletten Zyklus eines Motors) sielt dies letzten Endes keine Rolle, da bei Rückweg die entsrechende Arbeit vo Syste wieder nach außen abgegeben wird. Nutz Ausnahe: Wenn ein Phasenübergang (z.b. Schelzen oder Verdaen) stattindet, dann kann die Teeratur trotz Wärezuuhr oder Wäreabuhr konstant bleiben. Man sricht dann von latenter Wäre! hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 3/5
4 Wird der Kolben in Krat-Richtung bewegt, dann wird das Voluen wird u Ad s kleiner, dv = Ad s F ds Die Arbeit dw = Ad s ür eine ininitesiale Voluenänderung ist deshalb dw = dv dv dw = dv V [Gl ] Die Arbeit bei einer Zustandsänderung, (z.b. bei Koression V V it V < V ) ergibt sich dann durch Integration: W V ( ) = V dv V Weg b Weg a Arbeit a [Gl ] V V V Der Betrag der Voluenänderungsarbeit ist also gleich der Fläche unter (V)-Kurve! W = Fläche unter (V)-Kurve Die Arbeit ist eine Prozessgröße, sie ist abhängig vo Weg (V) i -V-Diagra. Z.B. ist in der obigen Skizze die Arbeit au Weg a verschieden von der Arbeit au Weg b, W W! a b Aus der Vorzeichenkonvention ergibt sich : Bei der Koression ist W ositiv: V > V W > 0 Energiezuuhr! Bei der Exansion ist W negativ: V < V W < 0 Energieabgabe! dw = dv ist die Voluenänderungsarbeit. Die sogenannte technische Arbeit (auch Wellenarbeit, engl. shatwork ) ist deiniert als d W t = V d. Selbstverständlich ist auch die Voluenänderungsarbeit Arbeit i Sinne der Technik. Bei oenen Systeen ist es aber ot günstiger, anstatt der Fläche zur V-Achse ( dw = dv ) die Fläche zur -Achse ( d W t = V d ) zu betrachten. Da wir in der Physikvorlesung zunächst geschlossene Systee behandeln, werden wir dies nicht weiter vertieen. Mehr über W t können Sie in eine Buch oder einer Vorlesung über Technische Therodynaik (z.b. i Studiengang MB) lernen! hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 4/5
5 5.4.3 Der. Hautsatz der Therodynaik 84 erkannte Julius Robert Mayer (geb in Heilbronn, gest in Heilbronn) die Äquivalenz von echanischer Arbeit und Wäre, d.h. er betrachtete als erster die Wäre als eine Energieor. 845 bestite Robert Mayer das echanische Wäreäquivalent und orulierte das Gesetz von der Erhaltung der Energie. Als ersten Hautsatz der Therodynaik bezeichnen wir heute diese Erweiterung des Energiesatzes der Mechanik, die die innere Energie U des Systes it einbezieht. Energieerhaltung,.Hautsatz der Therodynaik : I abgeschlossenen Syste ist der Gesatbetrag der Energie konstant. Energie kann nicht erzeugt und nicht vernichtet werden. Energie kann lediglich von einer in eine andere For ugewandelt werden. Z.B. können Wäreenergie und echanische Energie wechselseitig ineinander ugewandelt werden. Die Gesatenergie eines abgeschlossenen therodynaischen Systes ist konstant Energie kann aber z.b. als Wäre oder Arbeit zwischen Teilen des Systes ausgetauscht werden Teil Teil Austausch von Arbeit/Wäre zwischen den Teilen Es gibt kein Peretuu Mobile. Art (Ein Peretuu Mobile wäre eine Maschine, die Energie aus de Nichts erzeugt) Abgeschl. Syste Wird eine Syste bei eine Prozess (Anangszustand Endzustand ) Energie zugeührt bzw. entnoen so verändert sich die innere Energie U des Änderung der de Syste zugeührte Systes. Die Energie- inneren Energie = Arbeit + Wäre Zuuhr/Abgabe kann erolgen in For von Wäre Q Voluenänderungsarbeit W Wir können diese Kernaussage des ersten Hautsatzes in verschiedener Weise durch Foreln beschreiben: Zugeührte Wäre oder Arbeit vergrößert, abgeührte Wäre oder Arbeit verkleinert die innere Energie: U U = Qzu Qab + Wzu Wab [Gl ] Wenn wir die Vorzeichenkonvention beachten, dann üssen die zu-/abgeührte Energiegrößen nicht getrennt augeührt werden. Ob Energie ins Syste hinein oder heraus ließt ergibt sich ja bereits aus de Vorzeichen von Q bzw. W : U U = Q + W [Gl ] hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 5/5
6 Alternativ können wir eine (endliche) Veränderung der inneren Energie it Δ U, die zugeührte/abgeührte Wäre bzw. Arbeit it Δ Q bzw. Δ W bezeichnen: Δ U = ΔQ + ΔW [Gl ] Häuig ist es nützlich, zunächst ininitesial kleine Änderungen der inneren Energie zu betrachten, die durch ininitesial 3 kleine Zuuhr/Abuhr von Wäre bzw. Arbeit bewirkt werden: d U = dq + dw [Gl ] Wenn an nun noch die Voluenänderungsarbeit durch dw = dv ausdrückt, erhält an du = dq dv [Gl ] Wärekaazität Eine Energiezuuhr (als Wäre) ührt zu einer Erhöhung der inneren Energie U und dait zu einer Teeraturerhöhung Die Teeraturerhöhung ist roortional zur zugeührten Energie Als Wärekaazität wird bezeichnet die dq Energiezuuhr / Teeraturänderung, C = [Gl ] d T Die Wäre, die zu einer gewissen Teeraturveränderung zu- oder abgeührt werden uss, berechnet sich dezuolge zu dq = C dt oder Q = C ΔT Δ oder Q C ( T ) = [Gl ] T Da die Wäre (und dait auch die Wärekaazität) von der Stoenge bzw. der Masse abhängen, können wir diese Gleichungen wahlweise it der Wärekaazität C des Systes oder it der seziischen Wärekaazität c bzw. der olaren Wärekaazität C schreiben: Q = C ( T T ) Q c ( T T ) Q = n C ( T ) = [Gl ] T it C Wärekaazität (eines Körers, des Systes) c seziische Wärekaazität (eines Materials), ro kg! C olare Wärekaazität (eines Materials), ro Mol! 3 d U ist das (totale oder vollständige) Dierential der Zustandsgröße U. Wäre Q und Arbeit W sind aber (wegabhängige) Prozessgrößen; sie haben nur unvollständige Dierentiale. Mit dq und dw sind also keinesalls totale Dierentiale geeint. In anchen Büchern wird dies ~ unterschieden durch die Schreibweise, z.b. d U = δq + δw, d U = d Q + ~ d W etc.. Au diese Feinheiten wird hier verzichtet. hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 6/5
7 Bei größeren Teeraturdierenzen uss berücksichtigt werden, dass die Wärekaazität (bzw. seziische Wärekaazität) von der Teeratur abhängt (vergl. Ka !). Die obigen Foreln düren dann nur noch ür (ininitesial) kleine Teeraturveränderungen angewendet werden: dq = C dt. Die gesate Wäre zur Teeraturerhöhung von T au T ergibt sich dann durch Integration: = dq = C( T ) Q dt [Gl ] T T Wärekaazität idealer Gase Gase dehnen sich bei Erwärung noralerweise sehr stark aus. Wird eine Gas Wäre zugeührt, so kot es darau an, ob sich das Gas in eine Geäß it este Voluen beindet oder ob der Druck konstant gehalten wird und sich das Voluen während der Wärezuuhr vergrößert. I letzteren Falle wird die Energiezuuhr durch Wäre nicht nur die innere Energie (und die Teeratur) vergrößern, sondern es wird auch noch Voluenänderungsarbeit verrichtet. Bei Gasen uss deshalb zwischen Wärekaazität C V bei konstante Voluen (Index V, Ka ) und Wärekaazität C bei konstante Druck (Index, Ka ) unterschieden werden. In Festkörern und Flüssigkeiten ist die Wäreausdehnung (und dait der erwähnte Anteil der Voluenänderungsarbeit) so klein, dass zwischen C und C V nicht unterschieden werden uss! Wärekaazität idealer Gase bei konstante Voluen: C V, C, c V Ein Gas, das sein Voluen nicht verändert, verrichtet wegen dw = dv keine Voluenänderungsarbeit. Die de Gas zugeührte Wäreenergie wird also vollständig in die innere Energie gesteckt und ührt zur entsrechenden Teeraturerhöhung. V = const. keine Arbeit d W = 0 00 % der Wäreenergie ür Teeratur-Erhöhung! Änderung der inneren Energie: d U d Q + dw. = V = const d U = d Q = n C dt [Gl ] =. Dabei ist C die olare Wärekaazität bei konstante Voluen. Aus der kinetischen Theorie des idealen Gases ergibt sich ür die innere Energie U = n RT, ür d U also du = n R dt. Durch Vergleich it [Gl ] ergibt sich ür alle (idealen) Gase die V const olare Wärekaazität bei konst. Vol. C : C = R [Gl ] hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 7/5
8 Molekülor C Bs. (geessene Werte) 3 J -atoig 3 R =,47 He:,47 J/(ol K) ol K -atoig, J 5 starr 5 R = 0,79 Lut: 0,77 J/(ol K) ol K -atoig, J 7 9,0 schwingend 7 R = Cl : 5,74 J/(ol K) ol K ehratoig, starr 6 J R 4,94 CH 4 : 6,9 J/(ol K) ol K 6 = Enthalie H Wie deinieren zunächst rein orell eine neue energetische Zustandsgröße, die Enthalie H (bzw. H die seziische Enthalie h = ): Enthalie : H = U + V [Gl ] Beachten Sie:. Die Enthalie H ist geäß dieser Deinition eine Zustandsgröße, weil auch die innere Energie U, der Druck und das Voluen V Zustandsgrößen sind.. Die Deinition H = U + V ist nur öglich, weil U und V die gleiche Einheit (Joule) U = J, [ V ] = J haben: [ ] (Dies bedeutet noch nicht autoatisch, dass jede in dieser Weise gebastelte Zustandsgröße auch ür irgend etwas nützlich wäre!) Es zeigt sich, dass die Betrachtung der Enthalie z.b. nützlich ist bei Prozessen, bei denen Energiezuuhr durch Wäre die Teeratur nicht erhöht (Schelzen, Verdaen, latente Wäre ) oder nicht ausschließlich die Teeratur bzw. innere Energie erhöht (Erwären eines Gase bei konst. Druck, Vol.-Ausdehnung, ein Teil der Energie Ausdehnungsarbeit!) Wir betrachten dazu die Änderung der Enthalie d H, d.h. das totale Dierential von H ( U, V, ) : Totales Dierential von H = H ( U, V, ) (siehe Mathe-Buch oder Vorl.!): H H H d H = du + dv + d U V Für H = U + V ergibt sich dait d H = du + dv + V d [Gl ] hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 8/5
9 Nach de ersten Hautsatz ist d U = dq + dw du = d Q dv Dait wird d H zu d H = dq dv + dv + V d d H = dq + V d [Gl ] Wenn wir jetzt einen Prozess betrachten, bei de eine Gas bei konstante Druck ( = const.!) Wäre zugeührt wird, dann gilt: d H dq + V d. = = const Die Enthalie-Änderung ist also gleich der bei konstante Druck zugeührten Wäre: d H = dq = const. [Gl ] Gewichtskrat sorgt ür konstanten Druck! Arbeit W Q Wir ühren de Syste also Energie in For von Wäre zu. Dies erhöht die innere Energie; i Beisiel erhöht sich die Teeratur des Gases. Allerdings ist die Erhöhung der inneren Energie geringer als die Wärezuuhr, da sich das Gas ausdehnt und dabei wieder Energie in For von Voluenänderungsarbeit nach außen abgibt! Isobare Wärezuuhr: Wärezuuhr erhöht die Enthalie innere Energie Voluenänderungsarbeit Phasenuwandlungen Übergänge zwischen den Aggregatzuständen est/lüssig/gasörig (Schelzen / Erstarren, Verdaen / Kondensieren, Subliieren / Desubliieren) sowie Übergänge zwischen verschiedenen Modiikationen eines Festkörers werden Phasenuwandlungen genannt. Bei diesen Übergängen werden zu Teil erhebliche Energien zu- oder abgeührt. Z.B. werden benötigt bei 0 C zu Schelzen von Eis zu Wasser 335 kj/kg bei 00 C zu Verdaen von Wasser 57 kj/kg Dagegen braucht an nur 48 kj/kg u lüssiges Wasser von 0 C au 00 C zu erhitzen. Bei Phasenübergängen wird Wäre zu- oder abgeührt, ohne dass sich die Teeratur ändert. Diese Wäre wird deshalb latente Wäre genannt (Beisiel: Ein Latentwäreseicher seichert Energie durch Phasenuwandlung bestiter Salze und kann u.u. eine Standheizung i Auto ersetzen). Die Wärezuuhr, z.b. bei Schelzen, geschieht bei konstante Druck (und konstanter Teeratur), sie erhöht also direkt die Enthalie des Systes. hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 9/5
10 kj Flüssiges Wasser bei 0 C hat eine u Δh S = 335 höhere seziische Enthalie als Eis bei 0 C. kg Δ hs ist die seziische Schelzenthalie kj Wasserda bei 00 C hat eine u Δh V = 57 höhere sez. Enthalie als Wasser bei 00 C. kg Δ hv ist die seziische Verdaungsenthalie Ergänzung: Drosselrozess 4, Joule-Thoson-Eekt Ein Gas werde an einer Drossel vo Druck au den kleineren Druck entsannt. Der Vorgang soll adiabat (d.h. ohne Wäreaustausch it der Ugebung) ablauen. Als Drossel kann ein Diahraga, ein Ventil oder eine Kaillare verwendet werden. Vor und hinter der Drossel wird dabei ein konstanter Druck aurecht erhalten. Bei realen Gasen beobachtet an i Gegensatz zu idealen Gas dann eine Teeraturänderung (+ oder -!). Die Erklärung daür sind die Anziehungskräte zwischen den Molekülen (siehe Kaitel 5.3., van der Waalssche Zustandsgleichung!), die bei der Exansion überwunden werden üssen. Die Arbeit, die dazu gebraucht wird, verringert die innere Energie. Die Teeraturänderung kann it Hile der van der Waalsschen Gleichung berechnet werden. Oberhalb der sogenannten Inversionsteeratur a Ti = (a, b : Konstanten in der van-der-waals-gleichung) erhöht sich die Teeratur; Rb unterhalb der Inversionsteeratur tritt eine Teeraturerniedrigung au. Der Joule-Thoson-Eekt besitzt große raktische Bedeutung in der Kältetechnik, insbesondere bei der Lutverlüssigung nach de Linde-Verahren. Nach de. Hautsatz ist die Änderung der inneren Energie Δ U (adiabatischer Prozess, keine Wäre!) gleich der Dierenz der vo Syste bei augenoenen ( W = V ) und der bei abgegebenen Voluenarbeit ( W = V ): Δ U = U U = V V. Daraus olgt U + = + H =! V U V H Bei adiabaten Drosselrozess bleibt die Enthalie H konstant! 4 Da bei eine adiabaten Drosselrozess die Enthalie konstant bleibt wurde die Enthalie auch Drosselunktion genannt. hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 0/5
11 Wärekaazität idealer Gase bei konstante Druck: C, C, c I letzten Kaitel wurde gezeigt [Gl ], dass die Wärezuuhr bei este Druck gleich der Veränderung der Enthalie des Systes ist: d H = dq = const. Diese Wäreenge hängt über die Wärekaazität bei konstante Druck C (olare WK: C, seziische WK: c ) it der Teeraturveränderung zusaen: d H = dq = n C dt = const. = c dt Nach [Gl ] ist d H = du + dv + V d. Bei isobaren Prozessen ällt der letzte Ter weg. n C d T = du + dv Da die innere Energie U eine Zustandsgröße ist und nur von der Teeratur T abhängt, kann die Veränderung von U bei isobaren Prozess auch durch einen gedachten isochoren Übergang zwischen den gleichen Teeraturen berechnet werden! zwischen gleichen Teeraturen: ΔU (isochor) = ΔU (isobar) ΔU Arbeit ΔU U(T ) U(T ) V Mit du = n C dt erhält an dann eine Beziehung zwischen den Wärekaazitäten bei konstante Druck und konstante Voluen: n C d T = n C dt + dv n ( C C ) d T = dv ( C C ) dv = [Gl ] n dt dv Da > 0 ist, olgt daraus: dt C > C. Wärezuuhr bei konstante Voluen erhöht die innere Energie (und dait die Teeratur). Bei isobarer Wärezuuhr dagegen wird ein Teil der Wäreenergie in Voluenänderungsarbeit ugewandelt und vo Syste wieder abgegeben. Man braucht deshalb ehr Energie ür die gleiche Teeraturerhöhung, die Wärekaazität C ist größer! hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. /5
12 U die in [Gl ] autretende Ableitung V Ideales Gas: = nr T n dv n V = R T = dt Einsetzen in [Gl ] ergibt n ( C C ) = + R n R dv dt zu berechnen, betrachten wir ein Ideales Gas: [Gl ] C = C + R [Gl ] Die olaren Wärekaazitäten bei konstante Druck und konstante Voluen unterscheiden sich gerade u eine Einheit der universellen Gaskonstanten R. Mit Hile der Anzahl der Freiheitsgrade (siehe Ka. 5.3) kann auch C durch R.dargestellt werden: C = R C = R + R = + R [Gl ] Das Verhältnis ( Kaa ) der Wärekaazitäten bei konstante Druck und konstante Voluen C C c κ = = = CV C cv heißt Adiabatenexonent (oder auch Isentroenexonent ) und ist eine wichtige Stoeigenschat. Bei Verhältnis sielt es natürlich keine Rolle, ob an die Wärekaazität, die olare (ro Mol!) Wärekaazität oder die seziische (ro kg!) Wärekaazität verwendet. C κ = C + R = R = + [Gl ] Molekülor κ =+ Bs. (ge. Werte κ) -atoig 3,67 He:,67 -atoig, starr -atoig, schwingend 5,40 7,9 Lut:,40 Cl :,35 ehratoig, starr 6,33 CH 4 :,3 hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. /5
13 5.4.6 Wärekaazität bei Festkörern Dulong-Petitsches-Gesetz Bei Festkörern sitzen die Atoe an esten Gitterlätzen und können nur Schwingungen u die Ruhelage i Kristall ausühren. Mit den 3 Schwingungsrichtungen (x,y,z) erhalten wir = 6 Freiheitsgrade. Aus diese einachen Modell ergibt sich die olare Wärekaazität eines Festkörers zu 6 J C = R = 4,94 (Dulong-Petitsches-Gesetz) [Gl ] ol K Anerkung: In Festkörern ist die Wäreausdehnung so klein, dass zwischen C und C V nicht dv unterschieden werden uss: ( C C ) = = γ { V 0 n dt n Tatsächlich ist die Wärekaazität eines realen Festkörers eist kleiner als der Wert nach Dulong-Petit. Bei tieen Teeraturen ( T 0 ) strebt die Wärekaazität sogar gegen Null ( C 0). Bei Teeraturen, die groß gegen die sogenannte Debye-Teeratur T D (Materialkonstante ) sind, geht die Wärekaazität der Festkörer asytotisch gegen den Dulong- T Petit-Wert C = 3R. Die olare Wärekaazität C hängt lediglich vo Verhältnis ab. Je größer T D, desto langsaer nähert sich die Wärekaazität de Grenzwert (siehe dazu auch nächstes Kaitel oder Physikbuch, Kaitel Festkörerhysik!). Beisiele: Pb: T D = 88 K, Cu: T D = 345 K, Al: T D = 48 K, Diaant: T D = 860 K, = 3α T D (Grahit) hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 3/5
14 5.4.7 Teeraturabhängigkeit der seziischen Wärekaazität Nicht nur die Wärekaazität der Festkörer sondern auch die der Gase ist von der Teeratur abhängig (Abb. b). I Kaitel 5.3 hatten wir geunden, dass die Wärekaazität wesentlich durch die Anzahl der Freiheitsgrade bestit wird. Wie kann sich aber die Anzahl der Freiheitsgrade it der Teeratur ändern? Als Freiheitsgrad zählt jede Energieor, die a therodynaischen Energieaustausch teilnit. Bei tieen Teeraturen wird die ittlere therische Energie E = kt natürlich kleiner, d.h. i Mittel werden die Translations- und Rotationsbewegungen langsaer und die Alitude der Schwingungen wird kleiner. In der klassischen Physik gibt es aber keine Erklärung daür, dass sich die Zahl der Freiheitsgrade verkleinert! Z.B. sollte ein Molekül, das bei Zierteeratur rotieren kann, auch bei tieen Teeraturen noch rotieren können (nur eben langsaer!). Die Wärekaazität der Gase scheint sich in Stuen zu ändern (Abb. a, scheatisch). Bei tieen Teeraturen (unter ca. 90 K) benit sich z.b. das H -Molekül wie ein (einatoiges!) Edelgas = 3 + 0, bei Zierteeratur dagegen wie ein -atoiges, ohne Rotationsreiheitsgrade ( ) starres (Hantel-) Molekül (Abb. c) it Rotationsreiheitsgraden ( = 3 + ). Die Teeraturabhängigkeit der seziischen Wärekaazität der Gase und Festkörer kann ohne Quantenhysik nicht erklärt werden! Bei tieen Teeraturen nit die Anzahl der Freiheitsgrade ab! Man sagt die Freiheitsgrade rieren ein E E 4 In der Quantenhysik können Elektronen, Atoe, Moleküle etc. nicht ehr beliebige Energien annehen. Erlaubt sind vielehr nur diskrete Energiewerte (z.b. die Energiestuen, die ein Elektron in der Atohülle annehen kann). Diese Einschränkung der öglichen Energiewerte gilt auch ür Schwingungs- und Rotationszustände eines Moleküls. ΔE E 3 E E hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 4/5
15 Ein Energieniveau it einer u Δ E größeren Energie kann bei therodynaischen Energieaustausch (durch Stöße) nur angeregt werden, wenn die ittlere therische Energie E = kt in der Größenordnung von Δ E liegt. Freiheitsgrad ist eingeroren alls kt << ΔE oen alls kt >> ΔE Au Grund der Geschwindigkeits- und Energieverteilung nit die seziische Wärekaazität allerdings nicht schlagartig zu. Die Anregung eines Freiheitsgrades wird dadurch über einen größeren Teeraturbereich verteilt, bei Wassersto z.b. erstreckt sich der Übergangsbereich bei der Anregung der Rotation über den Teeraturbereich von ca. 80 K bis ca. 50 K. hysik_5_4_erster_hs.doc, Pro. Dr. K. Rauschnabel, HHN, S. 5/5
Musterlösung Übung 3
 Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases. f=5 Translation + Rotation. f=7 Translation + Rotation +Vibration. Wiederholung
 1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
20. Kinetische Gastheorie
 Wärelehre Kinetische Gastheorie 0. Kinetische Gastheorie... behandelt ideale Gase, d.h., die Gasteilchen verhalten sich wie elastische Kugeln it vernachlässigbare Eigenvoluen.! 0.. Gasdruck und Zustandsgleichung
Wärelehre Kinetische Gastheorie 0. Kinetische Gastheorie... behandelt ideale Gase, d.h., die Gasteilchen verhalten sich wie elastische Kugeln it vernachlässigbare Eigenvoluen.! 0.. Gasdruck und Zustandsgleichung
3.3 Wärme als Energieform
 3.3 Wäre als Energiefor Erinnere: Herleitung der Zustandsgleichung p V=n R T hatten wir die Teperatur eingeführt als Basisgröße die proportional zur Molekülenergie sein soll: 1 3 ε kin = u = kt d.h.: zur
3.3 Wäre als Energiefor Erinnere: Herleitung der Zustandsgleichung p V=n R T hatten wir die Teperatur eingeführt als Basisgröße die proportional zur Molekülenergie sein soll: 1 3 ε kin = u = kt d.h.: zur
Physik I TU Dortmund WS2017/18 Gudrun Hiller Shaukat Khan Kapitel 6
 Physik I U Dortmund WS07/8 Gudrun Hiller Shaukat Khan Kaitel 6 Seziische Wärme von Gasen Bei einatomigen Gasen (z.b. He): Bei zweiatomigen Gasen (z.b. N, O ): N k A Freiheitsgrade ür die kinetische Energie
Physik I U Dortmund WS07/8 Gudrun Hiller Shaukat Khan Kaitel 6 Seziische Wärme von Gasen Bei einatomigen Gasen (z.b. He): Bei zweiatomigen Gasen (z.b. N, O ): N k A Freiheitsgrade ür die kinetische Energie
Thermodynamik (Wärmelehre) II Wärmeenergie
 Physik A L25 (06.12.2012) Therodynaik (Wärelehre) II Wäreenergie Wäreenge und Wärekaazität Energieerhaltung bei therodynaishen Systeen 1. Hautsatz der Therodynaik Arbeit und innere Energie bei Gasen 1
Physik A L25 (06.12.2012) Therodynaik (Wärelehre) II Wäreenergie Wäreenge und Wärekaazität Energieerhaltung bei therodynaishen Systeen 1. Hautsatz der Therodynaik Arbeit und innere Energie bei Gasen 1
Thermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden.
 Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Hochschule Heilbronn Technik Wirtschaft Informatik Heilbronn University Institut für math.-naturw. Grundlagen
 Technik Wirtschaft Inforatik Institut für ath-naturw Grundlagen Versuch : Kalorietrie 1 Aufgabenstellung Bestiung der Wärekapazität eines Kalorieters Bestiung der spezifischen Wärekapazität Festkörpern
Technik Wirtschaft Inforatik Institut für ath-naturw Grundlagen Versuch : Kalorietrie 1 Aufgabenstellung Bestiung der Wärekapazität eines Kalorieters Bestiung der spezifischen Wärekapazität Festkörpern
Der Joule-Thomson Effekt
 Der Joule-hoson Effekt Einleitung Der Joule-hoson Effekt bezeichnet die eeraturänderung eines realen Gases bei einer adiabatischen Voluenveränderung. Der Effekt wird großtechnisch zu Beisiel i Linde- Verfahren
Der Joule-hoson Effekt Einleitung Der Joule-hoson Effekt bezeichnet die eeraturänderung eines realen Gases bei einer adiabatischen Voluenveränderung. Der Effekt wird großtechnisch zu Beisiel i Linde- Verfahren
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
1u = A r = Die relativen Atom-, Molekül- und Ionenmassen. atomare Masseneinheit 1u. relative Atommasse A r :
 Die relativen Ato-, Molekül- und Ionenassen atoare Masseneinheit u: u Masse von Kohlenstoffato C u,6655 7 kg relative Atoasse A r : Masse eines Atos A r atoare Masseneinheit u relative Molekülasse M r
Die relativen Ato-, Molekül- und Ionenassen atoare Masseneinheit u: u Masse von Kohlenstoffato C u,6655 7 kg relative Atoasse A r : Masse eines Atos A r atoare Masseneinheit u relative Molekülasse M r
Die Maxwell-Boltzmann-Verteilung
 Die Maxwell-Boltzann-Verteilung Sebastian Meiss 5. Oktober 8 Mit der Maxwell-Boltzann-Verteilung kann an Aussagen über die Energie- bzw. Geschwindigkeitsverteilung von Teilchen in eine Syste beschreiben.
Die Maxwell-Boltzann-Verteilung Sebastian Meiss 5. Oktober 8 Mit der Maxwell-Boltzann-Verteilung kann an Aussagen über die Energie- bzw. Geschwindigkeitsverteilung von Teilchen in eine Syste beschreiben.
Physikalische Chemie Physikalsiche Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/10 5. Zustandsfunktionen Idealer und Realer Gase. ZustandsÄnderungen
 Prof. Dr. Norbert Ham 1/10 5. Zustandsfunktionen Idealer und Realer Gase ZustandsÄnderungen Die rennung zwischen unserem System und der ÅUmweltÇ wird durch eine Wand realisiert. WÄnde kånnen unterschiedliche
Prof. Dr. Norbert Ham 1/10 5. Zustandsfunktionen Idealer und Realer Gase ZustandsÄnderungen Die rennung zwischen unserem System und der ÅUmweltÇ wird durch eine Wand realisiert. WÄnde kånnen unterschiedliche
25. Adiabatische Expansion eines idealen Gases 1
 25. Adiabatische Exansion eines idealen Gases 1 25. ADABASHE EXPANSON ENES DEALEN GASES 1. Aufgabe Für Luft als annähernd ideales Gas sollen sowohl die Molwäre bei konstante Druck, d.h.,, als auch das
25. Adiabatische Exansion eines idealen Gases 1 25. ADABASHE EXPANSON ENES DEALEN GASES 1. Aufgabe Für Luft als annähernd ideales Gas sollen sowohl die Molwäre bei konstante Druck, d.h.,, als auch das
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seminar Thermische Abfallbehandlung - Veranstaltung 4 - Dampfkraftprozesse
 Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
Institut für Abfallwirtschaft und Altlasten, TU-Dresden Seinar Therische Abfallbehandlung - Veranstaltung 4 - Dapfkraftprozesse Dresden, 09. Juni 2008 Dipl.- Ing. Christoph Wünsch, Prof. Dr.- Ing. habil.
Aufgaben zum Stirlingschen Kreisprozess Ein Stirling-Motor arbeite mit 50 g Luft ( M= 30g mol 1 )zwischen den Temperaturen = 350 C und T3
 Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 8 Lösungsvorschlag
 T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
4.6 Hauptsätze der Thermodynamik
 Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Beispiel: Gegeben ist folgender Hebel mit den Kräften F
 Gynasiu Münchberg Grundwissen Physik Jahrgangsstufe 8 (G8) Stand: Juli 007 Seite von 6. Energie Hebel Thea Erklärung und Beispiele Drehoent = Kraft Hebelar, kurz: M = F a (dabei wird nur die Koponente
Gynasiu Münchberg Grundwissen Physik Jahrgangsstufe 8 (G8) Stand: Juli 007 Seite von 6. Energie Hebel Thea Erklärung und Beispiele Drehoent = Kraft Hebelar, kurz: M = F a (dabei wird nur die Koponente
1. Thermodynamische Potentiale, Maxwellgleichungen
 69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik -. Hauptsatz der Thermodynamik - Prof. Dr. Ulrich Hahn WS 2008/09 Energieerhaltung Erweiterung des Energieerhaltungssatzes der Mechanik Erfahrung: verschiedene
Physik III im Studiengang Elektrotechnik -. Hauptsatz der Thermodynamik - Prof. Dr. Ulrich Hahn WS 2008/09 Energieerhaltung Erweiterung des Energieerhaltungssatzes der Mechanik Erfahrung: verschiedene
Zur Thermodynamik des idealen Gases (GK Physik 1)
 Zur hermodynamik des idealen Gases (GK Physik 1 Zusammenfassung im Hinblick auf Prozesse. Reinhard Honegger, im Januar 2012. 1 Grundbegriffe 1.1 Zustandsgleichung = Ideale Gasgleichung Druck, olumen, emeratur
Zur hermodynamik des idealen Gases (GK Physik 1 Zusammenfassung im Hinblick auf Prozesse. Reinhard Honegger, im Januar 2012. 1 Grundbegriffe 1.1 Zustandsgleichung = Ideale Gasgleichung Druck, olumen, emeratur
GPH2 Thermodynamik. 27. September Dieser Entwurf ist weder vollständig oder fehlerfrei noch ein offizielles Script zur Vorlesung.
 GPH2 Thermodynamik Dieser Entwurf ist weder ollständig oder fehlerfrei noch ein offizielles Scrit zur Vorlesung. Für Anregungen und Kritik: mail@sibbar.de 27. Setember 2004 GPH2 Thermodynamik Seite 2 on
GPH2 Thermodynamik Dieser Entwurf ist weder ollständig oder fehlerfrei noch ein offizielles Scrit zur Vorlesung. Für Anregungen und Kritik: mail@sibbar.de 27. Setember 2004 GPH2 Thermodynamik Seite 2 on
8.1. Kinetische Theorie der Wärme
 8.1. Kinetische Theorie der Wärme Deinition: Ein ideales Gas ist ein System von harten Massenpunkten, die untereinander und mit den Wänden elastische Stöße durchühren und keiner anderen Wechselwirkung
8.1. Kinetische Theorie der Wärme Deinition: Ein ideales Gas ist ein System von harten Massenpunkten, die untereinander und mit den Wänden elastische Stöße durchühren und keiner anderen Wechselwirkung
2. Klausur zur Vorlesung Einführung in die physikalische Chemie für Lehramtskandidaten Modul 4, Wintersemester 05/06
 . Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
. Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
(b) Schritt I: freie adiabatische Expansion, also ist δw = 0, δq = 0 und damit T 2 = T 1. Folglich ist nach 1. Hauptsatz auch U = 0.
 3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
T 1 T T Zustandsverhalten einfacher Systeme (Starthilfe S ) - Prozess und Zustandsänderung. Prozess (Q 12
 . Zustandserhalten einfacher Systeme (Starthilfe S. 9-38) - Prozess und Zustandsänderung Zustandsänderung δq Prozess (Q ) - thermodynamisch einfache Systeme reiner Stoff feste flüssige damfförmige Phase
. Zustandserhalten einfacher Systeme (Starthilfe S. 9-38) - Prozess und Zustandsänderung Zustandsänderung δq Prozess (Q ) - thermodynamisch einfache Systeme reiner Stoff feste flüssige damfförmige Phase
1. Geschwindigkeit von Elektronen in Drähten (2+2+2)
 Lösungen zur Übungen zur Physik (Elektrodynaik) SS 5 6 Übungsblatt 955 Bearbeitung bis Mi 555 Geschwindigkeit on Elektronen in Drähten (++) Ein Kupferdraht it de Durchesse durchflossen Berechnen Sie a)
Lösungen zur Übungen zur Physik (Elektrodynaik) SS 5 6 Übungsblatt 955 Bearbeitung bis Mi 555 Geschwindigkeit on Elektronen in Drähten (++) Ein Kupferdraht it de Durchesse durchflossen Berechnen Sie a)
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
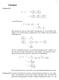 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
Chemische Grundgesetze
 Björn Schulz Berlin,.10.001 p.1 Cheische Grundgesetze Gesetz von der Erhaltung der Masse (Lavoisier 1785) Abbrennen einer Kerze Massenverlust geschlossenes Syste Eisennagel rostet Massenzunahe konstante
Björn Schulz Berlin,.10.001 p.1 Cheische Grundgesetze Gesetz von der Erhaltung der Masse (Lavoisier 1785) Abbrennen einer Kerze Massenverlust geschlossenes Syste Eisennagel rostet Massenzunahe konstante
10. Thermodynamik Der erste Hauptsatz Der zweite Hauptsatz Thermodynamischer Wirkungsgrad Der Carnotsche Kreisprozess
 Inhalt 10.10 Der zweite Hauptsatz 10.10.1 Thermodynamischer Wirkungsgrad 10.10.2 Der Carnotsche Kreisprozess Für kinetische Energie der ungeordneten Bewegung gilt: Frage: Frage: Wie kann man mit U Arbeit
Inhalt 10.10 Der zweite Hauptsatz 10.10.1 Thermodynamischer Wirkungsgrad 10.10.2 Der Carnotsche Kreisprozess Für kinetische Energie der ungeordneten Bewegung gilt: Frage: Frage: Wie kann man mit U Arbeit
d) Das ideale Gas makroskopisch
 d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
Mitschrift Thermodynamik
 Mitschrift hermodynamik Herleitung für den Gasdruck Berechnung des oberen Kreisradius d cosϕ dϕ dψ d N eilchen im Gesamtvolumen dn d N Aufschlagswahrscheinlichkeit eines eilchens Fläche df df sinϕ Gesamte
Mitschrift hermodynamik Herleitung für den Gasdruck Berechnung des oberen Kreisradius d cosϕ dϕ dψ d N eilchen im Gesamtvolumen dn d N Aufschlagswahrscheinlichkeit eines eilchens Fläche df df sinϕ Gesamte
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Der Zustand eines Systems ist durch Zustandsgrößen charakterisiert.
 Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Thermodynamik. Kapitel 4. Nicolas Thomas
 Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
3 Der 1. Hauptsatz der Thermodynamik
 3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
Welche Energieformen gibt es? mechanische Energie elektrische Energie chemische Energie thermische oder Wärmeenergie Strahlungsenergie
 Was ist nergie? nergie ist: eine rhaltungsgröße eine Rechengröße, die es eröglicht, Veränderungen zwischen Zuständen zu berechnen eine Größe, die es erlaubt, dass Vorgänge ablaufen, z.b. das Wasser erwärt
Was ist nergie? nergie ist: eine rhaltungsgröße eine Rechengröße, die es eröglicht, Veränderungen zwischen Zuständen zu berechnen eine Größe, die es erlaubt, dass Vorgänge ablaufen, z.b. das Wasser erwärt
1 I. Thermodynamik. 1.1 Ideales Gasgesetz. 1.2 Vereinfachte kinetische Gastheorie. 1.3 Erster Hauptsatz der Thermodynamik.
 1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
Der 1. Hauptsatz. Energieerhaltung:
 Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
Grundlagen der Physik 2 Schwingungen und Wärmelehre
 Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik 21. 05. 2007 Othmar Marti (Universität Ulm) Schwingungen und Wärmelehre 21. 05.
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik 21. 05. 2007 Othmar Marti (Universität Ulm) Schwingungen und Wärmelehre 21. 05.
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische heie Albert-Ludwigs-Universität Freiburg Lösungen zu 5. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 5. M Leiten Sie einen allgeeinen Ausdruck für die Änderung
Institut für hysikalische heie Albert-Ludwigs-Universität Freiburg Lösungen zu 5. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 5. M Leiten Sie einen allgeeinen Ausdruck für die Änderung
E2: Wärmelehre und Elektromagnetismus 4. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 4. Vorlesung 19.04.2018 Heute: - Freiheitsgrade realer Gase - Adiabatische Volumenänderungen - Kurze Einführung in die Quantenmechanik - Freiheitsgrade & Wärmekapazität
E2: Wärmelehre und Elektromagnetismus 4. Vorlesung 19.04.2018 Heute: - Freiheitsgrade realer Gase - Adiabatische Volumenänderungen - Kurze Einführung in die Quantenmechanik - Freiheitsgrade & Wärmekapazität
GRUNDLAGEN DER STRÖMUNGSMECHANIK
 Skriptu zu Fach Luftfahrzeugbau 4.Jahrgang HTL-Eisenstadt GRUNDLAGEN DER STRÖMUNGSMECHANIK Dipl.Ing.Dr.Günter Hacküller 009 Dipl.Ing.Dr.Günter Hacküller e-ail: guenter.hackueller@gx.at Grundlagen der Aerodynaik
Skriptu zu Fach Luftfahrzeugbau 4.Jahrgang HTL-Eisenstadt GRUNDLAGEN DER STRÖMUNGSMECHANIK Dipl.Ing.Dr.Günter Hacküller 009 Dipl.Ing.Dr.Günter Hacküller e-ail: guenter.hackueller@gx.at Grundlagen der Aerodynaik
Aufgaben Kreisprozesse. 1. Ein ideales Gas durchläuft den im V(T)- Diagramm dargestellten Kreisprozess. Es ist bekannt:
 Aufgaben Kreisrozesse. Ein ideales Gas durchläuft den im ()- Diagramm dargestellten Kreisrozess. Es ist bekannt: 8 cm 6 cm 00 K 8MPa MPa a) Geben Sie die fehlenden Zustandsgrößen, und für die Zustände
Aufgaben Kreisrozesse. Ein ideales Gas durchläuft den im ()- Diagramm dargestellten Kreisrozess. Es ist bekannt: 8 cm 6 cm 00 K 8MPa MPa a) Geben Sie die fehlenden Zustandsgrößen, und für die Zustände
Thermodynamik Thermodynamische Systeme
 Thermodynamik Thermodynamische Systeme p... Druck V... Volumen T... Temperatur (in Kelvin) U... innere Energie Q... Wärme W... Arbeit Idealisierung; für die Betrachtung spielt die Temperatur eine entscheidende
Thermodynamik Thermodynamische Systeme p... Druck V... Volumen T... Temperatur (in Kelvin) U... innere Energie Q... Wärme W... Arbeit Idealisierung; für die Betrachtung spielt die Temperatur eine entscheidende
E2: Wärmelehre und Elektromagnetismus 4. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 4. Vorlesung 19.04.2018 Heute: - Freiheitsgrade realer Gase - Adiabatische Volumenänderungen - Kurze Einführung in die Quantenmechanik - Freiheitsgrade & Wärmekapazität
E2: Wärmelehre und Elektromagnetismus 4. Vorlesung 19.04.2018 Heute: - Freiheitsgrade realer Gase - Adiabatische Volumenänderungen - Kurze Einführung in die Quantenmechanik - Freiheitsgrade & Wärmekapazität
Zwei neue Basisgrössen in der Physik
 Nachtrag zur orlesung am vergangenen Montag Zwei neue Basisgrössen in der Physik 9. Wärmelehre, kinetische Gastheorie Temperatur T: Wärme ist verknüpft mit ungeordneter Bewegung der Atome oder Moleküle.
Nachtrag zur orlesung am vergangenen Montag Zwei neue Basisgrössen in der Physik 9. Wärmelehre, kinetische Gastheorie Temperatur T: Wärme ist verknüpft mit ungeordneter Bewegung der Atome oder Moleküle.
m T 1 0.5kg 8.6K = 7535 m T 2 0.5kg 10.4K = 6923 J
 3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Ferienkurs - Experimentalphysik 2
 Technische Universität München Department of Physics Ferienkurs - Experimentalphysik 2 Wärmelehre Qi Li 22/08/2012 Inhaltsverzeichnis Inhaltsverzeichnis 1 Wärmelehre 1 2 Das ideale Gas 1 3 Nullter Hauptsatz
Technische Universität München Department of Physics Ferienkurs - Experimentalphysik 2 Wärmelehre Qi Li 22/08/2012 Inhaltsverzeichnis Inhaltsverzeichnis 1 Wärmelehre 1 2 Das ideale Gas 1 3 Nullter Hauptsatz
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik III (heorie F Statistische Mechanik) SS 17 Prof. Dr. Alexander Mirlin Blatt 2 PD Dr. Igor Gornyi,
Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik III (heorie F Statistische Mechanik) SS 17 Prof. Dr. Alexander Mirlin Blatt 2 PD Dr. Igor Gornyi,
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische heie lbert-ludwigs-universität Freiburg Lösungen zu 7. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 7. L Berechnen Sie aus der olaren Standardentropie des
Institut für hysikalische heie lbert-ludwigs-universität Freiburg Lösungen zu 7. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 7. L Berechnen Sie aus der olaren Standardentropie des
Zur Erinnerung. Wärmetransport durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung. Planck sches Strahlungsgesetz. Stefan-Boltzman-Gesetz
 Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
5.5 Zustandsänderungen idealer Gase
 5.5 Zustandsänderungen idealer Gase iele Gase verhalten sich bei technischen Anwendungen in guter Näherung wie ideale Gase (siehe Ka. 5..3). Bei einem technischen Prozess ändert sich nun der Zustand des
5.5 Zustandsänderungen idealer Gase iele Gase verhalten sich bei technischen Anwendungen in guter Näherung wie ideale Gase (siehe Ka. 5..3). Bei einem technischen Prozess ändert sich nun der Zustand des
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Lösungen zur Übungsklausur Thermodynamik WS 2003/04
 Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
I el U el. P el W V 23+W F23. Musterlösung SS Aufgabe (34 Punkte) a) Energiebilanz für die Kammer A im Zeitintervall t 12 :
 Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Der erste Hauptsatz der TD- Lernziele
 Der erste Hautsatz der D- Lernziele o Einleitung o Zustandgrössen und funktionen o Wärme, Arbeit und Energie o Innere Energie o Der erste Hautsatz der hermodynamik o olumenarbeit o Wärmeübergänge o Die
Der erste Hautsatz der D- Lernziele o Einleitung o Zustandgrössen und funktionen o Wärme, Arbeit und Energie o Innere Energie o Der erste Hautsatz der hermodynamik o olumenarbeit o Wärmeübergänge o Die
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 05. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 05. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 05. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 05. 07. 2007 Klausur Die Klausur
Allgemeines Gasgesetz. PV = K o T
 Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
4. Hamiltonformalismus
 4. Hamiltonormalismus Für die praktische Lösung von Problemen bietet der Hamiltonormalismus meist keinen Vorteil gegenüber dem Lagrangeormalismus. Allerdings bietet der Hamiltonormalismus einen direkten
4. Hamiltonormalismus Für die praktische Lösung von Problemen bietet der Hamiltonormalismus meist keinen Vorteil gegenüber dem Lagrangeormalismus. Allerdings bietet der Hamiltonormalismus einen direkten
II. Wärmelehre. II.2. Die Hauptsätze der Wärmelehre. Physik für Mediziner 1
 II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3Bilanzgleichungen 3.3.1Massenbilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3Bilanzgleichungen 3.3.1Massenbilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Musterlösung Aufgabe 1: Zweikammermesssysatem
 Klausur Thermodynamik I (08.09.2016) 1 Musterlösung Aufgabe 1: Zweikammermesssysatem Teilaufgabe a) Da die Membrane zunächst für Wärme undurchlässig ist, handelt es sich um eine adiabate Zustandsänderung
Klausur Thermodynamik I (08.09.2016) 1 Musterlösung Aufgabe 1: Zweikammermesssysatem Teilaufgabe a) Da die Membrane zunächst für Wärme undurchlässig ist, handelt es sich um eine adiabate Zustandsänderung
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Vorbemerkung. [disclaimer]
![Vorbemerkung. [disclaimer] Vorbemerkung. [disclaimer]](/thumbs/97/130802699.jpg) orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #7 am 18.01.006 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #7 am 18.01.006 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
Leseprobe. Günter Cerbe, Gernot Wilhelms. Technische Thermodynamik. Theoretische Grundlagen und praktische Anwendungen ISBN:
 Leseprobe Günter Cerbe, Gernot Wilhelms Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen ISBN: 978-3-446-4464-7 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-4464-7
Leseprobe Günter Cerbe, Gernot Wilhelms Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen ISBN: 978-3-446-4464-7 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-4464-7
Thermodynamik (Wärmelehre) III kinetische Gastheorie
 Physik A VL6 (07.1.01) Thermodynamik (Wärmelehre) III kinetische Gastheorie Thermische Bewegung Die kinetische Gastheorie Mikroskopische Betrachtung des Druckes Mawell sche Geschwindigkeitserteilung gdes
Physik A VL6 (07.1.01) Thermodynamik (Wärmelehre) III kinetische Gastheorie Thermische Bewegung Die kinetische Gastheorie Mikroskopische Betrachtung des Druckes Mawell sche Geschwindigkeitserteilung gdes
XII.1 Van der Waals-Gleichung Grundlage bei der Betrachtung idealer Gase war die Idealgasgleichung. p V = R T
 XII. Reale Gase In Kaitel XI hatten wir zwei wesentliche Annahen für ideale Gase geacht: 1. die Moleküle sind Punktassen. es existieren keine zwischenolekularen Kräfte Zude hatten wir bereits festgestellt,
XII. Reale Gase In Kaitel XI hatten wir zwei wesentliche Annahen für ideale Gase geacht: 1. die Moleküle sind Punktassen. es existieren keine zwischenolekularen Kräfte Zude hatten wir bereits festgestellt,
TU-München, Musterlösung. Experimentalphysik II - Ferienkurs Andreas Schindewolf
 TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
Protokoll zum physikalischen Anfängerpraktikum: Adiabatenexponent
 Protokoll zum physikalischen Anfängerpraktikum: Adiabatenexponent Jan Korger, Studiengang Physik-Diplom, Universität Konstanz Sonja Bernhardt, Studiengang Physik-Diplom, Universität Konstanz durchgeführt
Protokoll zum physikalischen Anfängerpraktikum: Adiabatenexponent Jan Korger, Studiengang Physik-Diplom, Universität Konstanz Sonja Bernhardt, Studiengang Physik-Diplom, Universität Konstanz durchgeführt
Zur Erinnerung. p isotherm. Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: Kreisprozesse:
 Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
4.6.5 Dritter Hauptsatz der Thermodynamik
 4.6 Hauptsätze der Thermodynamik Entropie S: ds = dq rev T (4.97) Zustandsgröße, die den Grad der Irreversibilität eines Vorgangs angibt. Sie ist ein Maß für die Unordnung eines Systems. Vorgänge finden
4.6 Hauptsätze der Thermodynamik Entropie S: ds = dq rev T (4.97) Zustandsgröße, die den Grad der Irreversibilität eines Vorgangs angibt. Sie ist ein Maß für die Unordnung eines Systems. Vorgänge finden
Thermodynamik Prof. Dr.-Ing. Peter Hakenesch peter.hakenesch@hm.edu www.lrz-muenchen.de/~hakenesch
 herodynaik _ herodynaik Prof. Dr.-Ing. Peter Hakenesch eter.hakenesch@h.edu www.lrz-uenchen.de/~hakenesch _ herodynaik Einleitung Grundbegriffe 3 Systebeschreibung 4 Zustandsgleichungen 5 Kinetische Gastheorie
herodynaik _ herodynaik Prof. Dr.-Ing. Peter Hakenesch eter.hakenesch@h.edu www.lrz-uenchen.de/~hakenesch _ herodynaik Einleitung Grundbegriffe 3 Systebeschreibung 4 Zustandsgleichungen 5 Kinetische Gastheorie
Physik 2 Hydrologen et al., SoSe 2013 Lösungen 3. Übung (KW 19/20) Carnot-Wärmekraftmaschine )
 3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
FAQ Entropie. S = k B ln W. 1.) Ist die Entropie für einen Zustand eindeutig definiert?
 FAQ Entroie S = k B ln W 1.) Ist die Entroie für einen Zustand eindeutig definiert? Antwort: Nein, zumindest nicht in der klassischen Physik. Es sei an die Betrachtung der Ortsraum-Entroie des idealen
FAQ Entroie S = k B ln W 1.) Ist die Entroie für einen Zustand eindeutig definiert? Antwort: Nein, zumindest nicht in der klassischen Physik. Es sei an die Betrachtung der Ortsraum-Entroie des idealen
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Kinematik und Dynamik eines Massepunktes GK
 Kineatik und Dynaik eines Massepunktes GK Rotation ) Notiere die Gleichung für a) Drehipuls (L=r v) b) Drehoent (M= r F) ) Erhaltungssätze Ohne äußere Krafteinwirkung gilt: a) Energieerhaltung (Evor =
Kineatik und Dynaik eines Massepunktes GK Rotation ) Notiere die Gleichung für a) Drehipuls (L=r v) b) Drehoent (M= r F) ) Erhaltungssätze Ohne äußere Krafteinwirkung gilt: a) Energieerhaltung (Evor =
4 Hauptsätze der Thermodynamik
 I Wärmelehre -21-4 Hauptsätze der hermodynamik 4.1 Energieformen und Energieumwandlung Innere Energie U Die innere Energie U eines Körpers oder eines Systems ist die gesamte Energie die darin steckt. Es
I Wärmelehre -21-4 Hauptsätze der hermodynamik 4.1 Energieformen und Energieumwandlung Innere Energie U Die innere Energie U eines Körpers oder eines Systems ist die gesamte Energie die darin steckt. Es
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 09. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 09. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 09. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 09. 07. 2007 Klausur Die Klausur
Mode der Bewegung, Freiheitsgrade
 Mode der Bewegung, Freiheitsgrade Bewegungsmoden (normal modes of motion) : Jede UNABHÄNGIGE Bewegungsmöglichkeit der Atome (unabhängig: im quantenmechanischen Sinne durch orthogonale Wellenfunktionen
Mode der Bewegung, Freiheitsgrade Bewegungsmoden (normal modes of motion) : Jede UNABHÄNGIGE Bewegungsmöglichkeit der Atome (unabhängig: im quantenmechanischen Sinne durch orthogonale Wellenfunktionen
12 Der erste Hauptsatz der Thermodynamik für geschlossene Systeme
 Der erste Hauptsatz der Thermodynamik für geschlossene Systeme Der erste Hauptsatz ist die thermodynamische Formulierung des Satzes von der Erhaltung der Energie. Er besagt, daß Energie weder erzeugt noch
Der erste Hauptsatz der Thermodynamik für geschlossene Systeme Der erste Hauptsatz ist die thermodynamische Formulierung des Satzes von der Erhaltung der Energie. Er besagt, daß Energie weder erzeugt noch
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene)
 Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Theoretische Physik 4 Thermodynamik und Statistische Physik
 Theoretische Phsik 4 Thermodnamik und Statistische Phsik Prof. Dr. Eric Lutz Universität Erlangen-Nürnberg Inhaltsverzeichnis 1 Thermodnamische Konzete 3 1.1 Was ist Thermodnamik?...........................
Theoretische Phsik 4 Thermodnamik und Statistische Phsik Prof. Dr. Eric Lutz Universität Erlangen-Nürnberg Inhaltsverzeichnis 1 Thermodnamische Konzete 3 1.1 Was ist Thermodnamik?...........................
Die Innere Energie U
 Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Aufgaben zur Experimentalphysik II: Thermodynamik
 Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Wärme. 1. Makroskopische Betrachtung KAPITEL C
 25 KAPITEL C Wärme 1. Makroskopische Betrachtung a) Definition von Wärme Bringt man zwei Systeme mit unterschiedlichen Temperaturen in Kontakt, so wird nach einer Ausgleichszeit ein Gleichgewichtszustand
25 KAPITEL C Wärme 1. Makroskopische Betrachtung a) Definition von Wärme Bringt man zwei Systeme mit unterschiedlichen Temperaturen in Kontakt, so wird nach einer Ausgleichszeit ein Gleichgewichtszustand
Thermodynamik. Thermodynamics. Markus Arndt. Quantenoptik, Quantennanophysik und Quanteninformation Universität Wien January 2008
 Thermodynamik Thermodynamics Markus Arndt Quantenoptik, Quantennanophysik und Quanteninformation Universität Wien January 2008 Die Hauptsätze der Thermodynamik & Anwendungen in Wärmekraft und Kältemaschinen
Thermodynamik Thermodynamics Markus Arndt Quantenoptik, Quantennanophysik und Quanteninformation Universität Wien January 2008 Die Hauptsätze der Thermodynamik & Anwendungen in Wärmekraft und Kältemaschinen
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti.
 (c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
(c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
wegen adiabater Kompression, d.h. kein Wärmeaustausch mit der Umgebung, gilt:
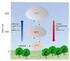 Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Kleine Formelsammlung Technische Thermodynamik
 Kleine Formelsammlung Technische Thermodynamik on Hans-Joachim Kretzschmar, Ingo Kraft überarbeitet Kleine Formelsammlung Technische Thermodynamik Kretzschmar / Kraft schnell und ortofrei erhältlich bei
Kleine Formelsammlung Technische Thermodynamik on Hans-Joachim Kretzschmar, Ingo Kraft überarbeitet Kleine Formelsammlung Technische Thermodynamik Kretzschmar / Kraft schnell und ortofrei erhältlich bei
Versuch: Sieden durch Abkühlen
 ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - Kondensation https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert 1
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - Kondensation https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert 1
