. V2. = p 2 T 1 T 2. Normbedingungen Das Volumen von 1 Mol eines idealen Gases beträgt bei Normbedingungen (1.013 bar, 0 C) Liter.
|
|
|
- Jesko Knopp
- vor 7 Jahren
- Abrufe
Transkript
1 Wäreausdehnung der Gase LMPG_GASE LABA/B Während bei Flüssigkeiten und Festkörpern die Wäreausdehnung auch von der Art des Stoffes abhängt, ist dies bei Gasen nicht der Fall. Bei konstante Druck und einer Ausgangsteperatur von 0 C haben alle Gase den Ausdehnungskoeffizienten /7 -. Da sich aber bei eperaturänderungen eines Gases eist auch der Druck ändert, wird das physikalische erhalten von Gasen a besten durch die allgeeine Gasgleichung erfasst:. p Druck in bar, bar, Pa oluen in L, L,, d eperatur in p. p Norbedingungen Das oluen von Mol eines idealen Gases beträgt bei Norbedingungen (.0 bar, 0 C).4 Liter. Alternativ: Die Gasgesetze lassen sich it der allgeeinen Gasgleichung in eine sehr praktische For verallgeeinern: p Druck in bar oluen in L eperatur in p L bar R Gaskonstante R ol n R A.äser /A. Soi.0.07
2 Beispiele: LMPG_GASE LABA/B Welches oluen nehen Mol eines Gases bei 0 C und bar ein? 4.4 L Gegeben sind 0.0 Heliu bei 5 C und.0 bar. Bestien Sie das oluen bei -6 C und 5.6 * 0 4 Pa Übungsblatt. In Bodennähe enthält ein Freiballon bei 8 C und 00bar 00 Gas, in grösserer Höhe bei 480bar dagegen 50. Welche eperatur hat das Füllgas dabei angenoen? t 6.5 C. Wie gross ist der Druck in einer 40L fassenden Druckflasche, die bei 8 C 4.47kg Sauerstoffgas enthält (Mol Sauerstoffgas g)? 78.4bar. In eine See bildet sich in der iefe bei 4,0 C und eine Druck von 6 bar eine 0.d grosse Luftblase. Nachde sie zur Wasseroberfläche aufgestiegen ist, hat sie eine eperatur von 8,0 C und steht nun unter eine Druck von bar. Welches oluen hat die Luftblase jetzt? 0.68 d Weitere Aufgaben i Buch echnische Matheatik und Datenauswertung für Laborberufe: - Aufgaben zu..4:,,, und 4 Seite 89 - Aufgaben, und Seite 47 A.äser /A. Soi.0.07
3 LMPG_GASE LABA/B Lösungen: : P P > 00 bar bar 50 bar > bar > 56.9 bar t[ C] > t 6.5 C bar : Lösungsweg : über P n R 447g n 9.59 ol > g /ol L bar 40L 9.59ol ol 40L 6.88 L bar > P 78.4 bar. > Lösungsweg : Über das olare oluen bei Norbedingungen (NB) ol Gas nehen bei NB.4 L ein, also nehen 9.59 ol ein oluen von 904. L ein. P P >.0 bar 904.L 40L > P bar L P 78.4 bar. L 78.4 bar bar L 0.79 L > A.äser /A. Soi.0.07
4 LMPG_GASE LABA/B. P > P 6bar 0.d 77.5 > bar bar 8.5 d bar > 0.68d bar d bar 0.68 d. Das oluen der Blase niit wie erwartet zu, da sich die Blase bei aufsteigen erwärt und infolge der Druckabnahe ausdehnt. Lösungen Aufgaben i Buch S. 89 : Der Druck i Glockengasbehälter bleibt konstant > P P > > > Das oluen der Erdgasportion nit u: zu. : Da sich das Gas viel stärker ausdehnt als der Gasbehälter, kann die Ausdehnung des Behälters vernachlässigt werde. Da die Luft ausströen kann bleibt der Gasdruck konstant. P P > 50 L > L L > L 98.5 Es ströen: 7.88 L - 50 L L c Luft aus. A.äser /A. Soi
5 LMPG_GASE LABA/B : Bei 0 C und 0 bar nehen.99 g Luft ein oluen von d ein. Erwärant an die Luft bei konstante Druck, so nit das oluen zu: d > d > d g soit ist Dichte der Luft bei 0 C:.07d ρ.047 g/d. 4: Da die Scheibe beweglich ist bleibt der Druck konstant. Fläche der beweglichen Scheibe: ax A*h ax > A 50*0 / 67 > A.4*0 0 C : oluen: Höhe: 0 ax C 75 *0 h ax h 0 C 67 / C : oluen: C 75 0 > 0 C * Höhe: A h > h >. 0 C 0 C 0 C h0 C Die Scheibe senkt sich soit u: A.äser /A. Soi
6 Lösungen Aufgaben i Buch S. 47 LMPG_GASE LABA/B : Die Gasaus wird so befüllt, dass in der Maus kein Überdruck herrscht. Der Gasdruck in der Maus entspricht daher de Atosphärendruck. Masse des Gases: g g g Gas Gas 0.699g Stoffenge des Gases: n Gas MGas MGas Anwendung der Gasgleichung liefert die olare Masse des Gases: n R > 0.699g L bar.0bar 0.58L > M ol L bar M Gas Gas g L bar > ol 7.08 g L bar MGas.00 g /ol L bar ol M Gas g/ol es könnte sich u O handeln. A.äser /A. Soi
7 LMPG_GASE LABA/B Die folgenden Aufgaben handeln von der Bestiung der olaren Masse nach iktor-mayer. Bitte lesen Sie die heorie i Buch durch. Die folgende Abbildung soll Ihnen klar achen, wie sich der Gasdruck i Gasauffangzylinder zusaensetzt bzw. berechnet. A.äser /A. Soi
8 LMPG_GASE LABA/B s s s A.äser /A. Soi
Welcher Bewegungsspielraum ist für die beweglichen Auflager der Brücke zu berücksichtigen?
 Ü 4. Längendehnung einer Autobahnbrücke Bei 0 beträgt die Länge einer Autobahnbrücke 60. Die eperaturschwankung beträgt -0 i Winter bis zu +4 i Soer. Der Wäredehnungskoeffizient des bei der Brückenkonstruktion
Ü 4. Längendehnung einer Autobahnbrücke Bei 0 beträgt die Länge einer Autobahnbrücke 60. Die eperaturschwankung beträgt -0 i Winter bis zu +4 i Soer. Der Wäredehnungskoeffizient des bei der Brückenkonstruktion
31. Der im p-v-diagramm angegebene
 Aufgaben zur allgeeinen Zustandsgleichung. Eine kugelförige Luftblase steigt i Wasser auf. In einer Tiefe von hat sie einen Durchesser von c. Welchen Durchesser hat sie kurz vor Erreichen der Oberfläche?
Aufgaben zur allgeeinen Zustandsgleichung. Eine kugelförige Luftblase steigt i Wasser auf. In einer Tiefe von hat sie einen Durchesser von c. Welchen Durchesser hat sie kurz vor Erreichen der Oberfläche?
Versuch MG: Molmassenbestimmung eines Gases nach der Methode von Dumas
 Dies ist ein Beispielprotokoll zu fiktiven Versuch Molassenbestiung, das Ihnen insbesondere für die physikalischcheischen Versuche (GMS, ABS, BSP, MWG, LFG) aufzeigt, wie Ihr Protokoll auszusehen hat.
Dies ist ein Beispielprotokoll zu fiktiven Versuch Molassenbestiung, das Ihnen insbesondere für die physikalischcheischen Versuche (GMS, ABS, BSP, MWG, LFG) aufzeigt, wie Ihr Protokoll auszusehen hat.
1u = A r = Die relativen Atom-, Molekül- und Ionenmassen. atomare Masseneinheit 1u. relative Atommasse A r :
 Die relativen Ato-, Molekül- und Ionenassen atoare Masseneinheit u: u Masse von Kohlenstoffato C u,6655 7 kg relative Atoasse A r : Masse eines Atos A r atoare Masseneinheit u relative Molekülasse M r
Die relativen Ato-, Molekül- und Ionenassen atoare Masseneinheit u: u Masse von Kohlenstoffato C u,6655 7 kg relative Atoasse A r : Masse eines Atos A r atoare Masseneinheit u relative Molekülasse M r
b ) den mittleren isobaren thermischen Volumenausdehnungskoeffizienten von Ethanol. Hinweis: Zustand 2 t 2 = 80 C = 23, kg m 3
 Aufgabe 26 Ein Pyknometer ist ein Behälter aus Glas mit eingeschliffenem Stopfen, durch den eine kapillarförmige Öffnung führt. Es hat ein sehr genau bestimmtes Volumen und wird zur Dichtebestimmung von
Aufgabe 26 Ein Pyknometer ist ein Behälter aus Glas mit eingeschliffenem Stopfen, durch den eine kapillarförmige Öffnung führt. Es hat ein sehr genau bestimmtes Volumen und wird zur Dichtebestimmung von
Der Joule-Thomson Effekt
 Der Joule-hoson Effekt Einleitung Der Joule-hoson Effekt bezeichnet die eeraturänderung eines realen Gases bei einer adiabatischen Voluenveränderung. Der Effekt wird großtechnisch zu Beisiel i Linde- Verfahren
Der Joule-hoson Effekt Einleitung Der Joule-hoson Effekt bezeichnet die eeraturänderung eines realen Gases bei einer adiabatischen Voluenveränderung. Der Effekt wird großtechnisch zu Beisiel i Linde- Verfahren
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische heie lbert-ludwigs-universität Freiburg Lösungen zu 7. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 7. L Berechnen Sie aus der olaren Standardentropie des
Institut für hysikalische heie lbert-ludwigs-universität Freiburg Lösungen zu 7. Übungsblatt zur orlesung hysikalische heie I SS 04 rof. Dr. Bartsch 7. L Berechnen Sie aus der olaren Standardentropie des
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Modelle zur Beschreibung von Gasen und deren Eigenschaften
 Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Gase. Der Druck in Gasen. Auftrieb in Gasen. inkl. Exkurs: Ideale Gase
 Physik L17 (16.11.212) Der Druck in n inkl. Exkurs: Ideale uftrieb in n 1 Wiederholung: Der Druck in Flüssigkeiten Der Druck in Flüssigkeiten nit it zunehender Tiefe zu: Schweredruck Die oberen Wasserschichten
Physik L17 (16.11.212) Der Druck in n inkl. Exkurs: Ideale uftrieb in n 1 Wiederholung: Der Druck in Flüssigkeiten Der Druck in Flüssigkeiten nit it zunehender Tiefe zu: Schweredruck Die oberen Wasserschichten
Physik I Übung 3 - Lösungshinweise
 Physik I Übung 3 - Lösungshinweise Stefan Reutter SoSe 2012 Moritz Kütt Stand: 04.05.2012 Franz Fujara Einige der Aufgaben sind Diskussionsaufgaben. Bei ihnen kann an nichts oder nur wenig rechnen, dafür
Physik I Übung 3 - Lösungshinweise Stefan Reutter SoSe 2012 Moritz Kütt Stand: 04.05.2012 Franz Fujara Einige der Aufgaben sind Diskussionsaufgaben. Bei ihnen kann an nichts oder nur wenig rechnen, dafür
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
2. GV: Ideale Gasgesetze
 Physik Praktiku I: WS 2005/06 Protokoll zu Praktiku 2. GV: Ideale Gasgesetze Protokollanten Jörg Mönnich - Anton Friesen - Betreuer Holger Versuchstag Dienstag, 06.12.2005 Einleitung Der Zustand eines
Physik Praktiku I: WS 2005/06 Protokoll zu Praktiku 2. GV: Ideale Gasgesetze Protokollanten Jörg Mönnich - Anton Friesen - Betreuer Holger Versuchstag Dienstag, 06.12.2005 Einleitung Der Zustand eines
25. Adiabatische Expansion eines idealen Gases 1
 25. Adiabatische Exansion eines idealen Gases 1 25. ADABASHE EXPANSON ENES DEALEN GASES 1. Aufgabe Für Luft als annähernd ideales Gas sollen sowohl die Molwäre bei konstante Druck, d.h.,, als auch das
25. Adiabatische Exansion eines idealen Gases 1 25. ADABASHE EXPANSON ENES DEALEN GASES 1. Aufgabe Für Luft als annähernd ideales Gas sollen sowohl die Molwäre bei konstante Druck, d.h.,, als auch das
Uwe Rath Eckleinjarten 13a Bremerhaven
 8. Ruhende Flüssigkeiten Eine Flüssigkeit ist Materie i flüssigen ggregatzustand, nach einer akroskopischen Definition ein Stoff, welcher einer Foränderung so gut wie keinen, einer Voluenänderung hingegen
8. Ruhende Flüssigkeiten Eine Flüssigkeit ist Materie i flüssigen ggregatzustand, nach einer akroskopischen Definition ein Stoff, welcher einer Foränderung so gut wie keinen, einer Voluenänderung hingegen
Die Maxwell-Boltzmann-Verteilung
 Die Maxwell-Boltzann-Verteilung Sebastian Meiss 5. Oktober 8 Mit der Maxwell-Boltzann-Verteilung kann an Aussagen über die Energie- bzw. Geschwindigkeitsverteilung von Teilchen in eine Syste beschreiben.
Die Maxwell-Boltzann-Verteilung Sebastian Meiss 5. Oktober 8 Mit der Maxwell-Boltzann-Verteilung kann an Aussagen über die Energie- bzw. Geschwindigkeitsverteilung von Teilchen in eine Syste beschreiben.
W2 Gasthermometer. 1. Grundlagen: 1.1 Gasthermometer und Temperaturmessung
 W2 Gasthermometer Stoffgebiet: Versuchsziel: Literatur: emperaturmessung, Gasthermometer, Gasgesetze Mit Hilfe eines Gasthermometers ist der Ausdehnungs- und Druckkoeffizient von Luft zu bestimmen. Beschäftigung
W2 Gasthermometer Stoffgebiet: Versuchsziel: Literatur: emperaturmessung, Gasthermometer, Gasgesetze Mit Hilfe eines Gasthermometers ist der Ausdehnungs- und Druckkoeffizient von Luft zu bestimmen. Beschäftigung
2. Klausur zur Vorlesung Einführung in die physikalische Chemie für Lehramtskandidaten Modul 4, Wintersemester 05/06
 . Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
. Klausur zur Vorlesung Einführung in die hysikalische Cheie für Lehratskandidaten Modul 4, Winterseester 5/6 3. März 6, 9 5 45 Uhr Nae, Vornae:... Geburtsdatu, -ort:... Matrikelnuer:... Fachseester,.
1. Wärmelehre 1.1. Temperatur Wiederholung
 1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
Chemische Grundgesetze
 Björn Schulz Berlin,.10.001 p.1 Cheische Grundgesetze Gesetz von der Erhaltung der Masse (Lavoisier 1785) Abbrennen einer Kerze Massenverlust geschlossenes Syste Eisennagel rostet Massenzunahe konstante
Björn Schulz Berlin,.10.001 p.1 Cheische Grundgesetze Gesetz von der Erhaltung der Masse (Lavoisier 1785) Abbrennen einer Kerze Massenverlust geschlossenes Syste Eisennagel rostet Massenzunahe konstante
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Cheie lbert-ludwigs-universität Freiburg Lösungen zu 8. Übungsblatt zur Vorlesung hysikalische Cheie I SS 00 rof. Dr. Bartsch 8. (5 unkte) Benzol erstarrt unter at bei 5,5 C;
Institut für hysikalische Cheie lbert-ludwigs-universität Freiburg Lösungen zu 8. Übungsblatt zur Vorlesung hysikalische Cheie I SS 00 rof. Dr. Bartsch 8. (5 unkte) Benzol erstarrt unter at bei 5,5 C;
5.2 Thermische Ausdehnung (thermische Zustandsgleichung)
 5.2 herische Ausdehnung (therische Zustandsgleichung) Praktisch alle festen, gasförigen und flüssigen Stoffe dehnen sich bei Erwärung bei konstante Druck aus, vergrößern also ihr Voluen. Alle Stoffe lassen
5.2 herische Ausdehnung (therische Zustandsgleichung) Praktisch alle festen, gasförigen und flüssigen Stoffe dehnen sich bei Erwärung bei konstante Druck aus, vergrößern also ihr Voluen. Alle Stoffe lassen
2.2 Arbeit und Energie. Aufgaben
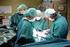 Technische Mechanik 3 2.2-1 Prof. Dr. Wandinger Aufgabe 1 Auf eine Katapult befindet sich eine Kugel der Masse, die durch eine Feder beschleunigt wird. Die Feder ist a Anfang u die Strecke s 0 zusaengedrückt.
Technische Mechanik 3 2.2-1 Prof. Dr. Wandinger Aufgabe 1 Auf eine Katapult befindet sich eine Kugel der Masse, die durch eine Feder beschleunigt wird. Die Feder ist a Anfang u die Strecke s 0 zusaengedrückt.
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
Stickstoff kann als ideales Gas betrachtet werden mit einer spezifischen Gaskonstante von R N2 = 0,297 kj
 Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Der Magnus-Effekt. Rotierender Körper in äußerer Strömung: Anwendungen:
 Der Magnus-Effekt Rotierender Körper in äußerer Strömung: Ohne Strömung: Körper führt umgebendes Medium an seinen Oberflächen mit Keine resultierende Gesamtkraft. ω Mit Strömung: Geschwindigkeiten der
Der Magnus-Effekt Rotierender Körper in äußerer Strömung: Ohne Strömung: Körper führt umgebendes Medium an seinen Oberflächen mit Keine resultierende Gesamtkraft. ω Mit Strömung: Geschwindigkeiten der
3.3 Wärme als Energieform
 3.3 Wäre als Energiefor Erinnere: Herleitung der Zustandsgleichung p V=n R T hatten wir die Teperatur eingeführt als Basisgröße die proportional zur Molekülenergie sein soll: 1 3 ε kin = u = kt d.h.: zur
3.3 Wäre als Energiefor Erinnere: Herleitung der Zustandsgleichung p V=n R T hatten wir die Teperatur eingeführt als Basisgröße die proportional zur Molekülenergie sein soll: 1 3 ε kin = u = kt d.h.: zur
Formelsammlung Bauphysik
 Forelsalung Bauphysik. Wäreschutz Physikalische Größen Wäre Q c ( Θ Θ ) Wärestro Wärestrodichte Wäreleitungsgleichung ransissionsgrad Absorptionsgrad Reflexionsgrad Stefan-Boltzann-Gesetz schwarzer Strahler
Forelsalung Bauphysik. Wäreschutz Physikalische Größen Wäre Q c ( Θ Θ ) Wärestro Wärestrodichte Wäreleitungsgleichung ransissionsgrad Absorptionsgrad Reflexionsgrad Stefan-Boltzann-Gesetz schwarzer Strahler
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Schweredruck. p S =ρ g h
 Schweredruck p S =ρ g h Ein Zylinder ist mit einer Flüssigkeit gefüllit: Wie hoch muss er jeweils mit den folgenden Stoffen gefüllt werden, damit der Bodendruck 1 bar beträgt? (Dichte Tabelle in Kapitel
Schweredruck p S =ρ g h Ein Zylinder ist mit einer Flüssigkeit gefüllit: Wie hoch muss er jeweils mit den folgenden Stoffen gefüllt werden, damit der Bodendruck 1 bar beträgt? (Dichte Tabelle in Kapitel
Suszeptibilitätsmessungen mit der Magnetwaage Mark I von Johnson-Matthey
 Einführung in hysialisch-cheische ethoden i anorganischcheischen rundratiu (Dilostudiengang Cheie) Ausgegeben seit Soerseester 007 Suszetibilitätsessungen it der agnetwaage ar I von Johnson-atthey are
Einführung in hysialisch-cheische ethoden i anorganischcheischen rundratiu (Dilostudiengang Cheie) Ausgegeben seit Soerseester 007 Suszetibilitätsessungen it der agnetwaage ar I von Johnson-atthey are
Physikalische Chemie Praktikum. Reale Gase, Kritischer Punkt
 Hochschule Eden / Leer Physikalische Cheie Praktiku Reale Gase, Kritischer Punkt Vers.Nr. 1 April 015 Allgeeine Grundlagen Reale Gase, Kopressionsfaktor (Realgasfaktor), Van der Waals Gleichung, Kritischer
Hochschule Eden / Leer Physikalische Cheie Praktiku Reale Gase, Kritischer Punkt Vers.Nr. 1 April 015 Allgeeine Grundlagen Reale Gase, Kopressionsfaktor (Realgasfaktor), Van der Waals Gleichung, Kritischer
2.2 Arbeit und Energie. Aufgaben
 2.2 Arbeit und Energie Aufgaben Aufgabe 1: Auf eine Katapult befindet sich eine Kugel der Masse, die durch eine Feder beschleunigt wird. Die Feder ist a Anfang u die Strecke s 0 zusaengedrückt. Für die
2.2 Arbeit und Energie Aufgaben Aufgabe 1: Auf eine Katapult befindet sich eine Kugel der Masse, die durch eine Feder beschleunigt wird. Die Feder ist a Anfang u die Strecke s 0 zusaengedrückt. Für die
Lösung zu: Bau einer Windkraftanlage, Aufgabe: Windkraft Ina Dorothea Kleinehollenhorst und Olga Hartmann. Lösungsvorschläge
 Ina Dorothea Kleinehollenhorst und Olga Hartann Lösungsvorschläge 1. Einflussfaktoren welche die Windlast auf eine Windkraftanlage beeinflussen sind zu Beispiel: a. Standort der WKA & Ugebung b. Höhe c.
Ina Dorothea Kleinehollenhorst und Olga Hartann Lösungsvorschläge 1. Einflussfaktoren welche die Windlast auf eine Windkraftanlage beeinflussen sind zu Beispiel: a. Standort der WKA & Ugebung b. Höhe c.
Demonstrationsexperimente WS 04/05. Thema: Dichte der Luft Dichtebestimmung mittels Luftgewichtsmesser
 Deonstrationsexperiente WS 04/05 Thea: Dichte der Luft Dichtebestiung ittels Luftgewichtsesser Monika Schorn 9..004. Versuchsbeschreibung. Materialliste - Luftgewichtsesser (hohle Kugel it Ventil zu Befüllen)
Deonstrationsexperiente WS 04/05 Thea: Dichte der Luft Dichtebestiung ittels Luftgewichtsesser Monika Schorn 9..004. Versuchsbeschreibung. Materialliste - Luftgewichtsesser (hohle Kugel it Ventil zu Befüllen)
2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg
![2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg 2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg](/thumbs/75/72774995.jpg) 2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
Grundlagen der Physik 3 Lösung zu Übungsblatt 2
 Grundlagen der Physik 3 Lösung zu Übungsblatt 2 Daniel Weiss 17. Oktober 2010 Inhaltsverzeichnis Aufgabe 1 - Zustandsfunktion eines Van-der-Waals-Gases 1 a) Zustandsfunktion.................................
Grundlagen der Physik 3 Lösung zu Übungsblatt 2 Daniel Weiss 17. Oktober 2010 Inhaltsverzeichnis Aufgabe 1 - Zustandsfunktion eines Van-der-Waals-Gases 1 a) Zustandsfunktion.................................
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Tutorium Hydromechanik I und II
 Tutorium Hydromechanik I und II WS 2016/2017 Vorlesung 10 09.01.2017 Prof. Dr. rer. nat. M. Koch 1 Aufgabe 1 Gegeben ist ein Manometer mit zwei Behältern, die mit Wasser gefüllt sind. Im Rohr befindet
Tutorium Hydromechanik I und II WS 2016/2017 Vorlesung 10 09.01.2017 Prof. Dr. rer. nat. M. Koch 1 Aufgabe 1 Gegeben ist ein Manometer mit zwei Behältern, die mit Wasser gefüllt sind. Im Rohr befindet
B06A DAMPFDRUCK VON WASSER B06A
 B06A DAMPFDRUCK VON WASSER B06A 1. ZIELE Wir aten euchtere Lut aus als ein. Müssen wir daür Enerie auwenden? Waru werden die Kartoeln in eine Dapdrucktop schneller ar? Was passiert, wenn Wasser verdapt?
B06A DAMPFDRUCK VON WASSER B06A 1. ZIELE Wir aten euchtere Lut aus als ein. Müssen wir daür Enerie auwenden? Waru werden die Kartoeln in eine Dapdrucktop schneller ar? Was passiert, wenn Wasser verdapt?
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Physikalische Größen von Feststoffen
 III Physikalische Größen von Feststoffen Inhaltsverzeichnis 1 Einleitung 2 2 Grundlagen 3 2.1 Beschreibung von Schüttgütern 3 2.2 Physikalische Größen von Schüttgütern 4 2.2.1 Schüttdichte von Schüttgütern
III Physikalische Größen von Feststoffen Inhaltsverzeichnis 1 Einleitung 2 2 Grundlagen 3 2.1 Beschreibung von Schüttgütern 3 2.2 Physikalische Größen von Schüttgütern 4 2.2.1 Schüttdichte von Schüttgütern
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Einführung in die Physik I. Mechanik deformierbarer Körper 1. O. von der Lühe und U. Landgraf
 Einführung in die Physik I Mechanik deformierbarer Körer O. von der Lühe und U. Landgraf Deformationen Deformationen, die das olumen ändern Dehnung Stauchung Deformationen, die das olumen nicht ändern
Einführung in die Physik I Mechanik deformierbarer Körer O. von der Lühe und U. Landgraf Deformationen Deformationen, die das olumen ändern Dehnung Stauchung Deformationen, die das olumen nicht ändern
PC-Übung Nr.1 vom
 PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
Tutorium Physik 2. Fluide
 1 Tutorium Physik 2. Fluide SS 16 2.Semester BSc. Oec. und BSc. CH 2 Themen 7. Fluide 8. Rotation 9. Schwingungen 10. Elektrizität 11. Optik 12. Radioaktivität 3 7. FLUIDE 7.1 Modellvorstellung Fluide:
1 Tutorium Physik 2. Fluide SS 16 2.Semester BSc. Oec. und BSc. CH 2 Themen 7. Fluide 8. Rotation 9. Schwingungen 10. Elektrizität 11. Optik 12. Radioaktivität 3 7. FLUIDE 7.1 Modellvorstellung Fluide:
Anwendungsaufgaben - Mechanik der Flüssigkeiten und Gase - Lösungen
 nwendunsaufaben - Mechanik der üssikeiten und Gase - Lösunen 1 Die Gewichtskraft der Person wird auf zwei üße verteit, so dass auf jeden uß eine Kraft von 0,5 600 wirkt. 0,5 600 0,5 600 = = 1, S = = 0,5
nwendunsaufaben - Mechanik der üssikeiten und Gase - Lösunen 1 Die Gewichtskraft der Person wird auf zwei üße verteit, so dass auf jeden uß eine Kraft von 0,5 600 wirkt. 0,5 600 0,5 600 = = 1, S = = 0,5
Gasvolumetrie. Aufgabenstellung. Grundlagen. Institut für Anorganische Chemie der Universität Wien S. Ayromlou
 Chemisches Grundpraktikum - 1 - Theoretische Grundlagen / 2000 Institut für Anorganische Chemie der Universität Wien S. Ayromlou Chemisches Grundpraktikum Beispiel 10 / 2003 Gasvolumetrie Aufgabenstellung
Chemisches Grundpraktikum - 1 - Theoretische Grundlagen / 2000 Institut für Anorganische Chemie der Universität Wien S. Ayromlou Chemisches Grundpraktikum Beispiel 10 / 2003 Gasvolumetrie Aufgabenstellung
Analyse Auftriebs KKKraftwerk Fa Gaja 1 Erstellt am e.r.
 Analyse Auftriebs KKKraftwerk Fa Gaja 1 Funktionsprinzip des Auftriebskraftwerks In einem mit Wasser gefüllten Tank befinden sich Behälter in Form eines halbierten Zylinders, die mit einem Kettentrieb
Analyse Auftriebs KKKraftwerk Fa Gaja 1 Funktionsprinzip des Auftriebskraftwerks In einem mit Wasser gefüllten Tank befinden sich Behälter in Form eines halbierten Zylinders, die mit einem Kettentrieb
3.2 Gasthermometer 203
 3.2 Gasthermometer 203 3.2. Gasthermometer Ziel Verifizierung von Zusammenhängen, die durch die ideale Gasgleichung beschrieben werden (isotherme und isochore Zustandsänderung), Bestimmung des absoluten
3.2 Gasthermometer 203 3.2. Gasthermometer Ziel Verifizierung von Zusammenhängen, die durch die ideale Gasgleichung beschrieben werden (isotherme und isochore Zustandsänderung), Bestimmung des absoluten
WS 17/18 1. Sem. B.Sc. Catering und Hospitality Services
 2 Physik 1. Fluide. WS 17/18 1. Sem. B.Sc. Catering und Hospitality Services Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nicht-kommerziell Weitergabe unter gleichen Bedingungen
2 Physik 1. Fluide. WS 17/18 1. Sem. B.Sc. Catering und Hospitality Services Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nicht-kommerziell Weitergabe unter gleichen Bedingungen
Zustandsformen der Materie Thermische Eigenschaften der Materie. Temperatur. skalare Zustandsgröße der Materie Maß für die Bewegung der Moleküle
 Zustandsformen der Materie hermische Eigenschaften der Materie Aggregatzustände: fest flüssig suprafluide gasförmig überkritisch emperatur skalare Zustandsgröße der Materie Maß für die Bewegung der Moleküle
Zustandsformen der Materie hermische Eigenschaften der Materie Aggregatzustände: fest flüssig suprafluide gasförmig überkritisch emperatur skalare Zustandsgröße der Materie Maß für die Bewegung der Moleküle
Gasthermometer. durchgeführt am von Matthias Dräger, Alexander Narweleit und Fabian Pirzer
 Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Wie ist der Druck p allgemein definiert. Wie groß ist der Luftdruck unter Normalbedingungen ungefähr? Welche Einheit hat er?
 Wie ist der Druck p allgemein definiert? Welche Einheit hat er? Wie groß ist der Luftdruck unter Normalbedingungen ungefähr? Was kann man sich anschaulich unter dem Stempeldruck in einer Flüssigkeit vorstellen?
Wie ist der Druck p allgemein definiert? Welche Einheit hat er? Wie groß ist der Luftdruck unter Normalbedingungen ungefähr? Was kann man sich anschaulich unter dem Stempeldruck in einer Flüssigkeit vorstellen?
Lösungsvorschlag Übung 1
 Lösungsvorschlag Übung Aufgabe : Physikalische Einheiten a) Es existieren insgesamt sieben Basisgrössen im SI-System. Diese sind mit der zugehörigen physikalischen Einheit und dem Einheitenzeichen in der
Lösungsvorschlag Übung Aufgabe : Physikalische Einheiten a) Es existieren insgesamt sieben Basisgrössen im SI-System. Diese sind mit der zugehörigen physikalischen Einheit und dem Einheitenzeichen in der
Physik-Vorlesung SS Fluide.
 Physik Fluide 3 Physik-Vorlesung SS 2016. Fluide. SS 16 2. Sem. B.Sc. Oec. und B.Sc. CH Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe unter gleichen
Physik Fluide 3 Physik-Vorlesung SS 2016. Fluide. SS 16 2. Sem. B.Sc. Oec. und B.Sc. CH Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe unter gleichen
Physikalisches Praktikum I
 Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Thermodynamik Prof. Dr.-Ing. Peter Hakenesch peter.hakenesch@hm.edu www.lrz-muenchen.de/~hakenesch
 herodynaik _ herodynaik Prof. Dr.-Ing. Peter Hakenesch eter.hakenesch@h.edu www.lrz-uenchen.de/~hakenesch _ herodynaik Einleitung Grundbegriffe 3 Systebeschreibung 4 Zustandsgleichungen 5 Kinetische Gastheorie
herodynaik _ herodynaik Prof. Dr.-Ing. Peter Hakenesch eter.hakenesch@h.edu www.lrz-uenchen.de/~hakenesch _ herodynaik Einleitung Grundbegriffe 3 Systebeschreibung 4 Zustandsgleichungen 5 Kinetische Gastheorie
Hydr. Druck, Luftdruck
 Hydr. Druck, Luftdruck Den Begriff Druck verwenden wir oft im täglichen Leben. Wir hören im Zusammenhang mit den Wettervorhersagen täglich vom. oder. (z.b.oder..). Wir haben einen bestimmten.in unseren
Hydr. Druck, Luftdruck Den Begriff Druck verwenden wir oft im täglichen Leben. Wir hören im Zusammenhang mit den Wettervorhersagen täglich vom. oder. (z.b.oder..). Wir haben einen bestimmten.in unseren
Lösung. Nachholklausur zur Vorlesung Physikalische Chemie I - Sommersemester 2002
 Lösung Nachholklausur zur orlesung Physikalische hemie I - Sommersemester 00 6. Oktober 00, 9 5-5 Uhr Hineise - Bitte Namen auf jedes Blatt schreiben. - Auch Blatt-Rückseiten beschreiben. - Ggf. eitere
Lösung Nachholklausur zur orlesung Physikalische hemie I - Sommersemester 00 6. Oktober 00, 9 5-5 Uhr Hineise - Bitte Namen auf jedes Blatt schreiben. - Auch Blatt-Rückseiten beschreiben. - Ggf. eitere
Gase, Flüssigkeiten, Feststoffe
 Gase, Flüssigkeiten, Feststoffe Charakteristische Eigenschaften der Aggregatzustände Gas: Flüssigkeit: Feststoff: Nimmt das Volumen und die Form seines Behälters an. Ist komprimierbar. Fliesst leicht.
Gase, Flüssigkeiten, Feststoffe Charakteristische Eigenschaften der Aggregatzustände Gas: Flüssigkeit: Feststoff: Nimmt das Volumen und die Form seines Behälters an. Ist komprimierbar. Fliesst leicht.
Übungsaufgabe. Bestimmen Sie das molare Volumen für Ammoniak bei einem Druck von 1 MPa und einer Temperatur von 100 C nach
 Übungsaufgabe Bestien Sie das olare Voluen für Aoniak bei eine Druck von 1 MPa und einer Teperatur von 100 C nach a) de idealen Gasgesetz b) der Van der Waals-Gleichung c) der Redlich-Kwong- Gleichung
Übungsaufgabe Bestien Sie das olare Voluen für Aoniak bei eine Druck von 1 MPa und einer Teperatur von 100 C nach a) de idealen Gasgesetz b) der Van der Waals-Gleichung c) der Redlich-Kwong- Gleichung
Hydrogeochemische Modellierung mit PhreeqC
 ( Blockkurs Geowissenschaftliches Modellieren (01. 03.04.2009) Aufgabe 1: Erhöhung CO 2 -Gehalt in der Atmosphäre durch Änderung der Lufttemperatur? Aus vielen Untersuchungen (z.b. an Eiskernen) wissen
( Blockkurs Geowissenschaftliches Modellieren (01. 03.04.2009) Aufgabe 1: Erhöhung CO 2 -Gehalt in der Atmosphäre durch Änderung der Lufttemperatur? Aus vielen Untersuchungen (z.b. an Eiskernen) wissen
Temperatur.nb. Ã Frage. Ã Antwort Vorbereitung Lehrbuch-Formel Eigentlicher Wirkungsgrad
 Teperatur.nb Fragesteller: 7. 3.006 Dr. Norbert Südland Bearbeitung: 7. 3.006 4. 3.006 Dr. Norbert Südland Letzte Berechnung: 4. 3.006 Dr. Norbert Südland à 36.1. Frage Gibt es sinnvolle Alternativen zur
Teperatur.nb Fragesteller: 7. 3.006 Dr. Norbert Südland Bearbeitung: 7. 3.006 4. 3.006 Dr. Norbert Südland Letzte Berechnung: 4. 3.006 Dr. Norbert Südland à 36.1. Frage Gibt es sinnvolle Alternativen zur
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Tutorium Hydromechanik I + II. S. Mohammad Hosseiny Sohi Dezember 2015
 Tutorium Hydromechanik I + II S. Mohammad Hosseiny Sohi Dezember 2015 FB14/Geohydraulik und Ingenieurhydrologie/ Tutorium Hydromechanik/ Mohammad Hosseiny Sohi 14.12.2015 In einer hessischen Wetterstation
Tutorium Hydromechanik I + II S. Mohammad Hosseiny Sohi Dezember 2015 FB14/Geohydraulik und Ingenieurhydrologie/ Tutorium Hydromechanik/ Mohammad Hosseiny Sohi 14.12.2015 In einer hessischen Wetterstation
2. so rasch ausströmen, dass keine Wärmeübertragung stattfinden kann.
 Aufgabe 33 Aus einer Druckluftflasche V 50 dm 3 ) mit einem Anfangsdruck p 0 60 bar strömt solange Luft in die Umgebung p U bar, T U 300 K), bis der Druck in der Flasche auf 0 bar gefallen ist. Dabei soll
Aufgabe 33 Aus einer Druckluftflasche V 50 dm 3 ) mit einem Anfangsdruck p 0 60 bar strömt solange Luft in die Umgebung p U bar, T U 300 K), bis der Druck in der Flasche auf 0 bar gefallen ist. Dabei soll
Vorwort. Gernot Wilhelms. Übungsaufgaben Technische Thermodynamik ISBN: Weitere Informationen oder Bestellungen unter
 Vorwort Gernot Wilhels Übungsaufgaben Technische Therodynaik ISBN: 978-3-446-42514-9 Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-42514-9 sowie i Buchhandel. Carl Hanser
Vorwort Gernot Wilhels Übungsaufgaben Technische Therodynaik ISBN: 978-3-446-42514-9 Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-42514-9 sowie i Buchhandel. Carl Hanser
Die Zustandsgleichung realer Gase
 Die Zustandsgleichung realer Gase Grolik Benno, Kopp Joachim 2. Januar 2003 1 Grundlagen des Versuchs Der Zustand eines idealen Gases wird durch die drei elementaren Zustandsgrößen Druck p, Temperatur
Die Zustandsgleichung realer Gase Grolik Benno, Kopp Joachim 2. Januar 2003 1 Grundlagen des Versuchs Der Zustand eines idealen Gases wird durch die drei elementaren Zustandsgrößen Druck p, Temperatur
Was ist Physikalische Chemie? Die klassischen Teilgebiete der Physikalischen Chemie sind:
 Was ist Physikalische Chemie? Die klassischen eilgebiete der Physikalischen Chemie sind: 1) hermodynamik (z. B. Energetik chemischer Reaktionen, Lage von Gleichgewichten). 2) Kinetik chemischer Reaktionen
Was ist Physikalische Chemie? Die klassischen eilgebiete der Physikalischen Chemie sind: 1) hermodynamik (z. B. Energetik chemischer Reaktionen, Lage von Gleichgewichten). 2) Kinetik chemischer Reaktionen
8. Vorlesung EP. EPI WS 2007/08 Dünnweber/Faessler
 8. Vorlesung EP I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik (Fortsetzung: Auftrieb) c) Oberflächenspannung und Kapillarität Versuche:
8. Vorlesung EP I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik (Fortsetzung: Auftrieb) c) Oberflächenspannung und Kapillarität Versuche:
2 Wärmelehre. Reibungswärme Reaktionswärme Stromwärme
 2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
Tabellen und Formelsammlung Chemie
 Tabellen und Forelsalung Cheie Fakultät Maschinenbau Stand SS 2015 Nachfolgende Tabellen und Inforationen staen aus de Lehrbuch G. Kickelbick, Cheie für Ingenieure, Pearson-Verlag, 2008 soweit nicht anderweitig
Tabellen und Forelsalung Cheie Fakultät Maschinenbau Stand SS 2015 Nachfolgende Tabellen und Inforationen staen aus de Lehrbuch G. Kickelbick, Cheie für Ingenieure, Pearson-Verlag, 2008 soweit nicht anderweitig
Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 (MOL)
 Seite 1 Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 1 Literatur W. Walcher, Praktikum der Physik, Teubner Themengebiet: Thermodynamik Bundesanstalt für Arbeitsschutz und
Seite 1 Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 1 Literatur W. Walcher, Praktikum der Physik, Teubner Themengebiet: Thermodynamik Bundesanstalt für Arbeitsschutz und
2. Physikschulaufgabe. - Lösungen -
 Realschule. Physikschulaufgabe Klasse 8 I - Lösungen - Thea: Mechanik der en und Gase 1.1 Versuchsaufbau In eine Präzisionsglasrohr it geschliffener Innenwand befindet sich eine fast reibungsfrei bewegliche
Realschule. Physikschulaufgabe Klasse 8 I - Lösungen - Thea: Mechanik der en und Gase 1.1 Versuchsaufbau In eine Präzisionsglasrohr it geschliffener Innenwand befindet sich eine fast reibungsfrei bewegliche
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
Gander Daniel, WS 2004 Mayrhofer Reinhard; GEOPHYSICS & GEODYNAMICS TU GRAZ
 Gander Daniel, WS 004 TECHNISCHE BEICHT st lab: Gravity and Pressure in the Earth s Interior POBLEMSTELLUNG... LÖSUNG UND EGEBNISSE.... Berechnung der Massen.... Berechnung der Schwerebeschleunigung...4.
Gander Daniel, WS 004 TECHNISCHE BEICHT st lab: Gravity and Pressure in the Earth s Interior POBLEMSTELLUNG... LÖSUNG UND EGEBNISSE.... Berechnung der Massen.... Berechnung der Schwerebeschleunigung...4.
0.1 Barometrische Höhenformel
 0. Barometrische Höhenformel Da, wie aus den bisherigen Überlegungen hervorgegeangen ist, Gase komressibel sind, kann deren Dichte nicht als konstant angesehen werden. Dies hat Konsequenzen auf den Schweredruck
0. Barometrische Höhenformel Da, wie aus den bisherigen Überlegungen hervorgegeangen ist, Gase komressibel sind, kann deren Dichte nicht als konstant angesehen werden. Dies hat Konsequenzen auf den Schweredruck
IFV - Duisburg. Entgasung flüssiger Medien. Dipl.-Ing. Heinz Sievering
 1 IFV - Duisburg Dipl.-Ing. Heinz Sievering Entgasung flüssiger Medien IFV-Duisburg 2008 2 Einfaches Prinzip große Wirkung Daten und Fakten Flüssige Medien lassen sich physikalisch nicht zusammenpressen.
1 IFV - Duisburg Dipl.-Ing. Heinz Sievering Entgasung flüssiger Medien IFV-Duisburg 2008 2 Einfaches Prinzip große Wirkung Daten und Fakten Flüssige Medien lassen sich physikalisch nicht zusammenpressen.
Aufgaben zur Wärmelehre
 Aufgaben zur Wärmelehre 1. Ein falsch kalibriertes Quecksilberthermometer zeigt -5 C eingetaucht im schmelzenden Eis und 103 C im kochenden Wasser. Welche ist die richtige Temperatur, wenn das Thermometer
Aufgaben zur Wärmelehre 1. Ein falsch kalibriertes Quecksilberthermometer zeigt -5 C eingetaucht im schmelzenden Eis und 103 C im kochenden Wasser. Welche ist die richtige Temperatur, wenn das Thermometer
Grundlagen der DURCHFLUSSMESSUNG mittels Heißfilmanemometer
 Grundlagen der DURCHFLUSSMESSUNG ittels Heißfilaneoeter 1/9 Inhaltsverzeichnis: 1. Definitionen 1.1. Luftgeschwindigkeit 1.2. Gasenge 1.. Durchfluss 1..1. Massendurchfluss (Massenstro) 1..2. Voluendurchfluss
Grundlagen der DURCHFLUSSMESSUNG ittels Heißfilaneoeter 1/9 Inhaltsverzeichnis: 1. Definitionen 1.1. Luftgeschwindigkeit 1.2. Gasenge 1.. Durchfluss 1..1. Massendurchfluss (Massenstro) 1..2. Voluendurchfluss
Reale Gase. 1. Grundlagen. a 2. pv m. 1.1. Van der Waals-Gleichung. Die allgemeine Gasgleichung für ideale Gase lautet:
 Reale Gase Stichworte: Van der Waals-Gleichung, Phasenuwandlung 1 Grundlagen 11 Van der Waals-Gleichung Die allgeeine Gasgleichung für ideale Gase lautet: pv RT it p: Druck (1) V : Molvoluen des Gases
Reale Gase Stichworte: Van der Waals-Gleichung, Phasenuwandlung 1 Grundlagen 11 Van der Waals-Gleichung Die allgeeine Gasgleichung für ideale Gase lautet: pv RT it p: Druck (1) V : Molvoluen des Gases
c ) Wie verhält sich die Enthalpieänderung, wenn das Wasser in einer Düse beschleunigt wird?
 Aufgabe 4 An einer Drosselstelle wird ein kontinuierlich fließender Strom von Wasser von p 8 bar auf p 2 2 bar entspannt. Die Geschwindigkeiten vor und nach der Drosselung sollen gleich sein. Beim des
Aufgabe 4 An einer Drosselstelle wird ein kontinuierlich fließender Strom von Wasser von p 8 bar auf p 2 2 bar entspannt. Die Geschwindigkeiten vor und nach der Drosselung sollen gleich sein. Beim des
Versuch 1 Bestimmung der Dichte einer Flüssigkeit
 Versuh 1 Bestiung der Dihte einer Flüssigkeit Versuh 1 Bestiung der Dihte einer Flüssigkeit Dihteessung it de digitalen Dihteeßgerät nah DIN 51757 ( Verfahren D ) Die Dihte ρ ist eine wihtige und vielfah
Versuh 1 Bestiung der Dihte einer Flüssigkeit Versuh 1 Bestiung der Dihte einer Flüssigkeit Dihteessung it de digitalen Dihteeßgerät nah DIN 51757 ( Verfahren D ) Die Dihte ρ ist eine wihtige und vielfah
Hydrostatik. Von Wasser und Luft und anderem 1. OG. Stiftsschule Engelberg, Schuljahr 2016/2017
 Hydrostatik Von Wasser und Luft und anderem 1. OG Stiftsschule Engelberg, Schuljahr 2016/2017 1 Die Dichte Ziele dieses Kapitels Du weisst, was die Dichte ist und wie man sie messen kann. Du kannst Berechnungen
Hydrostatik Von Wasser und Luft und anderem 1. OG Stiftsschule Engelberg, Schuljahr 2016/2017 1 Die Dichte Ziele dieses Kapitels Du weisst, was die Dichte ist und wie man sie messen kann. Du kannst Berechnungen
Physikalische Chemie 1
 Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Physikalisches Anfaengerpraktikum. Zustandsgleichung idealer Gase und kritischer Punkt
 Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Physikalisch-Chemisches Grundpraktikum
 Physikalisch-Cheisches Grundpraktiku Versuch Nuer G3: Bestiung der Oberflächen- spannung it der Blasenethode Gliederung: I. Aufgabenbeschreibung II. Theoretischer Hintergrund III. Versuchsanordnung IV.
Physikalisch-Cheisches Grundpraktiku Versuch Nuer G3: Bestiung der Oberflächen- spannung it der Blasenethode Gliederung: I. Aufgabenbeschreibung II. Theoretischer Hintergrund III. Versuchsanordnung IV.
Übung zur Vorlesung PC I Chemische Thermodynamik B.Sc. Blatt 2
 Prof. Dr. Norbert Ha Soerseester 009.05.009 Übung zur orlesung PC I Cheische Therodynaik B.Sc. Blatt. Abweichungen o idealen erhalten bei Gasen lassen sich durch Angabe des Koressionsfaktors Z = / RT charakterisieren,
Prof. Dr. Norbert Ha Soerseester 009.05.009 Übung zur orlesung PC I Cheische Therodynaik B.Sc. Blatt. Abweichungen o idealen erhalten bei Gasen lassen sich durch Angabe des Koressionsfaktors Z = / RT charakterisieren,
Bestimmung der Molaren Masse nach Dumas (MOL) Gruppe 8 Simone Lingitz, Sebastian Jakob
 Bestiun der Molaren Masse nach Duas (MO Gruppe 8 Sione initz, Sebastian Jakob 1. Grundlaen In diese ersuch wird nach de erfahren von Duas die Molare Masse von hlorofor bestit. Dazu wird anenoen, daß hlorofor
Bestiun der Molaren Masse nach Duas (MO Gruppe 8 Sione initz, Sebastian Jakob 1. Grundlaen In diese ersuch wird nach de erfahren von Duas die Molare Masse von hlorofor bestit. Dazu wird anenoen, daß hlorofor
Thermodynamik 1 Klausur 08. September 2016
 Thermodynamik 1 Klausur 08. September 2016 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten Alle Unterlagen zur Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Thermodynamik 1 Klausur 08. September 2016 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten Alle Unterlagen zur Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Klausur. Strömungsmechanik
 Strömungsmechanik Klausur Strömungsmechanik. Juli 007 Name, Vorname: Matrikelnummer: Fachrichtung: Unterschrift: Bewertung: Aufgabe : Aufgabe : Aufgabe 3: Aufgabe 4: Gesamtpunktzahl: Klausur Strömungsmechanik
Strömungsmechanik Klausur Strömungsmechanik. Juli 007 Name, Vorname: Matrikelnummer: Fachrichtung: Unterschrift: Bewertung: Aufgabe : Aufgabe : Aufgabe 3: Aufgabe 4: Gesamtpunktzahl: Klausur Strömungsmechanik
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Allgemeine Chemie / Lösungsvorschläge Aufgaben
 Allgemeine Chemie / Lösungsvorschläge Aufgaben 1) offene Systeme >>> Erlenmeyerkolben ohne Stopfen geschlossene Systeme >>>> Luftballon abgeschlossen>>>> Thermoskanne 2) M(Ausgangsstoff) = 404 g/mol n(fe
Allgemeine Chemie / Lösungsvorschläge Aufgaben 1) offene Systeme >>> Erlenmeyerkolben ohne Stopfen geschlossene Systeme >>>> Luftballon abgeschlossen>>>> Thermoskanne 2) M(Ausgangsstoff) = 404 g/mol n(fe
